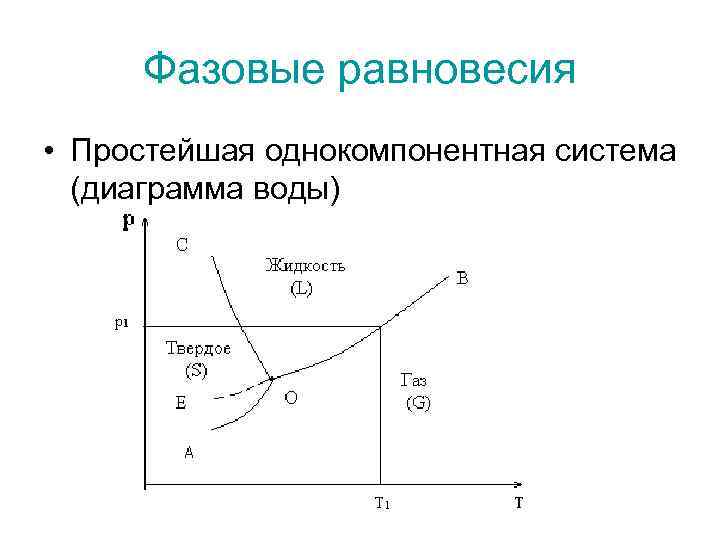
 Фазовые равновесия • Простейшая однокомпонентная система (диаграмма воды)
Фазовые равновесия • Простейшая однокомпонентная система (диаграмма воды)
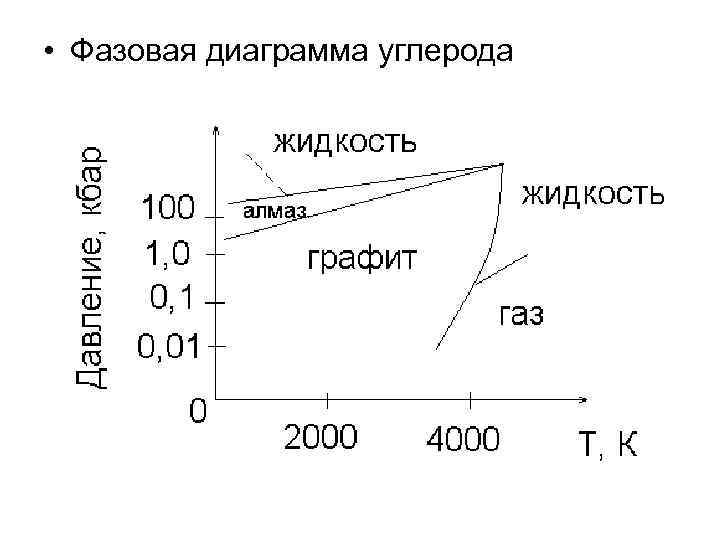 • Фазовая диаграмма углерода
• Фазовая диаграмма углерода
 Правило фаз Гиббса • Фазой (Ф) называется совокупность телесных объектов, имеющих определенный химический состав и т/д свойства, отделенная от других фаз поверхностью раздела. Однородная часть неоднородной системы, которая может быть извлечена из системы каким либо механическим способом.
Правило фаз Гиббса • Фазой (Ф) называется совокупность телесных объектов, имеющих определенный химический состав и т/д свойства, отделенная от других фаз поверхностью раздела. Однородная часть неоднородной системы, которая может быть извлечена из системы каким либо механическим способом.
 • Числом компонентов (К) называется число индивидуальных веществ, входящих в систему, за вычетом числа химических уравнений, связывающих эти свойства. Н 2, О 2 и Н 2 О при высоких температурах: Н 2+1/2 О 2= Н 2 О К=3 -1=2 при низких температурах: К=3
• Числом компонентов (К) называется число индивидуальных веществ, входящих в систему, за вычетом числа химических уравнений, связывающих эти свойства. Н 2, О 2 и Н 2 О при высоких температурах: Н 2+1/2 О 2= Н 2 О К=3 -1=2 при низких температурах: К=3
 • Числом степеней свободы (С) называется число параметров (Т, р, концентрация), которые полностью определяют состояние системы при равновесии. Число параметров, которые можно менять в определенных пределах без изменения числа и природы фаз.
• Числом степеней свободы (С) называется число параметров (Т, р, концентрация), которые полностью определяют состояние системы при равновесии. Число параметров, которые можно менять в определенных пределах без изменения числа и природы фаз.
 Найдем связь между К, Ф и С. П – число параметров системы. Для всех фаз число параметров, характеризующих концентрацию равно КФ. Учитываем температуру и давление. П=КФ+2 Концентрации компонентов в разных фазах связаны условиями равенства химических потенциалов.
Найдем связь между К, Ф и С. П – число параметров системы. Для всех фаз число параметров, характеризующих концентрацию равно КФ. Учитываем температуру и давление. П=КФ+2 Концентрации компонентов в разных фазах связаны условиями равенства химических потенциалов.
 Первый к-т Второй к-т …………………………. К-тый к-т Число уравнений, связывающих все i для каждого компонента составит (Ф-1). Для всех компонентов К(Ф-1). Для каждой фазы существует уравнение состояния. Их общее количество равно Ф
Первый к-т Второй к-т …………………………. К-тый к-т Число уравнений, связывающих все i для каждого компонента составит (Ф-1). Для всех компонентов К(Ф-1). Для каждой фазы существует уравнение состояния. Их общее количество равно Ф
 Общее число уравнений У, связывающих параметры, равно У=К(Ф-1)+Ф С=П-У=КФ+2 -К(Ф-1)-Ф=К-Ф+2 Выражение правила фаз Очевидно, что число степеней свободы не может быть отрицательным, т. е. К+2≥Ф Для однокомпонентных систем С=0=1+2 -Ф, т. е. Ф=3
Общее число уравнений У, связывающих параметры, равно У=К(Ф-1)+Ф С=П-У=КФ+2 -К(Ф-1)-Ф=К-Ф+2 Выражение правила фаз Очевидно, что число степеней свободы не может быть отрицательным, т. е. К+2≥Ф Для однокомпонентных систем С=0=1+2 -Ф, т. е. Ф=3
 При наличии, например, воды и пара С=1+2 -2=1 Максимальное количество фаз, которое может существовать одновременно: в двухкомпонетной системе: 0=2+2 -Ф Ф=4 в трехкомпонентной системе: 0=3+2 -Ф Ф=5 При постоянном давлении С=К+1 -Ф
При наличии, например, воды и пара С=1+2 -2=1 Максимальное количество фаз, которое может существовать одновременно: в двухкомпонетной системе: 0=2+2 -Ф Ф=4 в трехкомпонентной системе: 0=3+2 -Ф Ф=5 При постоянном давлении С=К+1 -Ф