5d5111b5c0f75a7ae2fceddf33c2193a.ppt
- Количество слайдов: 16
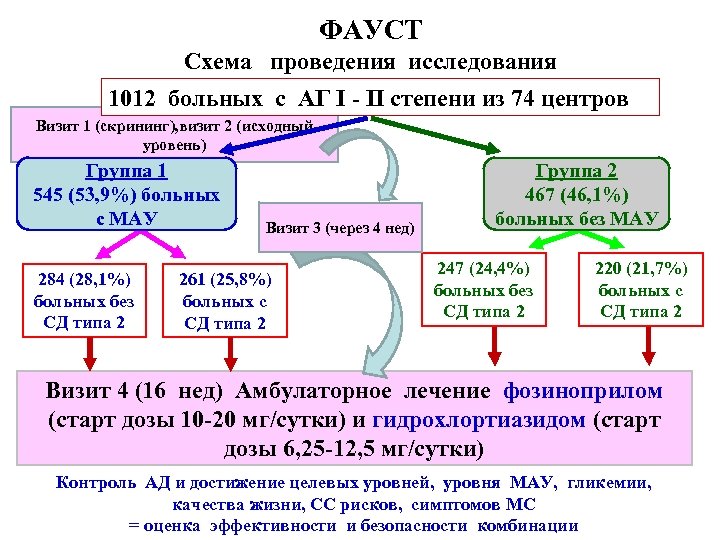
ФАУСТ Схема проведения исследования 1012 больных с АГ I - II степени из 74 центров Визит 1 (скрининг), визит 2 (исходный уровень) Группа 1 545 (53, 9%) больных с МАУ 284 (28, 1%) больных без СД типа 2 Визит 3 (через 4 нед) 261 (25, 8%) больных с СД типа 2 Группа 2 467 (46, 1%) больных без МАУ 247 (24, 4%) больных без СД типа 2 220 (21, 7%) больных с СД типа 2 Визит 4 (16 нед) Амбулаторное лечение фозиноприлом (старт дозы 10 -20 мг/сутки) и гидрохлортиазидом (старт дозы 6, 25 -12, 5 мг/сутки) Контроль АД и достижение целевых уровней, уровня МАУ, гликемии, качества жизни, СС рисков, симптомов МС = оценка эффективности и безопасности комбинации

ФАУСТ, цели исследования Первичные: Ø Оценить эффективность применения комбинации препаратов Фозиноприл и Гидрохлортиазид в течение 16 недель лечения у пациентов с I (мягкой) или II степенью (умеренной) эссенциальной АГ. Ø Оценить наличие/отсутствие МАУ у пациентов в начале программы и по завершении 16 недель лечения (для пациентов с исходно определяемой МАУ). Вторичные: Ø оценить данные по безопасности применения комбинации препаратов Фозиноприл и Гидрохлортиазид; Ø оценить качество жизни, риск развития сердечно-сосудистых заболеваний; Ø определить долю пациентов с МС среди пациентов, принимающих участие в программе; Ø оценить изменение выраженности симптомов МС среди пациентов, принимающих участие в программе, после 16 недель лечения Фозиноприлом и Гидрохлортиазидом.

ФАУСТ, оценка эффективности лечения Первичная переменная эффективности: Ø Достижение целевых уровней АД (для подгруппы пациентов с СД целевым считался уровень АД 130/80 мм рт. ст. , для подгруппы пациентов без СД - 140/90 рт. ст. Или снижение САД на 20 мм рт. ст. и более по сравнению с исходным уровнем у всех пациентов. Или снижение ДАД на 10 мм рт. ст. и более по сравнению с исходным уровнем у всех пациентов. Вторичные переменные эффективности: Ø Ø Ø микроальбуминурия качество жизни пациентов сердечно-сосудистый риск пациентов симптомы метаболического синдрома. Безопасность оценивалась на основании данных о регистрируемых в течение программы нежелательных явлениях, жизненно-важных показателях и на оценке лабораторных параметров.

Критерии включения Ø Возраст пациента от 18 до 80 лет. Ø Уровень САД 140 -179 мм рт. ст. и/или ДАД 90 -109 мм рт. ст. , что соответствует АГ I – II степени (мягкая или умеренная). Ø Отсутствие приема ингибиторов АПФ, АРА, диуретиков в течение хотя бы 2 -х недель до начала скрининга (визит 1). Ø Нерегулярная, неэффективная или не проводимая ранее антигипертензивная терапия. Ø Подписанное информированное согласие пациента на участие в программе. Ø Наличие МАУ у 50% пациентов. МАУ исследовалась трижды и больной включался только по результатам всех 3 или 2 одинаковых повторившихся результатов. Пациенты с макроальбуминурией исключались. Ø Среди пациентов как с МАУ, так и без МАУ должен был присутствовать СД типа 2.

ФАУСТ Исходная характеристика больных в сравниваемых группах показате ль МАУ без СД МАУ + СД Без МАУ без СД Без МАУ + СД Возраст 53, 4± 10, 9 57, 5± 9, 2 53, 0± 10, 3 57, 1± 8, 8 р<0, 001 Пол, м/ж 131 (46. 1%) / 153(53. 9%) р<0, 001 86 (39. 1%) / 99 (40. 1%) / 134(60. 9%) 147(59. 5%) 97(37. 2%) / 164(62. 8%) р=0, 037 Курение, % 23, 2 11, 9 18, 2 II степень АГ, % 81, 7 87, 7 66 САД, мм рт. ст. 157, 2 + 12, 2 160, 0 + 10, 9 154, 5 + 12, 1 ДАД, мм рт. ст. 94, 7 + 7, 3 95, 7 + 8, 1 93, 9 + 8, 5 94, 3 + 6, 8 ЧСС, уд. мин 73, 3 + 8, 2 75, 1 + 7, 5 73, 0 + 7, 3 73, 7 + 6, 3 р<0, 001 20, 5 р<0, 001 р=0, 04 р<0, 001 77, 3 р=0, 005 156, 9 + 11, 2 р=0, 032
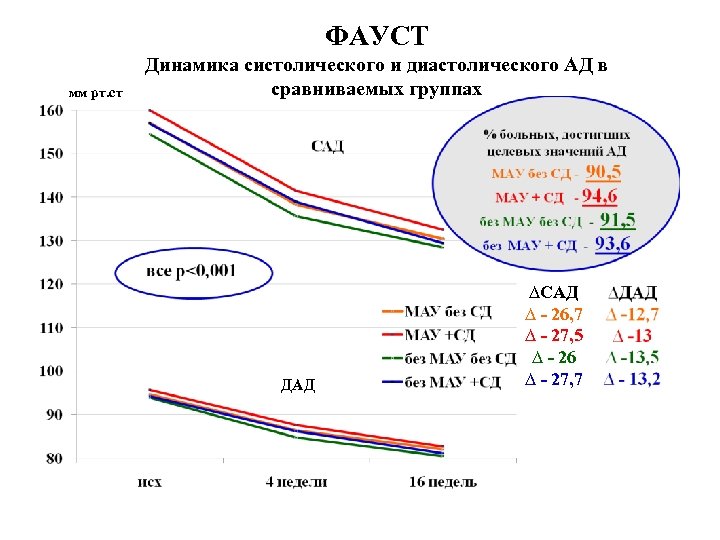
ФАУСТ мм рт. ст Динамика систолического и диастолического АД в сравниваемых группах ДАД ∆САД ∆ - 26, 7 ∆ - 27, 5 ∆ - 26 ∆ - 27, 7
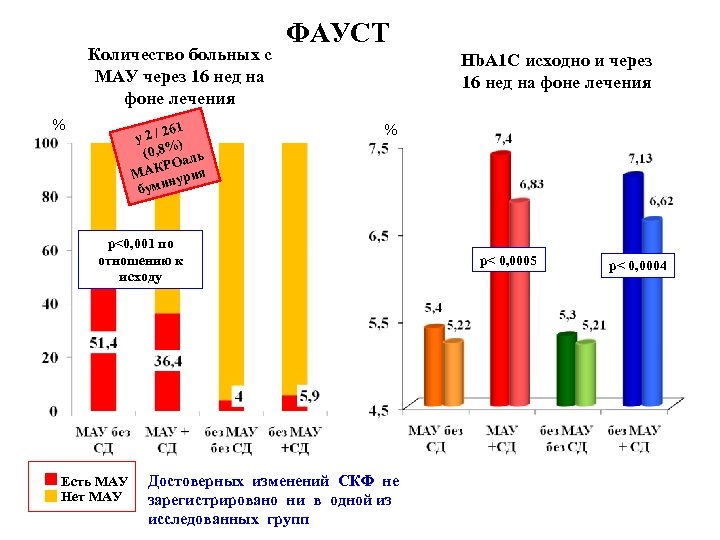
Количество больных с МАУ через 16 нед на фоне лечения % 261 у2/ ) (0, 8% аль РО МАК урия н буми ФАУСТ Hb. A 1 C исходно и через 16 нед на фоне лечения % p<0, 001 по отношению к исходу Есть МАУ Нет МАУ Достоверных изменений СКФ не зарегистрировано ни в одной из исследованных групп p< 0, 0005 p< 0, 0004
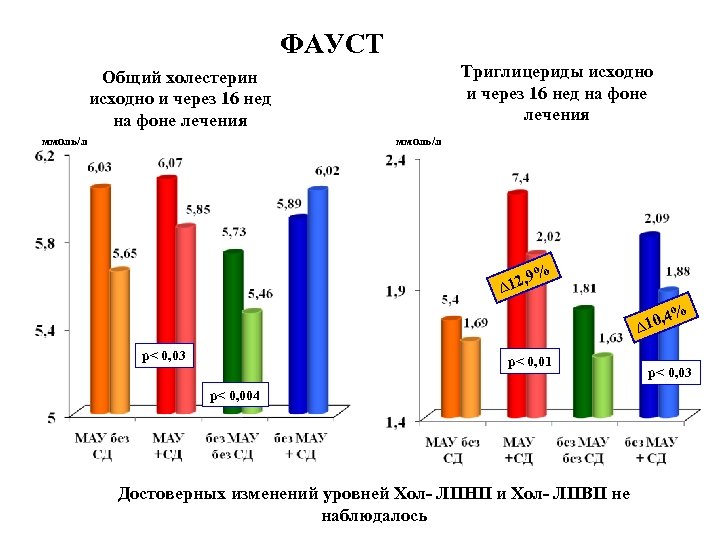
ФАУСТ Триглицериды исходно и через 16 нед на фоне лечения Общий холестерин исходно и через 16 нед на фоне лечения ммоль/л , 9 ∆12 % % , 4 ∆10 p< 0, 03 p< 0, 01 p< 0, 004 Достоверных изменений уровней Хол- ЛПНП и Хол- ЛПВП не наблюдалось p< 0, 03
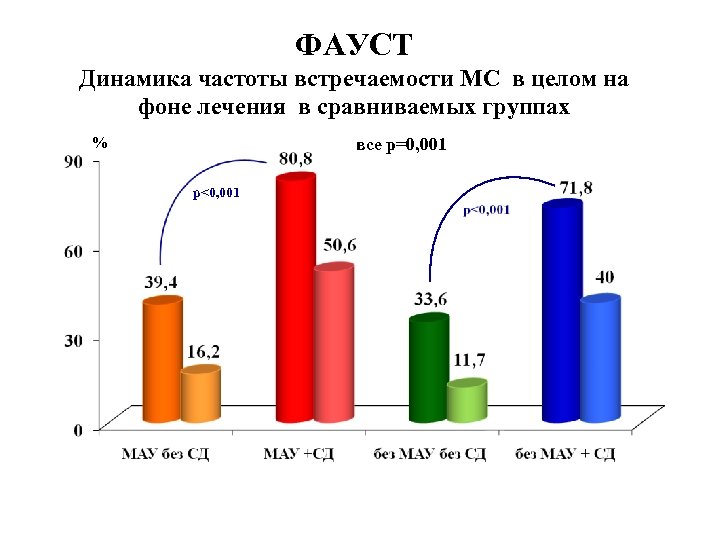
ФАУСТ Динамика частоты встречаемости МС в целом на фоне лечения в сравниваемых группах % все р=0, 001 р<0, 001
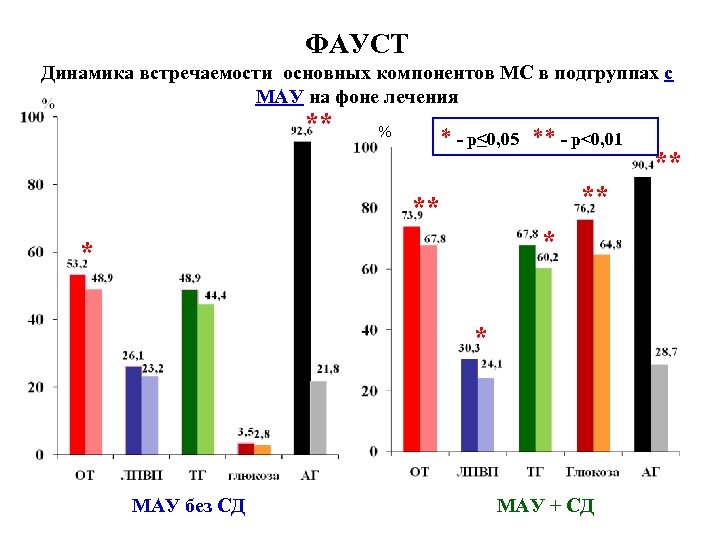
ФАУСТ Динамика встречаемости основных компонентов МС в подгруппах с МАУ на фоне лечения ** % * - р≤ 0, 05 ** - p<0, 01 ** ** * МАУ без СД МАУ + СД **
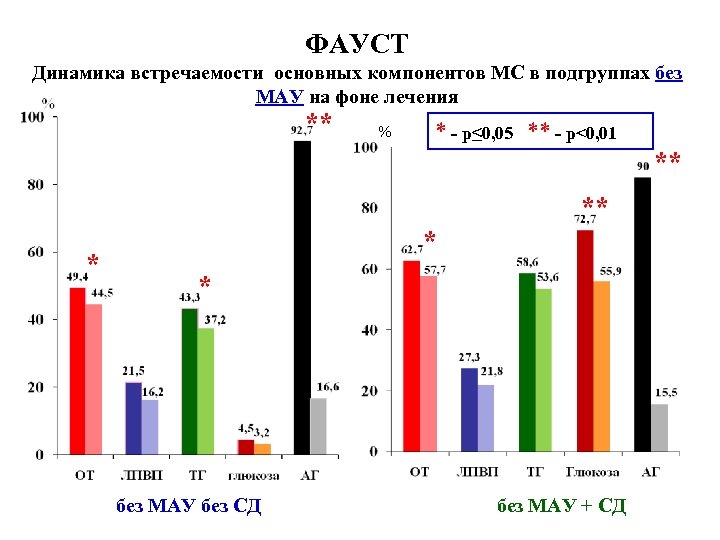
ФАУСТ Динамика встречаемости основных компонентов МС в подгруппах без МАУ на фоне лечения ** % * - р≤ 0, 05 ** - p<0, 01 ** ** * без МАУ без СД без МАУ + СД
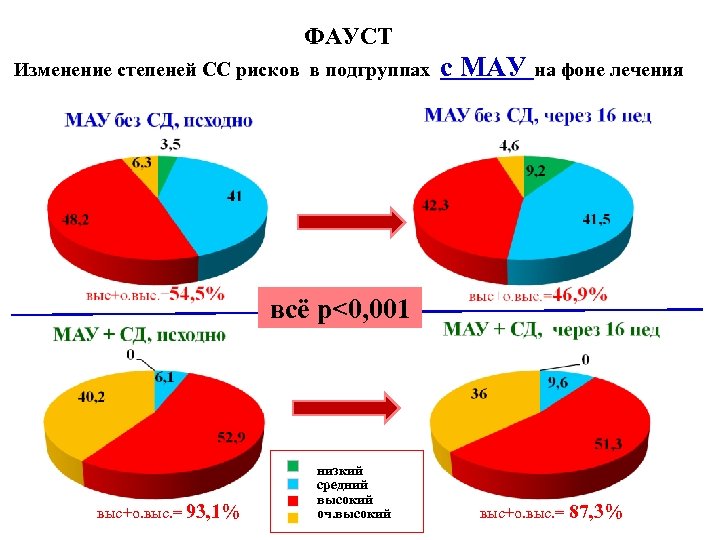
ФАУСТ Изменение степеней СС рисков в подгруппах с МАУ на фоне лечения всё p<0, 001 выс+о. выс. = 93, 1% низкий средний высокий оч. высокий выс+о. выс. = 87, 3%
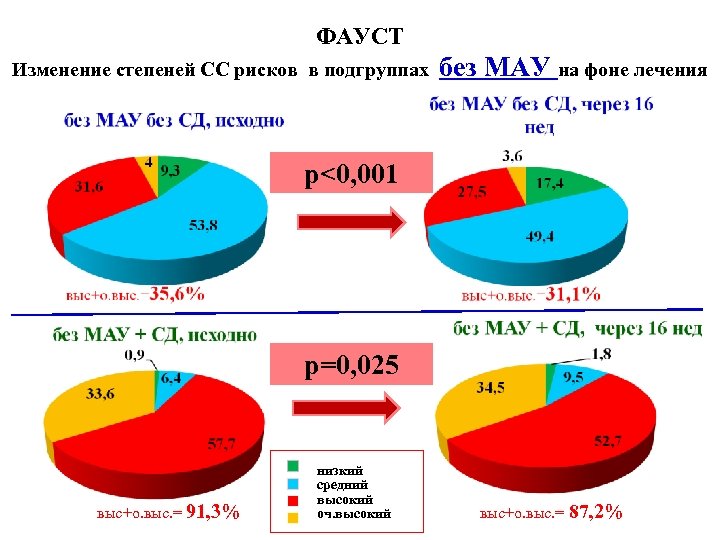
ФАУСТ Изменение степеней СС рисков в подгруппах без МАУ на фоне лечения p<0, 001 р=0, 025 выс+о. выс. = 91, 3% низкий средний высокий оч. высокий выс+о. выс. = 87, 2%
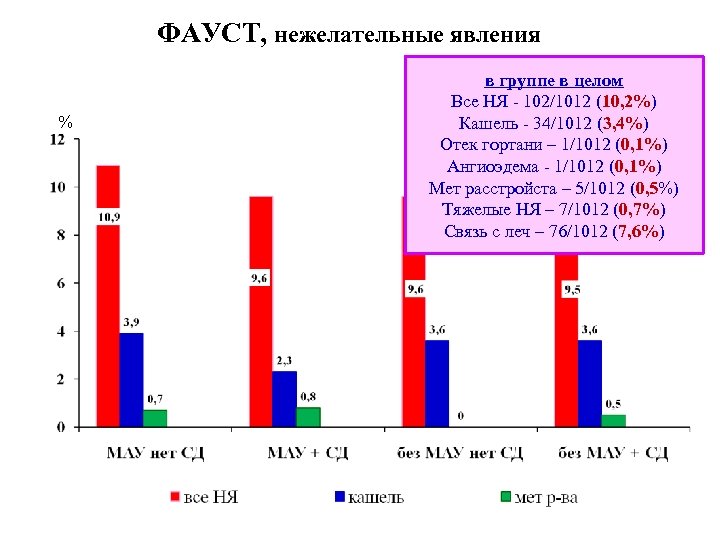
ФАУСТ, нежелательные явления % в группе в целом Все НЯ - 102/1012 (10, 2%) Кашель - 34/1012 (3, 4%) Отек гортани – 1/1012 (0, 1%) Ангиоэдема - 1/1012 (0, 1%) Мет расстройста – 5/1012 (0, 5%) Тяжелые НЯ – 7/1012 (0, 7%) Связь с леч – 76/1012 (7, 6%)
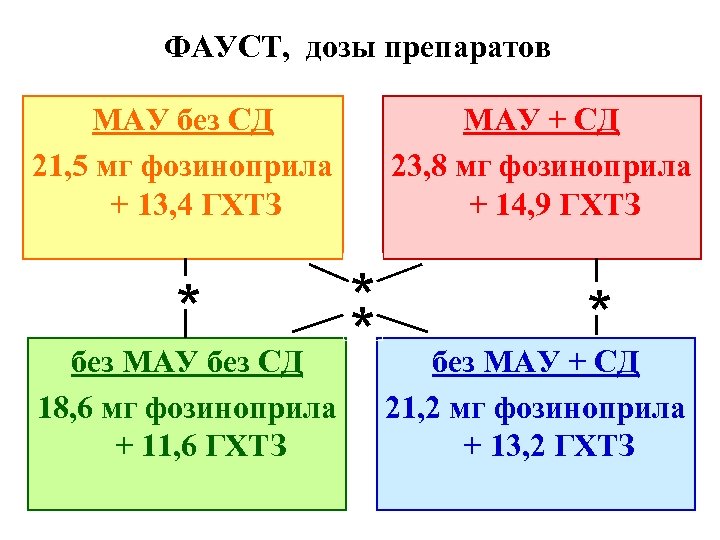
ФАУСТ, дозы препаратов МАУ без СД 21, 5 мг фозиноприла + 13, 4 ГХТЗ * без МАУ без СД 18, 6 мг фозиноприла + 11, 6 ГХТЗ МАУ + СД 23, 8 мг фозиноприла + 14, 9 ГХТЗ * * * без МАУ + СД 21, 2 мг фозиноприла + 13, 2 ГХТЗ

ФАУСТ, выводы Ø Терапия комбинацией ФОЗИНОПРИЛА с ГХТЗ (средние дозы 21, 2+13, 2 мг) позволяет нормализовать АД у подавляющего числа б-х с АГ (более 90%), в том числе с сопутствующей МАУ и/или СД Ø Лечение позволяет достоверно снизить частоту МАУ вдвое для больных без СД и на 2/3 для больных с СД Ø Достоверно снижается число больных с МС, а также высоким и очень высоким СС риском во всех исследуемых подгруппах Ø Проводимое лечение высоко безопасно Ø Фозиноприл успешно нивелирует возможные недостатки ГХТЗ и такая комбинация может быть рекомендована как средство «первой линии» для лечения пациентов с осложненной АГ в сочетании с нарушением функции почек и сахарным диабетом
5d5111b5c0f75a7ae2fceddf33c2193a.ppt