24.09.12.ppt
- Количество слайдов: 113
 Фармакология - наука по изысканию новых лекарственных веществ и изучению их действия на живой организм
Фармакология - наука по изысканию новых лекарственных веществ и изучению их действия на живой организм
 РАЗДЕЛЫ ФАРМАКОЛОГИИ 1. Теоретическая (история, теории, концепции, методы, расчёты и т. д. ); 2. Экспериментальная (фундаментальная); 3. Клиническая
РАЗДЕЛЫ ФАРМАКОЛОГИИ 1. Теоретическая (история, теории, концепции, методы, расчёты и т. д. ); 2. Экспериментальная (фундаментальная); 3. Клиническая
 КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ это совокупность научно-обоснованных принципов рационального выбора лекарственных средств для терапии заболевания или синдрома, индивидуального подбора фармакологических препаратов каждому больному, а также комплекс методов контроля терапевтической эффективности и безопасности лекарств
КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ это совокупность научно-обоснованных принципов рационального выбора лекарственных средств для терапии заболевания или синдрома, индивидуального подбора фармакологических препаратов каждому больному, а также комплекс методов контроля терапевтической эффективности и безопасности лекарств
 Терапия Инф. болезни Патологическая физиология Анатомия Хирургия Стоматология ЛОР-болезни ФАРМАКОЛОГИЯ (общая, частная, клиническая, экспериментальная) Гистология Биология Педиатрия Акушерство Патологическая анатомия Физиология Микробиология Биохимия
Терапия Инф. болезни Патологическая физиология Анатомия Хирургия Стоматология ЛОР-болезни ФАРМАКОЛОГИЯ (общая, частная, клиническая, экспериментальная) Гистология Биология Педиатрия Акушерство Патологическая анатомия Физиология Микробиология Биохимия
 История фармакологии (1) Дата Открытия Авторы Первое из известных описаний лекарственных средств в Египте Папирус. Эбер XVI в. до (упоминаются опий, гиосциламус, са (автор н. э. слабительное из растения клещевина, неизвестен) мята, бальзамы, печень и др. ) IV-III в. Систематизация показаний к применению Гиппократ до н. э. лекарственных средств древней медицины. Описание более 900 лекарственных I в. н. э. Диоскорид средств (применяемых) Разработка принципов лечебного и профилактического назначения II в. н. э. лекарственных средств. Первые шаги к Гален очистки лекарственных средств от балластных элементов.
История фармакологии (1) Дата Открытия Авторы Первое из известных описаний лекарственных средств в Египте Папирус. Эбер XVI в. до (упоминаются опий, гиосциламус, са (автор н. э. слабительное из растения клещевина, неизвестен) мята, бальзамы, печень и др. ) IV-III в. Систематизация показаний к применению Гиппократ до н. э. лекарственных средств древней медицины. Описание более 900 лекарственных I в. н. э. Диоскорид средств (применяемых) Разработка принципов лечебного и профилактического назначения II в. н. э. лекарственных средств. Первые шаги к Гален очистки лекарственных средств от балластных элементов.
 История фармакологии (2) Дата Открытия Систематизация лекарственных средств и показаний к их примению. Авторы Абу-Али. Ибн X-XI в. Сина(Авиценна) Филиппус. Теофрас Внедрение в практическую медицину тус. Бомбастус фон XV-XVI в. солей металлов (ртуть — для лечения Гогенхейм(Парац сифилиса) ельс) Внедрение в медицину препаратов 1785 г. Уитеринг наперстянки Выделения из опия алкалоиды 1806 г. Сертюрнер морфина Внедрение экспериментов на 1809 г. животных в фармакологию. Анализ Мажанди действия стрихнина. Выделение из коры хинного дерева 1820 г. Пеллетье, Кавенту алкалоида хинина.
История фармакологии (2) Дата Открытия Систематизация лекарственных средств и показаний к их примению. Авторы Абу-Али. Ибн X-XI в. Сина(Авиценна) Филиппус. Теофрас Внедрение в практическую медицину тус. Бомбастус фон XV-XVI в. солей металлов (ртуть — для лечения Гогенхейм(Парац сифилиса) ельс) Внедрение в медицину препаратов 1785 г. Уитеринг наперстянки Выделения из опия алкалоиды 1806 г. Сертюрнер морфина Внедрение экспериментов на 1809 г. животных в фармакологию. Анализ Мажанди действия стрихнина. Выделение из коры хинного дерева 1820 г. Пеллетье, Кавенту алкалоида хинина.
 История фармакологии (3) Дата Открытия 1831 г. Выделение алкалоида атропина Применение для хирургического наркоза 1844 г. азота закиси. Первая демонстрация наркотического 1846 г. действия эфира. Применение для хирургического наркоза 1847 г. хлороформа. 1848 г. Выделение из опия алкалоиды папаверина 1850 г. Установление механизма действия Кураре Внедрение в практику снотворного 1869 г. средства хлоргидрата. Применение нитроглицерина для лечения 1879 г. «грудной жабы» Открытие анестезирующих свойств у 1879 г. кокаина. Авторы Майн Уэллс Мортон Симпсон Мерк Бернар Либрих Меррил Анреп.
История фармакологии (3) Дата Открытия 1831 г. Выделение алкалоида атропина Применение для хирургического наркоза 1844 г. азота закиси. Первая демонстрация наркотического 1846 г. действия эфира. Применение для хирургического наркоза 1847 г. хлороформа. 1848 г. Выделение из опия алкалоиды папаверина 1850 г. Установление механизма действия Кураре Внедрение в практику снотворного 1869 г. средства хлоргидрата. Применение нитроглицерина для лечения 1879 г. «грудной жабы» Открытие анестезирующих свойств у 1879 г. кокаина. Авторы Майн Уэллс Мортон Симпсон Мерк Бернар Либрих Меррил Анреп.
 История фармакологии (4) Дата Открытия Авторы Получение синтетического анестетика 1904 г. Эйнхорн новокаина. Разработка общих принципов Начало химиотерапии. Получение и применение Эрлих XIX в. противоспирохетозного средства сальварсана 1911 г. Выделение первого витамина (В 1) Функ 1916 – Мак-Лен, Выделение гепарина 1917 гг. Хауэл 1921 – Выделение инсулина Бентинг, Бест 1922 гг. 1929 г. Открытие пенициллина Флеминг 1937 г. Открытие противогистаминных средств Бовэ 1943 – Выделение и применение в медицинской Кэндал, Райх 1949 гг. практике кортизона. штейш, Хенч
История фармакологии (4) Дата Открытия Авторы Получение синтетического анестетика 1904 г. Эйнхорн новокаина. Разработка общих принципов Начало химиотерапии. Получение и применение Эрлих XIX в. противоспирохетозного средства сальварсана 1911 г. Выделение первого витамина (В 1) Функ 1916 – Мак-Лен, Выделение гепарина 1917 гг. Хауэл 1921 – Выделение инсулина Бентинг, Бест 1922 гг. 1929 г. Открытие пенициллина Флеминг 1937 г. Открытие противогистаминных средств Бовэ 1943 – Выделение и применение в медицинской Кэндал, Райх 1949 гг. практике кортизона. штейш, Хенч
 История фармакологии (5) Дата Открытия Авторы Выделение противотуберкулезного 1944 г. Ваксман средства стрептомицина Получение и применение в медицинской Шарпантье, К 1950 – практике первого нейтролептика — урвуазье, Лаб 1952 гг. аминазина орн. Внедрение в практику первого противодиабетического средства из группы 1954 г. Франке, Фукс производных сульфонилмочевины, эффективного приеме внутрь
История фармакологии (5) Дата Открытия Авторы Выделение противотуберкулезного 1944 г. Ваксман средства стрептомицина Получение и применение в медицинской Шарпантье, К 1950 – практике первого нейтролептика — урвуазье, Лаб 1952 гг. аминазина орн. Внедрение в практику первого противодиабетического средства из группы 1954 г. Франке, Фукс производных сульфонилмочевины, эффективного приеме внутрь
 История фармакологии (6) Дата 1958 г. 1966 г. 1972 г. Открытия Получение первого блокатора aадренорецепторов Синтез инсулина Получение блокаторов Н 2 гистаминорецепторов 1975 – Выделение эндогенных болеутоляющих 1976 гг. веществ — энкефалинов и эндорфинов Авторы Пауэлл, Слэте р Катсоянис Юлэк Хьюз, Костер лиц, Ерениус, Ли
История фармакологии (6) Дата 1958 г. 1966 г. 1972 г. Открытия Получение первого блокатора aадренорецепторов Синтез инсулина Получение блокаторов Н 2 гистаминорецепторов 1975 – Выделение эндогенных болеутоляющих 1976 гг. веществ — энкефалинов и эндорфинов Авторы Пауэлл, Слэте р Катсоянис Юлэк Хьюз, Костер лиц, Ерениус, Ли
 История фармакологии 1847 -1848 гг. Дерпт (Юрьев) профессор Рудольф Бухгейм открытие первой экспериментальной фармакологической лаборатории
История фармакологии 1847 -1848 гг. Дерпт (Юрьев) профессор Рудольф Бухгейм открытие первой экспериментальной фармакологической лаборатории
 24. 2. (8. 3). 1865, Рязань, — 24. 4. 1924, Ленинград русский фармаколог, основоположник отечественной фармакологии член-корреспондент Российской АН (1920), академик Военно-медицинской академии (1914). Николай Павлович Кравков
24. 2. (8. 3). 1865, Рязань, — 24. 4. 1924, Ленинград русский фармаколог, основоположник отечественной фармакологии член-корреспондент Российской АН (1920), академик Военно-медицинской академии (1914). Николай Павлович Кравков
 Лекарственное вещество • биологически активное вещество установленной структуры, которое применяются в определённых дозах для профилактики, лечения или диагностики заболеваний
Лекарственное вещество • биологически активное вещество установленной структуры, которое применяются в определённых дозах для профилактики, лечения или диагностики заболеваний
 Лекарственная форма • это форма лекарственного вещества удобная для хранения и применения. Существуют твёрдые, мягкие и жидкие лекарственные формы
Лекарственная форма • это форма лекарственного вещества удобная для хранения и применения. Существуют твёрдые, мягкие и жидкие лекарственные формы
 НОВЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ • ПРЕДНАЗНАЧЕНЫ ДЛЯ КОНТРОЛИРУЕМОЙ ДОСТАВКИ ЛЕКАРСТВЕПННОГО ВЕЩЕСТВА В ОПРЕДЕЛЁННЫЕ УЧАСТКИ ОРГАНИЗМА С ЦЕЛЬЮ УПРАВЛЕНИЯ ТЕРАПЕВТИЧЕСКИМ ЭФФЕКТОМ
НОВЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ • ПРЕДНАЗНАЧЕНЫ ДЛЯ КОНТРОЛИРУЕМОЙ ДОСТАВКИ ЛЕКАРСТВЕПННОГО ВЕЩЕСТВА В ОПРЕДЕЛЁННЫЕ УЧАСТКИ ОРГАНИЗМА С ЦЕЛЬЮ УПРАВЛЕНИЯ ТЕРАПЕВТИЧЕСКИМ ЭФФЕКТОМ
 ЗАДАЧИ СОЗДАНИЯ НОВЫХ СИСТЕМ И СРЕДСТВ ДОСТАВКИ ЛЕКАРСТВ • 1. ПОВЫШЕНИЕ БИОДОСТУПНОСТИ, • 2. УВЕЛИЧЕНИЕ ДЛИТЕЛЬНОСТИ ДЕЙСТВИЯ, • 3. ЦЕЛЕНАПРАВЛЕННАЯ ДОСТАВКА К ФАРМАКОЛОГИЧЕСКОЙ МИШЕНИ.
ЗАДАЧИ СОЗДАНИЯ НОВЫХ СИСТЕМ И СРЕДСТВ ДОСТАВКИ ЛЕКАРСТВ • 1. ПОВЫШЕНИЕ БИОДОСТУПНОСТИ, • 2. УВЕЛИЧЕНИЕ ДЛИТЕЛЬНОСТИ ДЕЙСТВИЯ, • 3. ЦЕЛЕНАПРАВЛЕННАЯ ДОСТАВКА К ФАРМАКОЛОГИЧЕСКОЙ МИШЕНИ.
 ВИДЫ ПЕРОРАЛЬНЫХ ЛЕКАРСТВЕННЫХ ФОРМ С МОДИФИЦИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ • 1. УЛУЧШАЮЩИЕ РАСТВОРИМОСТЬ, ВСАСЫВАНИЕ, ПОВЫШАЮЩИЕ БИОДОСТУПНОСТЬ, • 2. С КОНТРОЛИРУЕМЫМ ВЫСВОБОЖДЕНИЕМ Л. В. , • 3. С ПУЛЬСИРУЮЩИМ ИЛИ ОТСРОЧЕННЫМ ВЫСВОБОЖДЕНИЕМ Л. В. , • 4. С ЦЕЛЕНАПРАВЛЕННЫМ ВЫСВОБОЖДЕНИЕМ Л. В. В РАЗНЫХ ОТДЕЛАХ ЖКТ.
ВИДЫ ПЕРОРАЛЬНЫХ ЛЕКАРСТВЕННЫХ ФОРМ С МОДИФИЦИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ • 1. УЛУЧШАЮЩИЕ РАСТВОРИМОСТЬ, ВСАСЫВАНИЕ, ПОВЫШАЮЩИЕ БИОДОСТУПНОСТЬ, • 2. С КОНТРОЛИРУЕМЫМ ВЫСВОБОЖДЕНИЕМ Л. В. , • 3. С ПУЛЬСИРУЮЩИМ ИЛИ ОТСРОЧЕННЫМ ВЫСВОБОЖДЕНИЕМ Л. В. , • 4. С ЦЕЛЕНАПРАВЛЕННЫМ ВЫСВОБОЖДЕНИЕМ Л. В. В РАЗНЫХ ОТДЕЛАХ ЖКТ.
 РАЗЛИЧНЫЕ ВИДЫ МАТРИКСОВ ЛЕКАРСТВ Гелеобразующий растворимый нерастворимый матриксы
РАЗЛИЧНЫЕ ВИДЫ МАТРИКСОВ ЛЕКАРСТВ Гелеобразующий растворимый нерастворимый матриксы
 ТЕХНОЛОГИИ МОДИФИЦИРОВАННОГО ВЫСВОБОЖДЕНИЯ Л. В. • 1. МАТРИКСНЫЕ ТАБЛЕТКИ, • 2. ОСМОТИЧЕСКИЕ СИСТЕМЫ, • 3. РЕЗЕРВУАРНЫЕ СИСТЕМЫ С ДОЗИРУЮЩИМИ ОБОЛОЧКАМИ, • 4. МНОЖЕСТВЕННЫЕ МИКРОГРАНУЛЫ (ПИЛЛЕТЫ),
ТЕХНОЛОГИИ МОДИФИЦИРОВАННОГО ВЫСВОБОЖДЕНИЯ Л. В. • 1. МАТРИКСНЫЕ ТАБЛЕТКИ, • 2. ОСМОТИЧЕСКИЕ СИСТЕМЫ, • 3. РЕЗЕРВУАРНЫЕ СИСТЕМЫ С ДОЗИРУЮЩИМИ ОБОЛОЧКАМИ, • 4. МНОЖЕСТВЕННЫЕ МИКРОГРАНУЛЫ (ПИЛЛЕТЫ),
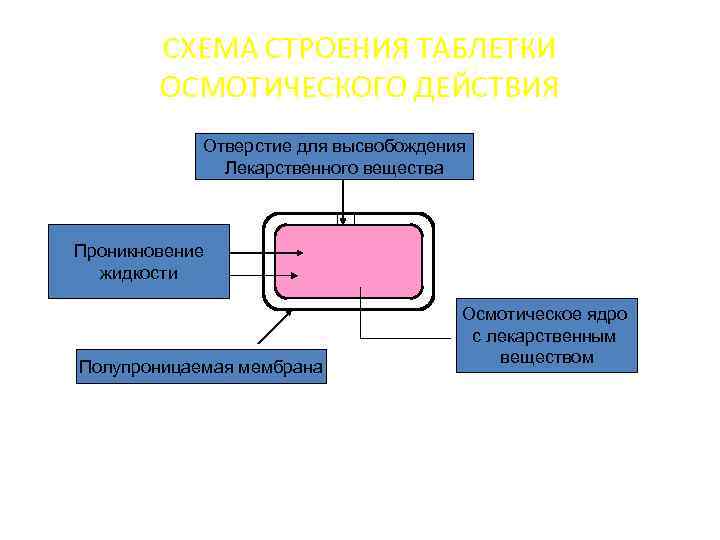 СХЕМА СТРОЕНИЯ ТАБЛЕТКИ ОСМОТИЧЕСКОГО ДЕЙСТВИЯ Отверстие для высвобождения Лекарственного вещества Проникновение жидкости Полупроницаемая мембрана Осмотическое ядро с лекарственным веществом
СХЕМА СТРОЕНИЯ ТАБЛЕТКИ ОСМОТИЧЕСКОГО ДЕЙСТВИЯ Отверстие для высвобождения Лекарственного вещества Проникновение жидкости Полупроницаемая мембрана Осмотическое ядро с лекарственным веществом
 отверстие Высвобождение Лекарственного вещества Наружная Полупроницаемая мембрана Слой осмотического вещества Барьерный слой Исходное состояние Действие в ЖКТ
отверстие Высвобождение Лекарственного вещества Наружная Полупроницаемая мембрана Слой осмотического вещества Барьерный слой Исходное состояние Действие в ЖКТ
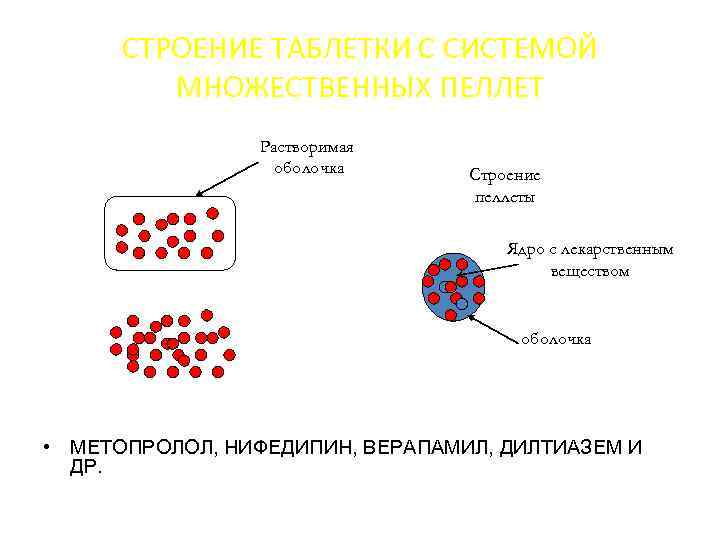 СТРОЕНИЕ ТАБЛЕТКИ С СИСТЕМОЙ МНОЖЕСТВЕННЫХ ПЕЛЛЕТ Растворимая оболочка Строение пеллеты Ядро с лекарственным веществом оболочка • МЕТОПРОЛОЛ, НИФЕДИПИН, ВЕРАПАМИЛ, ДИЛТИАЗЕМ И ДР.
СТРОЕНИЕ ТАБЛЕТКИ С СИСТЕМОЙ МНОЖЕСТВЕННЫХ ПЕЛЛЕТ Растворимая оболочка Строение пеллеты Ядро с лекарственным веществом оболочка • МЕТОПРОЛОЛ, НИФЕДИПИН, ВЕРАПАМИЛ, ДИЛТИАЗЕМ И ДР.
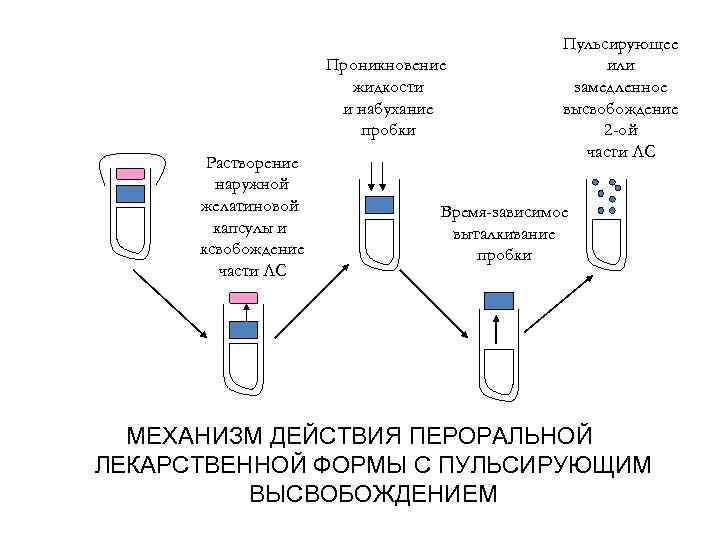 Проникновение жидкости и набухание пробки Растворение наружной желатиновой капсулы и ксвобождение части ЛС Пульсирующее или замедленное высвобождение 2 -ой части ЛС Время-зависимое выталкивание пробки МЕХАНИЗМ ДЕЙСТВИЯ ПЕРОРАЛЬНОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ С ПУЛЬСИРУЮЩИМ ВЫСВОБОЖДЕНИЕМ
Проникновение жидкости и набухание пробки Растворение наружной желатиновой капсулы и ксвобождение части ЛС Пульсирующее или замедленное высвобождение 2 -ой части ЛС Время-зависимое выталкивание пробки МЕХАНИЗМ ДЕЙСТВИЯ ПЕРОРАЛЬНОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ С ПУЛЬСИРУЮЩИМ ВЫСВОБОЖДЕНИЕМ
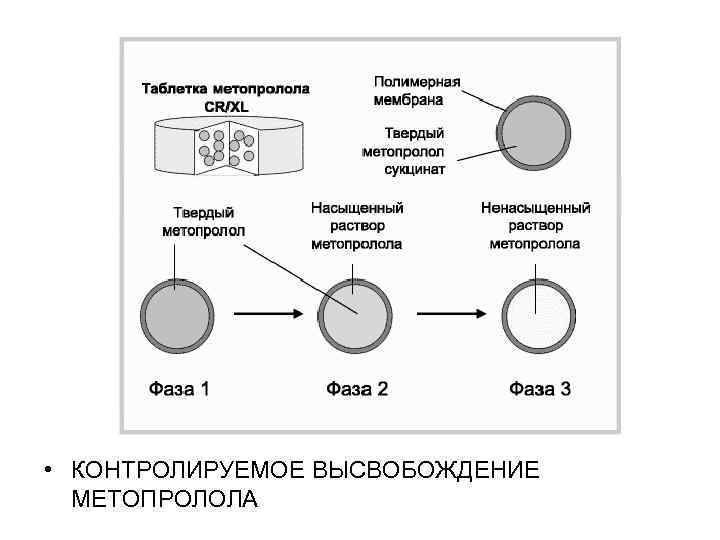 • КОНТРОЛИРУЕМОЕ ВЫСВОБОЖДЕНИЕ МЕТОПРОЛОЛА
• КОНТРОЛИРУЕМОЕ ВЫСВОБОЖДЕНИЕ МЕТОПРОЛОЛА
 ТРАНСДЕРМАЛЬНЫЕ ТЕРАПЕВТИЧЕСКИЕ СИСТЕМЫ • ЭТО СПЕЦИАЛЬНАЯ СЛОЖНАЯ ЛЕКАРСТВЕННАЯ ФОРМА, ПРЕДНАЗНАЧЕННАЯ ДЛЯ ВВЕДЕНИЯ ЛЕКАРСТВ ЧЕРЕЗ КОЖУ БЕЗ ИНЪЕКЦИЙ.
ТРАНСДЕРМАЛЬНЫЕ ТЕРАПЕВТИЧЕСКИЕ СИСТЕМЫ • ЭТО СПЕЦИАЛЬНАЯ СЛОЖНАЯ ЛЕКАРСТВЕННАЯ ФОРМА, ПРЕДНАЗНАЧЕННАЯ ДЛЯ ВВЕДЕНИЯ ЛЕКАРСТВ ЧЕРЕЗ КОЖУ БЕЗ ИНЪЕКЦИЙ.
 СТРОЕНИЕ КОЖИ • ТРУДНОПРОХОДИМА ДЛЯ ЛЕКАРСТВ
СТРОЕНИЕ КОЖИ • ТРУДНОПРОХОДИМА ДЛЯ ЛЕКАРСТВ
 СТРУКТУРА ТТС • 1. ОСНОВНАЯ МЕМБРАНА, ПРЕДОТВРАЩАЮЩАЯ ВЫСВОБОЖДЕНИЕ ЛВ, • 2. ЛЕКАРСТВЕННЫЙ РЕЗЕРВУАР, • 3. МЕМБАРАН ОБЕСПЕЧИВАЮЩАЯ ОПТИМАЛЬНУ. СКОРОСТЬ ВЫСВОБОЖДЕНИЯ ЛВ, • 4. КЛЕЙ, • 5. ЗАЩИТНАЯ ПЛЁНКА ДЛЯ ХРАНЕНИЯ СИСТЕМЫ.
СТРУКТУРА ТТС • 1. ОСНОВНАЯ МЕМБРАНА, ПРЕДОТВРАЩАЮЩАЯ ВЫСВОБОЖДЕНИЕ ЛВ, • 2. ЛЕКАРСТВЕННЫЙ РЕЗЕРВУАР, • 3. МЕМБАРАН ОБЕСПЕЧИВАЮЩАЯ ОПТИМАЛЬНУ. СКОРОСТЬ ВЫСВОБОЖДЕНИЯ ЛВ, • 4. КЛЕЙ, • 5. ЗАЩИТНАЯ ПЛЁНКА ДЛЯ ХРАНЕНИЯ СИСТЕМЫ.
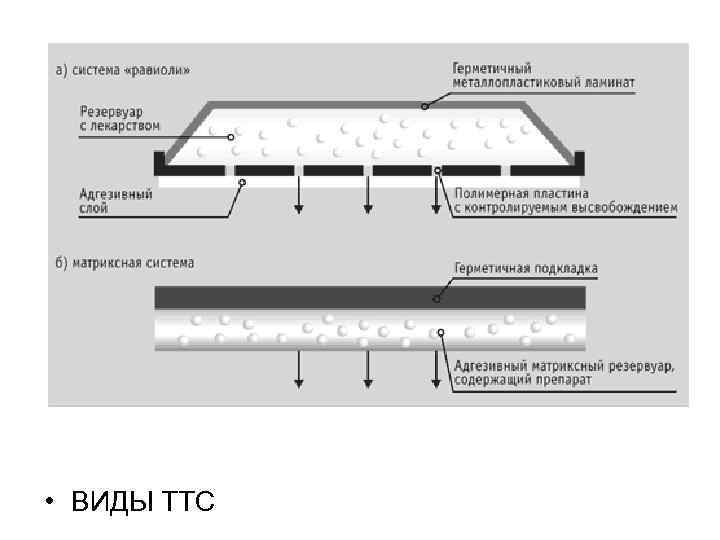 • ВИДЫ ТТС
• ВИДЫ ТТС

 Лекарственный препарат • это лекарственное средство в определённой дозе и лекарственной форме
Лекарственный препарат • это лекарственное средство в определённой дозе и лекарственной форме
 НАНОТЕХНОЛОГИИ В ФАРМАКОЛОГИИ • НАНОТЕХНОЛОГИИ ОПЕРИРУЮТ C ОБЪЕКТАМИ НАНОМЕТРИЧЕСКОГО РАЗМЕРА (ОТ ГРЕЧ. NANNOS – » КАРЛИК» ) НАЗЫВАЮТСЯ НАНОТЕХНОЛОГИЯМИ. ЭТИ ОБЪЕКТЫ ИСЧИСЛЯЮТСЯ МИЛЛИАРДНЫМИ ДОЛЯМИ МЕТРА (10 -9)
НАНОТЕХНОЛОГИИ В ФАРМАКОЛОГИИ • НАНОТЕХНОЛОГИИ ОПЕРИРУЮТ C ОБЪЕКТАМИ НАНОМЕТРИЧЕСКОГО РАЗМЕРА (ОТ ГРЕЧ. NANNOS – » КАРЛИК» ) НАЗЫВАЮТСЯ НАНОТЕХНОЛОГИЯМИ. ЭТИ ОБЪЕКТЫ ИСЧИСЛЯЮТСЯ МИЛЛИАРДНЫМИ ДОЛЯМИ МЕТРА (10 -9)
 ОБЛАСТИ ПРИМЕНЕНИЯ НАНОТЕХНОЛОГИЙ • 1. АНАЛИТИЧЕСКИЕ НАНОТЕХНОЛОГИИ ДЛЯ ДИАГНОСТИКИ. • 2. НАНОТЕХНОЛОГИИ ДЛЯ ТРАНСПОРТА ЛЕКАРСТВ. • 3. НАНОМАТЕРИАЛЫ. • 4. НАНОРОБОТЫ В МЕДИЦИНЕ.
ОБЛАСТИ ПРИМЕНЕНИЯ НАНОТЕХНОЛОГИЙ • 1. АНАЛИТИЧЕСКИЕ НАНОТЕХНОЛОГИИ ДЛЯ ДИАГНОСТИКИ. • 2. НАНОТЕХНОЛОГИИ ДЛЯ ТРАНСПОРТА ЛЕКАРСТВ. • 3. НАНОМАТЕРИАЛЫ. • 4. НАНОРОБОТЫ В МЕДИЦИНЕ.
 ПУТИ ИСПОЛЬЗОВАНИЯ НАНОЧАСТИЦ ДЛЯ СОЗДАНИЯ ЛЕКАРСТВ • 1. ЛИПОСОМЫ (МУЛЬТИЛАМЕНАРНЫЕ ДО 10 МКМ И СОСТОЯЩИЕ ИЗ 1 ЛАМЕЛЫ -20 -50 НМ (ПЛАСТИНКИ) – ПРЕПАРАТ ЦЕЛИКС. • 2. НАНОСФЕРЫ, НА КОТОРЫХ РАПРЕДЕЛЯЕТСЯ АКТИВНОЕ ВЕЩЕСТВО – ПРЕПАРАТ ПЕГАСИС (ЛЕЧ. ГЕПАТИТА С). • 3. НАНОКАПСУЛЫ СОСТОЯЩИЕ ИЗ ПОЛИМЕРНОЙ ОБОЛОЧКИ, ОХВАТЫВАЮЩЕЙ ПОЛОСТЬ С ЖИДКОСТЬЮ – ПРЕПАРАТ НЕЙЛАСТА ДЛЯ ЛЕЧЕНИЯ НЕЙТРОПЕНИИ. • 4. АКТИВНЫЕ НАНОКРИСТАЛЛЫ (200 -600 НМ) В ВИДЕ СУСПЕНЗИИ. • 5. ДЕНДРИМЕРЫ (ДЕРЕВО) РАЗВЕРТВЛЁННЫЕ ДО РАЗМЕРОВ МЕЛКИХ ПРОТЕИНОВ, НА НИХ РАСПОЛАГАЕТСЯ ДЕЙСТВУЮЩЕЕ ВЕЩЕСТВО, ПРИМЕР – ВИВИГЕЛЬ, ДЛЯ ЛЕЧЕНИЯ СПИДА.
ПУТИ ИСПОЛЬЗОВАНИЯ НАНОЧАСТИЦ ДЛЯ СОЗДАНИЯ ЛЕКАРСТВ • 1. ЛИПОСОМЫ (МУЛЬТИЛАМЕНАРНЫЕ ДО 10 МКМ И СОСТОЯЩИЕ ИЗ 1 ЛАМЕЛЫ -20 -50 НМ (ПЛАСТИНКИ) – ПРЕПАРАТ ЦЕЛИКС. • 2. НАНОСФЕРЫ, НА КОТОРЫХ РАПРЕДЕЛЯЕТСЯ АКТИВНОЕ ВЕЩЕСТВО – ПРЕПАРАТ ПЕГАСИС (ЛЕЧ. ГЕПАТИТА С). • 3. НАНОКАПСУЛЫ СОСТОЯЩИЕ ИЗ ПОЛИМЕРНОЙ ОБОЛОЧКИ, ОХВАТЫВАЮЩЕЙ ПОЛОСТЬ С ЖИДКОСТЬЮ – ПРЕПАРАТ НЕЙЛАСТА ДЛЯ ЛЕЧЕНИЯ НЕЙТРОПЕНИИ. • 4. АКТИВНЫЕ НАНОКРИСТАЛЛЫ (200 -600 НМ) В ВИДЕ СУСПЕНЗИИ. • 5. ДЕНДРИМЕРЫ (ДЕРЕВО) РАЗВЕРТВЛЁННЫЕ ДО РАЗМЕРОВ МЕЛКИХ ПРОТЕИНОВ, НА НИХ РАСПОЛАГАЕТСЯ ДЕЙСТВУЮЩЕЕ ВЕЩЕСТВО, ПРИМЕР – ВИВИГЕЛЬ, ДЛЯ ЛЕЧЕНИЯ СПИДА.
 Лекарственное средство • Препарат, содержащий сумму действующих веществ разного или неустановленного строения (например, в растительном лекарственном сырье)
Лекарственное средство • Препарат, содержащий сумму действующих веществ разного или неустановленного строения (например, в растительном лекарственном сырье)
 Источники получения лекарств: 1. Лекарственные растения 2. Животный мир 3. Минералы 4. Микроорганизмы 5. Химический синтез
Источники получения лекарств: 1. Лекарственные растения 2. Животный мир 3. Минералы 4. Микроорганизмы 5. Химический синтез
 Пути поиска новых лекарственных веществ среди вновь синтезированных соединений: 1. 2. 3. 4. 5. Эмпирическое изучение Модификация известных химических структур Составление комбинированных препаратов Целенаправленный синтез Лекарственная биотехнология.
Пути поиска новых лекарственных веществ среди вновь синтезированных соединений: 1. 2. 3. 4. 5. Эмпирическое изучение Модификация известных химических структур Составление комбинированных препаратов Целенаправленный синтез Лекарственная биотехнология.
 Геномика • наука, занимающаяся изучением структуры и функций генов. Её технологии позволяют установить индивидуальную вариабельность организма на действие лекарственного вещества и на этой основе создавать эффективные и безопасные лекарственные средства.
Геномика • наука, занимающаяся изучением структуры и функций генов. Её технологии позволяют установить индивидуальную вариабельность организма на действие лекарственного вещества и на этой основе создавать эффективные и безопасные лекарственные средства.
 Протеомика • (от слов протеин и геномика) – наука, занимающаяся изучением совокупности белков и их взаимодействий в живых организмах. Она ориентирована на создание новых лекарственных средств, основой действия которых будут те или иные белки, а также на исследования действия препаратов на белковые совокупности и их взаимодействие в организме.
Протеомика • (от слов протеин и геномика) – наука, занимающаяся изучением совокупности белков и их взаимодействий в живых организмах. Она ориентирована на создание новых лекарственных средств, основой действия которых будут те или иные белки, а также на исследования действия препаратов на белковые совокупности и их взаимодействие в организме.
 Этапы изучения и внедрения новых ЛС: I Доклинические (экспериментальные) исследования II Клинические исследования (I-IV фазы)
Этапы изучения и внедрения новых ЛС: I Доклинические (экспериментальные) исследования II Клинические исследования (I-IV фазы)
 Стандарт GLP • ( «Good Laboratory Practice» , Надлежащая лабораторная практика) — система норм, правил и указаний, направленных на обеспечение согласованности и достоверности результатов лабораторных исследований.
Стандарт GLP • ( «Good Laboratory Practice» , Надлежащая лабораторная практика) — система норм, правил и указаний, направленных на обеспечение согласованности и достоверности результатов лабораторных исследований.
 Стандарт GCP • (Good Clinical Practice - Надлежащая клиническая практика) - международный стандарт этических норм и качества научных исследований, описывающий правила разработки, проведения, ведения документации и отчетности об исследованиях, которые подразумевают участие человека в качестве испытуемого (клинические исследования).
Стандарт GCP • (Good Clinical Practice - Надлежащая клиническая практика) - международный стандарт этических норм и качества научных исследований, описывающий правила разработки, проведения, ведения документации и отчетности об исследованиях, которые подразумевают участие человека в качестве испытуемого (клинические исследования).
 Стандарт GMP • (Good Manufacturing Practice - Надлежащая производственная практика) - система норм, правил и указаний в отношении производства лекарственных средств, медицинских устройств, изделий диагностического назначения, пищевых добавок и активных ингредиентов.
Стандарт GMP • (Good Manufacturing Practice - Надлежащая производственная практика) - система норм, правил и указаний в отношении производства лекарственных средств, медицинских устройств, изделий диагностического назначения, пищевых добавок и активных ингредиентов.
 Классификация лекарственных средств обусловлена следующими принципами: • 1. Терапевтическое применение – противоаритмические средства, наркозные средства, противоопухолевые средства и т. д. • 2. Точки приложения или механизм действия: • а) молекулярный уровень - стимуляторы или блокаторы рецепторов, • б) влияние на ферментативную активность (ингибиторы АПФ), ионные каналы (блокаторы кальциевых каналов) и т. д. ; • в) уровень органа – гепатопротекторы, гастропротекторы, стимуляторы ЦНС и т. д. ; • г) уровень физиологической системы – антисклеротические средства, влияющие на систему РАСК и т. д. • 3. Химическое строение: производные фенотиазина, бензодиазепины, барбитураты и т. д.
Классификация лекарственных средств обусловлена следующими принципами: • 1. Терапевтическое применение – противоаритмические средства, наркозные средства, противоопухолевые средства и т. д. • 2. Точки приложения или механизм действия: • а) молекулярный уровень - стимуляторы или блокаторы рецепторов, • б) влияние на ферментативную активность (ингибиторы АПФ), ионные каналы (блокаторы кальциевых каналов) и т. д. ; • в) уровень органа – гепатопротекторы, гастропротекторы, стимуляторы ЦНС и т. д. ; • г) уровень физиологической системы – антисклеротические средства, влияющие на систему РАСК и т. д. • 3. Химическое строение: производные фенотиазина, бензодиазепины, барбитураты и т. д.
 Анатомо-терапевтическо-химическая классификация — международная система классификации лекарственных средств. Используются сокращения: латиницей АТС (от Anatomical Therapeutic Chemical) или русское: АТХ (анатомо-терапевтическо-химическая). Полное английское название — Anatomical Therapeutic Chemical Classification System.
Анатомо-терапевтическо-химическая классификация — международная система классификации лекарственных средств. Используются сокращения: латиницей АТС (от Anatomical Therapeutic Chemical) или русское: АТХ (анатомо-терапевтическо-химическая). Полное английское название — Anatomical Therapeutic Chemical Classification System.
 Классификация CAS • (Chemical Abstracts Service). Представляет собой однозначный идентификатор химических субстанций, где определенной химической структуре присвоен регистровый номер.
Классификация CAS • (Chemical Abstracts Service). Представляет собой однозначный идентификатор химических субстанций, где определенной химической структуре присвоен регистровый номер.
 Формулярная система • (англ. formulary – свод правил) – это обязательный стандарт лечения, основанный на доказательной медицине. Это система выбора лекарственного средства в ежедневной практике врача, которая должна быть свободна от внешнего воздействия и коммерческого давления.
Формулярная система • (англ. formulary – свод правил) – это обязательный стандарт лечения, основанный на доказательной медицине. Это система выбора лекарственного средства в ежедневной практике врача, которая должна быть свободна от внешнего воздействия и коммерческого давления.
 Доказательная медицина • (медицина основанная на доказательствах) включает в себя добросовестное, точное, осмысленное использование лучших результатов клинических исследований для выбора лечения больного.
Доказательная медицина • (медицина основанная на доказательствах) включает в себя добросовестное, точное, осмысленное использование лучших результатов клинических исследований для выбора лечения больного.
 Источники информации • Официальными источниками информации о лекарственных препаратах (ЛП), в которых прописана вся информационная база, являются: фармакопейная статья, клинико-фармакологическая статья (типовая клиникофармакологическая статья ЛС и клиникофармакологическая статья ЛП), паспорт ЛП, Государственный реестр лекарственных средств РФ. Источником информации о лекарствах являются инструкции по применению препарата, Перечень жизненно необходимых лекарственных средств (общий и по основным направлениям: педиатрия, кардиология и т. д. ), Федеральное руководство по использованию лекарственных препаратов (формулярная система) а также научные статьи, справочники, учебники, интернет, в частности: сайт RLSNET. RU – самый посещаемый, сайт MEDI. RU, сайт VIDAL. RU.
Источники информации • Официальными источниками информации о лекарственных препаратах (ЛП), в которых прописана вся информационная база, являются: фармакопейная статья, клинико-фармакологическая статья (типовая клиникофармакологическая статья ЛС и клиникофармакологическая статья ЛП), паспорт ЛП, Государственный реестр лекарственных средств РФ. Источником информации о лекарствах являются инструкции по применению препарата, Перечень жизненно необходимых лекарственных средств (общий и по основным направлениям: педиатрия, кардиология и т. д. ), Федеральное руководство по использованию лекарственных препаратов (формулярная система) а также научные статьи, справочники, учебники, интернет, в частности: сайт RLSNET. RU – самый посещаемый, сайт MEDI. RU, сайт VIDAL. RU.
 Алгоритм характеристики ЛС 1. 2. 3. 4. 5. 6. 7. 8. Групповая принадлежность Фармакодинамика Фармакокинетика Принципы назначения Показания к применению Дозы, формы выпуска и пути введения Побочные эффекты и меры их предупреждения Противопоказания к назначению
Алгоритм характеристики ЛС 1. 2. 3. 4. 5. 6. 7. 8. Групповая принадлежность Фармакодинамика Фармакокинетика Принципы назначения Показания к применению Дозы, формы выпуска и пути введения Побочные эффекты и меры их предупреждения Противопоказания к назначению
 Общая фармакология Фармакокинетика – раздел фармакологии, изучающий процессы всасывания, распределения, метаболизма и выведения лекарственных веществ в сопоставлении с изменениями, вызываемыми ими в организме.
Общая фармакология Фармакокинетика – раздел фармакологии, изучающий процессы всасывания, распределения, метаболизма и выведения лекарственных веществ в сопоставлении с изменениями, вызываемыми ими в организме.
 Фармакокинетика От греч. Pharmakon - лекарство, kinetikos -движущий) - раздел фармакологии, изучающий процессы • • всасывания, распределения, метаболизма, выделения лекарственных средств.
Фармакокинетика От греч. Pharmakon - лекарство, kinetikos -движущий) - раздел фармакологии, изучающий процессы • • всасывания, распределения, метаболизма, выделения лекарственных средств.
 Основные фармакокинетические процессы • Высвобождение из лекарственной формы • Всасывание (адсорбция) • Распределение • Метаболизм • Выведение (экскреция)
Основные фармакокинетические процессы • Высвобождение из лекарственной формы • Всасывание (адсорбция) • Распределение • Метаболизм • Выведение (экскреция)
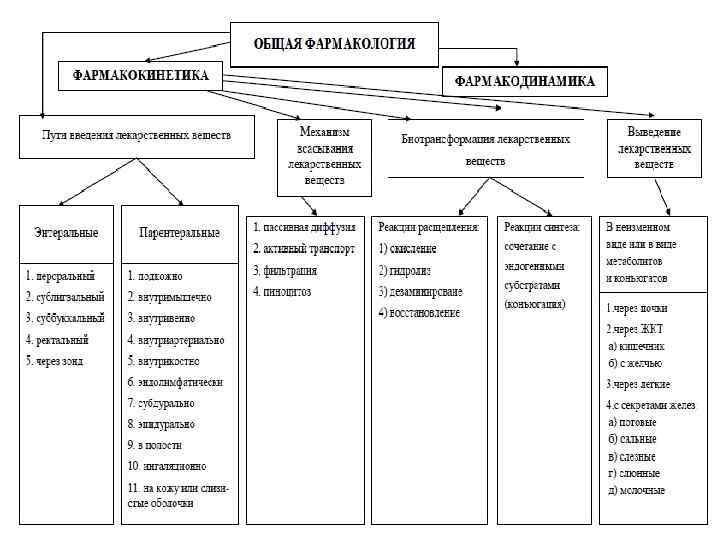
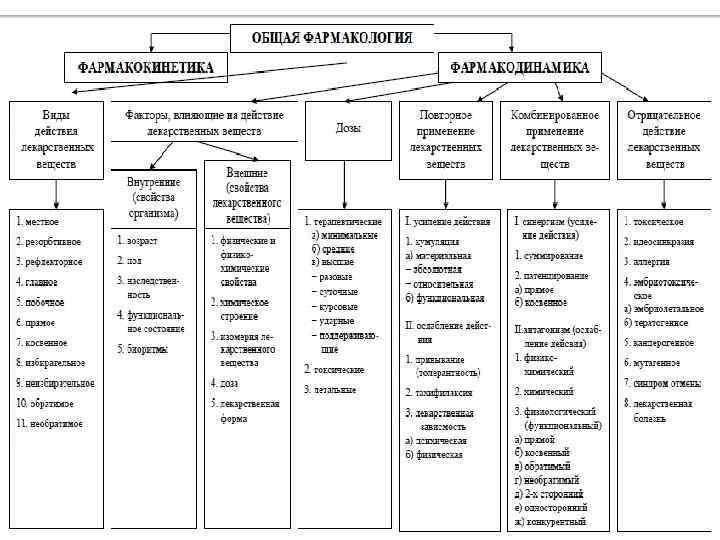
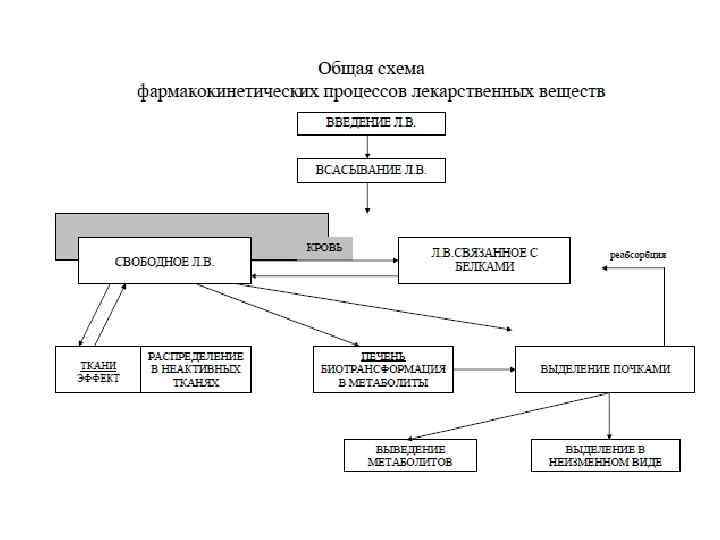

 Проникновение веществ в клетку
Проникновение веществ в клетку
 Влияние р. Н желудка на всасывание • Слабые кислоты • Слабые основания р. Н (щелочная среда) Степень ионизации Липофильность Всасывание р. Н (кислая среда) Степень ионизации Липофильность Всасывание
Влияние р. Н желудка на всасывание • Слабые кислоты • Слабые основания р. Н (щелочная среда) Степень ионизации Липофильность Всасывание р. Н (кислая среда) Степень ионизации Липофильность Всасывание
 Биодоступность (F) • Показатель, характеризующий полноту и скорость всасывания ЛВ в кровь. • Для суждения о биодоступности измеряют площадь под кривой, отражающей зависимость между концентрацией вещества в плазме крови и временем
Биодоступность (F) • Показатель, характеризующий полноту и скорость всасывания ЛВ в кровь. • Для суждения о биодоступности измеряют площадь под кривой, отражающей зависимость между концентрацией вещества в плазме крови и временем
 Кажущийся объем распределения (Vd) • Предположительный объем жидкости, в котором распределяется вещество (условно принимается, что концентрация вещества в плазме и других жидких средах одинакова) Общее кол-во в-ва в ор-ме • Vd = ------------------ Концентрация в-ва в плазме
Кажущийся объем распределения (Vd) • Предположительный объем жидкости, в котором распределяется вещество (условно принимается, что концентрация вещества в плазме и других жидких средах одинакова) Общее кол-во в-ва в ор-ме • Vd = ------------------ Концентрация в-ва в плазме
 Кажущийся объем распределения • Дает представление о фракции вещества, находящейся в плазме крови. • Если объем распределения меньше 0, 5 л/кг , ЛВ находится преимущественно в плазме крови. • Если объем распределения больше 1 л/кг, ЛВ содержится преимущественно в липидах, мышцах и других тканях.
Кажущийся объем распределения • Дает представление о фракции вещества, находящейся в плазме крови. • Если объем распределения меньше 0, 5 л/кг , ЛВ находится преимущественно в плазме крови. • Если объем распределения больше 1 л/кг, ЛВ содержится преимущественно в липидах, мышцах и других тканях.
 Сmin Концентрация лекарственного препараты в плазме Сmax Время
Сmin Концентрация лекарственного препараты в плазме Сmax Время
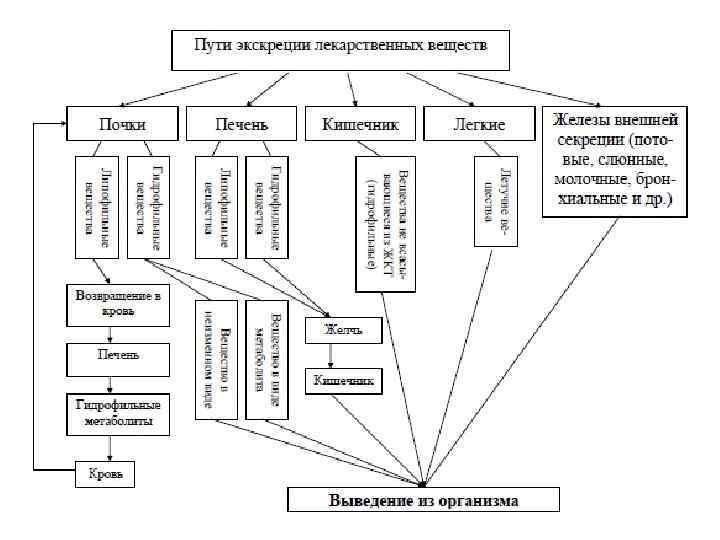
 Пути выведения ЛС из организма Пути выведения С мочой Механизмы выведения ЛС Клубочковая фильтрация, активная канальцевая секреция Большинстве ЛС в не связанной с белками форме С жёлчью Активный транспорт, пассивная диффузия, пиноцитоз Дигитоксин, пенициллины, тетрациклины, стрептомицин, хинин, стрихнин, четвертичные аммониевые соединения Через кишечник Пассивная диффузия, жёлчная секреция без реабсорбции Доксициклин, ионизированные органические кислоты Со слюной Пассивная диффузия, активный транспорт Пеницнллииы, сульфаниламиды, салицнлаты, бензодиазепины, тиамин, этанол Через лёгкие Пассивная диффузия Средства для ингаляционного наркоза, ноднды, камфора, этанол, эфирные масла С потом Пассивная диффузия Некоторые сульфаниламиды, тиамин С молоком Пассивная диффузия, активный транспорт Антикоагулянты, антибиотики, тиреостатики, литий, карбамазепин
Пути выведения ЛС из организма Пути выведения С мочой Механизмы выведения ЛС Клубочковая фильтрация, активная канальцевая секреция Большинстве ЛС в не связанной с белками форме С жёлчью Активный транспорт, пассивная диффузия, пиноцитоз Дигитоксин, пенициллины, тетрациклины, стрептомицин, хинин, стрихнин, четвертичные аммониевые соединения Через кишечник Пассивная диффузия, жёлчная секреция без реабсорбции Доксициклин, ионизированные органические кислоты Со слюной Пассивная диффузия, активный транспорт Пеницнллииы, сульфаниламиды, салицнлаты, бензодиазепины, тиамин, этанол Через лёгкие Пассивная диффузия Средства для ингаляционного наркоза, ноднды, камфора, этанол, эфирные масла С потом Пассивная диффузия Некоторые сульфаниламиды, тиамин С молоком Пассивная диффузия, активный транспорт Антикоагулянты, антибиотики, тиреостатики, литий, карбамазепин
 Константы элиминации • К elim- отражает скорость удаления вещества из организма; • Т ½ - период полужизни ЛВ • С 1 – клиренс – отражает скорость очищения плазмы крови от вещества • Понятие о клиренсе общем, почечном, печеночном.
Константы элиминации • К elim- отражает скорость удаления вещества из организма; • Т ½ - период полужизни ЛВ • С 1 – клиренс – отражает скорость очищения плазмы крови от вещества • Понятие о клиренсе общем, почечном, печеночном.
 Вопросы фармакодинамики 1. Локализация действия ЛВ 2. Механизм действия 3. Биологические эффекты
Вопросы фармакодинамики 1. Локализация действия ЛВ 2. Механизм действия 3. Биологические эффекты
 Мишени воздействия для ЛС 1. 2. 3. 4. 5. Рецепторы Ионные каналы Ферменты Транспортные системы Гены
Мишени воздействия для ЛС 1. 2. 3. 4. 5. Рецепторы Ионные каналы Ферменты Транспортные системы Гены
 Типы рецепторов 1. Рецепторы, осуществляющие прямой контроль за функцией ионных каналов (Н-ХР, ГАМК-А-рецепторы, глутаматные рецепторы) 2. Рецепторы, сопряженные с эффектором через систему “G-белки” – вторичные передатчики или ионные каналы (М-ХР, АР, рецепторы для гормонов, медиаторов) 3. Рецепторы, осуществляющие прямой контроль функции эффекторного фермента (инсулин) 4. Рецепторы, контролирующие транскрипцию ДНК. Это внутриклеточные рецепторы, с которыми взаимодействуют стероидные и тиреоидные гормоны
Типы рецепторов 1. Рецепторы, осуществляющие прямой контроль за функцией ионных каналов (Н-ХР, ГАМК-А-рецепторы, глутаматные рецепторы) 2. Рецепторы, сопряженные с эффектором через систему “G-белки” – вторичные передатчики или ионные каналы (М-ХР, АР, рецепторы для гормонов, медиаторов) 3. Рецепторы, осуществляющие прямой контроль функции эффекторного фермента (инсулин) 4. Рецепторы, контролирующие транскрипцию ДНК. Это внутриклеточные рецепторы, с которыми взаимодействуют стероидные и тиреоидные гормоны
 Разновидности рецепторов Рецепторы Подтипы Аденозиновые рецепторы А 1, А 2 В, АЗ Альфа 1 - Адренорецепторы Альфа 1 А, альфа 1 В, альфа 1 С Альфа 2 -Адренорецепторы Альфа 2 А, альфа 2 В, альфа 2 С Бета-Адренорецепторы Бета 1, бета 2, бета. З Ангиотензиновые рецепторы АТ 1, АТ 2 Брадикининовые рецепторы В 1, В 2 ГАМК-рецепторы GABAa, GABAb, GABAc Гистаминовые рецепторы Н 1, Н 2, НЗ Дофаминовые рецепторы D 1, D 2, D 3, D 4, D 5 Лейкотриеновые рецепторы LTB 4, LTC 4, LTD 4 М-холинорецепторы М 1, М 2, МЗ, М 4 Н-холинорецепторы Мышечного типа, нейронального типа
Разновидности рецепторов Рецепторы Подтипы Аденозиновые рецепторы А 1, А 2 В, АЗ Альфа 1 - Адренорецепторы Альфа 1 А, альфа 1 В, альфа 1 С Альфа 2 -Адренорецепторы Альфа 2 А, альфа 2 В, альфа 2 С Бета-Адренорецепторы Бета 1, бета 2, бета. З Ангиотензиновые рецепторы АТ 1, АТ 2 Брадикининовые рецепторы В 1, В 2 ГАМК-рецепторы GABAa, GABAb, GABAc Гистаминовые рецепторы Н 1, Н 2, НЗ Дофаминовые рецепторы D 1, D 2, D 3, D 4, D 5 Лейкотриеновые рецепторы LTB 4, LTC 4, LTD 4 М-холинорецепторы М 1, М 2, МЗ, М 4 Н-холинорецепторы Мышечного типа, нейронального типа
 Опиоидные рецепторы μ, δ , κ Простаноидные рецепторы DP, FP, IP, TP, EPl , TP 2 , TP 3 Пуриновые рецепторы Р P 2 X, P 2 Y, P 2 Z, P 2 T, P 2 U Рецепторы возбуждающих аминокислот (ионотропные) NMDА, АМРА, каинатные Рецепторы нейроппептида Y Y 1, Y 2 Рецепторы предсердного натрийуретического пептида ANPA , ANPB Серотониновые рецептор 5 -HTl(A-F), 5 -HT 2(A-C), 5 -HT 3, 5 -HT 4, 5 -HT 5 (A-B), 5 -HT 6, 5 -HT 7 Холецистокининовые рецепторы CCK-A, CCK-B Имидазолиновые рецепторы I 1, I 2
Опиоидные рецепторы μ, δ , κ Простаноидные рецепторы DP, FP, IP, TP, EPl , TP 2 , TP 3 Пуриновые рецепторы Р P 2 X, P 2 Y, P 2 Z, P 2 T, P 2 U Рецепторы возбуждающих аминокислот (ионотропные) NMDА, АМРА, каинатные Рецепторы нейроппептида Y Y 1, Y 2 Рецепторы предсердного натрийуретического пептида ANPA , ANPB Серотониновые рецептор 5 -HTl(A-F), 5 -HT 2(A-C), 5 -HT 3, 5 -HT 4, 5 -HT 5 (A-B), 5 -HT 6, 5 -HT 7 Холецистокининовые рецепторы CCK-A, CCK-B Имидазолиновые рецепторы I 1, I 2
 Взаимодействие ЛВ с рецепторами Этапы взаимодействия: Ориентация молекулы ЛВ Притяжение Контактирование
Взаимодействие ЛВ с рецепторами Этапы взаимодействия: Ориентация молекулы ЛВ Притяжение Контактирование
 Факторы, влияющие на фармакодинамику и фармакокинетику 1. Физико-химические свойства ЛС 2. Индивидуальные особенности организма больного 3. Факторы внешней среды 4. Суточные ритмы (вопросы хронофармакологии)
Факторы, влияющие на фармакодинамику и фармакокинетику 1. Физико-химические свойства ЛС 2. Индивидуальные особенности организма больного 3. Факторы внешней среды 4. Суточные ритмы (вопросы хронофармакологии)
 Повторное применение ЛС Усиление эффекта при повторном применении – кумуляция (материальная, функциональная). Снижение эффекта при повторном применении – привыкание (простое, перекрестное), тахифилаксия.
Повторное применение ЛС Усиление эффекта при повторном применении – кумуляция (материальная, функциональная). Снижение эффекта при повторном применении – привыкание (простое, перекрестное), тахифилаксия.
 Виды лекарственного взаимодействия 1. Фармацевтическое происходит вне организма больного, обусловлено физикохимическими реакциями. 2. Фармакодинамическое один лекарственный препарат влияет на реализацию фармакологического эффекта другого препарата. 3. Физиологическое лекарственные препараты оказывают независимое действие на различные органы и ткани, образующие часть одной и той же физиологической системы. 4. Фармакокинетическое под влиянием одного лекарственного препарата изменяется концентрация в крови другого медикамента или его активного метаболита.
Виды лекарственного взаимодействия 1. Фармацевтическое происходит вне организма больного, обусловлено физикохимическими реакциями. 2. Фармакодинамическое один лекарственный препарат влияет на реализацию фармакологического эффекта другого препарата. 3. Физиологическое лекарственные препараты оказывают независимое действие на различные органы и ткани, образующие часть одной и той же физиологической системы. 4. Фармакокинетическое под влиянием одного лекарственного препарата изменяется концентрация в крови другого медикамента или его активного метаболита.
 Виды синергизма Схема Суммация Аддитивное действие Сенситизация Эаб =Эа + Эб Примеры 1. фуросемид + этакриновая кислота 2. триметоприм + сульфаметоказол Эаб>Эа, Эб, но Эа, 1. тетрациклин + эритромицин Эб< Эа + Эб 2. фуросемид + гипотиазид 3. нитроглицерин + β- блокаторы Эаб>Эа+Эб при Эа=0 1. линкомицин + миорелаксант Потенцирование Эаб> Эа+ Эб при 1. глюкокортикоиды + теофиллин Эа>0 и Эб>0 2. пенициллин + гентамицин (на стафилококк, энтерококк) 3. транквилизаторы + клофелин
Виды синергизма Схема Суммация Аддитивное действие Сенситизация Эаб =Эа + Эб Примеры 1. фуросемид + этакриновая кислота 2. триметоприм + сульфаметоказол Эаб>Эа, Эб, но Эа, 1. тетрациклин + эритромицин Эб< Эа + Эб 2. фуросемид + гипотиазид 3. нитроглицерин + β- блокаторы Эаб>Эа+Эб при Эа=0 1. линкомицин + миорелаксант Потенцирование Эаб> Эа+ Эб при 1. глюкокортикоиды + теофиллин Эа>0 и Эб>0 2. пенициллин + гентамицин (на стафилококк, энтерококк) 3. транквилизаторы + клофелин
 Виды лекарственной терапии • • • Профилактическая Этиотропная Заместительная Симптоматическая Патогенетическая
Виды лекарственной терапии • • • Профилактическая Этиотропная Заместительная Симптоматическая Патогенетическая


 Анестезия – обратимое угнетение всех видов чувствительности. Местные анестетики (МА) - выключение болевой и других видов чувствительности при болезненных манипуляциях.
Анестезия – обратимое угнетение всех видов чувствительности. Местные анестетики (МА) - выключение болевой и других видов чувствительности при болезненных манипуляциях.
 Местная анестезия - блокада: 1. Формирования ПД в чувствительных нервных окончаниях 2. проведения возбуждения по нервному волокну при сохранении сознания.
Местная анестезия - блокада: 1. Формирования ПД в чувствительных нервных окончаниях 2. проведения возбуждения по нервному волокну при сохранении сознания.
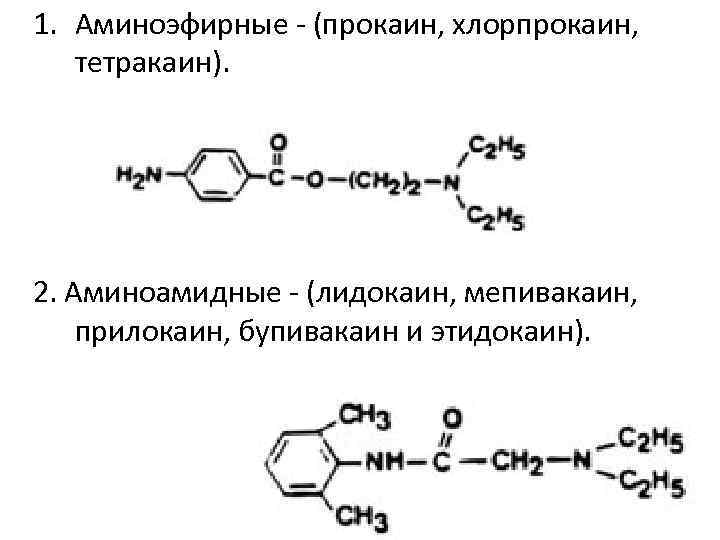 1. Аминоэфирные - (прокаин, хлорпрокаин, тетракаин). 2. Аминоамидные - (лидокаин, мепивакаин, прилокаин, бупивакаин и этидокаин).
1. Аминоэфирные - (прокаин, хлорпрокаин, тетракаин). 2. Аминоамидные - (лидокаин, мепивакаин, прилокаин, бупивакаин и этидокаин).
 Механизм действия МА блокада натриевых каналов плазматических мембран нервных волокон, вследствие чего увеличивается порог возбуждения и уменьшается величина ПД.
Механизм действия МА блокада натриевых каналов плазматических мембран нервных волокон, вследствие чего увеличивается порог возбуждения и уменьшается величина ПД.


 Альфа-субъединица Бета 1 H 3 N мембрана цитозоль -OOC S 4 “+” I II IV + 12345 + P P МА H 3 N - Бета 2 P P COO- P P - субстрат фосфорилирования ПК-А - субстрат фосфорилирования ПК-С. Тетродотоксин, сакситоксин (SS 2). H 3 N РЕЦЕПТОР МА SS 1 -SS 2 в S 6 –домене Фен-1764 (замещенная аминная группа МА)III, Тир 1771 (ароматический радикал) I, Изолейцин 1760 (наружная граница рецептора). IV
Альфа-субъединица Бета 1 H 3 N мембрана цитозоль -OOC S 4 “+” I II IV + 12345 + P P МА H 3 N - Бета 2 P P COO- P P - субстрат фосфорилирования ПК-А - субстрат фосфорилирования ПК-С. Тетродотоксин, сакситоксин (SS 2). H 3 N РЕЦЕПТОР МА SS 1 -SS 2 в S 6 –домене Фен-1764 (замещенная аминная группа МА)III, Тир 1771 (ароматический радикал) I, Изолейцин 1760 (наружная граница рецептора). IV

 Na+- каналы в состоянии покоя имеют значительно меньшую аффинность к МА, чем активные (открытые) или инактивированные каналы. Т. О. , эффект MA более выражен в активных действующих аксонах, чем в находящихся в состоянии покоя.
Na+- каналы в состоянии покоя имеют значительно меньшую аффинность к МА, чем активные (открытые) или инактивированные каналы. Т. О. , эффект MA более выражен в активных действующих аксонах, чем в находящихся в состоянии покоя.
 • Повышение уровня внеклеточного Са++ частично блокирует действие MA за счет увеличения потенциала мембраны, которое переводит ее в состояние покоя. • Наоборот, повышение концентрации внеклеточного К+ деполяризует мембранный потенциал усиливает эффект МА.
• Повышение уровня внеклеточного Са++ частично блокирует действие MA за счет увеличения потенциала мембраны, которое переводит ее в состояние покоя. • Наоборот, повышение концентрации внеклеточного К+ деполяризует мембранный потенциал усиливает эффект МА.

 Препарат Хим. класс р. Ка % оснований при р. Н=7, 5 Начало, мин Прилокаин Аминоамид 7, 7 35 2 -4 Лидокаин " 7, 7 35 2 -4 Этидокаин " 7, 7 35 2 -4 Бупивакаин " 8, 1 20 5 -8 Тетракаин Аминоэфир 8, 6 5 10 -15 Прокаин “ 8, 9 2 14 -18
Препарат Хим. класс р. Ка % оснований при р. Н=7, 5 Начало, мин Прилокаин Аминоамид 7, 7 35 2 -4 Лидокаин " 7, 7 35 2 -4 Этидокаин " 7, 7 35 2 -4 Бупивакаин " 8, 1 20 5 -8 Тетракаин Аминоэфир 8, 6 5 10 -15 Прокаин “ 8, 9 2 14 -18


 действие у аминоэфиров значительно сильнее, чем у аминоамидов даже при одинаковых коэффициентах распределения
действие у аминоэфиров значительно сильнее, чем у аминоамидов даже при одинаковых коэффициентах распределения
 • Препараты слабой обезболивающей активности и кратковременного действия - прокаин и хлоропрокаин. • Препараты промежуточной обезболивающей активности и средней продолжительности действия - лидокаин, мепивакаин и прилокаин. • Препараты высокой обезболивающей активности и большой продолжительности действия - тетракаин, бупивакаин и этидокаин.
• Препараты слабой обезболивающей активности и кратковременного действия - прокаин и хлоропрокаин. • Препараты промежуточной обезболивающей активности и средней продолжительности действия - лидокаин, мепивакаин и прилокаин. • Препараты высокой обезболивающей активности и большой продолжительности действия - тетракаин, бупивакаин и этидокаин.
 Сроки наступления анестезии • быстрый эффект - хлоропрокаин, лидокаин, мепивакаин, прилокаин и этидокаин • промежуточного действия - Бупивакаин • замедленно вызывающие обезболивание - прокаин и тетракаин
Сроки наступления анестезии • быстрый эффект - хлоропрокаин, лидокаин, мепивакаин, прилокаин и этидокаин • промежуточного действия - Бупивакаин • замедленно вызывающие обезболивание - прокаин и тетракаин
 • Наиболее подвержены действию МА безмиелиновые и тонкие миелиновые волокна (температурные и болевые импульсы). • Толстые миелиновые волокна, (тактильные) менее чувствительны к действию МА.
• Наиболее подвержены действию МА безмиелиновые и тонкие миелиновые волокна (температурные и болевые импульсы). • Толстые миелиновые волокна, (тактильные) менее чувствительны к действию МА.
 Для прекращения проведения по миелинизированным волокнам необходимо, чтобы блокада распространилась на 3 последовательных узла.
Для прекращения проведения по миелинизированным волокнам необходимо, чтобы блокада распространилась на 3 последовательных узла.
 • Блокада более выражена при большей частоте и длительности деполяризации. Сенсорные, особенно болевые, волокна имеют высокую частоту импульсации и сравнительно длительный потенциал действия (до 5 мс). Двигательные волокна посылают импульсы с меньшей частотой и более коротким ПД (< 0. 5 мс), потому они блокируются позже и большими концентрациями МА, чем сенсорные волокна.
• Блокада более выражена при большей частоте и длительности деполяризации. Сенсорные, особенно болевые, волокна имеют высокую частоту импульсации и сравнительно длительный потенциал действия (до 5 мс). Двигательные волокна посылают импульсы с меньшей частотой и более коротким ПД (< 0. 5 мс), потому они блокируются позже и большими концентрациями МА, чем сенсорные волокна.
 виды местной анестезии: • Терминальная (поверхностная, аппликационная анестезия) смазывание кожных покровов и слизистых оболочек. закапывание, орошение. • Инфильтрационная анестезия - пропитывание р-ром МА тканей в области операционного доступа. • Проводниковая (регионарная) анестезия - прерывание проводимости по нервному стволу. • Эпидуральная и каудальная анестезия используется при оперативных вмешательствах на органах малого таза, промежности, нижних конечностей. • Субарахноидальная (спинальная) анестезия широко используется при оперативных вмешательствах на органах малого таза, промежности, нижних конечностей и др. • Внутрикостная анестезия применяется при операциях на конечностях. • Новокаиновые блокады. При ряде заболеваний или травмах для хорошего обезболивания показаны новокаиновые блокады.
виды местной анестезии: • Терминальная (поверхностная, аппликационная анестезия) смазывание кожных покровов и слизистых оболочек. закапывание, орошение. • Инфильтрационная анестезия - пропитывание р-ром МА тканей в области операционного доступа. • Проводниковая (регионарная) анестезия - прерывание проводимости по нервному стволу. • Эпидуральная и каудальная анестезия используется при оперативных вмешательствах на органах малого таза, промежности, нижних конечностей. • Субарахноидальная (спинальная) анестезия широко используется при оперативных вмешательствах на органах малого таза, промежности, нижних конечностей и др. • Внутрикостная анестезия применяется при операциях на конечностях. • Новокаиновые блокады. При ряде заболеваний или травмах для хорошего обезболивания показаны новокаиновые блокады.
 ТОКСИЧНОСТЬ • ЦНС - головокружение, нарушения зрения и слуха, остановка дыхания или кровообращения • Судороги • синусовая брадикардия • Аллергические реакции
ТОКСИЧНОСТЬ • ЦНС - головокружение, нарушения зрения и слуха, остановка дыхания или кровообращения • Судороги • синусовая брадикардия • Аллергические реакции
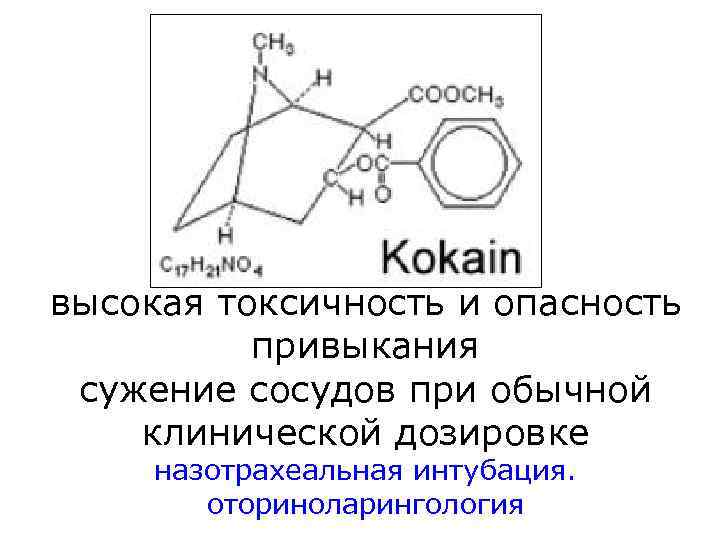 высокая токсичность и опасность привыкания сужение сосудов при обычной клинической дозировке назотрахеальная интубация. оториноларингология
высокая токсичность и опасность привыкания сужение сосудов при обычной клинической дозировке назотрахеальная интубация. оториноларингология
 Прокаин (новокаин) Максимальная доза без адреналина 800 мг, с адреналином 1000 мг сравнительно слабое обезболивающее действие, которое проявляется медленно и длится недолго; инфильтрационная анестезия
Прокаин (новокаин) Максимальная доза без адреналина 800 мг, с адреналином 1000 мг сравнительно слабое обезболивающее действие, которое проявляется медленно и длится недолго; инфильтрационная анестезия
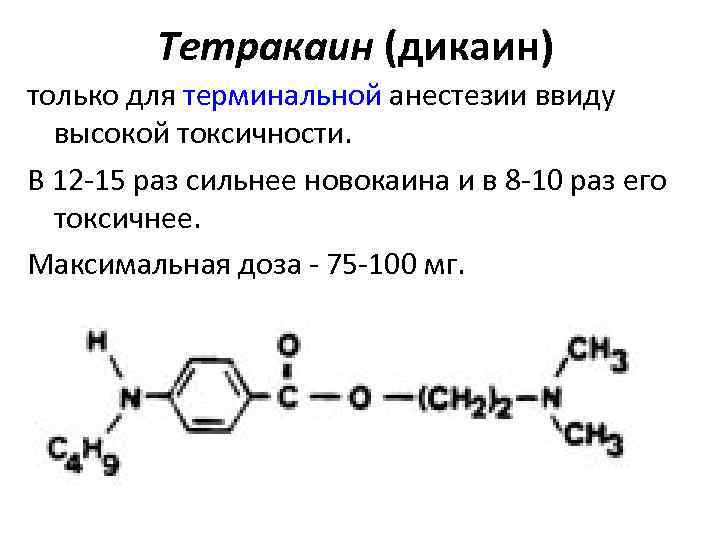 Тетракаин (дикаин) только для терминальной анестезии ввиду высокой токсичности. В 12 -15 раз сильнее новокаина и в 8 -10 раз его токсичнее. Максимальная доза - 75 -100 мг.
Тетракаин (дикаин) только для терминальной анестезии ввиду высокой токсичности. В 12 -15 раз сильнее новокаина и в 8 -10 раз его токсичнее. Максимальная доза - 75 -100 мг.
 Лидокаин В 2 раза сильнее и токсичнее новокаина. применяют для инфильтрационной анестезии, для блокирования периферических нервов и для перидуральной анестезии. Расширяет сосуды. также в мазях, геле и в аэрозолях для локальной анестезии при различных процедурах. АА
Лидокаин В 2 раза сильнее и токсичнее новокаина. применяют для инфильтрационной анестезии, для блокирования периферических нервов и для перидуральной анестезии. Расширяет сосуды. также в мазях, геле и в аэрозолях для локальной анестезии при различных процедурах. АА
 Прилокаин клиническое действие как у лидокаина. Но - не вызывает расширения сосудов - можно применять без адреналина. наименее токсичный препарат из группы аминоамидов. в/в введение (региональная анестезия). токсические изменения после снятия жгута развиваются редко (преимущественно со стороны ЦНС) излишне высокие дозы - может осложниться метгемоглобинемией. - ограничение применения в акушерской практике.
Прилокаин клиническое действие как у лидокаина. Но - не вызывает расширения сосудов - можно применять без адреналина. наименее токсичный препарат из группы аминоамидов. в/в введение (региональная анестезия). токсические изменения после снятия жгута развиваются редко (преимущественно со стороны ЦНС) излишне высокие дозы - может осложниться метгемоглобинемией. - ограничение применения в акушерской практике.
 Артикаин (альфакаин, брилокаин, септонест, ультракаин). • в 3 -5 раз активнее и в 1, 5 раза токсичнее новокаина. Имеет оптимальное соотношение показателей активности и токсичности (самую большую широту терапевтического действия). Кардиодепрессивный эффект у артикаина выражен слабее, чем у других амидных МА. Стоматология
Артикаин (альфакаин, брилокаин, септонест, ультракаин). • в 3 -5 раз активнее и в 1, 5 раза токсичнее новокаина. Имеет оптимальное соотношение показателей активности и токсичности (самую большую широту терапевтического действия). Кардиодепрессивный эффект у артикаина выражен слабее, чем у других амидных МА. Стоматология
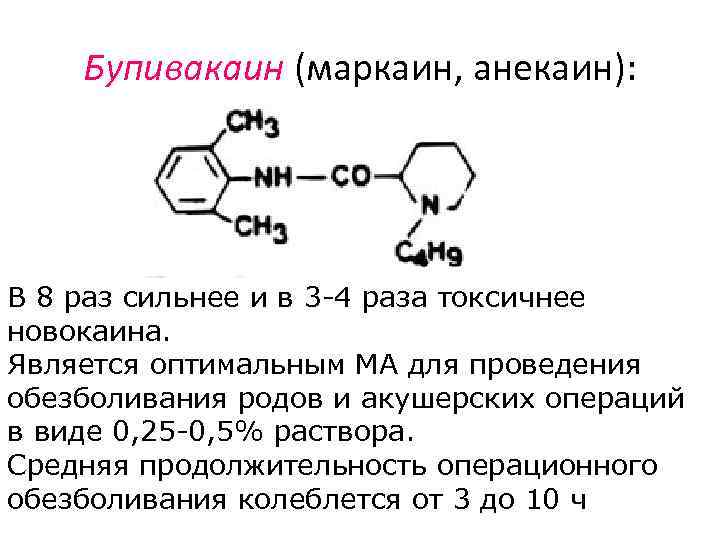 Бупивакаин (маркаин, анекаин): В 8 раз сильнее и в 3 -4 раза токсичнее новокаина. Является оптимальным МА для проведения обезболивания родов и акушерских операций в виде 0, 25 -0, 5% раствора. Средняя продолжительность операционного обезболивания колеблется от 3 до 10 ч
Бупивакаин (маркаин, анекаин): В 8 раз сильнее и в 3 -4 раза токсичнее новокаина. Является оптимальным МА для проведения обезболивания родов и акушерских операций в виде 0, 25 -0, 5% раствора. Средняя продолжительность операционного обезболивания колеблется от 3 до 10 ч
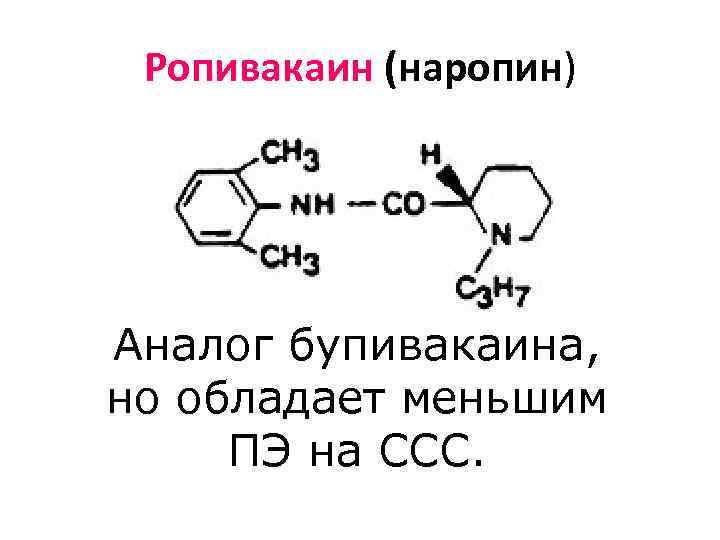 Ропивакаин (наропин) Аналог бупивакаина, но обладает меньшим ПЭ на ССС.
Ропивакаин (наропин) Аналог бупивакаина, но обладает меньшим ПЭ на ССС.
 ПРОТИВОПОКАЗАНИЯ 1. Гиперчувствительность. 2. к применению сосудосуживающих средств в сочетании с МА: а) Абсолютные противопоказания: - Нестабильная ИБС; - Недавно перенесенный инфаркт миокарда; - Недавнее коронарное шунтирование; - Трудноизлечимая аритмия; - Неконтролируемое высокое кровяное давление; - Закупорка сердечных сосудов; - Гипертиреоз; - диабет; - чувствительность к сульфитам, - кортико-зависимая астма, - феохромоцитома.
ПРОТИВОПОКАЗАНИЯ 1. Гиперчувствительность. 2. к применению сосудосуживающих средств в сочетании с МА: а) Абсолютные противопоказания: - Нестабильная ИБС; - Недавно перенесенный инфаркт миокарда; - Недавнее коронарное шунтирование; - Трудноизлечимая аритмия; - Неконтролируемое высокое кровяное давление; - Закупорка сердечных сосудов; - Гипертиреоз; - диабет; - чувствительность к сульфитам, - кортико-зависимая астма, - феохромоцитома.