90de18351ddabbbb7185726f98fc4e58.ppt
- Количество слайдов: 78
 ФАРМАКОКИНЕТИКА
ФАРМАКОКИНЕТИКА
 Фармакокинетика— изучает влияние организма на лекарственное вещество, пути его поступления, распределения, биотрансформации и выведения лекарств из организма. Судьба лекарственного вещества от момента его попадания в организм до выведения.
Фармакокинетика— изучает влияние организма на лекарственное вещество, пути его поступления, распределения, биотрансформации и выведения лекарств из организма. Судьба лекарственного вещества от момента его попадания в организм до выведения.
 История развития
История развития
 В 1913 немецкие биохимики Л. Михаэлис и M. Ментен предложили уравнение кинетики ферментативных процессов, широко используемое в современной фармакокинетике для описания метаболизма лекарственных средств. Шведские физиологи Э. Видмарк, Д. Тандберг (1924) и T. Теорелл (1937) применяли системы дифференциальных уравнений при анализе различных способов введения лекарственных средств. Американский физиолог В. Гамильтон и другие (1931) использовали метод статистических моментов для оценки параметров фармакокинетики по экспериментальным данным. Основы метаболизма лекарственных средств были заложены английскими биохимиками X. Бреем, В. Торпом и К. Уайтом (1951). Практические аспекты применения фармакокинетики для оптимизации фармакотерапии разрабатывали К. Лапп во Франции (1948— 1956), А. ван Гемерт и др. в Дании (1950), Э. Крюгер-Тиммер (1960) и, собственно фармакокинетику, — Дост (1953— 1968) в Германии (последний — автор термина «фармакокинетика» ). Развитие фармакокинетики до начала 50 -х гг. 20 в. сдерживалось отсутствием высокочувствительных и селективных методов анализа микроконцентраций лекарственных веществ в биологических средах и недостаточной компьютеризацией исследований. С решением этих проблем фармакокинетика получила дальнейшее развитие. В России развитие фармакокинетики началось в 60 -х гг. и связано с именами В. А. Филова, В. H. Соловьёва и В. П. Яковлева.
В 1913 немецкие биохимики Л. Михаэлис и M. Ментен предложили уравнение кинетики ферментативных процессов, широко используемое в современной фармакокинетике для описания метаболизма лекарственных средств. Шведские физиологи Э. Видмарк, Д. Тандберг (1924) и T. Теорелл (1937) применяли системы дифференциальных уравнений при анализе различных способов введения лекарственных средств. Американский физиолог В. Гамильтон и другие (1931) использовали метод статистических моментов для оценки параметров фармакокинетики по экспериментальным данным. Основы метаболизма лекарственных средств были заложены английскими биохимиками X. Бреем, В. Торпом и К. Уайтом (1951). Практические аспекты применения фармакокинетики для оптимизации фармакотерапии разрабатывали К. Лапп во Франции (1948— 1956), А. ван Гемерт и др. в Дании (1950), Э. Крюгер-Тиммер (1960) и, собственно фармакокинетику, — Дост (1953— 1968) в Германии (последний — автор термина «фармакокинетика» ). Развитие фармакокинетики до начала 50 -х гг. 20 в. сдерживалось отсутствием высокочувствительных и селективных методов анализа микроконцентраций лекарственных веществ в биологических средах и недостаточной компьютеризацией исследований. С решением этих проблем фармакокинетика получила дальнейшее развитие. В России развитие фармакокинетики началось в 60 -х гг. и связано с именами В. А. Филова, В. H. Соловьёва и В. П. Яковлева.
 Фармакокинетические процессы -всасывание -распределение -депонирование -биотрансформация -выведение
Фармакокинетические процессы -всасывание -распределение -депонирование -биотрансформация -выведение
 Фармакокинетические процессы связаны с проникновением ЛВ через биологические мембраны (в основном через цитоплазматические мембраны клеток). Существуют следующие способы проникновения веществ через биологические мембраны: пассивная диффузия, фильтрация, активный транспорт, облегченная диффузия, пиноцитоз.
Фармакокинетические процессы связаны с проникновением ЛВ через биологические мембраны (в основном через цитоплазматические мембраны клеток). Существуют следующие способы проникновения веществ через биологические мембраны: пассивная диффузия, фильтрация, активный транспорт, облегченная диффузия, пиноцитоз.
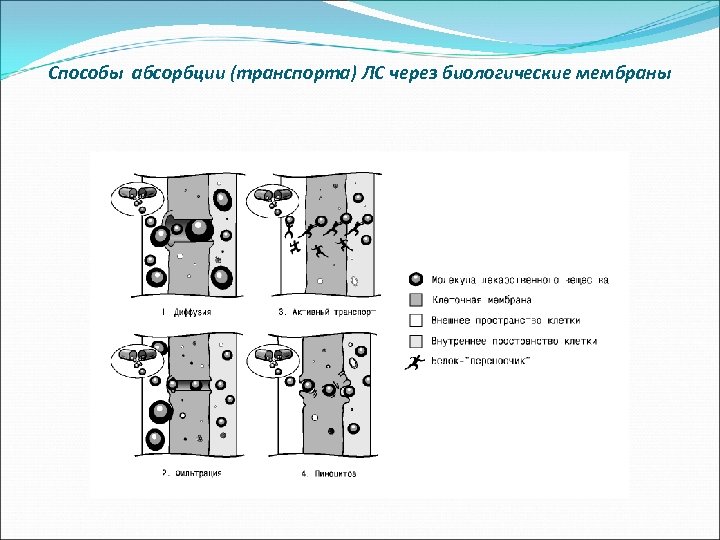 Способы абсорбции (транспорта) ЛС через биологические мембраны
Способы абсорбции (транспорта) ЛС через биологические мембраны
 Пассивная диффузия Путем пассивной диффузии вещества проникают через мембрану по градиенту концентрации Этот процесс не требует затраты энергии. Поскольку биологические мембраны в основном состоят из липидов, таким способом через них легко проникают вещества, растворимые в липидах и не имеющие заряда, т. е. липофильные неполярные вещества. Гидрофильные полярные соединения непосредственно через липиды мембран практически не проникают.
Пассивная диффузия Путем пассивной диффузии вещества проникают через мембрану по градиенту концентрации Этот процесс не требует затраты энергии. Поскольку биологические мембраны в основном состоят из липидов, таким способом через них легко проникают вещества, растворимые в липидах и не имеющие заряда, т. е. липофильные неполярные вещества. Гидрофильные полярные соединения непосредственно через липиды мембран практически не проникают.
 Если ЛВ являются слабыми электролитами (слабыми кислотами или слабыми основаниями), то проникновение таких веществ через мембраны зависит от степени их ионизации, так как путем пассивной диффузии через двойной липидный слой мембраны легко проходят только неионизированные (незаряженные) молекулы вещества. Степень ионизации слабых кислот и слабых оснований определяется: 1) значениями р. Н среды; 2) константой ионизации (Ка) веществ.
Если ЛВ являются слабыми электролитами (слабыми кислотами или слабыми основаниями), то проникновение таких веществ через мембраны зависит от степени их ионизации, так как путем пассивной диффузии через двойной липидный слой мембраны легко проходят только неионизированные (незаряженные) молекулы вещества. Степень ионизации слабых кислот и слабых оснований определяется: 1) значениями р. Н среды; 2) константой ионизации (Ка) веществ.
 Слабые кислоты в большей степени ионизированы в щелочной среде, а слабые основания — в кислой. Ионизация слабых кислот: кислая среда щелочная среда Ионизация слабых оснований: кислая среда щелочная среда
Слабые кислоты в большей степени ионизированы в щелочной среде, а слабые основания — в кислой. Ионизация слабых кислот: кислая среда щелочная среда Ионизация слабых оснований: кислая среда щелочная среда
 Константа ионизации (Ка) характеризует способность вещества к ионизации при определённом значении р. Н среды (численно равна концентрации водородных ионов в среде, при которой ионизирована половина молекул данного вещества). На практике для характеристики способности веществ к ионизации используют показатель р. Ка, который является отрицательным логарифмом Ка (–lg Ka . Показатель p. Ка численно равен значению р. Н среды, при котором ионизирована половина молекул данного вещества.
Константа ионизации (Ка) характеризует способность вещества к ионизации при определённом значении р. Н среды (численно равна концентрации водородных ионов в среде, при которой ионизирована половина молекул данного вещества). На практике для характеристики способности веществ к ионизации используют показатель р. Ка, который является отрицательным логарифмом Ка (–lg Ka . Показатель p. Ка численно равен значению р. Н среды, при котором ионизирована половина молекул данного вещества.
 Степень ионизации слабой кислоты или слабого основания можно рассчитать по формуле Гендерсона–Гассельбальха: для слабых кислот Для слабых оснований
Степень ионизации слабой кислоты или слабого основания можно рассчитать по формуле Гендерсона–Гассельбальха: для слабых кислот Для слабых оснований
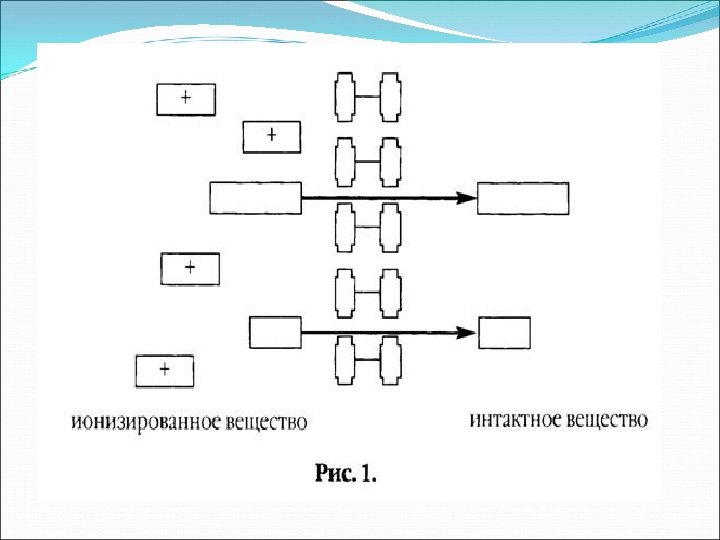
 Уравнение Гендерсона–Гассельбальха Это уравнение позволяет : §оценить степень ионизации лекарственного вещества при данном значении р. Н §и предсказать вероятность его проникновения через клеточные мембраны. Изменяя р. Н среды, можно изменить (увеличить или уменьшить) степень проникновения слабых кислот и слабых оснований через мембраны.
Уравнение Гендерсона–Гассельбальха Это уравнение позволяет : §оценить степень ионизации лекарственного вещества при данном значении р. Н §и предсказать вероятность его проникновения через клеточные мембраны. Изменяя р. Н среды, можно изменить (увеличить или уменьшить) степень проникновения слабых кислот и слабых оснований через мембраны.
 Henderson-Hasselbalch Ацетилсалициловая кислота (аспирин) р. Н 4, 5 будет мало диссоциировать. р. Ка аспирина= 3, 5 кодеин — слабое основание с р. Ка 8, 2 — из щелочной среды двенадцатиперстной кишки (р. Н = 8) всасывается на 61, 4%, тогда как из кислой среды желудка (р. Н = 2, 5) — менее чем на 0, 0002%.
Henderson-Hasselbalch Ацетилсалициловая кислота (аспирин) р. Н 4, 5 будет мало диссоциировать. р. Ка аспирина= 3, 5 кодеин — слабое основание с р. Ка 8, 2 — из щелочной среды двенадцатиперстной кишки (р. Н = 8) всасывается на 61, 4%, тогда как из кислой среды желудка (р. Н = 2, 5) — менее чем на 0, 0002%.
 Определить кодеин — слабое основание, р. Ка= 7 Определить всасывание в двенадцатиперстной кишке (р. Н = 8) , в желудке (р. Н = 2, 5).
Определить кодеин — слабое основание, р. Ка= 7 Определить всасывание в двенадцатиперстной кишке (р. Н = 8) , в желудке (р. Н = 2, 5).
 Как действуют лекарственные вещества, являющиеся слабыми основаниями? Большинство лекарственных веществ — слабые основания, т. е. в щелочной среде остаются в нейтральном состоянии. Однако в кислой среде нейтральная молекула приобретает протон [Н+], превращаясь в заряженную (протонированную, ионизированную) форму, которая не проникает через клеточные мембраны. Отсюда следует, что слабые основания могут попадать в клетки только из щелочной среды.
Как действуют лекарственные вещества, являющиеся слабыми основаниями? Большинство лекарственных веществ — слабые основания, т. е. в щелочной среде остаются в нейтральном состоянии. Однако в кислой среде нейтральная молекула приобретает протон [Н+], превращаясь в заряженную (протонированную, ионизированную) форму, которая не проникает через клеточные мембраны. Отсюда следует, что слабые основания могут попадать в клетки только из щелочной среды.
 Как действуют лекарственные вещества, являющиеся слабыми кислотами? В кислой среде слабые кислоты находятся в протонированном состоянии, но в щелочной — отдают протон, образуя анион и катион (молекула ионизируется). Таким образом, слабые кислоты оказываются более липофильными в протонированном (недиссоциированном, неионизированном) состоянии.
Как действуют лекарственные вещества, являющиеся слабыми кислотами? В кислой среде слабые кислоты находятся в протонированном состоянии, но в щелочной — отдают протон, образуя анион и катион (молекула ионизируется). Таким образом, слабые кислоты оказываются более липофильными в протонированном (недиссоциированном, неионизированном) состоянии.
 ФИЛЬТРАЦИЯ Фильтрация (водная диффузия) – пассивное перемещение молекул вещества по градиенту концентрации через заполненные водой поры в мембране каждой клетки (водные поры) и между соседними клетками (межклеточные промежутки). Характерен для воды, некоторых ионов, мелких гидрофильных молекул (мочевина).
ФИЛЬТРАЦИЯ Фильтрация (водная диффузия) – пассивное перемещение молекул вещества по градиенту концентрации через заполненные водой поры в мембране каждой клетки (водные поры) и между соседними клетками (межклеточные промежутки). Характерен для воды, некоторых ионов, мелких гидрофильных молекул (мочевина).
 Так как межклеточные промежутки в различных тканях не одинаковы по величине, гидрофильные ЛВ при различных путях введения всасываются в неодинаковой степени и распределяются в организме неравномерно. Например, промежутки между эпителиальными клетками слизистой оболочки кишечника невелики, что затрудняет всасывание гидрофильных Л В из кишечника в кровь. Промежутки между эндотелиальными клетками сосудов периферических тканей (скелетных мышц, подкожной клетчатки, внутренних органов) имеют достаточно большие размеры (порядка 2 нм) и пропускают большинство гидрофильных Л В, что обеспечивает достаточно быстрое проникновение Л В из тканей в кровь и из крови в ткани. В то же время в эндотелии сосудов мозга межклеточные промежутки отсутствуют. Эндотелиальные клетки плотно прилегают к другу, образуя барьер (гематоэнцефалический барьер), препятствующий проникновению гидрофильных полярных веществ из крови в мозг.
Так как межклеточные промежутки в различных тканях не одинаковы по величине, гидрофильные ЛВ при различных путях введения всасываются в неодинаковой степени и распределяются в организме неравномерно. Например, промежутки между эпителиальными клетками слизистой оболочки кишечника невелики, что затрудняет всасывание гидрофильных Л В из кишечника в кровь. Промежутки между эндотелиальными клетками сосудов периферических тканей (скелетных мышц, подкожной клетчатки, внутренних органов) имеют достаточно большие размеры (порядка 2 нм) и пропускают большинство гидрофильных Л В, что обеспечивает достаточно быстрое проникновение Л В из тканей в кровь и из крови в ткани. В то же время в эндотелии сосудов мозга межклеточные промежутки отсутствуют. Эндотелиальные клетки плотно прилегают к другу, образуя барьер (гематоэнцефалический барьер), препятствующий проникновению гидрофильных полярных веществ из крови в мозг.
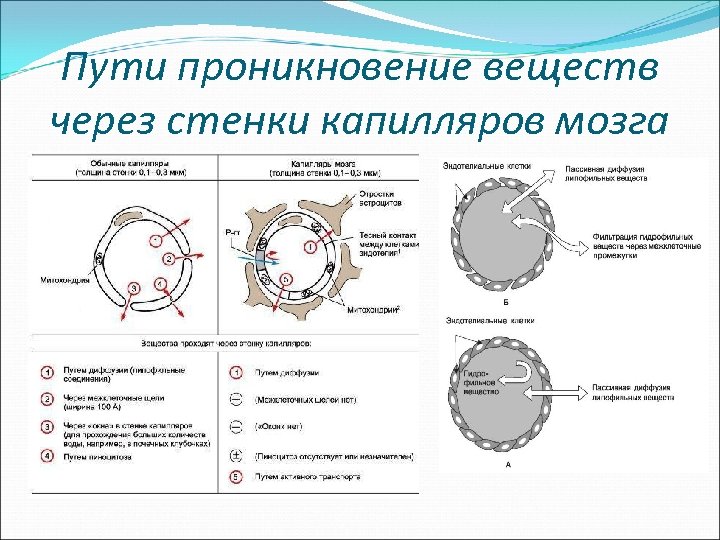 Пути проникновение веществ через стенки капилляров мозга
Пути проникновение веществ через стенки капилляров мозга
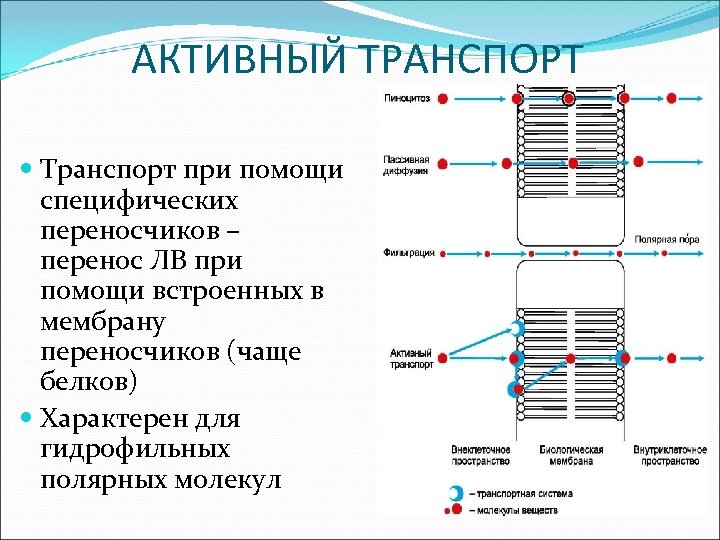 АКТИВНЫЙ ТРАНСПОРТ Транспорт при помощи специфических переносчиков – перенос ЛВ при помощи встроенных в мембрану переносчиков (чаще белков) Характерен для гидрофильных полярных молекул
АКТИВНЫЙ ТРАНСПОРТ Транспорт при помощи специфических переносчиков – перенос ЛВ при помощи встроенных в мембрану переносчиков (чаще белков) Характерен для гидрофильных полярных молекул
 Активный транспорт веществ через мембрану обладает следующими характеристиками: специфичностью (транспортные белки избирательно связывают и переносят через мембрану только определенные вещества), насыщаемостью (при связывании всех белковпереносчиков количество вещества, переносимого через мембрану, не увеличивается), происходит против градиента концентрации, требует затраты энергии (поэтому угнетается метаболическими ядами).
Активный транспорт веществ через мембрану обладает следующими характеристиками: специфичностью (транспортные белки избирательно связывают и переносят через мембрану только определенные вещества), насыщаемостью (при связывании всех белковпереносчиков количество вещества, переносимого через мембрану, не увеличивается), происходит против градиента концентрации, требует затраты энергии (поэтому угнетается метаболическими ядами).
 ОБЛЕГЧЁННАЯ ДИФФУЗИЯ Облегченная диффузия — перенос веществ через мембраны с помощью транспортных систем, который осуществляется по градиенту концентрации и не требует затраты энергии. Так же, как активный транспорт, облегченная диффузия — это специфичный по отношению к определенным веществам и насыщаемый процесс. Этот транспорт облегчает поступление в клетку гидрофильных полярных веществ. Таким образом через мембрану клеток может транспортироваться глюкоза.
ОБЛЕГЧЁННАЯ ДИФФУЗИЯ Облегченная диффузия — перенос веществ через мембраны с помощью транспортных систем, который осуществляется по градиенту концентрации и не требует затраты энергии. Так же, как активный транспорт, облегченная диффузия — это специфичный по отношению к определенным веществам и насыщаемый процесс. Этот транспорт облегчает поступление в клетку гидрофильных полярных веществ. Таким образом через мембрану клеток может транспортироваться глюкоза.
 Р-гликопротеины специальный мембранный транспортер, способствует выведению веществ из клетки и препятствует их абсорбции. Основная функция Р-гликопротеинового транспортера - выведение из клеток лекарственных средств и других ксенобиотиков. Он образуется в тонкой кишке, печени, почках, в гематоэнцефалическом барьере, плаценте, тестикулах, в опухолевых клетках.
Р-гликопротеины специальный мембранный транспортер, способствует выведению веществ из клетки и препятствует их абсорбции. Основная функция Р-гликопротеинового транспортера - выведение из клеток лекарственных средств и других ксенобиотиков. Он образуется в тонкой кишке, печени, почках, в гематоэнцефалическом барьере, плаценте, тестикулах, в опухолевых клетках.
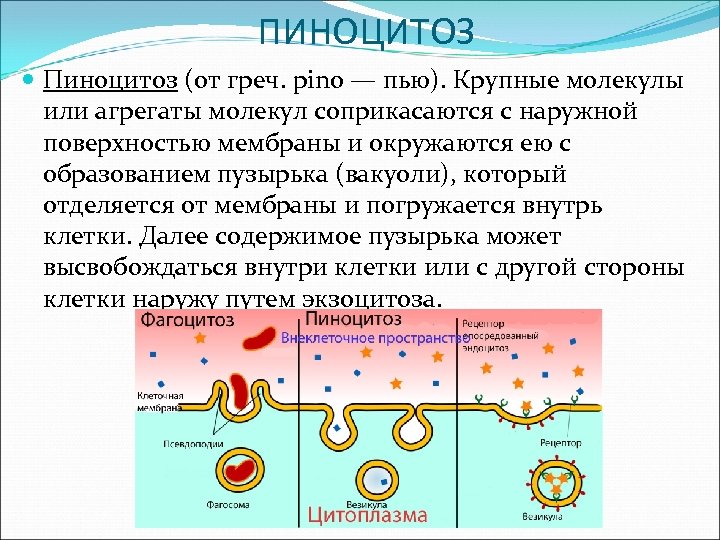 ПИНОЦИТОЗ Пиноцитоз (от греч. pino — пью). Крупные молекулы или агрегаты молекул соприкасаются с наружной поверхностью мембраны и окружаются ею с образованием пузырька (вакуоли), который отделяется от мембраны и погружается внутрь клетки. Далее содержимое пузырька может высвобождаться внутри клетки или с другой стороны клетки наружу путем экзоцитоза.
ПИНОЦИТОЗ Пиноцитоз (от греч. pino — пью). Крупные молекулы или агрегаты молекул соприкасаются с наружной поверхностью мембраны и окружаются ею с образованием пузырька (вакуоли), который отделяется от мембраны и погружается внутрь клетки. Далее содержимое пузырька может высвобождаться внутри клетки или с другой стороны клетки наружу путем экзоцитоза.
 ВСАСЫВАНИЕ ЛС
ВСАСЫВАНИЕ ЛС
 Всасывание (абсорбция, от лат. absorbeo — всасываю) — процесс, в результате которого вещество поступает с места введения в кровь и/или лимфатическую систему. Всасывание Л В начинается сразу после введения Л В в организм. От того, каким путем Л В вводится в организм, зависит скорость и степень его всасывания, а в конечном итоге скорость наступления эффекта, его величина и продолжительность.
Всасывание (абсорбция, от лат. absorbeo — всасываю) — процесс, в результате которого вещество поступает с места введения в кровь и/или лимфатическую систему. Всасывание Л В начинается сразу после введения Л В в организм. От того, каким путем Л В вводится в организм, зависит скорость и степень его всасывания, а в конечном итоге скорость наступления эффекта, его величина и продолжительность.
 Энтеральные пути введения • сублингвальный (под язык); • трансбуккальный (за щеку); • пероральный (внутрь, peros) • ректальный (через прямую кишку, per rectum). Парентеральные пути введения • внутривенный; • внутриартериальный; • интрастернальный; • внутримышечный; • подкожный; • внутрибрюшинный; • под оболочки мозга; и некоторые другие.
Энтеральные пути введения • сублингвальный (под язык); • трансбуккальный (за щеку); • пероральный (внутрь, peros) • ректальный (через прямую кишку, per rectum). Парентеральные пути введения • внутривенный; • внутриартериальный; • интрастернальный; • внутримышечный; • подкожный; • внутрибрюшинный; • под оболочки мозга; и некоторые другие.
 Пресистемная элиминация ЛС (эффект первого прохождения) процесс биотрансформации лекарства до попадания ЛС в системный кровоток. В пресистемной элиминации при пероральном введении лекарства участвуют ферментативные системы кишечника, крови воротной вены и гепатоциты. При внутривенном введении пресистемная элиминация отсутствует.
Пресистемная элиминация ЛС (эффект первого прохождения) процесс биотрансформации лекарства до попадания ЛС в системный кровоток. В пресистемной элиминации при пероральном введении лекарства участвуют ферментативные системы кишечника, крови воротной вены и гепатоциты. При внутривенном введении пресистемная элиминация отсутствует.
 В связи с тем, что лекарственные вещества оказывают резорбтивное действие только после того как они достигли системного кровотока (и затем распределились по органам и тканям), вводится понятие биодоступность.
В связи с тем, что лекарственные вещества оказывают резорбтивное действие только после того как они достигли системного кровотока (и затем распределились по органам и тканям), вводится понятие биодоступность.
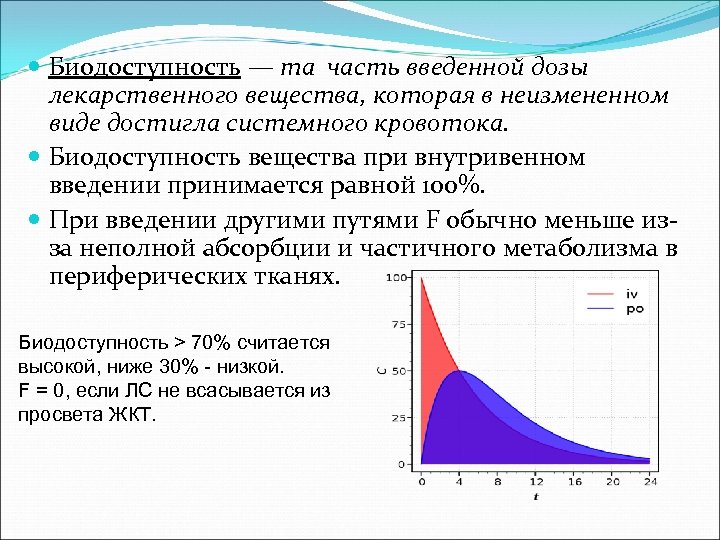 Биодоступность — та часть введенной дозы лекарственного вещества, которая в неизмененном виде достигла системного кровотока. Биодоступность вещества при внутривенном введении принимается равной 100%. При введении другими путями F обычно меньше изза неполной абсорбции и частичного метаболизма в периферических тканях. Биодоступность > 70% считается высокой, ниже 30% - низкой. F = 0, если ЛС не всасывается из просвета ЖКТ.
Биодоступность — та часть введенной дозы лекарственного вещества, которая в неизмененном виде достигла системного кровотока. Биодоступность вещества при внутривенном введении принимается равной 100%. При введении другими путями F обычно меньше изза неполной абсорбции и частичного метаболизма в периферических тканях. Биодоступность > 70% считается высокой, ниже 30% - низкой. F = 0, если ЛС не всасывается из просвета ЖКТ.
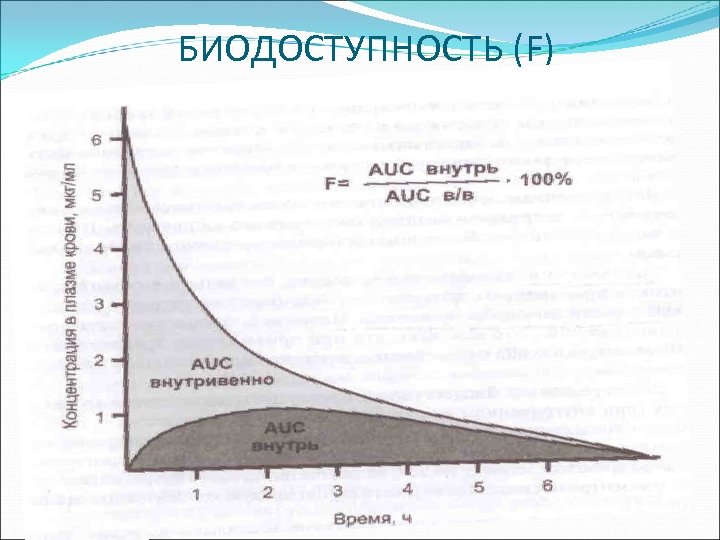 БИОДОСТУПНОСТЬ (F)
БИОДОСТУПНОСТЬ (F)
 Детерминанты биодоступности: 1) скорость всасывания 2) полнота всасывания - недостаточная абсорбция ЛС вследствие его очень высокой гидрофильности или липофильности, метаболизма бактериями кишечника при энтеральном введении и т. д. 3) пресистемная элиминация – при высокой биотрансформация в печени F ЛС низкая (нитроглицерин при пероральном введении). 4) лекарственная форма - сублингвальные таблетки и ректальные суппозитории помогают ЛС избежать пресистемной элиминации
Детерминанты биодоступности: 1) скорость всасывания 2) полнота всасывания - недостаточная абсорбция ЛС вследствие его очень высокой гидрофильности или липофильности, метаболизма бактериями кишечника при энтеральном введении и т. д. 3) пресистемная элиминация – при высокой биотрансформация в печени F ЛС низкая (нитроглицерин при пероральном введении). 4) лекарственная форма - сублингвальные таблетки и ректальные суппозитории помогают ЛС избежать пресистемной элиминации
 Для сравнительной характеристики препаратов, в частности, препаратов, производимых различными фармацевтическими предприятиями и содержащих одно и то же вещество в одинаковой дозе, используют понятие «биоэквивалентность» . Два препарата считаются биоэквивалентными, если они обладают одинаковой биодоступностью и константой скорости всасывания (характеризует скорость поступления ЛВ в системный кровоток из места введения). При этом биоэквивалентные препараты должны обеспечивать одинаковую скорость достижения максимальной концентрации вещества в крови.
Для сравнительной характеристики препаратов, в частности, препаратов, производимых различными фармацевтическими предприятиями и содержащих одно и то же вещество в одинаковой дозе, используют понятие «биоэквивалентность» . Два препарата считаются биоэквивалентными, если они обладают одинаковой биодоступностью и константой скорости всасывания (характеризует скорость поступления ЛВ в системный кровоток из места введения). При этом биоэквивалентные препараты должны обеспечивать одинаковую скорость достижения максимальной концентрации вещества в крови.
 РАСПРЕДЕЛЕНИЕ ЛС
РАСПРЕДЕЛЕНИЕ ЛС
 Распределение ЛС - процесс распространения ЛС по органам и тканям после того, как они поступят в системный кровоток. Отсеки распределения: 1. Внеклеточное пространство (плазма, межклеточная жидкость) 2. Клетки (цитоплазма, мембрана органелл) 3. Жировая и костная ткань (депонирование ЛС) Характер распределения ЛВ во многом определяется их способностью растворяться в воде или липидах (т. е. их относительной гидрофильностью или липофильностью), а также интенсивностью регионарного кровотока.
Распределение ЛС - процесс распространения ЛС по органам и тканям после того, как они поступят в системный кровоток. Отсеки распределения: 1. Внеклеточное пространство (плазма, межклеточная жидкость) 2. Клетки (цитоплазма, мембрана органелл) 3. Жировая и костная ткань (депонирование ЛС) Характер распределения ЛВ во многом определяется их способностью растворяться в воде или липидах (т. е. их относительной гидрофильностью или липофильностью), а также интенсивностью регионарного кровотока.
 Гидрофильные полярные вещества распределяются в организме неравномерно. Большинство гидрофильных ЛВ не проникают в клетки и распределяются в основном в плазме крови и интерстициальной жидкости. В интерстициальную жидкость они попадают через межклеточные промежутки в эндотелии сосудов. В эндотелии капилляров мозга межклеточные промежутки отсутствуют -эндотелиальные клетки плотно прилегают друг к другу (между клетками имеются так называемые плотные контакты). Такой непрерывный слой эндотелиальных клеток образует гематоэнцефалический барьер (ГЭБ), препятствующий распределению гидрофильных полярных веществ (в том числе ионизированных молекул) в ткани мозга. Через этот барьер немногие гидрофильные ЛВ (например, леводопа) проникают только с помощью активного транспорта.
Гидрофильные полярные вещества распределяются в организме неравномерно. Большинство гидрофильных ЛВ не проникают в клетки и распределяются в основном в плазме крови и интерстициальной жидкости. В интерстициальную жидкость они попадают через межклеточные промежутки в эндотелии сосудов. В эндотелии капилляров мозга межклеточные промежутки отсутствуют -эндотелиальные клетки плотно прилегают друг к другу (между клетками имеются так называемые плотные контакты). Такой непрерывный слой эндотелиальных клеток образует гематоэнцефалический барьер (ГЭБ), препятствующий распределению гидрофильных полярных веществ (в том числе ионизированных молекул) в ткани мозга. Через этот барьер немногие гидрофильные ЛВ (например, леводопа) проникают только с помощью активного транспорта.
 Однако есть участки мозга, не защищенные гематоэнцефалическим барьером. Триггерная зона рвотного центра доступна для действия веществ, не проникающих через ГЭБ, таких как антагонист дофаминовых рецепторов домперидон. Кроме того, при воспалении мозговых оболочек гематоэнцефалический барьер становится более проницаемым для гидрофильных Л В (это позволяет вводить внутривенно натриевую соль бензилпенициллина для лечения бактериального менингита).
Однако есть участки мозга, не защищенные гематоэнцефалическим барьером. Триггерная зона рвотного центра доступна для действия веществ, не проникающих через ГЭБ, таких как антагонист дофаминовых рецепторов домперидон. Кроме того, при воспалении мозговых оболочек гематоэнцефалический барьер становится более проницаемым для гидрофильных Л В (это позволяет вводить внутривенно натриевую соль бензилпенициллина для лечения бактериального менингита).
 Кроме ГЭБ, в организме есть другие гистогематические барьеры (т. е. барьеры, отделяющие кровь от тканей), которые являются препятствием для распределения гидрофильных Л В. К ним относятся: гематоофтальмический барьер гематотестикулярный, гематоплацентарный барьеры.
Кроме ГЭБ, в организме есть другие гистогематические барьеры (т. е. барьеры, отделяющие кровь от тканей), которые являются препятствием для распределения гидрофильных Л В. К ним относятся: гематоофтальмический барьер гематотестикулярный, гематоплацентарный барьеры.
 Относительно равномерно распределяются в организме липофильные неполярные вещества. Они проникают путем пассивной диффузии через мембраны клеток и распределяются как во внеклеточной, так и во внутриклеточной жидкостях организма. Липофильные ЛВ проходят через все гистогематические барьеры, в частности, диффундируют непосредственно через мембраны эндотелиальных клеток капилляров в ткани мозга. Липофильные Л В легко проходят через плацентарный барьер.
Относительно равномерно распределяются в организме липофильные неполярные вещества. Они проникают путем пассивной диффузии через мембраны клеток и распределяются как во внеклеточной, так и во внутриклеточной жидкостях организма. Липофильные ЛВ проходят через все гистогематические барьеры, в частности, диффундируют непосредственно через мембраны эндотелиальных клеток капилляров в ткани мозга. Липофильные Л В легко проходят через плацентарный барьер.
 В клинической практике используют параметр, который получил название кажущийся объем распределения (apparent volume of distribution, Vd). Кажущийся объем распределения - гипотетический объем жидкости организма, в котором лекарственное вещество распределено равномерно и при этом находится в концентрации, равной концентрации данного вещества в плазме крови. Vd= общее количество вещества в организме ∕ концентрация в плазме крови.
В клинической практике используют параметр, который получил название кажущийся объем распределения (apparent volume of distribution, Vd). Кажущийся объем распределения - гипотетический объем жидкости организма, в котором лекарственное вещество распределено равномерно и при этом находится в концентрации, равной концентрации данного вещества в плазме крови. Vd= общее количество вещества в организме ∕ концентрация в плазме крови.
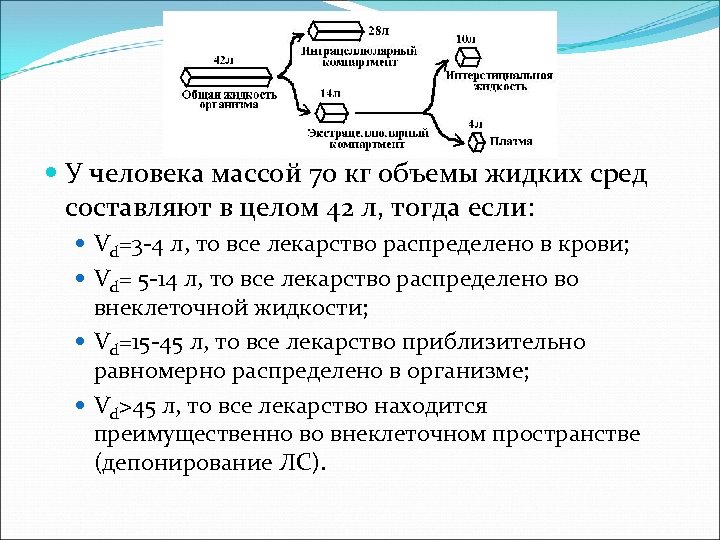 У человека массой 70 кг объемы жидких сред составляют в целом 42 л, тогда если: Vd=3 -4 л, то все лекарство распределено в крови; Vd= 5 -14 л, то все лекарство распределено во внеклеточной жидкости; Vd=15 -45 л, то все лекарство приблизительно равномерно распределено в организме; Vd>45 л, то все лекарство находится преимущественно во внеклеточном пространстве (депонирование ЛС).
У человека массой 70 кг объемы жидких сред составляют в целом 42 л, тогда если: Vd=3 -4 л, то все лекарство распределено в крови; Vd= 5 -14 л, то все лекарство распределено во внеклеточной жидкости; Vd=15 -45 л, то все лекарство приблизительно равномерно распределено в организме; Vd>45 л, то все лекарство находится преимущественно во внеклеточном пространстве (депонирование ЛС).
 Детерминанты распределения Природа ЛС - чем меньше размеры молекулы и липофильнее ЛС, тем быстрее и равномернее его распределение. Размер органов – чем больше размер органа, тем больше лекарственного средства может поступить в него без существенного изменения градиента концентраций Кровоток в органе - в хорошо перфузируемых тканях (мозг, сердце, почки) терапевтическая концентрация вещества создается значительно раньше, чем в тканях плохо перфузируемых (жировая, костная) Наличие гистогематических барьеров – ЛС легко проникают в ткани с плохо выраженным ГГБ Связывание лекарства с белками плазмы - чем больше связанная фракция ЛС, тем хуже его распределение в ткани, т. к. покидать капилляр могут лишь свободные молекулы. Депонирование лекарства в тканях - связывание ЛС с белками тканей способствует его накоплению в них, т. к. снижается концентрация свободного ЛС в периваскулярном пространстве и постоянно поддерживается высокий градиент концентраций между кровью и тканями.
Детерминанты распределения Природа ЛС - чем меньше размеры молекулы и липофильнее ЛС, тем быстрее и равномернее его распределение. Размер органов – чем больше размер органа, тем больше лекарственного средства может поступить в него без существенного изменения градиента концентраций Кровоток в органе - в хорошо перфузируемых тканях (мозг, сердце, почки) терапевтическая концентрация вещества создается значительно раньше, чем в тканях плохо перфузируемых (жировая, костная) Наличие гистогематических барьеров – ЛС легко проникают в ткани с плохо выраженным ГГБ Связывание лекарства с белками плазмы - чем больше связанная фракция ЛС, тем хуже его распределение в ткани, т. к. покидать капилляр могут лишь свободные молекулы. Депонирование лекарства в тканях - связывание ЛС с белками тканей способствует его накоплению в них, т. к. снижается концентрация свободного ЛС в периваскулярном пространстве и постоянно поддерживается высокий градиент концентраций между кровью и тканями.
 ДЕПОНИРОВАНИЕ ЛС
ДЕПОНИРОВАНИЕ ЛС
 При распределении в организме некоторые Л В частично могут задерживаться и накапливаться в различных тканях. Происходит это в основном вследствие обратимого связывания ЛВ с белками, фосфолипидами и нуклеопротеинами клеток. Этот процесс носит название депонирование. Концентрация вещества в месте его депонирования (в депо) может быть достаточно высокой. Из депо вещество постепенно высвобождается в кровь и распределяется по другим органам и тканям, в том числе достигая места своего действия. Депонирование может привести к удлинению (пролонгированию) действия препарата или возникновению эффекта последействия. Депонирование ЛВ в некоторых тканях может привести к развитию побочных эффектов.
При распределении в организме некоторые Л В частично могут задерживаться и накапливаться в различных тканях. Происходит это в основном вследствие обратимого связывания ЛВ с белками, фосфолипидами и нуклеопротеинами клеток. Этот процесс носит название депонирование. Концентрация вещества в месте его депонирования (в депо) может быть достаточно высокой. Из депо вещество постепенно высвобождается в кровь и распределяется по другим органам и тканям, в том числе достигая места своего действия. Депонирование может привести к удлинению (пролонгированию) действия препарата или возникновению эффекта последействия. Депонирование ЛВ в некоторых тканях может привести к развитию побочных эффектов.
 Многие Л В связываются с белками плазмы крови. Слабокислые соединения (нестероидные противовоспалительные средства, сульфаниламиды) связываются в основном с альбуминами (самой большой фракцией белков плазмы), а слабые основания с гликопротеинами и некоторыми другими белками плазмы крови. Связывание ЛВ с плазменными белками- обратимый процесс, который может быть представлен следующим образом: ЛВ + белок <=> комплекс ЛВ-белок.
Многие Л В связываются с белками плазмы крови. Слабокислые соединения (нестероидные противовоспалительные средства, сульфаниламиды) связываются в основном с альбуминами (самой большой фракцией белков плазмы), а слабые основания с гликопротеинами и некоторыми другими белками плазмы крови. Связывание ЛВ с плазменными белками- обратимый процесс, который может быть представлен следующим образом: ЛВ + белок <=> комплекс ЛВ-белок.
 Комплексы «вещество — белок» не проникают через мембраны клеток и через межклеточные промежутки в эндотелии сосудов (не фильтруются они и в капиллярах почечных клубочков) и поэтому являются своеобразным резервуаром или депо данного вещества в крови. Связанное с белками ЛВ не проявляет фармакологической активности. Но поскольку это связывание обратимо, часть вещества постоянно высвобождается из комплекса с белком (происходит это при снижении концентрации свободного вещества в плазме крови) и оказывает фармакологическое действие.
Комплексы «вещество — белок» не проникают через мембраны клеток и через межклеточные промежутки в эндотелии сосудов (не фильтруются они и в капиллярах почечных клубочков) и поэтому являются своеобразным резервуаром или депо данного вещества в крови. Связанное с белками ЛВ не проявляет фармакологической активности. Но поскольку это связывание обратимо, часть вещества постоянно высвобождается из комплекса с белком (происходит это при снижении концентрации свободного вещества в плазме крови) и оказывает фармакологическое действие.
 БИОТРАНСФОРМАЦИЯ ЛС
БИОТРАНСФОРМАЦИЯ ЛС
 Биотрансформация (метаболизм) изменение химической структуры лекарственных веществ и их физикохимических свойств под действием ферментов организма. Биологический смысл биотрансформации ЛС Создание субстрата, удобного для последующей утилизации (в качестве энергетического или пластического материала) или в ускорении выведения ЛС из организма. Основная направленность метаболических превращений ЛС Неполярные ЛС → полярные (гидрофильные) метаболиты, выводимые с мочой.
Биотрансформация (метаболизм) изменение химической структуры лекарственных веществ и их физикохимических свойств под действием ферментов организма. Биологический смысл биотрансформации ЛС Создание субстрата, удобного для последующей утилизации (в качестве энергетического или пластического материала) или в ускорении выведения ЛС из организма. Основная направленность метаболических превращений ЛС Неполярные ЛС → полярные (гидрофильные) метаболиты, выводимые с мочой.
 Различают два основных вида метаболизма лекарственных веществ: - несинтетические реакции (метаболическая трансформация); - синтетические реакции (конъюгация). Лекарственные вещества могут подвергаться или метаболической биотрансформации (при этом образуются вещества, называемые метаболитами), или конъюгации (образуются конъюгаты). Но большинство Л В сначала метаболизируется при участии несинтетических реакций с образованием реакционноспособных метаболитов, которые затем вступают в реакции конъюгации
Различают два основных вида метаболизма лекарственных веществ: - несинтетические реакции (метаболическая трансформация); - синтетические реакции (конъюгация). Лекарственные вещества могут подвергаться или метаболической биотрансформации (при этом образуются вещества, называемые метаболитами), или конъюгации (образуются конъюгаты). Но большинство Л В сначала метаболизируется при участии несинтетических реакций с образованием реакционноспособных метаболитов, которые затем вступают в реакции конъюгации
 К метаболической трансформации относятся следующие реакции: Окисление (в печени под влиянием микросомальной системы ферментов) , восстановление, Гидролиз (осуществляется в основном немикросомальными ферментами (эстеразами, амидазами, фосфатазами) в плазме крови и тканях).
К метаболической трансформации относятся следующие реакции: Окисление (в печени под влиянием микросомальной системы ферментов) , восстановление, Гидролиз (осуществляется в основном немикросомальными ферментами (эстеразами, амидазами, фосфатазами) в плазме крови и тканях).
 Метаболиты, которые образуются в результате несинтетических реакций, могут в отдельных случаях обладать более высокой активностью, чем исходные соединения. Примером повышения активности лекарственных веществ в процессе метаболизма является использование предшественников лекарств (пролекарства).
Метаболиты, которые образуются в результате несинтетических реакций, могут в отдельных случаях обладать более высокой активностью, чем исходные соединения. Примером повышения активности лекарственных веществ в процессе метаболизма является использование предшественников лекарств (пролекарства).
 Пролекарства фармакологически неактивны, но в организме они превращаются в активные вещества Пролекарства обладают рядом преимуществ. Очень часто с их помощью решаются проблемы с доставкой лекарственного вещества к месту его действия. Например, леводопа является предшественником дофамина, но в отличие от дофамина она проникает через гематоэнцефалический барьер в ЦНС, где под действием ДОФАдекарбоксилазы превращается в активное вещество дофамин.
Пролекарства фармакологически неактивны, но в организме они превращаются в активные вещества Пролекарства обладают рядом преимуществ. Очень часто с их помощью решаются проблемы с доставкой лекарственного вещества к месту его действия. Например, леводопа является предшественником дофамина, но в отличие от дофамина она проникает через гематоэнцефалический барьер в ЦНС, где под действием ДОФАдекарбоксилазы превращается в активное вещество дофамин.
 В процессе биосинтетических реакций (конъюгация) к функциональным группировкам молекул лекарственных веществ или их метаболитов присоединяются остатки эндогенных соединений (глюкуроновой кислоты, глутатиона, глицина, сульфаты и др. ) или высокополярные химические группы (ацетильные, метильные группы). В процессе конъюгации образуются высокополярные гидрофильные соединения, которые быстро выводятся почками (многие метаболиты также подвергаются конъюгации).
В процессе биосинтетических реакций (конъюгация) к функциональным группировкам молекул лекарственных веществ или их метаболитов присоединяются остатки эндогенных соединений (глюкуроновой кислоты, глутатиона, глицина, сульфаты и др. ) или высокополярные химические группы (ацетильные, метильные группы). В процессе конъюгации образуются высокополярные гидрофильные соединения, которые быстро выводятся почками (многие метаболиты также подвергаются конъюгации).
 Под действием некоторых лекарственных веществ (фенобарбитал, рифампицин, карбамазепин, гризеофульвин) может происходить индукция (увеличение скорости синтеза) микросомальных ферментов печени. В результате при одновременном назначении с индукторами микросомальных ферментов других препаратов (например, глюкокортикоидов, пероральных контрацептивов) повышается скорость метаболизма последних и снижается их действие.
Под действием некоторых лекарственных веществ (фенобарбитал, рифампицин, карбамазепин, гризеофульвин) может происходить индукция (увеличение скорости синтеза) микросомальных ферментов печени. В результате при одновременном назначении с индукторами микросомальных ферментов других препаратов (например, глюкокортикоидов, пероральных контрацептивов) повышается скорость метаболизма последних и снижается их действие.
 Некоторые лекарственные вещества (циметидин, хлорамфеникол, кетоконазол, этанол) снижают активность метаболизирующих ферментов. Например, циметидин является ингибитором микросомального окисления и, замедляя метаболизм варфарина, может повысить его антикоагулянтный эффект и спровоцировать кровотечение. Известны вещества (фуранокумарины), содержащиеся в грейпфрутовом соке, которые угнетают метаболизм таких лекарственных веществ, как циклоспорин, мидазолам, алпразолам и, следовательно, усиливают их действие.
Некоторые лекарственные вещества (циметидин, хлорамфеникол, кетоконазол, этанол) снижают активность метаболизирующих ферментов. Например, циметидин является ингибитором микросомального окисления и, замедляя метаболизм варфарина, может повысить его антикоагулянтный эффект и спровоцировать кровотечение. Известны вещества (фуранокумарины), содержащиеся в грейпфрутовом соке, которые угнетают метаболизм таких лекарственных веществ, как циклоспорин, мидазолам, алпразолам и, следовательно, усиливают их действие.
 ВЫВЕДЕНИЕ ЛС ИЗ ОРГАНИЗМА
ВЫВЕДЕНИЕ ЛС ИЗ ОРГАНИЗМА
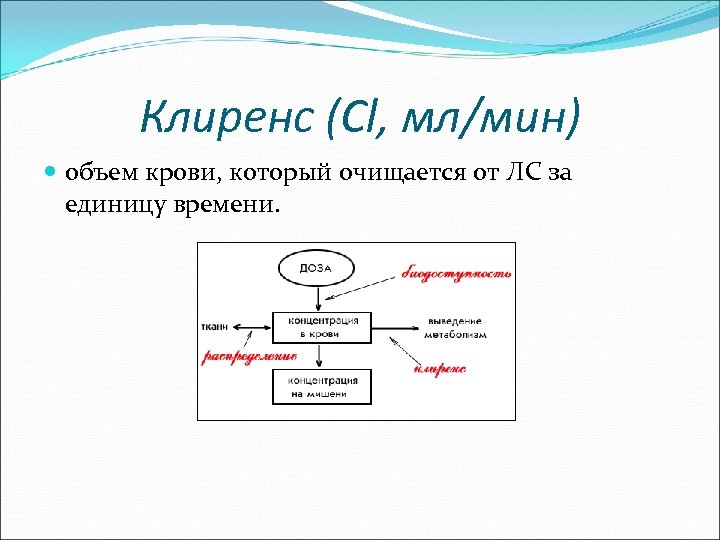 Клиренс (Cl, мл/мин) объем крови, который очищается от ЛС за единицу времени.
Клиренс (Cl, мл/мин) объем крови, который очищается от ЛС за единицу времени.
 Клиренс, размерность и связь с другими фармакокинетическими показателями. Т. к. плазма (кровь) - «видимая» часть объема распределения, то клиренс – фракция объема распределения, из которой лекарство выделяется в единицу времени. Если обозначить общее количество лекарства в организме через Аобщ, а количество, которое выделилось через Авыд, то : С другой стороны, из определения объема распределения следует, что общее количество лекарства в организме составляет Аобщ=Vd Cтер/плазма. Подставляя это значение в формулу клиренса, мы получим:
Клиренс, размерность и связь с другими фармакокинетическими показателями. Т. к. плазма (кровь) - «видимая» часть объема распределения, то клиренс – фракция объема распределения, из которой лекарство выделяется в единицу времени. Если обозначить общее количество лекарства в организме через Аобщ, а количество, которое выделилось через Авыд, то : С другой стороны, из определения объема распределения следует, что общее количество лекарства в организме составляет Аобщ=Vd Cтер/плазма. Подставляя это значение в формулу клиренса, мы получим:
 В таком виде формулу клиренса используют для расчета поддерживающей дозы лекарства (Dп), т. е той дозы лекарственного средства, которая должна скомпенсировать потерю лекарства и поддержать его уровень на постоянном уровне: Скорость введения = скорость выведения = Cl Cтер (доза/мин), т. е. : Dп = скорость введения ( - интервал, между приемом лекарства) ⇒ Dn=Cl Cтер
В таком виде формулу клиренса используют для расчета поддерживающей дозы лекарства (Dп), т. е той дозы лекарственного средства, которая должна скомпенсировать потерю лекарства и поддержать его уровень на постоянном уровне: Скорость введения = скорость выведения = Cl Cтер (доза/мин), т. е. : Dп = скорость введения ( - интервал, между приемом лекарства) ⇒ Dn=Cl Cтер
 Клиренс аддитивен, т. е. элиминация вещества из организма может происходить с участием процессов, идущих в почках, легких, печени и других органах: Clсистемный = Clпочечн. + Clпечени + Clдр. Клиренс так же связан с периодом полуэлиминации ЛС и объемом распределения: t 1/2=0, 7*Vd/Cl
Клиренс аддитивен, т. е. элиминация вещества из организма может происходить с участием процессов, идущих в почках, легких, печени и других органах: Clсистемный = Clпочечн. + Clпечени + Clдр. Клиренс так же связан с периодом полуэлиминации ЛС и объемом распределения: t 1/2=0, 7*Vd/Cl
 Период полувыведения лекарств Период полуэлиминации (t½, мин) – это время, необходимое для снижения концентрации ЛС в крови ровно наполовину. Период полуэлиминации определяют по формуле: Период полувыведения – важнейший фармакокинетический параметр, позволяющий: а) рассчитать время наступления равновесной концентрации (равно 4 -5 периодам полуэлиминации) б) определить время полной элиминации препарата в) предсказать концентрацию ЛС в любой момент времени (для ЛС с кинетикой первого порядка).
Период полувыведения лекарств Период полуэлиминации (t½, мин) – это время, необходимое для снижения концентрации ЛС в крови ровно наполовину. Период полуэлиминации определяют по формуле: Период полувыведения – важнейший фармакокинетический параметр, позволяющий: а) рассчитать время наступления равновесной концентрации (равно 4 -5 периодам полуэлиминации) б) определить время полной элиминации препарата в) предсказать концентрацию ЛС в любой момент времени (для ЛС с кинетикой первого порядка).
 Константа элиминации Константа скорости элиминации (kel, мин-1) – показывает, какая часть ЛС элиминируется из организма в единицу времени : Kel = Aвыд / Аобщ где Авыд – количество ЛС, выделяемое в ед. времени, Аобщ – общее количество ЛС в организме. [Kel] = час-1/мин-1=доля в час. Константа элиминации прямо пропорциональна клиренсу и обратно пропорционально объему распределения (из определения клиренса): Kel=CL/Vd
Константа элиминации Константа скорости элиминации (kel, мин-1) – показывает, какая часть ЛС элиминируется из организма в единицу времени : Kel = Aвыд / Аобщ где Авыд – количество ЛС, выделяемое в ед. времени, Аобщ – общее количество ЛС в организме. [Kel] = час-1/мин-1=доля в час. Константа элиминации прямо пропорциональна клиренсу и обратно пропорционально объему распределения (из определения клиренса): Kel=CL/Vd
 Почечный клиренс лекарств Почечный клиренс - это мера объема плазмы крови, которая очищается от лекарственного вещества в единицу времени почками: Cl (мл/мин) = U × V/P, где U - концентрация ЛС в мл мочи, V – объем мочи, выделяемой в мин P = концентрация ЛС в мл плазмы.
Почечный клиренс лекарств Почечный клиренс - это мера объема плазмы крови, которая очищается от лекарственного вещества в единицу времени почками: Cl (мл/мин) = U × V/P, где U - концентрация ЛС в мл мочи, V – объем мочи, выделяемой в мин P = концентрация ЛС в мл плазмы.
 Механизмы почечного клиренса клубочковая фильтрация, активная секреция в проксимальных канальцах и канальцевая реабсорбция. Факторы, влияющие на почечный Cl: а) гломерулярная фильтрация б) скорость почечного кровотока в) максимальная скорость секреции г) объём мочи д) фракция несвязанная в крови
Механизмы почечного клиренса клубочковая фильтрация, активная секреция в проксимальных канальцах и канальцевая реабсорбция. Факторы, влияющие на почечный Cl: а) гломерулярная фильтрация б) скорость почечного кровотока в) максимальная скорость секреции г) объём мочи д) фракция несвязанная в крови
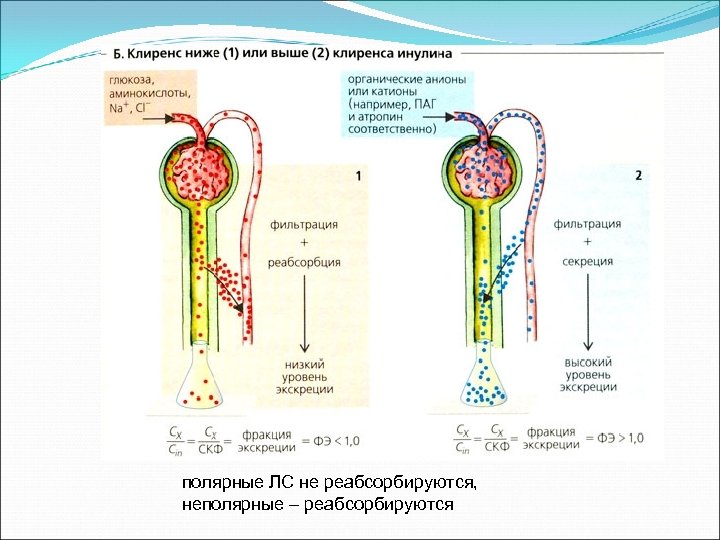 полярные ЛС не реабсорбируются, неполярные – реабсорбируются
полярные ЛС не реабсорбируются, неполярные – реабсорбируются
 Выведение почками слабых кислот и слабых оснований Кислая реакция мочи способствует экскреции слабых оснований и затрудняет выделение слабых кислот. Чтобы ускорить выведение почками слабых оснований, следует изменить реакцию мочи в кислую сторону (снизить р. Н мочи). Обычно в таких случаях назначают хлорид аммония. И наоборот, если необходимо повысить экскрецию слабых кислот, назначают натрия гидрокарбонат, сдвигающий реакцию мочи в щелочную сторону (повышают р. Н мочи).
Выведение почками слабых кислот и слабых оснований Кислая реакция мочи способствует экскреции слабых оснований и затрудняет выделение слабых кислот. Чтобы ускорить выведение почками слабых оснований, следует изменить реакцию мочи в кислую сторону (снизить р. Н мочи). Обычно в таких случаях назначают хлорид аммония. И наоборот, если необходимо повысить экскрецию слабых кислот, назначают натрия гидрокарбонат, сдвигающий реакцию мочи в щелочную сторону (повышают р. Н мочи).
 Энтерогепатический цикл ЛС Движение лекарства по циклической системе: кровоток → печень → желчные пути → кишечник → кровоток
Энтерогепатический цикл ЛС Движение лекарства по циклической системе: кровоток → печень → желчные пути → кишечник → кровоток
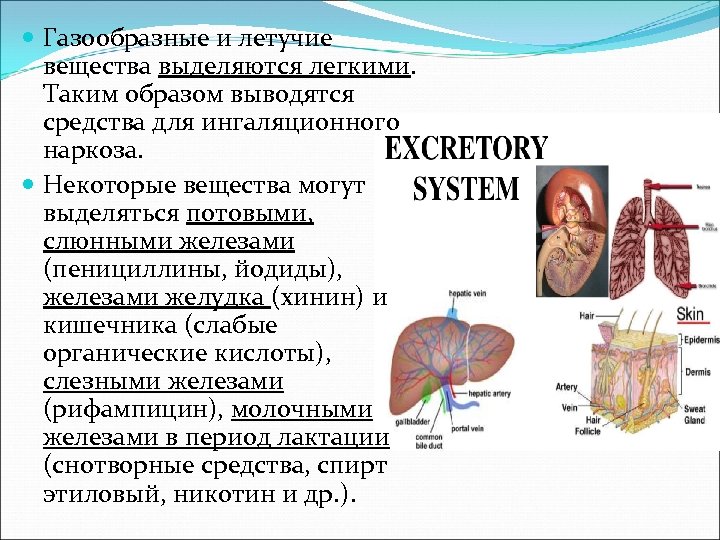 Газообразные и летучие вещества выделяются легкими. Таким образом выводятся средства для ингаляционного наркоза. Некоторые вещества могут выделяться потовыми, слюнными железами (пенициллины, йодиды), железами желудка (хинин) и кишечника (слабые органические кислоты), слезными железами (рифампицин), молочными железами в период лактации (снотворные средства, спирт этиловый, никотин и др. ).
Газообразные и летучие вещества выделяются легкими. Таким образом выводятся средства для ингаляционного наркоза. Некоторые вещества могут выделяться потовыми, слюнными железами (пенициллины, йодиды), железами желудка (хинин) и кишечника (слабые органические кислоты), слезными железами (рифампицин), молочными железами в период лактации (снотворные средства, спирт этиловый, никотин и др. ).
 Равновесная стационарная концентрация (Css). Для достижения оптимального терапевтического эффекта ЛВ необходимо постоянно поддерживать его терапевтическую концентрацию в крови. Постоянно поддерживаемый уровень вещества в плазме крови обозначается как стационарная концентрация (Css). Сss –концентрация ЛС, достигаемая при скорости введения равной скорости выведения. Подходы к управлению уровнем Сss: • изменить вводимую дозу ЛС (D); • изменить интервал введения (ΔT).
Равновесная стационарная концентрация (Css). Для достижения оптимального терапевтического эффекта ЛВ необходимо постоянно поддерживать его терапевтическую концентрацию в крови. Постоянно поддерживаемый уровень вещества в плазме крови обозначается как стационарная концентрация (Css). Сss –концентрация ЛС, достигаемая при скорости введения равной скорости выведения. Подходы к управлению уровнем Сss: • изменить вводимую дозу ЛС (D); • изменить интервал введения (ΔT).
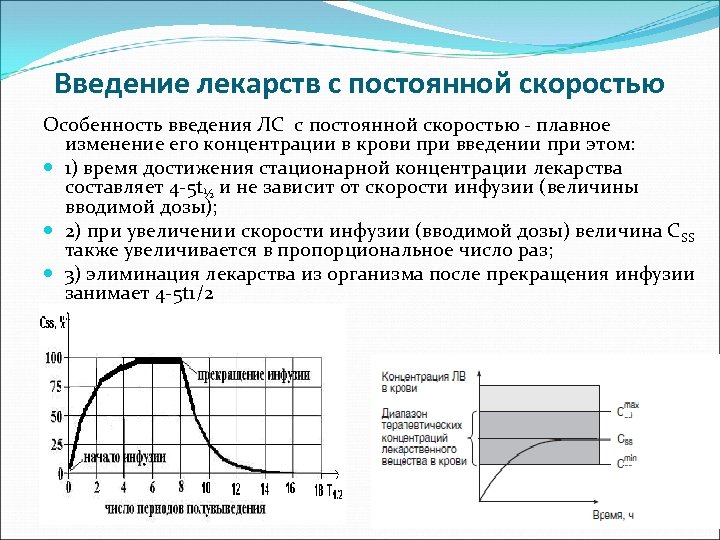 Введение лекарств с постоянной скоростью Особенность введения ЛС с постоянной скоростью - плавное изменение его концентрации в крови при введении при этом: 1) время достижения стационарной концентрации лекарства составляет 4 -5 t½ и не зависит от скорости инфузии (величины вводимой дозы); 2) при увеличении скорости инфузии (вводимой дозы) величина С SS также увеличивается в пропорциональное число раз; 3) элиминация лекарства из организма после прекращения инфузии занимает 4 -5 t 1/2
Введение лекарств с постоянной скоростью Особенность введения ЛС с постоянной скоростью - плавное изменение его концентрации в крови при введении при этом: 1) время достижения стационарной концентрации лекарства составляет 4 -5 t½ и не зависит от скорости инфузии (величины вводимой дозы); 2) при увеличении скорости инфузии (вводимой дозы) величина С SS также увеличивается в пропорциональное число раз; 3) элиминация лекарства из организма после прекращения инфузии занимает 4 -5 t 1/2
 Прерывистое введение лекарств Управление колебаниями Css: 1. Изменить дозу ЛС: при увеличении дозы ЛС диапазон колебаний его Css пропорционально увеличивается 2. Изменить интервал введения ЛС: при увеличении интервала введения ЛС диапазон колебаний его Css пропорционально уменьшается 3. Одновременно изменить дозу и интервал введения
Прерывистое введение лекарств Управление колебаниями Css: 1. Изменить дозу ЛС: при увеличении дозы ЛС диапазон колебаний его Css пропорционально увеличивается 2. Изменить интервал введения ЛС: при увеличении интервала введения ЛС диапазон колебаний его Css пропорционально уменьшается 3. Одновременно изменить дозу и интервал введения
 Вводная (загрузочная) доза – доза, вводимая за один прием и заполняющая весь объем распределения в действующей терапевтической концентрации. ВД=(Css*Vd)/F ; где Css –равновесная стационарная концентрация, Vd- кажущийся объем распределения, F- биодоступность. Терапевтический смысл Вводная доза быстро обеспечивает действующую терапевтическую концентрацию ЛС в крови, что позволяет, например, быстро купировать приступ БА, аритмии и т. д.
Вводная (загрузочная) доза – доза, вводимая за один прием и заполняющая весь объем распределения в действующей терапевтической концентрации. ВД=(Css*Vd)/F ; где Css –равновесная стационарная концентрация, Vd- кажущийся объем распределения, F- биодоступность. Терапевтический смысл Вводная доза быстро обеспечивает действующую терапевтическую концентрацию ЛС в крови, что позволяет, например, быстро купировать приступ БА, аритмии и т. д.
 Поддерживающая доза ЛС, вводимая систематически, которая заполняет объем клиренса, т. е. тот фрагмент объема распределения (Vd), который очищается от ЛС за интервал времени T: ПД=(Css*Cl* T)/F. Терапевтический смысл Поддерживающая доза компенсирует потери с клиренсом за интервал между введениями препарата.
Поддерживающая доза ЛС, вводимая систематически, которая заполняет объем клиренса, т. е. тот фрагмент объема распределения (Vd), который очищается от ЛС за интервал времени T: ПД=(Css*Cl* T)/F. Терапевтический смысл Поддерживающая доза компенсирует потери с клиренсом за интервал между введениями препарата.
 Факторы, количественно и качественно изменяющие эффект лекарств 1. Физиологические факторы: а) возраст - дети часто более чувствительны к вызываемым лекарствами изменениям в водном и электролитном обмене, кислотно-щелочном балансе; пожилые больные могут необычно реагировать из-за нарушений распределения, инактивации и выведения лекарства вследствие возрастных анатомических и физиологических изменений в организме, а также из-за сопутствующих заболеваний; б) пол - женщины, особенно во время беременности, могут быть более чувствительными к лекарствам; в) хронестезия и хронергия; хропестезия - циклические изменения в чувствительности биологических систем организма к лекарствам (циркадные изменения - в течение суток; циркатригентантные - в течение месяца; цирканнуальные - в течение года); хропергия - ритмические изменения в биосистемных эффектах, в частности в эффективности лекарств; учет хронергии позволяет определять время достижения оптимального эффекта при минимальном риске побочных эффектов, например гормональных препаратов.
Факторы, количественно и качественно изменяющие эффект лекарств 1. Физиологические факторы: а) возраст - дети часто более чувствительны к вызываемым лекарствами изменениям в водном и электролитном обмене, кислотно-щелочном балансе; пожилые больные могут необычно реагировать из-за нарушений распределения, инактивации и выведения лекарства вследствие возрастных анатомических и физиологических изменений в организме, а также из-за сопутствующих заболеваний; б) пол - женщины, особенно во время беременности, могут быть более чувствительными к лекарствам; в) хронестезия и хронергия; хропестезия - циклические изменения в чувствительности биологических систем организма к лекарствам (циркадные изменения - в течение суток; циркатригентантные - в течение месяца; цирканнуальные - в течение года); хропергия - ритмические изменения в биосистемных эффектах, в частности в эффективности лекарств; учет хронергии позволяет определять время достижения оптимального эффекта при минимальном риске побочных эффектов, например гормональных препаратов.
 Факторы, количественно и качественно изменяющие эффект лекарств 2. Особенности индивидуальной фармакокинетики лекарств. 3. Время приёма лекарств в зависимости от приёма и характера пищи, влияния факторов внешней среды. 4. Генетические факторы, влияющие на биоусвояемость и эффективность лекарств. 5. Лекарственное взаимодействие приёме нескольких лекарств. 6. Сопутствующие патологические изменения в органах (печень, почки, желудочно-кишечный тракт). 7. Чувствительность больного к лекарству. 8. Приверженность больного назначаемому врачом лечению
Факторы, количественно и качественно изменяющие эффект лекарств 2. Особенности индивидуальной фармакокинетики лекарств. 3. Время приёма лекарств в зависимости от приёма и характера пищи, влияния факторов внешней среды. 4. Генетические факторы, влияющие на биоусвояемость и эффективность лекарств. 5. Лекарственное взаимодействие приёме нескольких лекарств. 6. Сопутствующие патологические изменения в органах (печень, почки, желудочно-кишечный тракт). 7. Чувствительность больного к лекарству. 8. Приверженность больного назначаемому врачом лечению
 СПАСИБО ЗА ВНИМАНИЕ
СПАСИБО ЗА ВНИМАНИЕ


