11.ФГ рецепторных образований.ppt
- Количество слайдов: 63

Фармакогенетика рецепторных образований Лекция 11

Молекулярно-генетические методы, совмещенные с традиционными фармакологическими и биохимическими подходами дают возможность более глубокого понимания значения изменений рецепторных белков. В таблице 1 в хронологическом порядке указаны связанные наблюдения. с рецепторами фармакогенетические
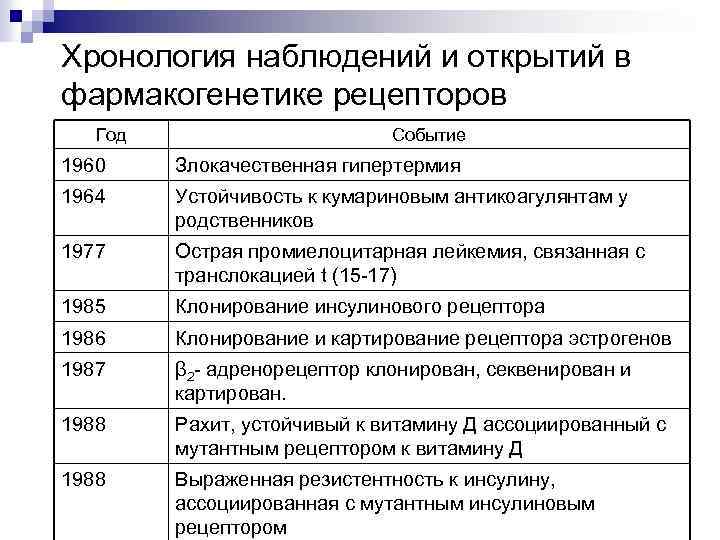
Хронология наблюдений и открытий в фармакогенетике рецепторов Год Событие 1960 Злокачественная гипертермия 1964 Устойчивость к кумариновым антикоагулянтам у родственников 1977 Острая промиелоцитарная лейкемия, связанная с транслокацией t (15 -17) 1985 Клонирование инсулинового рецептора 1986 Клонирование и картирование рецептора эстрогенов 1987 β 2 - адренорецептор клонирован, секвенирован и картирован. 1988 Рахит, устойчивый к витамину Д ассоциированный с мутантным рецептором к витамину Д 1988 Выраженная резистентность к инсулину, ассоциированная с мутантным инсулиновым рецептором
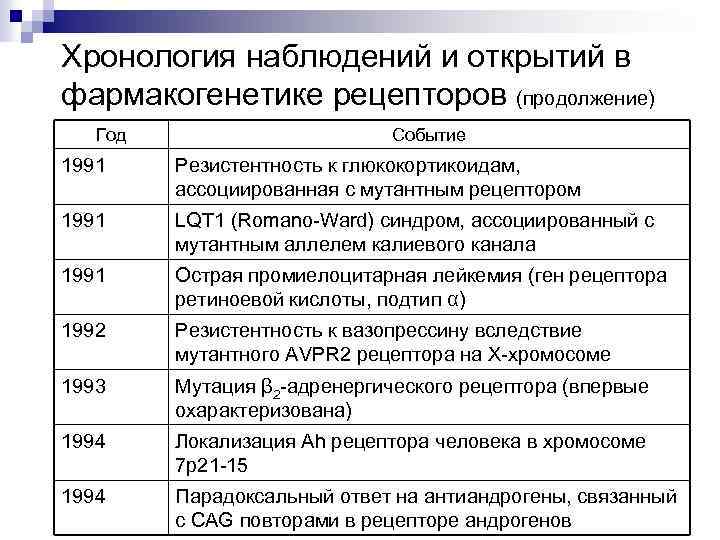
Хронология наблюдений и открытий в фармакогенетике рецепторов (продолжение) Год Событие 1991 Резистентность к глюкокортикоидам, ассоциированная с мутантным рецептором 1991 LQT 1 (Romano-Ward) синдром, ассоциированный с мутантным аллелем калиевого канала 1991 Острая промиелоцитарная лейкемия (ген рецептора ретиноевой кислоты, подтип α) 1992 Резистентность к вазопрессину вследствие мутантного AVPR 2 рецептора на Х-хромосоме 1993 Мутация β 2 -адренергического рецептора (впервые охарактеризована) 1994 Локализация Аh рецептора человека в хромосоме 7 р21 -15 1994 Парадоксальный ответ на антиандрогены, связанный с CAG повторами в рецепторе андрогенов
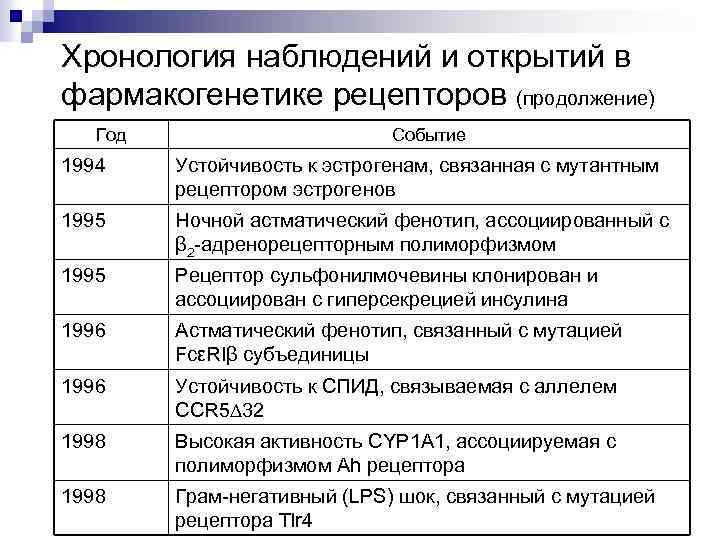
Хронология наблюдений и открытий в фармакогенетике рецепторов (продолжение) Год Событие 1994 Устойчивость к эстрогенам, связанная с мутантным рецептором эстрогенов 1995 Ночной астматический фенотип, ассоциированный с β 2 -адренорецепторным полиморфизмом 1995 Рецептор сульфонилмочевины клонирован и ассоциирован с гиперсекрецией инсулина 1996 Астматический фенотип, связанный с мутацией FcεRIβ субъединицы 1996 Устойчивость к СПИД, связываемая с аллелем CCR 5 32 1998 Высокая активность CYP 1 A 1, ассоциируемая с полиморфизмом Аh рецептора 1998 Грам-негативный (LPS) шок, связанный с мутацией рецептора Tlr 4
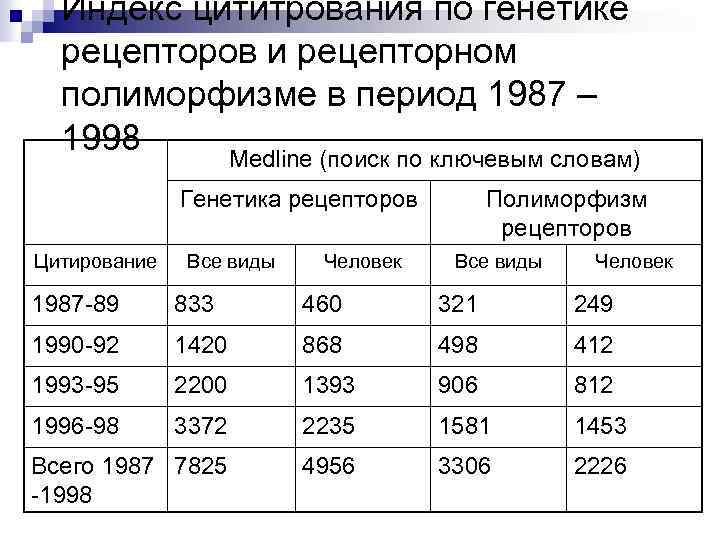
Индекс цититрования по генетике рецепторов и рецепторном полиморфизме в период 1987 – 1998 Medline (поиск по ключевым словам) Генетика рецепторов Цитирование Все виды Человек Полиморфизм рецепторов Все виды Человек 1987 -89 833 460 321 249 1990 -92 1420 868 498 412 1993 -95 2200 1393 906 812 1996 -98 3372 2235 1581 1453 Всего 1987 7825 -1998 4956 3306 2226

1. Резистентность к инсулину, обусловленная мутациями Инсулин играет ведущую роль в регуляции углеводного, липидного и белкового обмена, в обеспечении клеточного роста. Биологические функции инсулина в клетках-мишенях опосредуются одним белком – инсулиновым рецептором. Инсулиновый рецептор является мембранным гликопротеином, его синтез обеспечивается одним геном, после чего в несколько этапов происходит посттрансляционный процессинг, который включает глюкозилирование и протеолитическое разделение на две α и β субъединицы. Далее сформированный рецептор транспортируется и внедряется в плазматическую мембрану. Когда инсулин присоединяется к экстрацеллюлярному домену рецептора, возникает активация связанной с мембраной тирозинкиназы. Из предыдущей лекции Вы знаете, что именно активация тирозинкиназы обеспечивает все биологические ответы на инсулин в клеткахмишенях.

1. 2. 3. 4. 1. 1. Нарушение разделения прорецептора инсулина на α и β субъединицы. 23 -летней японке диагноз диабета был установлен с 6 -ти лет. Симптоматика включала признаки инсулинорезистентного диабета типа А с заметным увеличением инсулина в сыворотке, акантозом, гирсутизмом, вирилизацией. Ее старшая сестра была также больна. У обеих имелась задержка умственного развития, сниженный рост, дентальная дисплазия. Исследования в трансформированной вирусом Эпштейна-Барра культуре лимфоцитов выявили следующие нарушения: Заметное снижение связывания инсулина; Отсутствие сформированныех α и β субъединиц; Увеличение уровня иммунопреципитабельного материала. В 210 к. Д соответствующего по размеру неразделенному, полностью глюкозилированному рецептору; Автофосфорилирование белка 210 к. Д происходило только при высоких концентрациях инсулина.

Дополнительные исследования показали, что в клетках больной происходит синтез белков 190 к. Д и 210 к. Д с кинетикой, характерной для нормальных клеткок, однако с отсутствием белков, соответствующих α и β субъединицам. Уровень м. РНК инсулинового рецептора в трансформированных лимфоцитах больной оказался нормальным. Различий в размере транскриптов, которые гибридизировались с пробой ДНК инсулинового рецептора не выявлено. Установленные факты позволяют заключить, что экспрессия гена рецептора инсулина не нарушена, однако при нормальном транспорте, глюкозидации и встройке в мембрану отсутствует посттрансляционное разделение предшественника рецептора на α и β субъединицы. Анализ фрагмента в 275 пар оснований экзона 2 выявило однонуклеотидное замещение в кодоне 735 (AGC → AGT), ведущее к замене Arg на Ser, в результате участок разделения превращается из "Arg-Lys-Arg" в "Arg-Lys-Arg-Ser". Мягкая трипсинизация мутантного прорецептора привела к почти 5 кратному увеличению связывания инсулина, вероятно за счет образования нормальных α субъединиц.

2 -й случай Нарушенная активность тирозинкиназы, связанная с делецией киназного домена β субъединицы 17 -летняя японка с инсулин-резистентной формой диабета, рост снижен, акантоз. Было проведено исследование больной и ее семьи по параметрам, указанным в таблице 3.
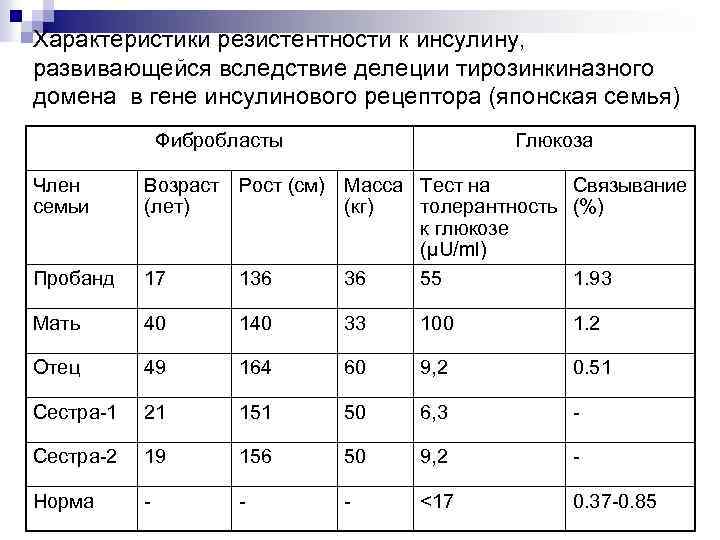
Характеристики резистентности к инсулину, развивающейся вследствие делеции тирозинкиназного домена в гене инсулинового рецептора (японская семья) Фибробласты Член семьи Глюкоза Пробанд Возраст Рост (см) Масса Тест на Связывание (лет) (кг) толерантность (%) к глюкозе (μU/ml) 17 136 36 55 1. 93 Мать 40 140 33 100 1. 2 Отец 49 164 60 9, 2 0. 51 Сестра-1 21 151 50 6, 3 - Сестра-2 19 156 50 9, 2 - Норма - - - <17 0. 37 -0. 85

Мать пациентки имела тот же фенотип, тогда как отец и 2 сестры не были больны. В родословной установлено, что прадедушка пробанда по материнской линии умер в тяжелом диабетическом статусе в 45 лет, несмотря на терапию инсулином. У дяди пробанда по материнской линии была выявлена резистентность к инсулину при операции по поводу язвы желудка, он умер, несмотря на введение инсулина. Свидетельств о близко родственных браках в семье не было. Эритроциты и культивированные фибробласты пробанда и ее матери имели нормальный уровень инсулинового связывания. Однако, степень инсулин-стимулированного автофосфорилирования инсулиновых рецепторов составляла лишь половину от контрольного уровня субъектов не больных диабетом. Активность тирозинкиназы по отношению к экзогенному субстрату была значительно редуцирована. Анализ ДНК инсулинового рецептора позволил выделить 3 аллеля А, В и С. Аллель С был найден у пробанда и матери, но не у 9 -ти других членов семьи и не у 103 контрольных японцев. Как сказано, прадедушка и дядя пробанда были диабетиками и имели низкий рост. Таким образом, в данной семье инсулин-резистентный диабет был связан с аллелем С и возможно наследовался как аутосомнодоминантный признак.

Исследование специфических участков с. ДНК инсулинового рецептора показало, что аллель С – является 13 -ти килобазным фрагментом ДНК, происходящим из 23 килобазного фрагмента (аллель А). Обнаружена мутация в 17 -м экзоне кодирующем аминокислоты, локализованные в АТФ-связывающем участке рецептора, который обеспечивает активацию тирозинкиназы. Возможный продукт мутантного гена содержал новую последовательность из 65 аминокислот у С-концевого участка, которая не была гомологичной ни одному из известных ранее белков, таким образом, мутантный рецептор не должен был проявлять киназную активность. 3 -й случай – Гомозиготная делеция в гене рецептора инсулина. Лепречаунизм как результат. 15 -ти месячный новорожденный с лепречаунизмом был ребенком двоюродных брата и сестры. При рождении было отмечено незначительное отставание внутриутробного роста, заметный гирсутизм, атрофия конечностей, выбухание живота, небольшое треугольное лицо и выпуклые глаза. На 3 -й день после рождения у него развилась умеренная гипергликемия (глюкоза в плазме – 8 -19 ммоль/л) и заметно увеличился уровень инсулина в плазме (1100 -1700 μU/ml при норме – 0 -25 μU).

У ребенка отмечалось значительное отставание в росте и массе тела. Дополнительно возникли гипертрофическая кардиомиопатия, холестатическая желтуха, рекуррентные респираторные инфекции, наблюдалась общая задержка развития. Фибробласты новорожденного имели нормальный кариотип, цитогенетически определяемых делеций в хромосоме 19 р 13. 2 -13. 3, на которой локализован ген инсулина не выявлено. Однако при анализе геномной ДНК ребенка установлено отсутствие участков специфичных для рецептора инсулина, в то время как в ДНК обоих родителей они были определены. Эти данные подтверждены другими методами анализа ДНК, и таким образом, у пациента в гене рецептора инсулина была обнаружена гомозиготная делеция, приведшая к лепречаунизму. Вопреки ожиданиям, полная делеция гена инсулинового рецептора оказалась совместимой с жизнью.

Генетический аспект Генетическая предрасположенность к инсулин-резистентным состояниям – редкий признак, наследуемый полигенно. Имеются веские доказательства, что именно мутации в гене инсулинового рецептора являются важным фактором их патогенеза. Ряд таких мутаций, идентифицированных на 1998 год представлен в табл. 4. Основная их часть – мутации, нарушающие смысл, либо ведущие к преждевременному обрыву считывания. В редких случаях одна и та же мутация определялась у генетически несвязанных родителей, но большинство мутаций определено только у родственников. Некоторые пациенты имели два мутантных аллеля – например, вышеописанный пациент от близкородственного брака был гомозиготным по одной и той же мутации, некоторые были гетерозиготами. Несколько родословных инсулин-резистентных больных изучено в деталях. В некоторых мутации были рецессивными, и заболевшие являлись гомозиготами, в этих случаях гетерозиготные родители и сибсы не имели признаков заболевания. В других семьях мутация наследовалась как доминантный признак.
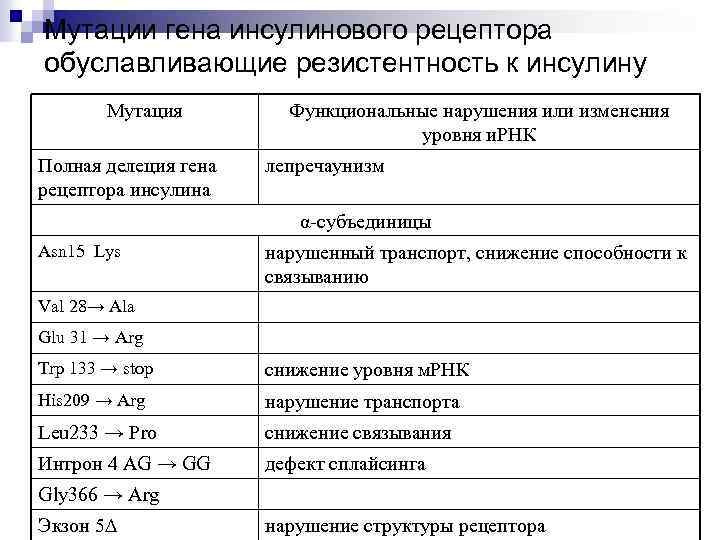
Мутации гена инсулинового рецептора обуславливающие резистентность к инсулину Мутация Полная делеция гена рецептора инсулина Функциональные нарушения или изменения уровня и. РНК лепречаунизм α-субъединицы Asn 15 Lys нарушенный транспорт, снижение способности к связыванию Val 28→ Ala Glu 31 → Arg Trp 133 → stop снижение уровня м. РНК His 209 → Arg нарушение транспорта Leu 233 → Pro снижение связывания Интрон 4 AG → GG дефект сплайсинга Gly 366 → Arg Экзон 5 нарушение структуры рецептора

Мутации гена инсулинового рецептора у устойчивых к инсулину субъектов Мутация Эффект на функцию или уровень м. РНК Phe 382 → Val нарушенный транспорт Lys 460 → Glu увеличение аффинности, снижение р. Н чувствительности Gln 672 → stop нарушение структуры рецептора Asn 452 → Ser снижение р. Н чувствительности Arg 735 → Ser неразделенный рецептор, снижение связывающей способности β - субъединица Arg 897 → Stop cнижен уровень м. РНК Экзон 14 нарушение структуры рецептора Val 985 → Met снижение активности тирозинкиназы Pro 986 → Leu снижение активности тирозинкиназы

Мутации гена инсулинового рецептора у устойчивых к инсулину субъектов Мутация Эффект на функцию или уровень м. РНК Arg 993 → Gln снижение активности тирозинкиназы Gly 1008 → Val снижение активности тирозинкиназы Lys 1058 → Glu снижение активности тирозинкиназы Ala 1134 → Trp снижение активности тирозинкиназы Ala 1135 → Leu снижение активности тирозинкиназы Met 1153 → Ile снижение активности тирозинкиназы Trp 1200 → Ser снижение активности тирозинкиназы

Молекулярные основы Ген рецептора инсулина человека состоит из 120 тысяч пар оснований и имеет 22 экзона. 11 экзонов, кодирующих αсубъединицу, охватывают 90 тысяча пар оснований, тогда как 11 экзонов, кодирующих β-субъединицу локализованы внутри участка, составляющего около 30 тысяч пар оснований. α- и β- субъединицы образуются в результате протеолитического процессинга прорецептора, состоящего из 1382 аминокислот. Последовательность из 731 аминокислоты - α- субъединица (Mr 135000) является внешней по отношению к цитоплазматической мембране и содержит инсулин-связывающий участок. α субъединица соединена внутрицепочечными дисульфидными мостиками с аминокислот β- субъединицей состоящей из 620. β- субъединица включает экстрацеллюлярный домен состоящий из 194 аминокислот, 23 х аминокислотный сегмент, проходящий через мембрану и 430 аминоксилотный цитоплазматический сегмент, обладающий тирозинкиназной активностью. α- субъединица и экстрацеллюлярная часть β- субъединицы гликозилированы.

Рассмотрим некоторые ключевые структурные участки гена рецептора инсулина. Phe 88 и Phe 89 и обогащенный цистеином домен играют роль в связывании инсулина. Cys 435 , Cys 468 , Cys 524 – обеспечивают сульфгидрильные группы для дисульфидных мостиков. Экзон 11 и 3'-конец α- субъединицы могут подвергаться вариабельному сплайсингу. Пять тирозинов ( Tyr 1158 , Tyr 1162 , Tyr 1163 , Tyr 1328, Tyr 1334) автофосфорилирования. Tyr 972 являются местами для - 4 -й аминокислотный остаток в мотиве Asn-Pro-Glu-Tyr играет существенную роль в рецепторном эндоцитозе. Впервые мутации в гене инсулинового рецептора были идентифицированы в 1988 г Kadowahi и Yoshimaso, с каждым годом их обнаруживается все больше, принципиально они могут быть разделены на 5 классов.

Класс 1. Нарушения биосинтеза рецептора. Снижение уровня рецепторной м. РНК, происходит в результате бессмысленных мутаций, сцепления интронов и экзонов, делеций, ведущих к нарушениям считывания. Остальные мутации, снижающие скорость транскрипции, картируются вне кодирующей области и наиболее вероятно локализованы в регуляторных доменах гена. Класс 2. Нарушения транспорта рецептора Некоторые мутации, обуславливают нарушение посттранскрипционной модификации т. е. N- или О-гликозилирование, образование дисульфидных мостиков между субъединицами, протеолитическое разделение на α и β-субъединицы, ацилирование. Они влияют на формирование и транспорт рецептора в место его локализации в мембране. Этот тип мутаций ведет к снижению числа рецепторов и к нарушению их аффинности к инсулину. Известные мутации этого класса Lys 15 Arg 209 , Val 382 , происходят в Nтерминальной части α – субъединицы.

Класс 3. Снижение аффинности к инсулину. Первая выявленная мутация этого класса аминокислоте 735, являющейся в картирована на мотиве Arg-Lys-Arg представленном в участке протеолитического разделения α и βсубъединиц. Замена Arg→Ser, ингибирует разделение предшественника рецептора, нарушает его конформацию, снижая аффинность к инсулину. Как отмечено выше, появление Lys 15 нарушает встраивание в мембрану, аффинности к инсулину. вызывая 5 -кратное снижение

Класс 4. Нарушение активности тирозинкиназы Многие мутации, идентифицированные в тирозинкиназном домене βсубъединицы, связаны с ингибированием киназной активности. Так, замена на Val 1008 является прототипом мутаций, которые ведут к инактивации тирозинкиназы, поскольку валин замещает глицин в мотиве Gly-X-XGly , являющимся АТФ-связывающим местом киназы. Другая интересная особенность мутаций тирозинкиназного домена состоит в том, что они определяют доминантное наследование резистентности к инсулину. Молекулярное объяснение этого следующее: инсулиновый рецептор имеет гетеротетрамерную структуру (α 2β 2). Возможны две симметричных формы α 2(βwt)2 и α 2(βmwt)2, и гибридная форма (α 2βwt βmwt). В исследованиях in vitro показано, что такие мутации могут заметно нарушают киназную активность, а также взаимодействие между субъединицами. Поэтому они проявляются как доминантное повреждение.

n Класс 5. Ускоренная деградация рецептора. n После соединения инсулина с рецептором дикого типа происходит эндоцитоз инсулин-рецепторного комплекса и освобождение инсулина при кислой р. Н, которая генерируется в эндосоме. Некоторые мутации, такие как Glu 460 и Ser 462 , нарушают освобождение инсулина, десенситизируя комплекс к кислой р. Н, что ведет рецептор к ускоренной деградации. Как результат - на поверхности клетки рециклизуется сниженное число мутантных рецепторов.

Злокачественная гипертермия – один из первых связанных с рецептором фармакогенетических феноменов который был описан более 30 лет назад, в связи с регистрацией летальных исходов при анестезии. У некоторых индивидуумов при галотановой анестезии наблюдалось повышение температуры, гиперметаболизм и мышечная ригидность. Клинический случай Австралиец 21 года был госпитализирован с переломом нижней конечности. Его беспокоила предстоящая общая анестезия, поскольку несколько его родственников умерли после эфирного наркоза. Справки у родителей пациента и семейного доктора показали, что из 38 родственников, получавших общую анестезию эфиром или этилхлоридом, 10 – умерли. Врач решил провести анестезию очень осторожно - без эфира, имея ввиду ее прекращение немедленно при возникновении побочных реакций. Пациенту была сделана премедикация (pethidine 100 мг, атропин 0, 6 мл) и анестезия тиопентоном (thiopentone 250 мг), а затем - оксид азота, кислород и галотан. Через 10 минут давление упало со 120 мм. рт. ст до 100, еще через 10 мин – до 80 мм. рт. ст. . Пульс возрос со 100 до 160 уд. в мин.

Анестезия была остановлена после 15 мин, но больной оставался без сознания в течение 30 мин. Его кожа была горячей и покрытой потом. Он постепенно восстановился в течение полутора часов и последующее лечение было нормальным. Через год он снова попал в стационар для удаления камня из желчного пузыря. Спинальная анестезия 11, 4 мл 0, 5% cinchocaine позволило удалить камень без осложнений. Генетический аспект Впервые была изучена большая австралийская родословная. Из 116 ее членов у 20 -ти ранее здоровых индивидуумов возникли побочные реакции в 21 случае применения анестезии. 8 случаев оказались летальными. На основе анализа этой и других родословных, был сделан вывод об аутосомно-доминантном наследовании осложнения. Регистрируемая частота зависела от возраста и составила 1: 15000 у детей и 1: 50000 – для взрослых.

Ген злокачественной гипертермии тесно связан с локусом гена ryanodine рецептора – кальций освобождающего канала саркоплазматического ретикулума. Последний расположен на длинном плече хромосомы 19 около локуса миотонической дистрофии. Молекулярные основы Прогресс в понимании механизмов дефекта обусловлен клонированием дефектного гена ryаnodine рецептора (RYR 1) от предрасположенных к ЗГ свиней. Эти исследования позволили идентифицировать единичную точковую мутацию (в нуклеотиде Т 1843 С) рецептора в кодоне 615, вызывающую замену аргинина у нечувствительных свиней на цистеин. Предполагается, что рецепторный белок (485000 Дальтон) действует как Са 2+ освобождающий канал и обеспечивает структурную связь канальной порой между саркоплазматическим ретикулумом и t-tubule в скелетных мышцах. У человека ген RYR 1 расположен в 19 -й хромосоме, 19 q 13. 1 -13. 2. Мутация найдена у 5% людей из семей со злокачественной гипертермией.

Вторая мутация Gly 248 Arg в гене рианодинового рецептора недавно обнаружена при изучении 35 семей. В других семьях злокачественная гипертермия не связана с рианодиновым локусом. Еще один локус, обуславливающий ЗГ, может принадлежать хромосоме 17 q 11. 2 -24. Альтернативной причиной осложнения рассматривают нарушения в клеточных сигнальных системах, включающих жирные кислоты и инозитол 1, 4. 5 -трифосфат (IP 3). Фенотип 3 Г также мог быть связан с хромосомой 3 q 13. 1. Несколько случаев 3 Г описаны в семьях с нарушенными натриевыми каналами. Фармакологический анализ биоптатов мышц человека и чувствительных животных показал, что метаболические ошибки при 3 Г увеличивают чувствительность мышц к расстройствам регуляции кальция в саркоплазматическом ретикулуме.

Для определения фенотипа 3 Г Kalow в 1970 г предложил тест, основанный на потенцировании галотаном мышечной контрактуры in vitro, вызываемой кофеином, так называемый галотан-кофеиновый контрактильный тест. Этот метод требует выполнения биопсии поперечно-полосатой мускулатуры и проводится в 40 лабораториях мира, причем 15 центров расположены на территории США и около 20 в европейских странах. Тест проводится следующим образом: мышечное волокно помещают в раствор кофеина, при этом в норме его разрыв происходит прикладывании усилия в > 0, 2 г, а при ПЗГ в > 0, 3 г. При помещении мышечного волокна в среду, содержащую галотан снижение концентрации галотана на 3% смещает точку разрыва волокна с > 0, 7 г до > 0, 5 г. Данные литературы позволяют утверждать, что этот тест является на 100% чувствительным и на 78% специфичным.

Диагностические признаки ЗГ • Тахикардия (необъяснимая) • Гиперкапния • Тахипноэ • Мышечная ригидность • Цианоз • Резкое повышение температуры (имеется в виду повышение температуры более, чем на 0, 5° С за 15 минут). • Нестабильное кровяное давление • Аритмия (желудочковая) • Ацидоз (респираторный и метаболический) • Коагулопатия (ДВС-синдром) Препараты, способные провоцировать ЗГ называются триггерными агентами. Традиционно триггерными считаются галогенсодержащие ингаляционные анестетики (галотан). сукцинилхолин и

Участие анестетиков в развитии ЗГ Триггерные препараты Сукцинилхолин Векуроний Панкуроний Декаметоний Диэтиловый эфир Галотан Энфлюран Изофлюран Дезфлюран Севофлюран Безопасные препараты Барбитураты Бензодиазепины Опиоиды Закись азота Нестероидные недеполяризующие мышечные релаксанты Все местные анестетики Этомидат Пропофол Кетамин

Значение Если при 3 Г не начать лечение немедленно, пациент может умереть за минуты от фибрилляции желудочков, в часы – от отека легких или коагулопатии, в течение дней – от неврологических и почечных расстройств. Внедрение нового внутримышечного релаксанта дантролена в качестве профилактического или терапевтического агента при 3 Г значительно улучшило ситуацию, т. к. первоначальная смертность при возникновении побочного эффекта - 70 -80% снизилась до 10%. Дантролен был введён в клиническую практику в 1975 году. Он был предложен как пероральный препарат, а несколько позже, в 1979 году, была приготовлена его лекарственная форма для в/в введения. Дантролен является мягким миорелаксантом с оригинальным, некурареподобным механизмом действия. После в/в введения натриевой соли дантролена эффект наступает спустя 620 минут. Достаточная концентрация в плазме сохраняется в течение 5 -6 часов. Длительность периода полуэлиминации у детей составляет 7 -10 часов, у взрослых около 12 часов. Дантролен подвергается метаболизму в печени и выводится из организма почечным путём.

Механизм действия дантролена состоит в замедлении высвобождения Са 2+ из саркоплазматического ретикулума, снижая, таким образом, концентрацию кальция в цитоплазме. В результате этого угнетается сократимость мышечных волокон и купируется гиперметаболизм мышечной клетки. 3. Доминантный пигментный ретинит. Варианты родопсина. Мутации в гене зрительного пигмента родопсина, члена семейства 7 трансмембранных рецепторов плазматической мембраны клетки, вызывают retinitis pigmentosa (RP) пигментный ретинит – группу наследственных заболеваний, ведущих к дегенерации фоторецепторов, палочек и колбочек в сетчатке. У лиц с такими заболеваниями обычно развивается ночная слепота в пубертатном периоде и они полностью слепнут в зрелом возрасте.

Последовательность спектральных изменений родопсина, индуцируемых светом Родопсин (11 -цис-ретиналь+опсин) (образуется основание шиффа с ε-аминогруппой Lys-296) Прелюмиродопсин (батородопсин) Лимиродопсин Метародопсин II (катализирует GTR GDP G-белка трансдуцина) Транс-ретиналь+опсин ТРАНСДУЦИН состоит из α- и βγ-субъединиц. α-субъединица связывается с GTR c. GMP βγ-субъединица активирует c. GMPфосфодиэстеразу c. GMP фосфодиэстераза гиперполяризация фоторецепторов

Генетический аспект Имеются примеры аутосомно-рецессивного, аутосомнодоминанатного и связанного с полом рецессивного наследования RP. RP, не связанный с другими нарушениями, наследуется наиболее часто по аутосомно-рецессивному типу – 84%, далее следует аутосомно-доминанатный тип – 10%. Случаи сцепленного с полом наследования обнаружены в белой популяции в США. Гены α-субъединицы G-белка трансдуцина и гены клеточных, связывающих ретинол белков I и II, локализованы на хромосоме 3. Локус для периферина (periferin – интегральный мембранный белок внешнего сегмента фоторецептора) расположен в хромосоме 6 р. Однако пока информации о хромосомных локусах других специфических компонентов, обеспечивающих каскад событий при зрении, недостаточно. Обнаруженные гены ответственны по одним данным за 25%, по другим – менее чем 2 -4% случаев заболеваний.

В 1989 г был найден первый молекулярный дефект в гене родопсина – замена Рro 23 His, ведущая к развитию RP. В последующем установлено около 40 дополнительных мутаций также связанных с заболеванием. Сопряжение восприятия света фоторецепторами с передачей нервного импульса осуществляется сложным комплексом структурно -конформационных перестроек родопсина и системы ц. ГМФ. Обнаруженные мутации нарушают эти процессы. Таким образом, патогенетические подходы к лечению состоят в коррекции функции мутантных белков.

4. Резистентность к вазопрессину. Нефрогенный несахарный диабет. Вазопрессин (аргинин - вазопрессин или AVP) – циклический нанопептид, участвующий в физиологической регуляции содержания воды, объема крови, сосудистого тонуса и кровяного давления. AVP также принадлежит к семейству вазоактивных и митогенных пептидов, влияющих на физиологический и патологический клеточный рост и дифференцировку. Гормон реализует свой эффект через мембранный AVPR 2 -рецептор вазопрессина, сопряженный с различными системами вторичных мессенджеров. Предполагается, что AVPR 2 рецептор представлен в почечных канальцах и в медуллярной части почки. Локус рецептора расположен совместно с хромосомным локусом нефрогенного несахарного диабета. Наследственный несахарный диабет проявляется неспособностью концентрировать мочу, несмотря на высокое содержание вазопрессина в плазме и при введении больших доз гормона и его аналогов.

У больных детей, преимущественно мальчиков, в неонатальном периоде наблюдается полиурия, лихорадка, периоды угрожающей жизни дегидратации, анорексия, рвота, нарушения развития, задержка роста. Нераспознанная нечувствительность к вазопрессину без лечения ведет к задержке умственного развития и смерти. У мужчин имеется тенденция к полной картине заболевания, тогда как у женщин проявляется в ранге статуса носителей, иногда неотличимо от нормы, до заметной полиурии. Антидиуретический эффект вазопрессина опосредуется через рецепторы почечного канала (V 2), тогда как прессорный и другие эффекты, такие как гликогенолиз, агрегация тромбоцитов опосредуется через сосудистые (V 1) рецепторы. V 2 рецепторы стимулируют аденилатциклазу и протеинкиназу А к генерации внутриклеточных ц. АМФ и вызывают резорбцию воды в дистальных извилистых канальцах и собирающем протоке нефрона.

V 1 рецепторы далее подразделяются на V 1α - cосудистые, печеночные и V 1β – рецепторы переднего гипофиза. V 1 рецепторы активируют фосфолипазу А 2, С и D, в результате чего образуется инозитол 1, 4, 5 -трифосфат (IP 3) и диацилглицерол (DAG), происходит мобилизация внутриклеточного кальция, вход экстраклеточного кальция, активация протеинкиназ и фосфорилирование белков, что ведет к вазоконстрикции. Лица с нефрогенным несахарным диабетом имеют нарушения в V 2 сигнальной системе, при нормальной V 1. Внепочечные эффекты V 2 рецепторов, такие как высвобождение фактора свертывания крови, фактора фибринолиза и увеличение уровня ренина в плазме – также нарушены.

История болезни Больной мальчик, родители литовцы, родился после беременности, осложненной гидроамниозом. В 13 месяцев имел дегидратацию, истощение, увеличение содержания натрия в крови, тяжелую полиурию, нечувствительную к воздействию вазопрессином или его аналогом десмопрессином. Ребенок был на поддерживающей терапии триазидными диуретиками с высококалорийной низкосолевой диетой и со свободным потреблением воды. На диуретики он отвечал снижением плазменной гиперосмолярности, улучшением концентрационной способности почек, умеренным снижением объема мочи и быстрым набором веса. Лабораторные исследования показали полную нечувствительность почек к вазопрессину, недостаточную концентрацию мочи, несмотря на высокий уровень вазопрессина в плазме. Введение 2 мкг десмопрессина не позволило увеличить осмолярность мочи.

Мать имела частичную почечную резистентность к вазопрессину со сдвигом вправо кривой доза-эффект, отражающей зависимость осмолярности мочи от концентрации вазопрессина в плазме. В последующем она родила разнояйцевых мальчиков-близнецов, у одного из которых через 10 недель после рождения было обнаружено увеличение содержания вазопрессина в плазме (12, 2 pg/ml) с осмолярностью плазмы 298 m osm/kg. Хотя лечение было начато немедленно, рост ребенка в первые 8 лет значительно отставал по сравнению с братом-близнецом. Генетический аспект нефрогенного несахарного диабета имеет историческое описание. Детальные генеалогические и клинические данные показывают, что Ulster Sсot, иммигрант, прибывший в Галифакс на корабле Hopewеll в 1761 г мог быть первым, принесшим это заболевание в северно-американские семьи. Однако выделение других мутаций в гене AVPR 2 рецептора опровергало эту гипотезу.

В первом медицинском описании заболевания Waring предложил, что это расстройство связано с Х-хромосомой и несколько других авторов опубликовали подтверждающие данные. Установлена локализация гена нефрогенного несахарного диабета - Xg 28. Молекулярные основы Изоляция гена V 2 рецепторов почек показала, что он контролирует синтез белка из 371 аминокислоты с относительной массой (Мr) 40, 285 (в отсутствие посттрансляционных модификаций). В гибридизационных исследованиях установлено, что ген V 2 рецептора находится в Х хромосоме и сублокализован в участке Х 27 qter. При молекулярном анализе выявлено, что ДНК пробанда содержит дополнительный цитозин, включенный в кодон для изолейцина 228. Больной брат-близнец имел ту же мутацию, тогда как у матери обнаружена смесь нормальных и мутантных последовательностей. У семьи нормальных субъектов таких мутаций не выявлено. Как результат этой мутации сдвига рамки 40% рецепторной последовательности в С-концевом отделе было оборвано преждевременным считыванием кодона и генерацией бессмысловых аминокислотных последовательностей.

Включение дополнительного цитозина также генерировало новый распознающий участок для рестрикционной эндонуклеазы Ear I, что проявляется в образцах RFLP и может быть использовано для выявления мутаций у больных мужчин и женщин – носителей. В нескольких других лабораториях также выявлены мутации гена AVPR 2, связанные с нефрогенным несахарным диабетом. Seibold и др. показали необычную структуру гена, включавшую два очень небольших интрона, второй из которых отделил последовательность, кодирующую 7 й трансмембранный участок рецептора от остального. В 1992 г Vander Ouweland тестировал 8 Х-связанных (X-linked) пробандов и их семьи и у трех из них выявил точковые мутации, которые вели к аминокислотному замещению, связанному с расстройством во всех семьях: глицин 185 в цистеин (G 353 Т), тирозин 205 в цистеин (А 614 G) и аргинин 203 в цистеин (C 604 T). Интересно, что все три точковые мутации вели к включению другого цистеина в рецепторный белок, предположительно нарушая образование дисульфидных мостиков, что могло повредить третичную структуру рецептора, влияя на связывание с гормоном или индуцированные им конформационные изменения.

Pan в 1992 г нашел 6 мутаций в V 2 рецепторе у 5 не родственников у одного из них выявлено две мутации. Большинство тяжело больных индивидуумов имели бессмысленные мутации, которые обрывали рецепторный белок в трансмембранном домене III. Из других установлено 3 бессмысленные мутации, сдвиг рамки и небольшая делеция внутри рамки. Нонсенс мутации кодона 119 у 4 -го пациента, произошли в результате СТ транзиции в Cp. G динуклеотиде. Эти мутации как бы "усекают" рецепторный белок внутри трансмембранного домена III и, возможно, ведут к образованию функционально недостаточного рецептора. Такая мутация была найдена у очень тяжелого пациента и рассматривается как новая, поскольку не была обнаружена в ДНК матери. Таким образом, обнаружение различных мутаций (миссенс и нонсенс точковых мутаций, мутаций сдвига рамки, небольших делеций), которые были определены у различных субъектов и в разных семьях доказывает генетическую гетерогенность нефрогенного несахарного диабета. Неполная резистентность к вазопрессину, наблюдаемая у некоторых больных, может быть связана с мутациями, которые лишь частично нарушают функциональные возможности рецептора вазопрессина.

Значение Выяснение природы, специфичности для родословных мутаций гена AVPR 2 дает большие возможности для обнаружения этого расстройства у женщин, статус носительства которых неизвестен. Молекулярный анализ этих рецепторов углубляет понимание их функционирования в здоровом и больном организме на этапах взаимодействия с гормоном и G-белками, что необходимо для совершенствования фармакотерапии.

Мутации в гене, кодирующем рецептор аргинин-вазопрессина (AVPR 2) Мутация Эффект на рецепторный белок Происхождение семьи, в которой установлена мутация Сдвиг считывания укорочение рамки в кодоне 277 Канада Ala 132→Asp Канада Tyr 128→Ser Канада Сдвиг считывания укорочение рамки в кодоне 230 США Gln 119→обрыв кодона укорочение США Arg 181→Cys и 247 -250 США Pro 286→Arg Эль-Сальвадор

Мутации в гене, кодирующем рецептор аргинин-вазопрессина (AVPR 2) Мутация Эффект на рецепторный белок Происхождение семьи, в которой установлена мутация Gly 185→Cys Нидерланды Arg 203→Cys Нидерланды Tyr 205→Cys Нидерланды Arg 202→Cys США Сдвиг считывания укорочение рамки в кодоне 228 Литва Arg 113→Trp Мейн (Шотландия) Trp 71→обрыв кодона укорочение США (Шотландское происхождение)

5. Антиандрогены и рак простаты Рак простаты – одна из наиболее распространенных форм злокачественных опухолей со смертельным исходом. Для дифференцировки и роста простаты необходимы андрогены, которые являются важным компонентом в канцерогенезе. Андрогены действуют через андрогенные рецепторы – члены суперсемейства лиганд-зависимых факторов транскрипции. Мутации в их рецепторах могут вызвать синдром андрогеннечувствительности, инактивации функций андрогенных рецепторов. Однако, мутации в генах андрогенных рецепторов, происходящие при раке простаты, не вызывают их инактивации. Более того, опухолевые клетки простаты могут содержать андрогенные рецепторы с мутациями, приводящими к стимуляции опухолевого роста эстрогенами, гестагенами и некоторыми антиандрогенами, например cyproterone acetate, hydroxyflutamide, nilutamide).

Генетический аспект После клонирования рецепторов андрогенов в 1988 г в их генах, , были обнаружены мутации типа миссенс, большие делеции, мутации сдвига рамки, в результате которых формируются андрогенные рецепторы либо неспособные, либо ограниченно способные связывать тестостерон. У этих форм повышена термолабильность и нарушена способность индуцировать транскрипцию. Это мутации относят к герминальным, влияющим в различной степени на развитие и формирование пола. Мутации андрогенного рецептора при раке простаты являются соматическими. Данные о них впервые получены в 1990 г. Пока не ясно, связаны ли они с наследованием или с предрасположенностью к раку простаты. В этнических группах и расах существует большая вариабельность по частоте развития заболевания. Так, американские негры рассматриваются как наиболее предрасположенные, тогда японцы – наименее. Эти различия в некоторой степени соответствуют отличиям в уровне тестостерона в сыворотке крови и 5α –редуктазной активности.

Гены андрогенных рецепторов у человека высоко полиморфны благодаря присутствию различных тринуклеотидных микросателлитов (CAG повторы) в 1 -м экзоне. В результате этого полиморфизма в N-терминальной части рецепторного белка транслируется различное число глутаминовых остатков. Андрогенные рецепторы при обычных, связанных с Х-хромосомой болезнях, например, спинальной и бульбарной мышечной атрофии, имеют увеличенное более чем в два раза число CAG повторов, что ограничивает их участие в процессах транскрипции. Имеются значительные различия в полиморфизме CAG повторов между белыми, черными и азиатами. Частоты аллелей бимодально распределены в каждой из групп, внутри групп частотный профиль сдвигается по направлению к более коротким аллелям у черных относительно двух других групп. Наиболее насыщенные аллели имеют 18, 21 и 22 CAG повторы у черных, белых и азиатов, соответственно. Различия между популяциями высоко достоверны. Важность полиморфизма по размеру CAG повторов неясна, но возможно, что такие последовательности ДНК могут быть потенциальными участками геномной нестабильности.

Молекулярные основы LNCа. P андрогенный рецептор опухолевых клеток простаты содержит единичную точковую мутацию, изменяющую смысл кодона 868 с треонина на аланин в лиганд-связывающем домене рецептора. LNCа. P опухолевые клетки содержат андрогенные рецепторы, которые отвечают на андрогены ростом клеточной культуры. В дополнение скорость роста увеличивается в присутствии низких доз эстрагенов и прогестагенов, при этом клетки не содержат ни эстрагенных, ни прогестагенных рецепторов. В противоположность ожидаемому, антиандрогены значительно стимулируют пролиферацию LNCа. P клеток. Их андрогенные рецепторы содержат ненормальные связывающие места со значительным увеличением афинности для прогестерона и эстрогенных стероидов.

WT и мутантный AP по-видимому имеют сходную аффинность для андрогенных соединений. Следовательно, точковая мутация, вызывающая замену треонина на аланин в функционально важном участке лигандсвязывающего домена андрогенного рецептора, ведет к снижению селективности связывания и полной реверсии эффектов антиандрогенов, которые обычно используются в терапии опухолей (cyproterone acetate, andronon). Для некоторых антиандрогенов, включая hydroxyflutamide, аффинность к мутантному андрогенному рецептору повышается, что усиливает взаимодействие рецептора с транскрипционными механизмами. Таким образом, можно представить, что мутация формирует "суперандрогенный" рецептор, обеспечивающий злокачественный рост даже в обедненной андрогенами среде. Были идентифицированы другие мутации андрогенного рецептора, влияющие на реакцию к лекарствам. У пациента, подвергшегося радикальной простатэктомии и имевшего признаки метастазирования, ген андрогенного рецептора в опухоли содержал полиморфный CAG микросателит, который кодировал различную длину повторов глутамина в рецепторном белке.

Анализ последовательности ДНК показал, что неопухолевые ткани содержат 24 CAG, тогда как опухолевые один фрагмент с24 CAG характерный для дикого типа и второй с18 CAG – мутантный тип. Остаток последовательности опухолевой и неопухолевой ДНК был идентичен последовательности дикого типа. Дальнейшее лечение показало, что у этого пациента специфичный для простаты антиген снижался после введения антиандрогена флутамида (flutamide), но позже увеличивался, несмотря на соответствующий кастрации уровень тестостерона. Исключение терапии флутамидом вело к быстрому снижению уровня антигена, что позволяет предполагать, что флутамид действовал парадоксально, как агонист.

Значение Парадоксальный эффект на прекращение терапии флутамидом был описан Scher и Kelly в 1993 г. Значение этого открытия заключается в том, что после начального ответа на андрогенную блокаду, болезнь прогрессировала, а при отмене препарата ее развитие замедлялось. Существование таких мутаций следует учитывать при терапии флутамидом. Похожий случай был описан с тамоксифеном при раке молочной железы. 6. Рецепторы эстрогенов, резистентность к эстрогенам. Ответы на антиэстрогены Эстрогены являются ключевыми регуляторами многих физиологических функций, особенно связанных с репродукцией и развитием молочных желез.

Рецептор эстрогенов был клонирован в 1986 г и локализован на хромосоме 6 g 25/1. Интактность эстрогенного рецептора важна для нормального роста скелета и развития, но мутации необязательно летальны. Описан высокий мужчина с открытыми эпифизами, сниженными толщиной и плотностью костей и увеличением уровня гонадотропинов и эстрогенов в плазме – уникальный случай такого состояния. Его симптомы объясняются точковой мутацией, в результате которой возникает сильно усеченный функционально инертный рецептор, теряющий как ДНК, - так и гормонсвязывающие домены. Терапия эстрогенами не способствовала снижению гонадотропинов, изменениям размеров костей или индукции гинекомастии. Такое продолжительное отсутствие ответа указывает на полную нечувствительность к эстрогенам. Информация о мутантных формах эстрогенных рецепторов быстро нарастает.

Несколько различных примеров м. РНК транскриптов эстрогенного рецептора ассоциированы с необычными ответами на эстрогены и антиандрогены. Фармакогенетический интерес имеют данные Mahfoudi 1995 г, который обнаружил, что замещения некоторых гидрофобных остатков в лигандсвязывающем домене (AF-2) драматически нарушают фармакологические свойства антагонистов эстрогенов, что может объяснить нечувствительность к тамоксифену в некоторых случаях рака молочной железы. Pink с соавторами в 1996 г выявил вариант эстрогенного рецептора, содержащего дупликацию внутри рамки экзонов 6 и 7. Этот вариант имеет 4 -5 копий дикого гена рецептора эстрогена вместо обычных двух копий. Он был открыт в клетках линии, развивающей эстрогеннезависимый рост. Работа является первой, в которой была обнаружена экспрессия мультикопий рецептора.

Montano в том же 1996 г описал рецепторы с точковой мутацией (Leu 540 Gln) с инвертированными свойствами. Они воспринимали антиэстрогены как эстрогены, активируясь ими, но не эстрадиолом. При этом их чувствительность к разным антиэстрогенам была неодинаковой. Zhang с соавторами в 1997 г выявили 3 миссенс спонтанных мутации, возникших в опухолевых клетках пациентов с метастатическим раком молочной железы. Одна из них (Tyr 537 Asn) не снижала транскрибирующую активность, по сравнению с диким типом, однако, такой рецептор оказался нечувствительным к тамоксифену или чистому антиэстрогену ICI 164384. Автор полагает, что аминокислотные замещения индуцировали конформационные изменения в рецепторе, которые придают ему конститутивную активность без влияния на его способность к димеризации. Другая мутация Asp 351 Tyr, конвертирует антиэстрогенное действие keoxifene в эстрогенное.

В 1997 г в журнале Science Pacch с соавторами опубликовал статью, демонстрирующую существование двух форм рецепторов эстрогенов α- и β. Эти генетически различные формы имеют неодинаковое распределение в нормальных и опухолевых клетках, различную реакцию на эстрогены и антиэстрогены. Их дальнейшие изучение более точно определит механизмы нечувствительности к эстрогенам и антиэстрогенам.
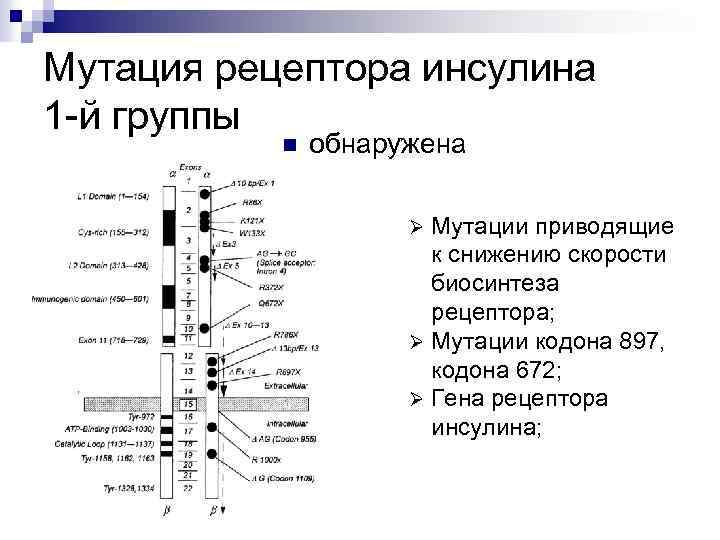
Мутация рецептора инсулина 1 -й группы n обнаружена Мутации приводящие к снижению скорости биосинтеза рецептора; Ø Мутации кодона 897, кодона 672; Ø Гена рецептора инсулина; Ø

Мутация рецептора инсулина 2 -й группы Ø Мутации, ухудшающие Ø Ø Ø внутриклеточный транспорт и посттрансляционный процессинг; Дефекты посттрансляционной модификации; Дефект транспорта рецептора к клеточной мембране; Снижение аффинности рецептора

Мутация рецептора инсулина 3 -й группы Ø Ø Ø Мутации, приводящие к дефектам связывания инсулина; Снижение аффинности; Мутация, приводящая к повышению аффинности инсулинового рецептора

Мутация рецептора инсулина 4 -й группы Ø Ø Мутации, сопровождающиеся снижением активности рецепторной тирозинкиназы; Мутации b-субъединицы рецептора, приводящие к снижению инсулинстимулированной рецепторной тирозинкиназы (делеции экзона 17 -22), мутации кодона 1109, мутации юкстамембранного домена, мутации, приводящие к снижению фосфорилирования IRS-1, мутации, внеклеточного домена со снижением активности тирозинкиназы, киназодефицитные мутации со снижением эндоцитоза инсулинрецкпторного комплекса и нарушением “down-regulation”.

Мутация рецептора инсулина 5 -й группы Ø Ø Мутации, ускоряющие деградацию инсулинового рецептора; Мутации глутамина – 460 (GLU-460), приводящие к ускорению деградации инсулинового рецептора
11.ФГ рецепторных образований.ppt