лек 6 фармакогенетика 23 09 08.ppt
- Количество слайдов: 35

ФАРМАКОГЕНЕТИКА Лекция СПб. ГУ № 6

ПЛАН ЛЕКЦИИ 1. Определение понятий (фармакотипирование, генотипирование, фармакогенетика, фармакогеномика) 2. Метаболим лекарств 3. Фазы детоксикации 4. Химические реакции биотрансформации 5. Индукция ферментов биотрансформации 6. Генетический полиморфизм ферментов 7. Взаимодействие цитохромов с лекарствами 8. Генетический полиморфизм и фармакотерапия 9. Чиповый метод анализа генетического полиморфизма


ОРГАНИЗМ И ЛЕКАРСТВО Фармакокинетика – абсорбция, распределение, метаболизм и выведение лекарства Фармакодинамика – взаимоотношение между концентрацией, местом действия и эффектом Фенотипирование лекарства- прямой метод определения активности лекарства по фармакокинетике субстрата Генотипирование - анализ полиморфизмов генов, определяющих метаболизм лекарства Генетическая гетерогенность - генный полиморфизм Фармакогенетика – индивидуальная реакция на лекарства Фармакогеномика – союз функциональной геномики и молекулярной фармакологии

Метаболизм лекарств Лекарства с высоким печеночным клиренсом: аминазин, аспирин, кортизон, , морфин, резерпин, метопролол, метилтестостерон, и др. Лекарства с низким печеночным клиренсом: теофеллин, парацетомол По скорости метаболизма лекарств различают: «Экстенсивные » метаболизаторы- норма «Медленные» метаболизаторы – сниженная «Быстрые или сверхактивные» метаболизаторы

ФАЗЫ ДЕТОКСИКАЦИИ Фаза 1 Несинтетические реакции (пролекарство – лекарство) Оксидазы со смешанной функцией Реакции восстановления и гидролиза Фаза II Синтетические реакции Коньюгация ЛС через метаболически активные радикалы (фазы I) Возможен метаболизм ЛС только за счет ферментов Фазы I или Фазы II
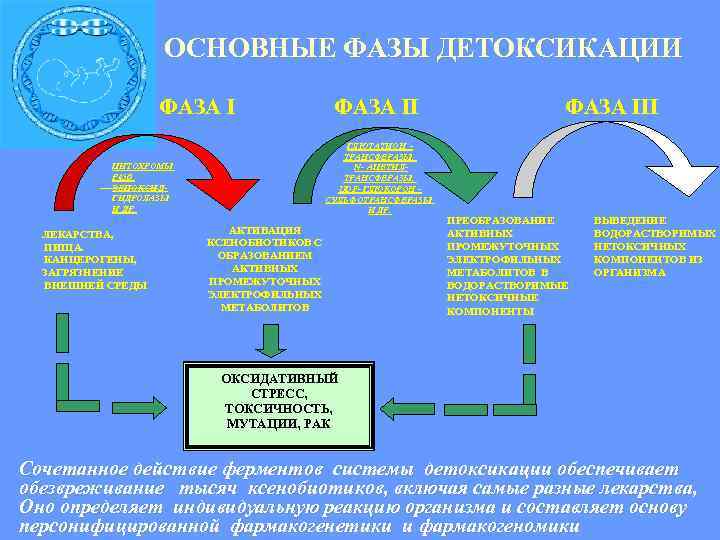
ОСНОВНЫЕ ФАЗЫ ДЕТОКСИКАЦИИ ФАЗА III ГЛЮТАТИОН - ТРАНСФЕРАЗЫ, ТРАНСФЕРАЗЫ ЦИТОХРОМЫ N- АЦЕТИЛ- АЦЕТИ P 450, P 450 ТРАНСФЕРАЗЫ, ТРАНСФЕРАЗЫ ЭЕПОКСИ Д- UDF- ГЛЮКОРОН - ГИДРОЛАЗЫ СУЛЬФОТРАНСФЕРАЗЫ И ДР. ДР ПРЕОБРАЗОВАНИЕ ВЫВЕДЕНИЕ ЛЕКАРСТВА, АКТИВАЦИЯ АКТИВНЫХ ВОДОРАСТВОРИМЫХ ПИЩА. КСЕНОБИОТИКОВ С ПРОМЕЖУТОЧНЫХ НЕТОКСИЧНЫХ КАНЦЕРОГЕНЫ, ОБРАЗОВАНИЕМ ЭЛЕКТРОФИЛЬНЫХ КОМПОНЕНТОВ ИЗ ЗАГРЯЗНЕНИЕ АКТИВНЫХ МЕТАБОЛИТОВ В ОРГАНИЗМА ВНЕШНЕЙ СРЕДЫ ПРОМЕЖУТОЧНЫХ ВОДОРАСТВОРИМЫЕ ЭЛЕКТРОФИЛЬНЫХ НЕТОКСИЧНЫЕ МЕТАБОЛИТОВ КОМПОНЕНТЫ ОКСИДАТИВНЫЙ СТРЕСС, ТОКСИЧНОСТЬ, МУТАЦИИ, РАК Сочетанное действие ферментов системы детоксикации обеспечивает обезвреживание тысяч ксенобиотиков, включая самые разные лекарства, Оно определяет индивидуальную реакцию организма и составляет основу персонифицированной фармакогенетики и фармакогеномики
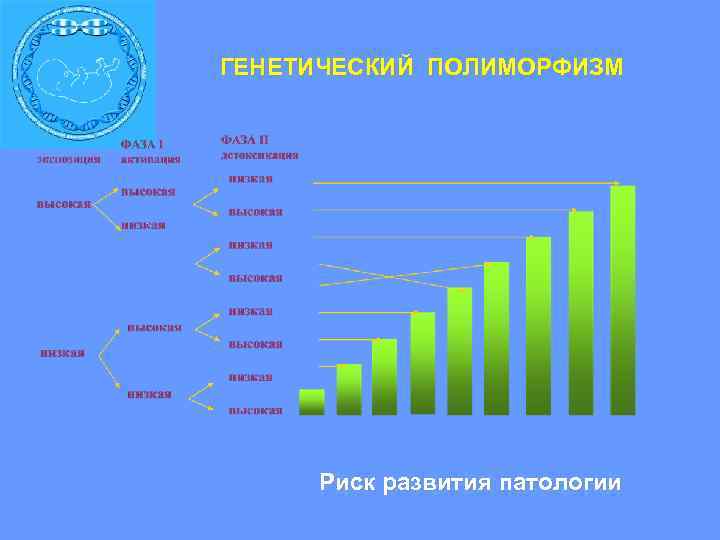
ГЕНЕТИЧЕСКИЙ ПОЛИМОРФИЗМ Риск развития патологии
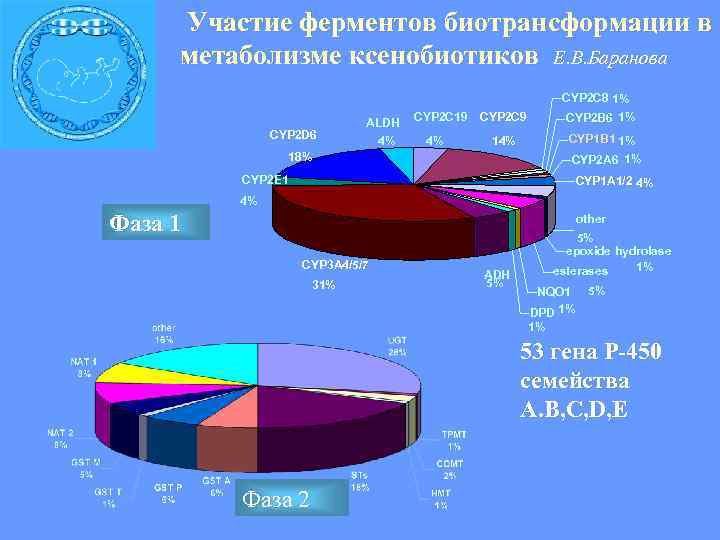
Участие ферментов биотрансформации в метаболизме ксенобиотиков Е. В. Баранова CYP 2 C 8 1% CYP 2 C 19 CYP 2 C 9 CYP 2 B 6 1% ALDH CYP 2 D 6 CYP 1 B 1 1% 4% 4% 14% 18% CYP 2 A 6 1% CYP 2 E 1 CYP 1 A 1/2 4% Фаза 1 5% other epoxide hydrolase CYP 3 A 4/5/7 1% ADH esterases 31% 5% NQO 1 5% DPD 1% 53 гена Р-450 семейства А. B, C, D, E Фаза 2

Основные химические реакции биотрансформации проканцерогенов с участием генов метаболизма Фаза II Образование (1 -3) или модификация Реакции (4 -8) функциональных групп коньюгирования 1. Гидроксилирование ароматического 1. Перенос ацетильных, кольца, алифатических цепей, метильных, аминов или амидов сульфгидрильных, 2. Эпоксидация ароматического кольца фосфорильных и или ненасыщенных олефинов глюкуронильных групп 3. S-, N- и Р-окисление 2. Конъюгация с 4. 0 -, N- и S-деалкилирование глютатионом 5. Гидролиз эфиров или амидов 6. Окислительное деаминирование 7. Редукция эпоксидов, гидроксил- аминов, нитрозосоединений. N- и S- оксидов 8. N- и С-трансоксигенирование

Индукция ферментов метаболизма 1. Фенобарбиталовый путь – активация промотора в регуляторной области гена Аутоиндукция – сам ксенобиотик активатор фермента 2. Рифампицин-дексаметазоновый тип – взаимодействие индуктора с рецепторами- регуляторами транскрипции 3. Этаноловый тип –стабилизация молекулы фермента метаболизма путем образования комплекса с некоторыми ксенобиотиками

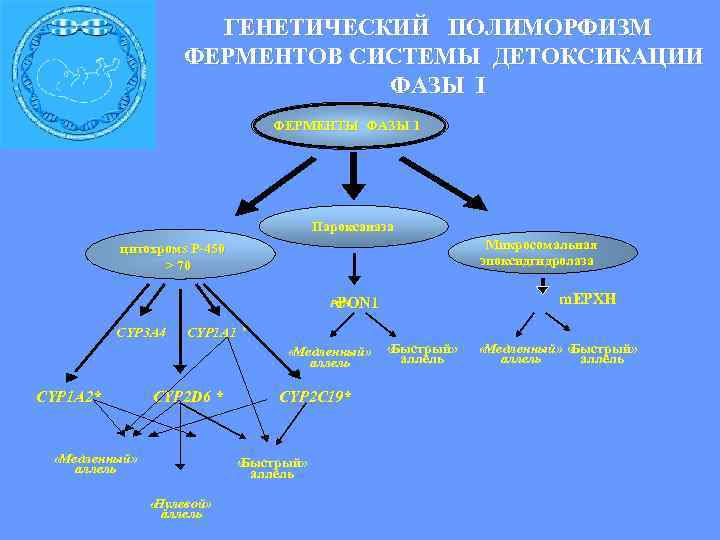
ГЕНЕТИЧЕСКИЙ ПОЛИМОРФИЗМ ФЕРМЕНТОВ CИСТЕМЫ ДЕТОКСИКАЦИИ ФАЗЫ I ФЕРМЕНТЫ ФАЗЫ 1 Пароксаназа цитохромs Р-450 Микросомальная > 70 эпоксидгидролаза PON 1 PON m. EPXH CYP 3 A 4 CYP 1 A 1 * «Медленный» «Быстрый» аллель аллель CYP 1 A 2* CYP 2 D 6 * CYP 2 C 19* «Медленный» «Быстрый» аллель «Нулевой» аллель
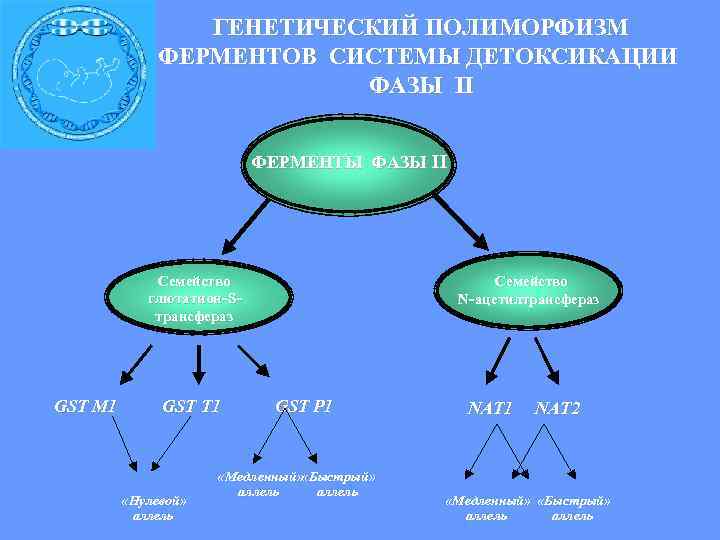
ГЕНЕТИЧЕСКИЙ ПОЛИМОРФИЗМ ФЕРМЕНТОВ СИСТЕМЫ ДЕТОКСИКАЦИИ ФАЗЫ II ФЕРМЕНТЫ ФАЗЫ II Семейство глютатион- S- N- ацетилтрансфераз трансфераз GST M 1 GST T 1 GST P 1 NAT 1 NAT 2 «Медленный» «Быстрый» аллель «Нулевой» «Медленный» «Быстрый» аллель аллель
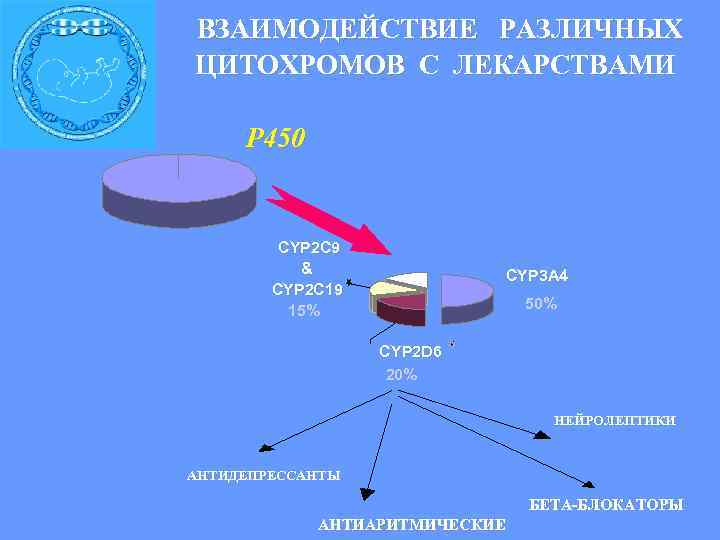
ВЗАИМОДЕЙСТВИЕ РАЗЛИЧНЫХ ЦИТОХРОМОВ С ЛЕКАРСТВАМИ P 450 CYP 2 C 9 & CYP 3 A 4 CYP 2 C 19 15% 50% CYP 2 D 6 20% НЕЙРОЛЕПТИКИ АНТИДЕПРЕССАНТЫ БЕТА-БЛОКАТОРЫ АНТИАРИТМИЧЕСКИЕ
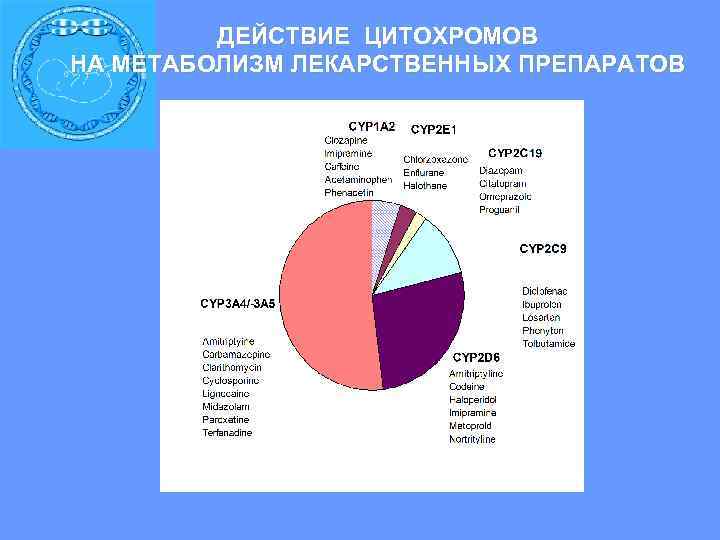
ДЕЙСТВИЕ ЦИТОХРОМОВ НА МЕТАБОЛИЗМ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ

Генетические механизмы индивидуальной чувствительности к лекарствам ФАРМАКОКИНЕТИЧЕСКИЕ: изменение абсорбции - инотиазид – NAT 2 превращение в активную форму кодеин –морфин –CYP 2 D 6 системные особенности метаболизма конкуренция препаратов за фермент индукция ферментов метаболизма индукция/ингибирование пищевыми продуктами ФРАМАКОДИНАМИЧЕСКИЕ: поступление /выведение препарата из клетки изменения в белках рецепторах
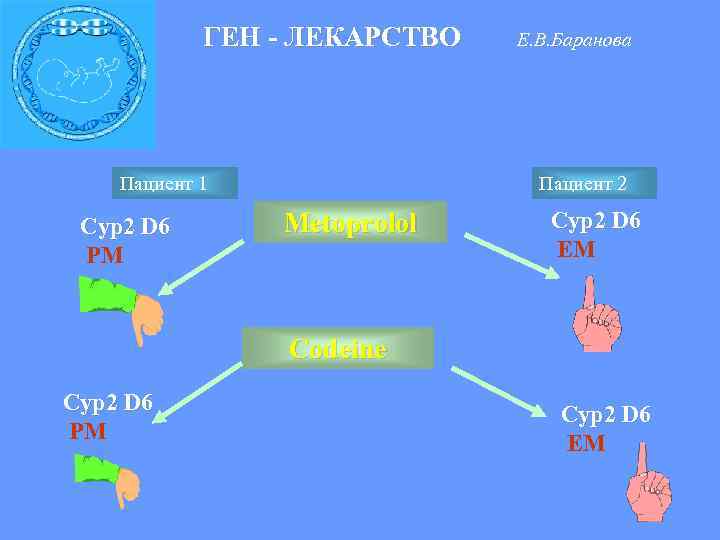
ГЕН - ЛЕКАРСТВО Е. В. Баранова Пациент 1 Пациент 2 Сyp 2 D 6 Metoprolol Сyp 2 D 6 PM EM Сodeine Сyp 2 D 6 Сyp 2 D 6 PM EM
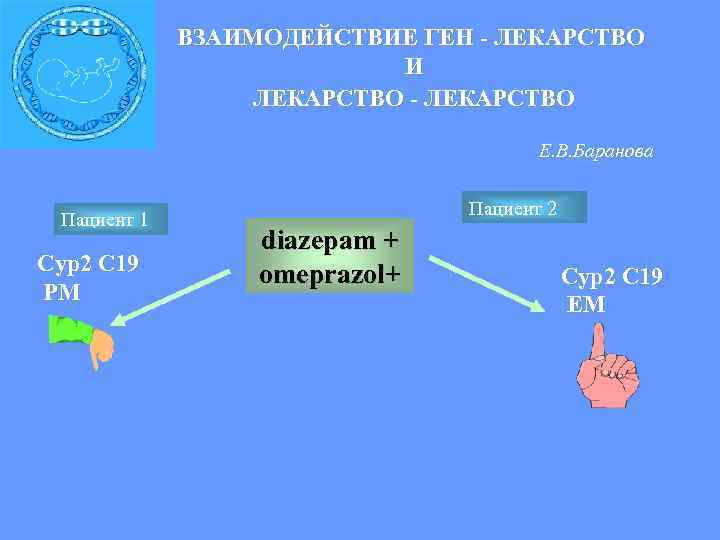
ВЗАИМОДЕЙСТВИЕ ГЕН - ЛЕКАРСТВО И ЛЕКАРСТВО - ЛЕКАРСТВО Е. В. Баранова Пациент 2 Пациент 1 diazepam + Сyp 2 С 19 omeprazol+ Сyp 2 С 19 PM EM
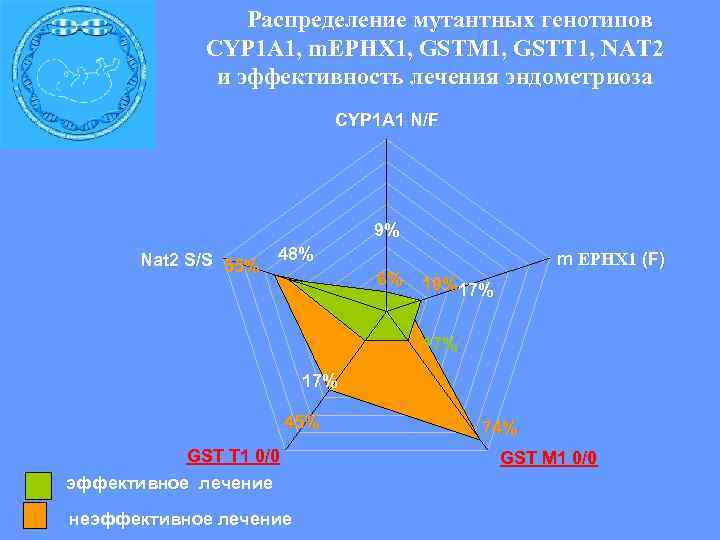
Распределение мутантных генотипов CYP 1 A 1, m. EPHX 1, GSTM 1, GSTT 1, NAT 2 и эффективность лечения эндометриоза CYP 1 A 1 N/F 9% Nat 2 S/S 55% 48% m EPHX 1 (F) 6% 10%17% 17% 45% 74% GST T 1 0/0 GST M 1 0/0 эффективное лечение неэффективное лечение

Частоты функционально неполноценных генотипов по генам фазы 2 детоксикации в разных группах больных эндометриозом неэффективное 27, 50% лечение 31, 40% 45, 10% GSTT 1 0/0, NAT 2 S/S эффективное 4, 30% лечение OR 8, 63(CI 95% 2, 17 -34, 229) 0 GSTM 10/0, GSTT 1 0/0 OR 10, 5 (CI 95% 1, 81 -60, 912) 8, 70% GSTM 1 0/0, NAT 2 S/S OR 8, 32 (CI 95% 1, 36 -51, 14).
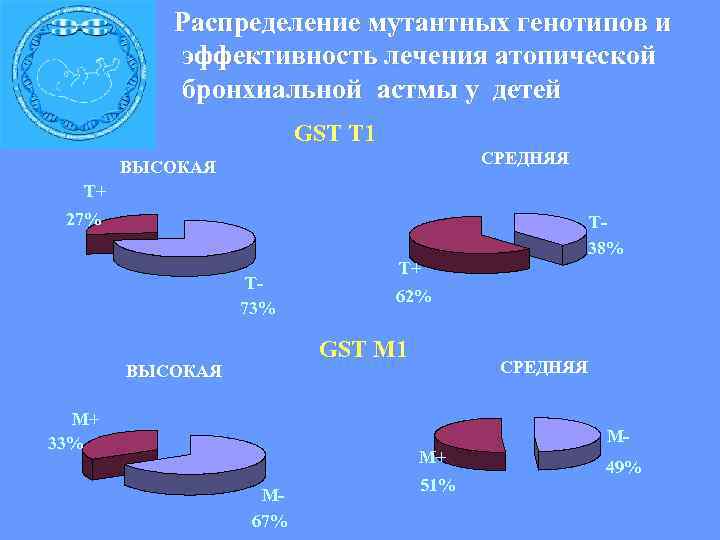
Распределение мутантных генотипов и эффективность лечения атопической бронхиальной астмы у детей GST T 1 СРЕДНЯЯ ВЫСОКАЯ Т+ 27% Т- 38% Т+ Т- 62% 73% GST M 1 ВЫСОКАЯ СРЕДНЯЯ М+ 33% М- М+ 49% 51% М- 67%
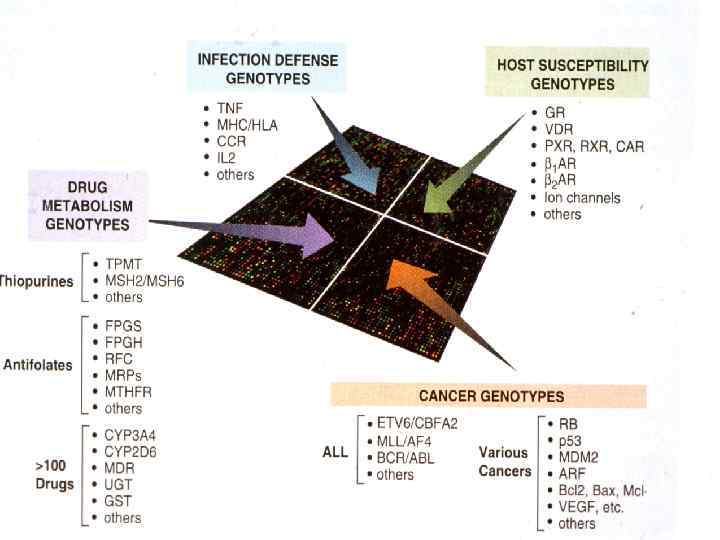

- Биочип - упорядоченная матрица ячеек, каждая из которых содержит молекулярный зонд (ДНК, РНК, белки, клетки) - Каждая ячейка биочипа – индивидуальная реакционная пробирка - Ячейки биочипа содержат ДНК-зонды, способные выявлять наличие определенной ДНК в образце, находить в ней фенотипически значимые мутации (наследственные заболевания, генетическую предрасположенность у человека, лекарственную устойчивость у бактерий и т. д. )

Центр биологических микрочипов ИМБ им. В. А. Энгельгардта РАН: На биочипе размещается несколько тысяч ячеек. Каждая гелевая ячейка содержит уникальную пробу. Диагностические биочипы содержат набор всех проб. 300 мкм гелевые ячейки
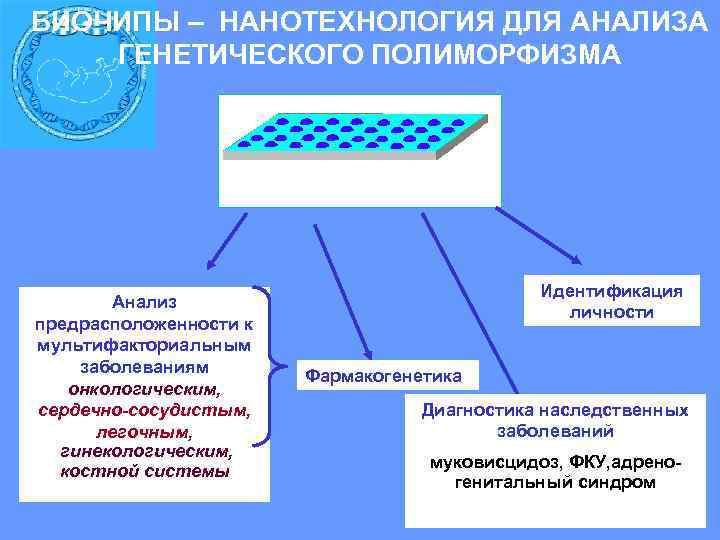
БИОЧИПЫ – НАНОТЕХНОЛОГИЯ ДЛЯ АНАЛИЗА ГЕНЕТИЧЕСКОГО ПОЛИМОРФИЗМА Идентификация Анализ личности предрасположенности к мультифакториальным заболеваниям Фармакогенетика онкологическим, сердечно-сосудистым, Диагностика наследственных легочным, заболеваний гинекологическим, костной системы муковисцидоз, ФКУ, адрено- генитальный синдром

Преимущества Биочиповой технологии: - возможность проведения множественного параллельного анализа биологических объектов (тысячи ячеек на 1 кв. см. ) - миниатюрность (удобство эксплуатации, экономия реактивов и т. д. ) - универсальность и дешевизна производства (одна производственная схема для различных микрочипов) - возможность использования в качестве иммобилизованных зондов фрагментов ДНК, РНК, белков (с сохранением ферментативных или антигенных свойств), а также живых клеток-биосенсоров

Производство биочипов Производство микрочипов путем сополимеризации Ячейки геля с light robot pin иммобили- Матрица с пробами зованными пробами Высокопроизводительный робот
Анализаторы изображения Результаты гибридизации регистрируются с помощью исследовательского (А) или портативного (Б) анализатора биочипов, соединенного с персональным компьютером А Б A Исследовательский Портативный анализатор
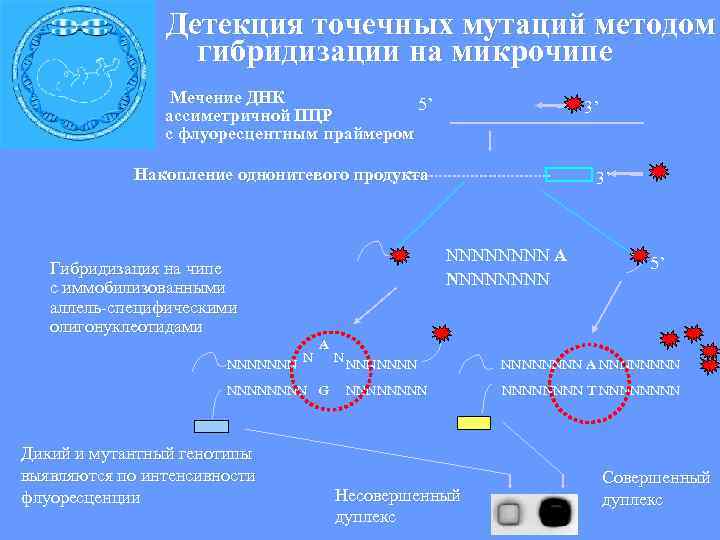
Детекция точечных мутаций методом гибридизации на микрочипе Мечение ДНК 5’ ассиметричной ПЦР 3’ с флуоресцентным праймером Накопление однонитевого продукта 3’ NNNN A 5’ Гибридизация на чипе с иммобилизованными NNNN аллель-специфическими олигонуклеотидами A NNNNNNN N N NNNNNNN A NNNN NNNN G NNNNNNNN T NNNN Дикий и мутантный генотипы выявляются по интенсивности Совершенный флуоресценции Несовершенный дуплекс
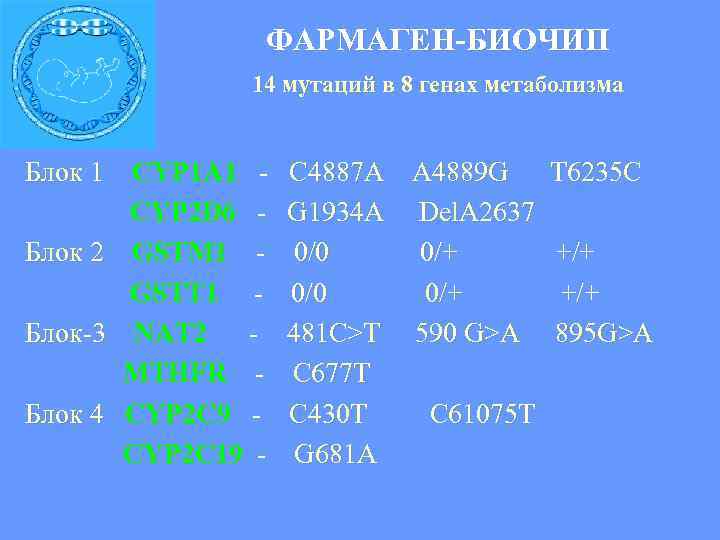
ФАРМАГЕН-БИОЧИП 14 мутаций в 8 генах метаболизма Блок 1 CYP 1 A 1 - C 4887 A A 4889 G T 6235 C CYP 2 D 6 - G 1934 A Del. A 2637 Блок 2 GSTM 1 - 0/0 0/+ +/+ GSTT 1 - 0/0 0/+ +/+ Блок-3 NAT 2 - 481 C>T 590 G>A 895 G>A MTHFR - C 677 T Блок 4 СYP 2 C 9 - C 430 T C 61075 T CYP 2 C 19 - G 681 A
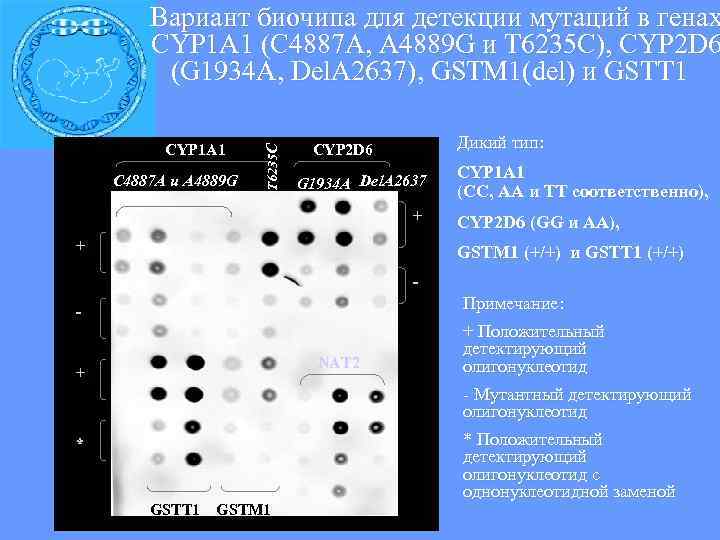
Вариант биочипа для детекции мутаций в генах CYP 1 A 1 (С 4887 А, A 4889 G и T 6235 C), CYP 2 D 6 (G 1934 A, Del. A 2637), GSTM 1(del) и GSTT 1 CYP 1 A 1 CYP 2 D 6 Дикий тип: T 6235 C С 4887 А и A 4889 G CYP 1 A 1 G 1934 A Del. A 2637 (СС, AA и TT соответственно), + CYP 2 D 6 (GG и AA), + GSTM 1 (+/+) и GSTT 1 (+/+) - - Примечание: + Положительный детектирующий NAT 2 олигонуклеотид + - Мутантный детектирующий олигонуклеотид * * Положительный детектирующий олигонуклеотид с однонуклеотидной заменой GSTT 1 GSTM 1

ТПМТ-БИОЧИП Структура и аллельные варианты гена ТРМТ. Ген Thiopurine S-methyltransferase (TPMT) локализован на хромосоме 6 p 22. 3 и состоит из 9 интронов и 10 экзонов. Белковый продукт гена TPMT инактивирует противоопухолевые препараты: меркаптопурин, азатиопурин, тиогуанин. 1 из 300 европейцев является гомозиготой по аллелю с очень низкой ферментной активностью по данному локусу. ~ 10 % индивидов - гетерозиготы по аллелю со средней белковой активностью. ~ 89% людей - гомозиготы по аллелю с высокой белковой активностью.

УЖЕ СУЩЕСТВУЮЩИЕ И РАЗРАБАТЫВАЕМЫЕ МИКРОЧИПЫ 1. Фармбиочип 2. Тромбочип 3. Кардиочип 4. ТМПТ-биочип 5. Остеопороз 6. Муковисцидоз 7. Бронхиальная 8. астма 9. 7. Ожирение 10. Онкология

ВЫВОДЫ 1. Чувствительность человека к экзогенным факторам в т. ч. к лекарственным препаратам определяется состоянием и функциональной активностью генов метаболизма 2. Основу индивидуальной чувствительности к лекарственным препаратам составляют особенности генетического полиморфизма 3. Выбор оптимальной индивидуальной дозировки лекарства должен производиться с учетом результатов тестирования соответствующих генов метаболизма 4. Технология биочипов существенно повышает эффективность популяционных и скринирующих программ по фармакогенетике и предиктивной медицине.
лек 6 фармакогенетика 23 09 08.ppt