bec24329cc0f672f15e3bbf6d95eea12.ppt
- Количество слайдов: 31
 Farma. Patent araştırma ve Danışmanlık http: //www. farmapatent. com. tr FARMASÖTİK BULUŞLARDA PATENT, RUHSATLANDIRMA VE HUKUKİ UYGULAMALAR SEMPOZYUMU 31 Mayıs – 1 Haziran 2012 Türkiye’de İlaç Patenti Uygulamaları Dr. Ecz. Pınar Bulut
Farma. Patent araştırma ve Danışmanlık http: //www. farmapatent. com. tr FARMASÖTİK BULUŞLARDA PATENT, RUHSATLANDIRMA VE HUKUKİ UYGULAMALAR SEMPOZYUMU 31 Mayıs – 1 Haziran 2012 Türkiye’de İlaç Patenti Uygulamaları Dr. Ecz. Pınar Bulut
 Marketing Approval Data Exclusivity Trademark İlaçlar Fikri Mülkiyet Koruması Patent Protection “Combined Use with Ritonavir Patent Protection (Molecule) Patent Protection (Treatment method) Patent Protection (Solvate) * Frank Daelemans Presentation Patent Protection (Composition) 2
Marketing Approval Data Exclusivity Trademark İlaçlar Fikri Mülkiyet Koruması Patent Protection “Combined Use with Ritonavir Patent Protection (Molecule) Patent Protection (Treatment method) Patent Protection (Solvate) * Frank Daelemans Presentation Patent Protection (Composition) 2
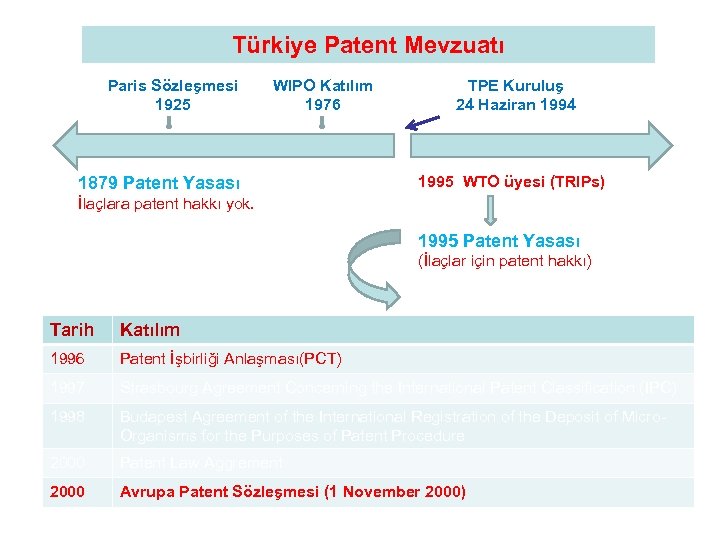 Türkiye Patent Mevzuatı Paris Sözleşmesi 1925 WIPO Katılım 1976 1879 Patent Yasası TPE Kuruluş 24 Haziran 1994 1995 WTO üyesi (TRIPs) İlaçlara patent hakkı yok. 1995 Patent Yasası (İlaçlar için patent hakkı) Tarih Katılım 1996 Patent İşbirliği Anlaşması(PCT) 1997 Strasbourg Agreement Concerning the International Patent Classification (IPC) 1998 Budapest Agreement of the International Registration of the Deposit of Micro. Organisms for the Purposes of Patent Procedure 2000 Patent Law Aggrement 2000 Avrupa Patent Sözleşmesi (1 November 2000)
Türkiye Patent Mevzuatı Paris Sözleşmesi 1925 WIPO Katılım 1976 1879 Patent Yasası TPE Kuruluş 24 Haziran 1994 1995 WTO üyesi (TRIPs) İlaçlara patent hakkı yok. 1995 Patent Yasası (İlaçlar için patent hakkı) Tarih Katılım 1996 Patent İşbirliği Anlaşması(PCT) 1997 Strasbourg Agreement Concerning the International Patent Classification (IPC) 1998 Budapest Agreement of the International Registration of the Deposit of Micro. Organisms for the Purposes of Patent Procedure 2000 Patent Law Aggrement 2000 Avrupa Patent Sözleşmesi (1 November 2000)
 UYGULAMALAR (TPE) Ürün patentleri , Proses Patentleri Bolar hakkı (ruhsat başvurusu istisnası) 551 KHK 75 -f- İlaçların ruhsatlandırılması ve bunun için gerekli test ve deneyler de dahil olmak üzere, ruhsat konusu buluşu içeren deneme amaçlı fiiller. İkinci endikasyon 551 KHK Md. 6 - Patent Verilemeyecek Konular ve Buluşlar e - İnsan veya hayvan vücuduna uygulanacak cerrahi ve tedavi usulleri ile … teşhis usulleri. (…. hüküm bu usullerin herhangi birinde kullanılan terkip ve maddeler ile bunların üretim usullerine uygulanmaz ) Zorunlu lisans Patentli buluşun kullanılmaması; Patentlerin ana konusunun bağımlılığı; Kamu yararı söz konusu olması. Ciprofloxacin (şarbon) Oseltamivir (kuş gribi) Anti-cancer drug Nexavar (sorafenib tosylate): Bayer refused Natco’s plea to grant voluntary license in December 2010. compulsory license (2012) …. . in India for just 3% of the patented drug's price in return for paying 6% royalty on sales to Bayer.
UYGULAMALAR (TPE) Ürün patentleri , Proses Patentleri Bolar hakkı (ruhsat başvurusu istisnası) 551 KHK 75 -f- İlaçların ruhsatlandırılması ve bunun için gerekli test ve deneyler de dahil olmak üzere, ruhsat konusu buluşu içeren deneme amaçlı fiiller. İkinci endikasyon 551 KHK Md. 6 - Patent Verilemeyecek Konular ve Buluşlar e - İnsan veya hayvan vücuduna uygulanacak cerrahi ve tedavi usulleri ile … teşhis usulleri. (…. hüküm bu usullerin herhangi birinde kullanılan terkip ve maddeler ile bunların üretim usullerine uygulanmaz ) Zorunlu lisans Patentli buluşun kullanılmaması; Patentlerin ana konusunun bağımlılığı; Kamu yararı söz konusu olması. Ciprofloxacin (şarbon) Oseltamivir (kuş gribi) Anti-cancer drug Nexavar (sorafenib tosylate): Bayer refused Natco’s plea to grant voluntary license in December 2010. compulsory license (2012) …. . in India for just 3% of the patented drug's price in return for paying 6% royalty on sales to Bayer.
 UYGULAMALAR (Sağlık Bakanlığı) Veri imtiyazı(6 yıl) > 1 Ocak 2005 (1 Ocak 2000’de kısmen) Jenerik ruhsat başvurularının orijinal firmalar tarafından öğrenilebilmesi • • ……Ruhsatlandırma Yönetmeliği …. . bilgilerin gizliliği kuralı; dosyadaki bilgi ve belgelerin başkalarının incelemesine açılmasının engellenmesi …. . ile sınırlı olup; anılan kural, ruhsat sahiplerinin, ruhsatlı ürünleri referans gösterilerek yapılan kısaltılmış ruhsat başvurularının varlığı hakkında bilgilendirilmelerine engel değildir. …. . davacıların ruhsatı referans gösterilerek kısaltılmış ruhsat başvurusu yapılıp yapılmadığı, yapılmış ise, bunların sayısı ve kimler tarafından yapıldığına ilişkin evrak kayıt bilgilerinin verilmesi …. . Patent – Ruhsat Bağlantısı ? ? ?
UYGULAMALAR (Sağlık Bakanlığı) Veri imtiyazı(6 yıl) > 1 Ocak 2005 (1 Ocak 2000’de kısmen) Jenerik ruhsat başvurularının orijinal firmalar tarafından öğrenilebilmesi • • ……Ruhsatlandırma Yönetmeliği …. . bilgilerin gizliliği kuralı; dosyadaki bilgi ve belgelerin başkalarının incelemesine açılmasının engellenmesi …. . ile sınırlı olup; anılan kural, ruhsat sahiplerinin, ruhsatlı ürünleri referans gösterilerek yapılan kısaltılmış ruhsat başvurularının varlığı hakkında bilgilendirilmelerine engel değildir. …. . davacıların ruhsatı referans gösterilerek kısaltılmış ruhsat başvurusu yapılıp yapılmadığı, yapılmış ise, bunların sayısı ve kimler tarafından yapıldığına ilişkin evrak kayıt bilgilerinin verilmesi …. . Patent – Ruhsat Bağlantısı ? ? ?
 UYGULANMAYANLAR ü Patent süresi uzatma (Supplementary Protection Certificate =SPC) Ruhsat alma tarihinden itibaren maksimum 15 yıl (ABD’de ruhsat alma tarihinden itibaren 14 yıl) Patent başvuru tarihinden itibaren 25 yılı aşamaz ü Pediatrik süre uzatımı (6 ay) (Paediatric Investigation Plan = PIP) ü Farmasötik formülasyonlar için faydalı model verilmiyor ü Tescil edilmiş patentler için TPE nezdinde hükümsüzlük veya patente tecavüz olmadığına dair inceleme talebi yapılamıyor ü TPE’de eczacı kökenli patent uzmanı bulunmuyor ü Türkiye ile AB arasında paralel ticaret yapılamıyor
UYGULANMAYANLAR ü Patent süresi uzatma (Supplementary Protection Certificate =SPC) Ruhsat alma tarihinden itibaren maksimum 15 yıl (ABD’de ruhsat alma tarihinden itibaren 14 yıl) Patent başvuru tarihinden itibaren 25 yılı aşamaz ü Pediatrik süre uzatımı (6 ay) (Paediatric Investigation Plan = PIP) ü Farmasötik formülasyonlar için faydalı model verilmiyor ü Tescil edilmiş patentler için TPE nezdinde hükümsüzlük veya patente tecavüz olmadığına dair inceleme talebi yapılamıyor ü TPE’de eczacı kökenli patent uzmanı bulunmuyor ü Türkiye ile AB arasında paralel ticaret yapılamıyor

 E) Fikri Mülkiyet Hakları (i) Veri münhasıriyeti 5: 1. Beşeri Tıbbi Ürünler Ruhsatlandırma Yönetmeliği’nde yer alan veri münhasıriyetine dair hükümlerin tam üyelik gerçekleşinceye kadar geçerliliğini sürdürmesi sağlanmalıdır. (ii) Ek Koruma Sertifikası: 1. “Ek koruma sertifikası uygulamasına tam üyelik gerçekleştikten sonra belirlenecek belirli bir süre içince geçilmelidir. 3. Ek koruma sertifikası hiçbir gerekçe ile geriye dönük olarak uygulanmamalıdır. ”
E) Fikri Mülkiyet Hakları (i) Veri münhasıriyeti 5: 1. Beşeri Tıbbi Ürünler Ruhsatlandırma Yönetmeliği’nde yer alan veri münhasıriyetine dair hükümlerin tam üyelik gerçekleşinceye kadar geçerliliğini sürdürmesi sağlanmalıdır. (ii) Ek Koruma Sertifikası: 1. “Ek koruma sertifikası uygulamasına tam üyelik gerçekleştikten sonra belirlenecek belirli bir süre içince geçilmelidir. 3. Ek koruma sertifikası hiçbir gerekçe ile geriye dönük olarak uygulanmamalıdır. ”
 E) Fikri Mülkiyet Hakları (iii) Paralel Ticaret: …. . yeni patent kanununda “patent ve faydalı modelde hakkın tüketilmesinin TC/AB gümrük alanı içinde “bölgesel tüketilmesi” ilkesi kabul edilmelidir. ” EK 8 FİKRİ SINAİ VE TİCARİ MÜLKİYETİN KORUNMASI Madde 10 (2) Taraflar arasındaki ticari ilişkilerde, fikri, sınai ve ticari mülkiyet haklarına, hakkın tüketilmesi ilkesinin uygulanması, bu karar ile öngörülmemiştir. Tasarı (17. 4. 2009 tarihli metin): Patentin Sağladığı Hakların Tüketilmesi Madde 20 - (1) Patent sahibi tarafından veya onun izni ile Türkiye’de satışa sunulmuş olan patentli ürünlerle ilgili fiiller, patentin sağladığı hakkın kapsamı dışında kalır.
E) Fikri Mülkiyet Hakları (iii) Paralel Ticaret: …. . yeni patent kanununda “patent ve faydalı modelde hakkın tüketilmesinin TC/AB gümrük alanı içinde “bölgesel tüketilmesi” ilkesi kabul edilmelidir. ” EK 8 FİKRİ SINAİ VE TİCARİ MÜLKİYETİN KORUNMASI Madde 10 (2) Taraflar arasındaki ticari ilişkilerde, fikri, sınai ve ticari mülkiyet haklarına, hakkın tüketilmesi ilkesinin uygulanması, bu karar ile öngörülmemiştir. Tasarı (17. 4. 2009 tarihli metin): Patentin Sağladığı Hakların Tüketilmesi Madde 20 - (1) Patent sahibi tarafından veya onun izni ile Türkiye’de satışa sunulmuş olan patentli ürünlerle ilgili fiiller, patentin sağladığı hakkın kapsamı dışında kalır.
 E) Fikri Mülkiyet Hakları (iv) Zorunlu Lisans: …. “Az gelişmiş ülkelere ve ilaç üretim kapasitesi olmayan veya yeterli olmayan ülkelere ihracat şartı ile patentli ilaç ve ilaç hammaddelerine talep üzerine zorunlu lisans verilir” Tasarı (17. 4. 2009 tarihli metin): Kamu sağlığı sorunları nedeniyle eczacılık ürünlerinin uygun ülkelere ihracatı durumunda zorunlu lisans MADDE 74 -(1) Eczacılık ürünlerini, bu alanda üretim kapasitesi olmayan veya yetersiz olan ülkelere kamu sağlığı sorunları nedeniyle ihraç etmek isteyenler, Yönetmeliğe uygun olarak zorunlu lisans verilmesini talep edebilir.
E) Fikri Mülkiyet Hakları (iv) Zorunlu Lisans: …. “Az gelişmiş ülkelere ve ilaç üretim kapasitesi olmayan veya yeterli olmayan ülkelere ihracat şartı ile patentli ilaç ve ilaç hammaddelerine talep üzerine zorunlu lisans verilir” Tasarı (17. 4. 2009 tarihli metin): Kamu sağlığı sorunları nedeniyle eczacılık ürünlerinin uygun ülkelere ihracatı durumunda zorunlu lisans MADDE 74 -(1) Eczacılık ürünlerini, bu alanda üretim kapasitesi olmayan veya yetersiz olan ülkelere kamu sağlığı sorunları nedeniyle ihraç etmek isteyenler, Yönetmeliğe uygun olarak zorunlu lisans verilmesini talep edebilir.
 CAUTION ! For most Generic Drug Developments, Molecule Patent expiry dates are the ‘Tip of the Iceberg’ (Leighton Howard – (CEO of Genericweb) ICSE 2005 , Madrid)
CAUTION ! For most Generic Drug Developments, Molecule Patent expiry dates are the ‘Tip of the Iceberg’ (Leighton Howard – (CEO of Genericweb) ICSE 2005 , Madrid)
 Ø Molekül, tek endikasyon, doz rejimi patentleri Ø Jenerik rekabet mümkün değildir Ø Patentin etrafından dolaşmak mümkün olmaz Ø ihtiyati tedbir zorunlu Ø Tuzlar, Hidratlar, Polimorflar vb…. Ø Jenerik rekabet mümkün Ø R&D ile patentin etrafından dolaşılabilir Ø Çeşitli formülasyon, proses patentleri Ø Jenerik rekabet mümkün Ø Patentin etrafından kolayca dolaşılabilir From Webinar of Leighton Howard
Ø Molekül, tek endikasyon, doz rejimi patentleri Ø Jenerik rekabet mümkün değildir Ø Patentin etrafından dolaşmak mümkün olmaz Ø ihtiyati tedbir zorunlu Ø Tuzlar, Hidratlar, Polimorflar vb…. Ø Jenerik rekabet mümkün Ø R&D ile patentin etrafından dolaşılabilir Ø Çeşitli formülasyon, proses patentleri Ø Jenerik rekabet mümkün Ø Patentin etrafından kolayca dolaşılabilir From Webinar of Leighton Howard
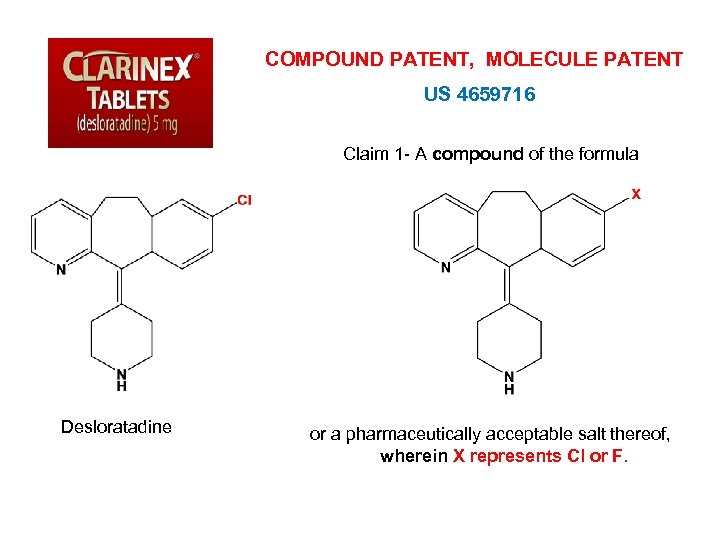 COMPOUND PATENT, MOLECULE PATENT US 4659716 Claim 1 - A compound of the formula Desloratadine or a pharmaceutically acceptable salt thereof, wherein X represents Cl or F.
COMPOUND PATENT, MOLECULE PATENT US 4659716 Claim 1 - A compound of the formula Desloratadine or a pharmaceutically acceptable salt thereof, wherein X represents Cl or F.
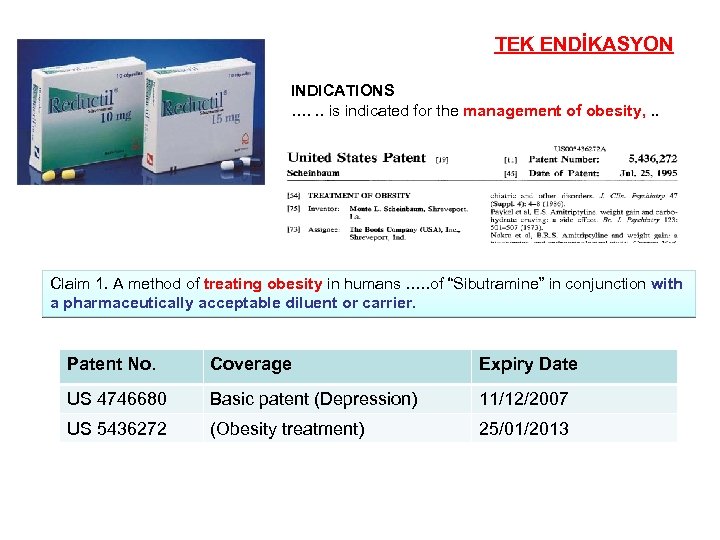 TEK ENDİKASYON INDICATIONS …. . . is indicated for the management of obesity, . . Claim 1. A method of treating obesity in humans …. . of “Sibutramine” in conjunction with a pharmaceutically acceptable diluent or carrier. Patent No. Coverage Expiry Date US 4746680 Basic patent (Depression) 11/12/2007 US 5436272 (Obesity treatment) 25/01/2013
TEK ENDİKASYON INDICATIONS …. . . is indicated for the management of obesity, . . Claim 1. A method of treating obesity in humans …. . of “Sibutramine” in conjunction with a pharmaceutically acceptable diluent or carrier. Patent No. Coverage Expiry Date US 4746680 Basic patent (Depression) 11/12/2007 US 5436272 (Obesity treatment) 25/01/2013
 NOVEL DOSE REGIMEN Posology: Ø c. SSTI without concurrent Staphylococcus aureus bacteraemia: Cubicin 4 mg/kg is administered once every 24 hours for 7 -14 days or until the infection is resolved. . TR 2001/ 00841 B (CUBIST) METHODS FOR ADMINISTRATION OF ANTIBIOTICS WO 2000/018419 EP 1115417 B 1 US 6468967 Claim 1. Use of a daptomycin for the manufacture of a medicament for treating a bacterial infection in a human patient in need of, wherein a dose for said treating is 3 to 75 mg/kg of daptomycin, wherein said dose is repeatedly administered in a dosage interval of once every 24 hours to once weekly. Problem: ……prolonged treatment with 3 mg/kg daptomycin every 12 hours was shown to cause occasional adverse effects (Baltz, supra). Transient muscular weakness and pain were observed in two of five human patients……
NOVEL DOSE REGIMEN Posology: Ø c. SSTI without concurrent Staphylococcus aureus bacteraemia: Cubicin 4 mg/kg is administered once every 24 hours for 7 -14 days or until the infection is resolved. . TR 2001/ 00841 B (CUBIST) METHODS FOR ADMINISTRATION OF ANTIBIOTICS WO 2000/018419 EP 1115417 B 1 US 6468967 Claim 1. Use of a daptomycin for the manufacture of a medicament for treating a bacterial infection in a human patient in need of, wherein a dose for said treating is 3 to 75 mg/kg of daptomycin, wherein said dose is repeatedly administered in a dosage interval of once every 24 hours to once weekly. Problem: ……prolonged treatment with 3 mg/kg daptomycin every 12 hours was shown to cause occasional adverse effects (Baltz, supra). Transient muscular weakness and pain were observed in two of five human patients……
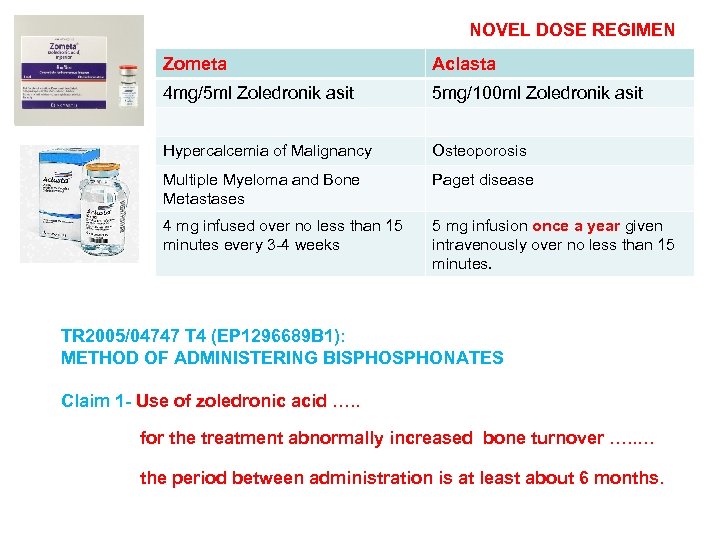 NOVEL DOSE REGIMEN Zometa Aclasta 4 mg/5 ml Zoledronik asit 5 mg/100 ml Zoledronik asit Hypercalcemia of Malignancy Osteoporosis Multiple Myeloma and Bone Metastases Paget disease 4 mg infused over no less than 15 minutes every 3 -4 weeks 5 mg infusion once a year given intravenously over no less than 15 minutes. TR 2005/04747 T 4 (EP 1296689 B 1): METHOD OF ADMINISTERING BISPHONATES Claim 1 - Use of zoledronic acid …. . for the treatment abnormally increased bone turnover …. . … the period between administration is at least about 6 months.
NOVEL DOSE REGIMEN Zometa Aclasta 4 mg/5 ml Zoledronik asit 5 mg/100 ml Zoledronik asit Hypercalcemia of Malignancy Osteoporosis Multiple Myeloma and Bone Metastases Paget disease 4 mg infused over no less than 15 minutes every 3 -4 weeks 5 mg infusion once a year given intravenously over no less than 15 minutes. TR 2005/04747 T 4 (EP 1296689 B 1): METHOD OF ADMINISTERING BISPHONATES Claim 1 - Use of zoledronic acid …. . for the treatment abnormally increased bone turnover …. . … the period between administration is at least about 6 months.
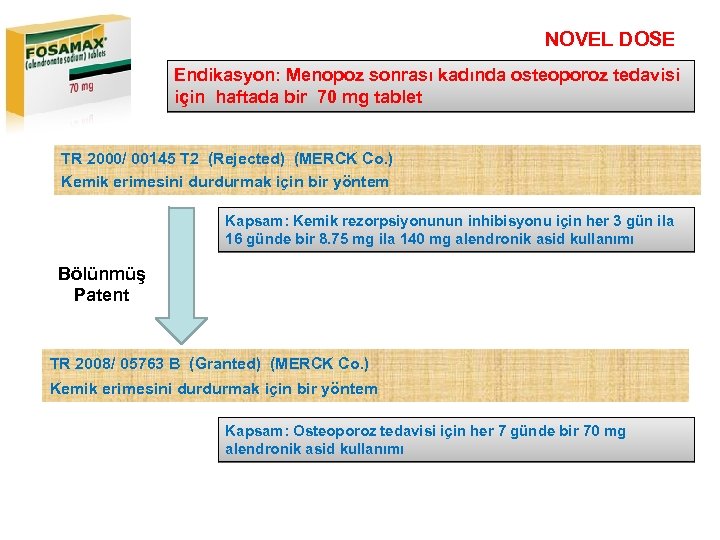 NOVEL DOSE Endikasyon: Menopoz sonrası kadında osteoporoz tedavisi için haftada bir 70 mg tablet TR 2000/ 00145 T 2 (Rejected) (MERCK Co. ) Kemik erimesini durdurmak için bir yöntem Kapsam: Kemik rezorpsiyonunun inhibisyonu için her 3 gün ila 16 günde bir 8. 75 mg ila 140 mg alendronik asid kullanımı Bölünmüş Patent TR 2008/ 05763 B (Granted) (MERCK Co. ) Kemik erimesini durdurmak için bir yöntem Kapsam: Osteoporoz tedavisi için her 7 günde bir 70 mg alendronik asid kullanımı
NOVEL DOSE Endikasyon: Menopoz sonrası kadında osteoporoz tedavisi için haftada bir 70 mg tablet TR 2000/ 00145 T 2 (Rejected) (MERCK Co. ) Kemik erimesini durdurmak için bir yöntem Kapsam: Kemik rezorpsiyonunun inhibisyonu için her 3 gün ila 16 günde bir 8. 75 mg ila 140 mg alendronik asid kullanımı Bölünmüş Patent TR 2008/ 05763 B (Granted) (MERCK Co. ) Kemik erimesini durdurmak için bir yöntem Kapsam: Osteoporoz tedavisi için her 7 günde bir 70 mg alendronik asid kullanımı
 Ø Tuzlar, Hidratlar, Polimorflar vb…. Ø Jenerik rekabet mümkün Ø R&D ile patentin etrafından dolaşılabilir Ø Legal yol (patent invalidation)
Ø Tuzlar, Hidratlar, Polimorflar vb…. Ø Jenerik rekabet mümkün Ø R&D ile patentin etrafından dolaşılabilir Ø Legal yol (patent invalidation)
 NOVEL SALT TR 2004/ 01793 T 4 (SERVIER= EP 1354873 B 1) Salt of perindopril and pharmaceutical compositions containing it (Expiry Date: 17 February 2023) Coversyl Tablet Coversyl Arginine. Tablet Perindopril t-butylamine 8 mg Perindopril Arginine 10 mg Launch Date 31/01/1990 (2, 4 mg) 31/12/2002 (8 mg) 31/03/2008 (2. 5, 5, 10 mg)
NOVEL SALT TR 2004/ 01793 T 4 (SERVIER= EP 1354873 B 1) Salt of perindopril and pharmaceutical compositions containing it (Expiry Date: 17 February 2023) Coversyl Tablet Coversyl Arginine. Tablet Perindopril t-butylamine 8 mg Perindopril Arginine 10 mg Launch Date 31/01/1990 (2, 4 mg) 31/12/2002 (8 mg) 31/03/2008 (2. 5, 5, 10 mg)
 NOVEL HYDRATE, SOLVATE TR 2004 / 02579 T 4 (B INGELHEIM EP 1326862 B 1) CRYSTALLINE MONOHYDRATE OF TIOTROPIUM BROMIDE, METHOD FOR PRODUCING THE SAME …. US 6777423 WO 0230928 SPIRIVA® Each capsule contains 22. 5 microgram tiotropium bromide monohydrate equivalent to 18 microgram tiotropium. üThe absorption of moisture …. . üUniform distribution of the medicament…. . üSince breakdown …. as a side effect of the grinding (or micronizing)……. üSurprisingly, it has been found that the monohydrate of tiotropium bromide, which can be obtained in crystalline form …. , meets the stringent requirements mentioned above and thus solves the problem on which the present invention is based.
NOVEL HYDRATE, SOLVATE TR 2004 / 02579 T 4 (B INGELHEIM EP 1326862 B 1) CRYSTALLINE MONOHYDRATE OF TIOTROPIUM BROMIDE, METHOD FOR PRODUCING THE SAME …. US 6777423 WO 0230928 SPIRIVA® Each capsule contains 22. 5 microgram tiotropium bromide monohydrate equivalent to 18 microgram tiotropium. üThe absorption of moisture …. . üUniform distribution of the medicament…. . üSince breakdown …. as a side effect of the grinding (or micronizing)……. üSurprisingly, it has been found that the monohydrate of tiotropium bromide, which can be obtained in crystalline form …. , meets the stringent requirements mentioned above and thus solves the problem on which the present invention is based.
 POLİMORFLAR Ranitidin hidroklorür (Form 1) …. . ranitidine hydrochloride can be prepared in a new crystalline form …. . designated Form 2 …… have larger crystals than the hitherto known Form 1 and exhibits more favourable filtration and drying characteristics. Furthermore, Form 2 is less hygroscopic than Form 1, …. .
POLİMORFLAR Ranitidin hidroklorür (Form 1) …. . ranitidine hydrochloride can be prepared in a new crystalline form …. . designated Form 2 …… have larger crystals than the hitherto known Form 1 and exhibits more favourable filtration and drying characteristics. Furthermore, Form 2 is less hygroscopic than Form 1, …. .
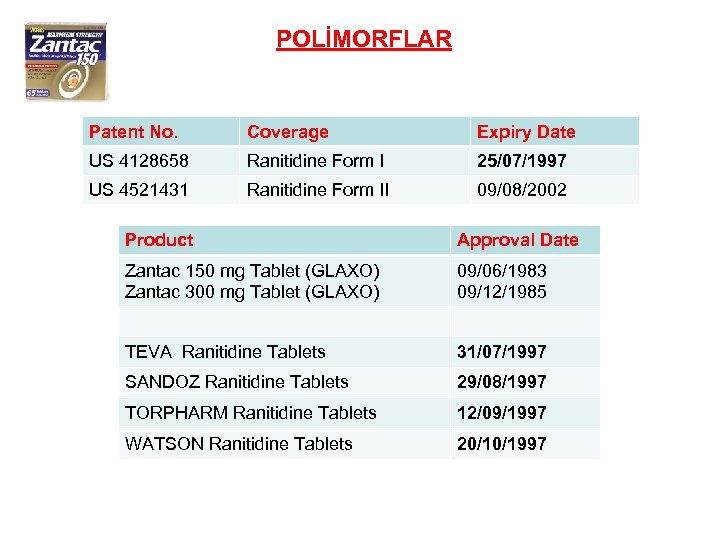 POLİMORFLAR Patent No. Coverage Expiry Date US 4128658 Ranitidine Form I 25/07/1997 US 4521431 Ranitidine Form II 09/08/2002 Product Approval Date Zantac 150 mg Tablet (GLAXO) Zantac 300 mg Tablet (GLAXO) 09/06/1983 09/12/1985 TEVA Ranitidine Tablets 31/07/1997 SANDOZ Ranitidine Tablets 29/08/1997 TORPHARM Ranitidine Tablets 12/09/1997 WATSON Ranitidine Tablets 20/10/1997
POLİMORFLAR Patent No. Coverage Expiry Date US 4128658 Ranitidine Form I 25/07/1997 US 4521431 Ranitidine Form II 09/08/2002 Product Approval Date Zantac 150 mg Tablet (GLAXO) Zantac 300 mg Tablet (GLAXO) 09/06/1983 09/12/1985 TEVA Ranitidine Tablets 31/07/1997 SANDOZ Ranitidine Tablets 29/08/1997 TORPHARM Ranitidine Tablets 12/09/1997 WATSON Ranitidine Tablets 20/10/1997
 Ø Çeşitli formülasyon, proses patentleri Ø Jenerik rekabet mümkün Ø Patentin etrafından kolayca dolaşılabilir
Ø Çeşitli formülasyon, proses patentleri Ø Jenerik rekabet mümkün Ø Patentin etrafından kolayca dolaşılabilir
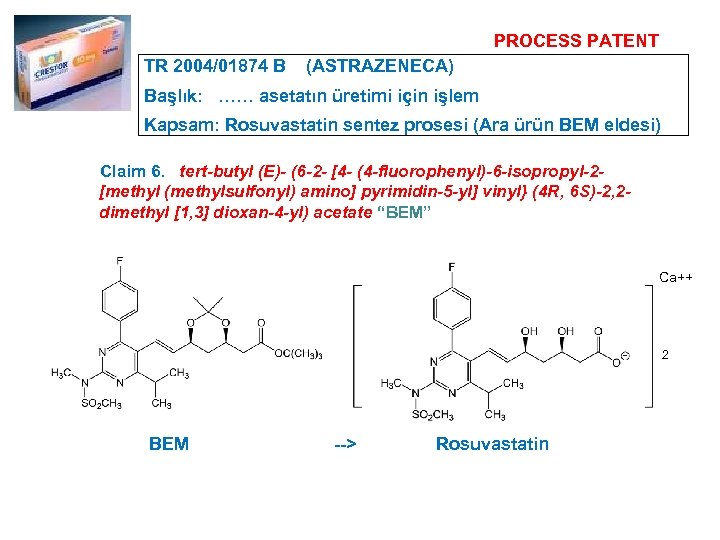 PROCESS PATENT TR 2004/01874 B (ASTRAZENECA) Başlık: …… asetatın üretimi için işlem Kapsam: Rosuvastatin sentez prosesi (Ara ürün BEM eldesi) Claim 6. tert-butyl (E)- (6 -2 - [4 - (4 -fluorophenyl)-6 -isopropyl-2 - [methyl (methylsulfonyl) amino] pyrimidin-5 -yl] vinyl} (4 R, 6 S)-2, 2 dimethyl [1, 3] dioxan-4 -yl) acetate “BEM” Ca++ 2 BEM --> Rosuvastatin
PROCESS PATENT TR 2004/01874 B (ASTRAZENECA) Başlık: …… asetatın üretimi için işlem Kapsam: Rosuvastatin sentez prosesi (Ara ürün BEM eldesi) Claim 6. tert-butyl (E)- (6 -2 - [4 - (4 -fluorophenyl)-6 -isopropyl-2 - [methyl (methylsulfonyl) amino] pyrimidin-5 -yl] vinyl} (4 R, 6 S)-2, 2 dimethyl [1, 3] dioxan-4 -yl) acetate “BEM” Ca++ 2 BEM --> Rosuvastatin
 NOVEL INDICATION TR 2008/ 06194 T 4 (UCB FARCHIM = EP 1569650 B 1) USE OF LEVOCETIRIZINE FOR THE TREATMENT OF PERSISTENT ALLERGIC RHINITIS CLAIM 1. Use of levocetirizine …for treating persistent allergic rhinitis or for decreasing the symptoms of persistent allergic rhinitis …. Xyzal Tablet Generic Tablet Symptomatic treatment of allergic rhinitis (including persistent allergic rhinitis) and chronic idiopathic urticaria. • Seasonal allergic rhinitis • Perennial allergic rhinitis • Chronic idiopathic urticaria
NOVEL INDICATION TR 2008/ 06194 T 4 (UCB FARCHIM = EP 1569650 B 1) USE OF LEVOCETIRIZINE FOR THE TREATMENT OF PERSISTENT ALLERGIC RHINITIS CLAIM 1. Use of levocetirizine …for treating persistent allergic rhinitis or for decreasing the symptoms of persistent allergic rhinitis …. Xyzal Tablet Generic Tablet Symptomatic treatment of allergic rhinitis (including persistent allergic rhinitis) and chronic idiopathic urticaria. • Seasonal allergic rhinitis • Perennial allergic rhinitis • Chronic idiopathic urticaria
 NOVEL PATIENT GROUP TR 2000/ 02837 B (ABBOTT / ORION) USE OF DEXMEDETOMIDINE FOR INTENSIVE CARE UNIT SEDATION WO 1999/049854 US 6716867 EP 1069893 Claim 1. Use of dexmedetomidine …. . for use in sedating a critically ill patient who is given intensive care, wherein the patient remains arousable and orientated Øgroup must be distinguishable with respect to physiological or pathological status, Ømay not overlap with previously treated group, Ømay not be selected arbitrarily
NOVEL PATIENT GROUP TR 2000/ 02837 B (ABBOTT / ORION) USE OF DEXMEDETOMIDINE FOR INTENSIVE CARE UNIT SEDATION WO 1999/049854 US 6716867 EP 1069893 Claim 1. Use of dexmedetomidine …. . for use in sedating a critically ill patient who is given intensive care, wherein the patient remains arousable and orientated Øgroup must be distinguishable with respect to physiological or pathological status, Ømay not overlap with previously treated group, Ømay not be selected arbitrarily
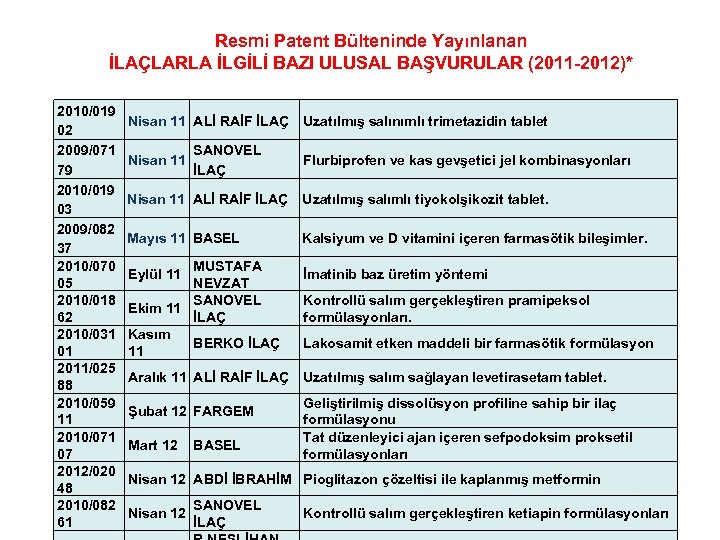 Resmi Patent Bülteninde Yayınlanan İLAÇLARLA İLGİLİ BAZI ULUSAL BAŞVURULAR (2011 -2012)* 2010/019 02 2009/071 79 2010/019 03 2009/082 37 2010/070 05 2010/018 62 2010/031 01 2011/025 88 2010/059 11 2010/071 07 2012/020 48 2010/082 61 Nisan 11 ALİ RAİF İLAÇ Uzatılmış salınımlı trimetazidin tablet Nisan 11 SANOVEL İLAÇ Flurbiprofen ve kas gevşetici jel kombinasyonları Nisan 11 ALİ RAİF İLAÇ Uzatılmış salımlı tiyokolşikozit tablet. Mayıs 11 BASEL MUSTAFA NEVZAT SANOVEL Ekim 11 İLAÇ Kasım BERKO İLAÇ 11 Eylül 11 Kalsiyum ve D vitamini içeren farmasötik bileşimler. İmatinib baz üretim yöntemi Kontrollü salım gerçekleştiren pramipeksol formülasyonları. Lakosamit etken maddeli bir farmasötik formülasyon Aralık 11 ALİ RAİF İLAÇ Uzatılmış salım sağlayan levetirasetam tablet. Şubat 12 FARGEM Mart 12 BASEL Geliştirilmiş dissolüsyon profiline sahip bir ilaç formülasyonu Tat düzenleyici ajan içeren sefpodoksim proksetil formülasyonları * www. farmapatent. com. tr Nisan 12 ABDİ İBRAHİM Pioglitazon çözeltisi ile kaplanmış metformin Nisan 12 SANOVEL İLAÇ Kontrollü salım gerçekleştiren ketiapin formülasyonları
Resmi Patent Bülteninde Yayınlanan İLAÇLARLA İLGİLİ BAZI ULUSAL BAŞVURULAR (2011 -2012)* 2010/019 02 2009/071 79 2010/019 03 2009/082 37 2010/070 05 2010/018 62 2010/031 01 2011/025 88 2010/059 11 2010/071 07 2012/020 48 2010/082 61 Nisan 11 ALİ RAİF İLAÇ Uzatılmış salınımlı trimetazidin tablet Nisan 11 SANOVEL İLAÇ Flurbiprofen ve kas gevşetici jel kombinasyonları Nisan 11 ALİ RAİF İLAÇ Uzatılmış salımlı tiyokolşikozit tablet. Mayıs 11 BASEL MUSTAFA NEVZAT SANOVEL Ekim 11 İLAÇ Kasım BERKO İLAÇ 11 Eylül 11 Kalsiyum ve D vitamini içeren farmasötik bileşimler. İmatinib baz üretim yöntemi Kontrollü salım gerçekleştiren pramipeksol formülasyonları. Lakosamit etken maddeli bir farmasötik formülasyon Aralık 11 ALİ RAİF İLAÇ Uzatılmış salım sağlayan levetirasetam tablet. Şubat 12 FARGEM Mart 12 BASEL Geliştirilmiş dissolüsyon profiline sahip bir ilaç formülasyonu Tat düzenleyici ajan içeren sefpodoksim proksetil formülasyonları * www. farmapatent. com. tr Nisan 12 ABDİ İBRAHİM Pioglitazon çözeltisi ile kaplanmış metformin Nisan 12 SANOVEL İLAÇ Kontrollü salım gerçekleştiren ketiapin formülasyonları
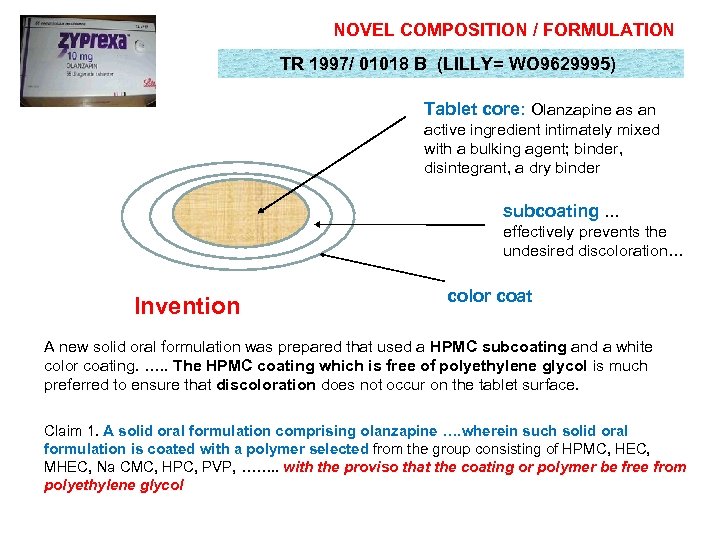 NOVEL COMPOSITION / FORMULATION TR 1997/ 01018 B (LILLY= WO 9629995) Tablet core: Olanzapine as an active ingredient intimately mixed with a bulking agent; binder, disintegrant, a dry binder subcoating … effectively prevents the undesired discoloration… Invention color coat A new solid oral formulation was prepared that used a HPMC subcoating and a white color coating. …. . The HPMC coating which is free of polyethylene glycol is much preferred to ensure that discoloration does not occur on the tablet surface. Claim 1. A solid oral formulation comprising olanzapine …. wherein such solid oral formulation is coated with a polymer selected from the group consisting of HPMC, HEC, MHEC, Na CMC, HPC, PVP, ……. . with the proviso that the coating or polymer be free from polyethylene glycol
NOVEL COMPOSITION / FORMULATION TR 1997/ 01018 B (LILLY= WO 9629995) Tablet core: Olanzapine as an active ingredient intimately mixed with a bulking agent; binder, disintegrant, a dry binder subcoating … effectively prevents the undesired discoloration… Invention color coat A new solid oral formulation was prepared that used a HPMC subcoating and a white color coating. …. . The HPMC coating which is free of polyethylene glycol is much preferred to ensure that discoloration does not occur on the tablet surface. Claim 1. A solid oral formulation comprising olanzapine …. wherein such solid oral formulation is coated with a polymer selected from the group consisting of HPMC, HEC, MHEC, Na CMC, HPC, PVP, ……. . with the proviso that the coating or polymer be free from polyethylene glycol
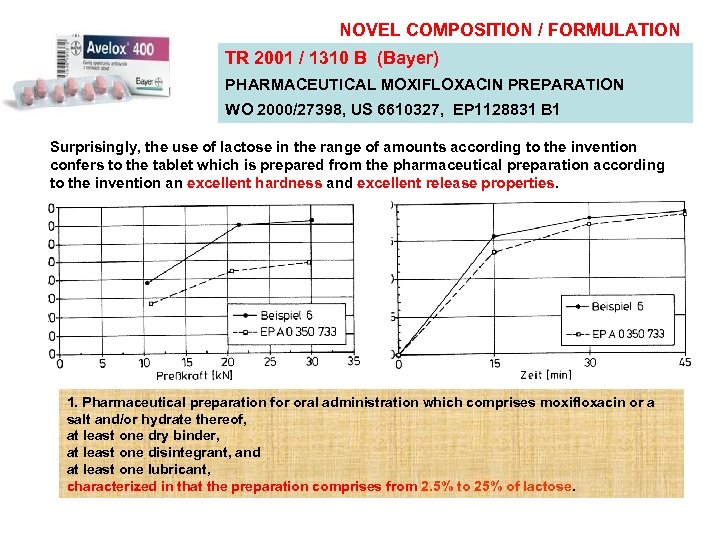 NOVEL COMPOSITION / FORMULATION TR 2001 / 1310 B (Bayer) PHARMACEUTICAL MOXIFLOXACIN PREPARATION WO 2000/27398, US 6610327, EP 1128831 B 1 Surprisingly, the use of lactose in the range of amounts according to the invention confers to the tablet which is prepared from the pharmaceutical preparation according to the invention an excellent hardness and excellent release properties. 1. Pharmaceutical preparation for oral administration which comprises moxifloxacin or a salt and/or hydrate thereof, at least one dry binder, at least one disintegrant, and at least one lubricant, characterized in that the preparation comprises from 2. 5% to 25% of lactose.
NOVEL COMPOSITION / FORMULATION TR 2001 / 1310 B (Bayer) PHARMACEUTICAL MOXIFLOXACIN PREPARATION WO 2000/27398, US 6610327, EP 1128831 B 1 Surprisingly, the use of lactose in the range of amounts according to the invention confers to the tablet which is prepared from the pharmaceutical preparation according to the invention an excellent hardness and excellent release properties. 1. Pharmaceutical preparation for oral administration which comprises moxifloxacin or a salt and/or hydrate thereof, at least one dry binder, at least one disintegrant, and at least one lubricant, characterized in that the preparation comprises from 2. 5% to 25% of lactose.
 NOVEL DOSAGE FORM / COMPOSITION TR 1997/00190 B (Wyeth) EXTENDED RELEASE FORMULATION CONTAINING VENLAFAXINE TR 1997/00190 B US 4138475 (Prior art) Etkin Madde Venlafaksin HCl Propranol Sferoid Mikrokristal selüloz + HPMC Mikrokristal selüloz Kaplama Etil selüloz + HPMC Problem/Solution: In the extrusion process, heat buildup occurred which dried out the extrudate so much that it was difficult to convert the extruded cylinders into spheroids. Addition of hydroxypropylmethylcellulose 2208 to the venlafaxine hydrochloride microcrystalline cellulose mix made production of spheroids practical. 1. An extended release formulation of venlafaxine hydrochloride comprising …. . spheroids comprised of …. . venlafaxine hydrochloride …. microcrystalline cellulose, …. hydroxypropylmethylcellulose, . . wherein the spheroids are coated with a film coating composition comprised of ethyl cellulose and hydroxypropylmethylcellulose.
NOVEL DOSAGE FORM / COMPOSITION TR 1997/00190 B (Wyeth) EXTENDED RELEASE FORMULATION CONTAINING VENLAFAXINE TR 1997/00190 B US 4138475 (Prior art) Etkin Madde Venlafaksin HCl Propranol Sferoid Mikrokristal selüloz + HPMC Mikrokristal selüloz Kaplama Etil selüloz + HPMC Problem/Solution: In the extrusion process, heat buildup occurred which dried out the extrudate so much that it was difficult to convert the extruded cylinders into spheroids. Addition of hydroxypropylmethylcellulose 2208 to the venlafaxine hydrochloride microcrystalline cellulose mix made production of spheroids practical. 1. An extended release formulation of venlafaxine hydrochloride comprising …. . spheroids comprised of …. . venlafaxine hydrochloride …. microcrystalline cellulose, …. hydroxypropylmethylcellulose, . . wherein the spheroids are coated with a film coating composition comprised of ethyl cellulose and hydroxypropylmethylcellulose.
 Farma. Patent Araştırma Danışmanlık http: //www. farmapatent. com. tr Teşekkürler
Farma. Patent Araştırma Danışmanlık http: //www. farmapatent. com. tr Teşekkürler


