26.Гетероциклы I 22.02.11.ppt
- Количество слайдов: 46
 Фарм. Ф Органическая химия Лекция 26 ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ I (трехчленные циклы, пятичленные циклы с одним гетероатомом)
Фарм. Ф Органическая химия Лекция 26 ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ I (трехчленные циклы, пятичленные циклы с одним гетероатомом)
 Фарм. Ф Органическая химия Гетероциклическими называются соединения, имеющие циклическую структуру и содержащие в цикле неуглеродные атомы (гетероатомы). Наибольшее распространение и практическое значение имеют пяти- и шестичленные циклы, содержащие в качестве гетероатомов кислород, серу и азот.
Фарм. Ф Органическая химия Гетероциклическими называются соединения, имеющие циклическую структуру и содержащие в цикле неуглеродные атомы (гетероатомы). Наибольшее распространение и практическое значение имеют пяти- и шестичленные циклы, содержащие в качестве гетероатомов кислород, серу и азот.
 Фарм. Ф Органическая химия Классификация и номенклатура гетероциклов Гетероциклы классифицируются: 1) по величине цикла и 2) по виду и количеству гетероатомов.
Фарм. Ф Органическая химия Классификация и номенклатура гетероциклов Гетероциклы классифицируются: 1) по величине цикла и 2) по виду и количеству гетероатомов.
 Фарм. Ф Органическая химия НОМЕНКЛАТУРА ГАНЧА Величина цикла Гетероатомы Общее количество атомов в цикле Суффикс в названии Вид гетероато ма Суффикс в названии 3 -ирин O -окс(а)- 5 -ол S -тиа- 6 -ин N -аз(а)- 7 -епин
Фарм. Ф Органическая химия НОМЕНКЛАТУРА ГАНЧА Величина цикла Гетероатомы Общее количество атомов в цикле Суффикс в названии Вид гетероато ма Суффикс в названии 3 -ирин O -окс(а)- 5 -ол S -тиа- 6 -ин N -аз(а)- 7 -епин
 Фарм. Ф Органическая химия Правила нумерации: Старшинство атомов: O>S>N 1) Нумерация начинается от самого старшего атома к наименее старшему по кратчайшему пути. 2) Из возможных вариантов предпочтителен тот, в котором номер положения заместителя наименьший.
Фарм. Ф Органическая химия Правила нумерации: Старшинство атомов: O>S>N 1) Нумерация начинается от самого старшего атома к наименее старшему по кратчайшему пути. 2) Из возможных вариантов предпочтителен тот, в котором номер положения заместителя наименьший.
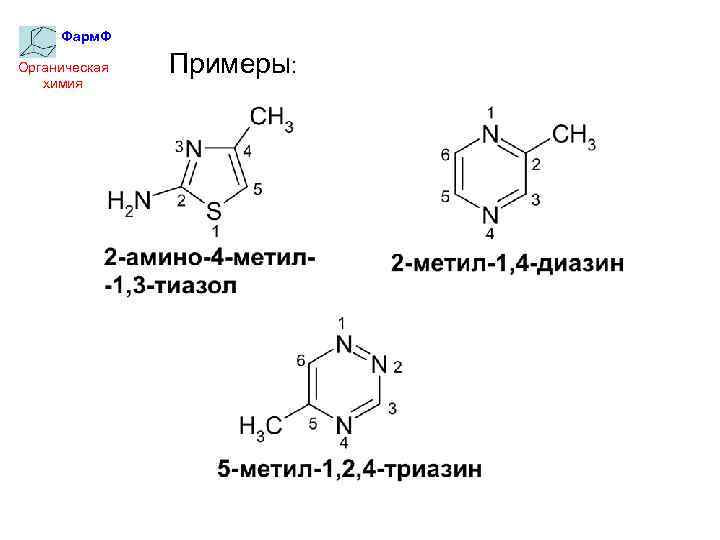 Фарм. Ф Органическая химия Примеры:
Фарм. Ф Органическая химия Примеры:
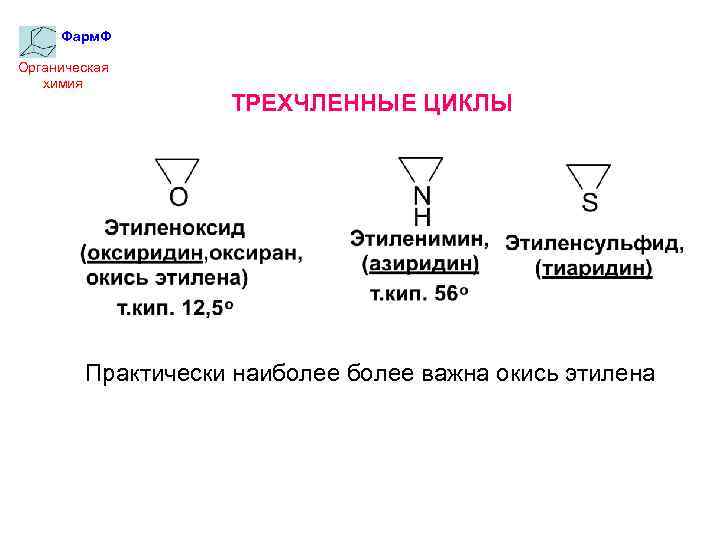 Фарм. Ф Органическая химия ТРЕХЧЛЕННЫЕ ЦИКЛЫ Практически наиболее важна окись этилена
Фарм. Ф Органическая химия ТРЕХЧЛЕННЫЕ ЦИКЛЫ Практически наиболее важна окись этилена
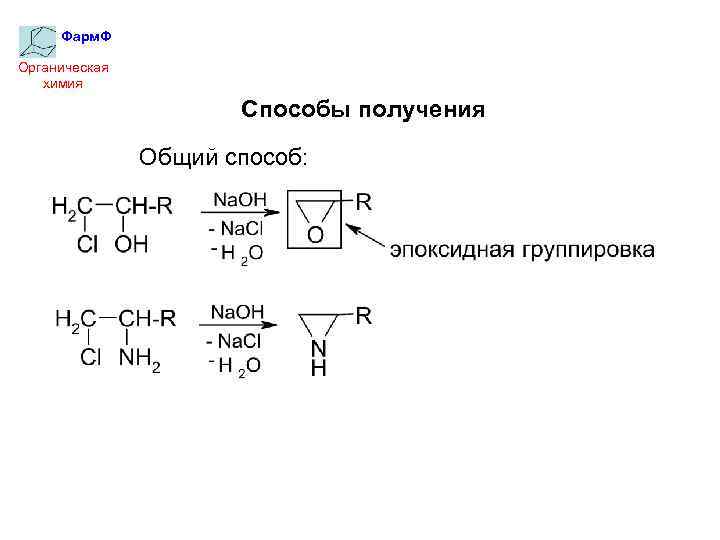 Фарм. Ф Органическая химия Способы получения Общий способ:
Фарм. Ф Органическая химия Способы получения Общий способ:
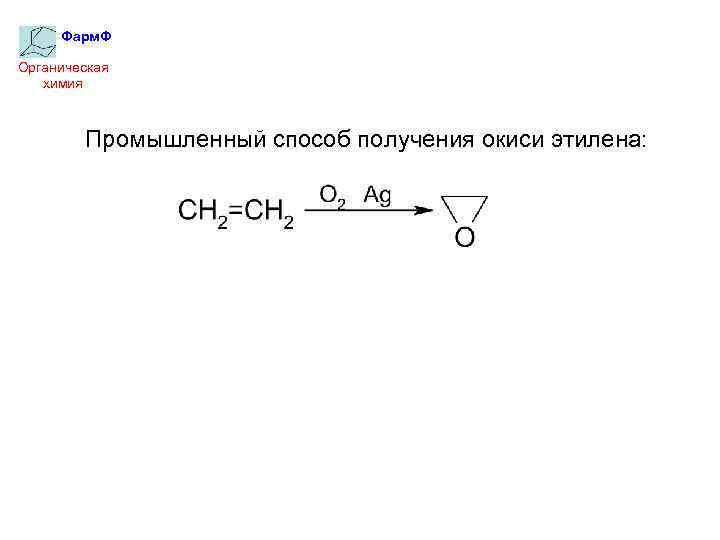 Фарм. Ф Органическая химия Промышленный способ получения окиси этилена:
Фарм. Ф Органическая химия Промышленный способ получения окиси этилена:
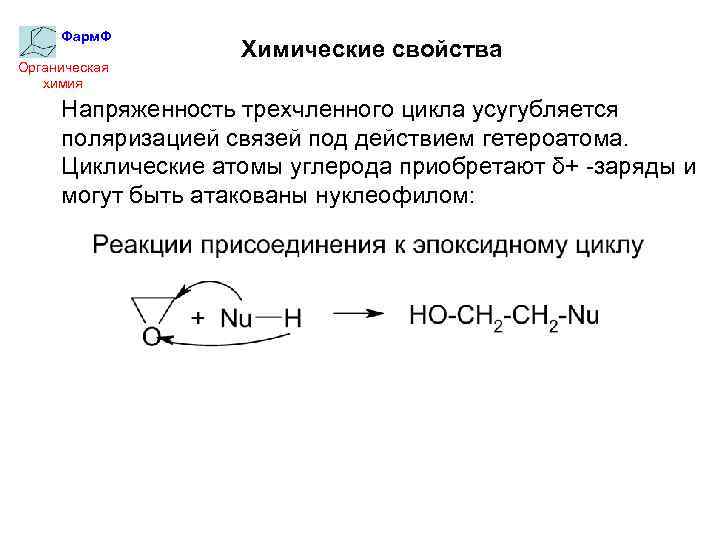 Фарм. Ф Органическая химия Химические свойства Напряженность трехчленного цикла усугубляется поляризацией связей под действием гетероатома. Циклические атомы углерода приобретают δ+ -заряды и могут быть атакованы нуклеофилом:
Фарм. Ф Органическая химия Химические свойства Напряженность трехчленного цикла усугубляется поляризацией связей под действием гетероатома. Циклические атомы углерода приобретают δ+ -заряды и могут быть атакованы нуклеофилом:
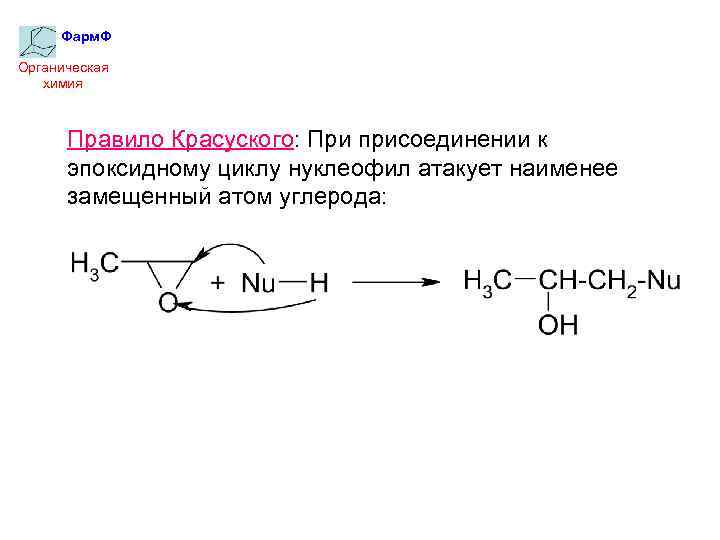 Фарм. Ф Органическая химия Правило Красуского: При присоединении к эпоксидному циклу нуклеофил атакует наименее замещенный атом углерода:
Фарм. Ф Органическая химия Правило Красуского: При присоединении к эпоксидному циклу нуклеофил атакует наименее замещенный атом углерода:
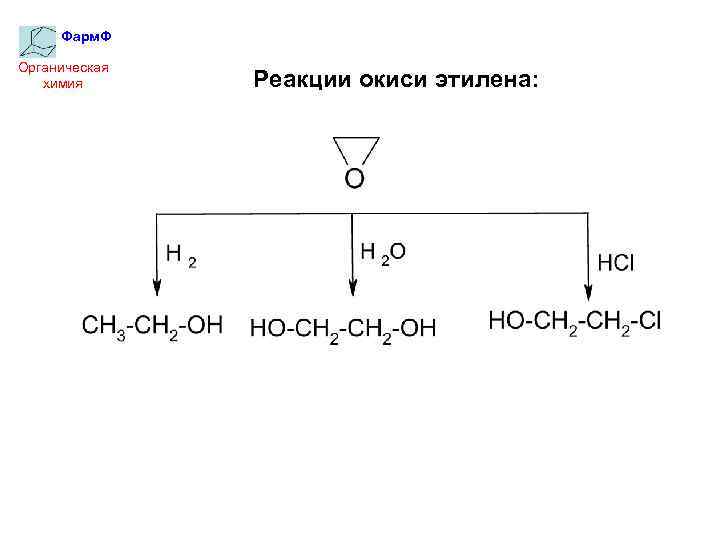 Фарм. Ф Органическая химия Реакции окиси этилена:
Фарм. Ф Органическая химия Реакции окиси этилена:
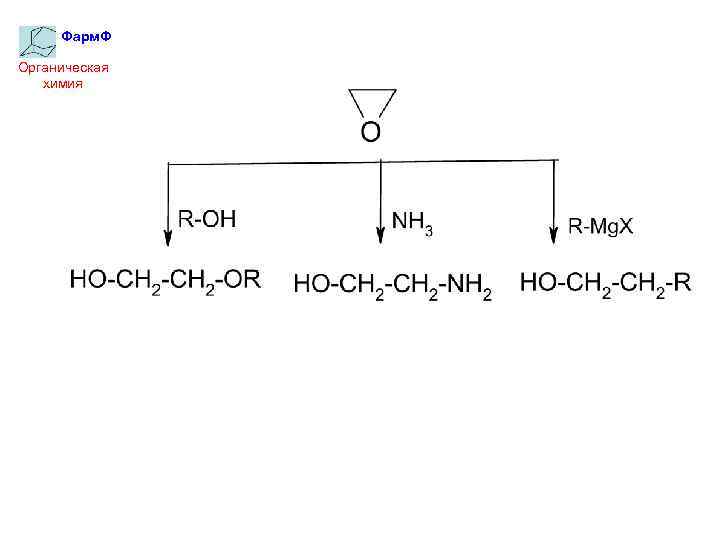 Фарм. Ф Органическая химия
Фарм. Ф Органическая химия
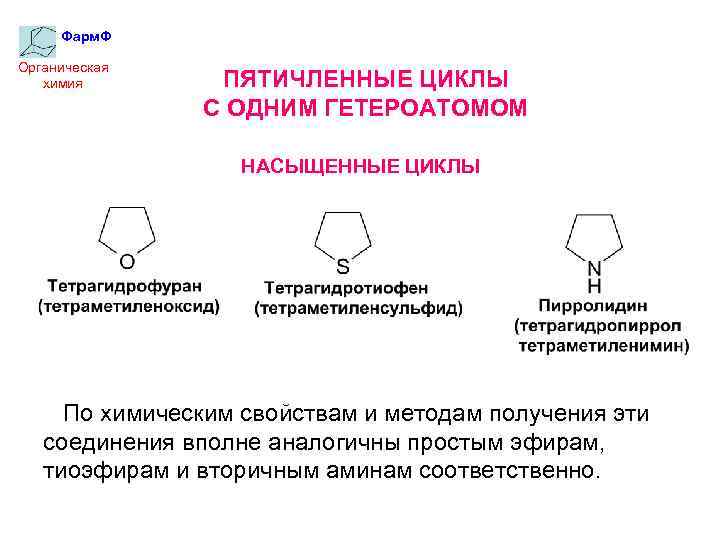 Фарм. Ф Органическая химия ПЯТИЧЛЕННЫЕ ЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ НАСЫЩЕННЫЕ ЦИКЛЫ По химическим свойствам и методам получения эти соединения вполне аналогичны простым эфирам, тиоэфирам и вторичным аминам соответственно.
Фарм. Ф Органическая химия ПЯТИЧЛЕННЫЕ ЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ НАСЫЩЕННЫЕ ЦИКЛЫ По химическим свойствам и методам получения эти соединения вполне аналогичны простым эфирам, тиоэфирам и вторичным аминам соответственно.
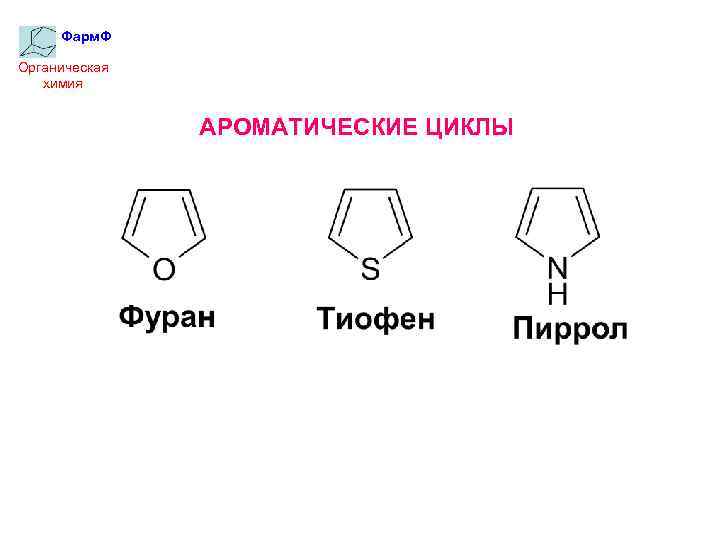 Фарм. Ф Органическая химия АРОМАТИЧЕСКИЕ ЦИКЛЫ
Фарм. Ф Органическая химия АРОМАТИЧЕСКИЕ ЦИКЛЫ
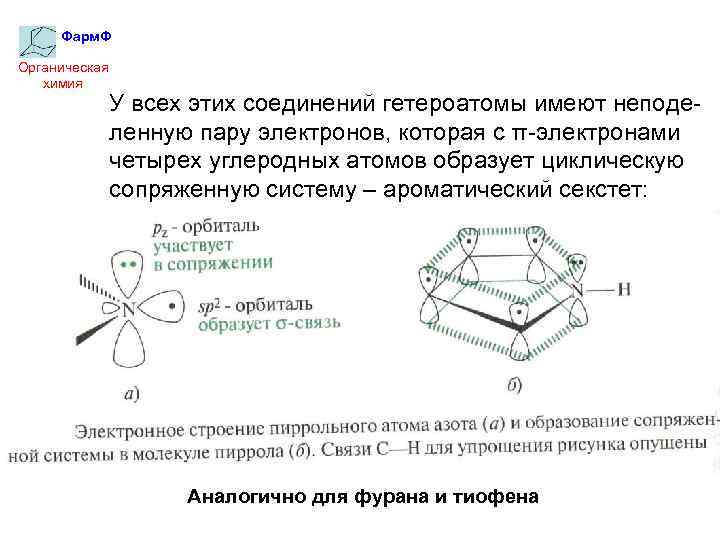 Фарм. Ф Органическая химия У всех этих соединений гетероатомы имеют неподеленную пару электронов, которая с π-электронами четырех углеродных атомов образует циклическую сопряженную систему – ароматический секстет: Аналогично для фурана и тиофена
Фарм. Ф Органическая химия У всех этих соединений гетероатомы имеют неподеленную пару электронов, которая с π-электронами четырех углеродных атомов образует циклическую сопряженную систему – ароматический секстет: Аналогично для фурана и тиофена
 Фарм. Ф Органическая химия Сравнительная ароматичность фурана, тиофена и пиррола Из всех трех циклов тиофен наиболее ароматичен, т. к. его энергия сопряжения выше, чем у фурана и пиррола (дополнительная резонансная структура за счет d-орбиталей атома серы). Наименее ароматичен фуран, т. к. его молекула наиболее полярна.
Фарм. Ф Органическая химия Сравнительная ароматичность фурана, тиофена и пиррола Из всех трех циклов тиофен наиболее ароматичен, т. к. его энергия сопряжения выше, чем у фурана и пиррола (дополнительная резонансная структура за счет d-орбиталей атома серы). Наименее ароматичен фуран, т. к. его молекула наиболее полярна.
 Фарм. Ф Органическая химия Средняя π-электронная плотность в расчете на 1 атом в циклах фурана, тиофена и пиррола больше, чем в бензоле, поэтому эти циклы называются π-избыточными.
Фарм. Ф Органическая химия Средняя π-электронная плотность в расчете на 1 атом в циклах фурана, тиофена и пиррола больше, чем в бензоле, поэтому эти циклы называются π-избыточными.
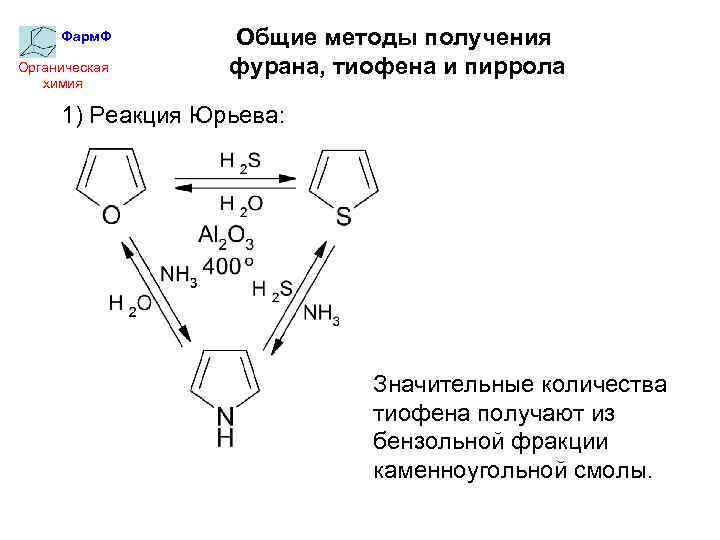 Фарм. Ф Органическая химия Общие методы получения фурана, тиофена и пиррола 1) Реакция Юрьева: Значительные количества тиофена получают из бензольной фракции каменноугольной смолы.
Фарм. Ф Органическая химия Общие методы получения фурана, тиофена и пиррола 1) Реакция Юрьева: Значительные количества тиофена получают из бензольной фракции каменноугольной смолы.
 Фарм. Ф Органическая химия 2) Синтез Кнорре:
Фарм. Ф Органическая химия 2) Синтез Кнорре:
 Фарм. Ф Органическая химия Химические свойства фурана, тиофена и пиррола По химическим свойствам фуран, тиофен и пиррол – это типичные ароматические соединения, отличающиеся тем, что из-за π-избыточности скорость их электрофильных реакций повышена и они сравнительно легко окисляются.
Фарм. Ф Органическая химия Химические свойства фурана, тиофена и пиррола По химическим свойствам фуран, тиофен и пиррол – это типичные ароматические соединения, отличающиеся тем, что из-за π-избыточности скорость их электрофильных реакций повышена и они сравнительно легко окисляются.
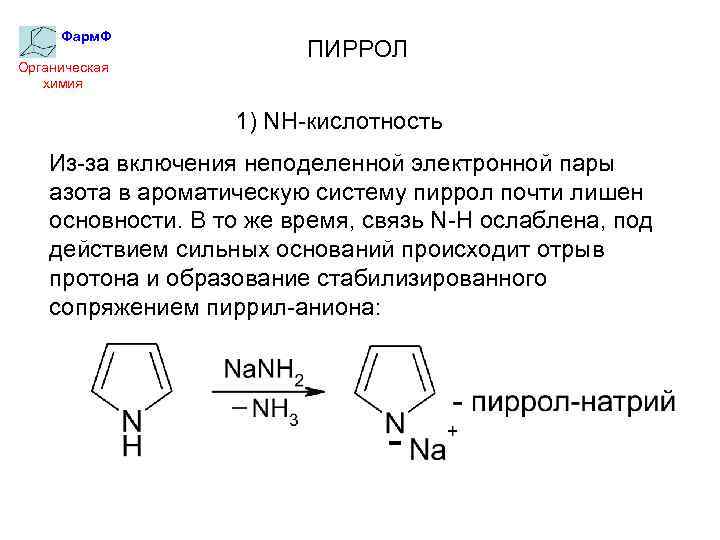 Фарм. Ф Органическая химия ПИРРОЛ 1) NH-кислотность Из-за включения неподеленной электронной пары азота в ароматическую систему пиррол почти лишен основности. В то же время, связь N-H ослаблена, под действием сильных оснований происходит отрыв протона и образование стабилизированного сопряжением пиррил-аниона:
Фарм. Ф Органическая химия ПИРРОЛ 1) NH-кислотность Из-за включения неподеленной электронной пары азота в ароматическую систему пиррол почти лишен основности. В то же время, связь N-H ослаблена, под действием сильных оснований происходит отрыв протона и образование стабилизированного сопряжением пиррил-аниона:
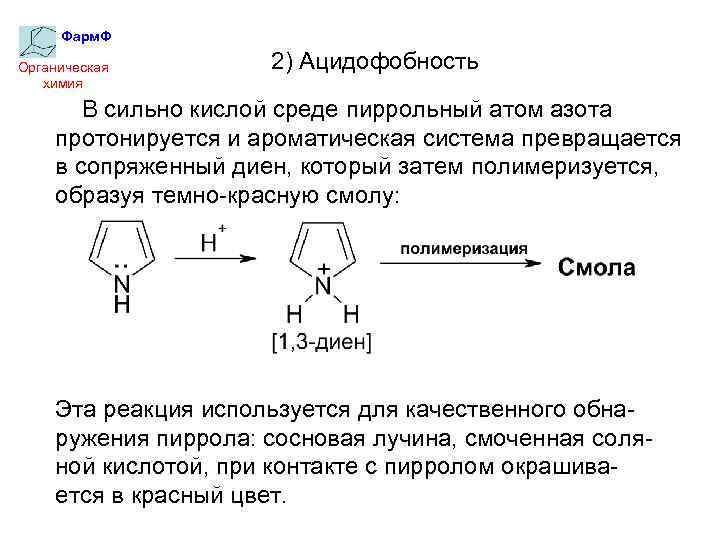 Фарм. Ф Органическая химия 2) Ацидофобность В сильно кислой среде пиррольный атом азота протонируется и ароматическая система превращается в сопряженный диен, который затем полимеризуется, образуя темно-красную смолу: Эта реакция используется для качественного обнаружения пиррола: сосновая лучина, смоченная соляной кислотой, при контакте с пирролом окрашивается в красный цвет.
Фарм. Ф Органическая химия 2) Ацидофобность В сильно кислой среде пиррольный атом азота протонируется и ароматическая система превращается в сопряженный диен, который затем полимеризуется, образуя темно-красную смолу: Эта реакция используется для качественного обнаружения пиррола: сосновая лучина, смоченная соляной кислотой, при контакте с пирролом окрашивается в красный цвет.
 Фарм. Ф Органическая химия 3) Реакции электрофильного замещения
Фарм. Ф Органическая химия 3) Реакции электрофильного замещения
 Фарм. Ф Органическая химия Из-за ацидофобности пиррола для сульфирования и нитрования применяются апротонные реагенты: пиридин-N-сульфотриоксид и ацетилнитрат (смешанный ангидрид азотной и уксусной кислот). При галогенировании пиррола даже при 0 о образуются только тетрагалогенопроизводные.
Фарм. Ф Органическая химия Из-за ацидофобности пиррола для сульфирования и нитрования применяются апротонные реагенты: пиридин-N-сульфотриоксид и ацетилнитрат (смешанный ангидрид азотной и уксусной кислот). При галогенировании пиррола даже при 0 о образуются только тетрагалогенопроизводные.
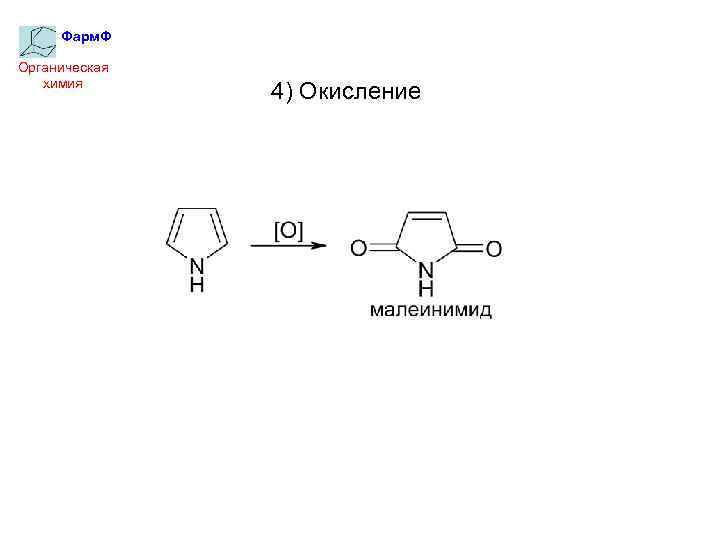 Фарм. Ф Органическая химия 4) Окисление
Фарм. Ф Органическая химия 4) Окисление
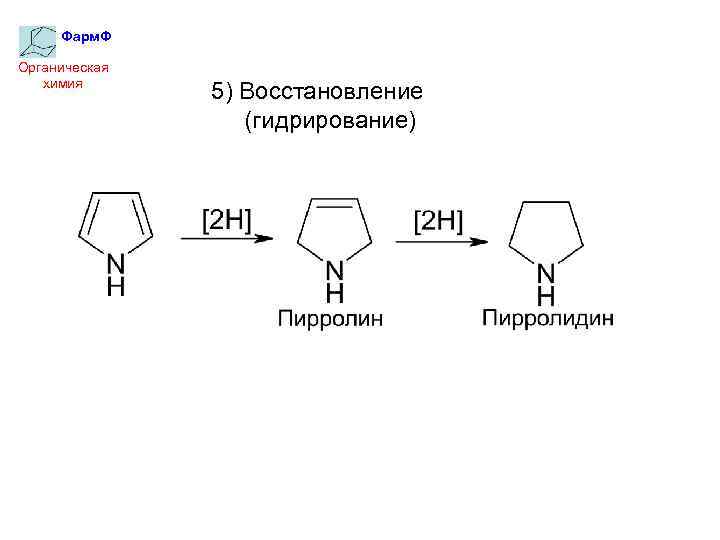 Фарм. Ф Органическая химия 5) Восстановление (гидрирование)
Фарм. Ф Органическая химия 5) Восстановление (гидрирование)
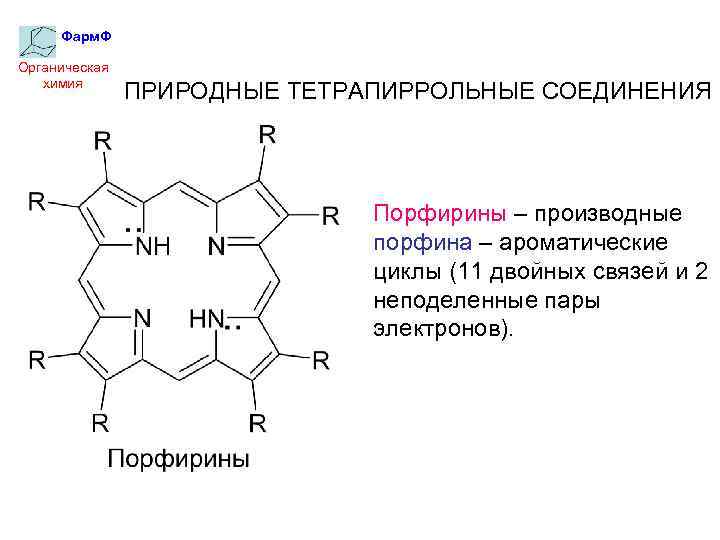 Фарм. Ф Органическая химия ПРИРОДНЫЕ ТЕТРАПИРРОЛЬНЫЕ СОЕДИНЕНИЯ Порфирины – производные порфина – ароматические циклы (11 двойных связей и 2 неподеленные пары электронов).
Фарм. Ф Органическая химия ПРИРОДНЫЕ ТЕТРАПИРРОЛЬНЫЕ СОЕДИНЕНИЯ Порфирины – производные порфина – ароматические циклы (11 двойных связей и 2 неподеленные пары электронов).
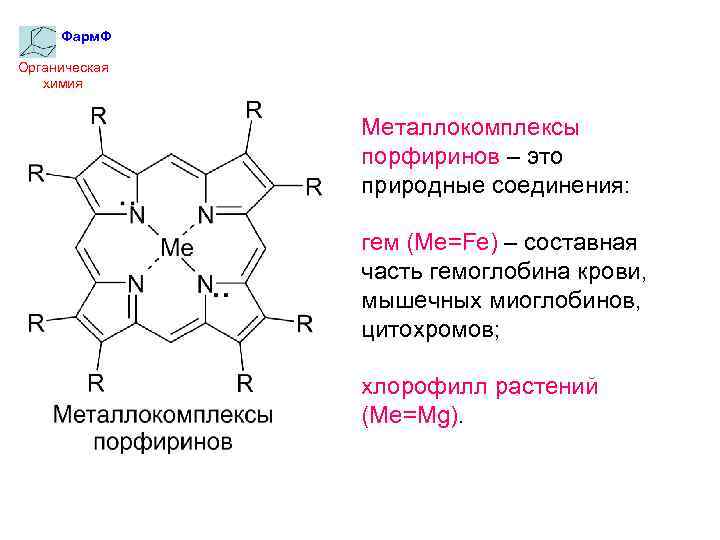 Фарм. Ф Органическая химия Металлокомплексы порфиринов – это природные соединения: гем (Me=Fe) – составная часть гемоглобина крови, мышечных миоглобинов, цитохромов; хлорофилл растений (Me=Mg).
Фарм. Ф Органическая химия Металлокомплексы порфиринов – это природные соединения: гем (Me=Fe) – составная часть гемоглобина крови, мышечных миоглобинов, цитохромов; хлорофилл растений (Me=Mg).
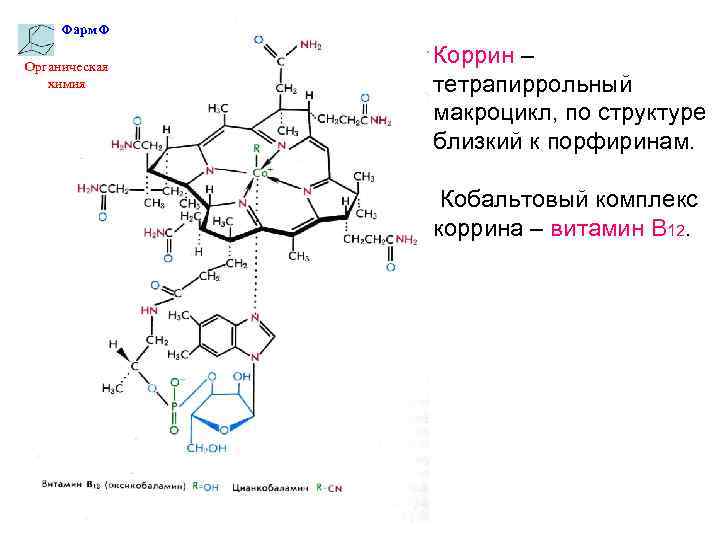 Фарм. Ф Органическая химия Коррин – тетрапиррольный макроцикл, по структуре близкий к порфиринам. Кобальтовый комплекс коррина – витамин В 12.
Фарм. Ф Органическая химия Коррин – тетрапиррольный макроцикл, по структуре близкий к порфиринам. Кобальтовый комплекс коррина – витамин В 12.
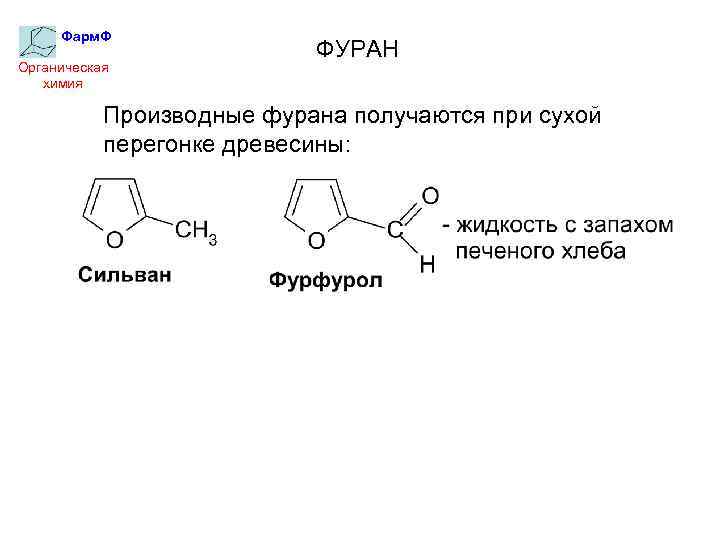 Фарм. Ф Органическая химия ФУРАН Производные фурана получаются при сухой перегонке древесины:
Фарм. Ф Органическая химия ФУРАН Производные фурана получаются при сухой перегонке древесины:
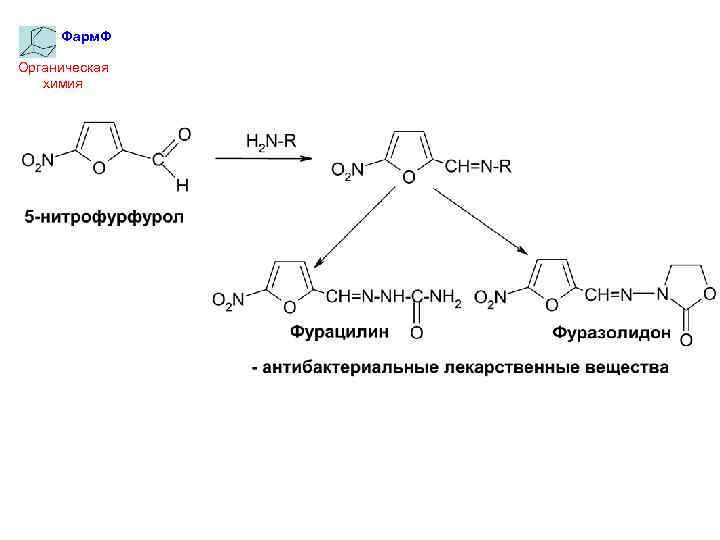
 Фарм. Ф Органическая химия Фуран – ароматический цикл, легко вступающий в реакции электрофильного замещения:
Фарм. Ф Органическая химия Фуран – ароматический цикл, легко вступающий в реакции электрофильного замещения:
 Фарм. Ф Органическая химия
Фарм. Ф Органическая химия
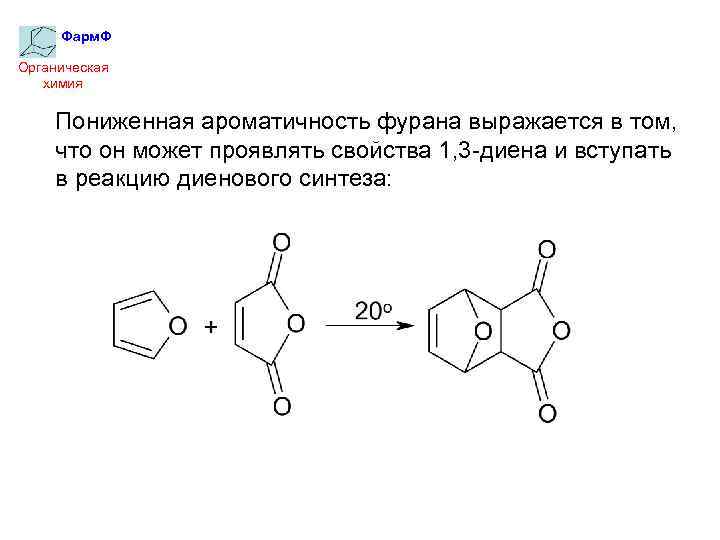 Фарм. Ф Органическая химия Пониженная ароматичность фурана выражается в том, что он может проявлять свойства 1, 3 -диена и вступать в реакцию диенового синтеза:
Фарм. Ф Органическая химия Пониженная ароматичность фурана выражается в том, что он может проявлять свойства 1, 3 -диена и вступать в реакцию диенового синтеза:
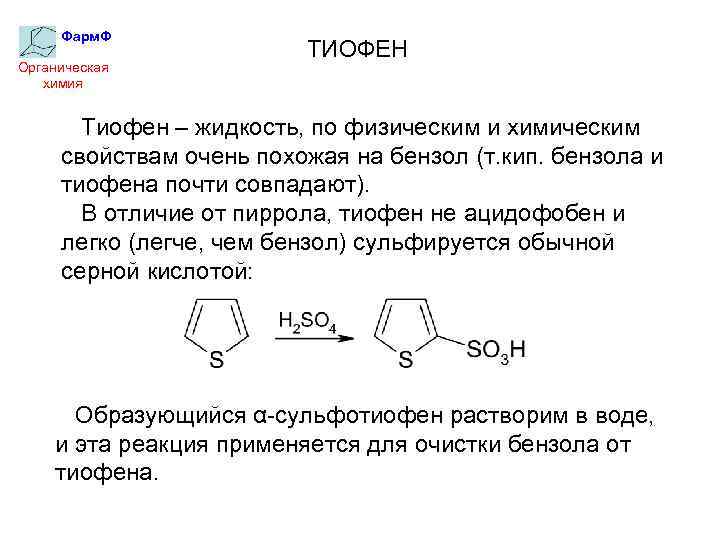 Фарм. Ф Органическая химия ТИОФЕН Тиофен – жидкость, по физическим и химическим свойствам очень похожая на бензол (т. кип. бензола и тиофена почти совпадают). В отличие от пиррола, тиофен не ацидофобен и легко (легче, чем бензол) сульфируется обычной серной кислотой: Образующийся α-сульфотиофен растворим в воде, и эта реакция применяется для очистки бензола от тиофена.
Фарм. Ф Органическая химия ТИОФЕН Тиофен – жидкость, по физическим и химическим свойствам очень похожая на бензол (т. кип. бензола и тиофена почти совпадают). В отличие от пиррола, тиофен не ацидофобен и легко (легче, чем бензол) сульфируется обычной серной кислотой: Образующийся α-сульфотиофен растворим в воде, и эта реакция применяется для очистки бензола от тиофена.
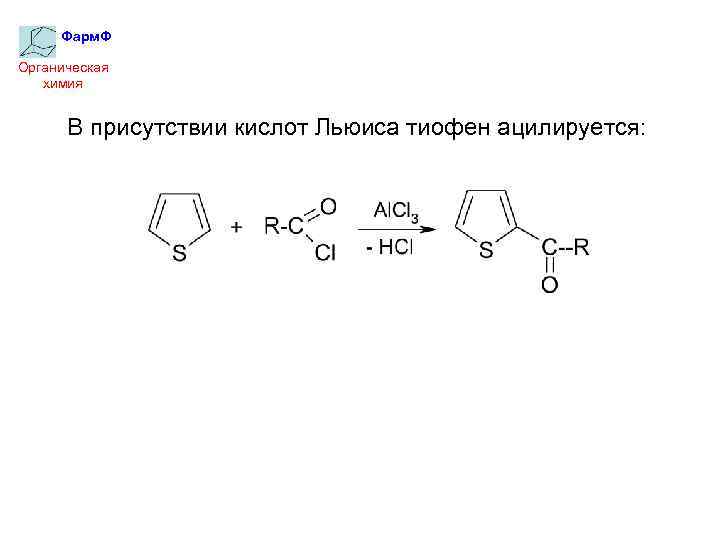 Фарм. Ф Органическая химия В присутствии кислот Льюиса тиофен ацилируется:
Фарм. Ф Органическая химия В присутствии кислот Льюиса тиофен ацилируется:
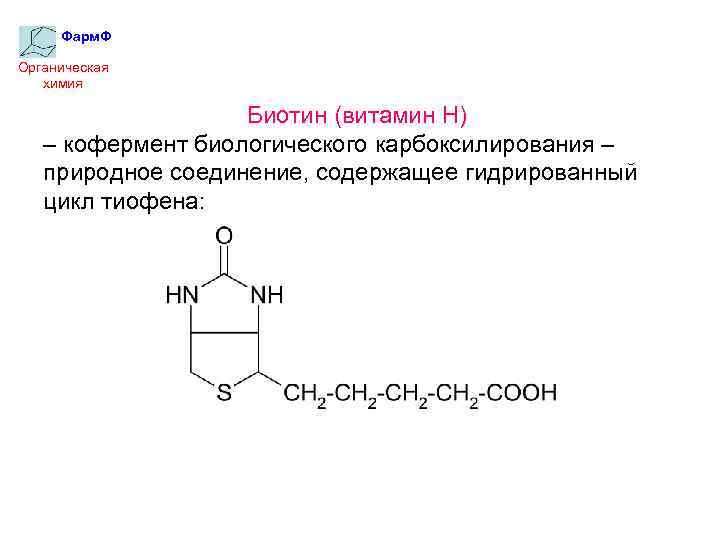 Фарм. Ф Органическая химия Биотин (витамин Н) – кофермент биологического карбоксилирования – природное соединение, содержащее гидрированный цикл тиофена:
Фарм. Ф Органическая химия Биотин (витамин Н) – кофермент биологического карбоксилирования – природное соединение, содержащее гидрированный цикл тиофена:
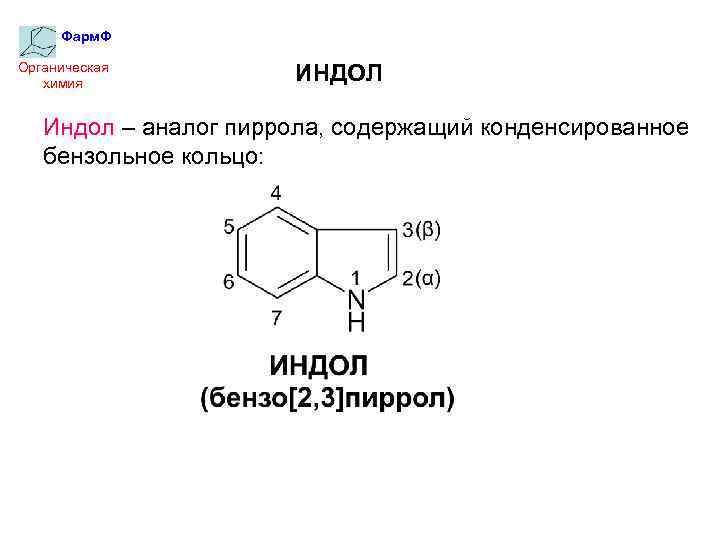 Фарм. Ф Органическая химия ИНДОЛ Индол – аналог пиррола, содержащий конденсированное бензольное кольцо:
Фарм. Ф Органическая химия ИНДОЛ Индол – аналог пиррола, содержащий конденсированное бензольное кольцо:
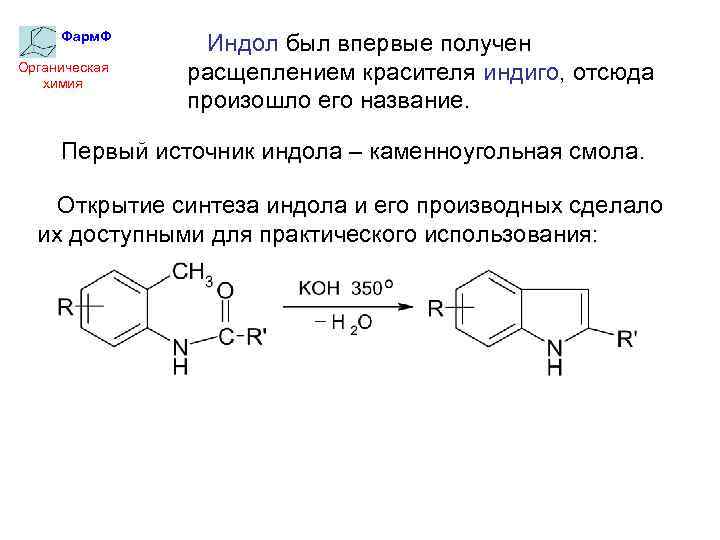 Фарм. Ф Органическая химия Индол был впервые получен расщеплением красителя индиго, отсюда произошло его название. Первый источник индола – каменноугольная смола. Открытие синтеза индола и его производных сделало их доступными для практического использования:
Фарм. Ф Органическая химия Индол был впервые получен расщеплением красителя индиго, отсюда произошло его название. Первый источник индола – каменноугольная смола. Открытие синтеза индола и его производных сделало их доступными для практического использования:
 Фарм. Ф Органическая химия Химические свойства индола По химическим свойствам индол является аналогом пиррола: это ароматический π-избыточный цикл. Индол подобно пирролу почти лишен основности и ацидофобен. Он обладает NH-кислотностью, близкой к кислотности спиртов, склонен к реакциям элетрофильного замещения и к окислению.
Фарм. Ф Органическая химия Химические свойства индола По химическим свойствам индол является аналогом пиррола: это ароматический π-избыточный цикл. Индол подобно пирролу почти лишен основности и ацидофобен. Он обладает NH-кислотностью, близкой к кислотности спиртов, склонен к реакциям элетрофильного замещения и к окислению.
 Фарм. Ф Органическая химия 1) Реакции электрофильного замещения Реакции SE идут по пиррольному циклу в положение 3, при этом промежуточный σ-комплекс стабилизирован сопряжением:
Фарм. Ф Органическая химия 1) Реакции электрофильного замещения Реакции SE идут по пиррольному циклу в положение 3, при этом промежуточный σ-комплекс стабилизирован сопряжением:
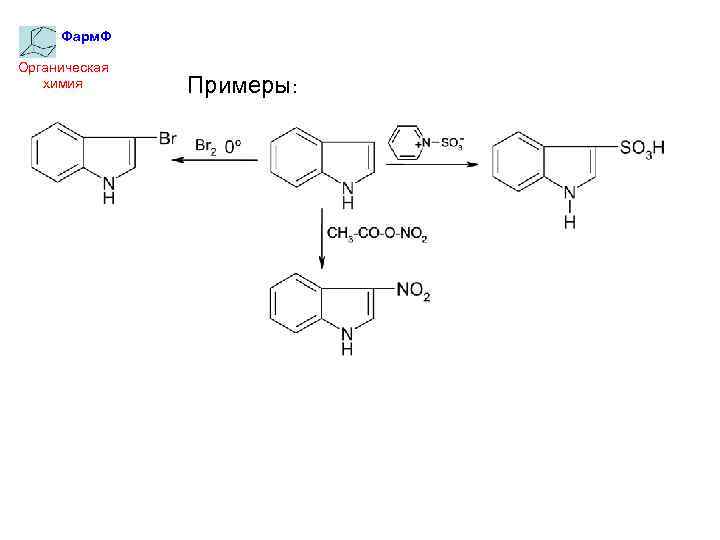 Фарм. Ф Органическая химия Примеры:
Фарм. Ф Органическая химия Примеры:
 Фарм. Ф Органическая химия 2) Окисление
Фарм. Ф Органическая химия 2) Окисление
 Фарм. Ф Органическая химия
Фарм. Ф Органическая химия
 Фарм. Ф Органическая химия Другие природные соединения индола
Фарм. Ф Органическая химия Другие природные соединения индола
 Фарм. Ф Органическая химия ЛИТЕРАТУРА: Основная 1. Тюкавкина Н. А. , Зурабян С. Э. , Белобородов В. Л. и др. – Органическая химия (специальный курс), кн. 2 – Дрофа, М. , 2008 г. , с. 41 -60. Дополнительная 1. Н. А. Тюкавкина, Ю. И. Бауков – Биоорганическая химия – ДРОФА, М. , 2007 г. , с. 278 -292. 22. 02. 11
Фарм. Ф Органическая химия ЛИТЕРАТУРА: Основная 1. Тюкавкина Н. А. , Зурабян С. Э. , Белобородов В. Л. и др. – Органическая химия (специальный курс), кн. 2 – Дрофа, М. , 2008 г. , с. 41 -60. Дополнительная 1. Н. А. Тюкавкина, Ю. И. Бауков – Биоорганическая химия – ДРОФА, М. , 2007 г. , с. 278 -292. 22. 02. 11


