18.Гетерофункциональные соед. 04.12.10.ppt
- Количество слайдов: 44
 Фарм. Ф Органическая химия Лекция 18 ГЕТЕРОФУНКЦИОНАЛЬНЫЕ ПРИРОДНЫЕ СОЕДИНЕНИЯ
Фарм. Ф Органическая химия Лекция 18 ГЕТЕРОФУНКЦИОНАЛЬНЫЕ ПРИРОДНЫЕ СОЕДИНЕНИЯ
 Фарм. Ф Органическая химия Большинство природных соединений являются гетерофункциональными, т. е. содержат различные функциональные группы. Наиболее часто встречающиеся группы: СООН, С=О, NH 2
Фарм. Ф Органическая химия Большинство природных соединений являются гетерофункциональными, т. е. содержат различные функциональные группы. Наиболее часто встречающиеся группы: СООН, С=О, NH 2
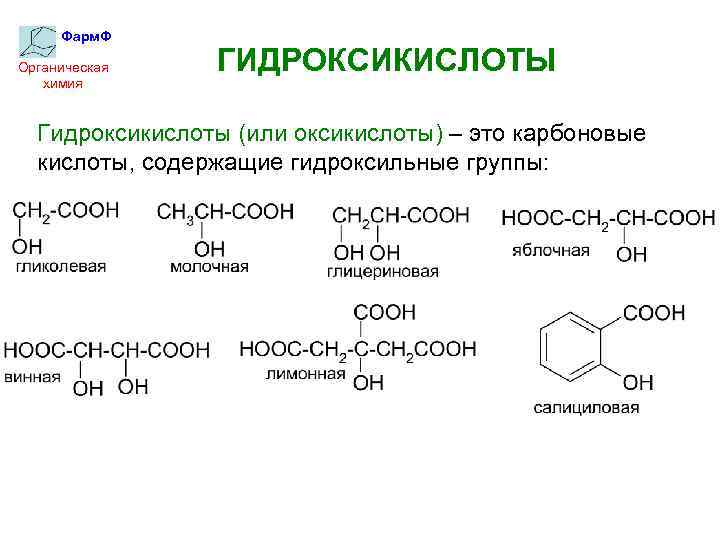 Фарм. Ф Органическая химия ГИДРОКСИКИСЛОТЫ Гидроксикислоты (или оксикислоты) – это карбоновые кислоты, содержащие гидроксильные группы:
Фарм. Ф Органическая химия ГИДРОКСИКИСЛОТЫ Гидроксикислоты (или оксикислоты) – это карбоновые кислоты, содержащие гидроксильные группы:
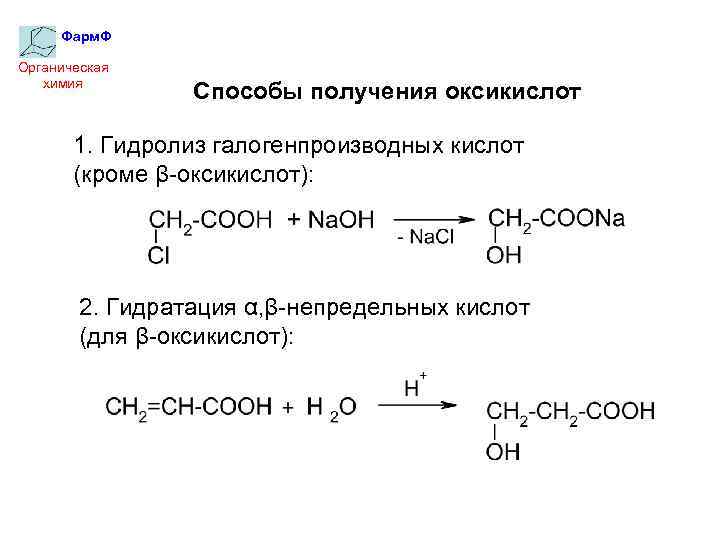 Фарм. Ф Органическая химия Способы получения оксикислот 1. Гидролиз галогенпроизводных кислот (кроме β-оксикислот): 2. Гидратация α, β-непредельных кислот (для β-оксикислот):
Фарм. Ф Органическая химия Способы получения оксикислот 1. Гидролиз галогенпроизводных кислот (кроме β-оксикислот): 2. Гидратация α, β-непредельных кислот (для β-оксикислот):
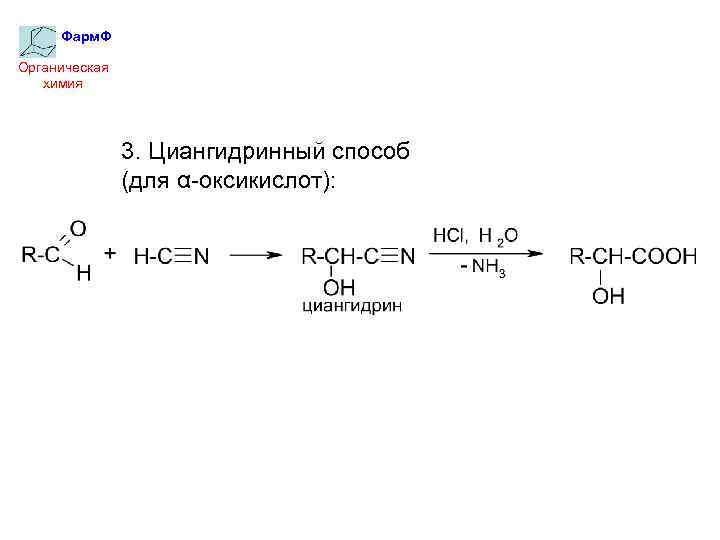 Фарм. Ф Органическая химия 3. Циангидринный способ (для α-оксикислот):
Фарм. Ф Органическая химия 3. Циангидринный способ (для α-оксикислот):
 Фарм. Ф Органическая химия Химические свойства оксикислот Оксикислоты объединяют в себе свойства карбоновых кислот и спиртов. Особые свойства оксикислот связаны с взаимодействием СООН- и ОН-групп. 1) Кислотность СООН-группы увеличивается за счет электроноакцепторного влияния ОН-группы, особенно сильно у α-оксикислот:
Фарм. Ф Органическая химия Химические свойства оксикислот Оксикислоты объединяют в себе свойства карбоновых кислот и спиртов. Особые свойства оксикислот связаны с взаимодействием СООН- и ОН-групп. 1) Кислотность СООН-группы увеличивается за счет электроноакцепторного влияния ОН-группы, особенно сильно у α-оксикислот:
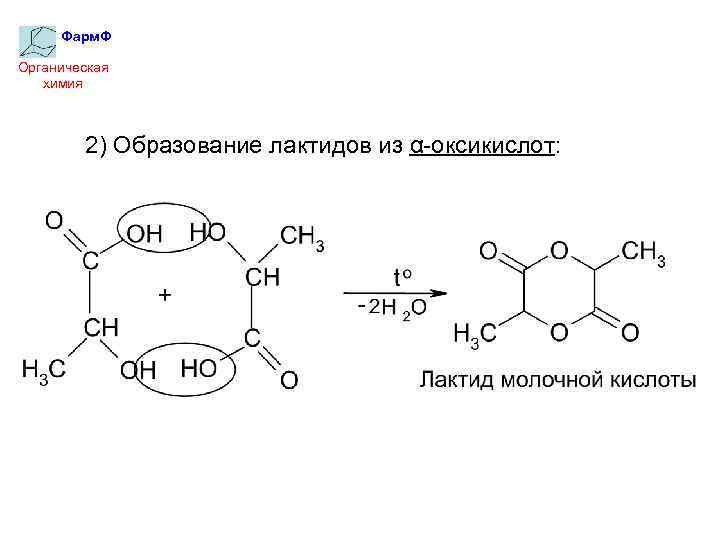 Фарм. Ф Органическая химия 2) Образование лактидов из α-оксикислот:
Фарм. Ф Органическая химия 2) Образование лактидов из α-оксикислот:
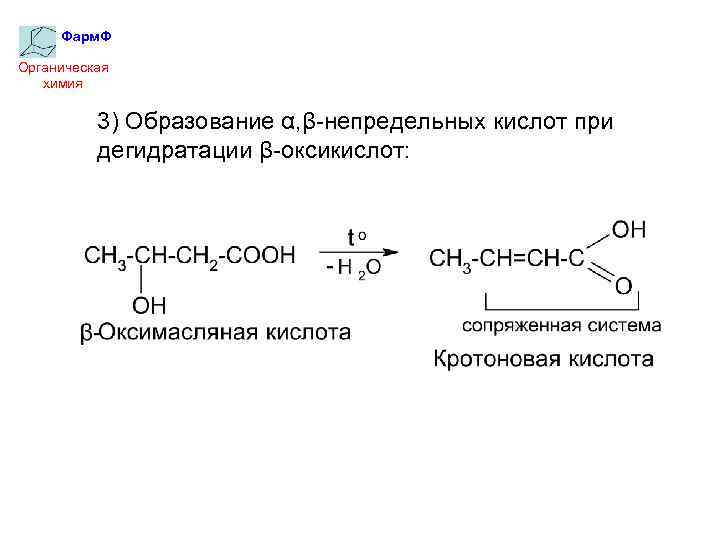 Фарм. Ф Органическая химия 3) Образование α, β-непредельных кислот при дегидратации β-оксикислот:
Фарм. Ф Органическая химия 3) Образование α, β-непредельных кислот при дегидратации β-оксикислот:
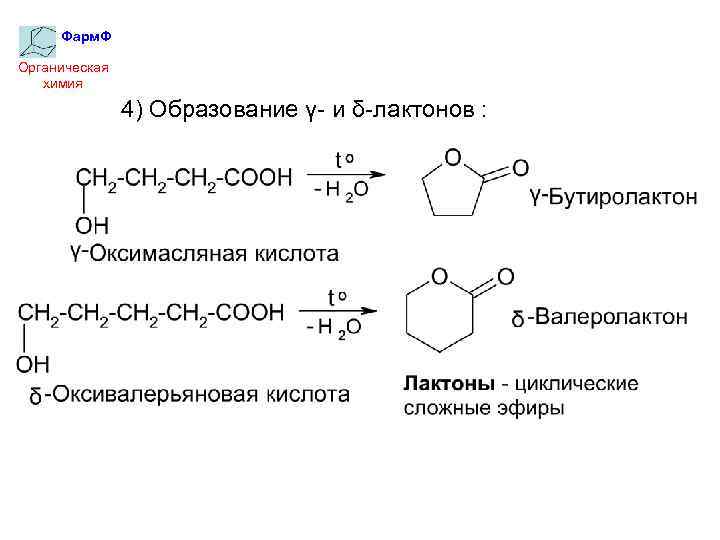 Фарм. Ф Органическая химия 4) Образование γ- и δ-лактонов :
Фарм. Ф Органическая химия 4) Образование γ- и δ-лактонов :
 Фарм. Ф Органическая химия Отдельные представители оксикислот Молочная кислота. Впервые выделена К Шееле из кислого молока (1780 г. ). Широко распространена как продукт биохимического брожения (гликолиз), является одним из ключевых метаболитов в обмене углеводов. Лимонная кислота. Содержится в лимонах (6 -8% сухой массы), в листьях махорки, откуда раньше получалась промышленным способом. Сейчас основной способ её получения – биохимическое лимоннокислое брожение под действием определенного штамма грибов. В организме лимонная кислота является одним из ключевых метаболитов энергетического обмена в цикле трикарбоновых кислот (цикл Кребса).
Фарм. Ф Органическая химия Отдельные представители оксикислот Молочная кислота. Впервые выделена К Шееле из кислого молока (1780 г. ). Широко распространена как продукт биохимического брожения (гликолиз), является одним из ключевых метаболитов в обмене углеводов. Лимонная кислота. Содержится в лимонах (6 -8% сухой массы), в листьях махорки, откуда раньше получалась промышленным способом. Сейчас основной способ её получения – биохимическое лимоннокислое брожение под действием определенного штамма грибов. В организме лимонная кислота является одним из ключевых метаболитов энергетического обмена в цикле трикарбоновых кислот (цикл Кребса).
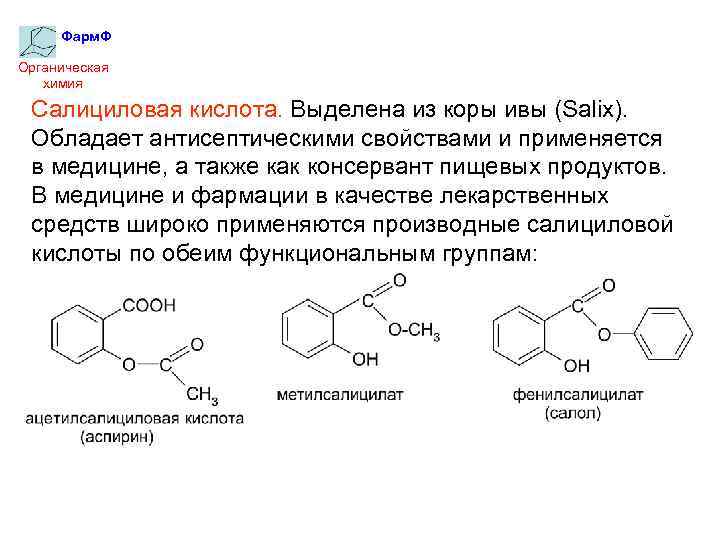 Фарм. Ф Органическая химия Салициловая кислота. Выделена из коры ивы (Salix). Обладает антисептическими свойствами и применяется в медицине, а также как консервант пищевых продуктов. В медицине и фармации в качестве лекарственных средств широко применяются производные салициловой кислоты по обеим функциональным группам:
Фарм. Ф Органическая химия Салициловая кислота. Выделена из коры ивы (Salix). Обладает антисептическими свойствами и применяется в медицине, а также как консервант пищевых продуктов. В медицине и фармации в качестве лекарственных средств широко применяются производные салициловой кислоты по обеим функциональным группам:
 Фарм. Ф Органическая химия ОКСОКИСЛОТЫ Оксокислоты – это карбоновые кислоты, содержащие оксогруппу:
Фарм. Ф Органическая химия ОКСОКИСЛОТЫ Оксокислоты – это карбоновые кислоты, содержащие оксогруппу:
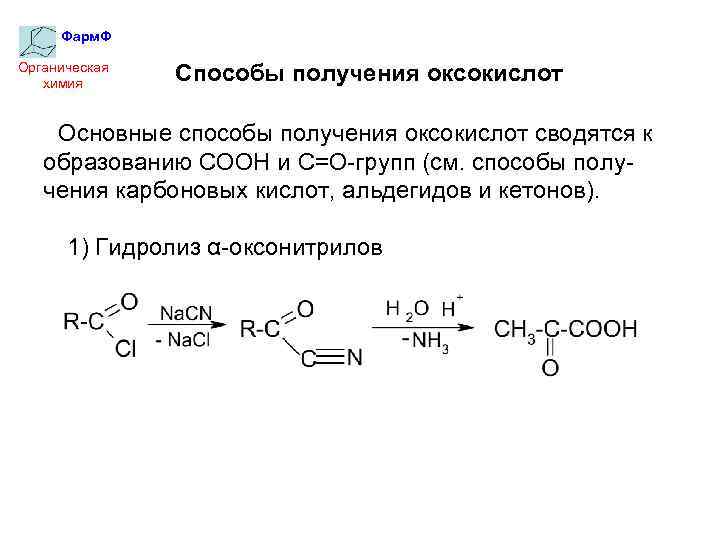 Фарм. Ф Органическая химия Способы получения оксокислот Основные способы получения оксокислот сводятся к образованию СООН и С=О-групп (см. способы получения карбоновых кислот, альдегидов и кетонов). 1) Гидролиз α-оксонитрилов
Фарм. Ф Органическая химия Способы получения оксокислот Основные способы получения оксокислот сводятся к образованию СООН и С=О-групп (см. способы получения карбоновых кислот, альдегидов и кетонов). 1) Гидролиз α-оксонитрилов
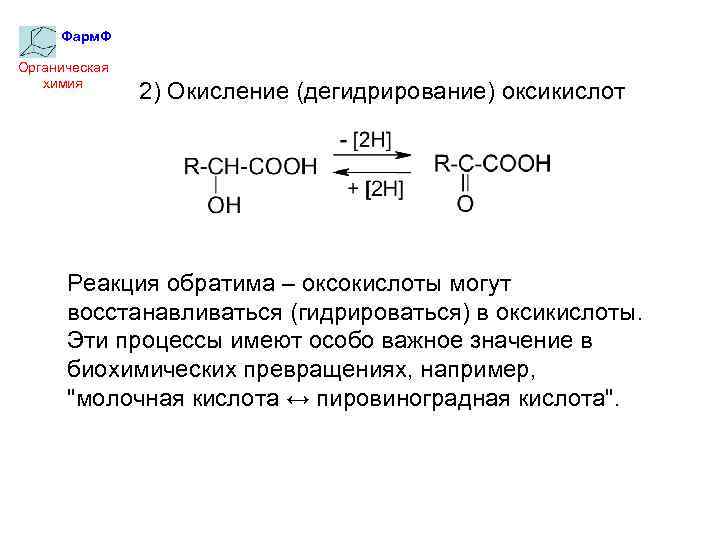 Фарм. Ф Органическая химия 2) Окисление (дегидрирование) оксикислот Реакция обратима – оксокислоты могут восстанавливаться (гидрироваться) в оксикислоты. Эти процессы имеют особо важное значение в биохимических превращениях, например, "молочная кислота ↔ пировиноградная кислота".
Фарм. Ф Органическая химия 2) Окисление (дегидрирование) оксикислот Реакция обратима – оксокислоты могут восстанавливаться (гидрироваться) в оксикислоты. Эти процессы имеют особо важное значение в биохимических превращениях, например, "молочная кислота ↔ пировиноградная кислота".
 Фарм. Ф Химические свойства оксокислот Органическая химия Оксокислоты образуют производные по карбоксильной и по карбонильной группам (см. химические свойства карбоновых кислот, альдегидов и кетонов). Особые свойства оксокислот связаны с взаимодействием СООН- и С=О-групп. 1) Кислотность
Фарм. Ф Химические свойства оксокислот Органическая химия Оксокислоты образуют производные по карбоксильной и по карбонильной группам (см. химические свойства карбоновых кислот, альдегидов и кетонов). Особые свойства оксокислот связаны с взаимодействием СООН- и С=О-групп. 1) Кислотность
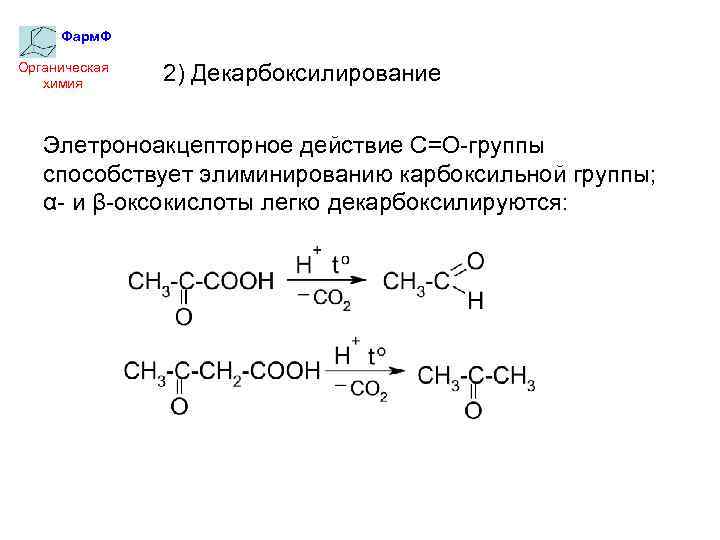 Фарм. Ф Органическая химия 2) Декарбоксилирование Элетроноакцепторное действие С=О-группы способствует элиминированию карбоксильной группы; α- и β-оксокислоты легко декарбоксилируются:
Фарм. Ф Органическая химия 2) Декарбоксилирование Элетроноакцепторное действие С=О-группы способствует элиминированию карбоксильной группы; α- и β-оксокислоты легко декарбоксилируются:
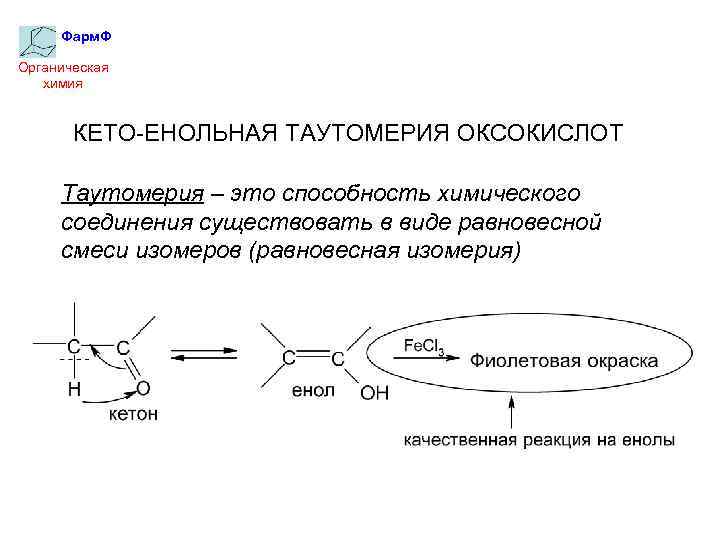 Фарм. Ф Органическая химия КЕТО-ЕНОЛЬНАЯ ТАУТОМЕРИЯ ОКСОКИСЛОТ Таутомерия – это способность химического соединения существовать в виде равновесной смеси изомеров (равновесная изомерия)
Фарм. Ф Органическая химия КЕТО-ЕНОЛЬНАЯ ТАУТОМЕРИЯ ОКСОКИСЛОТ Таутомерия – это способность химического соединения существовать в виде равновесной смеси изомеров (равновесная изомерия)
 Фарм. Ф Органическая химия Кето-енольное таутомерное равновесие возможно и в простых альдегидах и кетонах, но там содержание енольной формы ничтожно мало. Совместное электроноакцепторное влияние СООН- и С=О-групп в β-кетокислотах: 1) значительно увеличивает подвижность протонов у α-углеродного атома и 2) образующаяся енольная форма содержит сопряженную систему, что значительно увеличивает её термодинамическую устойчивость.
Фарм. Ф Органическая химия Кето-енольное таутомерное равновесие возможно и в простых альдегидах и кетонах, но там содержание енольной формы ничтожно мало. Совместное электроноакцепторное влияние СООН- и С=О-групп в β-кетокислотах: 1) значительно увеличивает подвижность протонов у α-углеродного атома и 2) образующаяся енольная форма содержит сопряженную систему, что значительно увеличивает её термодинамическую устойчивость.
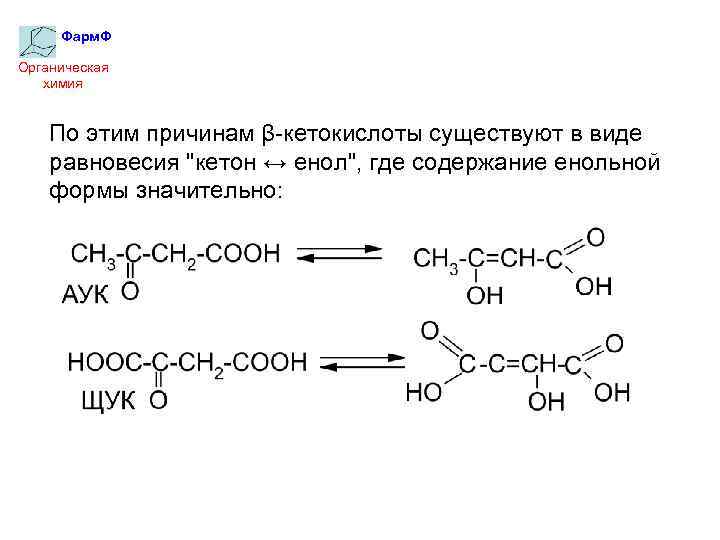 Фарм. Ф Органическая химия По этим причинам β-кетокислоты существуют в виде равновесия "кетон ↔ енол", где содержание енольной формы значительно:
Фарм. Ф Органическая химия По этим причинам β-кетокислоты существуют в виде равновесия "кетон ↔ енол", где содержание енольной формы значительно:
 Фарм. Ф Органическая химия АЦЕТОУКСУСНЫЙ ЭФИР Равновесие содержит около 8% енольной формы и её можно обнаружить с помощью цветной реакции с Fe. Cl 3.
Фарм. Ф Органическая химия АЦЕТОУКСУСНЫЙ ЭФИР Равновесие содержит около 8% енольной формы и её можно обнаружить с помощью цветной реакции с Fe. Cl 3.
 Фарм. Ф Органическая химия Применение ацетоуксусного эфира в органическом синтезе
Фарм. Ф Органическая химия Применение ацетоуксусного эфира в органическом синтезе
 Фарм. Ф Органическая химия АМИНОКИСЛОТЫ Наибольшее значение имеют α-аминокислоты , т. к. они являются метаболитами в обмене веществ и "строительным материалом" для важнейших биополимеров – полипептидов и белков
Фарм. Ф Органическая химия АМИНОКИСЛОТЫ Наибольшее значение имеют α-аминокислоты , т. к. они являются метаболитами в обмене веществ и "строительным материалом" для важнейших биополимеров – полипептидов и белков
 Фарм. Ф Органическая химия
Фарм. Ф Органическая химия
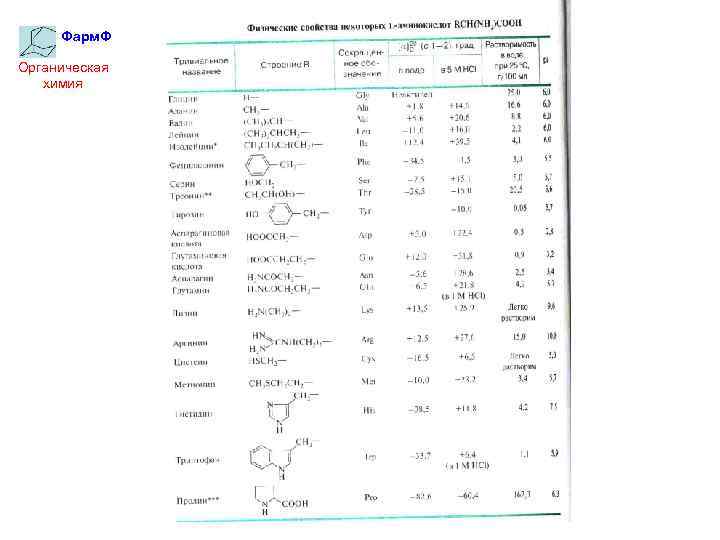
 Фарм. Ф Органическая химия ВЫУЧИТЬ! таблицу «Природные α-аминокислоты» Белобородов В. Л. , Зурабян С. Э. , Лузин А. П. , Тюкавкина Н. А. – Органическая химия (основной курс) – Дрофа, М. , 2003 г. , с. 584. Тюкавкина Н. А. , Бауков Ю. И. – Биоорганическая химия – ДРОФА, М. , 2007 г. , с. 317.
Фарм. Ф Органическая химия ВЫУЧИТЬ! таблицу «Природные α-аминокислоты» Белобородов В. Л. , Зурабян С. Э. , Лузин А. П. , Тюкавкина Н. А. – Органическая химия (основной курс) – Дрофа, М. , 2003 г. , с. 584. Тюкавкина Н. А. , Бауков Ю. И. – Биоорганическая химия – ДРОФА, М. , 2007 г. , с. 317.
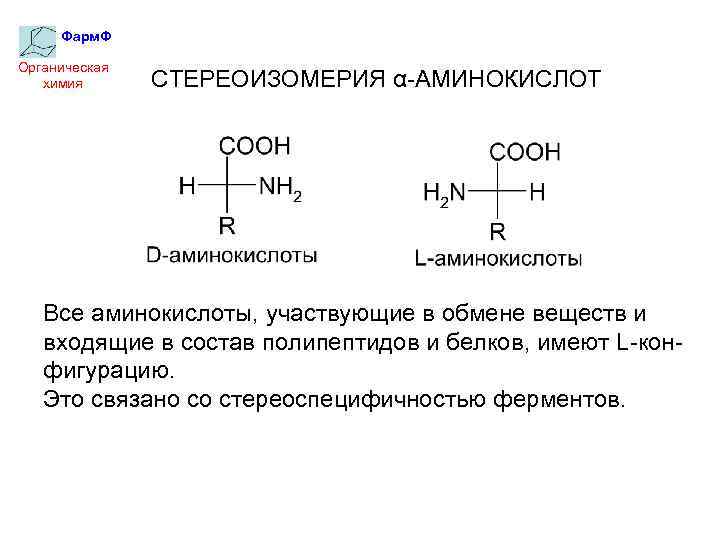 Фарм. Ф Органическая химия СТЕРЕОИЗОМЕРИЯ α-АМИНОКИСЛОТ Все аминокислоты, участвующие в обмене веществ и входящие в состав полипептидов и белков, имеют L-конфигурацию. Это связано со стереоспецифичностью ферментов.
Фарм. Ф Органическая химия СТЕРЕОИЗОМЕРИЯ α-АМИНОКИСЛОТ Все аминокислоты, участвующие в обмене веществ и входящие в состав полипептидов и белков, имеют L-конфигурацию. Это связано со стереоспецифичностью ферментов.
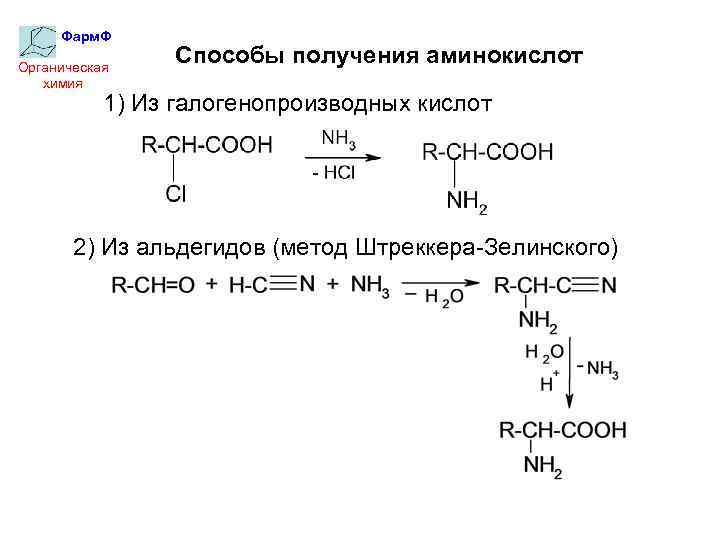 Фарм. Ф Органическая химия Способы получения аминокислот 1) Из галогенопроизводных кислот 2) Из альдегидов (метод Штреккера-Зелинского)
Фарм. Ф Органическая химия Способы получения аминокислот 1) Из галогенопроизводных кислот 2) Из альдегидов (метод Штреккера-Зелинского)
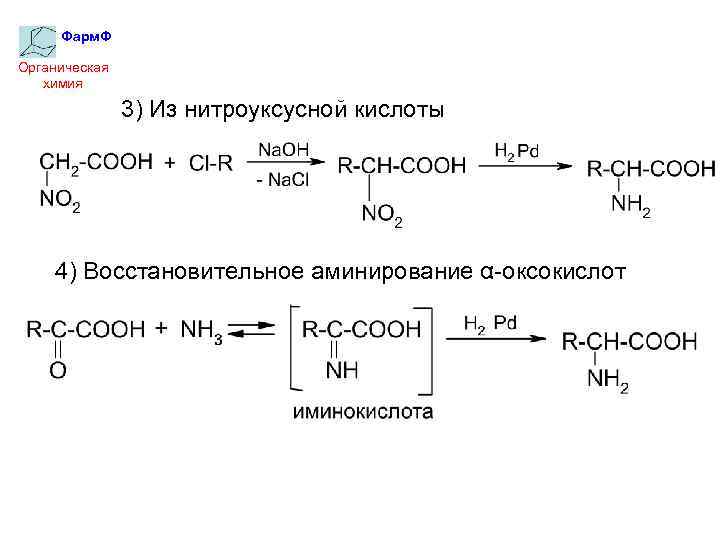 Фарм. Ф Органическая химия 3) Из нитроуксусной кислоты 4) Восстановительное аминирование α-оксокислот
Фарм. Ф Органическая химия 3) Из нитроуксусной кислоты 4) Восстановительное аминирование α-оксокислот
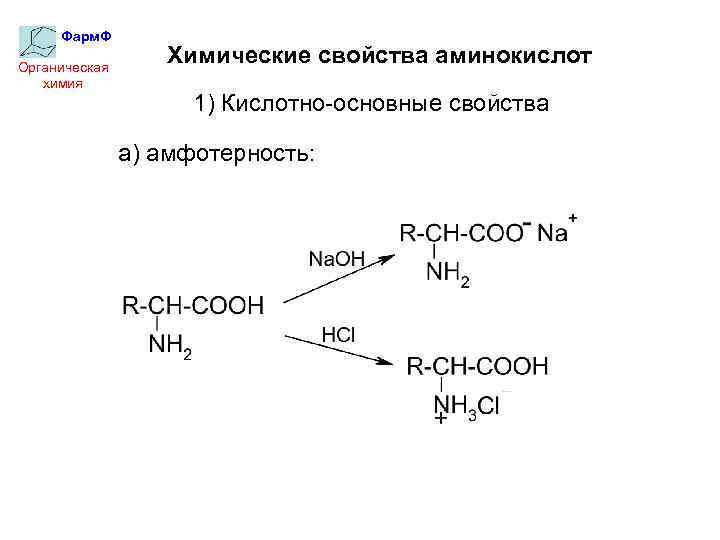 Фарм. Ф Органическая химия Химические свойства аминокислот 1) Кислотно-основные свойства а) амфотерность:
Фарм. Ф Органическая химия Химические свойства аминокислот 1) Кислотно-основные свойства а) амфотерность:
 Фарм. Ф Органическая химия б) образование биполярных ионов (цвиттер-ионов): Об этом свидетельствуют высокая полярность молекул аминокислот, их высокие температуры плавления и хорошая растворимость в воде.
Фарм. Ф Органическая химия б) образование биполярных ионов (цвиттер-ионов): Об этом свидетельствуют высокая полярность молекул аминокислот, их высокие температуры плавления и хорошая растворимость в воде.
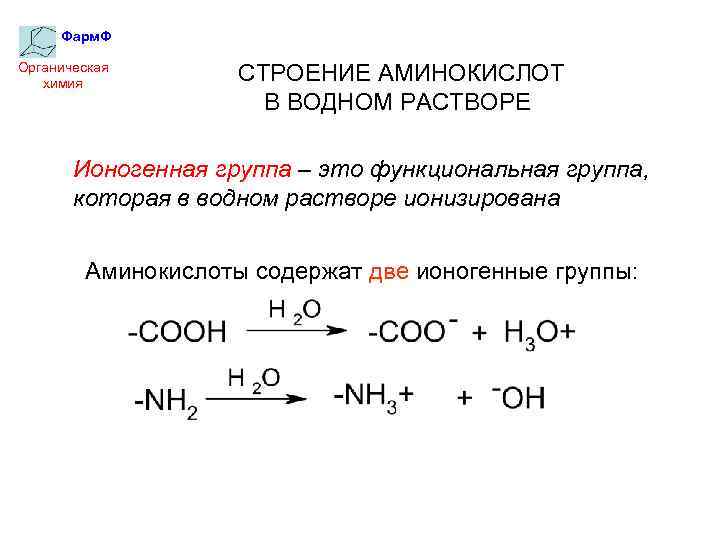 Фарм. Ф Органическая химия СТРОЕНИЕ АМИНОКИСЛОТ В ВОДНОМ РАСТВОРЕ Ионогенная группа – это функциональная группа, которая в водном растворе ионизирована Аминокислоты содержат две ионогенные группы:
Фарм. Ф Органическая химия СТРОЕНИЕ АМИНОКИСЛОТ В ВОДНОМ РАСТВОРЕ Ионогенная группа – это функциональная группа, которая в водном растворе ионизирована Аминокислоты содержат две ионогенные группы:
 Фарм. Ф Органическая химия В водном растворе молекулы аминокислот всегда имеют электрический заряд, изменяющийся при изменении р. Н раствора. Изоэлектрическая точка (ИЭТ, р. I) – это то значение р. Н, при котором суммарный заряд молекулы равен нулю. Различаются аминокислоты - нейтральные, - кислые, - основные.
Фарм. Ф Органическая химия В водном растворе молекулы аминокислот всегда имеют электрический заряд, изменяющийся при изменении р. Н раствора. Изоэлектрическая точка (ИЭТ, р. I) – это то значение р. Н, при котором суммарный заряд молекулы равен нулю. Различаются аминокислоты - нейтральные, - кислые, - основные.
 Фарм. Ф Органическая химия Нейтральные аминокислоты содержат 1 карбоксильную группу и 1 аминогруппу: Изоэлектрическая точка нейтральных аминокислот находится приблизительно в нейтральной точке р. Н.
Фарм. Ф Органическая химия Нейтральные аминокислоты содержат 1 карбоксильную группу и 1 аминогруппу: Изоэлектрическая точка нейтральных аминокислот находится приблизительно в нейтральной точке р. Н.
 Фарм. Ф Органическая химия Кислые аминокислоты содержат 2 карбоксильных группы и 1 аминогруппу: Изоэлектрическая точка кислых аминокислот находится в области кислотных значений р. Н.
Фарм. Ф Органическая химия Кислые аминокислоты содержат 2 карбоксильных группы и 1 аминогруппу: Изоэлектрическая точка кислых аминокислот находится в области кислотных значений р. Н.
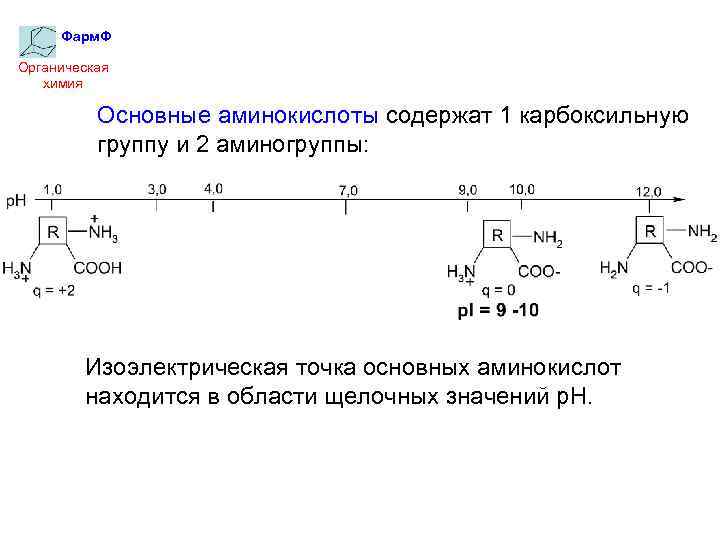 Фарм. Ф Органическая химия Основные аминокислоты содержат 1 карбоксильную группу и 2 аминогруппы: Изоэлектрическая точка основных аминокислот находится в области щелочных значений р. Н.
Фарм. Ф Органическая химия Основные аминокислоты содержат 1 карбоксильную группу и 2 аминогруппы: Изоэлектрическая точка основных аминокислот находится в области щелочных значений р. Н.
 Фарм. Ф Органическая химия Если р. Н раствора аминокислоты ниже ИЭТ, то её молекулы имеют положительный заряд, если р. Н раствора выше ИЭТ, то молекулы имеют отрицательный заряд.
Фарм. Ф Органическая химия Если р. Н раствора аминокислоты ниже ИЭТ, то её молекулы имеют положительный заряд, если р. Н раствора выше ИЭТ, то молекулы имеют отрицательный заряд.
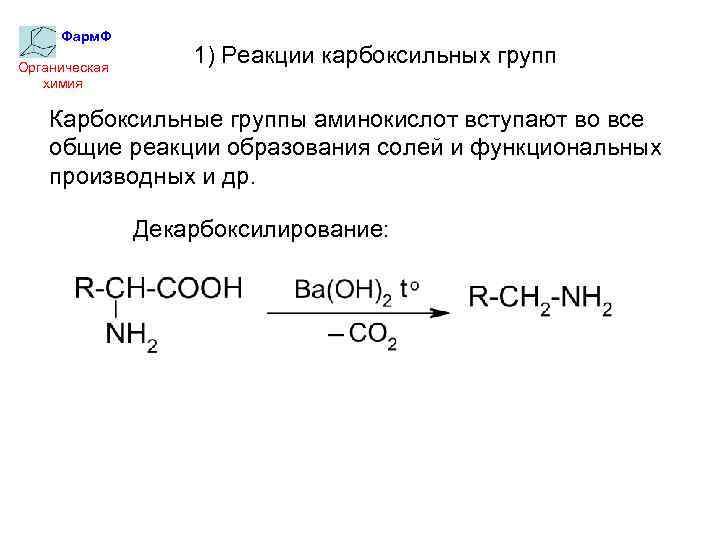 Фарм. Ф Органическая химия 1) Реакции карбоксильных групп Карбоксильные группы аминокислот вступают во все общие реакции образования солей и функциональных производных и др. Декарбоксилирование:
Фарм. Ф Органическая химия 1) Реакции карбоксильных групп Карбоксильные группы аминокислот вступают во все общие реакции образования солей и функциональных производных и др. Декарбоксилирование:
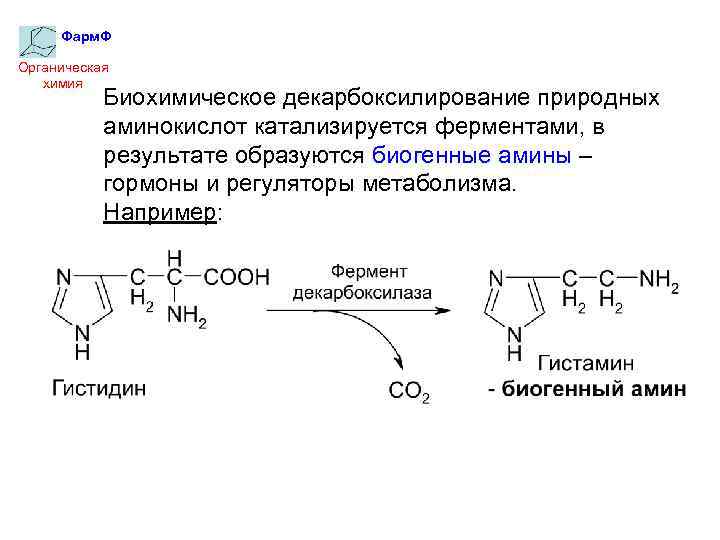 Фарм. Ф Органическая химия Биохимическое декарбоксилирование природных аминокислот катализируется ферментами, в результате образуются биогенные амины – гормоны и регуляторы метаболизма. Например:
Фарм. Ф Органическая химия Биохимическое декарбоксилирование природных аминокислот катализируется ферментами, в результате образуются биогенные амины – гормоны и регуляторы метаболизма. Например:
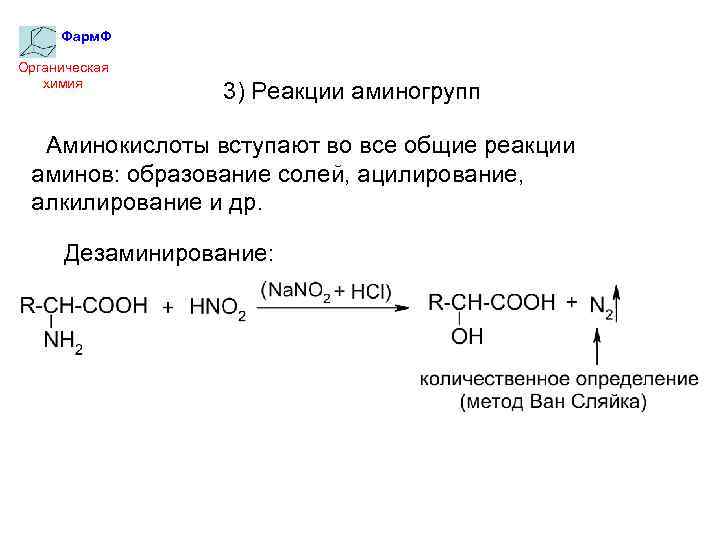 Фарм. Ф Органическая химия 3) Реакции аминогрупп Аминокислоты вступают во все общие реакции аминов: образование солей, ацилирование, алкилирование и др. Дезаминирование:
Фарм. Ф Органическая химия 3) Реакции аминогрупп Аминокислоты вступают во все общие реакции аминов: образование солей, ацилирование, алкилирование и др. Дезаминирование:
 Фарм. Ф Органическая химия Биологическое дезаминирование аминокислот начинается со стадии окислительного дегидрирования и заканчивается образованием кетокислоты – окислительное дезаминирование: Окислительное дезаминирование - основной путь выведения из организма избыточного азота.
Фарм. Ф Органическая химия Биологическое дезаминирование аминокислот начинается со стадии окислительного дегидрирования и заканчивается образованием кетокислоты – окислительное дезаминирование: Окислительное дезаминирование - основной путь выведения из организма избыточного азота.
 Фарм. Ф Органическая химия Биологическое значение и практическое применение аминокислот Наибольшее биологическое значение имеют α-аминокислоты. Они являются структурными компонентами полипептидов и белков, служат биологическими предшественниками биогенных аминов – гормонов и биорегуляторов.
Фарм. Ф Органическая химия Биологическое значение и практическое применение аминокислот Наибольшее биологическое значение имеют α-аминокислоты. Они являются структурными компонентами полипептидов и белков, служат биологическими предшественниками биогенных аминов – гормонов и биорегуляторов.
 Фарм. Ф Органическая химия Многие аминокислоты применяются как лекарственные препараты:
Фарм. Ф Органическая химия Многие аминокислоты применяются как лекарственные препараты:
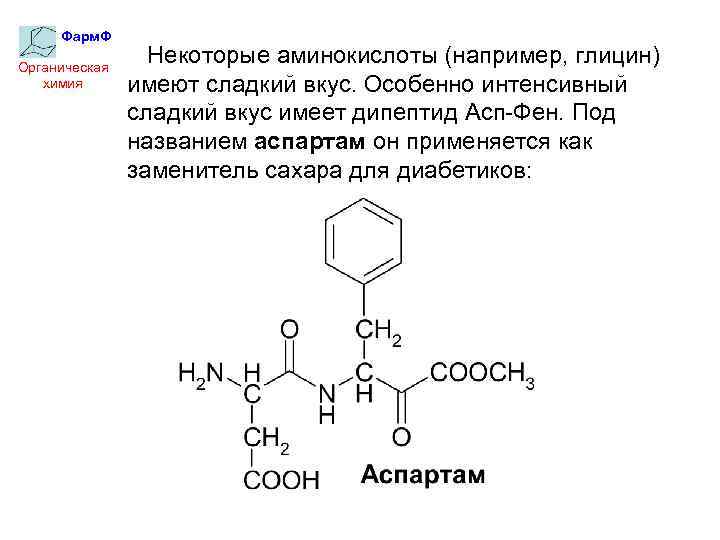 Фарм. Ф Органическая химия Некоторые аминокислоты (например, глицин) имеют сладкий вкус. Особенно интенсивный сладкий вкус имеет дипептид Асп-Фен. Под названием аспартам он применяется как заменитель сахара для диабетиков:
Фарм. Ф Органическая химия Некоторые аминокислоты (например, глицин) имеют сладкий вкус. Особенно интенсивный сладкий вкус имеет дипептид Асп-Фен. Под названием аспартам он применяется как заменитель сахара для диабетиков:
 Фарм. Ф Органическая химия ЛИТЕРАТУРА: Основная 1. Белобородов В. Л. , Зурабян С. Э. , Лузин А. П. , Тюкавкина Н. А. – Органическая химия (основной курс), кн. 1 – Дрофа, М. , 2003 г. , с. 558 -604. 1. Тюкавкина Н. А. , Зурабян С. Э. , Белобородов В. Л. и др. – Органическая химия (специальный курс), кн. 2 – Дрофа, М. , 2008 г. , с. 178 -207. Дополнительная 2. Н. А. Тюкавкина, Ю. И. Бауков – Биоорганическая химия – Дрофа, М. , 2007 г. , с. 316 -345. 04. 12. 10
Фарм. Ф Органическая химия ЛИТЕРАТУРА: Основная 1. Белобородов В. Л. , Зурабян С. Э. , Лузин А. П. , Тюкавкина Н. А. – Органическая химия (основной курс), кн. 1 – Дрофа, М. , 2003 г. , с. 558 -604. 1. Тюкавкина Н. А. , Зурабян С. Э. , Белобородов В. Л. и др. – Органическая химия (специальный курс), кн. 2 – Дрофа, М. , 2008 г. , с. 178 -207. Дополнительная 2. Н. А. Тюкавкина, Ю. И. Бауков – Биоорганическая химия – Дрофа, М. , 2007 г. , с. 316 -345. 04. 12. 10
 Фарм. Ф Органическая химия Выводы: 1) Если количества ионогенных групп (COOH и NH 2) в молекуле одинаковы, то изолектрическая точка вещества находится в области нейтрального р. Н (p. I = 7) - нейтральные аминокислоты. 2) Если в молекуле преобладают карбоксильные группы, то изолектрическая точка находится в кислотной области р. Н (p. I < 7) - кислые аминокислоты). 3) Если в молекуле преобладают аминогруппы, то изолектрическая точка находится в основной области р. Н (p. I > 7) - основные аминокислоты).
Фарм. Ф Органическая химия Выводы: 1) Если количества ионогенных групп (COOH и NH 2) в молекуле одинаковы, то изолектрическая точка вещества находится в области нейтрального р. Н (p. I = 7) - нейтральные аминокислоты. 2) Если в молекуле преобладают карбоксильные группы, то изолектрическая точка находится в кислотной области р. Н (p. I < 7) - кислые аминокислоты). 3) Если в молекуле преобладают аминогруппы, то изолектрическая точка находится в основной области р. Н (p. I > 7) - основные аминокислоты).


