16.Произв.мочевины.S-содер. соед.30.08.09.ppt
- Количество слайдов: 29
 Фарм. Ф Органическая химия Лекция 16 ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ И МОЧЕВИНЫ, СЕРОСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
Фарм. Ф Органическая химия Лекция 16 ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ И МОЧЕВИНЫ, СЕРОСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
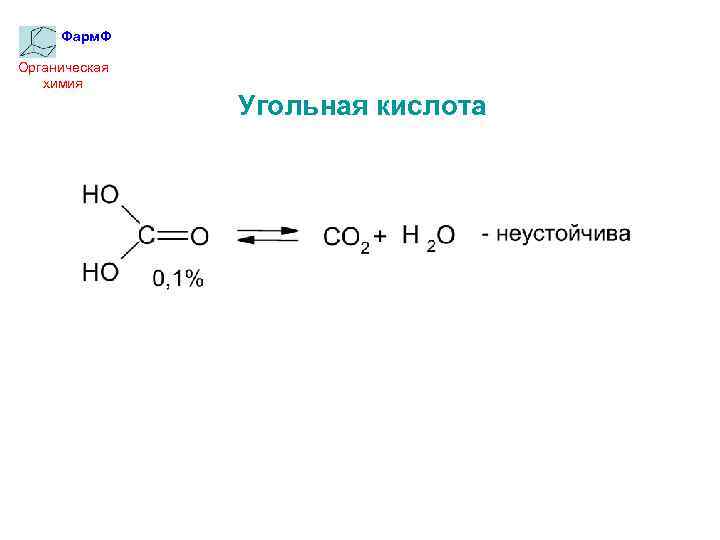 Фарм. Ф Органическая химия Угольная кислота
Фарм. Ф Органическая химия Угольная кислота
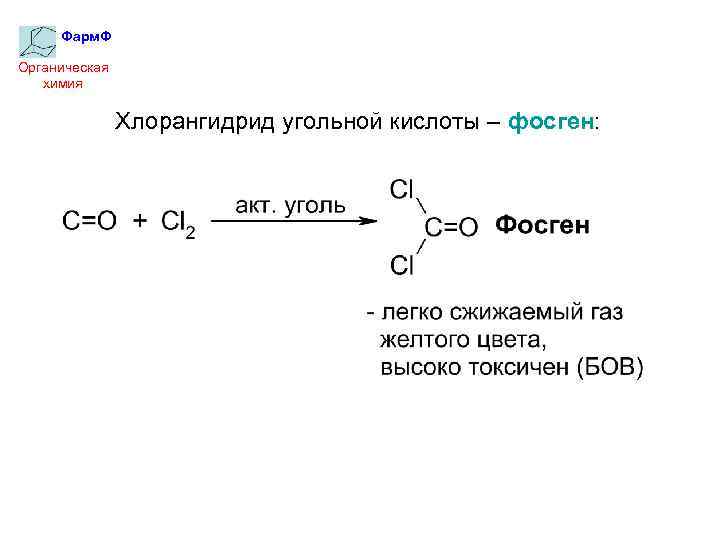 Фарм. Ф Органическая химия Хлорангидрид угольной кислоты – фосген:
Фарм. Ф Органическая химия Хлорангидрид угольной кислоты – фосген:
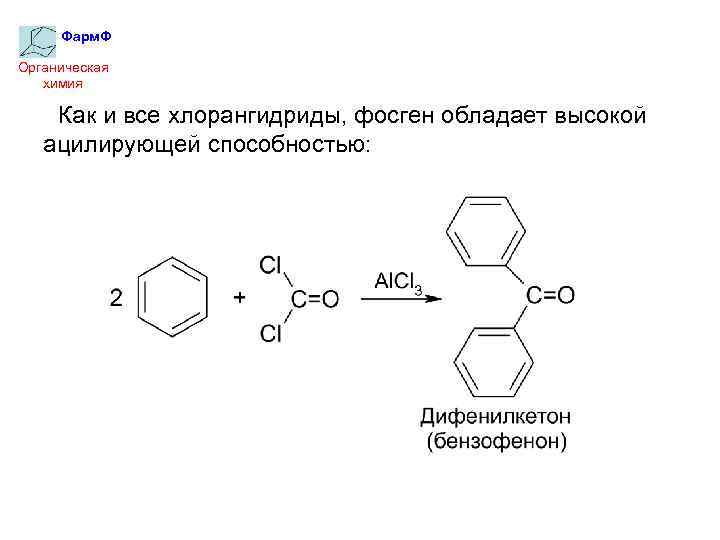 Фарм. Ф Органическая химия Как и все хлорангидриды, фосген обладает высокой ацилирующей способностью:
Фарм. Ф Органическая химия Как и все хлорангидриды, фосген обладает высокой ацилирующей способностью:
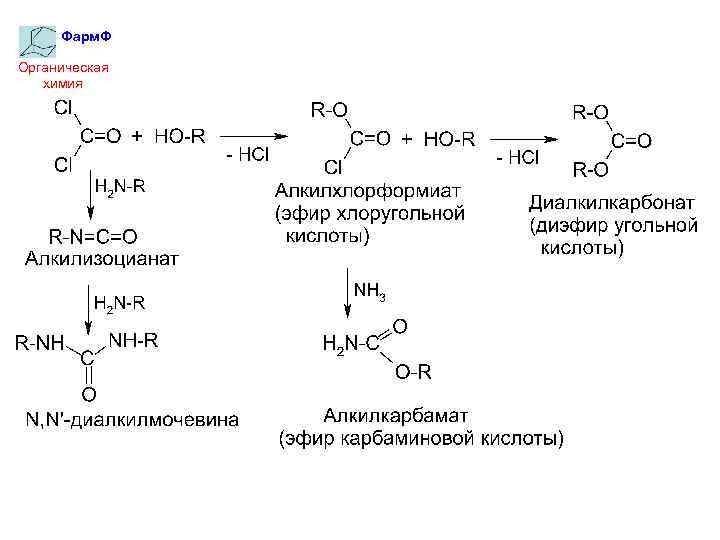 Фарм. Ф Органическая химия
Фарм. Ф Органическая химия
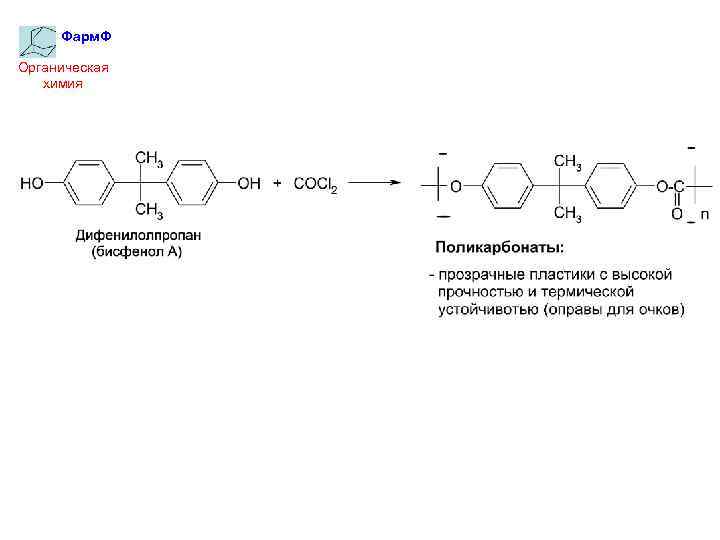 Фарм. Ф Органическая химия
Фарм. Ф Органическая химия
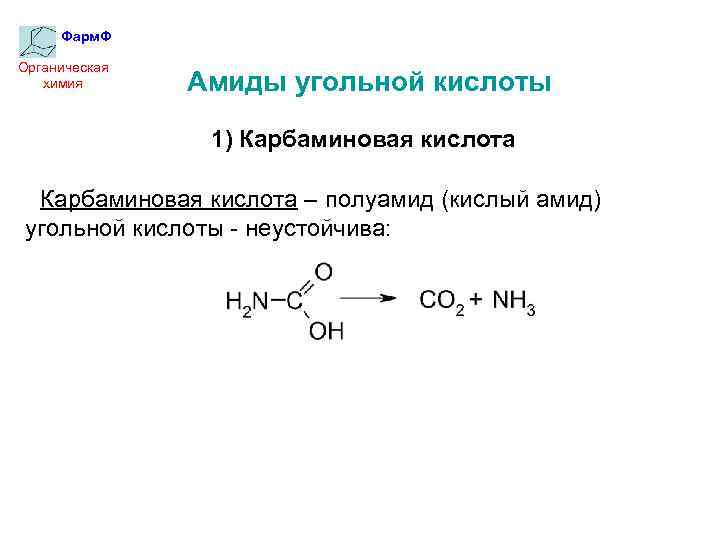 Фарм. Ф Органическая химия Амиды угольной кислоты 1) Карбаминовая кислота – полуамид (кислый амид) угольной кислоты - неустойчива:
Фарм. Ф Органическая химия Амиды угольной кислоты 1) Карбаминовая кислота – полуамид (кислый амид) угольной кислоты - неустойчива:
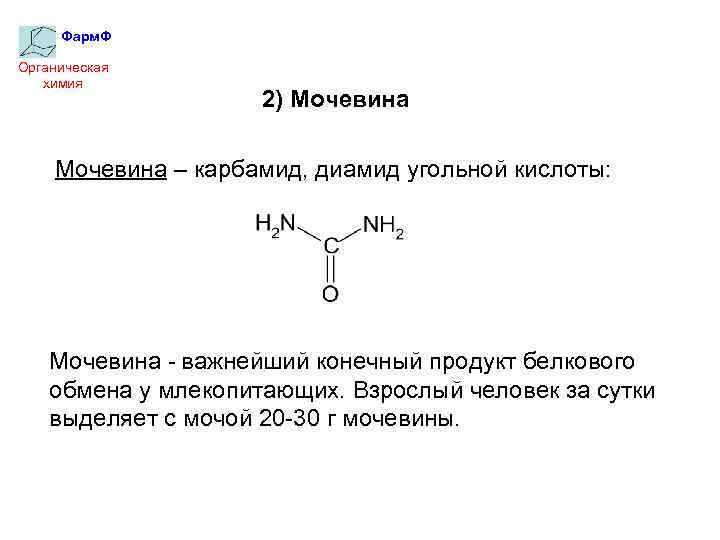 Фарм. Ф Органическая химия 2) Мочевина – карбамид, диамид угольной кислоты: Мочевина - важнейший конечный продукт белкового обмена у млекопитающих. Взрослый человек за сутки выделяет с мочой 20 -30 г мочевины.
Фарм. Ф Органическая химия 2) Мочевина – карбамид, диамид угольной кислоты: Мочевина - важнейший конечный продукт белкового обмена у млекопитающих. Взрослый человек за сутки выделяет с мочой 20 -30 г мочевины.
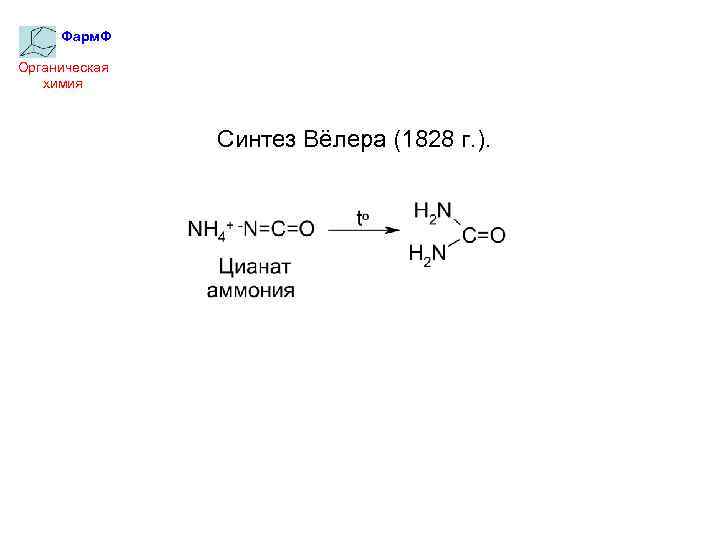 Фарм. Ф Органическая химия Синтез Вёлера (1828 г. ).
Фарм. Ф Органическая химия Синтез Вёлера (1828 г. ).
 Фарм. Ф Органическая химия Промышленный способ получения мочевины: Мочевина - многотоннажный продукт химической промышленности (мировое производство более 100 млн. тонн в год). Широко применяется как азотное удобрение и для получения мочевиноформальдегидных смол. В химико-фармацевтической промышленности используется для получения барбитуратов.
Фарм. Ф Органическая химия Промышленный способ получения мочевины: Мочевина - многотоннажный продукт химической промышленности (мировое производство более 100 млн. тонн в год). Широко применяется как азотное удобрение и для получения мочевиноформальдегидных смол. В химико-фармацевтической промышленности используется для получения барбитуратов.
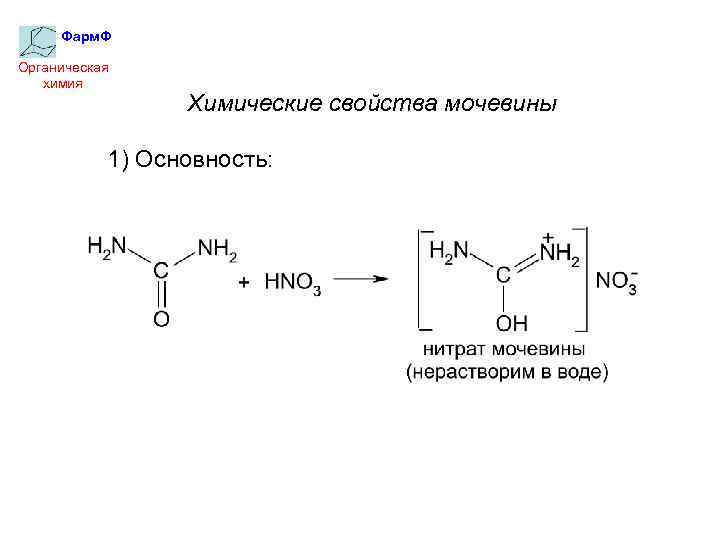 Фарм. Ф Органическая химия Химические свойства мочевины 1) Основность:
Фарм. Ф Органическая химия Химические свойства мочевины 1) Основность:
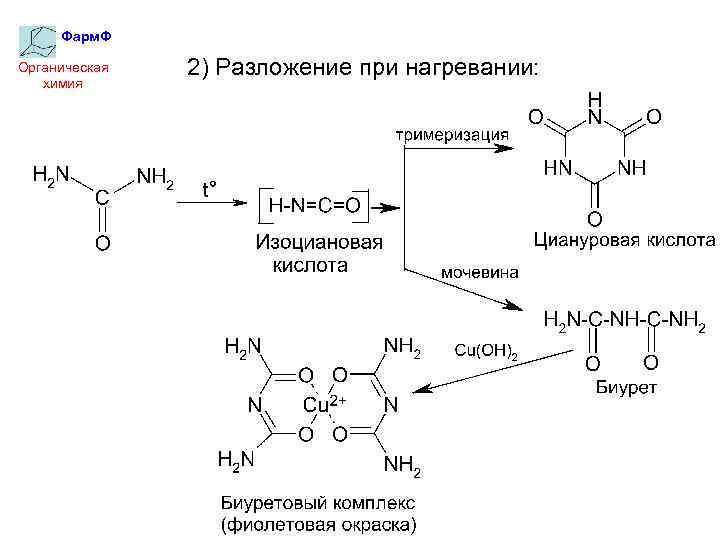 Фарм. Ф Органическая химия 2) Разложение при нагревании:
Фарм. Ф Органическая химия 2) Разложение при нагревании:
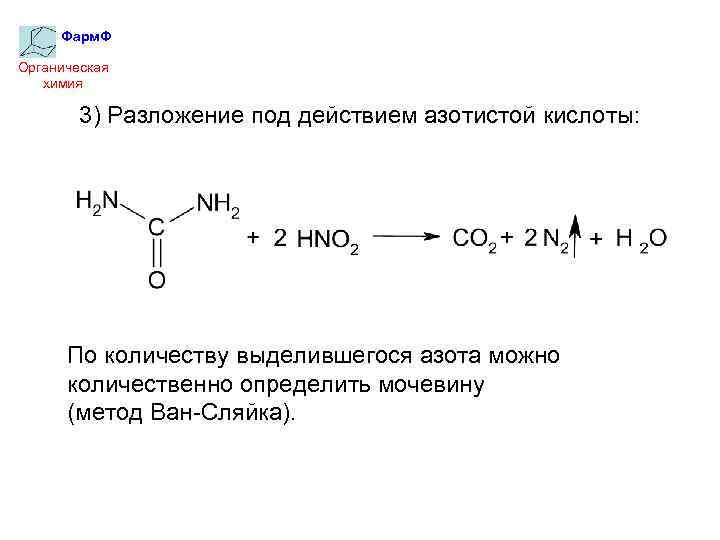 Фарм. Ф Органическая химия 3) Разложение под действием азотистой кислоты: По количеству выделившегося азота можно количественно определить мочевину (метод Ван-Сляйка).
Фарм. Ф Органическая химия 3) Разложение под действием азотистой кислоты: По количеству выделившегося азота можно количественно определить мочевину (метод Ван-Сляйка).
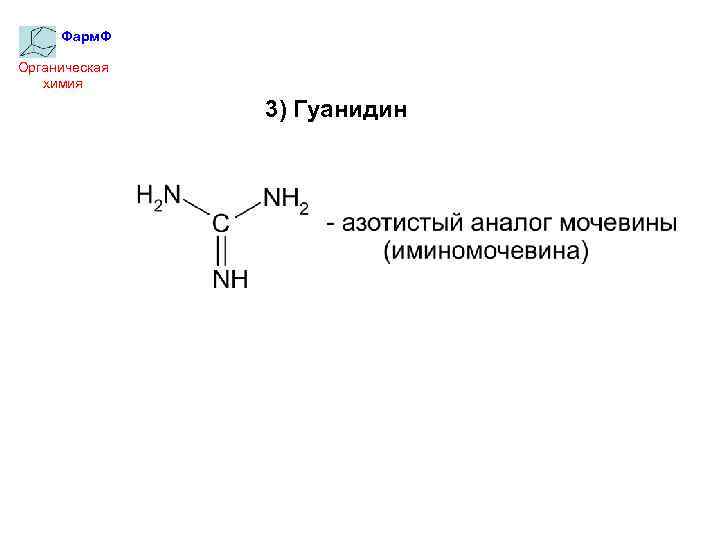 Фарм. Ф Органическая химия 3) Гуанидин
Фарм. Ф Органическая химия 3) Гуанидин
 Фарм. Ф Органическая химия Гуанидин обладает необычно высокой основностью, сравнимой с основностью неорганических щелочей. Это связано с высокой степенью структурной симметрии его протонированной формы и максимальной делокализацией (+)-заряда:
Фарм. Ф Органическая химия Гуанидин обладает необычно высокой основностью, сравнимой с основностью неорганических щелочей. Это связано с высокой степенью структурной симметрии его протонированной формы и максимальной делокализацией (+)-заряда:
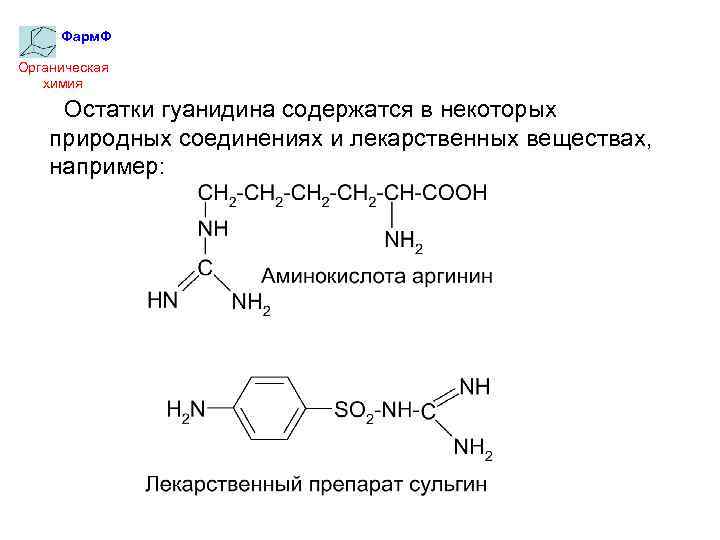 Фарм. Ф Органическая химия Остатки гуанидина содержатся в некоторых природных соединениях и лекарственных веществах, например:
Фарм. Ф Органическая химия Остатки гуанидина содержатся в некоторых природных соединениях и лекарственных веществах, например:
 Фарм. Ф Органическая химия СЕРОСОДЕРЖАЩИЕ СОЕДИНЕНИЯ Сера в составе органических соединений имеет различную степень окисления. Тиолы и тиоэфиры При замене галогена на SH-группу образуются тиолы:
Фарм. Ф Органическая химия СЕРОСОДЕРЖАЩИЕ СОЕДИНЕНИЯ Сера в составе органических соединений имеет различную степень окисления. Тиолы и тиоэфиры При замене галогена на SH-группу образуются тиолы:
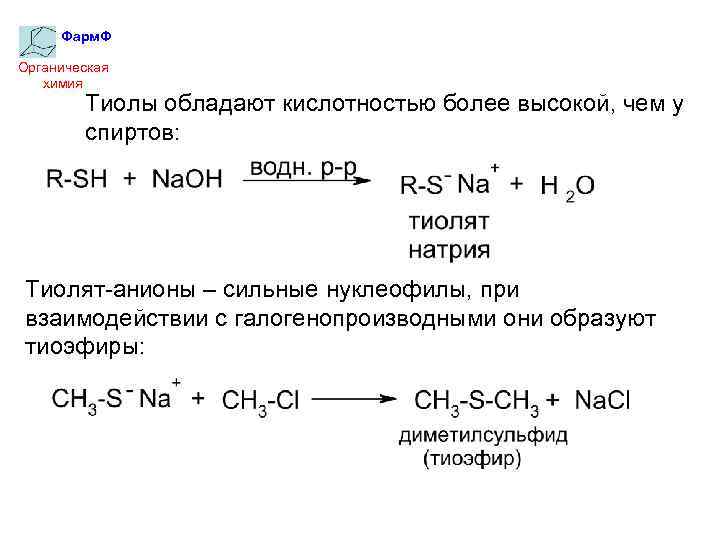 Фарм. Ф Органическая химия Тиолы обладают кислотностью более высокой, чем у спиртов: Тиолят-анионы – сильные нуклеофилы, при взаимодействии с галогенопроизводными они образуют тиоэфиры:
Фарм. Ф Органическая химия Тиолы обладают кислотностью более высокой, чем у спиртов: Тиолят-анионы – сильные нуклеофилы, при взаимодействии с галогенопроизводными они образуют тиоэфиры:
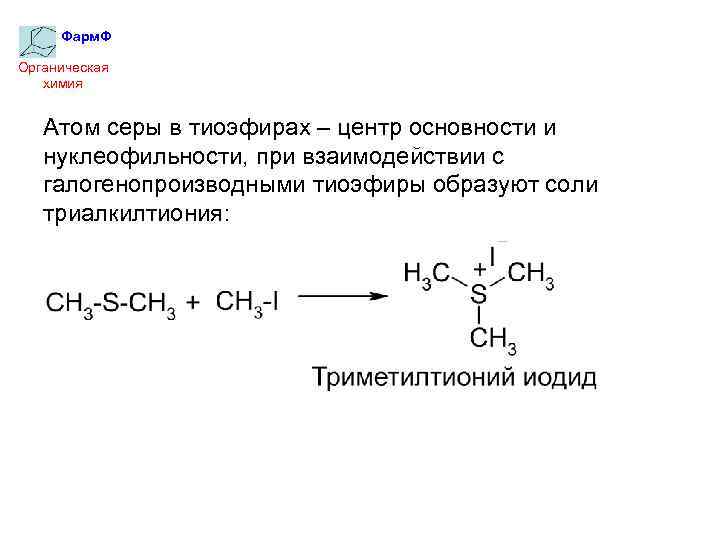 Фарм. Ф Органическая химия Атом серы в тиоэфирах – центр основности и нуклеофильности, при взаимодействии с галогенопроизводными тиоэфиры образуют соли триалкилтиония:
Фарм. Ф Органическая химия Атом серы в тиоэфирах – центр основности и нуклеофильности, при взаимодействии с галогенопроизводными тиоэфиры образуют соли триалкилтиония:
 Фарм. Ф Органическая химия Тиолы в мягких условиях легко окисляются, образуя дисульфиды: Направление реакции меняется при изменении ОВ-потенциала среды: при высоком ОВ-потенциале – вправо, при низком ОВ-потенциале – влево. Взаимопревращения "тиол-дисульфид" играют большую роль в формировании структуры и регулировании функций природных белков.
Фарм. Ф Органическая химия Тиолы в мягких условиях легко окисляются, образуя дисульфиды: Направление реакции меняется при изменении ОВ-потенциала среды: при высоком ОВ-потенциале – вправо, при низком ОВ-потенциале – влево. Взаимопревращения "тиол-дисульфид" играют большую роль в формировании структуры и регулировании функций природных белков.
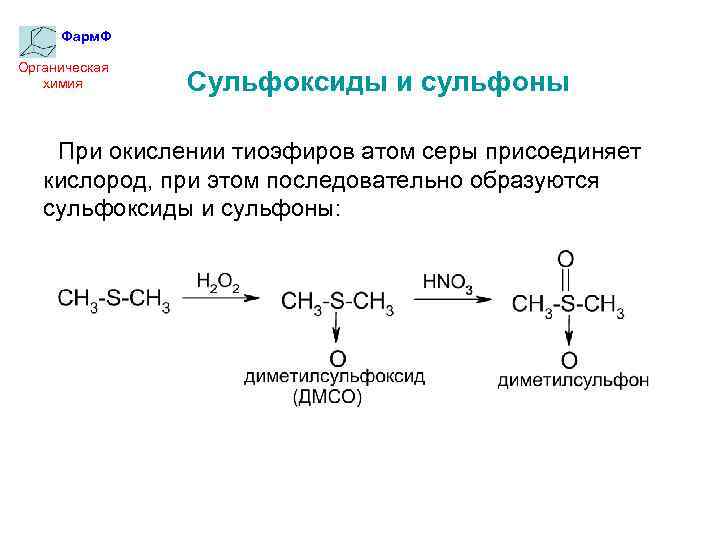 Фарм. Ф Органическая химия Сульфоксиды и сульфоны При окислении тиоэфиров атом серы присоединяет кислород, при этом последовательно образуются сульфоксиды и сульфоны:
Фарм. Ф Органическая химия Сульфоксиды и сульфоны При окислении тиоэфиров атом серы присоединяет кислород, при этом последовательно образуются сульфоксиды и сульфоны:
 Фарм. Ф Органическая химия Диметилсульфоксид (ДМСО, димексид) – бесцветная жидкость с т. кип. 189 о, растворим в воде и в органических растворителях. Широко применяется в органическом синтезе как полярный апротонный растворитель. Благодаря своей способности быстро диффундировать через кожу, пронося растворенные в нем вещества, используется в фармации как компонент лекарственных мазей.
Фарм. Ф Органическая химия Диметилсульфоксид (ДМСО, димексид) – бесцветная жидкость с т. кип. 189 о, растворим в воде и в органических растворителях. Широко применяется в органическом синтезе как полярный апротонный растворитель. Благодаря своей способности быстро диффундировать через кожу, пронося растворенные в нем вещества, используется в фармации как компонент лекарственных мазей.
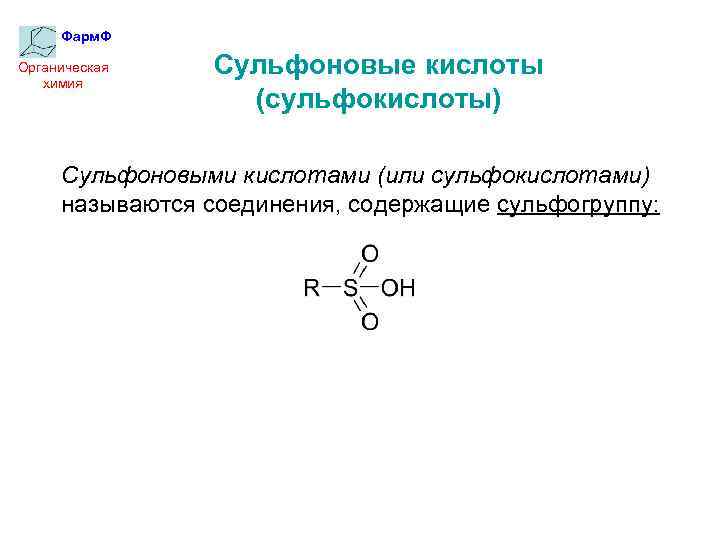 Фарм. Ф Органическая химия Сульфоновые кислоты (сульфокислоты) Сульфоновыми кислотами (или сульфокислотами) называются соединения, содержащие сульфогруппу:
Фарм. Ф Органическая химия Сульфоновые кислоты (сульфокислоты) Сульфоновыми кислотами (или сульфокислотами) называются соединения, содержащие сульфогруппу:
 Фарм. Ф Органическая химия Способы получения сульфокислот 1) Алифатические сульфокислоты 2) Ароматические сульфокислоты получаются сульфированием бензола и его производных (см. «Химические свойства аренов» )
Фарм. Ф Органическая химия Способы получения сульфокислот 1) Алифатические сульфокислоты 2) Ароматические сульфокислоты получаются сульфированием бензола и его производных (см. «Химические свойства аренов» )
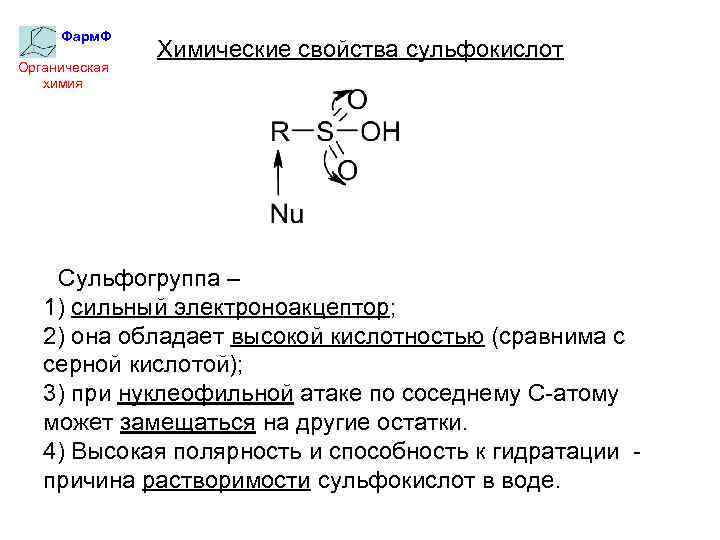 Фарм. Ф Органическая химия Химические свойства сульфокислот Сульфогруппа – 1) сильный электроноакцептор; 2) она обладает высокой кислотностью (сравнима с серной кислотой); 3) при нуклеофильной атаке по соседнему С-атому может замещаться на другие остатки. 4) Высокая полярность и способность к гидратации причина растворимости сульфокислот в воде.
Фарм. Ф Органическая химия Химические свойства сульфокислот Сульфогруппа – 1) сильный электроноакцептор; 2) она обладает высокой кислотностью (сравнима с серной кислотой); 3) при нуклеофильной атаке по соседнему С-атому может замещаться на другие остатки. 4) Высокая полярность и способность к гидратации причина растворимости сульфокислот в воде.
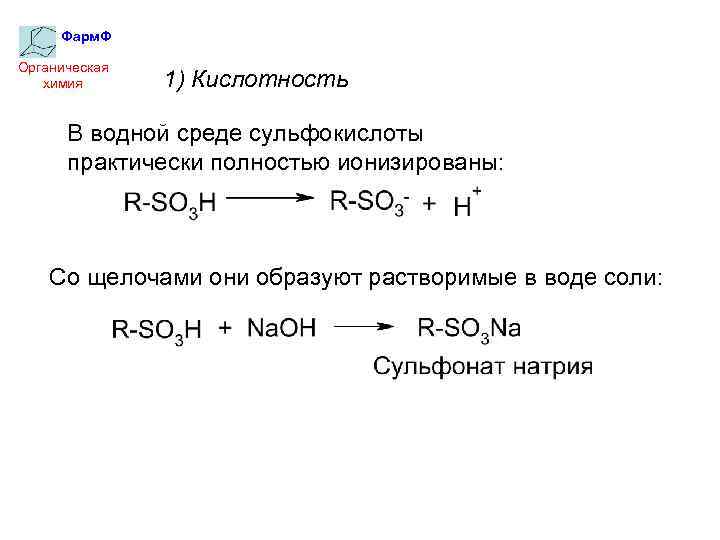 Фарм. Ф Органическая химия 1) Кислотность В водной среде сульфокислоты практически полностью ионизированы: Со щелочами они образуют растворимые в воде соли:
Фарм. Ф Органическая химия 1) Кислотность В водной среде сульфокислоты практически полностью ионизированы: Со щелочами они образуют растворимые в воде соли:
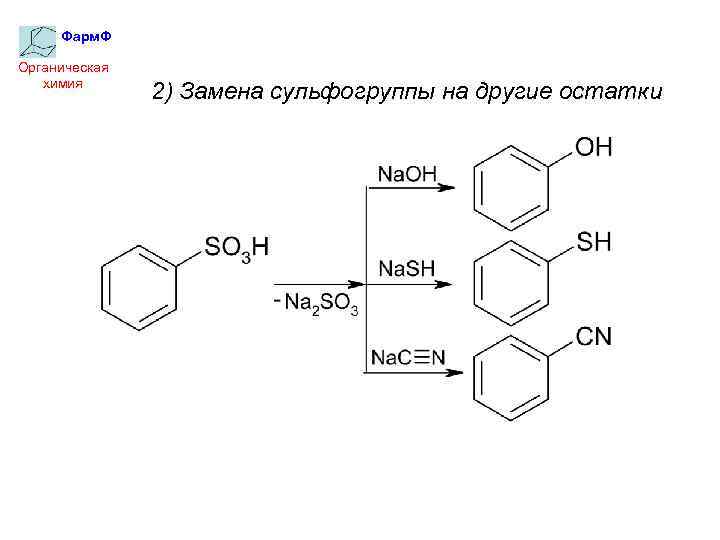 Фарм. Ф Органическая химия 2) Замена сульфогруппы на другие остатки
Фарм. Ф Органическая химия 2) Замена сульфогруппы на другие остатки
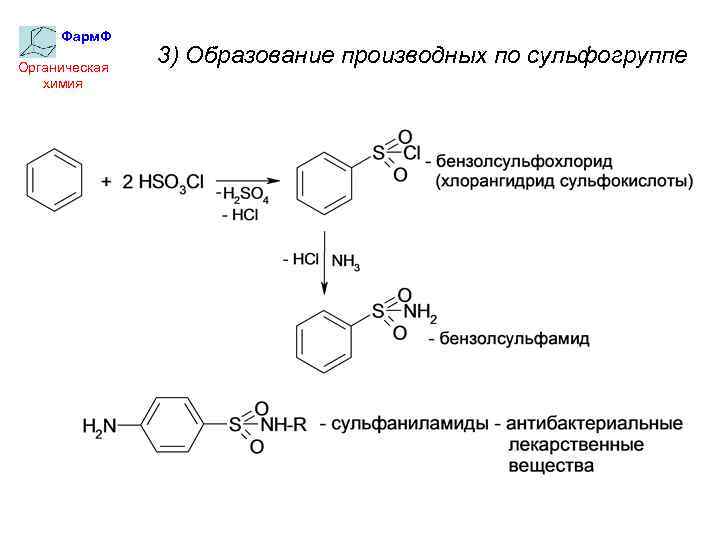 Фарм. Ф Органическая химия 3) Образование производных по сульфогруппе
Фарм. Ф Органическая химия 3) Образование производных по сульфогруппе
 Фарм. Ф Органическая химия Отдельные представители – см. учебник. ЛИТЕРАТУРА: 1. Белобородов В. Л. , Зурабян С. Э. , Лузин А. П. , Тюкавкина Н. А. – Органическая химия (основной курс) – ДРОФА, М. , 2003 г. , с. 408 – 419, 494 – 508. 30. 08. 09
Фарм. Ф Органическая химия Отдельные представители – см. учебник. ЛИТЕРАТУРА: 1. Белобородов В. Л. , Зурабян С. Э. , Лузин А. П. , Тюкавкина Н. А. – Органическая химия (основной курс) – ДРОФА, М. , 2003 г. , с. 408 – 419, 494 – 508. 30. 08. 09


