04.Кислотность и основность 11.08.09.ppt
- Количество слайдов: 36
 Фарм. Ф Лекция 4 Органическая химия КИСЛОТНОСТЬ И ОСНОВНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Фарм. Ф Лекция 4 Органическая химия КИСЛОТНОСТЬ И ОСНОВНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
 Фарм. Ф Органическая химия Кислотность и основность – важнейшие понятия, определяющие многие фундаментальные физикохимические свойства и биологическую активность органических соединений.
Фарм. Ф Органическая химия Кислотность и основность – важнейшие понятия, определяющие многие фундаментальные физикохимические свойства и биологическую активность органических соединений.
 Фарм. Ф Органическая химия Теории кислот и оснований: - теория электролитической диссоциации (Аррениус); - протолитическая теория (Бренстед-Лоури, 1923 г. ); - теория Льюиса (1925 г. ).
Фарм. Ф Органическая химия Теории кислот и оснований: - теория электролитической диссоциации (Аррениус); - протолитическая теория (Бренстед-Лоури, 1923 г. ); - теория Льюиса (1925 г. ).
 Фарм. Ф Органическая химия Протолитическая теории Бренстеда Кислота – это вещество, способное отдавать протон. Основание – это вещество, способное присоединять протон.
Фарм. Ф Органическая химия Протолитическая теории Бренстеда Кислота – это вещество, способное отдавать протон. Основание – это вещество, способное присоединять протон.
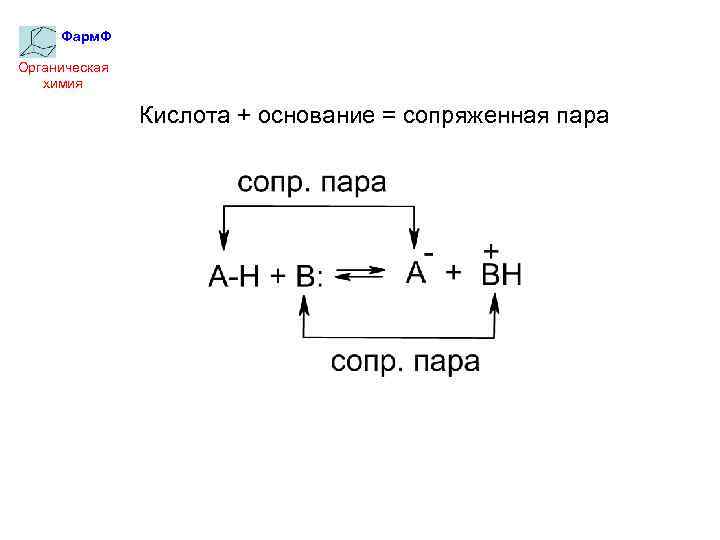 Фарм. Ф Органическая химия Кислота + основание = сопряженная пара
Фарм. Ф Органическая химия Кислота + основание = сопряженная пара
 Фарм. Ф Органическая химия Кислоты Атом, с которым связан протон, – центр кислотности. Центрами кислотности могут быть атомы C, O, N, S: Соответственно – CH-, OH-, NH- и SH-кислоты.
Фарм. Ф Органическая химия Кислоты Атом, с которым связан протон, – центр кислотности. Центрами кислотности могут быть атомы C, O, N, S: Соответственно – CH-, OH-, NH- и SH-кислоты.
 Фарм. Ф Органическая химия Основания Центрами основности являются атомы, имеющие неподеленную пару электронов (n-электроны): N, O, S. Соответственно различаются аммониевые, оксониевые и тиониевые основания (n-основания). Это могут быть нейтральные молекулы или анионы. Существуют также π-основания – соединения с кратными связями или сопряженной системой π-связей. Они присоединяют протон, образуя сопряженные кислоты – π-комплексы.
Фарм. Ф Органическая химия Основания Центрами основности являются атомы, имеющие неподеленную пару электронов (n-электроны): N, O, S. Соответственно различаются аммониевые, оксониевые и тиониевые основания (n-основания). Это могут быть нейтральные молекулы или анионы. Существуют также π-основания – соединения с кратными связями или сопряженной системой π-связей. Они присоединяют протон, образуя сопряженные кислоты – π-комплексы.
 Фарм. Ф Органическая химия Количественная оценка кислотности Сила кислоты – это степень сдвига вправо следующего равновесия:
Фарм. Ф Органическая химия Количественная оценка кислотности Сила кислоты – это степень сдвига вправо следующего равновесия:
 Фарм. Ф Органическая химия Количественной мерой кислотности являются: Ка – константа кислотности р. Ка = -lg. Ka – показатель кислотности сила кислоты↑ → Ка↑ → р. Ка↓
Фарм. Ф Органическая химия Количественной мерой кислотности являются: Ка – константа кислотности р. Ка = -lg. Ka – показатель кислотности сила кислоты↑ → Ка↑ → р. Ка↓
 Фарм. Ф Органическая химия Количественная оценка основности Сила основания – это степень сдвига вправо следующего равновесия:
Фарм. Ф Органическая химия Количественная оценка основности Сила основания – это степень сдвига вправо следующего равновесия:
 Фарм. Ф Органическая химия Из этих соотношений следует, что для сопряженной пары мерой основности основания В может быть кислотность сопряженной кислоты ВН+: р. КВ = 14 – р. КВН+ Сила основания↑ → КВ↑ → р. КВ↓ → р. КВН+↑
Фарм. Ф Органическая химия Из этих соотношений следует, что для сопряженной пары мерой основности основания В может быть кислотность сопряженной кислоты ВН+: р. КВ = 14 – р. КВН+ Сила основания↑ → КВ↑ → р. КВ↓ → р. КВН+↑
 Фарм. Ф Органическая химия Качественная оценка кислотности Сила кислоты определяется устойчивостью сопряженного основания (аниона). Чем стабильнее анион, тем сильнее кислота.
Фарм. Ф Органическая химия Качественная оценка кислотности Сила кислоты определяется устойчивостью сопряженного основания (аниона). Чем стабильнее анион, тем сильнее кислота.
 Фарм. Ф Органическая химия Устойчивость аниона, в свою очередь, зависит от следующих факторов: - свойства атома в центре кислотности – его электроотрицательность и поляризуемость; - степень делокализации (-)-заряда в анионе в результате сопряжения; - действие окружающих заместителей; - способность аниона к сольватации.
Фарм. Ф Органическая химия Устойчивость аниона, в свою очередь, зависит от следующих факторов: - свойства атома в центре кислотности – его электроотрицательность и поляризуемость; - степень делокализации (-)-заряда в анионе в результате сопряжения; - действие окружающих заместителей; - способность аниона к сольватации.
 Фарм. Ф Органическая химия Факторы, определяющие кислотность 1. Свойства атома в центре кислотности а) электроотрицательность С увеличением электроотрицательности атома Х полярность связи Х-Н увеличивается, прочность её уменьшается, облегчается отрыв протона. В результате кислотность увеличивается. ЭО↑ → Кислотность↑
Фарм. Ф Органическая химия Факторы, определяющие кислотность 1. Свойства атома в центре кислотности а) электроотрицательность С увеличением электроотрицательности атома Х полярность связи Х-Н увеличивается, прочность её уменьшается, облегчается отрыв протона. В результате кислотность увеличивается. ЭО↑ → Кислотность↑
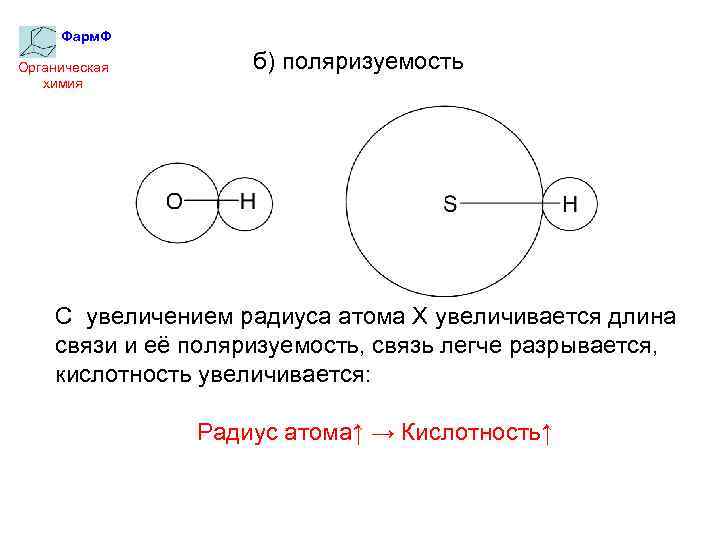 Фарм. Ф Органическая химия б) поляризуемость С увеличением радиуса атома Х увеличивается длина связи и её поляризуемость, связь легче разрывается, кислотность увеличивается: Радиус атома↑ → Кислотность↑
Фарм. Ф Органическая химия б) поляризуемость С увеличением радиуса атома Х увеличивается длина связи и её поляризуемость, связь легче разрывается, кислотность увеличивается: Радиус атома↑ → Кислотность↑
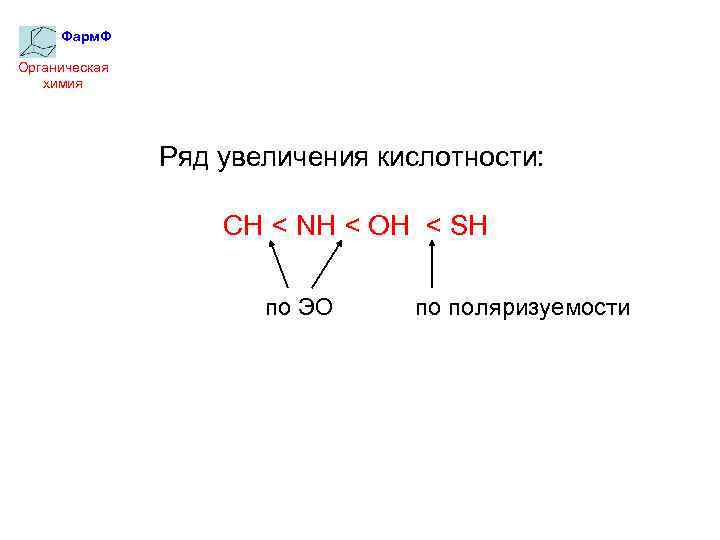 Фарм. Ф Органическая химия Ряд увеличения кислотности: CH < NH < OH < SH по ЭО по поляризуемости
Фарм. Ф Органическая химия Ряд увеличения кислотности: CH < NH < OH < SH по ЭО по поляризуемости
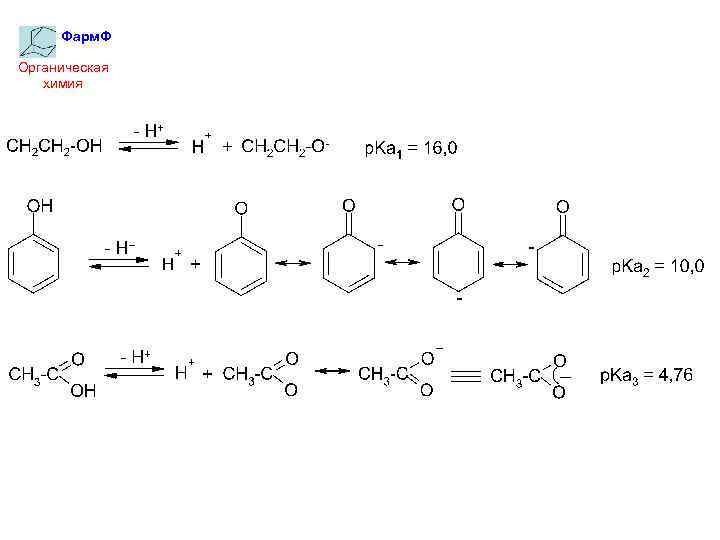
 Фарм. Ф Органическая химия 2. Делокализация заряда по сопряженной системе увеличивает стабильность аниона и соответственно увеличивает кислотность.
Фарм. Ф Органическая химия 2. Делокализация заряда по сопряженной системе увеличивает стабильность аниона и соответственно увеличивает кислотность.
 Фарм. Ф Органическая химия
Фарм. Ф Органическая химия
 Фарм. Ф Органическая химия 2. Влияние заместителей а) электроноакцепторы Электроноакцепторы способствуют делокализации заряда в анионе, увеличивают его устойчивость и, следовательно, увеличивают кислотность.
Фарм. Ф Органическая химия 2. Влияние заместителей а) электроноакцепторы Электроноакцепторы способствуют делокализации заряда в анионе, увеличивают его устойчивость и, следовательно, увеличивают кислотность.
 Фарм. Ф Органическая химия б) электронодоноры Электронодоноры препятствуют делокализации заряда в анионе, уменьшают его устойчивость и, следовательно, уменьшают кислотность.
Фарм. Ф Органическая химия б) электронодоноры Электронодоноры препятствуют делокализации заряда в анионе, уменьшают его устойчивость и, следовательно, уменьшают кислотность.
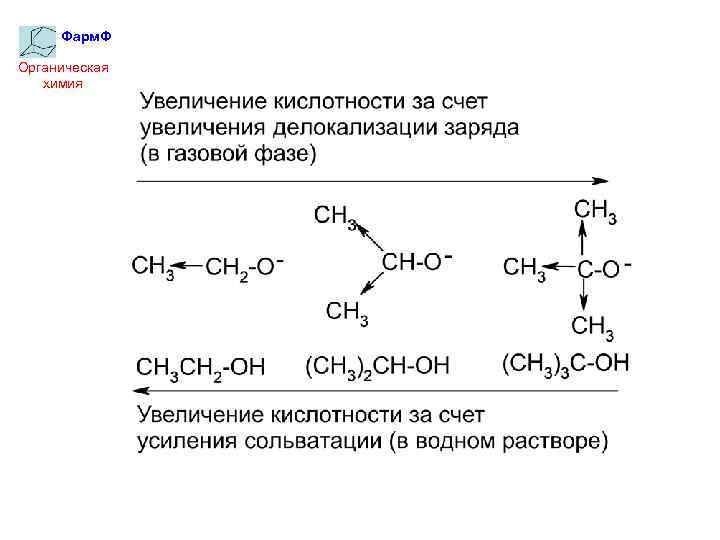
 Фарм. Ф Органическая химия 3. Эффект сольватации Сольватация образующего аниона способствует его устойчивости и увеличивает кислотность. (!) Чем меньше размер иона и чем больше в нем локализован заряд, тем легче он сольватируется.
Фарм. Ф Органическая химия 3. Эффект сольватации Сольватация образующего аниона способствует его устойчивости и увеличивает кислотность. (!) Чем меньше размер иона и чем больше в нем локализован заряд, тем легче он сольватируется.
 Фарм. Ф Органическая химия
Фарм. Ф Органическая химия
 Фарм. Ф Органическая химия Качественная оценка основности Наиболее сильные основания – анионы:
Фарм. Ф Органическая химия Качественная оценка основности Наиболее сильные основания – анионы:
 Фарм. Ф Органическая химия Нейтральные молекулы в реакциях с кислотами образуют ониевые соли:
Фарм. Ф Органическая химия Нейтральные молекулы в реакциях с кислотами образуют ониевые соли:
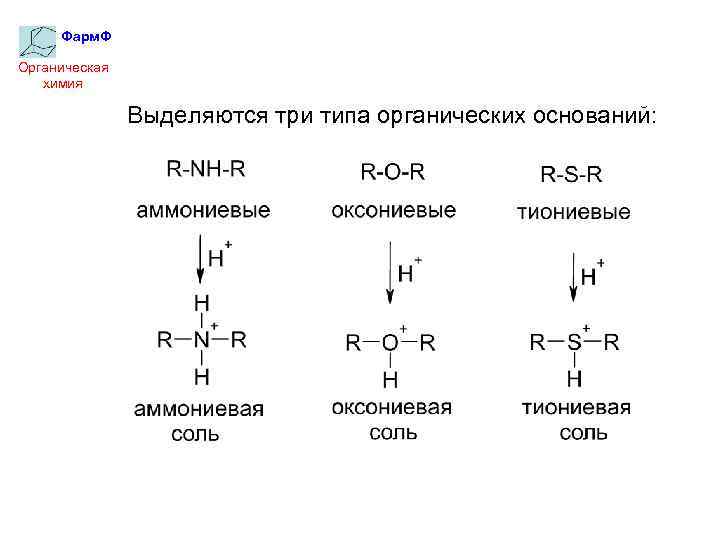 Фарм. Ф Органическая химия Выделяются три типа органических оснований:
Фарм. Ф Органическая химия Выделяются три типа органических оснований:
 Фарм. Ф Органическая химия Сила основания определяется стабильностью образующегося катиона, а также доступностью неподеленной пары электронов для присоединения протона. На силу основания влияют те же факторы, что и на силу кислоты, но направление действие их противоположно.
Фарм. Ф Органическая химия Сила основания определяется стабильностью образующегося катиона, а также доступностью неподеленной пары электронов для присоединения протона. На силу основания влияют те же факторы, что и на силу кислоты, но направление действие их противоположно.
 Фарм. Ф Органическая химия Амины – наиболее сильные основания. Они образуют с кислотами устойчивые соли растворимые в воде. Это свойство аминов широко применяется для их выделения и очистки, а также для получения растворимых лекарственных форм.
Фарм. Ф Органическая химия Амины – наиболее сильные основания. Они образуют с кислотами устойчивые соли растворимые в воде. Это свойство аминов широко применяется для их выделения и очистки, а также для получения растворимых лекарственных форм.
 Фарм. Ф Органическая химия Ряд уменьшения основности: R-NH-R > R-O-R > R-S-R - основность оксониевых оснований уменьшается за счет большей ЭО кислорода; - тиониевые основания более слабые, чем оксониевые потому, что больший радиус серы увеличивает длину связи S-H в катионе, делает её менее прочной и тем самым снижает устойчивость катиона.
Фарм. Ф Органическая химия Ряд уменьшения основности: R-NH-R > R-O-R > R-S-R - основность оксониевых оснований уменьшается за счет большей ЭО кислорода; - тиониевые основания более слабые, чем оксониевые потому, что больший радиус серы увеличивает длину связи S-H в катионе, делает её менее прочной и тем самым снижает устойчивость катиона.
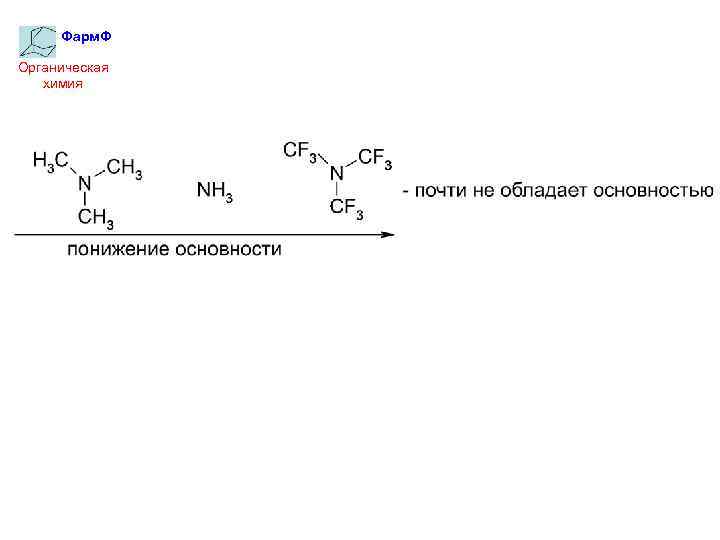
 Фарм. Ф Органическая химия На силу оснований большое влияние оказывают заместители у центра основности: а) электроноакцепторы Электроноакцепторы увеличивают (+)-заряд на катионе, уменьшают его устойчивость и, следовательно, уменьшают основность.
Фарм. Ф Органическая химия На силу оснований большое влияние оказывают заместители у центра основности: а) электроноакцепторы Электроноакцепторы увеличивают (+)-заряд на катионе, уменьшают его устойчивость и, следовательно, уменьшают основность.
 Фарм. Ф Органическая химия б) электронодоноры Электронодоноры уменьшают (+)-заряд на катионе, увеличивают его устойчивость и, следовательно, увеличивают основность.
Фарм. Ф Органическая химия б) электронодоноры Электронодоноры уменьшают (+)-заряд на катионе, увеличивают его устойчивость и, следовательно, увеличивают основность.
 Фарм. Ф Органическая химия
Фарм. Ф Органическая химия
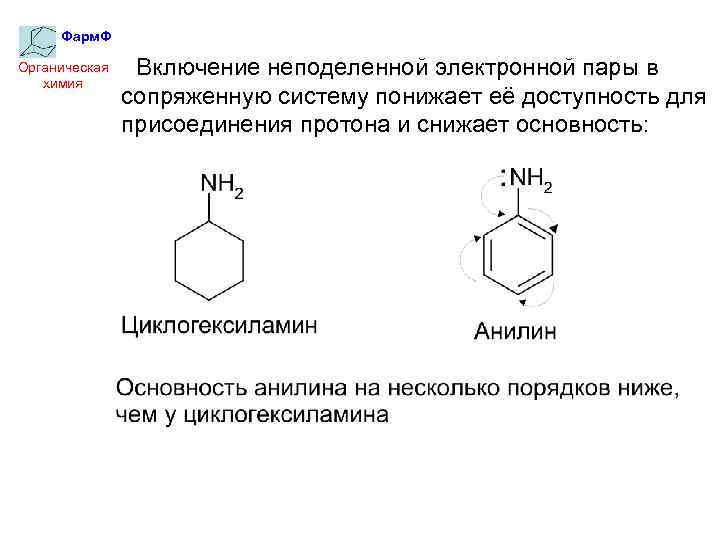 Фарм. Ф Органическая химия Включение неподеленной электронной пары в сопряженную систему понижает её доступность для присоединения протона и снижает основность:
Фарм. Ф Органическая химия Включение неподеленной электронной пары в сопряженную систему понижает её доступность для присоединения протона и снижает основность:
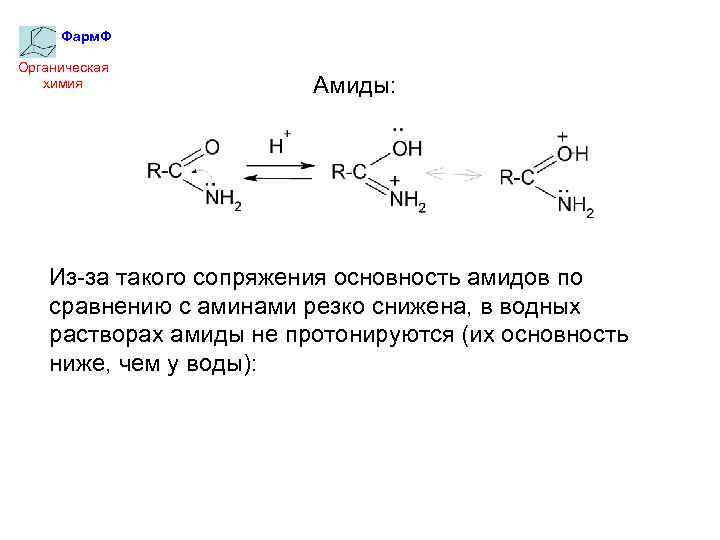 Фарм. Ф Органическая химия Амиды: Из-за такого сопряжения основность амидов по сравнению с аминами резко снижена, в водных растворах амиды не протонируются (их основность ниже, чем у воды):
Фарм. Ф Органическая химия Амиды: Из-за такого сопряжения основность амидов по сравнению с аминами резко снижена, в водных растворах амиды не протонируются (их основность ниже, чем у воды):
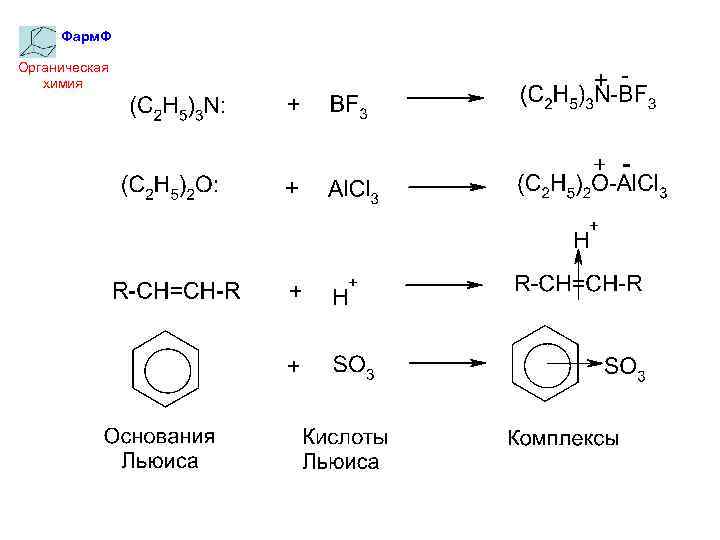
 Фарм. Ф Органическая химия Теория кислот и оснований Льюиса Кислота – акцептор электронов; Основание – донор электронов При взаимодействии кислот и оснований образуются донорно-акцепторные комплексы:
Фарм. Ф Органическая химия Теория кислот и оснований Льюиса Кислота – акцептор электронов; Основание – донор электронов При взаимодействии кислот и оснований образуются донорно-акцепторные комплексы:
 Фарм. Ф Органическая химия
Фарм. Ф Органическая химия
 Фарм. Ф Органическая химия ЛИТЕРАТУРА: Основная 1. Белобородов В. Л. , Зурабян С. Э. , Лузин А. П. , Тюкавкина Н. А. – Органическая химия (основной курс) – Дрофа, М. , 2003 г. , с. 138 – 157. Дополнительная 1. Н. А. Тюкавкина, Ю. И. Бауков – Биоорганическая химия – ДРОФА, М. , 2007 г. , с. 100 -111. 08. 09
Фарм. Ф Органическая химия ЛИТЕРАТУРА: Основная 1. Белобородов В. Л. , Зурабян С. Э. , Лузин А. П. , Тюкавкина Н. А. – Органическая химия (основной курс) – Дрофа, М. , 2003 г. , с. 138 – 157. Дополнительная 1. Н. А. Тюкавкина, Ю. И. Бауков – Биоорганическая химия – ДРОФА, М. , 2007 г. , с. 100 -111. 08. 09


