18.Полипептиды, белки 06.09.09.ppt
- Количество слайдов: 25

Фарм. Ф Лекция 18 Органическая химия ПОЛИПЕПТИДЫ, БЕЛКИ

Фарм. Ф Органическая химия "Жизнь – это форма существования белковых тел" (Ф. Энгельс) Полипептиды и белки – основные вещества живого организма. Их роль в обмене веществ уникальна, они выполняют все основные функции метаболизма: 1) Белки – пластический материал тканей. 2) Белки – один из трех видов питательных веществ, необходимых организму. 3) Белковые структуры являются ключевыми в составе ферментов – биохимических катализаторов, "двигателей" метаболизма.

Фарм. Ф Органическая химия 4) Белки играют ключевую роль в иммунитете – системе самозащиты организма от чужеродных веществ 5) Гормоны и вещества, регулирующие пути биохимических превращений – это в основном, полипептиды и белки. 6) Тканевые рецепторы гормонов, биорегуляторов и лекарственных веществ также представляют собой белковые структуры.

Фарм. Ф Органическая химия По химическому строению Полипептиды и белки – это биополимеры, состоящие из остатков аминокислот, связанных между собой пептидными связями. Считается, что полипептиды – это полимеры, содержащие до 100 аминокислотных остатков, более 100 остатков – это белки. Особо выделяются олигопептиды – до 10 аминокислотных остатков.

Фарм. Ф Органическая химия У белков существует иерархия структур: 1) первичная, 2) вторичная, 3) третичная, 4) четвертичная структуры
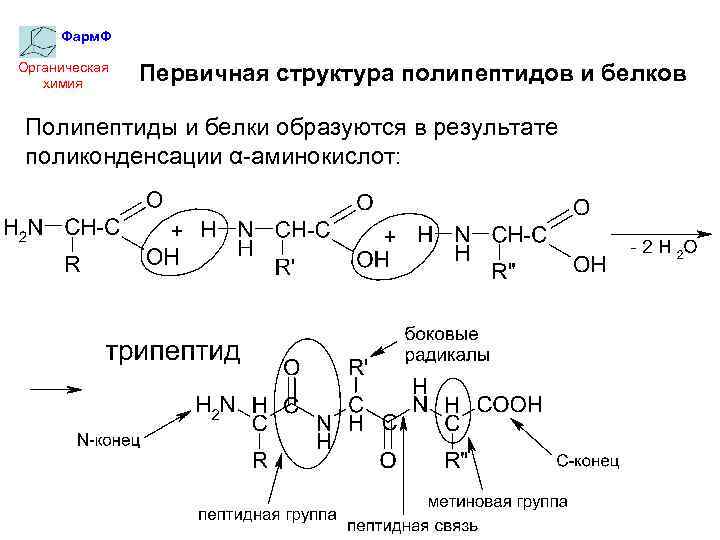
Фарм. Ф Органическая химия Первичная структура полипептидов и белков Полипептиды и белки образуются в результате поликонденсации α-аминокислот:
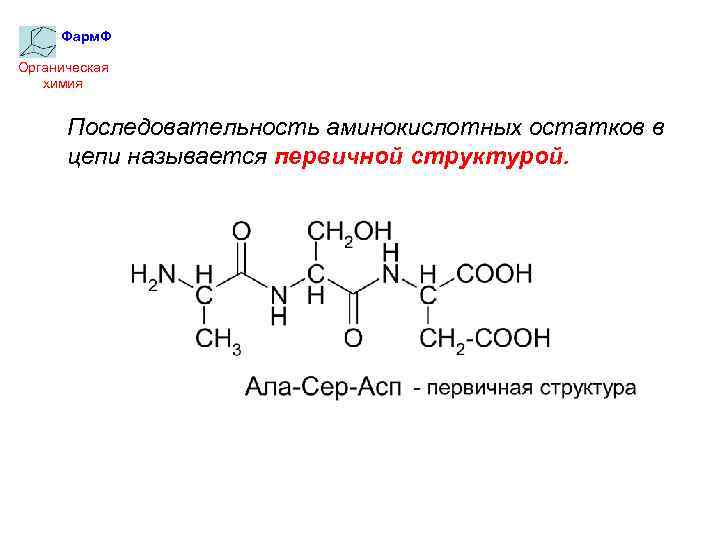
Фарм. Ф Органическая химия Последовательность аминокислотных остатков в цепи называется первичной структурой.
Фарм. Ф Органическая химия Пространственное строение белков и полипептидов Высокомолекулярные полипептиды и белки кроме первичной структуры имеют более высокие уровни пространственной организации: вторичную, третичную и четвертичную структуры.
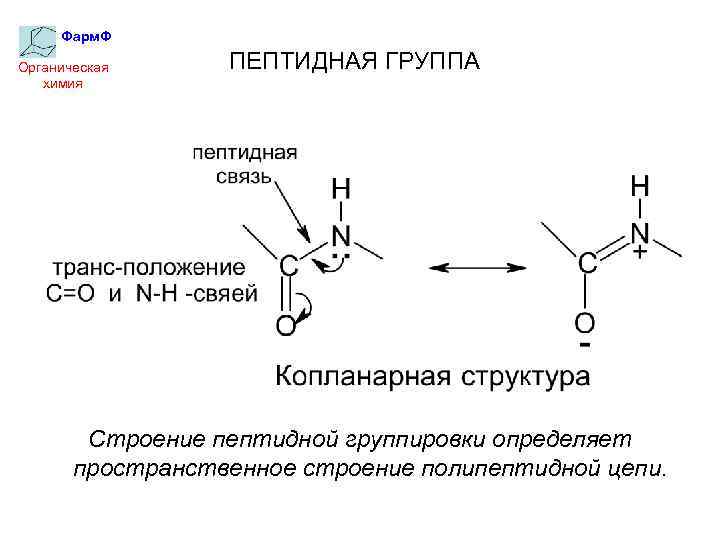
Фарм. Ф Органическая химия ПЕПТИДНАЯ ГРУППА Строение пептидной группировки определяет пространственное строение полипептидной цепи.

Фарм. Ф Органическая химия Вторичная структура 1) α-спираль Л. Полинг (1950 г. ) расчетным путем показал, что для α-полипептиной цепи одной из наиболее вероятных является структура правозакрученной α-пирали. Вскоре это было экспериментально подтверждено методом рентгено-структурного анализа. Между С=О 1 -го и N-H 5 -го аминокислотных остатков образуются водородные связи, направленные почти параллельно оси спирали, они скрепляют спираль. Боковые радикалы R расположены по периферии спирали:
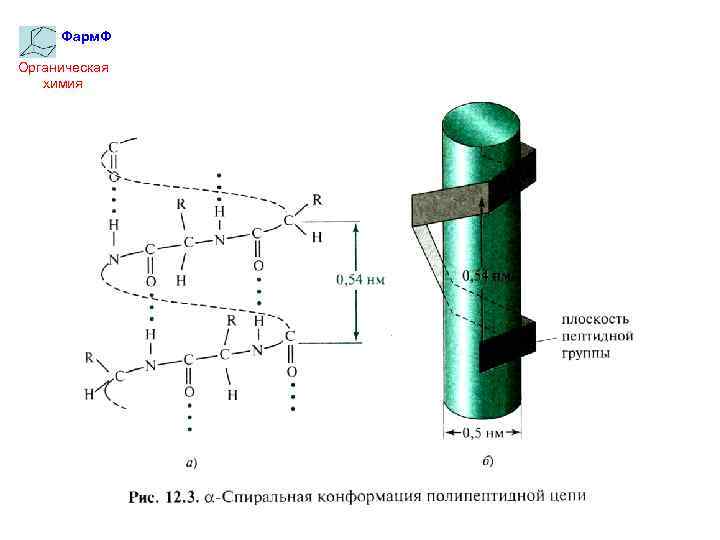
Фарм. Ф Органическая химия
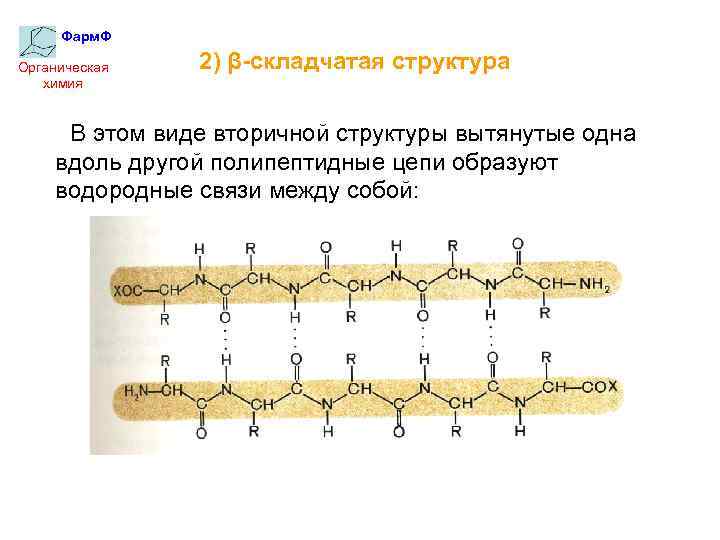
Фарм. Ф Органическая химия 2) β-складчатая структура В этом виде вторичной структуры вытянутые одна вдоль другой полипептидные цепи образуют водородные связи между собой:
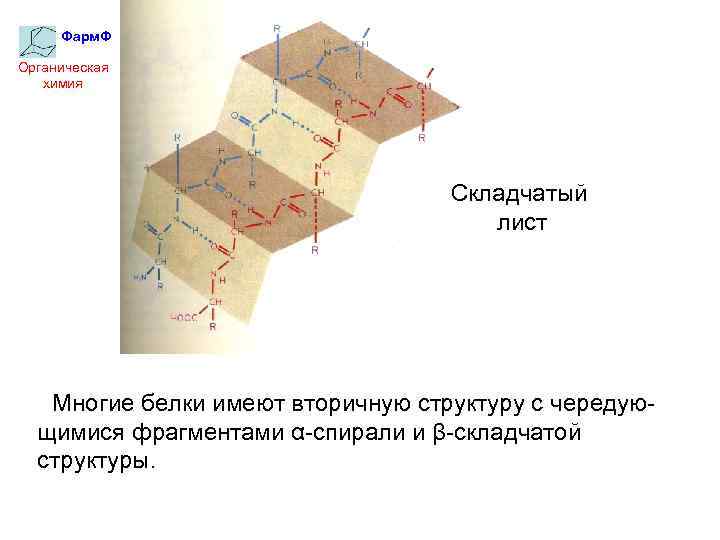
Фарм. Ф Органическая химия Складчатый лист Многие белки имеют вторичную структуру с чередующимися фрагментами α-спирали и β-складчатой структуры.

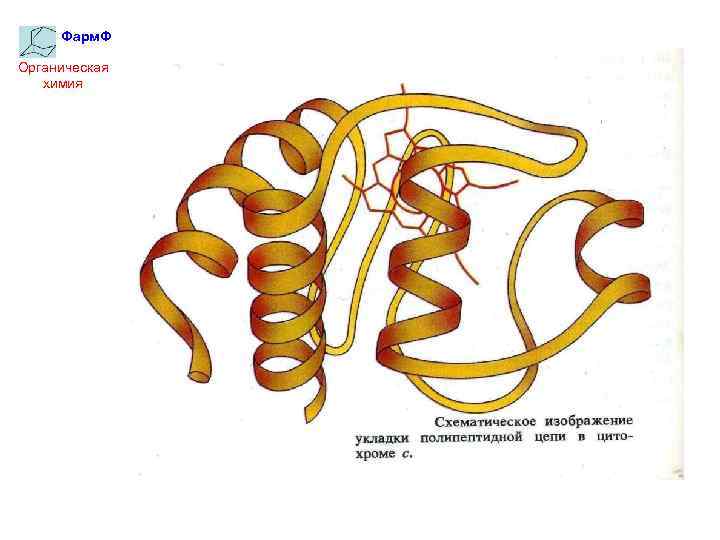
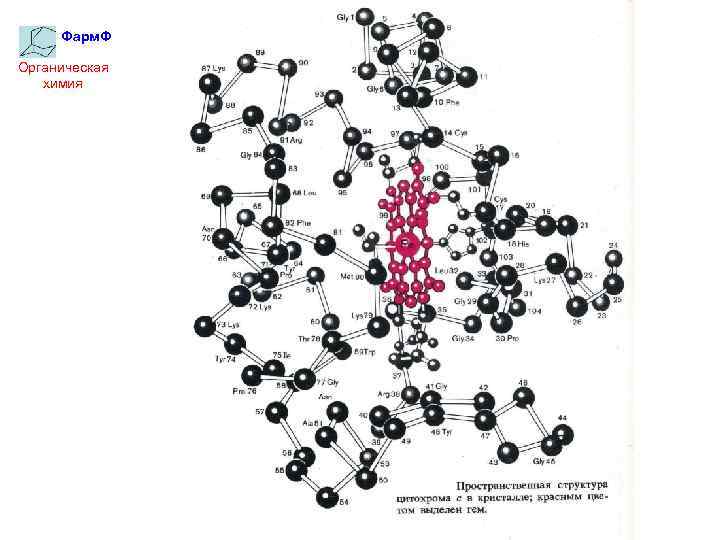
Фарм. Ф Органическая химия Третичная структура α-Спираль, будучи достаточно протяженной, изгибаясь, складывается в клубок. Образуется глобула:

Фарм. Ф Органическая химия
Фарм. Ф Органическая химия
Фарм. Ф Органическая химия

Фарм. Ф Органическая химия Образование глобулы происходит в результате взаимодействия боковых радикалов достаточно удаленных друг от друга.
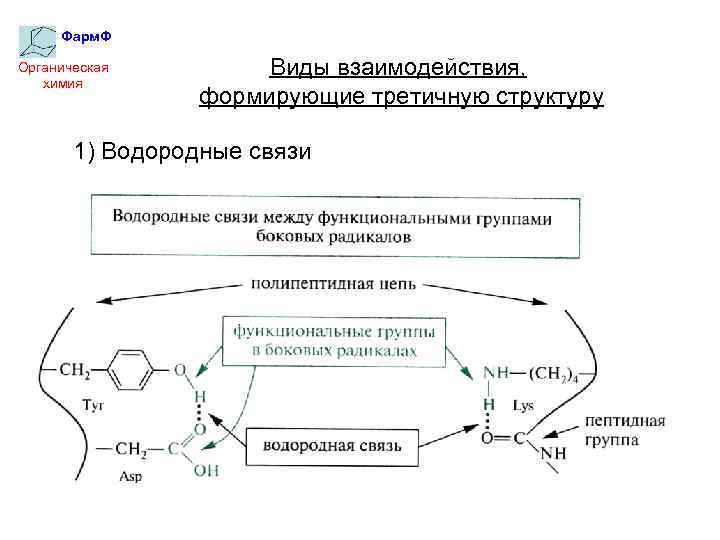
Фарм. Ф Органическая химия Виды взаимодействия, формирующие третичную структуру 1) Водородные связи

Фарм. Ф Органическая химия 2) Ионное взаимодействие
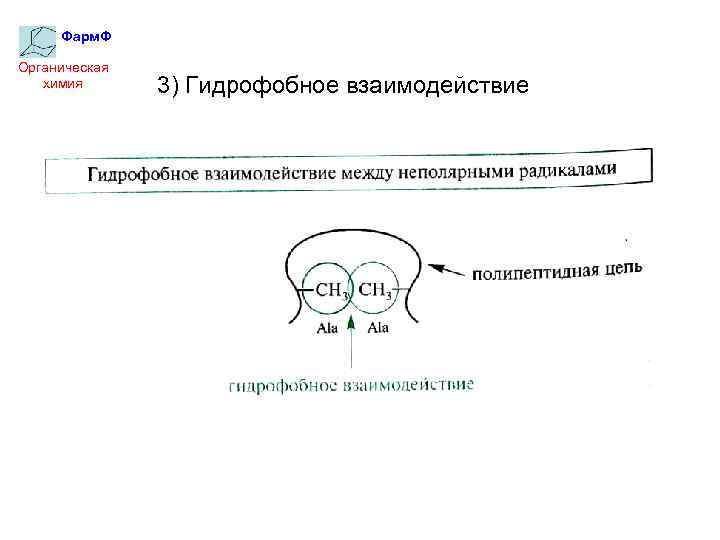
Фарм. Ф Органическая химия 3) Гидрофобное взаимодействие
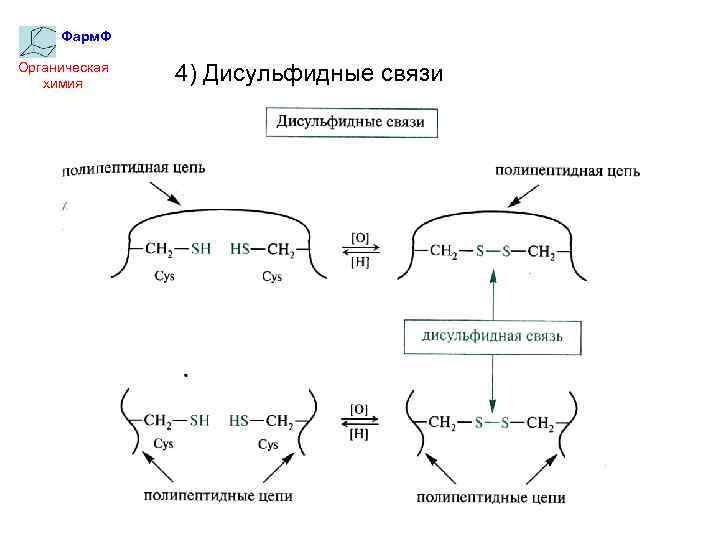
Фарм. Ф Органическая химия 4) Дисульфидные связи
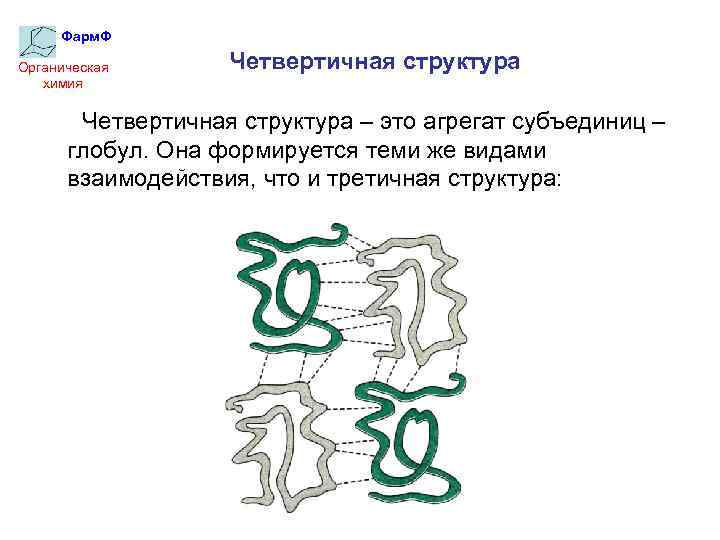
Фарм. Ф Органическая химия Четвертичная структура – это агрегат субъединиц – глобул. Она формируется теми же видами взаимодействия, что и третичная структура:
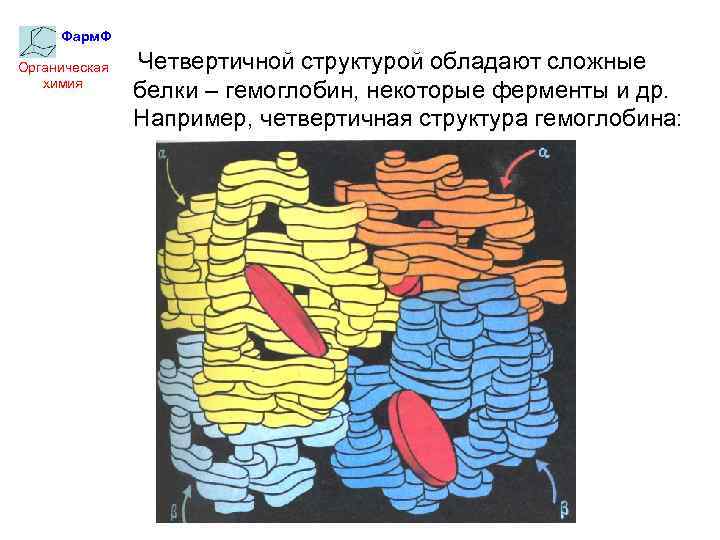
Фарм. Ф Органическая химия Четвертичной структурой обладают сложные белки – гемоглобин, некоторые ферменты и др. Например, четвертичная структура гемоглобина:

Фарм. Ф Органическая химия ЛИТЕРАТУРА: Основная 1. Тюкавкина Н. А. , Зурабян С. Э. , Белобородов В. Л. и др. – Органическая химия (специальный курс), кн. 2 – Дрофа, М. , 2008 г. , с. 207 -227. 2. Тюкавкина Н. А. , Бауков Ю. И. – Биоорганическая химия – Дрофа, М. , 2007, с. 314 -315, 345 -369. Дополнительная 1. Овчинников Ю. А. – Биоорганическая химия – М. , Просвещение, 1987, с. 20 -295. 06. 09
18.Полипептиды, белки 06.09.09.ppt