
ФАО • Модулі – 30 балів * 3 = 90 балів • Літучки - 2 бали * 5 = 10 балів Додаткові кредити: Реферат = 10 балів Перездача - 1 модуль Здача пропущеного не є перездачею і можлива за наявності причин пропуску (об’єктивних або творчих). На перездачу приходимо підготовленими!!! Перездачі можливі до подачі проміжних балів !!! “Мислью по древу” – не пройде !!! Джерела підготовки за бажанням – опитування по матеріалах лекцій !!!!

Основна література Варфоломеев С. Д. Химическая энзимология: Учебник. - М. : Академия. -2005 Плакунов В. К. Основы энзимологии. -М. : Логос. -2001. Фершт Э. Структура и механизм действия ферментов. - М. : Мир, 1980 Диксон М. , Уэбб Э. Ферменты: Т. 1 -3. -М. : Мир. -1982. Курганов Б. И. Физико-химические механизмы регуляции активности ферментов. - М. : Наука, 1992 Келети Т. Основы ферментативной кинетики. - М. : Мир, 1980 Коєн Ф. Регуляция ферментативной активности. М. : Мир. -1986

1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. Теми рефератів структурах Збірка мультиферментних комплексів на субклітинних Біохімічні наслідки адсорбції метаболітів Регуляція функціонування ензимів за механізмом зворотного зв’язку Вплив замісників на реакційний центр ферменту Багатоелектронні процеси в активних центрах ферментів Вплив субстрату на інактивацію ферменту Каталіз оточенням (вплив солей та розчинників) у ферментативних реакціях Межі між нуклеофільним та загально-кислотним каталізом у ферментативних реакціях Іон металу як місток між двома субстратами у ферментативних реакціях Ферментативний каталіз як результат комплексоутворення Ковалентні комплекси в ферментативному каталізі Нековалентні комплекси в ферментативному каталізі Непродуктивне зв’язування в ферментативному каталізі Теорії стереоспецифічності в ферментативному каталізі 10 балів – 7 балів захист, 3 балів написання Розмір – 5 -15 ст. “Вода” не включається

Білкова природа ферментів Особливості просторової організації молекул ензимів.

Швидкість реакції - зміна концентрації реагуючих речовин, що відбувається за одиницю часу. Каталіз – явище зміни швидкості хімічної реакції в присутності речовин, стан і кількість яких після реакції залишається незмінним. Ферменти (від лат. fermentum - шумування, закваска) - це специфічні білки, що є присутніми у всіх живих клітинах, де відіграють роль біологічних каталізаторів, тобто прискорюють протікання хімічних реакцій в організмі.

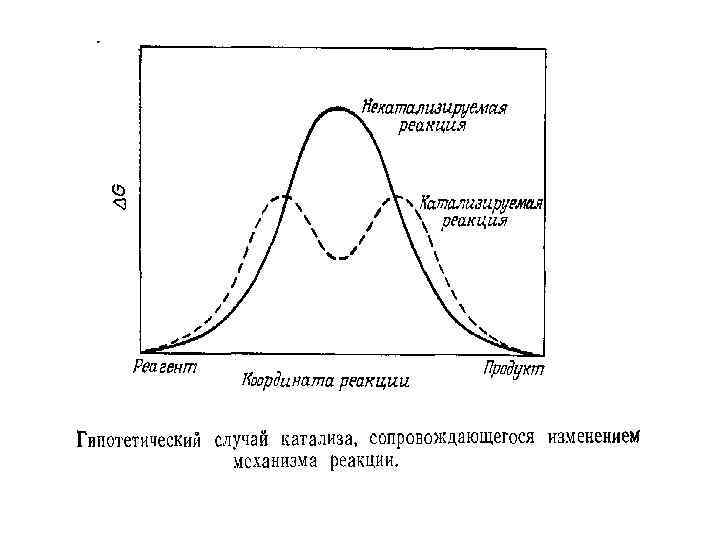
Альтернативний шлях • Відсутня лімітуюча стадія неферментативного перетворення • Продукти залишаються незмінними • Каталізатор легко витісняється з комплексу із продуктом • NB!!! Фермент не знижує енергію активації, а змінює шлях перебігу реакції

Промотор не є істинним каталізатором • Н. : луг “каталізує” розпад складного ефіру, але далі витрачається на нейтралізацію карбонової кислоти

Білкова природа ферментів • Білки водночас стійкі та мінливі • На поверхні білків існують різноманітні функціональні групи • Для них характерна велика кількість фізичних та хімічних перетворень • Здатні утворювати комплекси з іншими сполуками • Можливість внутрішньомолекулярних взаємодій • Здатні відповідати на зовнішній стимул зміною конформації і у подальшому повертатись до вихідного стану • Здатні до самоорганізації та саморегуляції

Особливості ферментативного каталізу • Швидкість хімічних реакцій прискорюється ферментами в 106 -1016 разів, у порівнянні з хімічними каталізаторами; • Ферменти працюють при нормальній температурі тіла (37 -42°) і нормальному тиску; • Здійснюється тонка регуляція ферментативної реакції, немає відходів і шлаків; • Ферментативні реакції підкоряються термодинамічній кінетиці; • Ферменти не зміщують рівновагу реакції, а тільки прискорюють її наближення.
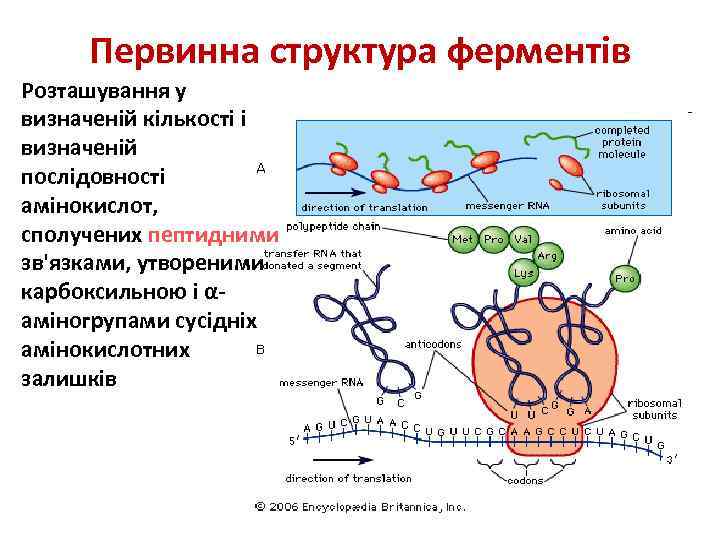
Первинна структура ферментів Розташування у визначеній кількості і визначеній послідовності амінокислот, сполучених пептидними зв'язками, утвореними карбоксильною і αаміногрупами сусідніх амінокислотних залишків
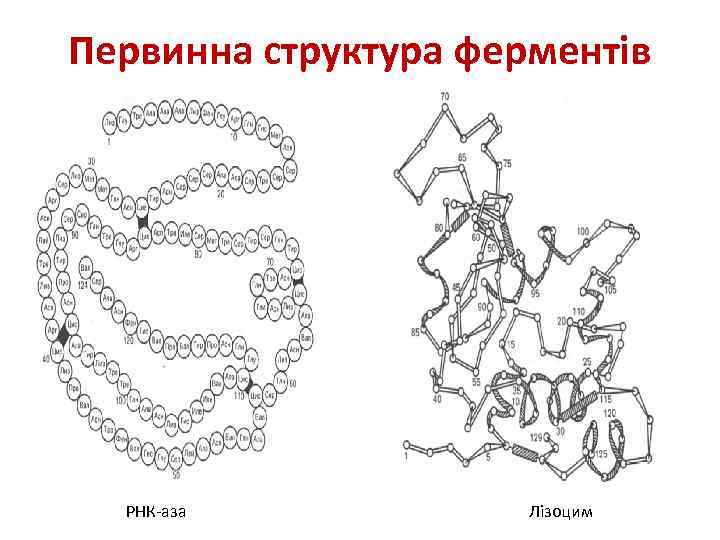
Первинна структура ферментів РНК-аза Лізоцим

Особливості первинної структури ферментів 1. у ферментів з різних об’єктів АК послідовність може різнитись – видоспецифічність Н. : гліцеральдегідрогенази свині та омара – 28 різних АК. 2. практично неможливі АК заміни в межах активного центра Н. : 17 АК активного центру гліцеральдегідрогенази різних видів ідентичні 3. часті консервативні заміни АК (Val ↔ Leu, Lys ↔ Arg), що не впливають на фізико-хімічні властивості ферментів

Особливості первинної структури ферментів 4. Ферменти з близькою функцією характеризуються подібною первинною структурою Н. : трипсин, хімотрипсин, еластаза, тромбін – серинові протеїнази, схожість приблизно на 50 %. З 240 АК – 42 АК ідентичні, інші гомологічні 5. При переході від менш складних до більш складних об’єктів ускладнюється первинна структура ензимів Н. : аміноацил-т. РНК-синтетази одноклітинних високий відсоток ідентичності та гомології, з печінки ссавців – молекулярна маса більша в 1, 5 -2 рази. 6. Усі АК заміни є наслідком точкових мутацій і можуть призводити до часткової чи повної інактивації ферменту. Н. : глобін у гемоглобіні – заміна Gly на Val у β-ланцюзі призводить до розвитку серповидно-клітинної анемії;
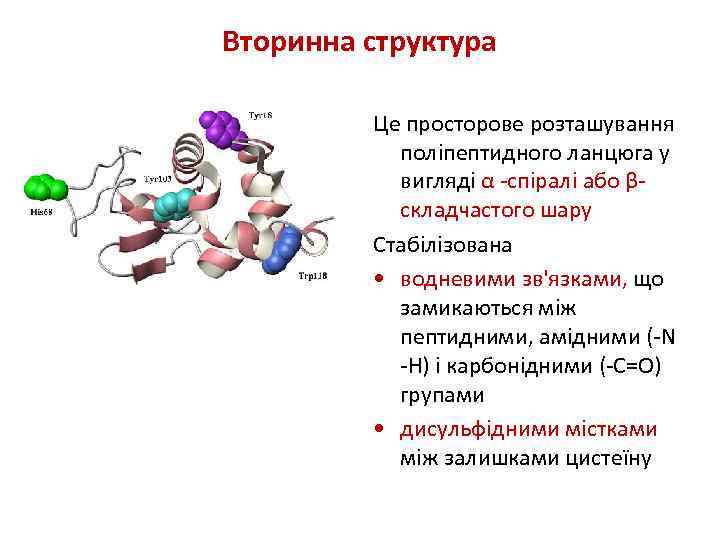
Вторинна структура Це просторове розташування поліпептидного ланцюга у вигляді α -спіралі або βскладчастого шару Стабілізована • водневими зв'язками, що замикаються між пептидними, амідними (-N -H) і карбонідними (-C=O) групами • дисульфідними містками між залишками цистеїну

Особливості вторинної структури ферментів 1. Незначна наявність α-спіралей Н. : карбоксипептидаза – кілька спіралей, αхімотрипсин – одну 2. Поширенність β-шарів – утворюють ядро глобул ферменту

Надвторинна структура термодинамічно або кінетично стабільний комплекс альфа-спіралей і бета-структур, що формується за рахунок міжрадикальних взаємодій Н. : тріозофосфатізомераза – β-бочка Лактатдегідрогеназа – 6 α-спіралей та 6 β-шарів
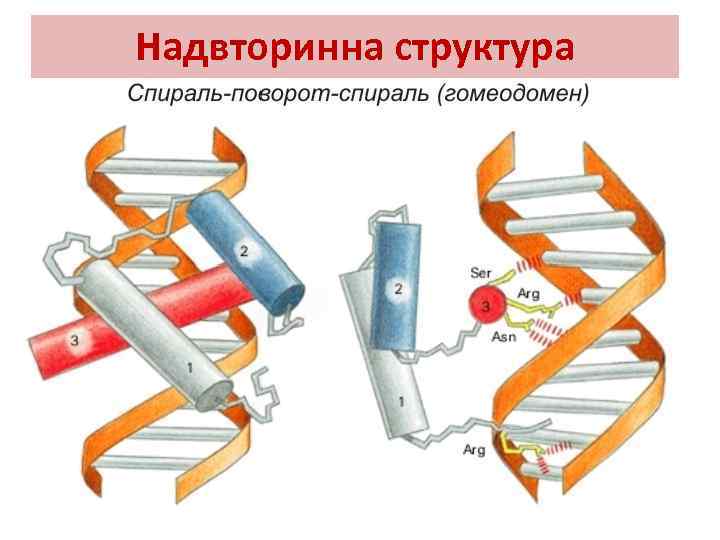
Надвторинна структура
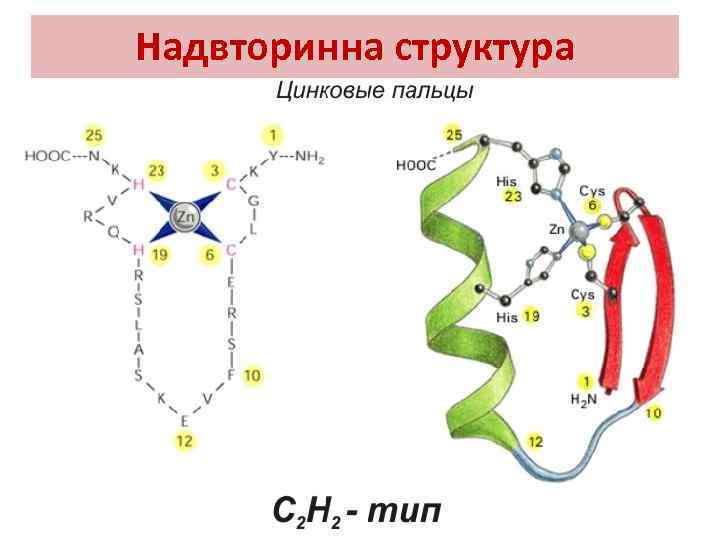
Надвторинна структура
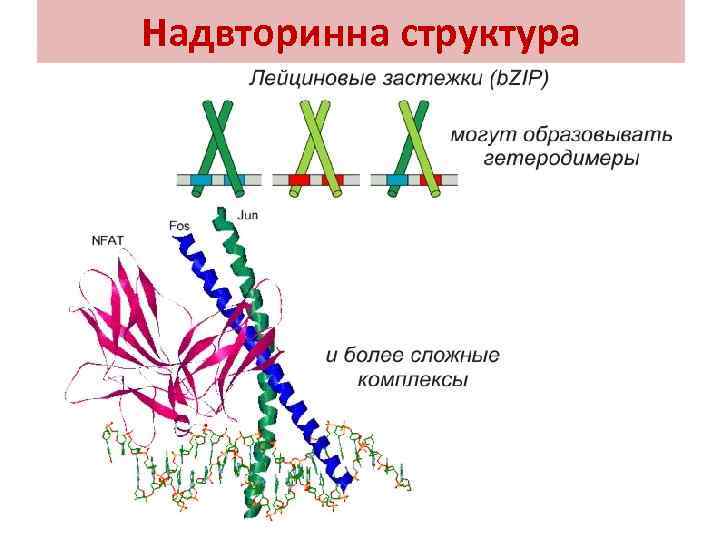
Надвторинна структура

Особливості надвторинної структури ферментів • Структури доменів, що виконують однакові функції – практично ідентичні Н. : NAD-залежний домен дегідрогеназ – 6 βшарів, 4 α-спіралі
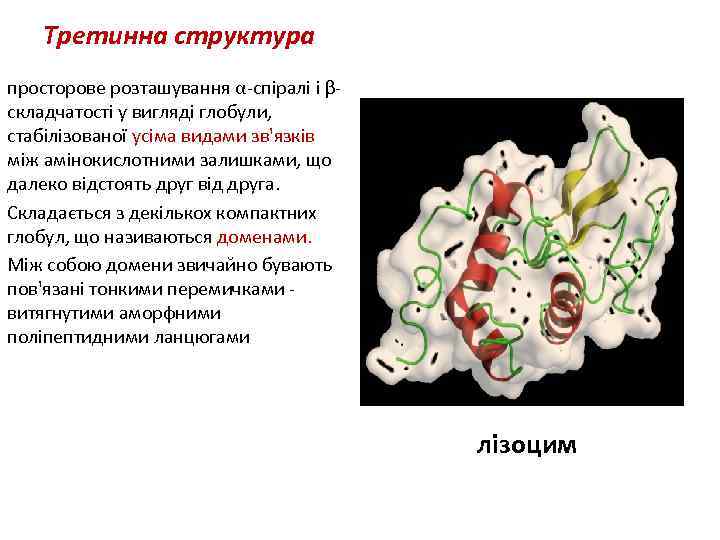
Третинна структура просторове розташування α-спіралі і βскладчатості у вигляді глобули, стабілізованої усіма видами зв'язків між амінокислотними залишками, що далеко відстоять друг від друга. Складається з декількох компактних глобул, що називаються доменами. Між собою домени звичайно бувають пов'язані тонкими перемичками витягнутими аморфними поліпептидними ланцюгами лізоцим

ΔG = -RTln. K = ΔH – TΔS ΔG<0 Термодинаміка згортання білкової глобули характеризується тим, що фактори, що сприяють утворенню компактної нативної структури, і фактори, що діють у протилежному напрямку, майже збалансовані. Зміна вільної енергії при згортанні білка, що містить приблизно 100 АК, становить близько 10 ккал/моль ( енергія водневого зв'язку становить близько 3 ккал/моль). Тому білкова глобула може втрачати стабільність, розвертатися вже при відносно невеликій зміні зазначених величин. Наприклад, втрата тільки одного водневого зв'язку при заміні в лізоцимі фага Т 4 thr → ile знижувала температуру денатурації білка на 11 градусів.
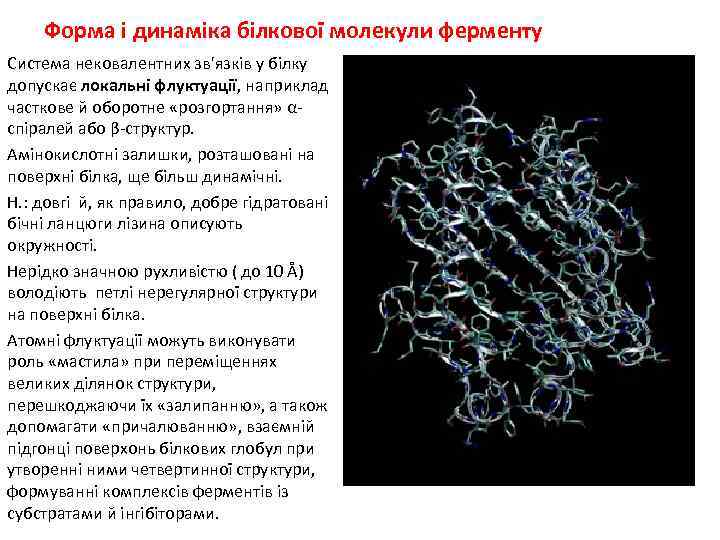
Форма і динаміка білкової молекули ферменту Сиcтема нековалентних зв'язків у білку допускає локальні флуктуації, наприклад часткове й оборотне «розгортання» αспіралей або β-структур. Амінокислотні залишки, розташовані на поверхні білка, ще більш динамічні. Н. : довгі й, як правило, добре гідратовані бічні ланцюги лізина описують окружності. Нерідко значною рухливістю ( до 10 Å) володіють петлі нерегулярної структури на поверхні білка. Атомні флуктуації можуть виконувати роль «мастила» при переміщеннях великих ділянок структури, перешкоджаючи їх «залипанню» , а також допомагати «причалюванню» , взаємній підгонці поверхонь білкових глобул при утворенні ними четвертинної структури, формуванні комплексів ферментів із субстратами й інгібіторами.
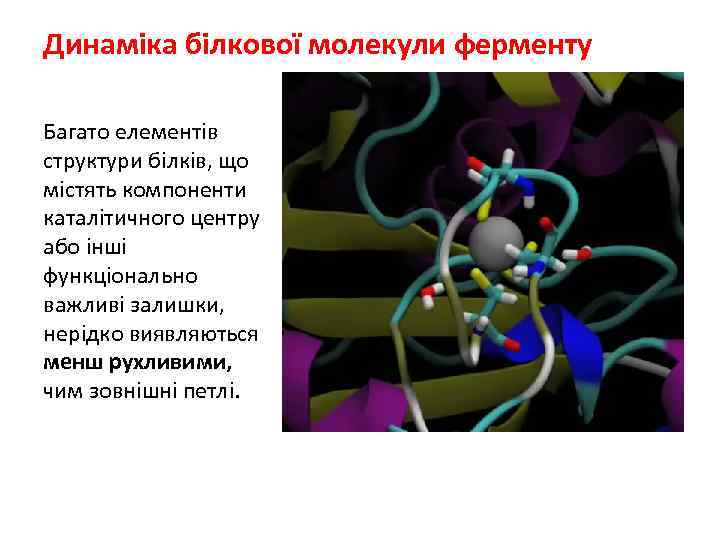
Динаміка білкової молекули ферменту Багато елементів структури білків, що містять компоненти каталітичного центру або інші функціонально важливі залишки, нерідко виявляються менш рухливими, чим зовнішні петлі.
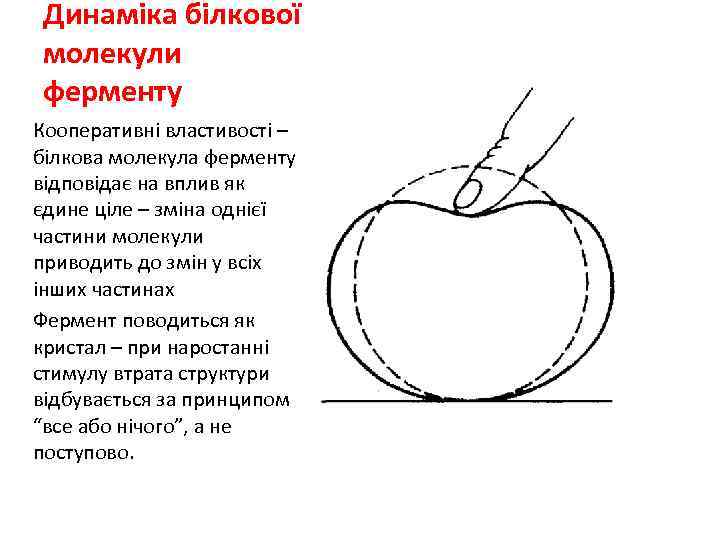
Динаміка білкової молекули ферменту Кооперативні властивості – білкова молекула ферменту відповідає на вплив як єдине ціле – зміна однієї частини молекули приводить до змін у всіх інших частинах Фермент поводиться як кристал – при наростанні стимулу втрата структури відбувається за принципом “все або нічого”, а не поступово.

Основні типи рухів в білковій молекулі

Особливості третинної структури ферментів 1. Завдяки їй утворюється активний центр, що знаходиться у щілині між різними структурами (доменами) 2. Часто є результатом посттрансляційних модифікацій Н. : обмежений протеоліз (протеази) 3. В межах третинної структури теж можливо утворення доменів
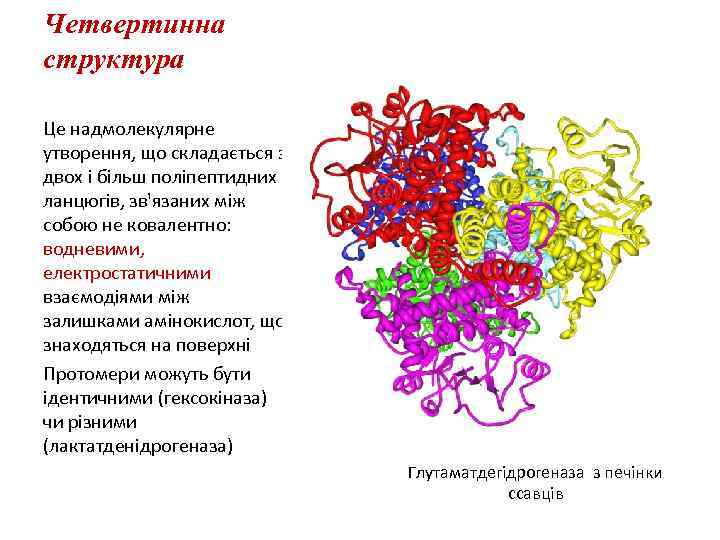
Четвертинна структура Це надмолекулярне утворення, що складається з двох і більш поліпептидних ланцюгів, зв'язаних між собою не ковалентно: водневими, електростатичними взаємодіями між залишками амінокислот, що знаходяться на поверхні Протомери можуть бути ідентичними (гексокіназа) чи різними (лактатденідрогеназа) Глутаматдегідрогеназа з печінки ссавців

Особливості четвертинної структури ферментів 1. Надає можливість об’єднання кількох взаємозв’язаних функцій в межах однієї молекули Н. : існування каталітичних та регуляторних субодиниць у протеїнкіназах 2. Забезпечує підвищення ферментативної активності шляхом збільшення кількості активних центрів 3. Архітектурна функція Н. : тріозофосфатізомераза - зона зв'язування субстрату утворена двома субодиницями, які при взаємодії з фосфатною групою субстрату зближаються, закриваючи його від навколишнього розчинника, так що реакція протікає при повній його відсутності

Особливості четвертинної структури ферментів 4. Поява кооперативних ефектів. 5. Забезпечення множинних взаємодій білка із протяжними структурами. Н. : За рахунок існування четвертинної структури імуноглобуліни G поєднують в одній молекулі два ідентичні центри зв'язування антигену. Кооперативність взаємодії таких центрів з макромолекулярними антигенами, наприклад, бактеріальними стінками, робить комплекси антиген -імуноглобулін набагато більш міцними, чим це спостерігалося б для мономерного білка. 6. Можливість поліфункціональності ферментативних систем – каталіз кількох реакцій. Н. : синтетази жирних кислот 7. Забезпечує наявність ізомерів.

Особливості четвертинної структури ферментів 8. Регуляторна функція Головна функціональна особливість четвертинної структури полягає в тому, що відносно слабкі взаємодії між субодиницями, характер яких суттєво залежить від третинної структури кожної з них, особливо зручні для регуляторних впливів, управління активністю білків. Через відносну слабість міжсубодиничних контактів зміни в третинній структурі якої-небудь субодиниці, викликані її взаємодією із субстратом або іншим лігандом, передаються на зону її контакту з іншою субодиницею, змінюючи характер цієї зони. Така зміна приводить до перебудови всієї четвертинної структури й забезпечує передачу ефекту від однієї субодиниці до інших.