гетерогенные+некат+процессы.ppt
- Количество слайдов: 12
 Факультет Энергетики и Нефтегазовой индустрии Кафедра химической инженерии ГЕТЕРОГЕННЫЕ НЕКАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ
Факультет Энергетики и Нефтегазовой индустрии Кафедра химической инженерии ГЕТЕРОГЕННЫЕ НЕКАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ
 БОЛЬШИНСТВО ХИМИКО-ТЕХНОЛОГИЧЕСКИХ ПРОЦЕССОВ ОТНОСЯТСЯ К ГЕТЕРОГЕННЫМ. При протекании гетерогенных реакций по меньшей мере один из реагентов или продуктов находится в фазовом состоянии, отличающемся от фазового состояния остальных участников реакции. Различают двухфазные системы: Г – Ж, Г-Т, Ж –Т и различные варианты трехфазных реакционных систем МЕХАНИЗМ ГЕТЕРОГЕННЫХ ПРОЦЕССОВ СЛОЖНЕЕ ГОМОГЕННЫХ. • РЕАГИРУЮЩИЕ ВЕЩЕСТВА НАХОДЯТСЯ В РАЗНЫХ ФАЗАХ И ПОДВОД ИХ К ПОВЕРХНОСТИ РАЗДЕЛА ФАЗ, ГДЕ ПРОИСХОДИТ ХИМИЧЕСКОЕ ВЗАИМОДЕЙСТВИЕ • А ТАКЖЕ МАССООБМЕН МЕЖДУ ФАЗАМИ ОСУЩЕСТВЛЯЮТСЯ В РЕЗУЛЬТАТЕ МОЛЕКУЛЯРНОЙ И КОНВЕКТИВНОЙ ДИФФУЗИИ, КОТОРЫЕ НАКЛАДЫВАЮТСЯ НА ОСНОВНОЙ ХИМИЧЕСКИЙ ПРОЦЕСС.
БОЛЬШИНСТВО ХИМИКО-ТЕХНОЛОГИЧЕСКИХ ПРОЦЕССОВ ОТНОСЯТСЯ К ГЕТЕРОГЕННЫМ. При протекании гетерогенных реакций по меньшей мере один из реагентов или продуктов находится в фазовом состоянии, отличающемся от фазового состояния остальных участников реакции. Различают двухфазные системы: Г – Ж, Г-Т, Ж –Т и различные варианты трехфазных реакционных систем МЕХАНИЗМ ГЕТЕРОГЕННЫХ ПРОЦЕССОВ СЛОЖНЕЕ ГОМОГЕННЫХ. • РЕАГИРУЮЩИЕ ВЕЩЕСТВА НАХОДЯТСЯ В РАЗНЫХ ФАЗАХ И ПОДВОД ИХ К ПОВЕРХНОСТИ РАЗДЕЛА ФАЗ, ГДЕ ПРОИСХОДИТ ХИМИЧЕСКОЕ ВЗАИМОДЕЙСТВИЕ • А ТАКЖЕ МАССООБМЕН МЕЖДУ ФАЗАМИ ОСУЩЕСТВЛЯЮТСЯ В РЕЗУЛЬТАТЕ МОЛЕКУЛЯРНОЙ И КОНВЕКТИВНОЙ ДИФФУЗИИ, КОТОРЫЕ НАКЛАДЫВАЮТСЯ НА ОСНОВНОЙ ХИМИЧЕСКИЙ ПРОЦЕСС.
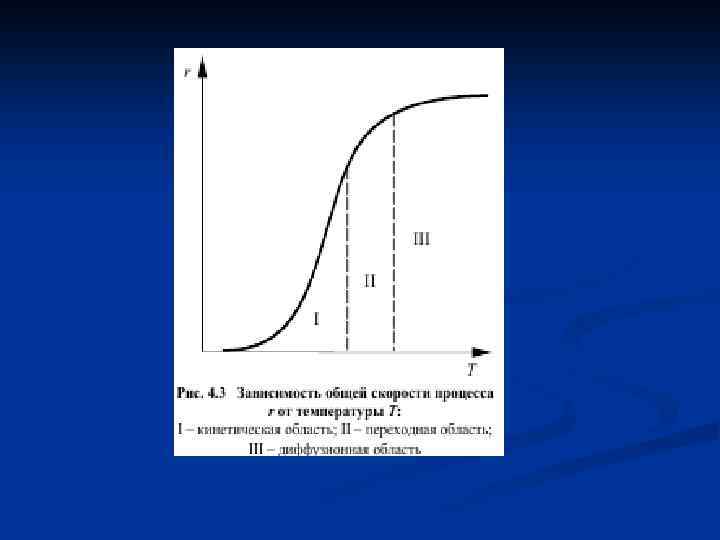
 Гетерогенные процессы протекают на поверхности раздела фаз. Скорость всего процесса определяется скоростью самой медленной стадии, которая называется лимитирующей стадией. Для установления лимитирующей стадии процесса существует несколько приемов. Рассмотрим способ определения лимитирующей стадии опытным путем: • Температура оказывает сильное влияние на скорость химических реакций. • Так, если опыт показывает, что повышение температуры оказывает сильное влияние на скорость процесса, то процесс протекает в кинетической области (рис. 4. 3, область I). • Если при дальнейшем повышении температуры ее влияние на скорость общего процесса уменьшается, значит процесс перешел в переходную область (рис. 4. 3, область II). Если же далее при повышении температуры общая скорость процесса практически не изменяется, значит процесс протекает в диффузионной области (рис. 4. 3, область III).
Гетерогенные процессы протекают на поверхности раздела фаз. Скорость всего процесса определяется скоростью самой медленной стадии, которая называется лимитирующей стадией. Для установления лимитирующей стадии процесса существует несколько приемов. Рассмотрим способ определения лимитирующей стадии опытным путем: • Температура оказывает сильное влияние на скорость химических реакций. • Так, если опыт показывает, что повышение температуры оказывает сильное влияние на скорость процесса, то процесс протекает в кинетической области (рис. 4. 3, область I). • Если при дальнейшем повышении температуры ее влияние на скорость общего процесса уменьшается, значит процесс перешел в переходную область (рис. 4. 3, область II). Если же далее при повышении температуры общая скорость процесса практически не изменяется, значит процесс протекает в диффузионной области (рис. 4. 3, область III).
 Скорость сложного гетерогенного процесса зависит от скоростей химической реакции и скоростей диффузионных стадий. Скорость диффузии зависит от плотности и вязкости среды, температуры, воздействия внешних сил и т. д. Закономерности диффузионных процессов описываются законами Фика. Первый закон Фика: количество вещества А, перенесенного вследствие диффузии в единицу времени через поверхность S, перпендикулярную направлению переноса, пропорционально градиенту концентрации этого вещества в данный момент времени: Коэффициент пропорциональности D называется коэффициентом молекулярной диффузии.
Скорость сложного гетерогенного процесса зависит от скоростей химической реакции и скоростей диффузионных стадий. Скорость диффузии зависит от плотности и вязкости среды, температуры, воздействия внешних сил и т. д. Закономерности диффузионных процессов описываются законами Фика. Первый закон Фика: количество вещества А, перенесенного вследствие диффузии в единицу времени через поверхность S, перпендикулярную направлению переноса, пропорционально градиенту концентрации этого вещества в данный момент времени: Коэффициент пропорциональности D называется коэффициентом молекулярной диффузии.
 Второй закон Фика описывает изменение концентрации вещества А во времени в результате молекулярной диффузии. Кинетические модели гетерогенных процессов в системе «газ- твердое вещество» . При описании гетерогенных процессов в системе « газ – твердое вещество » используют две модели: • квазигомогенная модель; • модель с фронтальным перемещением зоны реакции.
Второй закон Фика описывает изменение концентрации вещества А во времени в результате молекулярной диффузии. Кинетические модели гетерогенных процессов в системе «газ- твердое вещество» . При описании гетерогенных процессов в системе « газ – твердое вещество » используют две модели: • квазигомогенная модель; • модель с фронтальным перемещением зоны реакции.
 КВАЗИГОМОГЕННАЯ МОДЕЛЬ. Гетерогенный процесс протекает одновременно в любой точке объема твердой частицы. ЭТО УСЛОВИЕ ВОЗМОЖНО ПРИ СЛЕДУЮЩИХ УСЛОВИЯХ: • если газообразный реагент может достаточно свободно проникнуть внутрь твердой фазы, т. е. если частица твердого вещества пронизана большим числом пор. • химическая реакция, протекающая на поверхности этих пор, достаточно медленная.
КВАЗИГОМОГЕННАЯ МОДЕЛЬ. Гетерогенный процесс протекает одновременно в любой точке объема твердой частицы. ЭТО УСЛОВИЕ ВОЗМОЖНО ПРИ СЛЕДУЮЩИХ УСЛОВИЯХ: • если газообразный реагент может достаточно свободно проникнуть внутрь твердой фазы, т. е. если частица твердого вещества пронизана большим числом пор. • химическая реакция, протекающая на поверхности этих пор, достаточно медленная.
 МОДЕЛЬ С ФРОНТАЛЬНЫМ ПЕРЕМЕЩЕНИЕМ ЗОНЫ РЕАКЦИИ. 1. Химическая реакция сначала протекает на внешней поверхности частицы, и до тех пор, пока внешний слой пор твердого реагента полностью не превратится в соответствующие твердые или газообразные продукты реакции. 2. Постепенно зона химической реакции продвигается внутрь, оставляя за собой твердый продукт реакции и инертную часть исходного твердого реагента (золу). В произвольный момент времени твердая частица представляет собой внутреннее ядро, окруженное внешней оболочкой. Ядро состоит из непрореагировавшего реагента (поэтому эту модель называют иногда моделью с непрореагировавшим ядром).
МОДЕЛЬ С ФРОНТАЛЬНЫМ ПЕРЕМЕЩЕНИЕМ ЗОНЫ РЕАКЦИИ. 1. Химическая реакция сначала протекает на внешней поверхности частицы, и до тех пор, пока внешний слой пор твердого реагента полностью не превратится в соответствующие твердые или газообразные продукты реакции. 2. Постепенно зона химической реакции продвигается внутрь, оставляя за собой твердый продукт реакции и инертную часть исходного твердого реагента (золу). В произвольный момент времени твердая частица представляет собой внутреннее ядро, окруженное внешней оболочкой. Ядро состоит из непрореагировавшего реагента (поэтому эту модель называют иногда моделью с непрореагировавшим ядром).
 1. Внешняя диффузия — подвод реагента А к поверхности твердой частицы через слой газа. 2. Внутренняя диффузия — проникновение газообразного реагента через поры твердого продукта реакции к ядру твердого реагента; 3. Химическая реакция на поверхности непрореагировавшего ядра 4. Внутренняя диффузия газообразных продуктов через слой твердых продуктов. 5. Внешняя диффузия газообразных продуктов в ядро газового потока.
1. Внешняя диффузия — подвод реагента А к поверхности твердой частицы через слой газа. 2. Внутренняя диффузия — проникновение газообразного реагента через поры твердого продукта реакции к ядру твердого реагента; 3. Химическая реакция на поверхности непрореагировавшего ядра 4. Внутренняя диффузия газообразных продуктов через слой твердых продуктов. 5. Внешняя диффузия газообразных продуктов в ядро газового потока.
 ВНЕШНЯЯ ДИФФУЗИЯ. При внешней диффузии протекает быстрая химическая реакция, поэтому концентрация газообразного реагента А (г) у поверхности ядра твердой частицы очень мала и ее можно принять равной нулю (СА, г = 0). Суммарный перенос вещества вследствие молекулярной диффузии и конвективного переноса называется конвективной диффузией. Процесс конвективной диффузии может быть описан дифференциальным уравнением:
ВНЕШНЯЯ ДИФФУЗИЯ. При внешней диффузии протекает быстрая химическая реакция, поэтому концентрация газообразного реагента А (г) у поверхности ядра твердой частицы очень мала и ее можно принять равной нулю (СА, г = 0). Суммарный перенос вещества вследствие молекулярной диффузии и конвективного переноса называется конвективной диффузией. Процесс конвективной диффузии может быть описан дифференциальным уравнением:
 Скорость конвективной диффузии можно определить уравнением: ВНУТРЕННЯЯ ДИФФУЗИЯ. • Стадия, предшествующая химической реакции и следующей за внешней диффузией. • Проникновение газообразного реагента через слой твердых продуктов реакции к поверхности ядра, на которой осуществляется химическое взаимодействие.
Скорость конвективной диффузии можно определить уравнением: ВНУТРЕННЯЯ ДИФФУЗИЯ. • Стадия, предшествующая химической реакции и следующей за внешней диффузией. • Проникновение газообразного реагента через слой твердых продуктов реакции к поверхности ядра, на которой осуществляется химическое взаимодействие.
 Скорость внутренней диффузии: где Dэф — эффективный коэффициент диффузии, учитывающий пористость твердого вещества, извилистость пор и т. д. ПОВЕРХНОСТНАЯ ХИМИЧЕСКАЯ РЕАКЦИЯ. где ks — константа скорости поверхностной химической реакции; п — порядок реакции.
Скорость внутренней диффузии: где Dэф — эффективный коэффициент диффузии, учитывающий пористость твердого вещества, извилистость пор и т. д. ПОВЕРХНОСТНАЯ ХИМИЧЕСКАЯ РЕАКЦИЯ. где ks — константа скорости поверхностной химической реакции; п — порядок реакции.


