гемофилияФакторы свертывания крови VIII..ppt
- Количество слайдов: 15
 Факторы свертывания крови VIII.
Факторы свертывания крови VIII.
 Качество сырья: плазмозаготовка Плазмаферез Гравитационный Апаратный (сепараторы)
Качество сырья: плазмозаготовка Плазмаферез Гравитационный Апаратный (сепараторы)
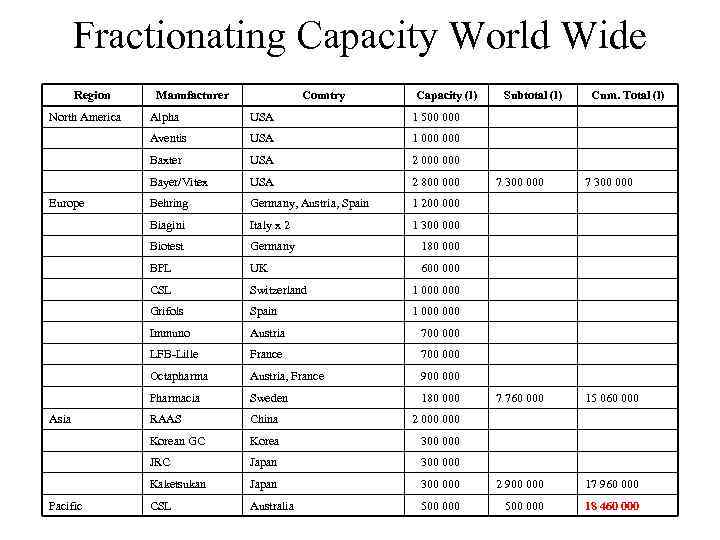 Fractionating Capacity World Wide Region North America Manufacturer Country Capacity (l) 1 000 USA 2 000 Bayer/Vitex USA 2 800 000 Behring Germany, Austria, Spain 1 200 000 Biagini Italy x 2 1 300 000 Biotest Germany 180 000 BPL UK 600 000 CSL Switzerland 1 000 Grifols Spain 1 000 Immuno Austria 700 000 LFB-Lille France 700 000 Octapharma Austria, France 900 000 Pharmacia Sweden 180 000 RAAS China 2 000 Korean GC Korea 300 000 JRC Japan 300 000 Kaketsukan Pacific USA Japan CSL Australia Cum. Total (l) 1 500 000 Baxter Asia USA Aventis Europe Alpha Subtotal (l) 7 300 000 7 760 000 15 060 000 300 000 2 900 000 17 960 000 500 000 18 460 000
Fractionating Capacity World Wide Region North America Manufacturer Country Capacity (l) 1 000 USA 2 000 Bayer/Vitex USA 2 800 000 Behring Germany, Austria, Spain 1 200 000 Biagini Italy x 2 1 300 000 Biotest Germany 180 000 BPL UK 600 000 CSL Switzerland 1 000 Grifols Spain 1 000 Immuno Austria 700 000 LFB-Lille France 700 000 Octapharma Austria, France 900 000 Pharmacia Sweden 180 000 RAAS China 2 000 Korean GC Korea 300 000 JRC Japan 300 000 Kaketsukan Pacific USA Japan CSL Australia Cum. Total (l) 1 500 000 Baxter Asia USA Aventis Europe Alpha Subtotal (l) 7 300 000 7 760 000 15 060 000 300 000 2 900 000 17 960 000 500 000 18 460 000
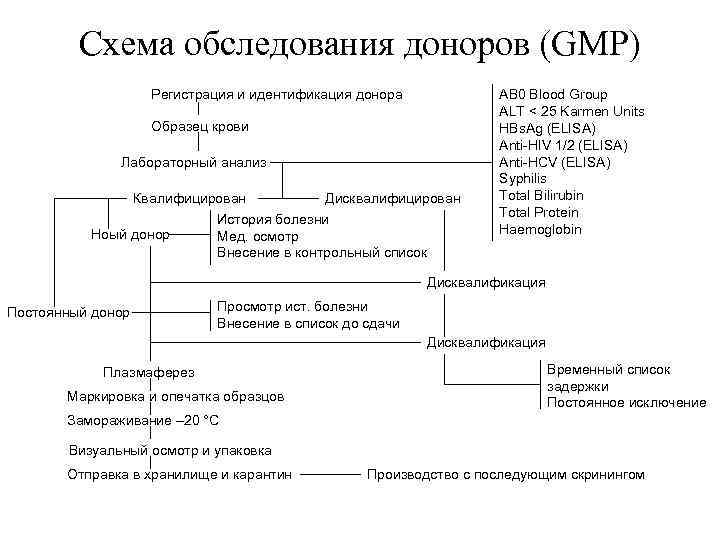 Схема обследования доноров (GMP) Регистрация и идентификация донора Образец крови Лабораторный анализ Квалифицирован Дисквалифицирован История болезни Ноый донор Мед. осмотр Внесение в контрольный список AB 0 Blood Group ALT < 25 Karmen Units HBs. Ag (ELISA) Anti-HIV 1/2 (ELISA) Anti-HCV (ELISA) Syphilis Total Bilirubin Total Protein Haemoglobin Дисквалификация Постоянный донор Просмотр ист. болезни Внесение в список до сдачи Дисквалификация Плазмаферез Маркировка и опечатка образцов Временный список задержки Постоянное исключение Замораживание – 20 °C Визуальный осмотр и упаковка Отправка в хранилище и карантин Производство с последующим скринингом
Схема обследования доноров (GMP) Регистрация и идентификация донора Образец крови Лабораторный анализ Квалифицирован Дисквалифицирован История болезни Ноый донор Мед. осмотр Внесение в контрольный список AB 0 Blood Group ALT < 25 Karmen Units HBs. Ag (ELISA) Anti-HIV 1/2 (ELISA) Anti-HCV (ELISA) Syphilis Total Bilirubin Total Protein Haemoglobin Дисквалификация Постоянный донор Просмотр ист. болезни Внесение в список до сдачи Дисквалификация Плазмаферез Маркировка и опечатка образцов Временный список задержки Постоянное исключение Замораживание – 20 °C Визуальный осмотр и упаковка Отправка в хранилище и карантин Производство с последующим скринингом
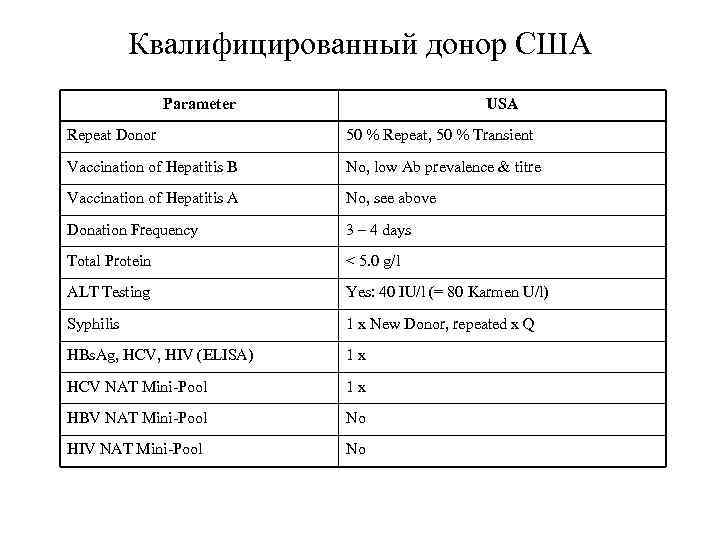 Квалифицированный донор США Parameter USA Repeat Donor 50 % Repeat, 50 % Transient Vaccination of Hepatitis B No, low Ab prevalence & titre Vaccination of Hepatitis A No, see above Donation Frequency 3 – 4 days Total Protein < 5. 0 g/l ALT Testing Yes: 40 IU/l (= 80 Karmen U/l) Syphilis 1 x New Donor, repeated x Q HBs. Ag, HCV, HIV (ELISA) 1 x HCV NAT Mini-Pool 1 x HBV NAT Mini-Pool No HIV NAT Mini-Pool No
Квалифицированный донор США Parameter USA Repeat Donor 50 % Repeat, 50 % Transient Vaccination of Hepatitis B No, low Ab prevalence & titre Vaccination of Hepatitis A No, see above Donation Frequency 3 – 4 days Total Protein < 5. 0 g/l ALT Testing Yes: 40 IU/l (= 80 Karmen U/l) Syphilis 1 x New Donor, repeated x Q HBs. Ag, HCV, HIV (ELISA) 1 x HCV NAT Mini-Pool 1 x HBV NAT Mini-Pool No HIV NAT Mini-Pool No
 Cohn Fractionation • Conditions Pooling Constituents Rapid Thawing Centrifugation Cryoprecipitation F VIII, v. WF (FNG, F XIII) Alcohol 8 %, 0 to - 2°C Fraction I FNG Alcohol 20 %, 0 to - 4°C Fraction II Ig. G (Ig. M) Alcohol 17 %, - 6°C Fraction II + III PCC, Ig. G (Ig. M) Alcohol 17 %, - 6°C Fraction III PCC, F IX Alcohol 40 %, - 6°C Fraction IV Discard Alcohol 40 %, - 6°C Fraction V Albumin
Cohn Fractionation • Conditions Pooling Constituents Rapid Thawing Centrifugation Cryoprecipitation F VIII, v. WF (FNG, F XIII) Alcohol 8 %, 0 to - 2°C Fraction I FNG Alcohol 20 %, 0 to - 4°C Fraction II Ig. G (Ig. M) Alcohol 17 %, - 6°C Fraction II + III PCC, Ig. G (Ig. M) Alcohol 17 %, - 6°C Fraction III PCC, F IX Alcohol 40 %, - 6°C Fraction IV Discard Alcohol 40 %, - 6°C Fraction V Albumin

 Производство FVIII Cryoprecipitate Fibrinogen Removal SD Virus Inactivation Ion Exch. Chromatography Freeze Drying Dry Heat 100 °C, 30 min HP=Specific Activity > 100 IU/mg IP= Specific Activity > 100 IU/mg
Производство FVIII Cryoprecipitate Fibrinogen Removal SD Virus Inactivation Ion Exch. Chromatography Freeze Drying Dry Heat 100 °C, 30 min HP=Specific Activity > 100 IU/mg IP= Specific Activity > 100 IU/mg
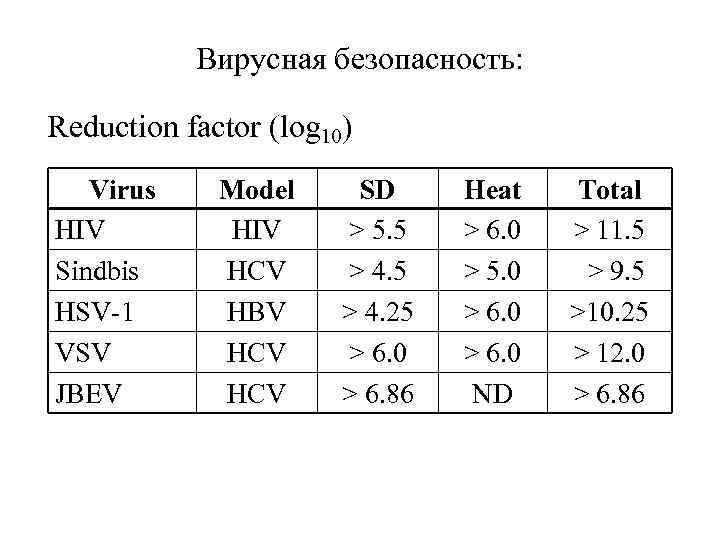 Вирусная безопасность: Reduction factor (log 10) Virus HIV Sindbis HSV-1 VSV JBEV Model HIV HCV HBV HCV SD > 5. 5 > 4. 25 > 6. 0 > 6. 86 Heat > 6. 0 > 5. 0 > 6. 0 ND Total > 11. 5 > 9. 5 >10. 25 > 12. 0 > 6. 86
Вирусная безопасность: Reduction factor (log 10) Virus HIV Sindbis HSV-1 VSV JBEV Model HIV HCV HBV HCV SD > 5. 5 > 4. 25 > 6. 0 > 6. 86 Heat > 6. 0 > 5. 0 > 6. 0 ND Total > 11. 5 > 9. 5 >10. 25 > 12. 0 > 6. 86
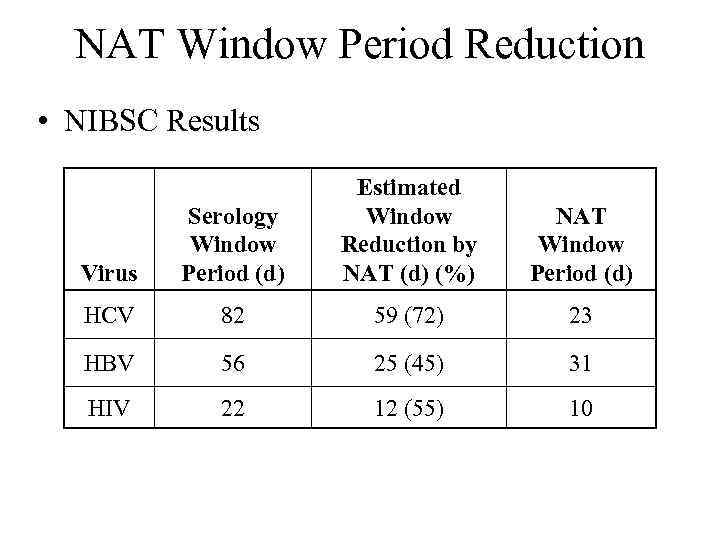 NAT Window Period Reduction • NIBSC Results Virus Serology Window Period (d) Estimated Window Reduction by NAT (d) (%) NAT Window Period (d) HCV 82 59 (72) 23 HBV 56 25 (45) 31 HIV 22 12 (55) 10
NAT Window Period Reduction • NIBSC Results Virus Serology Window Period (d) Estimated Window Reduction by NAT (d) (%) NAT Window Period (d) HCV 82 59 (72) 23 HBV 56 25 (45) 31 HIV 22 12 (55) 10
 Полная готовая формула продукта фактора VIII содержит (во флаконе): • • FVIII: C - не менее 80% от указанной Спец. активность – ≥ 0, 5 МЕ/мг протеина Натрий - ≤ 160 ммоль/л Глицин - ≤ 1, 5% Цитрат - ≤ 25 ммоль/л ПЭГ - ≤ 60 ppm Влажность - ≤ 3%
Полная готовая формула продукта фактора VIII содержит (во флаконе): • • FVIII: C - не менее 80% от указанной Спец. активность – ≥ 0, 5 МЕ/мг протеина Натрий - ≤ 160 ммоль/л Глицин - ≤ 1, 5% Цитрат - ≤ 25 ммоль/л ПЭГ - ≤ 60 ppm Влажность - ≤ 3%
 В производстве препарата при загрузке одной серии (2000 л) используется: • • • Трис буфер – 48 г. Спирт – 2000 л HCl – 1 л Натрий-гепарин – 45 г ПЭГ – 16 кг Твин-80 – 0, 9 кг Три-N-бутил фосфат – 0, 3 кг Глицин – 3, 5 кг Цитрат натрия – 2, 1 кг Дист. Вода (стерильная) – 1000 кг
В производстве препарата при загрузке одной серии (2000 л) используется: • • • Трис буфер – 48 г. Спирт – 2000 л HCl – 1 л Натрий-гепарин – 45 г ПЭГ – 16 кг Твин-80 – 0, 9 кг Три-N-бутил фосфат – 0, 3 кг Глицин – 3, 5 кг Цитрат натрия – 2, 1 кг Дист. Вода (стерильная) – 1000 кг
 Требования к «продукту» • Чистота (только специфическая активность фактора VIII – не имеет никакого отношение к стерильности); • Биологическая доступность (клинические и фармако-кинетические показатели – характеристика препарата проволится на большой группе пациентов) биоэквивалентность препаратов, не отражающая индивидуальные особенности пациента; • Вирусная безопасность (реальная и потенциальная) • Удобство использования (наличие полного набора для инъекций, скорость растворения, условия транспортировки и хранения).
Требования к «продукту» • Чистота (только специфическая активность фактора VIII – не имеет никакого отношение к стерильности); • Биологическая доступность (клинические и фармако-кинетические показатели – характеристика препарата проволится на большой группе пациентов) биоэквивалентность препаратов, не отражающая индивидуальные особенности пациента; • Вирусная безопасность (реальная и потенциальная) • Удобство использования (наличие полного набора для инъекций, скорость растворения, условия транспортировки и хранения).
 Требования к компании (доктрина побеждать!): • Знания о продуктах (технологиях, клинических результатах использования); • Социальная направленность (этичность поведения, распространение знаний, расширение круга заинтерисованных лиц, привлечение СМИ); • Представление накопленного опыта работы (мировой и внутренний); • Наличие отличительного стиля работы (…)
Требования к компании (доктрина побеждать!): • Знания о продуктах (технологиях, клинических результатах использования); • Социальная направленность (этичность поведения, распространение знаний, расширение круга заинтерисованных лиц, привлечение СМИ); • Представление накопленного опыта работы (мировой и внутренний); • Наличие отличительного стиля работы (…)