834f4afdf820504bff6c4649f1420745.ppt
- Количество слайдов: 36
 Faculté de Médecine Université Paris 7 Denis Diderot Service de Microbiologie CHU Saint Louis, Paris Principes et modalités du traitement antirétroviral post-exposition _ Suivi virologique pré et post-traitement Dr Constance Delaugerre SFLS - 10 février 2011
Faculté de Médecine Université Paris 7 Denis Diderot Service de Microbiologie CHU Saint Louis, Paris Principes et modalités du traitement antirétroviral post-exposition _ Suivi virologique pré et post-traitement Dr Constance Delaugerre SFLS - 10 février 2011
 Plan • Rationnel du traitement post-exposition (TPE) • Mécanismes d’action des antirétroviraux (ARV) • Choix du traitement post–exposition • Test de suivi virologique post AES – Dépistage du patient source – Suivi de la personne exposée
Plan • Rationnel du traitement post-exposition (TPE) • Mécanismes d’action des antirétroviraux (ARV) • Choix du traitement post–exposition • Test de suivi virologique post AES – Dépistage du patient source – Suivi de la personne exposée
 Rationnel du TPE
Rationnel du TPE
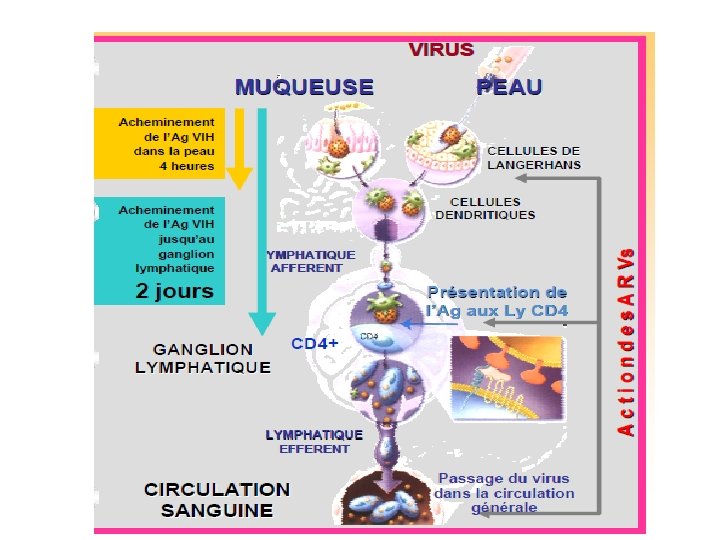
 Rationnel du TPE Utilisation des ARV en prévention • Principe : Elimination virale par le traitement + action du système immunitaire Agir avant l’atteinte de système immunitaire et la propagation virale donc URGENCE • Modèles animaux : – Inoculation IV SIV / macaque : Ténofovir (TSAI CC et al. Science, 1995, J Virol, 1998) – Transmission vaginale chez singe (OTTEN RA et al. J Virol, 2000) • Prophylaxie transmission mère-enfant : réduction du risque de 67% (Connor et al. , NEJM 1994 , Taha E et al. , JAMA 2004, Review Cochrane 2009) • Prophylaxie post-AES professionnel : – Échec étude prospective contrôlée – Perte de chance du groupe contrôle La. Fon et al. , ICAAC 1990, – Etude rétrospective : Cardo D et al. , NEJM 1997, – Efficacité admise malgré le faible nombre d’études cliniques (Review Cochrane 2009). • OBJECTIF du TPE: diminuer le risque de transmission du VIH en réduisant la charge virale
Rationnel du TPE Utilisation des ARV en prévention • Principe : Elimination virale par le traitement + action du système immunitaire Agir avant l’atteinte de système immunitaire et la propagation virale donc URGENCE • Modèles animaux : – Inoculation IV SIV / macaque : Ténofovir (TSAI CC et al. Science, 1995, J Virol, 1998) – Transmission vaginale chez singe (OTTEN RA et al. J Virol, 2000) • Prophylaxie transmission mère-enfant : réduction du risque de 67% (Connor et al. , NEJM 1994 , Taha E et al. , JAMA 2004, Review Cochrane 2009) • Prophylaxie post-AES professionnel : – Échec étude prospective contrôlée – Perte de chance du groupe contrôle La. Fon et al. , ICAAC 1990, – Etude rétrospective : Cardo D et al. , NEJM 1997, – Efficacité admise malgré le faible nombre d’études cliniques (Review Cochrane 2009). • OBJECTIF du TPE: diminuer le risque de transmission du VIH en réduisant la charge virale
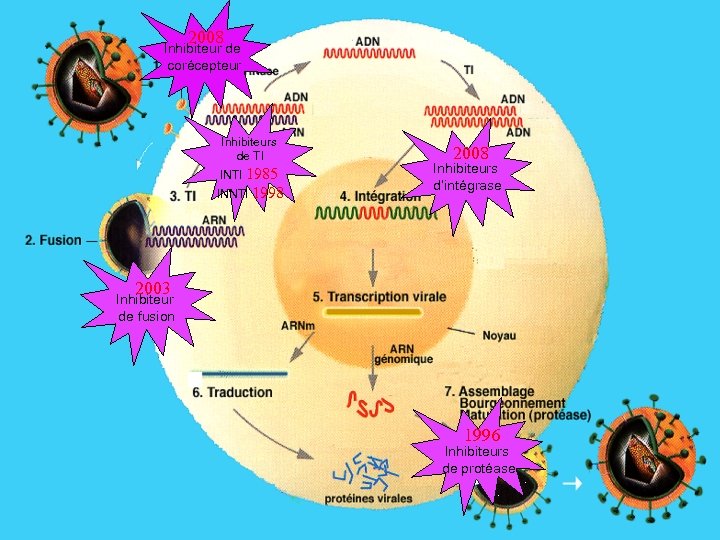 2008 Inhibiteur de corécepteur Inhibiteurs de TI INTI 1985 INNTI 1998 2008 Inhibiteurs d’intégrase 2003 Inhibiteur de fusion 1996 Inhibiteurs de protéase
2008 Inhibiteur de corécepteur Inhibiteurs de TI INTI 1985 INNTI 1998 2008 Inhibiteurs d’intégrase 2003 Inhibiteur de fusion 1996 Inhibiteurs de protéase
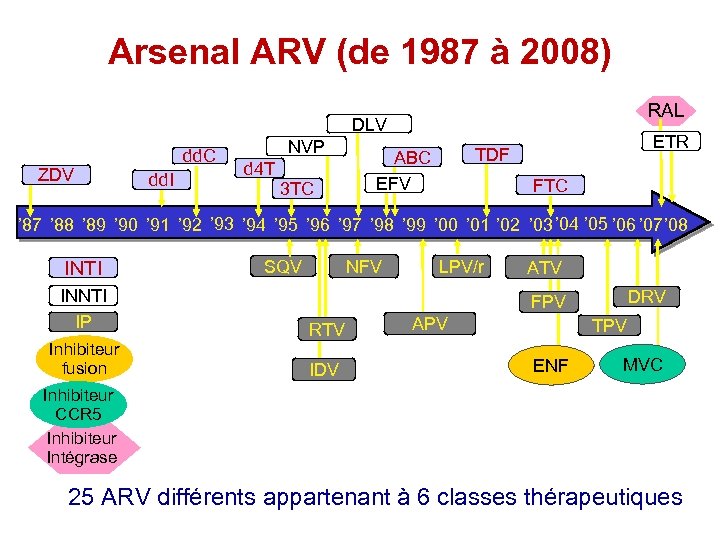 Arsenal ARV (de 1987 à 2008) RAL DLV ZDV dd. C dd. I NVP d 4 T 3 TC ETR TDF ABC EFV FTC ’ 87 ’ 88 ’ 89 ’ 90 ’ 91 ’ 92 ’ 93 ’ 94 ’ 95 ’ 96 ’ 97 ’ 98 ’ 99 ’ 00 ’ 01 ’ 02 ’ 03 ’ 04 ’ 05 ’ 06 ’ 07 ’ 08 INTI SQV NFV INNTI IP RTV Inhibiteur fusion IDV LPV/r ATV DRV FPV APV TPV ENF MVC Inhibiteur CCR 5 Inhibiteur Intégrase 25 ARV différents appartenant à 6 classes thérapeutiques
Arsenal ARV (de 1987 à 2008) RAL DLV ZDV dd. C dd. I NVP d 4 T 3 TC ETR TDF ABC EFV FTC ’ 87 ’ 88 ’ 89 ’ 90 ’ 91 ’ 92 ’ 93 ’ 94 ’ 95 ’ 96 ’ 97 ’ 98 ’ 99 ’ 00 ’ 01 ’ 02 ’ 03 ’ 04 ’ 05 ’ 06 ’ 07 ’ 08 INTI SQV NFV INNTI IP RTV Inhibiteur fusion IDV LPV/r ATV DRV FPV APV TPV ENF MVC Inhibiteur CCR 5 Inhibiteur Intégrase 25 ARV différents appartenant à 6 classes thérapeutiques
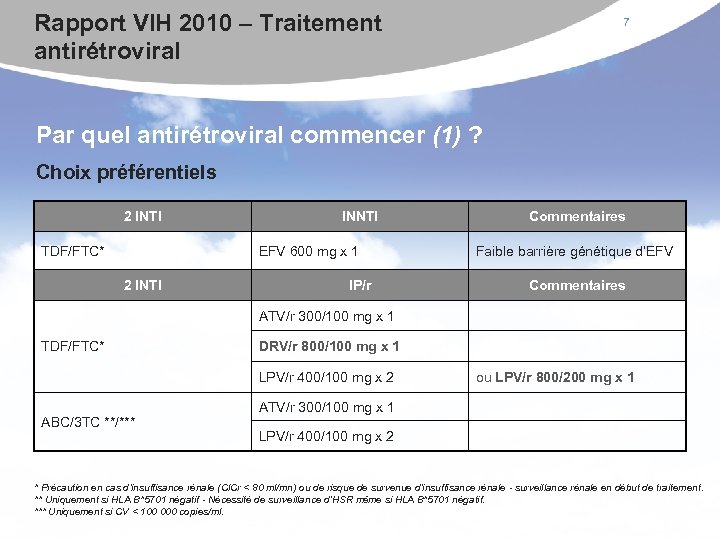 Rapport VIH 2010 – Traitement antirétroviral 7 Par quel antirétroviral commencer (1) ? Choix préférentiels 2 INTI TDF/FTC* INNTI EFV 600 mg x 1 2 INTI IP/r Commentaires Faible barrière génétique d’EFV Commentaires ATV/r 300/100 mg x 1 TDF/FTC* DRV/r 800/100 mg x 1 LPV/r 400/100 mg x 2 ABC/3 TC **/*** ou LPV/r 800/200 mg x 1 ATV/r 300/100 mg x 1 LPV/r 400/100 mg x 2 * Précaution en cas d’insuffisance rénale (Cl. Cr < 80 ml/mn) ou de risque de survenue d’insuffisance rénale - surveillance rénale en début de traitement. ** Uniquement si HLA B*5701 négatif - Nécessité de surveillance d’HSR même si HLA B*5701 négatif. *** Uniquement si CV < 100 000 copies/ml.
Rapport VIH 2010 – Traitement antirétroviral 7 Par quel antirétroviral commencer (1) ? Choix préférentiels 2 INTI TDF/FTC* INNTI EFV 600 mg x 1 2 INTI IP/r Commentaires Faible barrière génétique d’EFV Commentaires ATV/r 300/100 mg x 1 TDF/FTC* DRV/r 800/100 mg x 1 LPV/r 400/100 mg x 2 ABC/3 TC **/*** ou LPV/r 800/200 mg x 1 ATV/r 300/100 mg x 1 LPV/r 400/100 mg x 2 * Précaution en cas d’insuffisance rénale (Cl. Cr < 80 ml/mn) ou de risque de survenue d’insuffisance rénale - surveillance rénale en début de traitement. ** Uniquement si HLA B*5701 négatif - Nécessité de surveillance d’HSR même si HLA B*5701 négatif. *** Uniquement si CV < 100 000 copies/ml.
 Inhibiteurs de la Transcriptase Inverse Inhibiteurs nucléosidiques Inhibiteurs non-nucléosidiques
Inhibiteurs de la Transcriptase Inverse Inhibiteurs nucléosidiques Inhibiteurs non-nucléosidiques
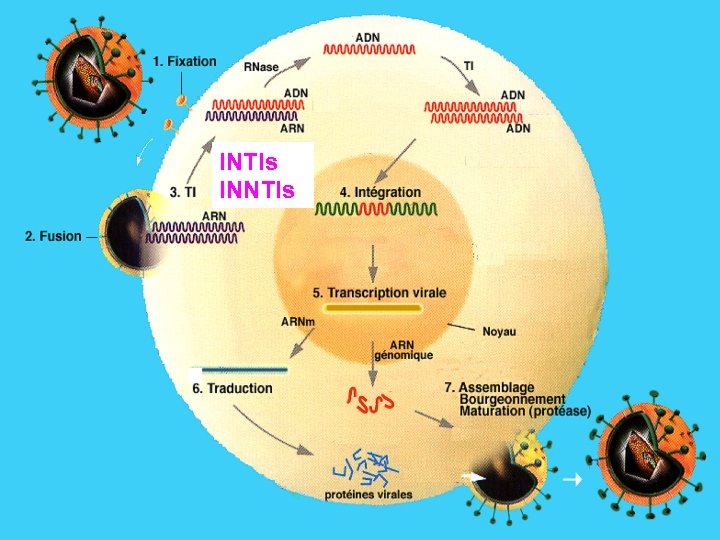 INTIs INNTIs
INTIs INNTIs
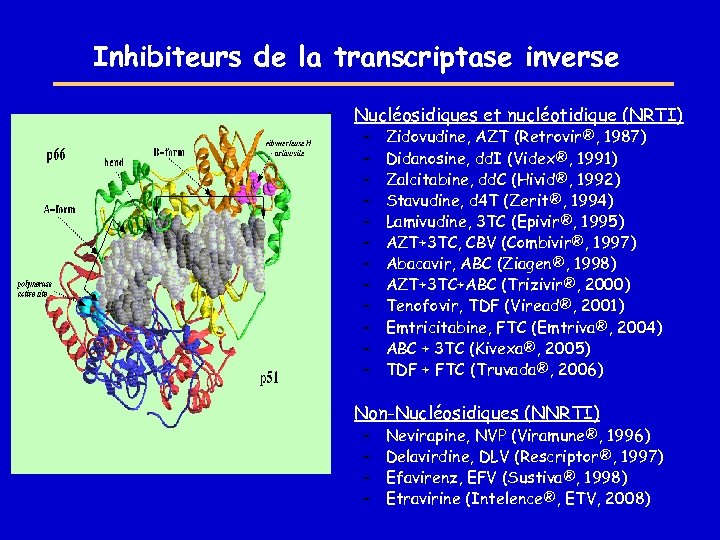 Inhibiteurs de la transcriptase inverse • Nucléosidiques et nucléotidique (NRTI) • Non-Nucléosidiques (NNRTI) – – – – Zidovudine, AZT (Retrovir®, 1987) Didanosine, dd. I (Videx®, 1991) Zalcitabine, dd. C (Hivid®, 1992) Stavudine, d 4 T (Zerit®, 1994) Lamivudine, 3 TC (Epivir®, 1995) AZT+3 TC, CBV (Combivir®, 1997) Abacavir, ABC (Ziagen®, 1998) AZT+3 TC+ABC (Trizivir®, 2000) Tenofovir, TDF (Viread®, 2001) Emtricitabine, FTC (Emtriva®, 2004) ABC + 3 TC (Kivexa®, 2005) TDF + FTC (Truvada®, 2006) Nevirapine, NVP (Viramune®, 1996) Delavirdine, DLV (Rescriptor®, 1997) Efavirenz, EFV (Sustiva®, 1998) Etravirine (Intelence®, ETV, 2008)
Inhibiteurs de la transcriptase inverse • Nucléosidiques et nucléotidique (NRTI) • Non-Nucléosidiques (NNRTI) – – – – Zidovudine, AZT (Retrovir®, 1987) Didanosine, dd. I (Videx®, 1991) Zalcitabine, dd. C (Hivid®, 1992) Stavudine, d 4 T (Zerit®, 1994) Lamivudine, 3 TC (Epivir®, 1995) AZT+3 TC, CBV (Combivir®, 1997) Abacavir, ABC (Ziagen®, 1998) AZT+3 TC+ABC (Trizivir®, 2000) Tenofovir, TDF (Viread®, 2001) Emtricitabine, FTC (Emtriva®, 2004) ABC + 3 TC (Kivexa®, 2005) TDF + FTC (Truvada®, 2006) Nevirapine, NVP (Viramune®, 1996) Delavirdine, DLV (Rescriptor®, 1997) Efavirenz, EFV (Sustiva®, 1998) Etravirine (Intelence®, ETV, 2008)
 Mécanisme d’action des INTIs • INTI sont des prodrogues : nécessite d’être - Inhibiteur précoce duleur incorporation dans la chaîne phosphorylés pour cycle viral d’ADN en cours de formation - Données +++ en prévention • Absence de groupement 3’OH empêche l’addition du - Prodrogue, nécessite d’être phosphorylés dans la cellule d. NTP suivant : terminateur de chaine et blocage de etl’élongation donc n’agissent pas immédiatement P P P Site actif RT P H P P AZT H Base DNA Acid P OH A P AZT A P (mime d. TTP) P AZT A U A RNA C Zidovudine P PO H T A U P P Incorporation INTI C P P P Terminaison de l’élongation du DNA
Mécanisme d’action des INTIs • INTI sont des prodrogues : nécessite d’être - Inhibiteur précoce duleur incorporation dans la chaîne phosphorylés pour cycle viral d’ADN en cours de formation - Données +++ en prévention • Absence de groupement 3’OH empêche l’addition du - Prodrogue, nécessite d’être phosphorylés dans la cellule d. NTP suivant : terminateur de chaine et blocage de etl’élongation donc n’agissent pas immédiatement P P P Site actif RT P H P P AZT H Base DNA Acid P OH A P AZT A P (mime d. TTP) P AZT A U A RNA C Zidovudine P PO H T A U P P Incorporation INTI C P P P Terminaison de l’élongation du DNA
 - Inhibiteur précoce du cycle viral - Agissent rapidement et très puissant - Effet indésirable grave Inhibiteurs non-nucléosidiques : blocage non-compétitif du site actif de l’enzyme
- Inhibiteur précoce du cycle viral - Agissent rapidement et très puissant - Effet indésirable grave Inhibiteurs non-nucléosidiques : blocage non-compétitif du site actif de l’enzyme
 Inhibiteurs de protéase
Inhibiteurs de protéase
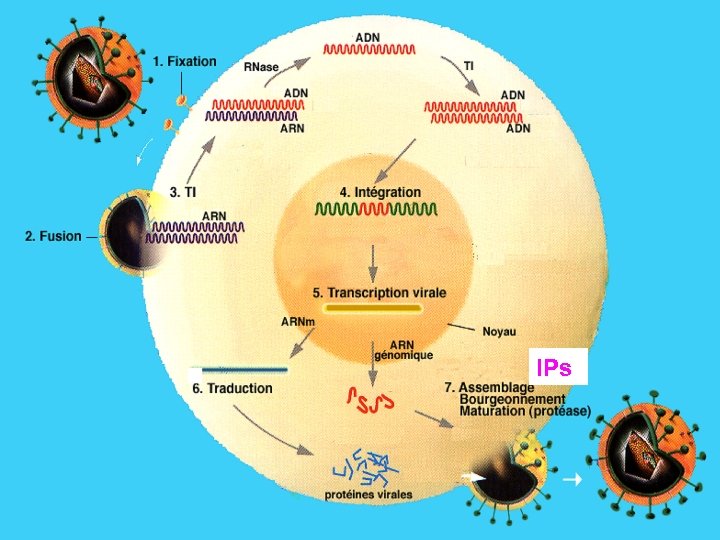 IPs
IPs
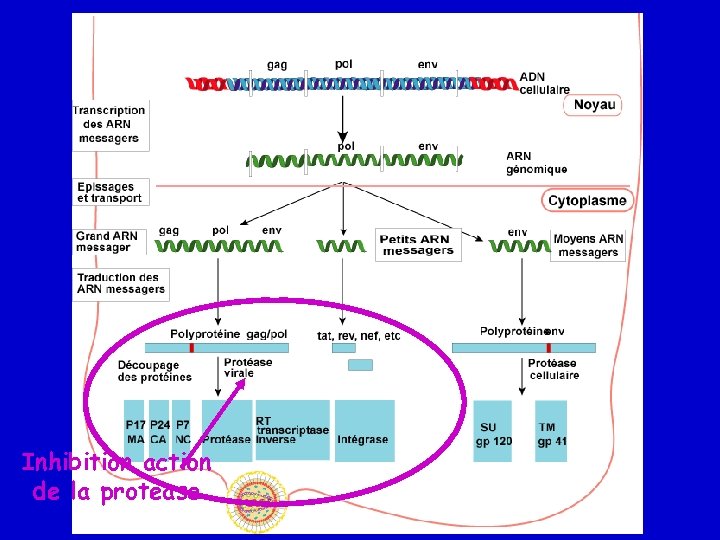 Inhibition action de la protease
Inhibition action de la protease
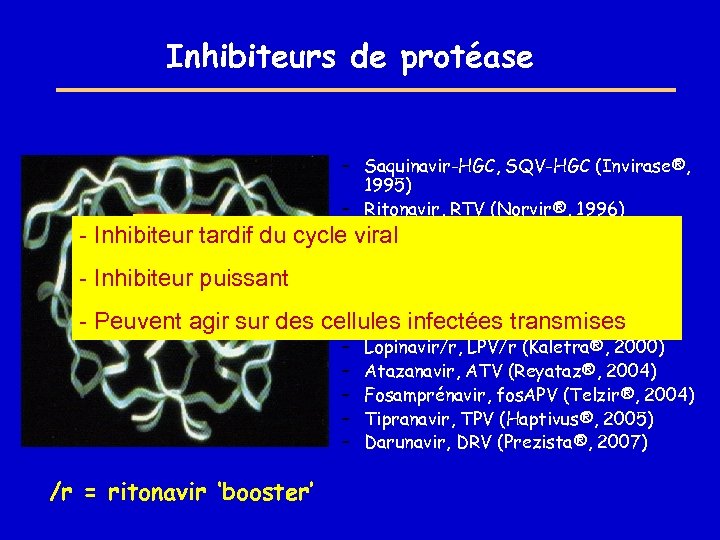 Inhibiteurs de protéase - – Saquinavir-HGC, SQV-HGC (Invirase®, 1995) – Ritonavir, RTV (Norvir®, 1996) – Indinavir, IDV (Crixivan®, 1996) Inhibiteur tardif du cycle viral – Nelfinavir, NFV (Viracept®, 1997) Inhibiteur puissant – Saquinavir-SGC, SQV-SGC (Fortovase®, 1997) Peuvent agir sur des cellules infectées transmises 1999) – Amprenavir, APV (Agenerase®, – Lopinavir/r, LPV/r (Kaletra®, 2000) – Atazanavir, ATV (Reyataz®, 2004) – Fosamprénavir, fos. APV (Telzir®, 2004) – Tipranavir, TPV (Haptivus®, 2005) – Darunavir, DRV (Prezista®, 2007) /r = ritonavir ‘booster’
Inhibiteurs de protéase - – Saquinavir-HGC, SQV-HGC (Invirase®, 1995) – Ritonavir, RTV (Norvir®, 1996) – Indinavir, IDV (Crixivan®, 1996) Inhibiteur tardif du cycle viral – Nelfinavir, NFV (Viracept®, 1997) Inhibiteur puissant – Saquinavir-SGC, SQV-SGC (Fortovase®, 1997) Peuvent agir sur des cellules infectées transmises 1999) – Amprenavir, APV (Agenerase®, – Lopinavir/r, LPV/r (Kaletra®, 2000) – Atazanavir, ATV (Reyataz®, 2004) – Fosamprénavir, fos. APV (Telzir®, 2004) – Tipranavir, TPV (Haptivus®, 2005) – Darunavir, DRV (Prezista®, 2007) /r = ritonavir ‘booster’
 Inhibiteurs d’entrée Inhibiteur de fusion (T 20, Enfuvirtide®, 2003) Inhibiteur des corécepteurs CCR 5 (Maraviroc, Celsentri®, 2008)
Inhibiteurs d’entrée Inhibiteur de fusion (T 20, Enfuvirtide®, 2003) Inhibiteur des corécepteurs CCR 5 (Maraviroc, Celsentri®, 2008)
 Inh co. R IF
Inh co. R IF
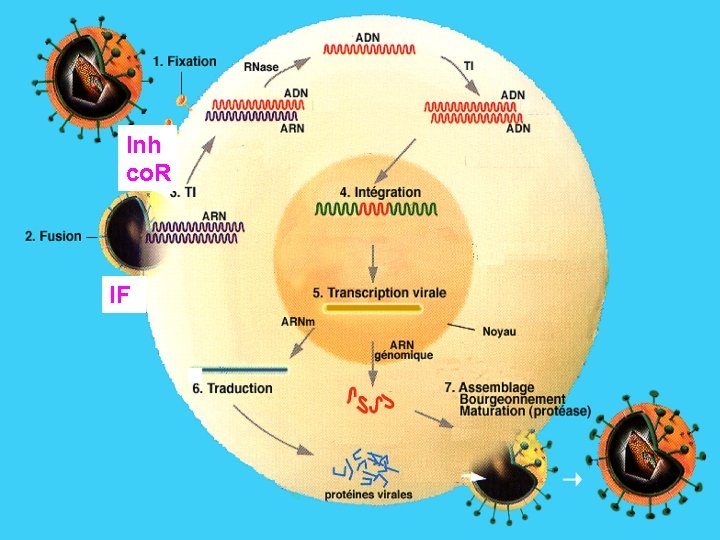
 Inhibiteurs d’entrée -Inhibition très précoce : bloque l’entrée du virus dans la cellule - Inhibiteur de fusion : T 20 , injectable! - Inhibiteur de CCR 5 : ne protège pas de l’infection par des virus CXCR 4 - Pourraient avoir un intérêt mais pas de recul sur leur utilisation comme préventif Ac Monoclonaux anti. CD 4 Inhibiteurs Co. R Inhibiteur de fusion
Inhibiteurs d’entrée -Inhibition très précoce : bloque l’entrée du virus dans la cellule - Inhibiteur de fusion : T 20 , injectable! - Inhibiteur de CCR 5 : ne protège pas de l’infection par des virus CXCR 4 - Pourraient avoir un intérêt mais pas de recul sur leur utilisation comme préventif Ac Monoclonaux anti. CD 4 Inhibiteurs Co. R Inhibiteur de fusion
 Inhibiteurs d’intégrase (Raltégravir, Isentress®, 2008)
Inhibiteurs d’intégrase (Raltégravir, Isentress®, 2008)
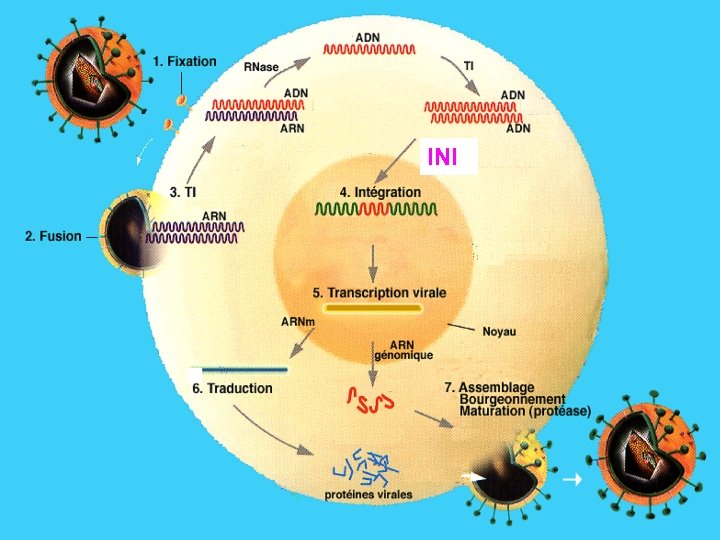 INI
INI
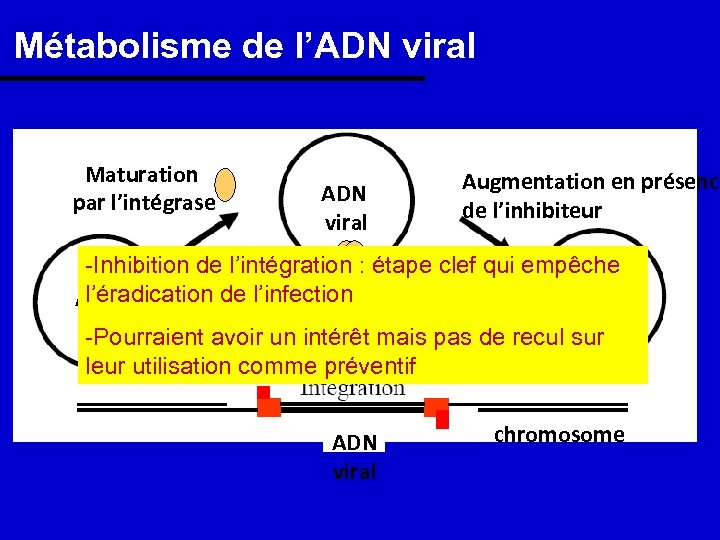 Métabolisme de l’ADN viral Maturation par l’intégrase ADN viral Augmentation en présence de l’inhibiteur -Inhibition de l’intégration : étape clef qui empêche ADN l’éradication de l’infection ADN Blocage viral -Pourraient avoir un intérêt maisl’inhibiteur pas de recul sur leur utilisation comme préventif ADN viral chromosome
Métabolisme de l’ADN viral Maturation par l’intégrase ADN viral Augmentation en présence de l’inhibiteur -Inhibition de l’intégration : étape clef qui empêche ADN l’éradication de l’infection ADN Blocage viral -Pourraient avoir un intérêt maisl’inhibiteur pas de recul sur leur utilisation comme préventif ADN viral chromosome
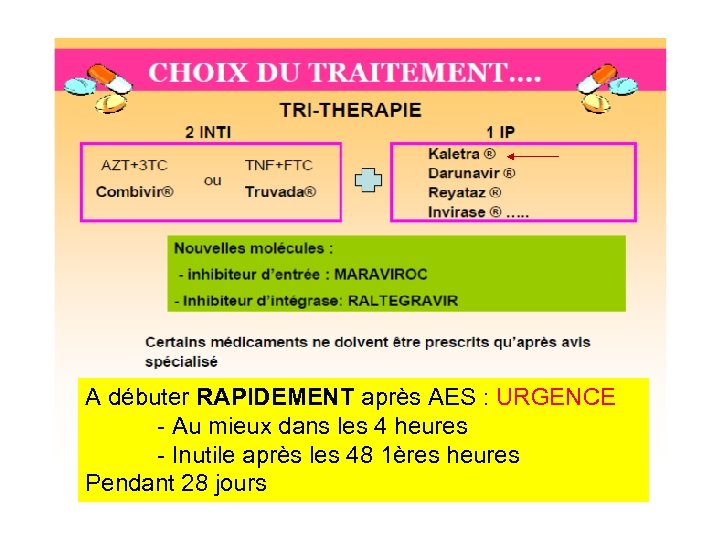 A débuter RAPIDEMENT après AES : URGENCE - Au mieux dans les 4 heures - Inutile après les 48 1ères heures Pendant 28 jours
A débuter RAPIDEMENT après AES : URGENCE - Au mieux dans les 4 heures - Inutile après les 48 1ères heures Pendant 28 jours
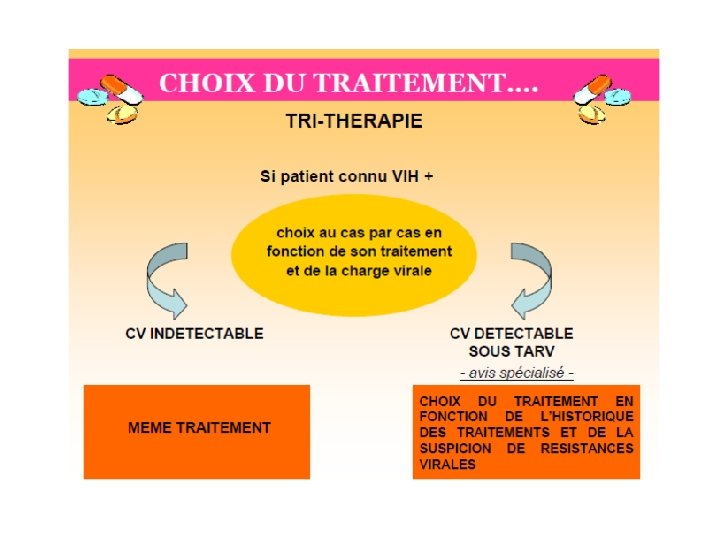
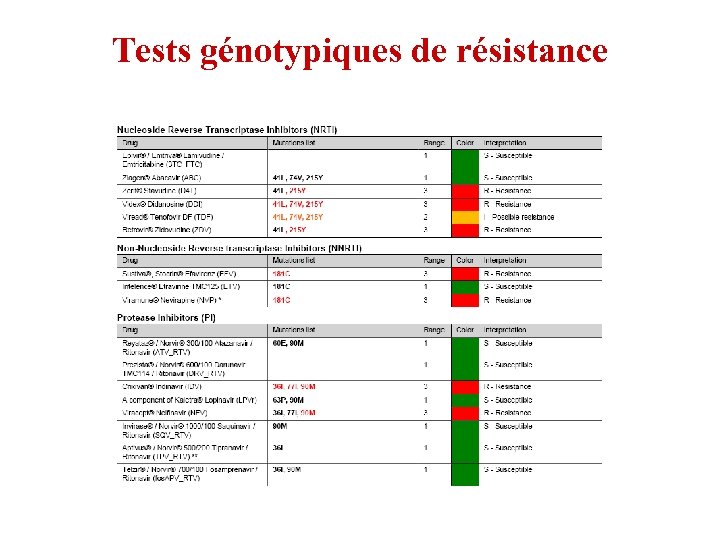 Tests génotypiques de résistance
Tests génotypiques de résistance


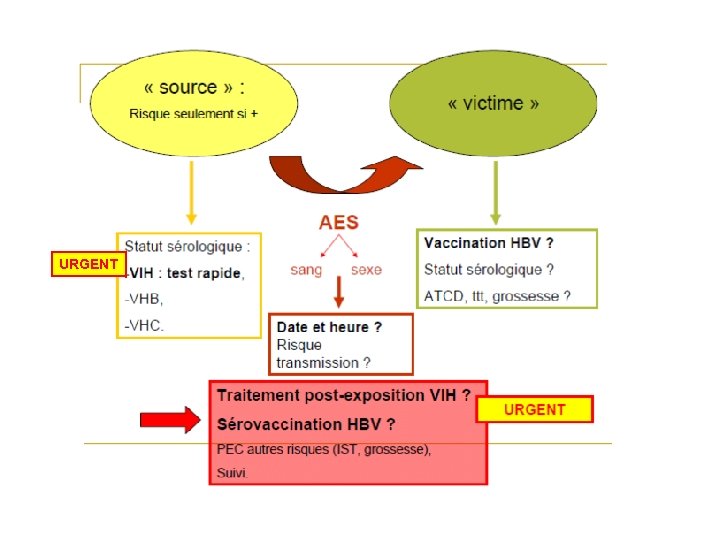 URGENT
URGENT
 Prévenir le labo viro/garde
Prévenir le labo viro/garde
 Tests unitaires rapides de détection des anticorps anti VIH-1 et anti VIH-2 Test rapide non valide négatif non valide positif IMPERATIF : confirmer par un test ELISA
Tests unitaires rapides de détection des anticorps anti VIH-1 et anti VIH-2 Test rapide non valide négatif non valide positif IMPERATIF : confirmer par un test ELISA
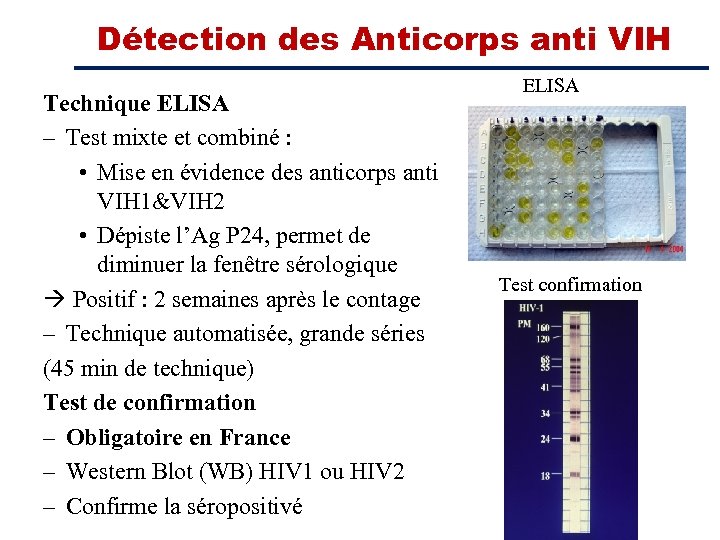 Détection des Anticorps anti VIH Technique ELISA – Test mixte et combiné : • Mise en évidence des anticorps anti VIH 1&VIH 2 • Dépiste l’Ag P 24, permet de diminuer la fenêtre sérologique Positif : 2 semaines après le contage – Technique automatisée, grande séries (45 min de technique) Test de confirmation – Obligatoire en France – Western Blot (WB) HIV 1 ou HIV 2 – Confirme la séropositivé ELISA Test confirmation
Détection des Anticorps anti VIH Technique ELISA – Test mixte et combiné : • Mise en évidence des anticorps anti VIH 1&VIH 2 • Dépiste l’Ag P 24, permet de diminuer la fenêtre sérologique Positif : 2 semaines après le contage – Technique automatisée, grande séries (45 min de technique) Test de confirmation – Obligatoire en France – Western Blot (WB) HIV 1 ou HIV 2 – Confirme la séropositivé ELISA Test confirmation
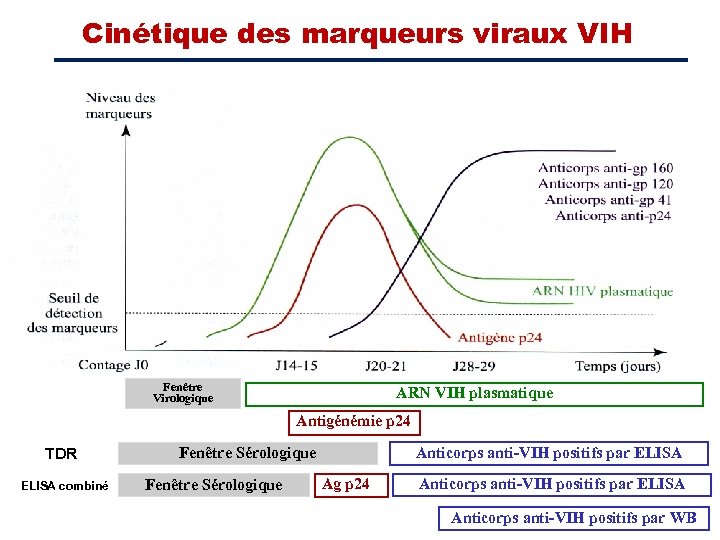 Cinétique des marqueurs viraux VIH Fenêtre Virologique ARN VIH plasmatique Antigénémie p 24 TDR ELISA combiné Fenêtre Sérologique Anticorps anti-VIH positifs par ELISA Ag p 24 Anticorps anti-VIH positifs par ELISA Anticorps anti-VIH positifs par WB
Cinétique des marqueurs viraux VIH Fenêtre Virologique ARN VIH plasmatique Antigénémie p 24 TDR ELISA combiné Fenêtre Sérologique Anticorps anti-VIH positifs par ELISA Ag p 24 Anticorps anti-VIH positifs par ELISA Anticorps anti-VIH positifs par WB
 Diagnostic et suivi d'une Hépatite C 4 Test de première intention (diagnostic indirect) pour le dépistage comme le diagnostic u test anticorps anti-VHC (EIA) u Positif 50 jours après contage 4 Recherche du génome VHC (diagnostic direct) u u PCR ARN VHC Détectable entre 7 à 21 jours après contage
Diagnostic et suivi d'une Hépatite C 4 Test de première intention (diagnostic indirect) pour le dépistage comme le diagnostic u test anticorps anti-VHC (EIA) u Positif 50 jours après contage 4 Recherche du génome VHC (diagnostic direct) u u PCR ARN VHC Détectable entre 7 à 21 jours après contage
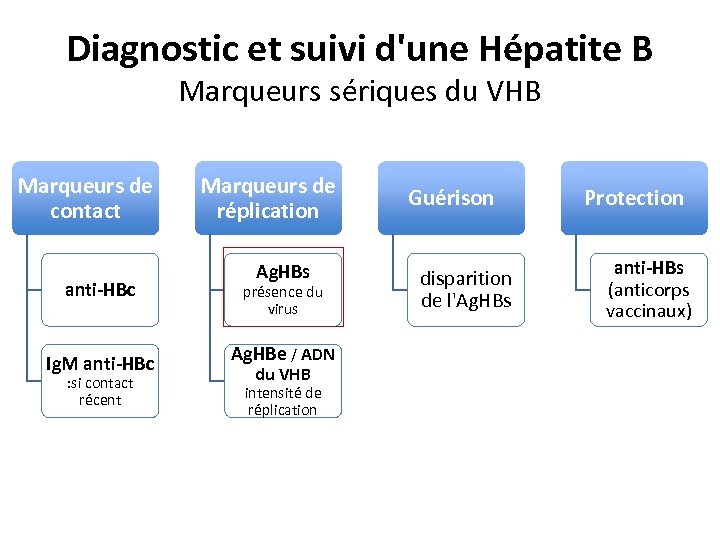 Diagnostic et suivi d'une Hépatite B Marqueurs sériques du VHB Marqueurs de contact anti-HBc Ig. M anti-HBc : si contact récent Marqueurs de réplication Ag. HBs présence du virus Ag. HBe / ADN du VHB intensité de réplication Guérison disparition de l'Ag. HBs Protection anti-HBs (anticorps vaccinaux)
Diagnostic et suivi d'une Hépatite B Marqueurs sériques du VHB Marqueurs de contact anti-HBc Ig. M anti-HBc : si contact récent Marqueurs de réplication Ag. HBs présence du virus Ag. HBe / ADN du VHB intensité de réplication Guérison disparition de l'Ag. HBs Protection anti-HBs (anticorps vaccinaux)

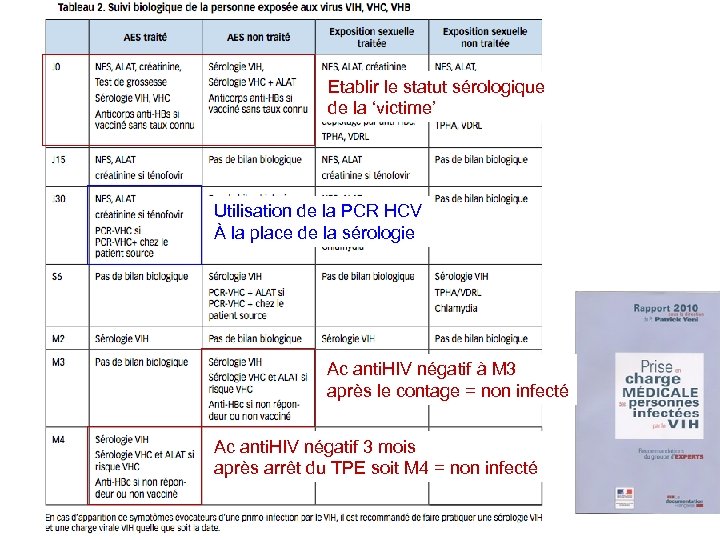 Etablir le statut sérologique de la ‘victime’ Utilisation de la PCR HCV À la place de la sérologie Ac anti. HIV négatif à M 3 après le contage = non infecté Ac anti. HIV négatif 3 mois après arrêt du TPE soit M 4 = non infecté
Etablir le statut sérologique de la ‘victime’ Utilisation de la PCR HCV À la place de la sérologie Ac anti. HIV négatif à M 3 après le contage = non infecté Ac anti. HIV négatif 3 mois après arrêt du TPE soit M 4 = non infecté


