д элем э.pptx
- Количество слайдов: 37

*F элементы

f-блок в периодической таблице элементов — электронная оболочка атомов, валентные электроны которых с наивысшей энергией занимают f-орбиталь. В данный блок входят актиноиды и лантаноиды. Фактическая электронная конфигурация элементов, входящих в этот блок, может отличаться от истинной и не может не подпадать под определение правила Клечковского. Данный блок делится на две группы: Элементы, у которых электроны находятся на 4 f-орбитали, относятся к лантаноидам, Элементы, у которых электроны находятся на 5 f-орбитали, относятся к актиноидам. Существует давний спор относительно того какие элементы следует относить к данным группам: актиний и лантан, или же лютеций и лоуренсий. Это связано с тем, что количество f-электронов, находящихся на внешнем электронном слое, может быть только 14


f-Элементы делятся на лантаноиды и актиноиды. Лантаноиды – это 14 элементов, следующих за лантаном, у которых к электронной конфигурации лантана последовательно добавляются 14 4 f-электронов. Общая электронная конфигурация лантаноидов – 4 f 2– 145 d 0– 16 s 2. У церия на 4 f-уровне находятся два электрона – один за счет увеличения порядкового номера по сравнению с лантаном на единицу, а другой переходит с 5 d-уровня на 4 f. До гадолиния происходит последовательное увеличение числа электронов на 4 f-уровне, а уровень 5 d остается незанятым. У гадолиния дополнительный электрон занимает 5 d-уровень, давая электронную конфигурацию 4 f 75 d 16 s 2, а у следующего за гадолинием тербия происходит, аналогично церию, переход 5 d-электрона на 4 f-уровень (4 f 96 s 2). Далее до иттербия наблюдается монотонное увеличение числа электронов до 4 f 14, а у завершающего ряд лютеция вновь появляется 5 d-электрон (4 f 145 d 16 s 2).
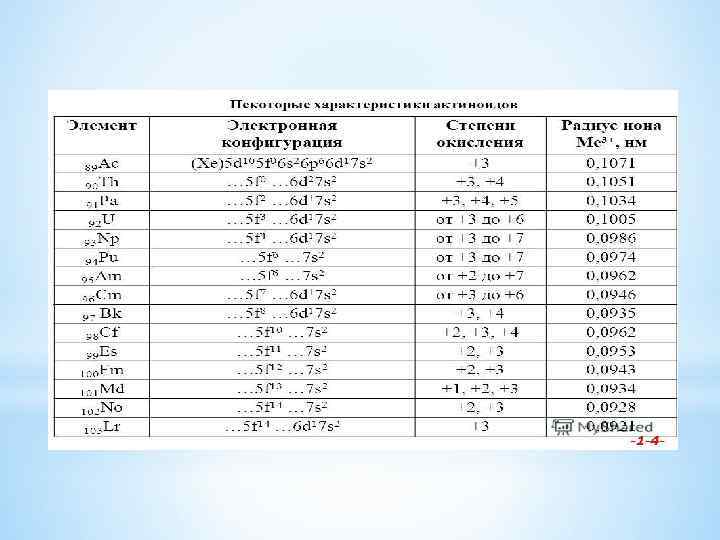
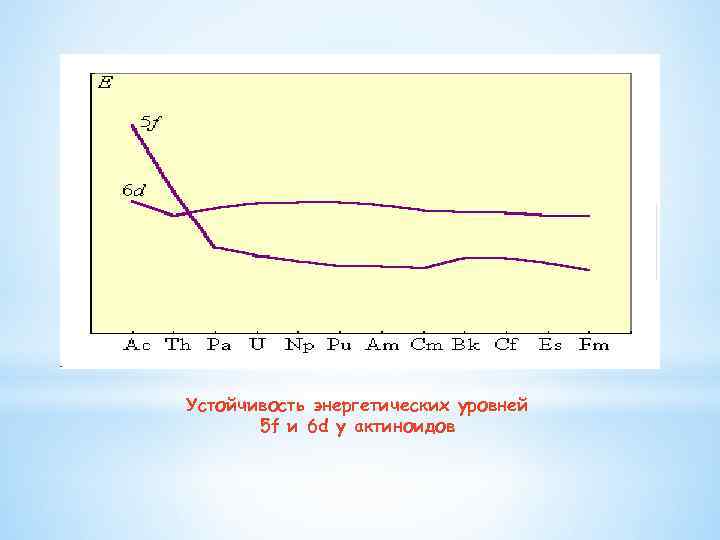
Устойчивость энергетических уровней 5 f и 6 d у актиноидов

Отличия актиноидов и лантаноидов что у актиноидов энергетические уровни 5 f и 6 d стабилизируются по мере возрастания атомного ядра несколько иным способом, чем у лантаноидов: у легких актиноидов более устойчивы 6 d-орбитали, а у тяжелых – 5 f Для элементов с атомными номерами 90– 95 энергия 5 f- и 6 dподуровней примерно одинакова. Этим объясняются различия в химии актиноидов и лантаноидов. У элементов с атомными номерами 91– 95 (Th–Am) электронные переходы происходят легко. Эти элементы поливалентны и в этом подобны d-элементам. Более того, для них степень окисления III вообще мало характерна. Получен семивалентный нептуний, уран легко может быть переведен в шестивалентное состояние, протактиний проявляет степень окисления пять, а для тория трудно получить соединения, в которых он имел бы степень окисления ниже четырех. Однако по мере заполнения 5 f-уровней электронные конфигурации атомов стабилизируются, переход 5 f-электронов в 6 d-состояние становится все более затрудненным. Поэтому элементы Bk–Lr, ведут себя как типичные f-элементы, а по свойствам близки к лантаноидам. Для них основной степенью окисления является III.

С водородом актиноиды образуют гидриды переменного состава (Th. H 2, Th 4 H 15; Pa. H 2– 2, 7; Am. H 2– 2, 7), но для урана можно получить и стехиометрический гидрид UH 3. В общем случае гидриды этих элементов термически менее устойчивы, чем гидриды 4 f-элементов. С кислородом актиноиды образуют оксиды, соответствующие их наиболее устойчивым степеням окисления (Th. O 2, Pa 2 O 5, Np. O 2 и др. ). К исключительно сложным следует отнести систему уран–кислород. Характерными для урана являются оксиды UO 2 – UO 2, 25; U 3 O 8 и UO 3, из них наиболее устойчив U 3 O 8 (UO 2∙ 2 UO 3) – урановая смолка. Отличительной особенностью кислородсодержащих соединений актиноидов в высших степенях окисления V, VI является наличие катионных группировок и или , . Эти группировки называются иловыми оксоионами. Например, – уранил, – протактинил. Оксоионы устойчивы и сохраняются без изменения в разнообразных химических реакциях:

Особая устойчивость оксоионов объясняется тем, что связь между атомами актиноида и кислорода формально можно рассматривать как тройную: Для ионов прочность связи увеличивается в ряду Am < Pu < Np. С галогенами актиноиды образуют многообразные галогениды ЭГn, где n = 3, 4, 5, 6. Фториды элементов в высших степенях окисления летучи, что позволило разделить изотопы урана 235 U и 238 U. Взаимодействие актиноидов с B, Si, C, N, P, S и Se приводит к образованию соединений нестехиометрического состава вследствие возможного присутствия элемента в разных степенях окисления. Уменьшение радиусов элементов в ряду Th–Lr приводит к ослаблению основных свойств соединений. Соединения актиноидов склонны к диспропорционированию.


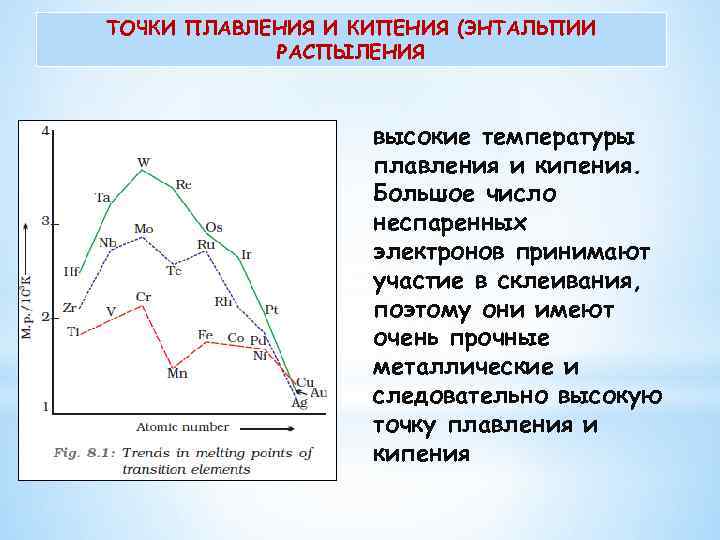
ТОЧКИ ПЛАВЛЕНИЯ И КИПЕНИЯ (ЭНТАЛЬПИИ РАСПЫЛЕНИЯ высокие температуры плавления и кипения. Большое число неспаренных электронов принимают участие в склеивания, поэтому они имеют очень прочные металлические и следовательно высокую точку плавления и кипения
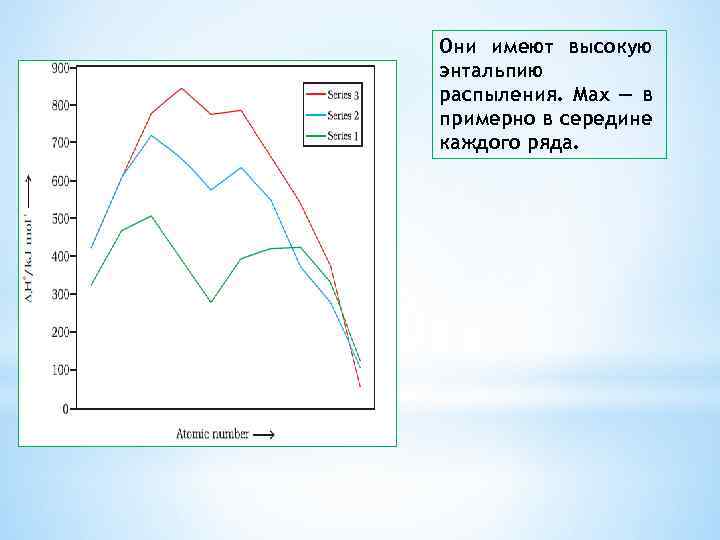
Они имеют высокую энтальпию распыления. Max — в примерно в середине каждого ряда.
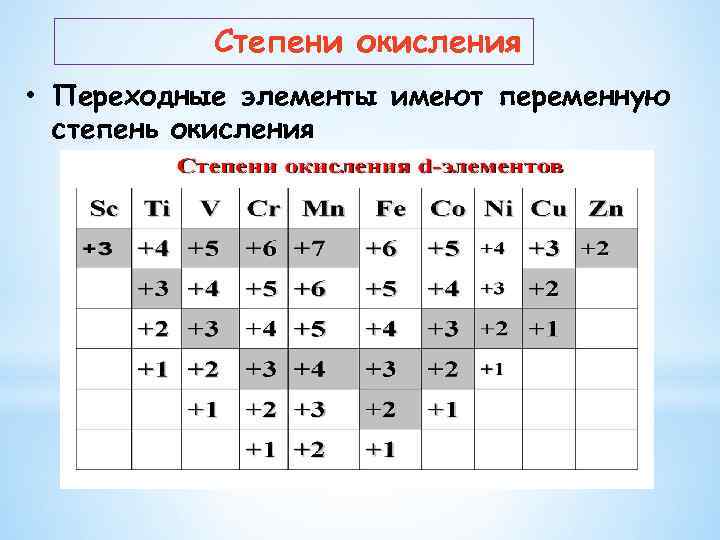
Степени окисления • Переходные элементы имеют переменную степень окисления

ЦВЕТНЫЕ ИОНЫ Большинство соединений переходных металлов (ионный а также ковалентные) окрашены как в твердом состоянии и в водном растворе. Обычно элементы/ионов, непарные электронов производят цветные соединения.
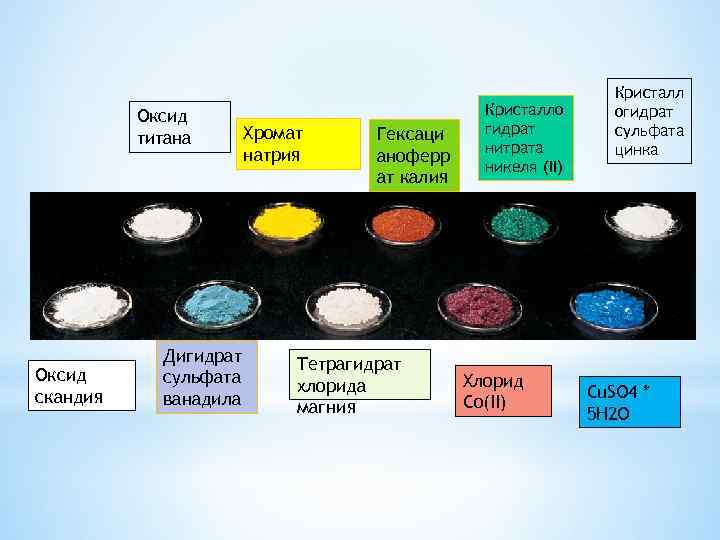
Оксид титана Оксид скандия Дигидрат сульфата ванадила Хромат натрия Гексаци аноферр ат калия Тетрагидрат хлорида магния Кристалло гидрат нитрата никеля (II) Хлорид Co(II) Кристалл огидрат сульфата цинка Cu. SO 4 * 5 H 2 O

Химические свойства d-элементов Сравнение d- и р-элементов в высших СО Группа VII р-элементы HCl. O 4 H 2 SO 4 VI V HPO 3 (HNO 3) d-элементы HMn. O 4 H 2 Cr. O 4 HVO 3

VIIB Mn: II, IV, VII Tc (IV, V) VII Re VIB Cr: II, III, VI Mo (IV, V), VI W VB V: II, IV, V Nb Ta (III, IV), V Устойчивость высшей степени окисления в В-подгруппах В отличии от s- и p-элементов у d-элементов устойчивость высшей СО возрастает вниз по подгруппе:
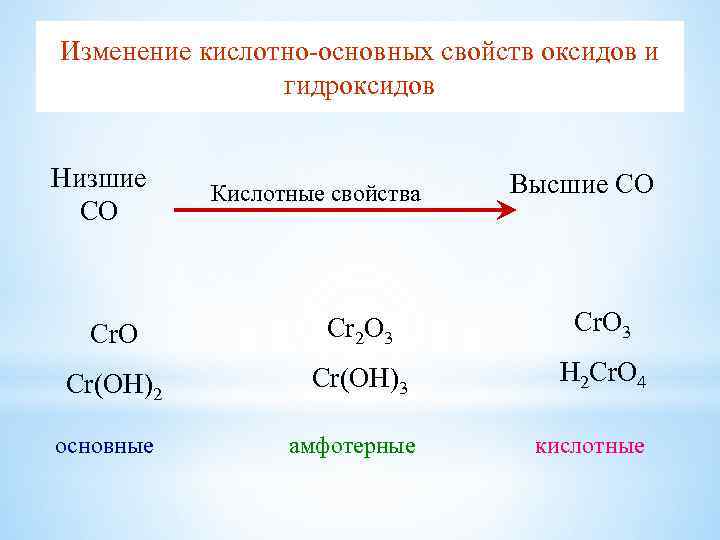
Изменение кислотно-основных свойcтв оксидов и гидроксидов Низшие СО Кислотные свойства Высшие СО Cr. O Cr 2 O 3 Cr(OH)2 Cr(OH)3 H 2 Cr. O 4 амфотерные кислотные основные
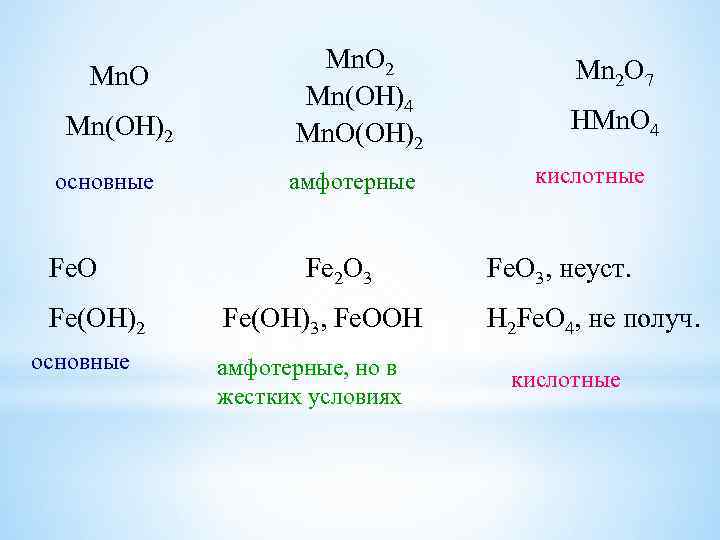
Mn. O Mn(OH)2 основные Fe. O Fe(OH)2 основные Mn. O 2 Mn(OH)4 Mn. O(OH)2 амфотерные Fe 2 O 3 Fe(OH)3, Fe. OOH амфотерные, но в жестких условиях Mn 2 O 7 HMn. O 4 кислотные Fe. O 3, неуст. H 2 Fe. O 4, не получ. кислотные
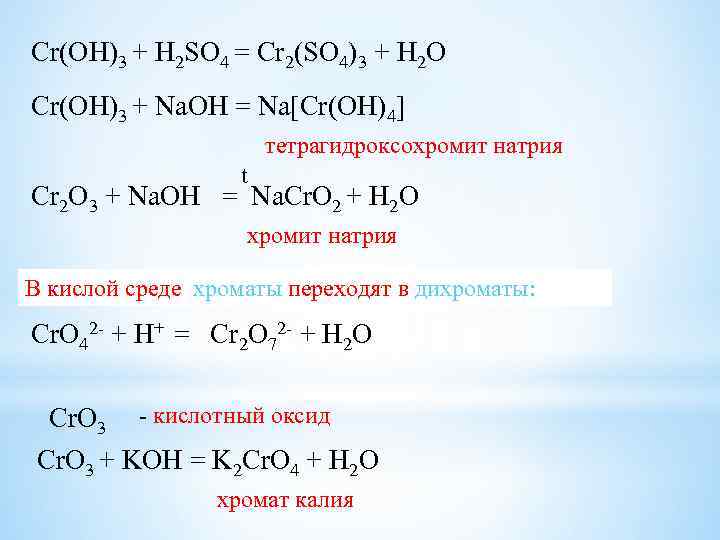
Cr(OH)3 + H 2 SO 4 = Cr 2(SO 4)3 + H 2 O Cr(OH)3 + Na. OH = Na[Cr(OH)4] тетрагидроксохромит натрия t Cr 2 O 3 + Na. OH = Na. Cr. O 2 + H 2 O хромит натрия В кислой среде хроматы переходят в дихроматы: Сr. O 42 - + H+ = Cr 2 O 72 - + H 2 O Сr. O 3 - кислотный оксид Cr. O 3 + KOH = K 2 Cr. O 4 + H 2 O хромат калия

Fe 2 O 3 - обладает амфотерными свойствами, но в жестких условиях: Fe 2 O 3 + HCl = Fe. Cl 3 + H 2 O t Fe 2 O 3 + KOH = KFe. O 2 + H 2 O феррит калия Ферриты - соли железистой кислоты HFe. O 2 Амфотерными являются оксид и гидроксид цинка: Zn. O, Zn(OH)2 Zn + HCl = Zn. Cl 2 + H 2 Zn + Na. OH + H 2 O = Na 2[Zn(OH)4] + H 2 Zn. O + Na. OH = Na 2[Zn(OH)4]

Изменение восстановительных свойств d-элементов V 2+, Cr 2+… Энергичные восстановители V 2+ Cr 2+ Ni 2+…. Окисляется только сильными окислителями Mn 2+ Zn 2+ Восстановителем не является Fe 2+ … Ni 2+ …Zn 2+ Восстановительные свойства
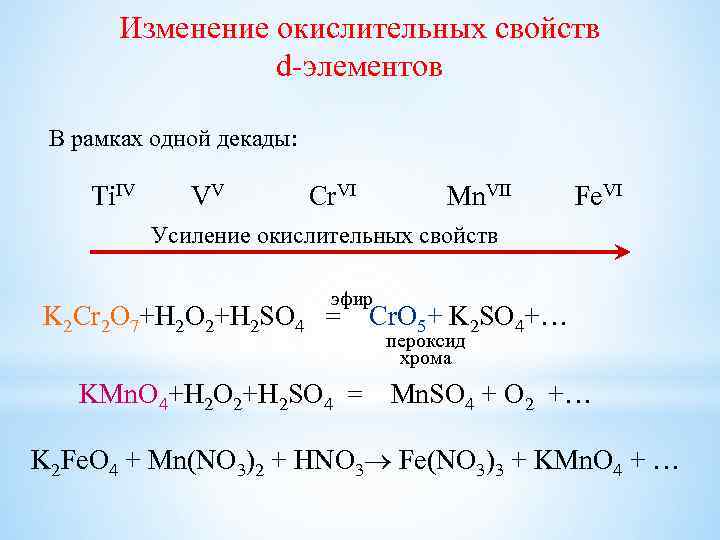
Изменение окислительных свойств d-элементов В рамках одной декады: Ti. IV VV Cr. VI Mn. VII Fe. VI Усиление окислительных свойств эфир K 2 Cr 2 O 7+H 2 O 2+H 2 SO 4 = KMn. O 4+H 2 O 2+H 2 SO 4 = Cr. O 5+ K 2 SO 4+… пероксид хрома Mn. SO 4 + O 2 +… K 2 Fe. O 4 + Mn(NO 3)2 + HNO 3 Fe(NO 3)3 + KMn. O 4 + …

В степени +II соединения хрома являются сильными восстановителями: Cr(OH)2 + H 2 O + O 2 = Cr(OH)3 Cоли Fe(II) легко окисляются и переходят в Fe(III) Fe. SO 4 + Cl 2 = Fe. Cl 3 + Fe 2(SO 4)3 Окисление солей железа (III) в щелочной среде приводит к образованию ферратов - соединений железа (VI) t Fe 2 O 3 + Cl 2 + KOH = K 2 Fe. O 4 + KCl + H 2 O окислительно-щелочное плавление

Дихроматы и хроматы являются сильными окислителями: K 2 Cr 2 O 7 + KJ + H 2 SO 4 = J 2 + Cr 2(SO 4)3 + K 2 SO 4 + H 2 O Перманганаты - сильнейшие окислители: Mn 2+ Mn. O 2 (p. H 7) Mn. O 42 - Mn. O 4 - (p. H 7) Ферраты - сильнейшие окислители
![Для d-элементов характерно образование комплексных соединений. Co. Cl 2 + 4 KSCN K 2[Co(SCN)4] Для d-элементов характерно образование комплексных соединений. Co. Cl 2 + 4 KSCN K 2[Co(SCN)4]](https://present5.com/presentation/247523521_444165478/image-27.jpg)
Для d-элементов характерно образование комплексных соединений. Co. Cl 2 + 4 KSCN K 2[Co(SCN)4] + 2 KCl Эту способность используют: 1) для очистки d-элементов от примесей Ni + 4 CO = [Ni(CO)4] Тетракарбонил никель Карбонилы являются особым типом комплексных соединений. [Fe(CO)5] пентакарбонил железа [Co(CO)4] тетракарбонил кобальта

РЯД НАПРЯЖЕНИЙ МЕТАЛЛОВ Li Cs Ca Na Mg Al Zn Fe Ni Pb H 2 Cu Ag Hg Au Усиление восстановительной способности атомов Li+Ca 2+Na+Mg 2+Al 3+Zn 2+Fe 2+Ni 2+Pb 2+H+Cu 2+Ag+Hg 2+Au 3+ Усиление окислительной способности ионов

Растворение металлов в кислотах и щелочах 1. Кислоты неокислители: HCl, H 2 SO 4, HBr… Zn + HCl = H 2 + Zn. Cl 2 Fe + HCl = H 2 + Fe. Cl 2 2. Кислоты окислители: HNO 3, H 2 SO 4 конц, … Hg + HNO 3 изб = Hg(NO 3)2 + NO + H 2 O Cd + H 2 SO 4 конц = Cd. SO 4 + SO 2 + H 2 O Sn + HNO 3 конц = H 2 Sn. O 3 + NO 2 + H 2 O - оловянная кислота
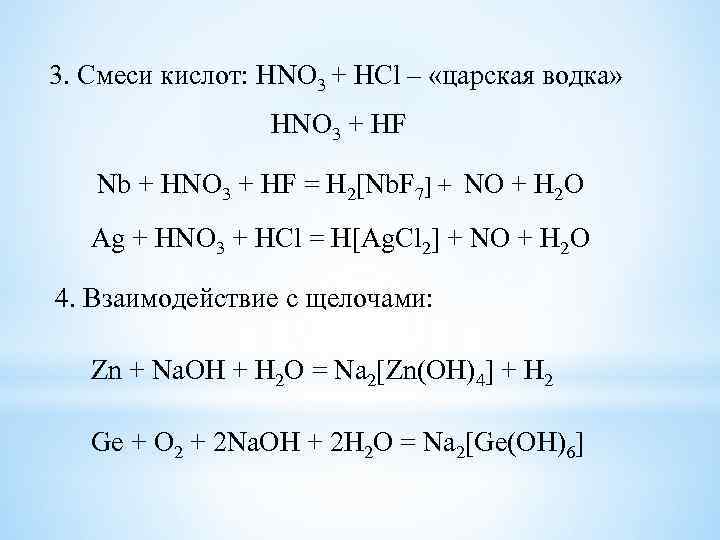
3. Смеси кислот: HNO 3 + HCl – «царская водка» HNO 3 + HF Nb + HNO 3 + HF = H 2[Nb. F 7] + NO + H 2 O Ag + HNO 3 + HCl = H[Ag. Cl 2] + NO + H 2 O 4. Взаимодействие с щелочами: Zn + Na. OH + H 2 O = Na 2[Zn(OH)4] + H 2 Ge + O 2 + 2 Na. OH + 2 H 2 O = Na 2[Ge(OH)6]
2 5. Взаимодействие с гидратом аммиака: Zn + NH 3·H 2 O = [Zn(NH 3)4](OH)2](https://present5.com/presentation/247523521_444165478/image-31.jpg)
5. Взаимодействие с гидратом аммиака: Zn + NH 3·H 2 O = [Zn(NH 3)4](OH)2 + H 2↑ Cd + O 2 + NH 3· H 2 O = [Cd(NH 3)4](OH)2 + H 2 O 6. Окислительное щелочное плавление (V, Nb, Ta, Cr, MO, W…): V + O 2 + Na 2 CO 3 = Na 3 VO 4 + CO 2 Cr + O 2 + Na. OH = Na 2 Cr O 4 + H 2 O Полученные соли легко растворяются в воде

Cпособы получения металлов Определяются характером сырья (рудой) 1. Пирометаллургия – окислительный обжиг сульфидов и восстановление металлов из оксидов при высокой температуре. Fe. S 2 + O 2 = Fe 2 O 3 + SO 2 Fe 2 O 3 + CO Fe + CO 2 2. Электрометаллургия - электролиз расплавов или растворов солей электролиз Zn. SO 4 + H 2 O Zn + O 2 + H 2 SO 4

3. Гидрометаллургия - выделение металлов из растворов их солей более активными металлами Cd. SO 4 + Zn цементация Cd + Zn. SO 4

Гидрометаллургический способ извлечения золота 1. Au + KCN + O 2 + H 2 O = K[Au(CN)2] + KOH K[Au(CN)2] + Zn = K 2[Zn(CN)4] + Au цементация золота 2. Растворение золота в ртути с последующей разгонкой амальгамы. Амальгама – сплав Hg с металлами (Zn, Cu, щелочные металлы).
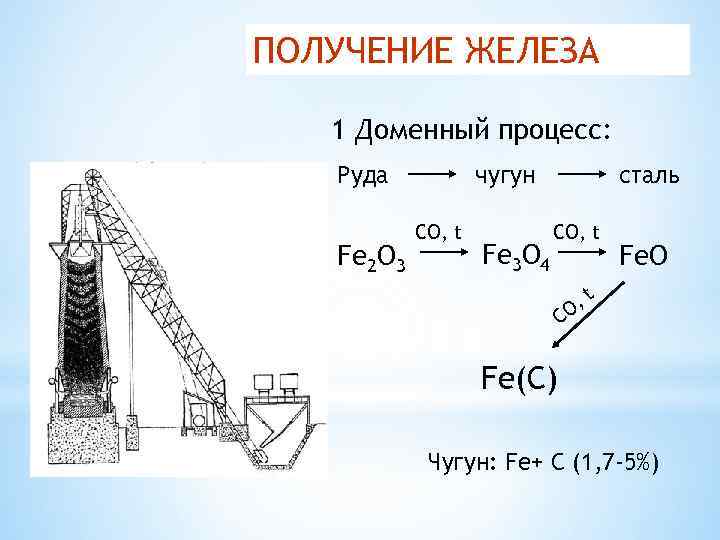
ПОЛУЧЕНИЕ ЖЕЛЕЗА 1 Доменный процесс: Руда Fe 2 O 3 чугун CO, t Fe 3 O 4 сталь CO, t Fe. O , t O C Fe(C) Чугун: Fe+ C (1, 7 -5%)

Получение металла высокой чистоты 1. Разложение карбонильных комплексов (Ni, Co, Cr…) Fe + 5 CO Порошок Pt, t [Fe(CO)5] = Fe(CO)5 желтая жидкость пентакарбонил железо 160 -200 о. С Fe + 5 CO Железо высокой чистоты 2. Иодидное рафинирование. 3. Электролиз водных растворов солей.

д элем э.pptx