Медицинская биология_клетка.ppt
- Количество слайдов: 97
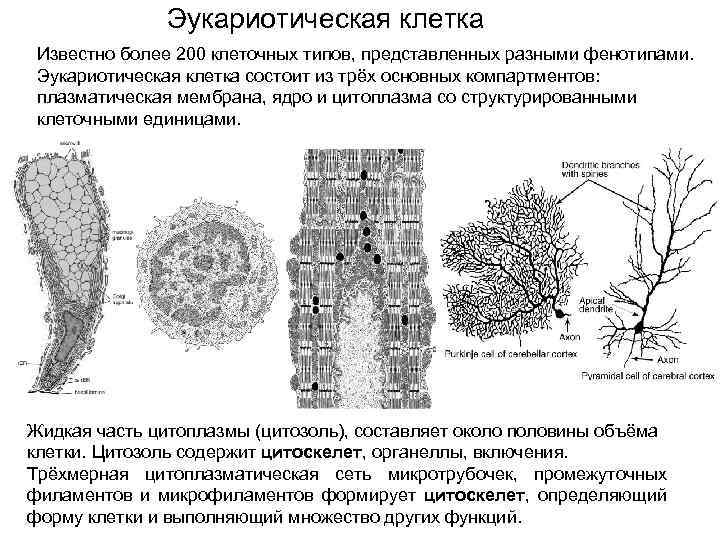
Эукариотическая клетка Известно более 200 клеточных типов, представленных разными фенотипами. Эукариотическая клетка состоит из трёх основных компартментов: плазматическая мембрана, ядро и цитоплазма со структурированными клеточными единицами. Жидкая часть цитоплазмы (цитозоль), составляет около половины объёма клетки. Цитозоль содержит цитоскелет, органеллы, включения. Трёхмерная цитоплазматическая сеть микротрубочек, промежуточных филаментов и микрофиламентов формирует цитоскелет, определяющий форму клетки и выполняющий множество других функций.

Клеточный тип ØОднородные группы клеток образуют клеточные популяции ØПопуляции разных клеточных типов формируют разные ткани организма ØКлеточный тип включает понятие клеточные фенотипы, а также пластичность и границы нормы клеточного типа. ØКлетки с идентичным набором разрешённых к экспрессии генов относятся к одному клеточному типу. Каждая скелетная мышца уникальна по спектру входящих в её состав мышечных волокон. Фенотип мышцы генетически детерминирован, а экспрессия того или иного признака зависит от активности специфических генов, регулируемых нервной и гуморальной системами. При различных функциональных и патологических состояниях организма структурно-функциональные характеристики мышцы изменяются в широких пределах, что является проявлением мышечной пластичности. Типы мышечных волокон Миозин Митохонд рии Миогло бин Утомля емость Гликоген быстрые красные быстрый IIa много высокое медленно высокое быстрые белые IIb быстрый немного низкое утомля емые медленные медленны много высокое медленно низкое высокое

Фенотипы скелетных мышечных волокон Гистохимическое выявление активности АТФазы миозина и сукцинатдегидрогеназы (СДГ). A — активность АТФазы миозина: тип I — медленносокращающиеся; II — быстросокращающиеся. Б — активность СДГ: А — белое (гликолитическое); B — промежуточное (окислительногликолитическое); C — красное (окислительное).

Органеллы эукариотической клетки

Согласно жидкостно-мозаичной модели, предложенной Nicholson. Singer, плазматическая мембрана — жидкая динамическая система с мозаичным расположением белков и липидов. Липиды составляют до 45% массы мембран. Липидные плотики (рафты) — дискретные мембранные домены, богатые сфинголипидами и холестерином. Рафты перемещаются в мембране латерально и могут связывать различные мембранные белки, участвуют в эндоцитозе и способны модифицировать сигнальные каскады.
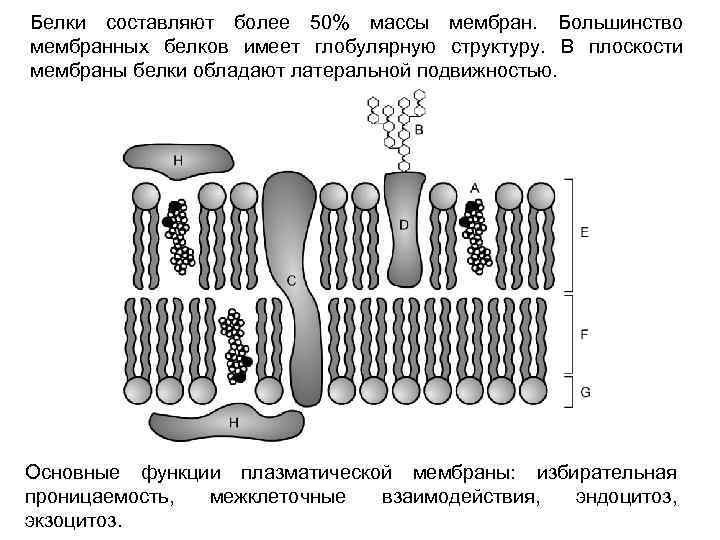
Белки составляют более 50% массы мембран. Большинство мембранных белков имеет глобулярную структуру. В плоскости мембраны белки обладают латеральной подвижностью. Основные функции плазматической мембраны: избирательная проницаемость, межклеточные взаимодействия, эндоцитоз, экзоцитоз.

Избирательная проницаемость Трансмембранная избирательная проницаемость поддерживает клеточный гомеостаз, оптимальное содержание в клетке ионов, воды, ферментов и субстратов. Неполярные вещества (например, холестерин и его производные) свободно проникают через биологические мембраны. Трансмембранный перенос полярных соединений осуществляют специальные системы, встроенные в биологические мембраны. Пути реализации избирательной проницаемости мембран: Øпассивный транспорт, Øоблегчённая диффузия, Øактивный транспорт.
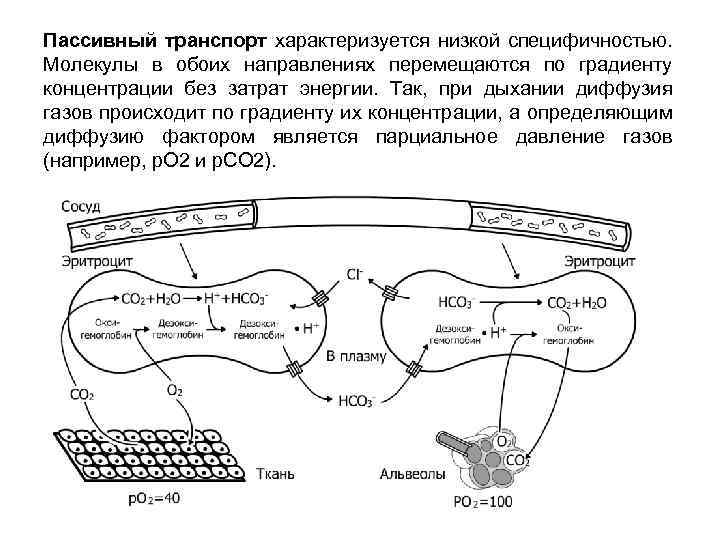
Пассивный транспорт характеризуется низкой специфичностью. Молекулы в обоих направлениях перемещаются по градиенту концентрации без затрат энергии. Так, при дыхании диффузия газов происходит по градиенту их концентрации, а определяющим диффузию фактором является парциальное давление газов (например, p. O 2 и p. CO 2).
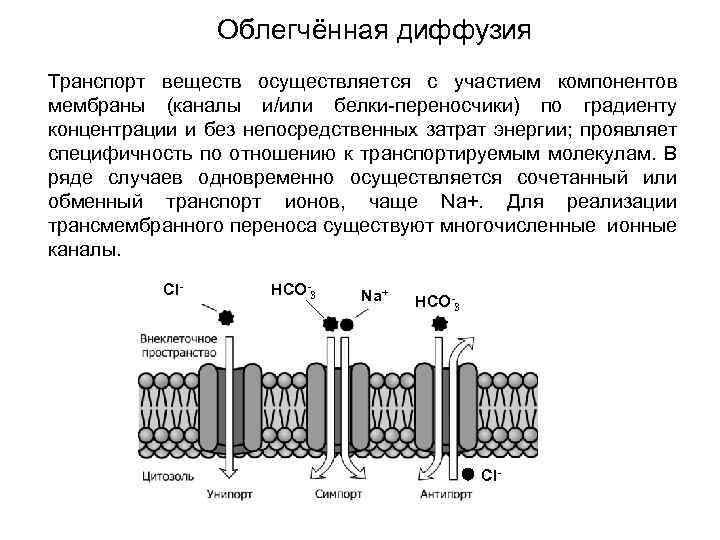
Облегчённая диффузия Транспорт веществ осуществляется с участием компонентов мембраны (каналы и/или белки-переносчики) по градиенту концентрации и без непосредственных затрат энергии; проявляет специфичность по отношению к транспортируемым молекулам. В ряде случаев одновременно осуществляется сочетанный или обменный транспорт ионов, чаще Na+. Для реализации трансмембранного переноса существуют многочисленные ионные каналы. Cl- HCO-3 Na+ HCO-3 Cl-
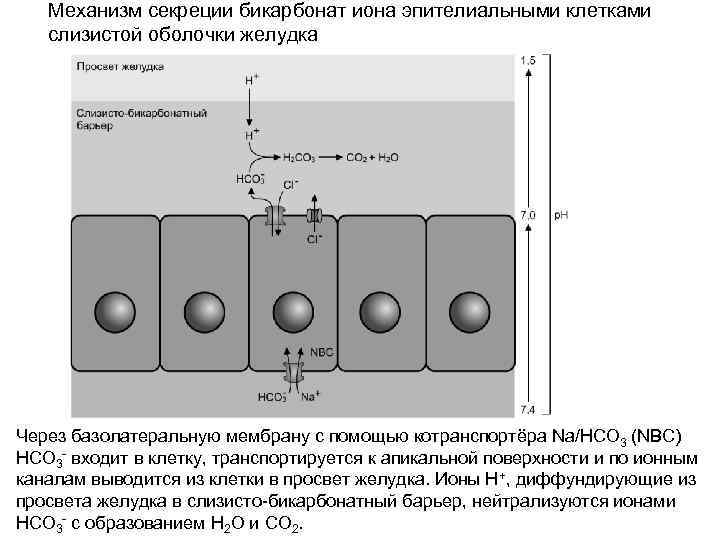
Механизм секреции бикарбонат иона эпителиальными клетками слизистой оболочки желудка Через базолатеральную мембрану с помощью котранспортёра Na/HCO 3 (NBC) HCO 3 - входит в клетку, транспортируется к апикальной поверхности и по ионным каналам выводится из клетки в просвет желудка. Ионы H+, диффундирующие из просвета желудка в слизисто-бикарбонатный барьер, нейтрализуются ионами HCO 3 - с образованием Н 2 О и СО 2.

Транспорт воды и поддержание клеточного объёма Поток воды через биологические мембраны (осмос) определяет разность осмотического и гидростатического давлений по обе стороны мембраны. Осмос — поток воды через полупроницаемую мембрану из компартмента с меньшей концентрацией растворённых в воде веществ в компартмент с большей их концентрацией. Осмотическое давление определяют как давление раствора, прекращающее его разведение водой через полупроницаемую мембрану. Численно осмотическое давление при равновесном состоянии (вода перестала проникать через полупроницаемую мембрану) равно гидростатическому давлению. Осмотичность растворов. В зависимости от осмоляльности, растворы могут быть изоосмотическими, гипер- и гипоосмотическими (иногда применяют термин «–тонический» , справедливый для электролитов). Изотоничные солевые растворы. Вливание изотоничного солевого раствора (0. 9% Na. CI) увеличивает объём межклеточной жидкости, но не влияет на объём внутриклеточной жидкости.
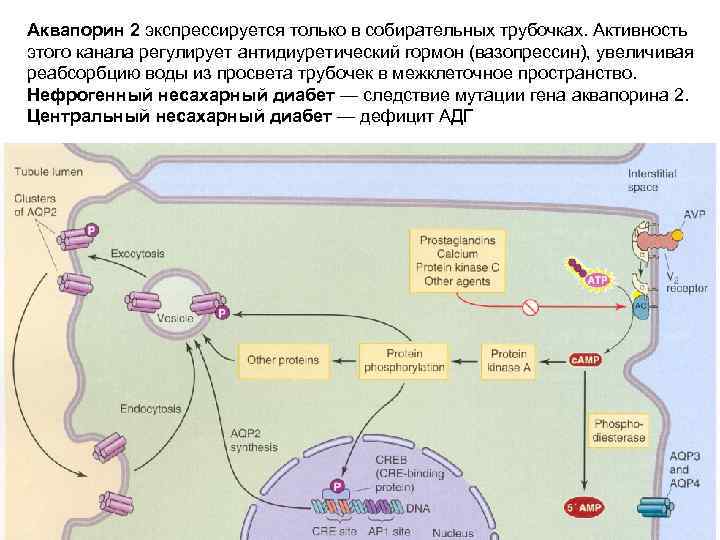
Аквапорин 2 экспрессируется только в собирательных трубочках. Активность этого канала регулирует антидиуретический гормон (вазопрессин), увеличивая реабсорбцию воды из просвета трубочек в межклеточное пространство. Нефрогенный несахарный диабет — следствие мутации гена аквапорина 2. Центральный несахарный диабет — дефицит АДГ
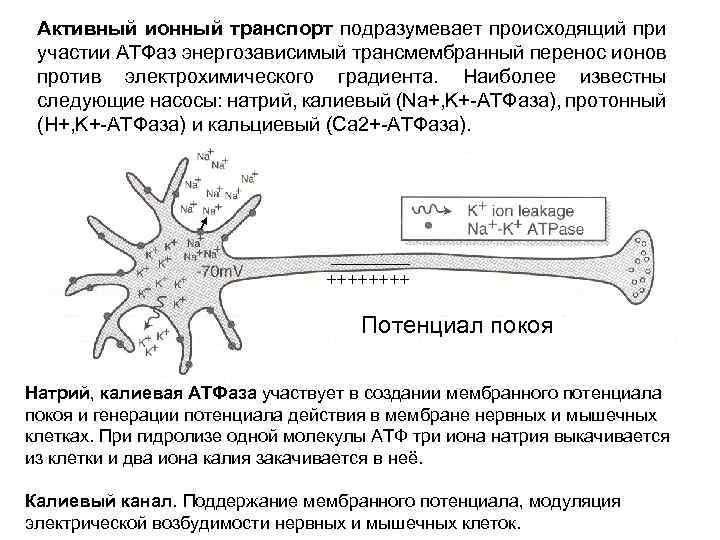
Активный ионный транспорт подразумевает происходящий при участии АТФаз энергозависимый трансмембранный перенос ионов против электрохимического градиента. Наиболее известны следующие насосы: натрий, калиевый (Na+, K+-АТФаза), протонный (H+, K+-АТФаза) и кальциевый (Ca 2+-АТФаза). ++++ Потенциал покоя Натрий, калиевая АТФаза участвует в создании мембранного потенциала покоя и генерации потенциала действия в мембране нервных и мышечных клетках. При гидролизе одной молекулы АТФ три иона натрия выкачивается из клетки и два иона калия закачивается в неё. Калиевый канал. Поддержание мембранного потенциала, модуляция электрической возбудимости нервных и мышечных клеток.
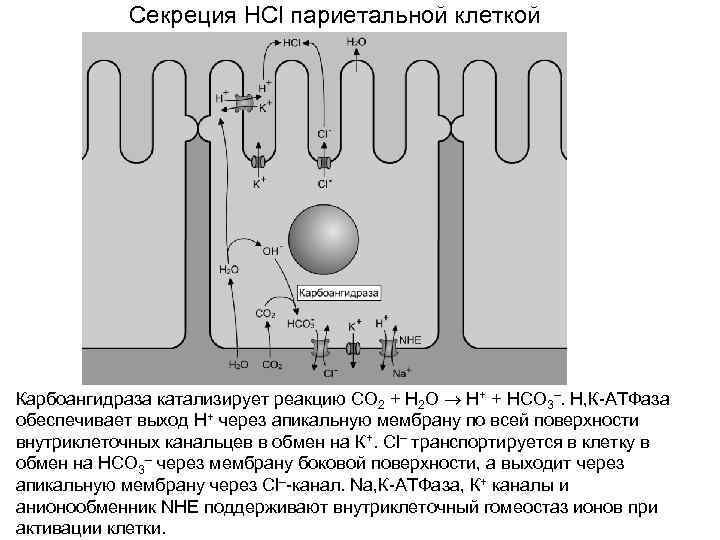
Секреция HCl париетальной клеткой Карбоангидраза катализирует реакцию CO 2 + H 2 O H+ + HCO 3–. Н, К-АТФаза обеспечивает выход H+ через апикальную мембрану по всей поверхности внутриклеточных канальцев в обмен на К+. Cl– транспортируется в клетку в обмен на HCO 3– через мембрану боковой поверхности, а выходит через апикальную мембрану через Cl–-канал. Na, К-АТФаза, К+ каналы и анионообменник NHE поддерживают внутриклеточный гомеостаз ионов при активации клетки.
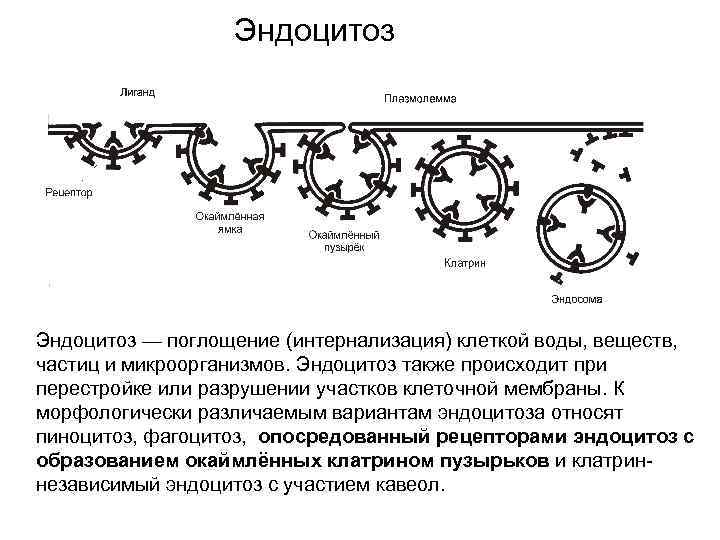
Эндоцитоз — поглощение (интернализация) клеткой воды, веществ, частиц и микроорганизмов. Эндоцитоз также происходит при перестройке или разрушении участков клеточной мембраны. К морфологически различаемым вариантам эндоцитоза относят пиноцитоз, фагоцитоз, опосредованный рецепторами эндоцитоз с образованием окаймлённых клатрином пузырьков и клатриннезависимый эндоцитоз с участием кавеол.
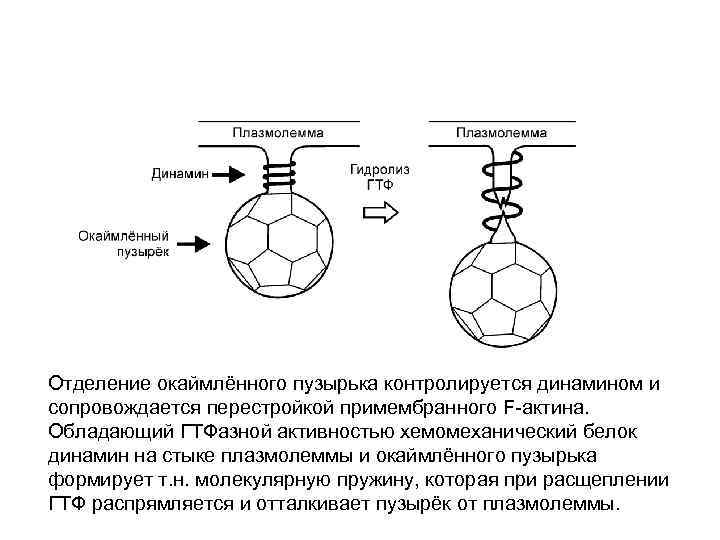
Отделение окаймлённого пузырька контролируется динамином и сопровождается перестройкой примембранного F-актина. Обладающий ГТФазной активностью хемомеханический белок динамин на стыке плазмолеммы и окаймлённого пузырька формирует т. н. молекулярную пружину, которая при расщеплении ГТФ распрямляется и отталкивает пузырёк от плазмолеммы.
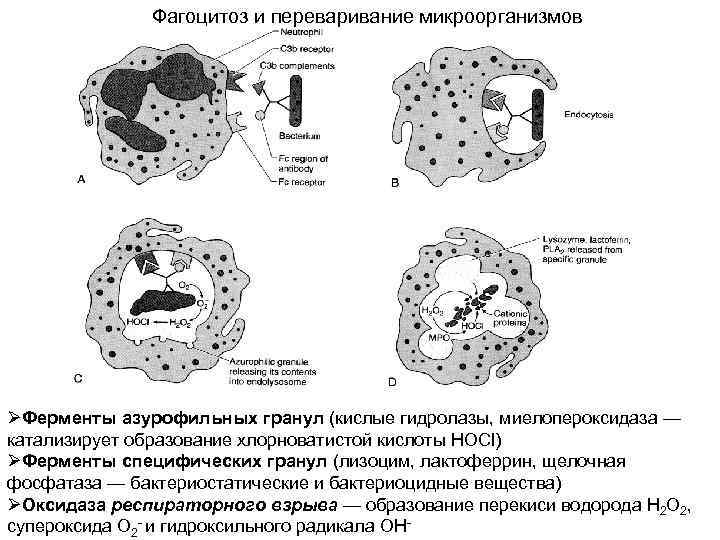
Фагоцитоз и переваривание микроорганизмов ØФерменты азурофильных гранул (кислые гидролазы, миелопероксидаза — катализирует образование хлорноватистой кислоты HOCl) ØФерменты специфических гранул (лизоцим, лактоферрин, щелочная фосфатаза — бактериостатические и бактериоцидные вещества) ØОксидаза респираторного взрыва — образование перекиси водорода Н 2 О 2, супероксида О 2 - и гидроксильного радикала ОН-
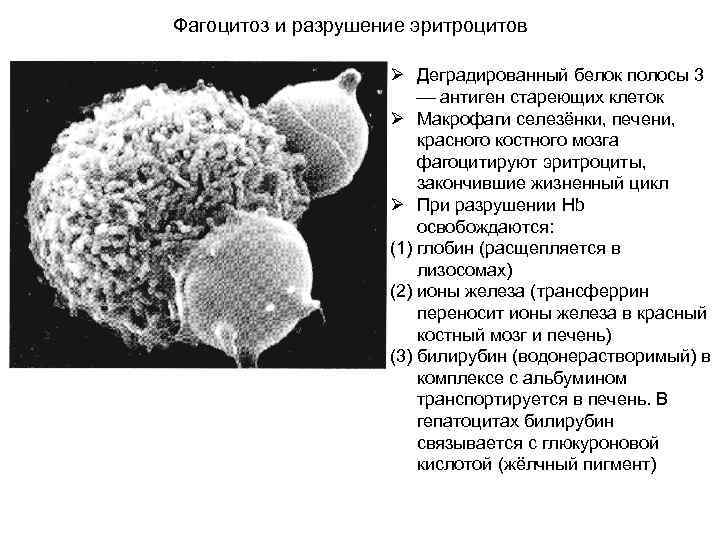
Фагоцитоз и разрушение эритроцитов Ø Деградированный белок полосы 3 антиген стареющих клеток Ø Макрофаги селезёнки, печени, красного костного мозга фагоцитируют эритроциты, закончившие жизненный цикл Ø При разрушении Hb освобождаются: (1) глобин (расщепляется в лизосомах) (2) ионы железа (трансферрин переносит ионы железа в красный костный мозг и печень) (3) билирубин (водонерастворимый) в комплексе с альбумином транспортируется в печень. В гепатоцитах билирубин связывается с глюкуроновой кислотой (жёлчный пигмент)
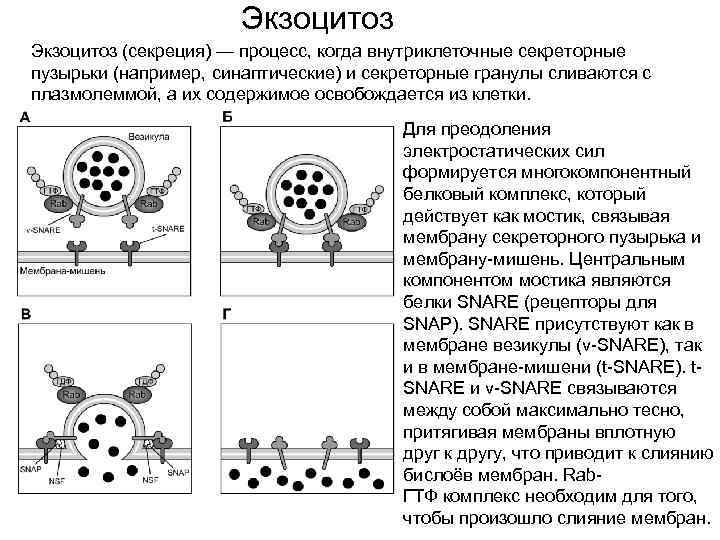
Экзоцитоз (секреция) — процесс, когда внутриклеточные секреторные пузырьки (например, синаптические) и секреторные гранулы сливаются с плазмолеммой, а их содержимое освобождается из клетки. Для преодоления электростатических сил формируется многокомпонентный белковый комплекс, который действует как мостик, связывая мембрану секреторного пузырька и мембрану-мишень. Центральным компонентом мостика являются белки SNARE (рецепторы для SNAP). SNARE присутствуют как в мембране везикулы (v-SNARE), так и в мембране-мишени (t-SNARE). t. SNARE и v-SNARE связываются между собой максимально тесно, притягивая мембраны вплотную друг к другу, что приводит к слиянию бислоёв мембран. Rab. ГТФ комплекс необходим для того, чтобы произошло слияние мембран.

Экзоцитоз может происходить по принципу «всё или ничего» с высвобождением содержимого всех гранул (например, как при дегрануляции тучной клетки). Для многих клеточных типов (нейроэндокринных, экзокринных) характерна секреция только небольшой части (1%) имеющегося большого резервного пула. Конститутивная секреция обеспечивает встраивание в плазмолемму вновь синтезированных белков и рецепторов, интернализованных при опосредованном рецепторами эндоцитозе. В регулируемом экзоцитозе участвуют секреторные гранулы, а также специализированные эндосомы (например, синаптические пузырьки). Процесс происходит чаще всего вследствие увеличения концентрации Са 2+ в цитозоле.
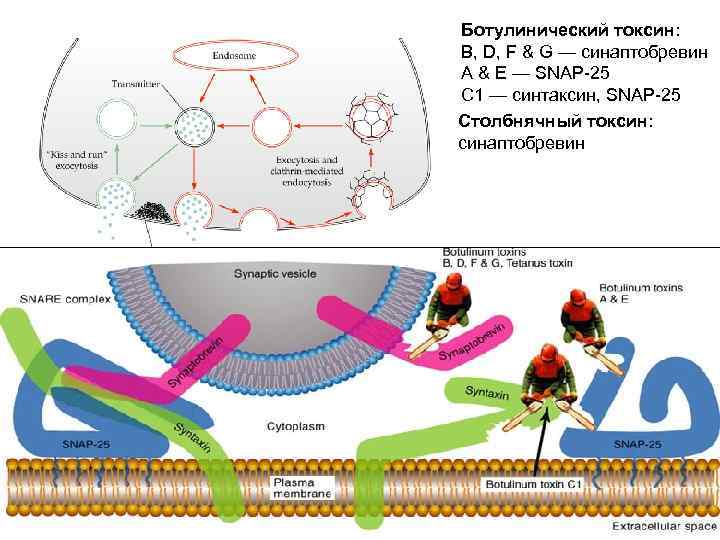
Ботулинический токсин: B, D, F & G — синаптобревин A & E — SNAP-25 C 1 — синтаксин, SNAP-25 Столбнячный токсин: синаптобревин

Ботулизм — острая бактериальная токсикоинфекция. Возбудитель ботулизма — Clostridium botulinum продуцирует нейротоксины. Симптомы заболевания обусловлен действием на организм нейротоксинов A/E, B, C 1, D, F и G, блокирующих секрецию ацетилхолина из нервной терминали. Под действием токсинов через 18 36 ч часто появляются нарушения со стороны вегетативной нервной системы (сухость во рту, раздвоение в глазах), позже развиваются парезы и параличи скелетной и гладкой мускулатуры. Смерть может наступить от паралича дыхательной мускулатуры.

Столбняк — острое тяжёлое инфекционное заболевание, протекающее с перемежающимися тоническими и клоническими судорогами скелетной мускулатуры, приводящими к асфиксии. Возбудитель — подвижная анаэробная спорообразующая палочка Clostridium tetani. В ране спора прорастает в вегетативную форму и продуцирует столбнячный нейротоксин (тетаноспазмин). Ретроградным аксонным транспортом нейротоксин попадает в перикарионы нейронов спинного мозга. Механизм действия токсина связан с блокированием секреции тормозных нейромедиаторов, в частности, глицина и gаминомасляной кислоты, вставочными нейронами (интернейронами), которые в норме подавляют импульсную активность мотонейронов, иннервирующих скелетные мышцы. Поэтому импульсация мотонейронов непрерывно передаётся на мышечные волокна, обусловливая тоническое напряжение мышц, переходящее в судороги. Характерно начало заболевания с судорожного сокращения жевательных мышц. К профилактическим мероприятиям столбняка относятся активная вакцинация в детстве, а также вакцинация сразу после полученной травмы.

Плазматическая мембрана обеспечивает межклеточные информационные взаимодействия А. Диффундирующие молекулы Сигнальная молекула (первый посредник) рецептор второй посредник ответ (изменение режима функционирования клетки) Б. Адгезия ØИнтегрины: клетка-матрикс (миграция) ØМолекулы адгезии клеток (кадгерины, NCAM): клетка-клетка (тканеобразование). метастазы и разрастания карцином желудка, эндометрия и яичника возникают вследствие нарушения адгезии опухолевых клеток, содержащих мутантный ген E-кадгерина, и экспрессии его дефектного продукта. В. Межклеточные контакты ØАдгезионные (формирование ткани) ØПлотные (барьер проницаемости) ØЩелевые (межклеточная коммуникация)
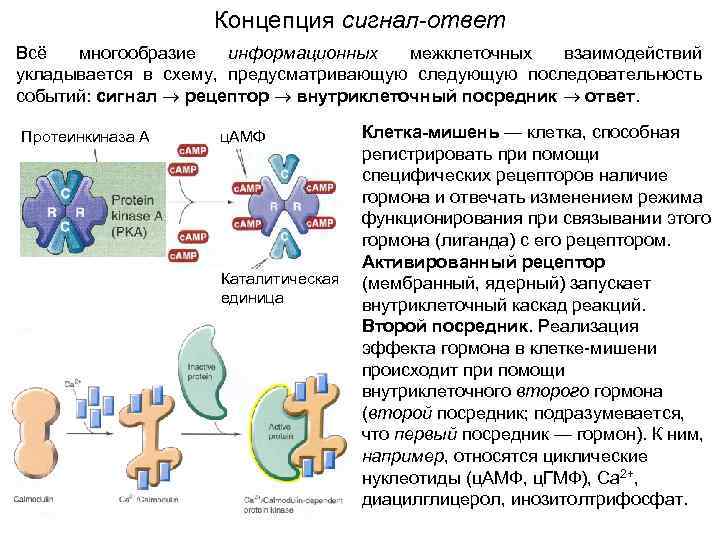
Концепция сигнал-ответ Всё многообразие информационных межклеточных взаимодействий укладывается в схему, предусматривающую следующую последовательность событий: сигнал рецептор внутриклеточный посредник ответ. Протеинкиназа А ц. АМФ Каталитическая единица Клетка-мишень — клетка, способная регистрировать при помощи специфических рецепторов наличие гормона и отвечать изменением режима функционирования при связывании этого гормона (лиганда) с его рецептором. Активированный рецептор (мембранный, ядерный) запускает внутриклеточный каскад реакций. Второй посредник. Реализация эффекта гормона в клетке-мишени происходит при помощи внутриклеточного второго гормона (второй посредник; подразумевается, что первый посредник — гормон). К ним, например, относятся циклические нуклеотиды (ц. АМФ, ц. ГМФ), Ca 2+, диацилглицерол, инозитолтрифосфат.
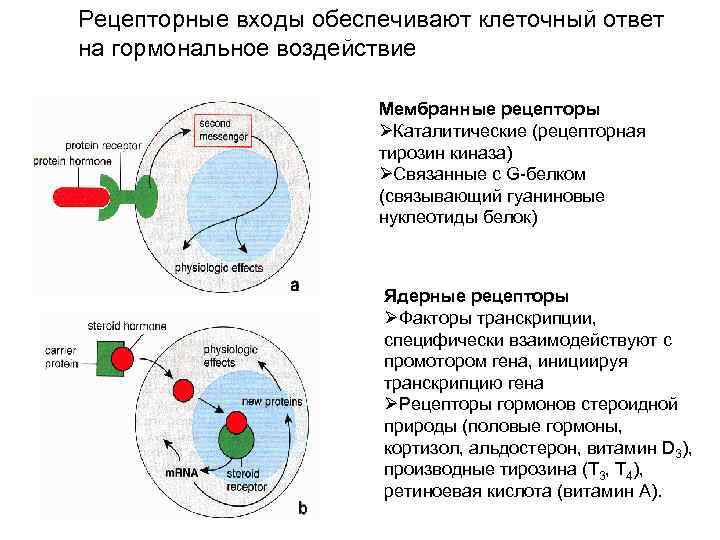
Рецепторные входы обеспечивают клеточный ответ на гормональное воздействие Мембранные рецепторы ØКаталитические (рецепторная тирозин киназа) ØСвязанные с G-белком (связывающий гуаниновые нуклеотиды белок) Ядерные рецепторы ØФакторы транскрипции, специфически взаимодействуют с промотором гена, инициируя транскрипцию гена ØРецепторы гормонов стероидной природы (половые гормоны, кортизол, альдостерон, витамин D 3), производные тирозина (Т 3, Т 4), ретиноевая кислота (витамин А).
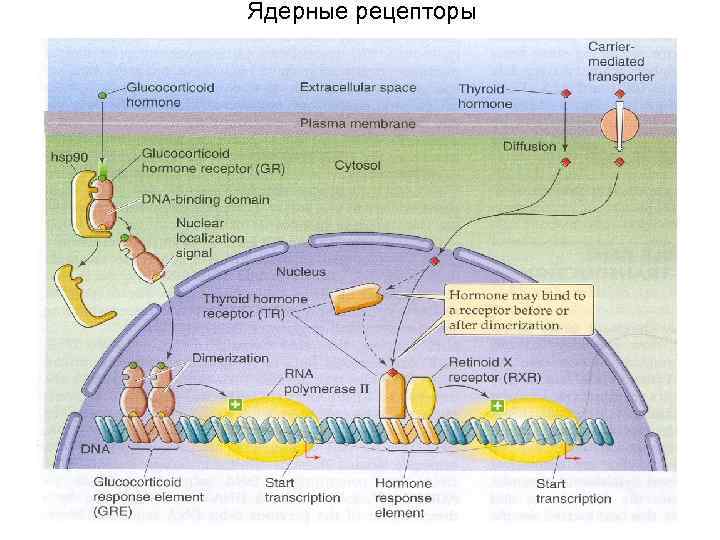
Ядерные рецепторы
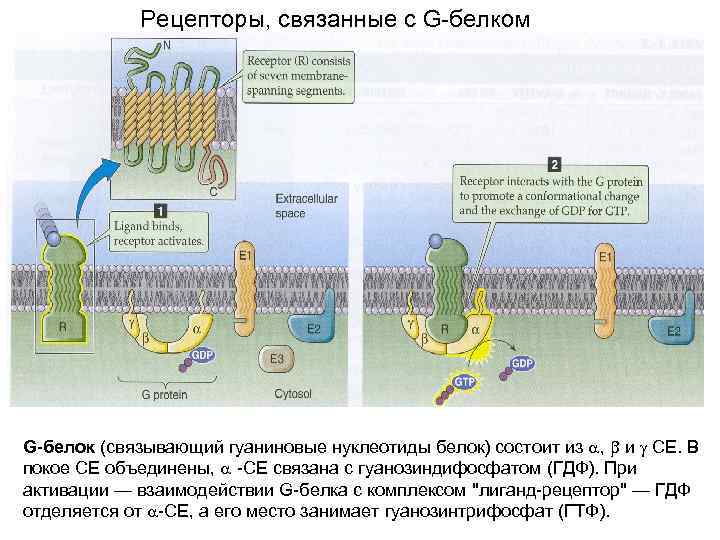
Рецепторы, связанные с G-белком G-белок (связывающий гуаниновые нуклеотиды белок) состоит из , и СЕ. В покое СЕ объединены, -СЕ связана с гуанозиндифосфатом (ГДФ). При активации — взаимодействии G-белка с комплексом "лиганд-рецептор" — ГДФ отделяется от -СЕ, а его место занимает гуанозинтрифосфат (ГТФ).
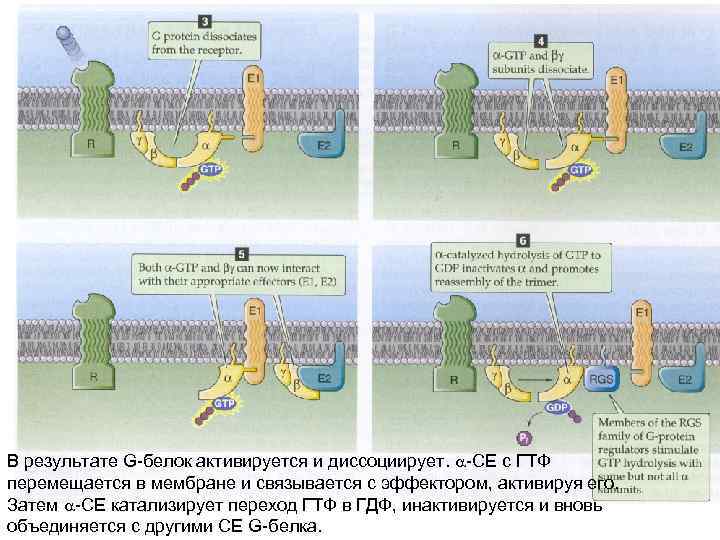
В результате G-белок активируется и диссоциирует. -СЕ с ГТФ перемещается в мембране и связывается с эффектором, активируя его. Затем -СЕ катализирует переход ГТФ в ГДФ, инактивируется и вновь объединяется с другими СЕ G-белка.
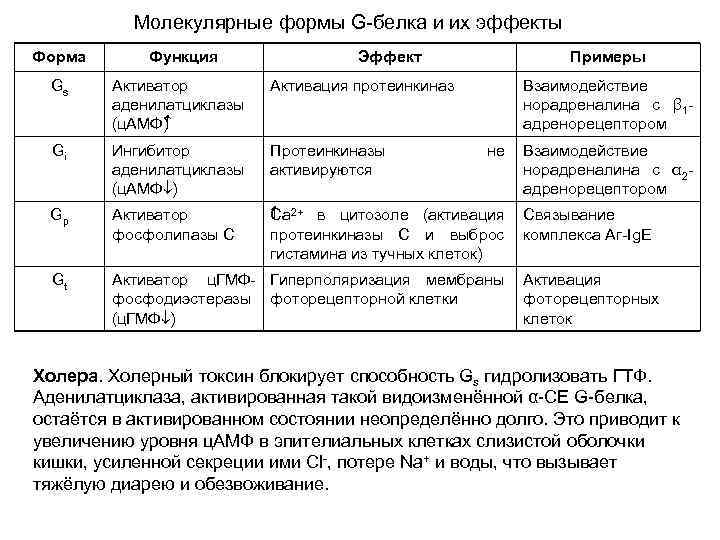
Молекулярные формы G-белка и их эффекты Форма Функция Эффект Примеры Gs Активатор аденилатциклазы (ц. АМФ ) Активация протеинкиназ Gi Ингибитор аденилатциклазы (ц. АМФ¯) Протеинкиназы активируются Gp Активатор фосфолипазы С C a 2+ в цитозоле (активация Связывание протеинкиназы С и выброс комплекса Аг-Ig. E гистамина из тучных клеток) Gt Активатор ц. ГМФ- Гиперполяризация мембраны Активация фосфодиэстеразы фоторецепторной клетки фоторецепторных (ц. ГМФ¯) клеток Взаимодействие норадреналина с β 1 адренорецептором не Взаимодействие норадреналина с α 2 адренорецептором Холера. Холерный токсин блокирует способность Gs гидролизовать ГТФ. Аденилатциклаза, активированная такой видоизменённой α-СЕ G-белка, остаётся в активированном состоянии неопределённо долго. Это приводит к увеличению уровня ц. АМФ в эпителиальных клетках слизистой оболочки кишки, усиленной секреции ими Cl-, потере Na+ и воды, что вызывает тяжёлую диарею и обезвоживание.
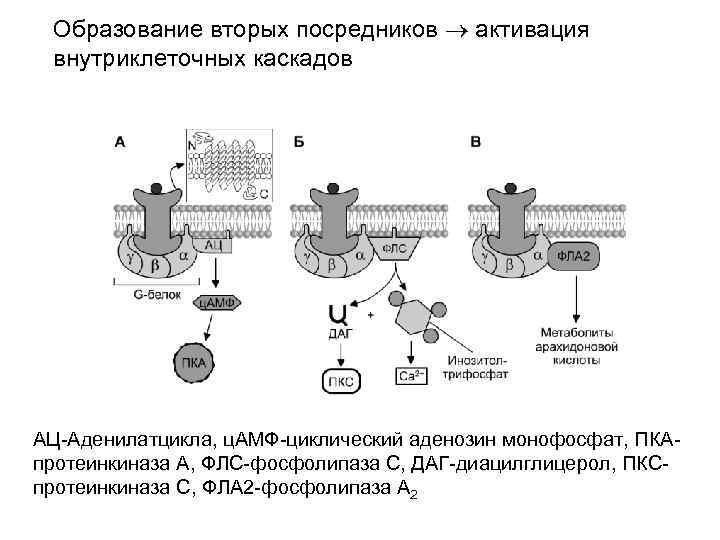
Образование вторых посредников активация внутриклеточных каскадов АЦ-Аденилатцикла, ц. АМФ-циклический аденозин монофосфат, ПКАпротеинкиназа А, ФЛС-фосфолипаза С, ДАГ-диацилглицерол, ПКСпротеинкиназа С, ФЛА 2 -фосфолипаза А 2
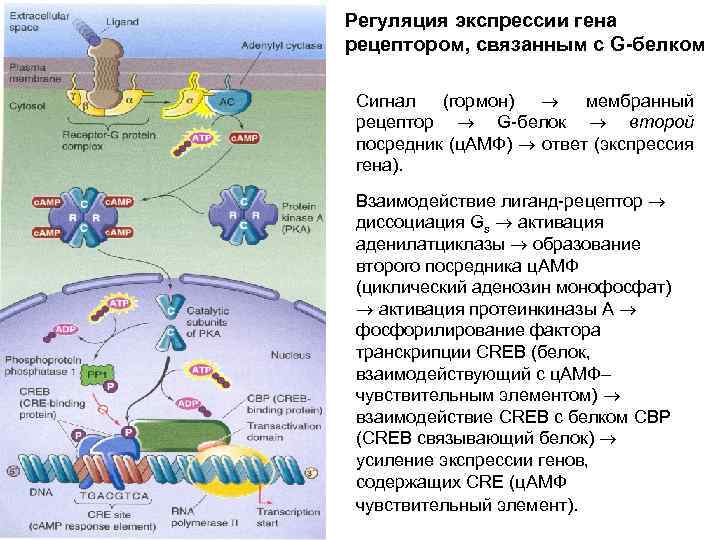
Регуляция экспрессии гена рецептором, связанным с G-белком Сигнал (гормон) мембранный рецептор G-белок второй посредник (ц. АМФ) ответ (экспрессия гена). Взаимодействие лиганд-рецептор диссоциация Gs активация аденилатциклазы образование второго посредника ц. АМФ (циклический аденозин монофосфат) активация протеинкиназы А фосфорилирование фактора транскрипции CREB (белок, взаимодействующий с ц. АМФ– чувствительным элементом) взаимодействие CREB с белком CBP (CREB связывающий белок) усиление экспрессии генов, содержащих CRE (ц. АМФ чувствительный элемент).
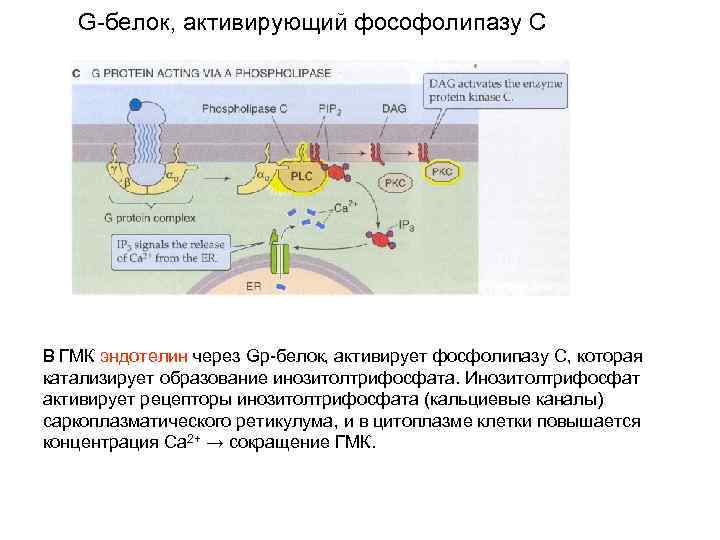
G-белок, активирующий фософолипазу С В ГМК эндотелин через Gp-белок, активирует фосфолипазу С, которая катализирует образование инозитолтрифосфата. Инозитолтрифосфат активирует рецепторы инозитолтрифосфата (кальциевые каналы) саркоплазматического ретикулума, и в цитоплазме клетки повышается концентрация Ca 2+ → сокращение ГМК.
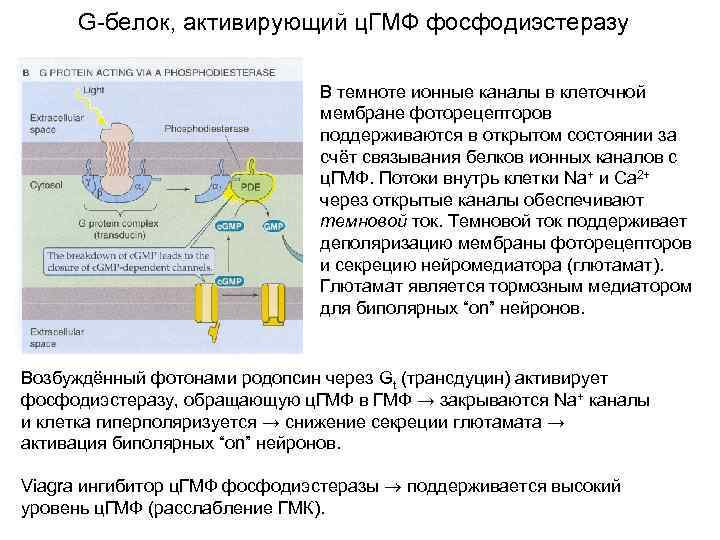
G-белок, активирующий ц. ГМФ фосфодиэстеразу В темноте ионные каналы в клеточной мембране фоторецепторов поддерживаются в открытом состоянии за счёт связывания белков ионных каналов с ц. ГМФ. Потоки внутрь клетки Na+ и Ca 2+ через открытые каналы обеспечивают темновой ток. Темновой ток поддерживает деполяризацию мембраны фоторецепторов и секрецию нейромедиатора (глютамат). Глютамат является тормозным медиатором для биполярных “on” нейронов. Возбуждённый фотонами родопсин через Gt (трансдуцин) активирует фосфодиэстеразу, обращающую ц. ГМФ в ГМФ → закрываются Na+ каналы и клетка гиперполяризуется → снижение секреции глютамата → активация биполярных “on” нейронов. Viagra ингибитор ц. ГМФ фосфодиэстеразы поддерживается высокий уровень ц. ГМФ (расслабление ГМК).
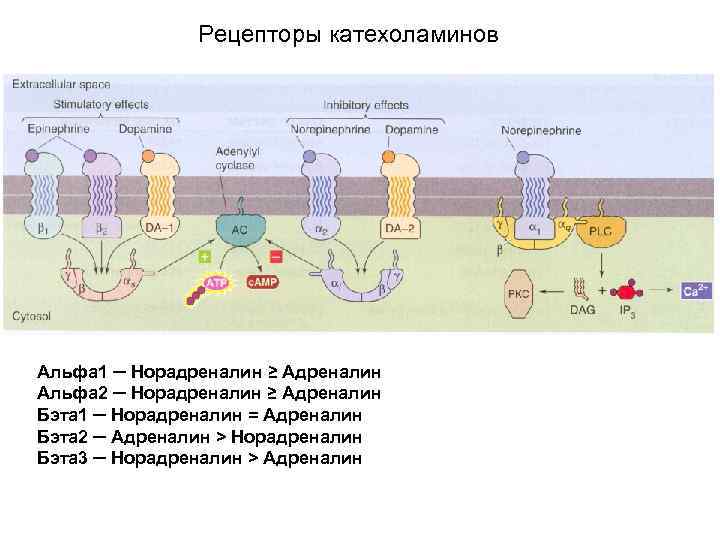
Рецепторы катехоламинов Альфа 1 ─ Норадреналин ≥ Адреналин Альфа 2 ─ Норадреналин ≥ Адреналин Бэта 1 ─ Норадреналин = Адреналин Бэта 2 ─ Адреналин > Норадреналин Бэта 3 ─ Норадреналин > Адреналин
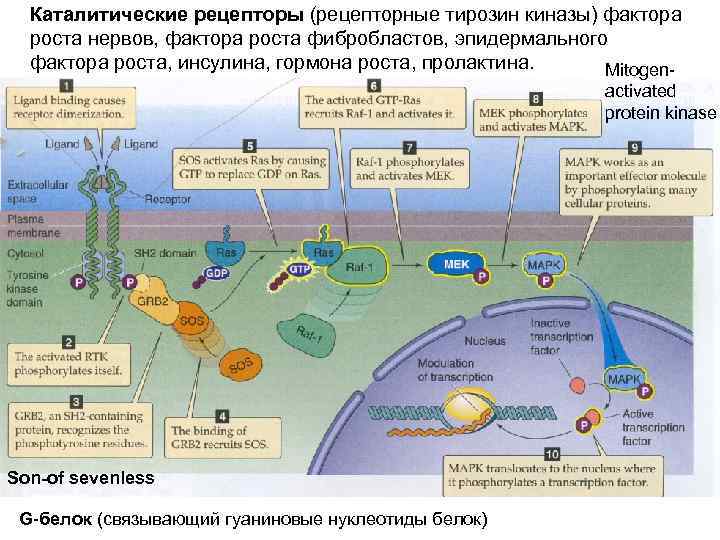
Каталитические рецепторы (рецепторные тирозин киназы) фактора роста нервов, фактора роста фибробластов, эпидермального фактора роста, инсулина, гормона роста, пролактина. Mitogenactivated protein kinase Son-of sevenless G-белок (связывающий гуаниновые нуклеотиды белок)
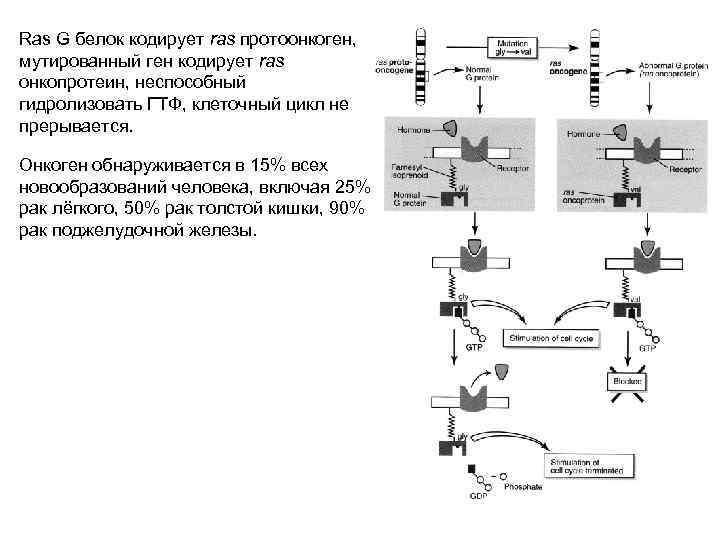
Ras G белок кодирует ras протоонкоген, мутированный ген кодирует ras онкопротеин, неспособный гидролизовать ГТФ, клеточный цикл не прерывается. Онкоген обнаруживается в 15% всех новообразований человека, включая 25% рак лёгкого, 50% рак толстой кишки, 90% рак поджелудочной железы.

Цитоскелет Микротрубочки (24 нм) ØПоддержание формы клеток ØВнутриклеточный транспорт (аксонный) ØВходят в состав аксонемы, базального тельца, центриоли Промежуточные филаменты (8 -11 нм) ØСоздают внутриклеточный каркас ØСтабилизируют адгезионные межклеточные контакты ØСостоят из белков, специфичных для определённого клеточного типа (кератин, десмин, виментин, глиальный фибриллярный кислый белок, белки нейрофиламентного триплета) Микрофиламенты (6 нм) ØВзаимодействуют с молекулами точечного адгезионного контакта ØПодвижность немышечных клеток ØЭндоцитоз и экзоцитоз ØСтабилизация локальных выпячиваний клеточной мембраны (микроворсинки)
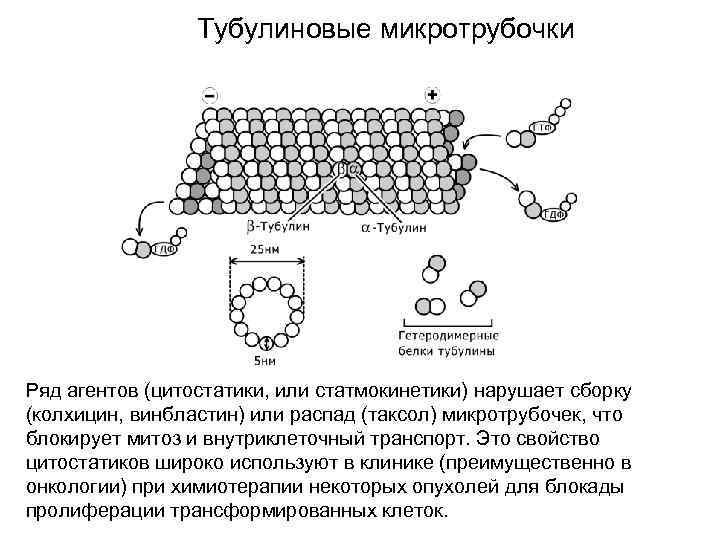
Тубулиновые микротрубочки Ряд агентов (цитостатики, или статмокинетики) нарушает сборку (колхицин, винбластин) или распад (таксол) микротрубочек, что блокирует митоз и внутриклеточный транспорт. Это свойство цитостатиков широко используют в клинике (преимущественно в онкологии) при химиотерапии некоторых опухолей для блокады пролиферации трансформированных клеток.
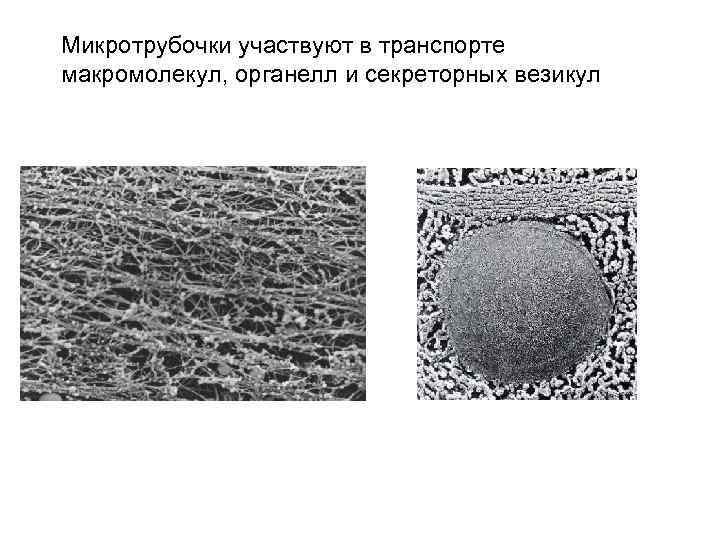
Микротрубочки участвуют в транспорте макромолекул, органелл и секреторных везикул
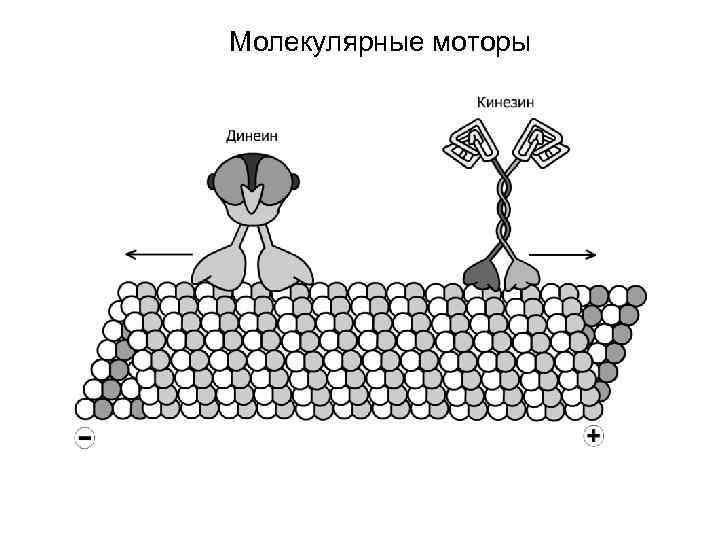
Молекулярные моторы
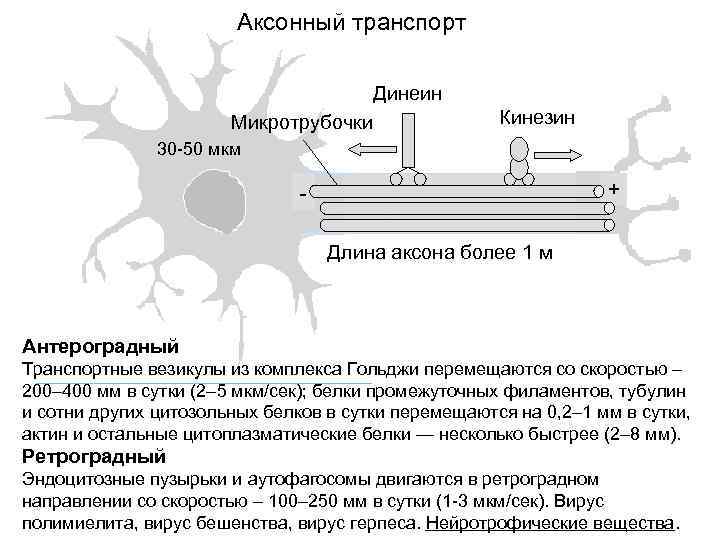
Аксонный транспорт Динеин Микротрубочки Кинезин 30 -50 мкм + Длина аксона более 1 м Антероградный Транспортные везикулы из комплекса Гольджи перемещаются со скоростью – 200– 400 мм в сутки (2– 5 мкм/сек); белки промежуточных филаментов, тубулин и сотни других цитозольных белков в сутки перемещаются на 0, 2– 1 мм в сутки, актин и остальные цитоплазматические белки — несколько быстрее (2– 8 мм). Ретроградный Эндоцитозные пузырьки и аутофагосомы двигаются в ретроградном направлении со скоростью – 100– 250 мм в сутки (1 -3 мкм/сек). Вирус полимиелита, вирус бешенства, вирус герпеса. Нейротрофические вещества.
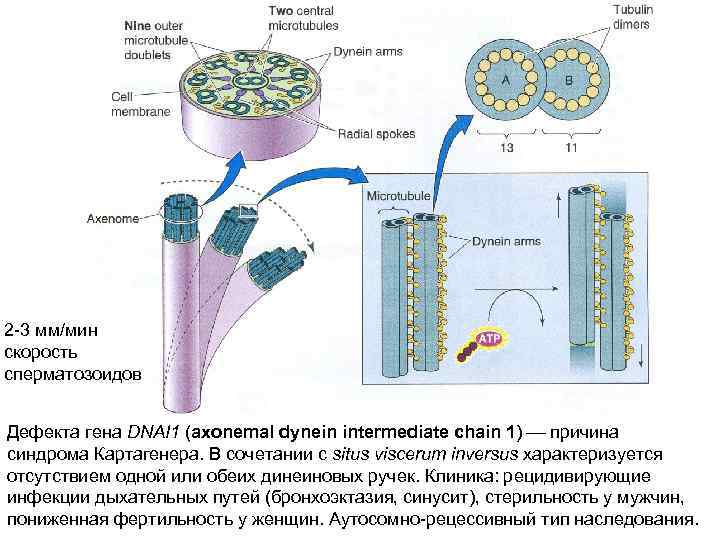
2 -3 мм/мин скорость сперматозоидов Дефекта гена DNAI 1 (аxonemal dynein intermediate chain 1) причина синдрома Картагенера. В сочетании с situs viscerum inversus характеризуется отсутствием одной или обеих динеиновых ручек. Клиника: рецидивирующие инфекции дыхательных путей (бронхоэктазия, синусит), стерильность у мужчин, пониженная фертильность у женщин. Аутосомно-рецессивный тип наследования.

Центросома Перицентриольный матрикс Центриоли В перицентриольном матриксе из 10– 13 молекул -тубулина формируются -тубулиновые кольца, которые служат затравками, инициирующими начало полимеризации тубулиновых гетеродимеров.
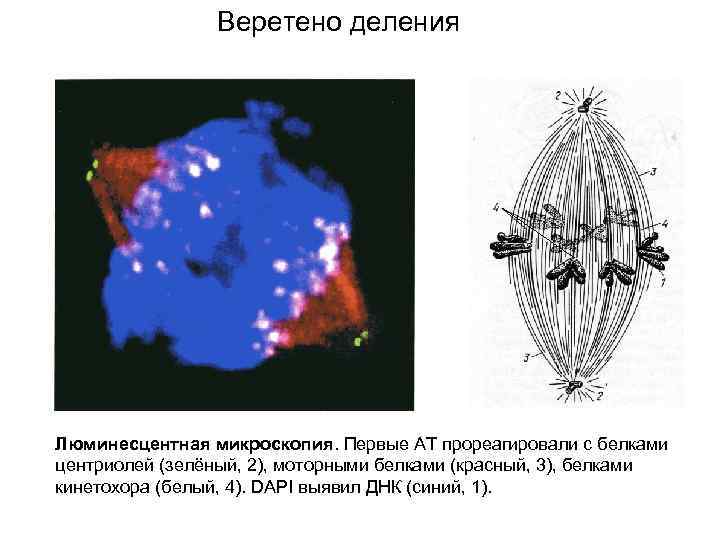
Веретено деления Люминесцентная микроскопия. Первые АТ прореагировали с белками центриолей (зелёный, 2), моторными белками (красный, 3), белками кинетохора (белый, 4). DAPI выявил ДНК (синий, 1).
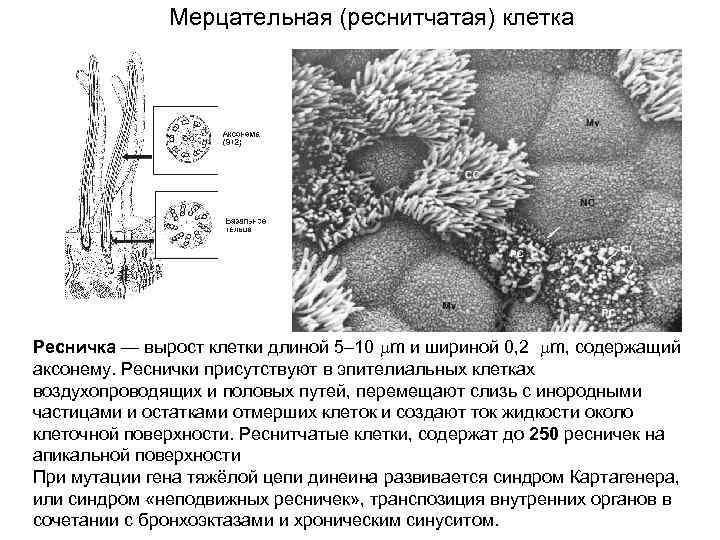
Мерцательная (реснитчатая) клетка Ресничка — вырост клетки длиной 5– 10 m и шириной 0, 2 m, содержащий аксонему. Реснички присутствуют в эпителиальных клетках воздухопроводящих и половых путей, перемещают слизь с инородными частицами и остатками отмерших клеток и создают ток жидкости около клеточной поверхности. Реснитчатые клетки, содержат до 250 ресничек на апикальной поверхности При мутации гена тяжёлой цепи динеина развивается синдром Картагенера, или синдром «неподвижных ресничек» , транспозиция внутренних органов в сочетании с бронхоэктазами и хроническим синуситом.

Обонятельная клетка Обонятельные нейроны, кроме центрального, имеют короткий периферический отросток (дендрит), заканчивающийся на поверхности обонятельного эпителия сферическим утолщением — обонятельной булавой диаметром 1– 2 мкм. В ней присутствуют митохондрии, мелкие вакуоли и базальные тельца для отходящих от вершины булавы 20– 80 обонятельных волосков длиной 30– 200 мкм, имеющих строение типичных ресничек. В мембране обонятельных ресничек присутствуют рецепторы пахучих веществ. В мембране хвоста сперматозоида присутствуют подобные рецепторные молекулы.
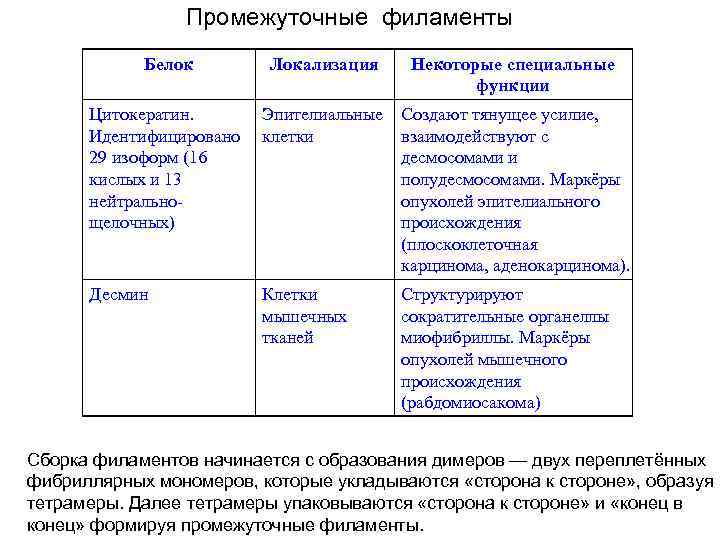
Промежуточные филаменты Белок Локализация Некоторые специальные функции Цитокератин. Эпителиальные Создают тянущее усилие, Идентифицировано клетки взаимодействуют с 29 изоформ (16 десмосомами и кислых и 13 полудесмосомами. Маркёры нейтральноопухолей эпителиального щелочных) происхождения (плоскоклеточная карцинома, аденокарцинома). Десмин Клетки мышечных тканей Структурируют сократительные органеллы миофибриллы. Маркёры опухолей мышечного происхождения (рабдомиосакома) Сборка филаментов начинается с образования димеров — двух переплетённых фибриллярных мономеров, которые укладываются «сторона к стороне» , образуя тетрамеры. Далее тетрамеры упаковываются «сторона к стороне» и «конец в конец» формируя промежуточные филаменты.
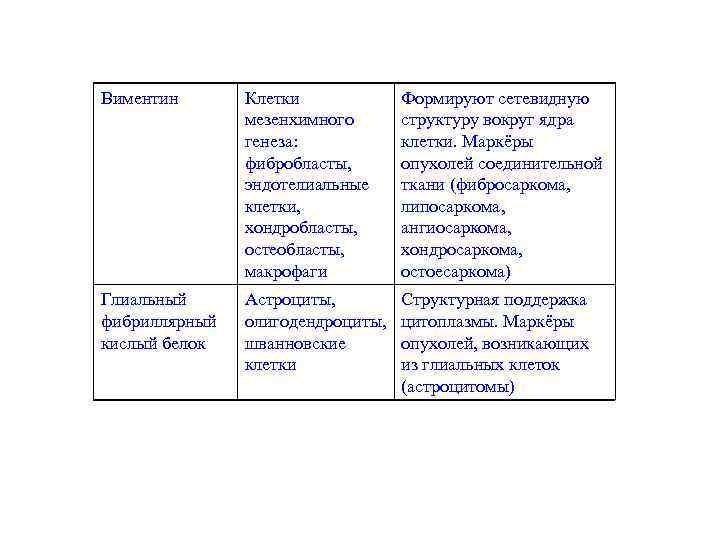
Виментин Клетки мезенхимного генеза: фибробласты, эндотелиальные клетки, хондробласты, остеобласты, макрофаги Формируют сетевидную структуру вокруг ядра клетки. Маркёры опухолей соединительной ткани (фибросаркома, липосаркома, ангиосаркома, хондросаркома, остоесаркома) Глиальный фибриллярный кислый белок Астроциты, олигодендроциты, шванновские клетки Структурная поддержка цитоплазмы. Маркёры опухолей, возникающих из глиальных клеток (астроцитомы)

Белки Нейроны нейрофиламентного триплета: NF-L (70 к. Д), NF-M (140 к. Д), NF-H (210 к. Д) Поддерживают структуру и форму отростков нейрона (аксонов и дендритов) Ламины A, B и C Организуют ядерную пластинку и лежащий около неё хроматин Ядерная пластинка
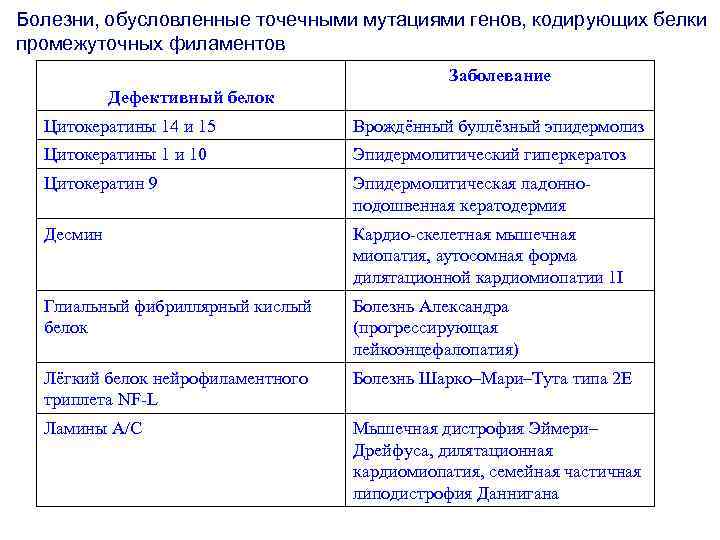
Болезни, обусловленные точечными мутациями генов, кодирующих белки промежуточных филаментов Заболевание Дефективный белок Цитокератины 14 и 15 Врождённый буллёзный эпидермолиз Цитокератины 1 и 10 Эпидермолитический гиперкератоз Цитокератин 9 Эпидермолитическая ладонноподошвенная кератодермия Десмин Кардио-скелетная мышечная миопатия, аутосомная форма дилятационной кардиомиопатии 1 I Глиальный фибриллярный кислый белок Болезнь Александра (прогрессирующая лейкоэнцефалопатия) Лёгкий белок нейрофиламентного триплета NF-L Болезнь Шарко–Мари–Тута типа 2 E Ламины А/С Мышечная дистрофия Эймери– Дрейфуса, дилятационная кардиомиопатия, семейная частичная липодистрофия Даннигана
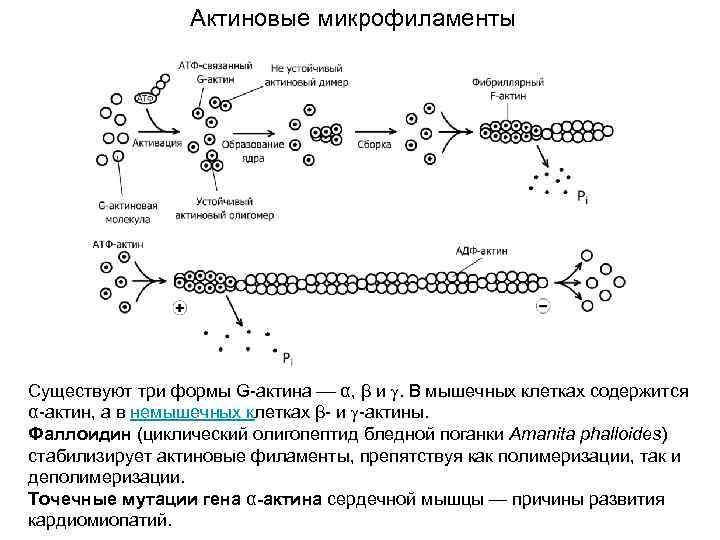
Актиновые микрофиламенты Существуют три формы G-актина α, β и . В мышечных клетках содержится α-актин, а в немышечных клетках β- и -актины. Фаллоидин (циклический олигопептид бледной поганки Amanita phalloides) стабилизирует актиновые филаменты, препятствуя как полимеризации, так и деполимеризации. Точечные мутации гена α-актина сердечной мышцы — причины развития кардиомиопатий.
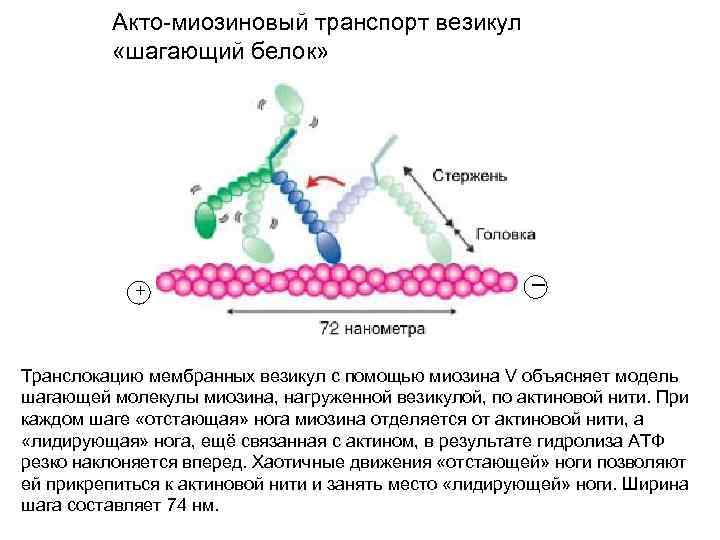
Акто-миозиновый транспорт везикул «шагающий белок» + ─ Транслокацию мембранных везикул с помощью миозина V объясняет модель шагающей молекулы миозина, нагруженной везикулой, по актиновой нити. При каждом шаге «отстающая» нога миозина отделяется от актиновой нити, а «лидирующая» нога, ещё связанная с актином, в результате гидролиза АТФ резко наклоняется вперед. Хаотичные движения «отстающей» ноги позволяют ей прикрепиться к актиновой нити и занять место «лидирующей» ноги. Ширина шага составляет 74 нм.
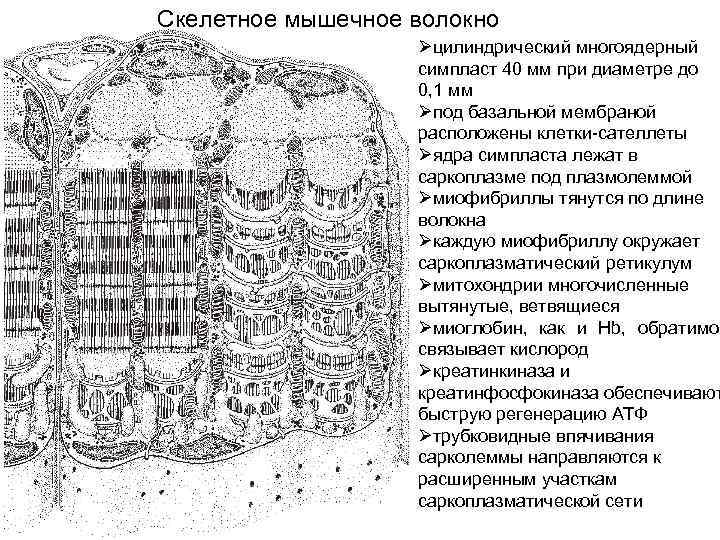
Скелетное мышечное волокно Øцилиндрический многоядерный симпласт 40 мм при диаметре до 0, 1 мм Øпод базальной мембраной расположены клетки-сателлеты Øядра симпласта лежат в саркоплазме под плазмолеммой Øмиофибриллы тянутся по длине волокна Øкаждую миофибриллу окружает саркоплазматический ретикулум Øмитохондрии многочисленные вытянутые, ветвящиеся Øмиоглобин, как и Hb, обратимо связывает кислород Øкреатинкиназа и креатинфосфокиназа обеспечивают быструю регенерацию АТФ Øтрубковидные впячивания сарколеммы направляются к расширенным участкам саркоплазматической сети
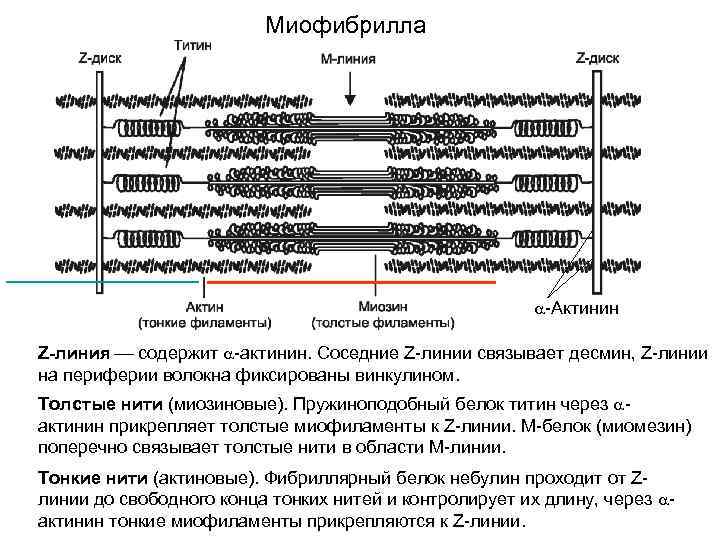
Миофибрилла -Актинин Z-линия содержит -актинин. Соседние Z-линии связывает десмин, Z-линии на периферии волокна фиксированы винкулином. Толстые нити (миозиновые). Пружиноподобный белок титин через актинин прикрепляет толстые миофиламенты к Z-линии. М-белок (миомезин) поперечно связывает толстые нити в области М-линии. Тонкие нити (актиновые). Фибриллярный белок небулин проходит от Zлинии до свободного конца тонких нитей и контролирует их длину, через актинин тонкие миофиламенты прикрепляются к Z-линии.
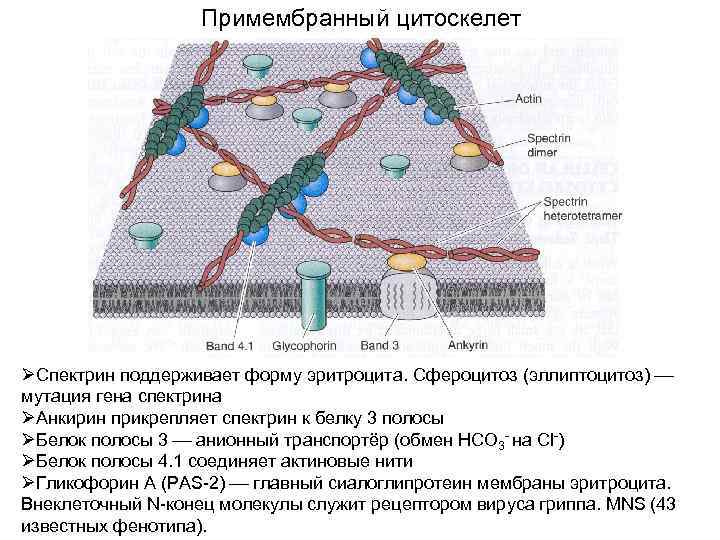
Примембранный цитоскелет ØСпектрин поддерживает форму эритроцита. Сфероцитоз (эллиптоцитоз) мутация гена спектрина ØАнкирин прикрепляет спектрин к белку 3 полосы ØБелок полосы 3 анионный транспортёр (обмен НСО 3 - на Cl-) ØБелок полосы 4. 1 соединяет актиновые нити ØГликофорин A (PAS-2) главный сиалоглипротеин мембраны эритроцита. Внеклеточный N-конец молекулы служит рецептором вируса гриппа. MNS (43 известных фенотипа).
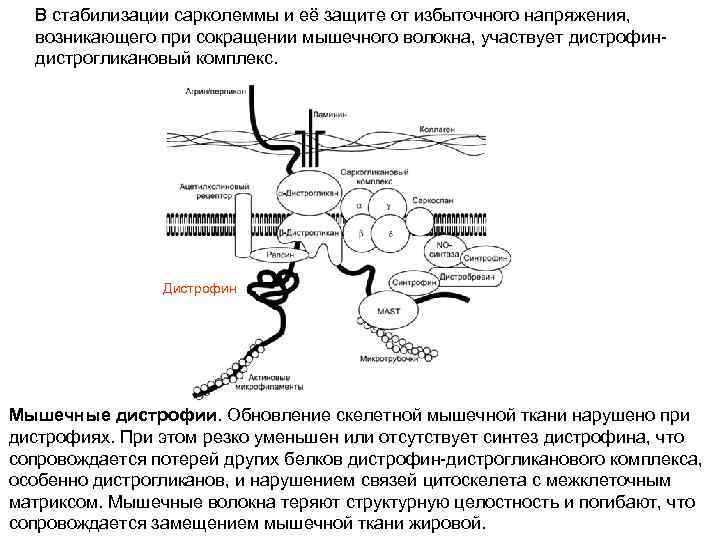
В стабилизации сарколеммы и её защите от избыточного напряжения, возникающего при сокращении мышечного волокна, участвует дистрофиндистрогликановый комплекс. Дистрофин Мышечные дистрофии. Обновление скелетной мышечной ткани нарушено при дистрофиях. При этом резко уменьшен или отсутствует синтез дистрофина, что сопровождается потерей других белков дистрофин-дистрогликанового комплекса, особенно дистрогликанов, и нарушением связей цитоскелета с межклеточным матриксом. Мышечные волокна теряют структурную целостность и погибают, что сопровождается замещением мышечной ткани жировой.
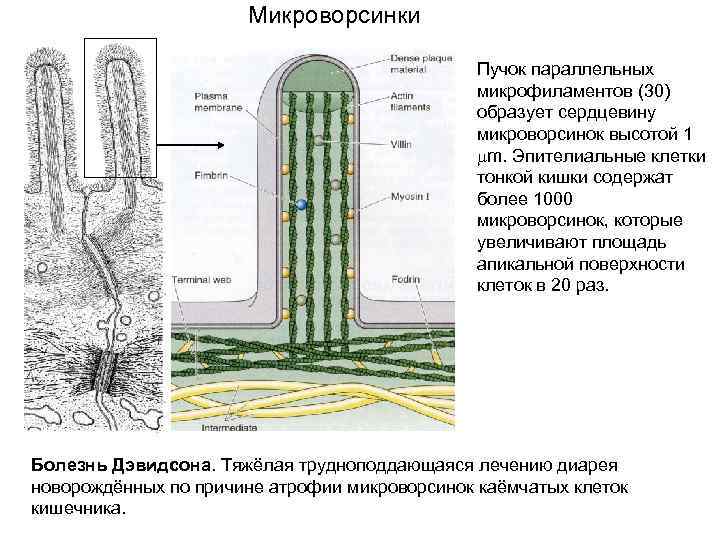
Микроворсинки Пучок параллельных микрофиламентов (30) образует сердцевину микроворсинок высотой 1 m. Эпителиальные клетки тонкой кишки содержат более 1000 микроворсинок, которые увеличивают площадь апикальной поверхности клеток в 20 раз. Болезнь Дэвидсона. Тяжёлая трудноподдающаяся лечению диарея новорождённых по причине атрофии микроворсинок каёмчатых клеток кишечника.

Каёмчатая клетка На апикальной поверхности клетка имеет более 1000 микроворсинок, покрытых гликокаликсом. Цепи олигосахаридов, ковалентно связанных с гликопротеинами и гликолипидами плазмолеммы, выступают на наружной поверхности мембран клетки и формируют поверхностную оболочку толщиной 50 нм. Гликокаликс содержит аминопептидазы и гликозидазы (мальтаза, лактаза), завершающие расщепление белков и углеводов, и энтерокиназу, конвертирующую трипсиноген в трипсин. Каёмчатые клетки всасывают продукты гидролиза белков, жиров и углеводов, витамины, химические элементы (Са 2+, Fe 2+ и др. ).
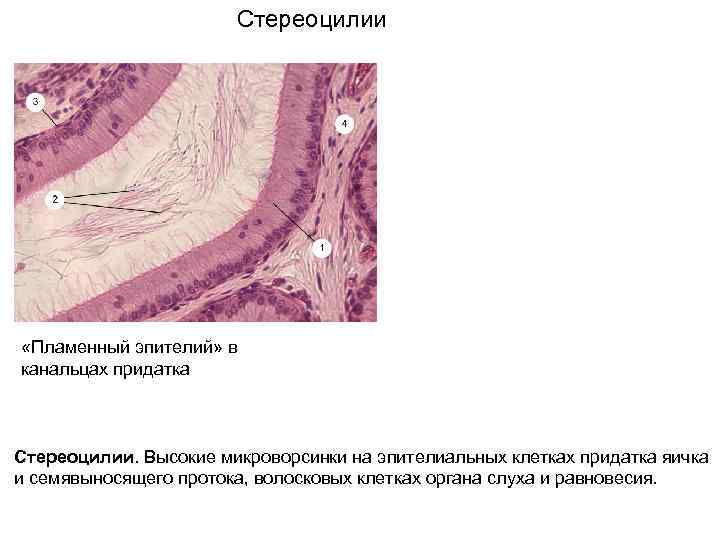
Стереоцилии «Пламенный эпителий» в канальцах придатка Стереоцилии. Высокие микроворсинки на эпителиальных клетках придатка яичка и семявыносящего протока, волосковых клетках органа слуха и равновесия.
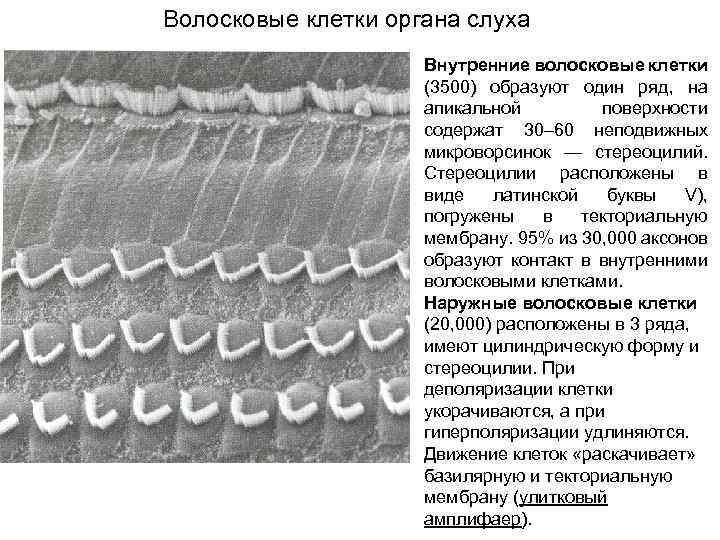
Волосковые клетки органа слуха Внутренние волосковые клетки (3500) образуют один ряд, на апикальной поверхности содержат 30– 60 неподвижных микроворсинок — стереоцилий. Стереоцилии расположены в виде латинской буквы V), погружены в текториальную мембрану. 95% из 30, 000 аксонов образуют контакт в внутренними волосковыми клетками. Наружные волосковые клетки (20, 000) расположены в 3 ряда, имеют цилиндрическую форму и стереоцилии. При деполяризации клетки укорачиваются, а при гиперполяризации удлиняются. Движение клеток «раскачивает» базилярную и текториальную мембрану (улитковый амплифаер).
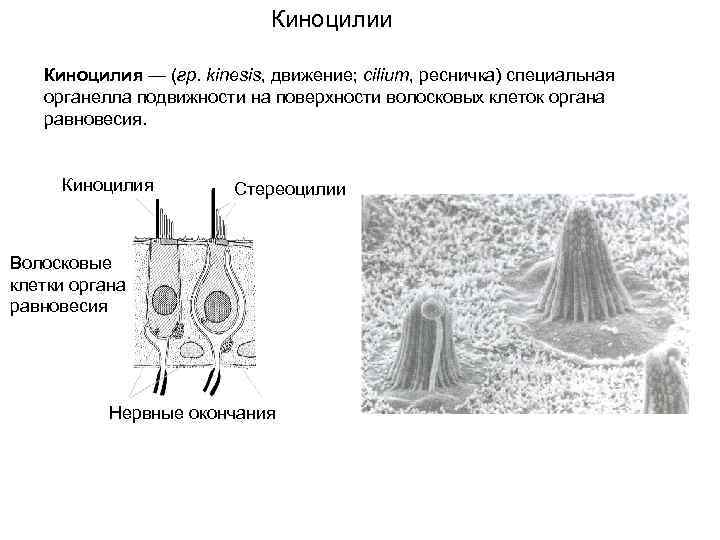
Киноцилии Киноцилия — (гр. kinesis, движение; cilium, ресничка) специальная органелла подвижности на поверхности волосковых клеток органа равновесия. Киноцилия Стереоцилии Волосковые клетки органа равновесия Нервные окончания
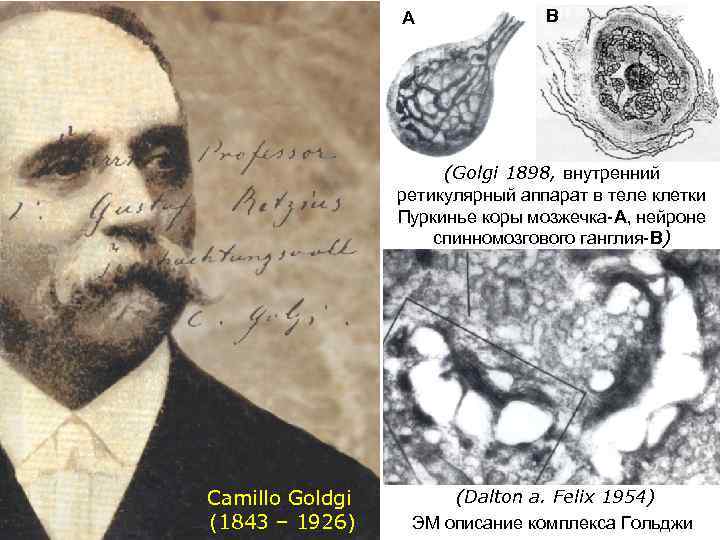
А В (Golgi 1898, внутренний ретикулярный аппарат в теле клетки Пуркинье коры мозжечка-А, нейроне спинномозгового ганглия-В) Camillo Goldgi (1843 – 1926) (Dalton a. Felix 1954) ЭМ описание комплекса Гольджи
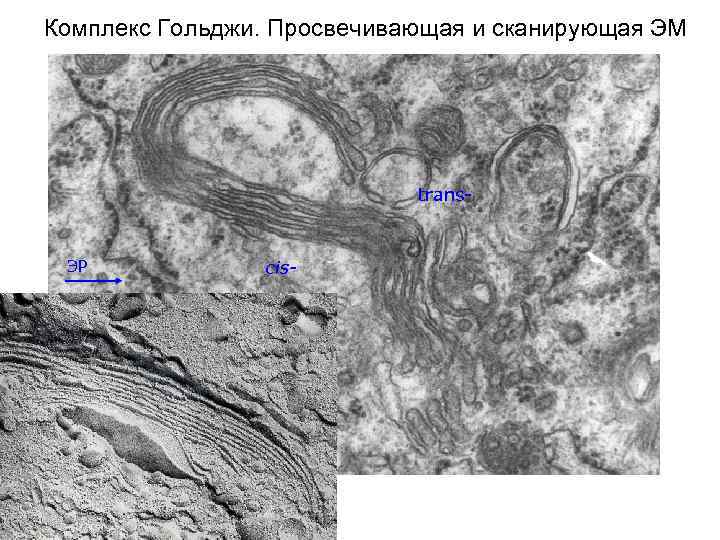
Комплекс Гольджи. Просвечивающая и сканирующая ЭМ trans- ЭР cis-
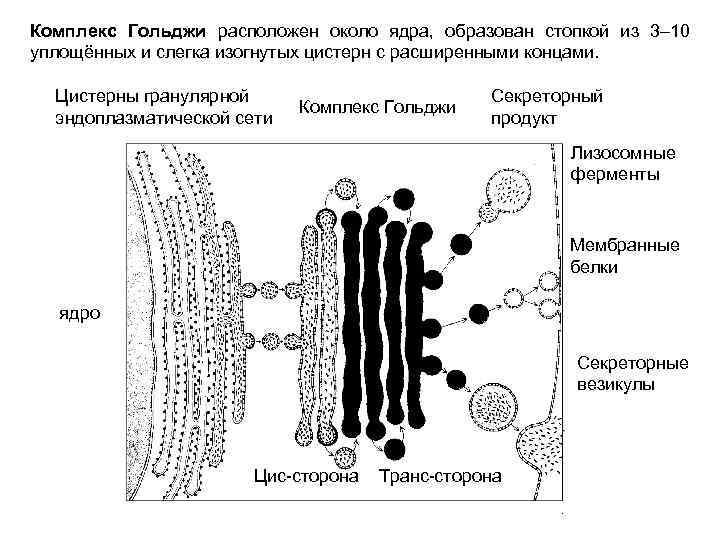
Комплекс Гольджи расположен около ядра, образован стопкой из 3– 10 уплощённых и слегка изогнутых цистерн с расширенными концами. Цистерны гранулярной эндоплазматической сети Комплекс Гольджи Секреторный продукт Лизосомные ферменты Мембранные белки ядро Секреторные везикулы Цис-сторона Транс-сторона

36 комплексов коатомер Функции: Øмодификация секреторного продукта Ø концентрирование Øсортировка и упаковка секреторного продукта Врождённая мышечная дистрофия. Гликозилтрансферазы (фукутин и связанный с фукутином белок) осуществляют гликозилирование дистрогликана в промежуточном компартменте. Мутация гена связанного с фукутином белка приводит к нарушению посттрансляционной модификации белка.
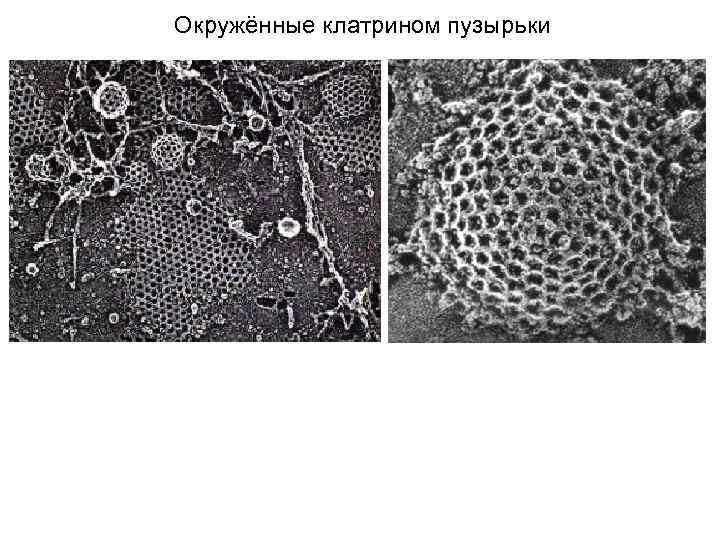
Окружённые клатрином пузырьки
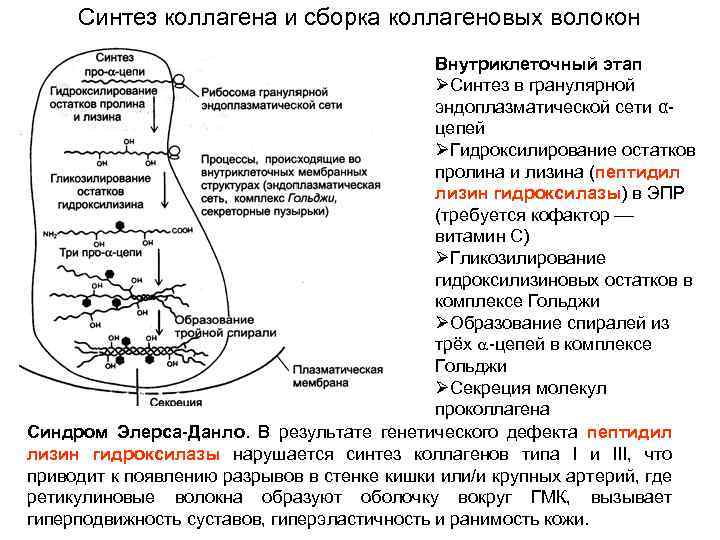
Синтез коллагена и сборка коллагеновых волокон Внутриклеточный этап ØСинтез в гранулярной эндоплазматической сети αцепей ØГидроксилирование остатков пролина и лизина (пептидил лизин гидроксилазы) в ЭПР (требуется кофактор витамин С) ØГликозилирование гидроксилизиновых остатков в комплексе Гольджи ØОбразование спиралей из трёх -цепей в комплексе Гольджи ØСекреция молекул проколлагена Синдром Элерса-Данло. В результате генетического дефекта пептидил лизин гидроксилазы нарушается синтез коллагенов типа I и III, что приводит к появлению разрывов в стенке кишки или/и крупных артерий, где ретикулиновые волокна образуют оболочку вокруг ГМК, вызывает гиперподвижность суставов, гиперэластичность и ранимость кожи.
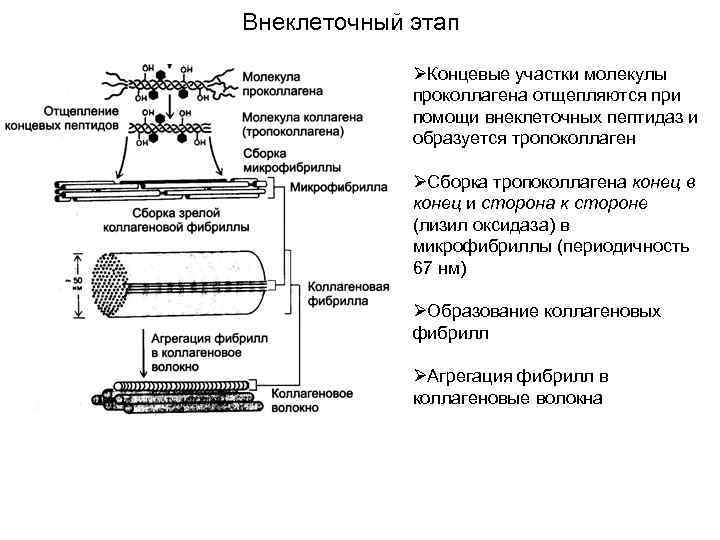
Внеклеточный этап ØКонцевые участки молекулы проколлагена отщепляются при помощи внеклеточных пептидаз и образуется тропоколлаген ØСборка тропоколлагена конец в конец и сторона к стороне (лизил оксидаза) в микрофибриллы (периодичность 67 нм) ØОбразование коллагеновых фибрилл ØАгрегация фибрилл в коллагеновые волокна
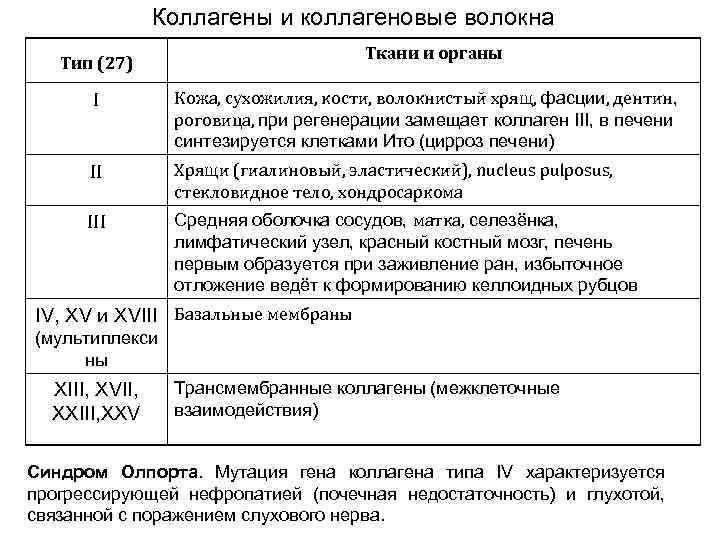
Коллагены и коллагеновые волокна Ткани и органы Тип (27) I Кожа, сухожилия, кости, волокнистый хрящ, фасции, дентин, роговица, при регенерации замещает коллаген III, в печени синтезируется клетками Ито (цирроз печени) II Хрящи (гиалиновый, эластический), nucleus pulposus, стекловидное тело, хондросаркома III Средняя оболочка сосудов, матка, селезёнка, лимфатический узел, красный костный мозг, печень первым образуется при заживление ран, избыточное отложение ведёт к формированию келлоидных рубцов IV, XV и XVIII Базальные мембраны (мультиплекси ны XIII, XVII, XXIII, XXV Трансмембранные коллагены (межклеточные взаимодействия) Синдром Олпорта. Мутация гена коллагена типа IV характеризуется прогрессирующей нефропатией (почечная недостаточность) и глухотой, связанной с поражением слухового нерва.
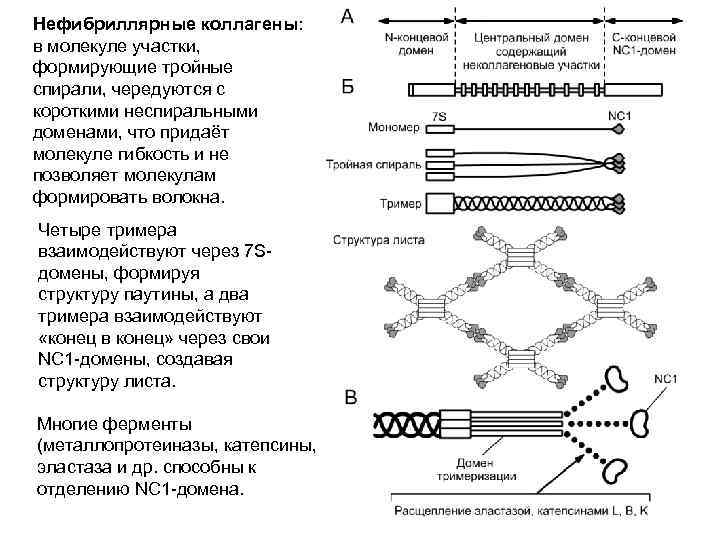
Нефибриллярные коллагены: в молекуле участки, формирующие тройные спирали, чередуются с короткими неспиральными доменами, что придаёт молекуле гибкость и не позволяет молекулам формировать волокна. Четыре тримера взаимодействуют через 7 Sдомены, формируя структуру паутины, а два тримера взаимодействуют «конец в конец» через свои NC 1 -домены, создавая структуру листа. Многие ферменты (металлопротеиназы, катепсины, эластаза и др. способны к отделению NC 1 -домена.

ДЕГРАДАЦИЯ КЛЕТОЧНЫХ БЕЛКОВ Деградация белков (цитозольный протеолиз) происходит по двум основным механизмам — убиквитин-протеосомный путь и опосредованная лизосомным протеолизом деградация. Протеосома Лизосомы

Лизосомы Образуются путём слияния перинуклеарных эндосом с везикулами, подлежащим деградации (периферической эндосомой, фагосомой, или аутофагоцитозной вакуолью). Лизосомные ферменты. Известно более 50 лизосомных ферментов: рибонуклеазы, дезоксирибонуклеазы, протеазы, сульфатазы, β‑глюкуронидазы, β‑галактозидазы, гликозидазы, липазы, эстеразы, фосфатазы и др. Лизосомы преимущественно работают внутриклеточно (утилизации «внутриклеточного мусора» ), однако некоторые клетки (например, нейтротрофилы, остеокласты) для выполнения своих функций секретируют лизосомы во внеклеточное пространство.
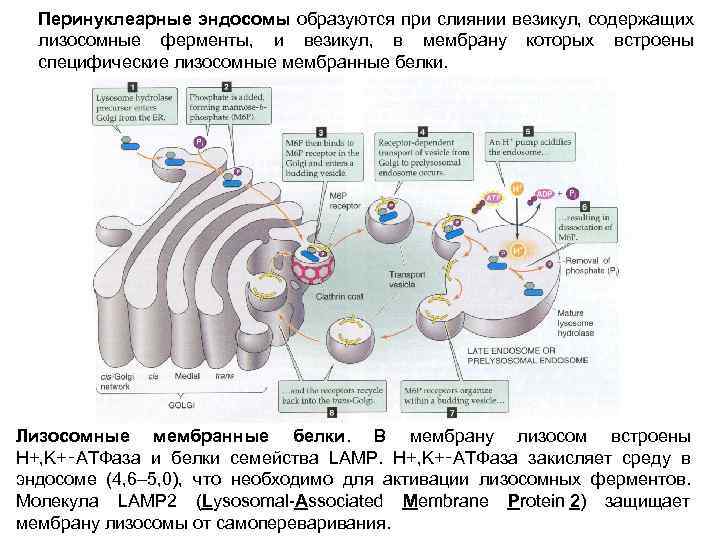
Перинуклеарные эндосомы образуются при слиянии везикул, содержащих лизосомные ферменты, и везикул, в мембрану которых встроены специфические лизосомные мембранные белки. Лизосомные мембранные белки. В мембрану лизосом встроены H+, K+‑ATФаза и белки семейства LAMP. H+, K+‑ATФаза закисляет среду в эндосоме (4, 6– 5, 0), что необходимо для активации лизосомных ферментов. Молекула LAMP 2 (Lysosomal-Associated Membrane Protein 2) защищает мембрану лизосомы от самопереваривания.
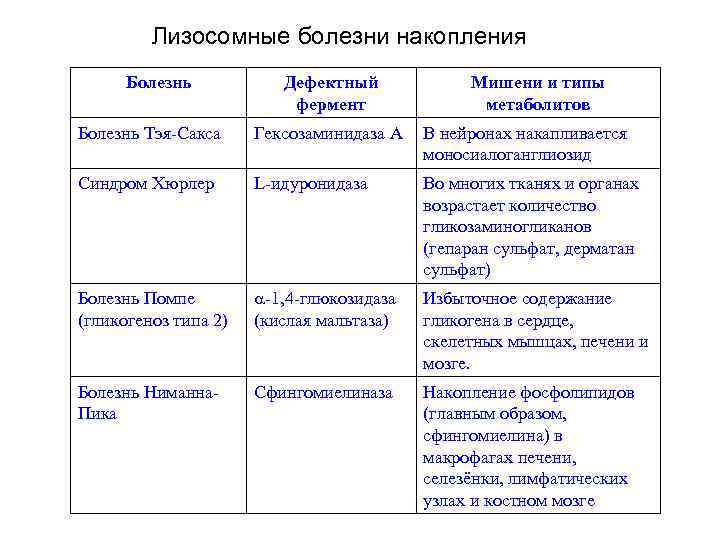
Лизосомные болезни накопления Болезнь Дефектный фермент Мишени и типы метаболитов Болезнь Тэя-Сакса Гексозаминидаза A В нейронах накапливается моносиалоганглиозид Синдром Хюрлер L-идуронидаза Во многих тканях и органах возрастает количество гликозаминогликанов (гепаран сульфат, дерматан сульфат) Болезнь Помпе (гликогеноз типа 2) -1, 4 -глюкозидаза (кислая мальтаза) Избыточное содержание гликогена в сердце, скелетных мышцах, печени и мозге. Болезнь Ниманна. Пика Сфингомиелиназа Накопление фосфолипидов (главным образом, сфингомиелина) в макрофагах печени, селезёнки, лимфатических узлах и костном мозге
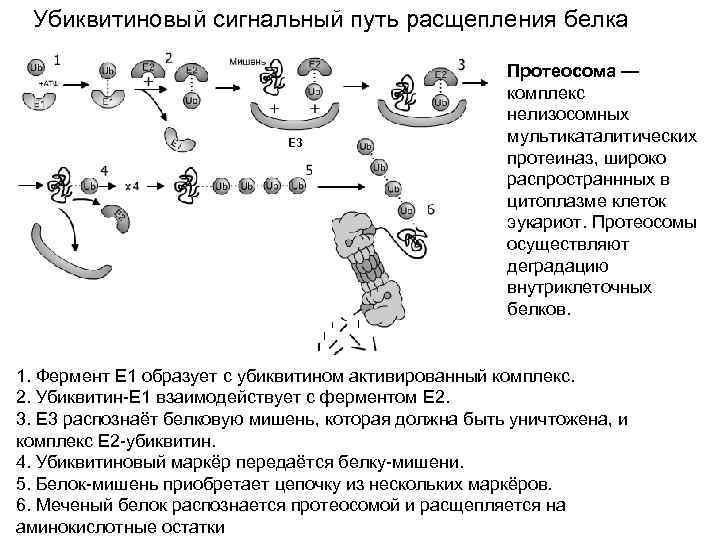
Убиквитиновый сигнальный путь расщепления белка Е 3 Протеосома — комплекс нелизосомных мультикаталитических протеиназ, широко распространнных в цитоплазме клеток эукариот. Протеосомы осуществляют деградацию внутриклеточных белков. 1. Фермент E 1 образует с убиквитином активированный комплекс. 2. Убиквитин-Е 1 взаимодействует с ферментом E 2. 3. E 3 распознаёт белковую мишень, которая должна быть уничтожена, и комплекс E 2 -убиквитин. 4. Убиквитиновый маркёр передаётся белку-мишени. 5. Белок-мишень приобретает цепочку из нескольких маркёров. 6. Меченый белок распознается протеосомой и расщепляется на аминокислотные остатки
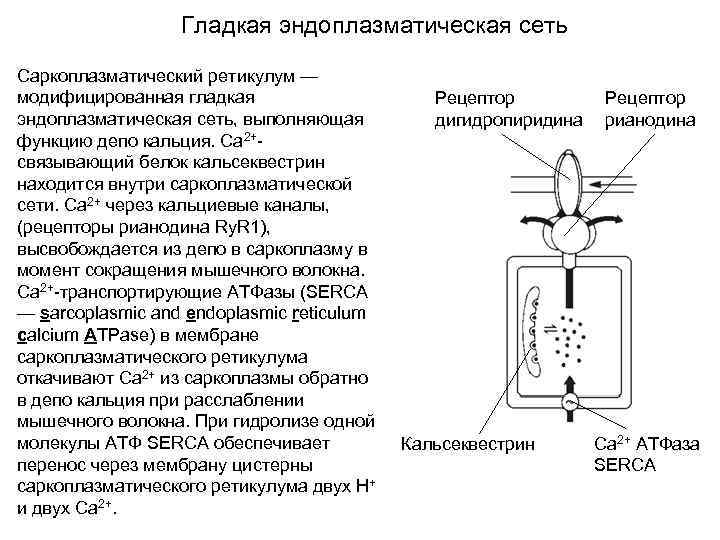
Гладкая эндоплазматическая сеть Саркоплазматический ретикулум — модифицированная гладкая эндоплазматическая сеть, выполняющая функцию депо кальция. Ca 2+связывающий белок кальсеквестрин находится внутри саркоплазматической сети. Ca 2+ через кальциевые каналы, (рецепторы рианодина Ry. R 1), высвобождается из депо в саркоплазму в момент сокращения мышечного волокна. Са 2+-транспортирующие АТФазы (SERCA — sarcoplasmic and endoplasmic reticulum calcium ATPase) в мембране саркоплазматического ретикулума откачивают Ca 2+ из саркоплазмы обратно в депо кальция при расслаблении мышечного волокна. При гидролизе одной молекулы АТФ SERCA обеспечивает перенос через мембрану цистерны сaркоплазматического ретикулума двух H+ и двух Ca 2+. Рецептор дигидропиридина Кальсеквестрин Рецептор рианодина Са 2+ АТФаза SERCA
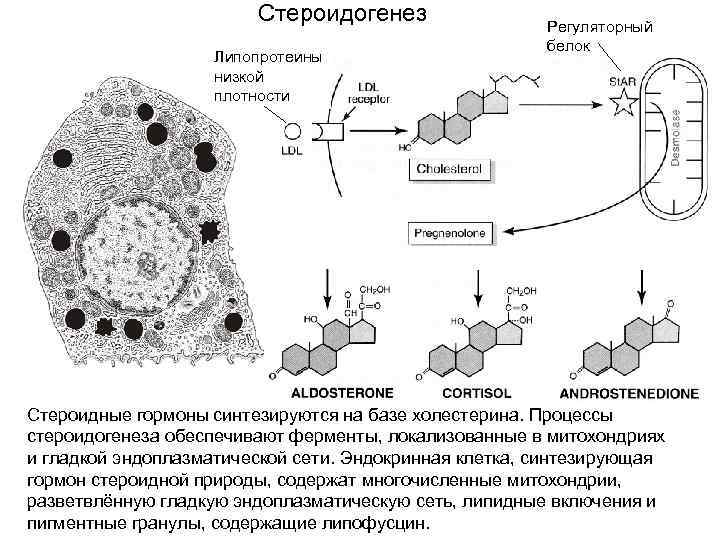
Стероидогенез Липопротеины низкой плотности Регуляторный белок Стероидные гормоны синтезируются на базе холестерина. Процессы стероидогенеза обеспечивают ферменты, локализованные в митохондриях и гладкой эндоплазматической сети. Эндокринная клетка, синтезирующая гормон стероидной природы, содержат многочисленные митохондрии, разветвлённую гладкую эндоплазматическую сеть, липидные включения и пигментные гранулы, содержащие липофусцин.
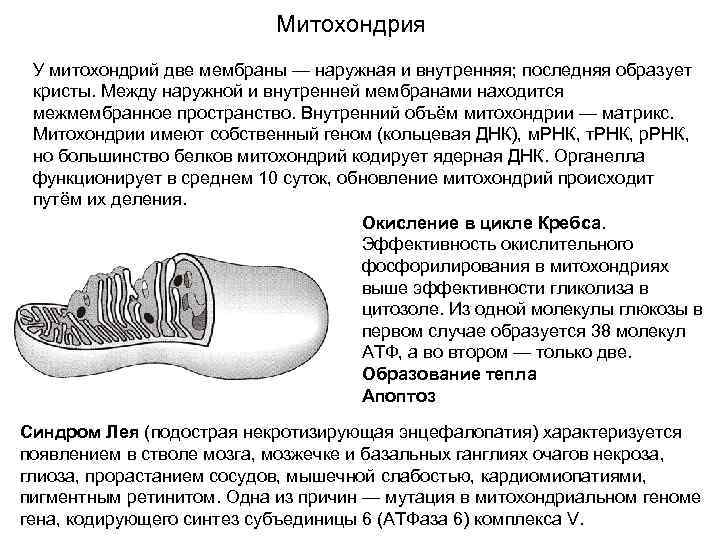
Митохондрия У митохондрий две мембраны — наружная и внутренняя; последняя образует кристы. Между наружной и внутренней мембранами находится межмембранное пространство. Внутренний объём митохондрии — матрикс. Митохондрии имеют собственный геном (кольцевая ДНК), м. РНК, т. РНК, р. РНК, но большинство белков митохондрий кодирует ядерная ДНК. Органелла функционирует в среднем 10 суток, обновление митохондрий происходит путём их деления. Окисление в цикле Кребса. Эффективность окислительного фосфорилирования в митохондриях выше эффективности гликолиза в цитозоле. Из одной молекулы глюкозы в первом случае образуется 38 молекул АТФ, а во втором — только две. Образование тепла Апоптоз Синдром Лея (подострая некротизирующая энцефалопатия) характеризуется появлением в стволе мозга, мозжечке и базальных ганглиях очагов некроза, глиоза, прорастанием сосудов, мышечной слабостью, кардиомиопатиями, пигментным ретинитом. Одна из причин — мутация в митохондриальном геноме гена, кодирующего синтез субъединицы 6 (АТФаза 6) комплекса V.
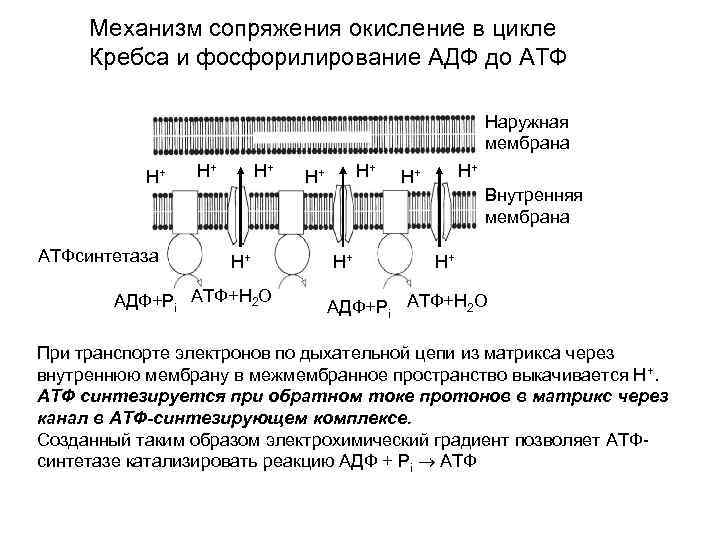
Механизм сопряжения окисление в цикле Кребса и фосфорилирование АДФ до АТФ Наружная мембрана Н+ АТФсинтетаза Н+ Н+ Н+ АДФ+Рi АТФ+Н 2 О Н+ Н+ Н+ Внутренняя мембрана Н+ АДФ+Рi АТФ+Н 2 О При транспорте электронов по дыхательной цепи из матрикса через внутреннюю мембрану в межмембранное пространство выкачивается H+. АТФ синтезируется при обратном токе протонов в матрикс через канал в АТФ-синтезирующем комплексе. Созданный таким образом электрохимический градиент позволяет АТФсинтетазе катализировать реакцию АДФ + Рi АТФ
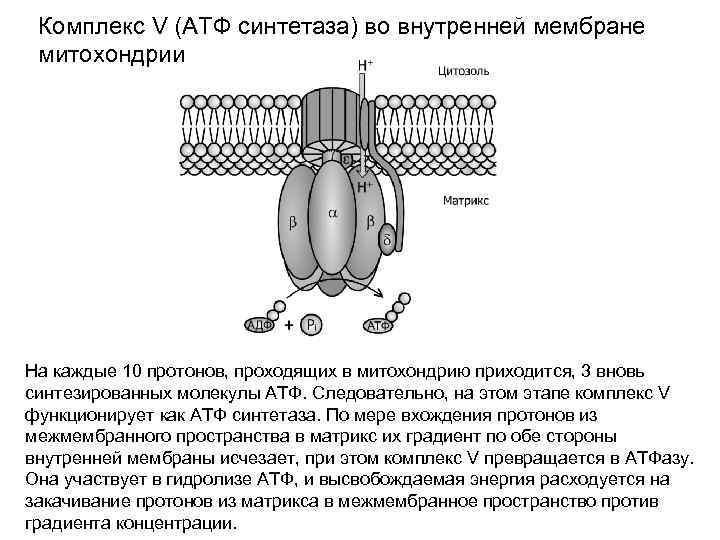
Комплекс V (АТФ синтетаза) во внутренней мембране митохондрии На каждые 10 протонов, проходящих в митохондрию приходится, 3 вновь синтезированных молекулы АТФ. Следовательно, на этом этапе комплекс V функционирует как АТФ синтетаза. По мере вхождения протонов из межмембранного пространства в матрикс их градиент по обе стороны внутренней мембраны исчезает, при этом комплекс V превращается в АТФазу. Она участвует в гидролизе АТФ, и высвобождаемая энергия расходуется на закачивание протонов из матрикса в межмембранное пространство против градиента концентрации.

Разобщение окислительного фосфорилирования Естественный механизм разобщения окислительного фосфорилирования функционирует в клетках бурого жира. В этих клетках митохондрии имеют атипичную структуру (уменьшен их объём, увеличена плотность матрикса, расширены межмембранные пространства) — конденсированные митохондрии. Такие митохондрии могут усиленно захватывать воду и набухать в ответ на тироксин, увеличение концентрации Ca 2+ в цитозоле, при этом усиливается разобщение окислительного фосфорилирования, и происходит выделение тепла. Эти процессы обеспечивает специальный разобщающий белок термогенин. Норадреналин из симпатического отдела вегетативной нервной системы усиливает экспрессию разобщающего белка и стимулирует теплопродукцию.
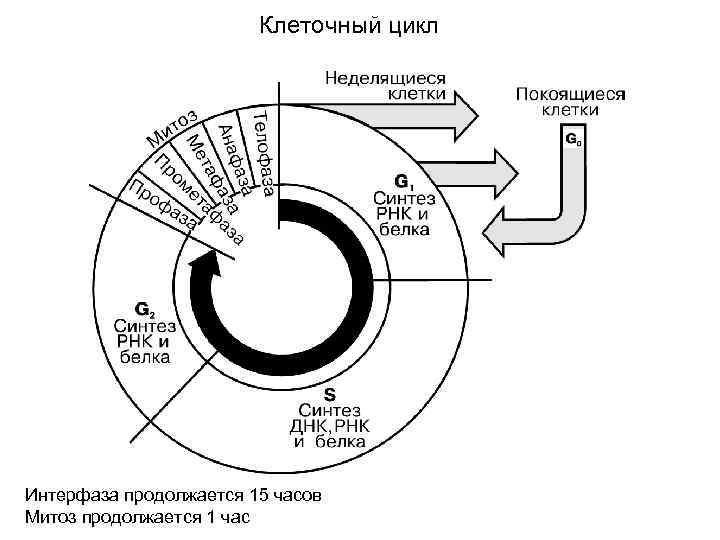
Клеточный цикл Интерфаза продолжается 15 часов Митоз продолжается 1 час

М-фаза клеточного цикла Профаза. Каждая хромосома состоит из двух сестринских хроматид, митотические центры располагаются вблизи ядерной мембраны. Прометофаза. В области центромер появляются кинетохоры, функционирующие как центры организации кинетохорных микротрубочек. Метафаза. Образуется метафазная пластинка. Хромосомы располагаются в области экватора веретена. Анафаза — расхождение дочерних хромосом к полюсам митотического веретена. Телофаза. Хроматиды подходят к полюсам, кинетохорные микротрубочки исчезают, а полюсные продолжают удлиняться. Образуется ядерная оболочка, появляется ядрышко.

Регуляторы клеточного цикла G 2 checkpoint G 1 checkpoint Циклин-зависимые протеинкиназы (Cdk) контролируют последовательные события клеточного цикла путём фосфорилирования белков-мишеней. Циклины (A, B, D, E) взаимодействуют с Cdk, контролируя их активность. Прото-онкогены кодируют белки, стимулирующие клеточный цикл (ras). Онкогены мутированные прото-онкогены. Анти-онкогены кодируют белки, блокирующие клеточный цикл (р53). Блокирует G 1 S, G 1 checkpoint.

Клеточное старение (cell senescence), также называемое репликативным старением, подразумевает ограниченную способность клеток к делению в культуре in vitro, впервые описанное Хейфликом и коллегами в 1965 году (лимит Хейфлика). В этих классических экспериментах было показано, что сначала первичные фибробласты кожи человека активно делятся в культуре. Затем после многих удвоений интенсивность пролиферации клеток постепенно, но неуклонно снижается. В конце концов, все клетки в культуре необратимо теряют способность к делению и приобретают характерные морфологические изменения. На этом этапе фибробласты можно поддерживать в жизнеспособном состоянии в течение нескольких недель, но такая культура неспособна к росту, несмотря на наличие всех необходимых условий. Предполагается, что подобное ограничение в количестве делений клеток может лежать в основе процессов старения организма. Несмотря на то, что ранее клеточное старение считалось необратимым, в настоящее время было показано, что определенные фармакологические препараты могут, по крайней мере частично, подавлять связанные со старением изменения.

Анти-онкогены Онкосупрессоры в нормальной клетке постоянно контролируют множество процессов, в том числе и пролиферацию клеток (точнее, онкосупрессоры блокируют клеточный цикл). Известно множество онкосупрессоров (например, Rb, p 27, p 53, PTEN), среди которых p 53 известен как главный супрессор развития опухоли. Мутации генов онкосупрессоров неизбежно приводят к появлению бесконтрольно пролиферирующего клеточного клона. Белок p 27 связывается с циклином и Cdk и блокирует вхождение клетки в S-фазу цикла. Определение р27 используют в диагностике рака молочной железы. Снижение уровня р27 является плохим прогностическим признаком.
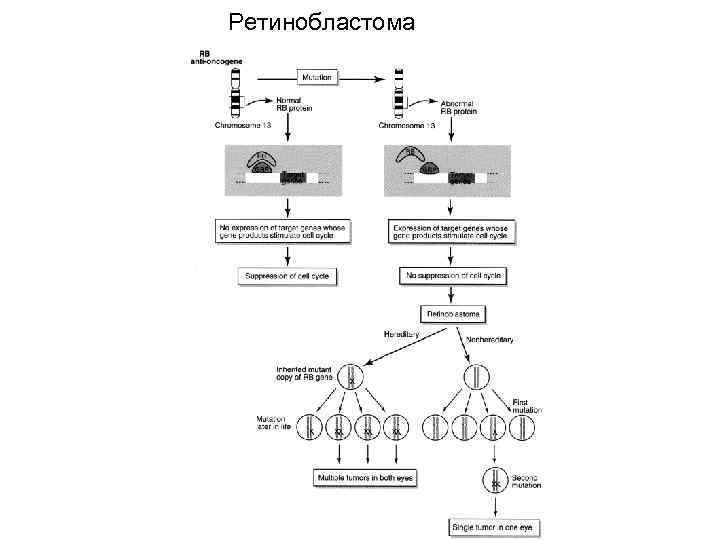
Ретинобластома
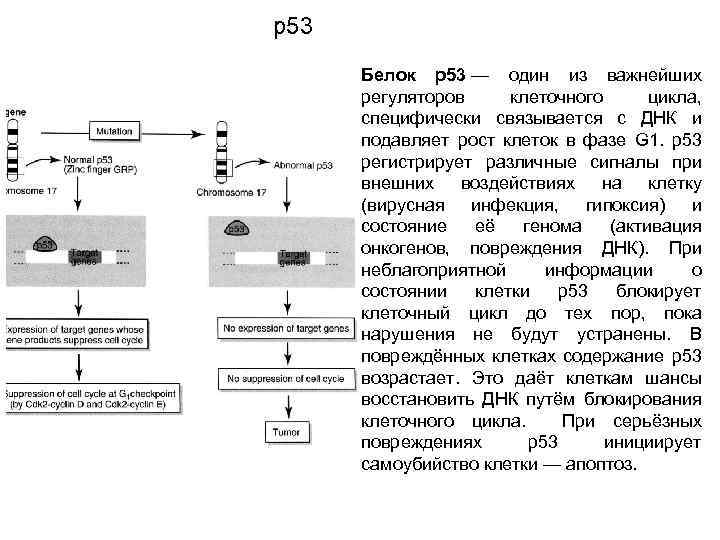
р53 Белок р53 — один из важнейших регуляторов клеточного цикла, специфически связывается с ДНК и подавляет рост клеток в фазе G 1. р53 регистрирует различные сигналы при внешних воздействиях на клетку (вирусная инфекция, гипоксия) и состояние её генома (активация онкогенов, повреждения ДНК). При неблагоприятной информации о состоянии клетки р53 блокирует клеточный цикл до тех пор, пока нарушения не будут устранены. В повреждённых клетках содержание р53 возрастает. Это даёт клеткам шансы восстановить ДНК путём блокирования клеточного цикла. При серьёзных повреждениях р53 инициирует самоубийство клетки — апоптоз.
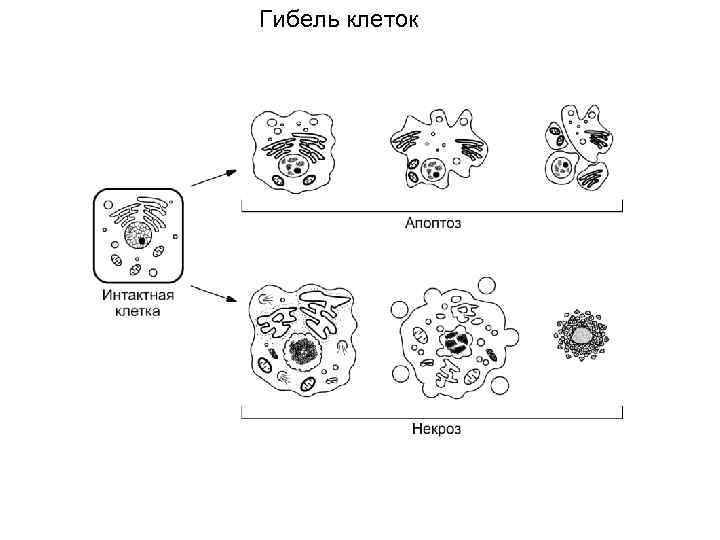
Гибель клеток
Признак Апоптоз Некроз Гибель клетки Программируемая Спонтанная Объём клетки Уменьшение Увеличение, набухание и лизис клеток Регулируемость процесса элиминации клетки Да Нет Фрагментация клеток на визикулы с внутриклеточным содержимым Да Нет Зависимость от наличия АТФ Да Нет Образование активных форм кислорода Да Нет Активация каспаз Да Нет Распространенность Одиночная клетка Группа клеток Воспалительный ответ Нет Обычно есть Распад на части Да Нет ДНК Внутриядерная конденсация с разрывом нитей в межнуклеосомных участках Диффузная локализация в некротизированной клетке Ядро Конденсация хроматина по периферии ядра Да Нет
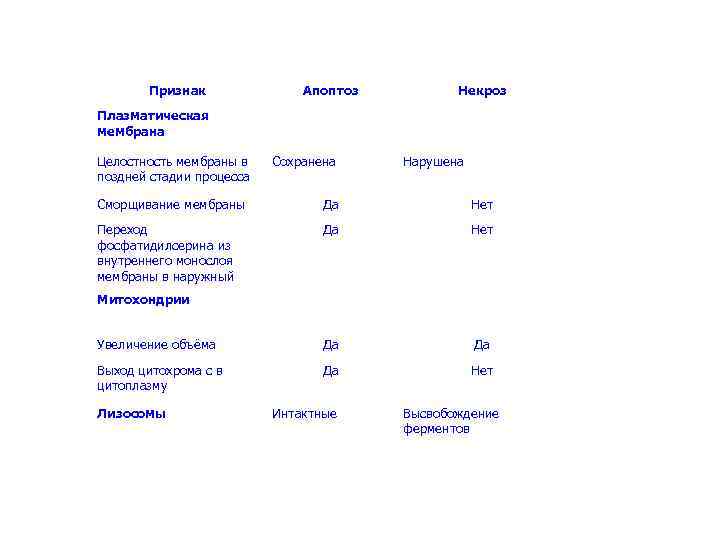
Признак Апоптоз Некроз Плазматическая мембрана Целостность мембраны в поздней стадии процесса Сохранена Нарушена Сморщивание мембраны Да Нет Переход фосфатидилсерина из внутреннего монослоя мембраны в наружный Да Нет Увеличение объёма Да Да Выход цитохрома с в цитоплазму Да Нет Митохондрии Лизосомы Интактные Высвобождение ферментов

Программа апоптоза консервативна и универсальна от червя до человека Феноменология: Øактивация эндогенных протеаз Øконденсация клеточного ядра и деградация ядерной ДНК Благодаря апоптозу осуществляются: Øэмбриогенез Øгормон-зависимая инволюция клеток в менструальном цикле Øудаление лишних или потенциально опасных клеток (лимфоциты) Øудаление опухолевых клеток Øудаление инфицированных вирусом клеток (Т киллерами) Гены, контролирующие апоптоз: Øгены смерти (ICE – interleukin-1β-converting enzyme) Øанти-апоптозный ген (bcl-2) Апоптоз и болезни: ØМногие опухоли используют BCL-2 для подавления клеточной гибели ØЭкспрессия bcl-2 плохой прогноз рака кишечника, рака предстательной железы ØИнгибиторы апоптоза ограничивают размеры инфаркта (сердца, мозга)
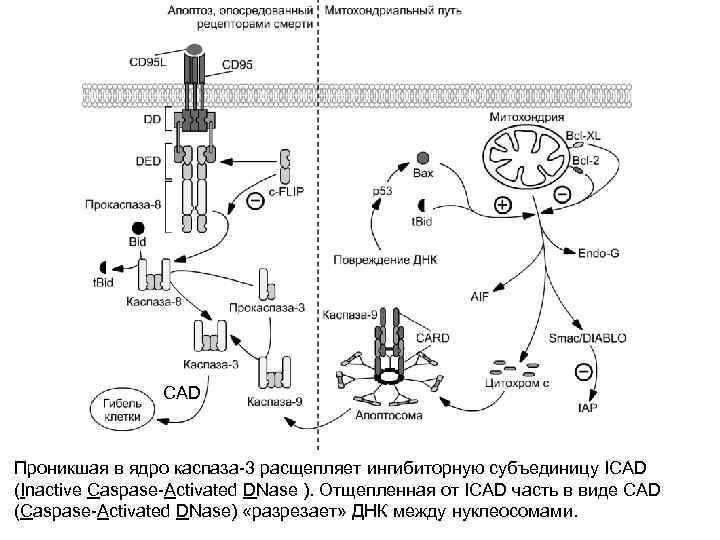
CAD Проникшая в ядро каспаза-3 расщепляет ингибиторную субъединицу ICAD (Inactive Caspase-Activated DNase ). Отщепленная от ICAD часть в виде CAD (Caspase-Activated DNase) «разрезает» ДНК между нуклеосомами.

Митохондрии — ключевой регулятор молекулярного механизма апоптоза Проапоптозные белки (Bax, Bak) способствуют образованию пор перехода проницаемости в мембране митохондрий и таким образом поддерживают проницаемость для ряда факторов, активирующих апоптоз и выходящих из митохондрий в цитозоль. Антиапоптозные белки (Bcl-2), наоборот, блокируют проницаемость мембраны митохондрий.
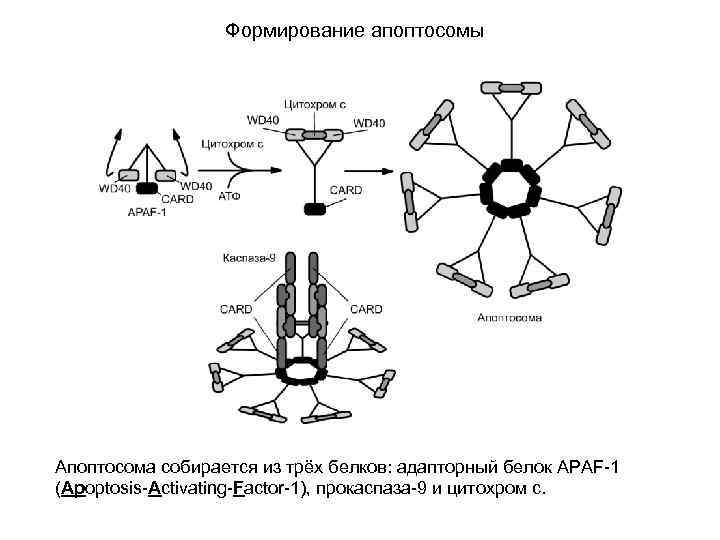
Формирование апоптосомы Апоптосома собирается из трёх белков: адапторный белок APAF-1 (Apoptosis-Activating-Factor-1), прокаспаза-9 и цитохром c.

Методы выявления апоптозных клеток Под действием каспаз в клетке, вступившей в апоптоз, появляются метки для последующего их распознавания и фагоцитоза. Подобной меткой служит принадлежащий к фосфолипидам внутреннего слоя плазматической мембраны фосфатидилсерин. В результате действия каспазы этот сигнал «выставляется» на поверхности клетки и распознаётся фагоцитом при участии молекулы CD 14. TUNEL-метод (Transferase mediated d. UTP Nick End Labeling) основан на выявлении 3’-ОН концов в молекуле ядерной ДНК, образующихся при её фрагментации в клетках, вступивших в апоптоз. 3'-Урацил, конъюгированный с биотином, с помощью терминальной дезоксинуклеотидил трансферазы (Td. T) включается в фрагменты ДНК. Далее биотинилированный нуклеотид выявляют с помощью стрептавидина, меченного пероксидазой хрена [стрептавидинбиотиновый метод, основанный на высокой аффинности (сродстве) биотина к стрептавидину].
Медицинская биология_клетка.ppt