
(этилен көмірсутектері - олефиндер)

Құрамында қос байланыс бар қосылыстарды қанықпаған көмірсутектер алкендер немесе этилен көмірсутектері алкендер этилен деп атайды. Жалпы формуласы: Сn. H 2 n
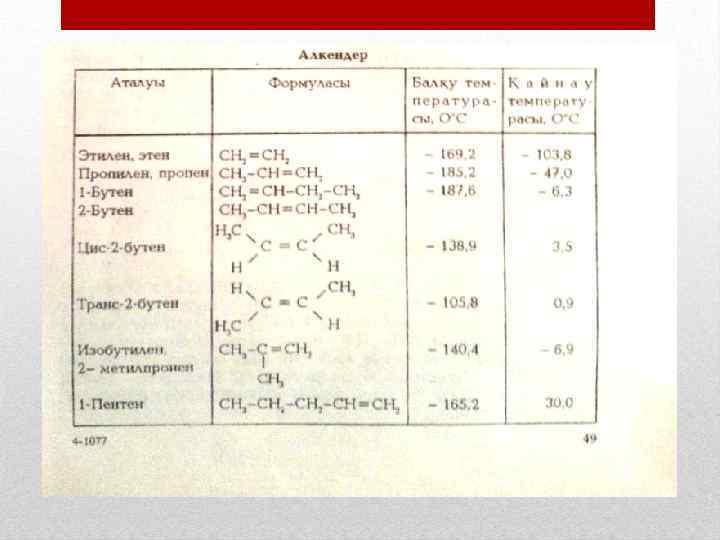

Олефиндердін аттары ИЮПАК номенклатурасы бойынша өздерімен құрылымы бірдей парафиндердің атынан түзіледі, сәйкес парафиннің атындағы ан деген қосымшасын -ен ге ауыстырады да, цифрмен қос байланыстың орнын көрсетеді. Бастапқы тізбек ретінде ең ұзын тізбек алынады. Көміртек атомдары қос байланыс жақын түрған жағынан бастап нөмірленеді.

Қатардың бірінші мүшелері үшін тривиалдық аты сақта лады: этилен, пропилен, изобутилен (7 кесте) радикалдары: СН 2 = СН — винил, Н 2 С = СН—СН 2 аллил. Көміртек тізбегінің қүрылымына байланысты болатын изомерлермен қатар, алкендердің тізбектегі қос байланыстың орнына байланысты құрылымдық изомериясы да болады:

Бұдан басқа алкендер қатарында цис транс изомерия деп аталатын кеңістік (геометриялық) изомерия да болады; цис изомерлерде қос цис байланыстағы көміртек атомдары (жеке жағдайда бір түрлі) немесе атомдар топтары осы қос байланыстың бір жағында, ал транс изомерлерде қарама қарсы жақта болады:

Алкендер қатарында геометриялық цис транс изомерия ның болуы екі көміртек атомдары изомерия арасындағы а байланыс өсі бойынша бос айналуға π байланыстың мүмкіндік бермеуіне байланысты. Цис және транс изомерлердің физикалық және транс химиялық қасиеттерінде елеулі айырмашы лықтар бар (7 кесге). Цис изомерлер "Z" (zusamen — бірге), транс изомерлер "Е" (entgegen қарама қарсы) символда рымен белгіленеді.

Алу тәсілдері. Табиғатта алкендер аз мөлшерде кездеседі, кейбір мүнайларда, әсіресе Канада мұнайында кеп болады. Мұнайдан таза күйінде С 6 Н 12 ден С 13 Н 26 –ға дейін көмірсутектер бөлініп алынады. Техникада оларды мұнайды табиғи және қосалқы газдарды химиялық өңдеу жолымен синтездейді. Алкендер және де тас көмір өнімдерін (кокстеу газдары) өңдеу арқылы алынады.

1. Алкендердің алғашқы төрт өкілі таза күйінде техника да мұнай крекингі өнімдерінің газ күйіндегі бөліктерінен қысыммен немесе төмен температурада айдау арқылы айдау және кокстау газдарынан (этилен, пропилен) бөлініп пропилен) алы нады. 2. Өндірісте алкендерді қаныққан көмірсутектерін дегидрогендеу арқылы да алады. дегидрогендеу Мысалы, алюмохромкалий катализаторының (K 2 O Cr 2 O 3 — А 12 O 3) қатысуымен 560 620°С температурада н бутаннан бутилендер алынады:

3. Спирттерді дегидратациялау (суды бөліп алу) алкендерді алудың ең көбірек қолданылатын тәсілінің бірі болады: Дегидратациялау (сусыздандыру) катализаторлары ретінде әр түрлі қышқылдар (күкірт, фосфор қышқылда ры), қышқылды түздар (KHS 04), алюминий оксиді (А 12 О 3), хлорлы мырыш (Zn. Cl 2) және т. б. (сұйық фазалы тәсіл) қол данылады. Этиленді спирттің буын А 12 О 3 катализаторы үстінен 380 400 °С температурада жіберу арқылы (бу фазалы де гидратация) луға болады: а

Спирттің құрылымына байланысты сусыздандыру процесі әр түрлі жағдайда өтеді, Әсіресе үшіншілік спирттер оңай сусызданады, олар қайта айдау кезінде суда өздігінен бөлініп кетеді. Судың бөлінуі Зайцев ережесі бойынша жүреді: су түзілгенде, сутек жақын тұрған ең аз сутектенген көміртек атомынан бөлінеді:

4. Алкендерді галоген туындылардан галогенсутектерін немесе галогенді үзіп алу арқылы жиі алады Моногалоген туындылары сілтілермен әрекеттескенде (дегидрогалогендеу) алкендер алынады:

Реакцияға КОН немесе Na. OH спирттік ерітіндісі немесе үнтақталған қатты сілті қолданылады. Осы жағдайда дегидрогалогендеудің багыты жоғарыда қаралған Зайцев ережесіне сәйкес жүреді: Зайцев ережесіне СН 3 — СНВr — СН 2— СН 3 — СН=СН — СН 3 Алкендерді алу үшін галоген атомдары көршілес көміртек атомдарында орналасқан дигалоген туындылардан галоген үзіп алу әдісі де пайдаланылады. Көбінесе бүл реакция мырыш үнтағының немесе жаңқасының су спирт ерітіндісінде жүреді: R — СНС 1 — СН 2 С 1 + Zn R — СН = СН 2 + Zn. Cl 2

Физикалық қасиеттері. Этилен көмірсутектері гомологтық қатарының бастапқы үш өкілі газ тәріздес пентеннен С 17 алкенге дейінгі олефиндер сұйықтар, одан әрі қарай қатты (7 кесте) болып табылады. Молекулалық масса лары өскен сайын балқу және қайнау температуралары артады. Көміртек атомдары нормалды тізбекті олефиндер өздерінің тармақталған тізбекті изомерлерінен гөрі жоға рырақ температурада қайнайды. Цис изомерлер әдетте Цис изомерлер трас изомерлерден гөрі жоғарырақ температурада қайнай ды, ал балқу температуралары керісінше. Алкендердің суда ерігіштігі тіпті аз, олардың тыгыздықтары бірден кем және гомологтық қатарда тығыздықтары артады.

Химиялық қасиеттері. Алкендер көбінесе қосылу реак циясына бейім болып келеді және олар тотыгу және полимерлену реакцияларына оңай түседі. Көміртек көміртек тізбегінің арасындағы π байланысты үзуге 251 к. Дж/моль энергия жүмсалса, байланысты үзуге 335 к. Дж/моль энергия қажет. Реагенттің шабуылы (әсері) алдымен π байланысқа бағытталады және де π байланысқа шабуыл оңай болады, себебі алкендерде π байланысқа жүретін реакция электроны жетіспейтін бөлшек арқылы басталады. Ондай бөлшектер катион, бос радикал немесе карбен болады. карбен Нәтижесінде π байланыс үзіліп, екі жаңа байланыс түзіледі, sр2 гибридтенген көміртек атомы sр3 гибридтенген күйге ауысады:

Олефинге қосылу реакциясы катионның π байланысқа шабуылынан басталады, содан кейін анион пайда болған шабуылынан карбкатионға қосылады. Реакция сатыларын жалпы түрде былай келтіруге болады:

Көміртек көміртек қос байланысындағы қосыду реакциялары көбінде электрофильді қасиет көрсетеді (АЕ), осы кезде қос байланыс электрондонор ретінде нуклеофильді қасиет көрсетеді. Олефиндердің қосылу реакциясының мынадай түрлерін келтіруге болады. 1. Гидрлеу. Алкендер катализаторлардың Pt, Pd қатысу . ында қалыпты температурада сутекті қосып алып, қанық қаң көмірсутектеріне айналады:

Егер катализатор ретінде ұсақ ұнтақталған никель алынса, реакция 150~300°С температурада (Сабтье реак циясы) жүреді, Гидрлеу жылдамдығы катализатордың та биғаты мен белсенділігіне, гидрлеу жагдайына және алкендердің қүрылымына байланысты болады. Платина мен палладийде гидрлеу реакциясы қалыпты температурада реакциясы жақсы жүреді, ал никель колданылғанда қыздыру қажет. Канықпаған байланыстарды гидрлеу техникадажәне аналитикалық тәжірибеде кеңінен қолданылады Майларды гидрлеу азық түлік өнеркәсібінде өте маңызды орын алады.

2. Галогендеу. Алкендерге галогендер өте оңай қосылып, дигалоген туындыларын береді. Галоген π байланыстың әсерінен поляризацияланады, жартылай оң зарядталған галоген π жүйесімен әрекет π жүйесімен тесіп, π комплекс түзеді: π комплекс
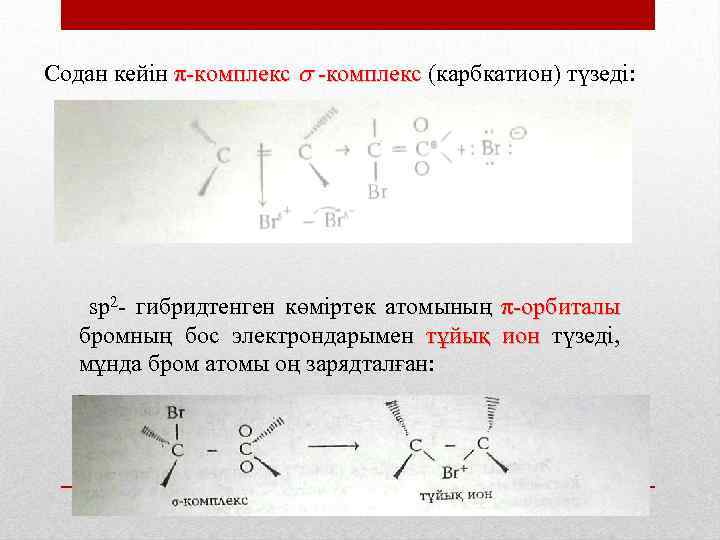
Содан кейін π комплекс (карбкатион) түзеді: комплекс sр2 гибридтенген көміртек атомының π орбиталы бромның бос электрондарымен тұйық ион түзеді, мұнда бром атомы оң зарядталған:
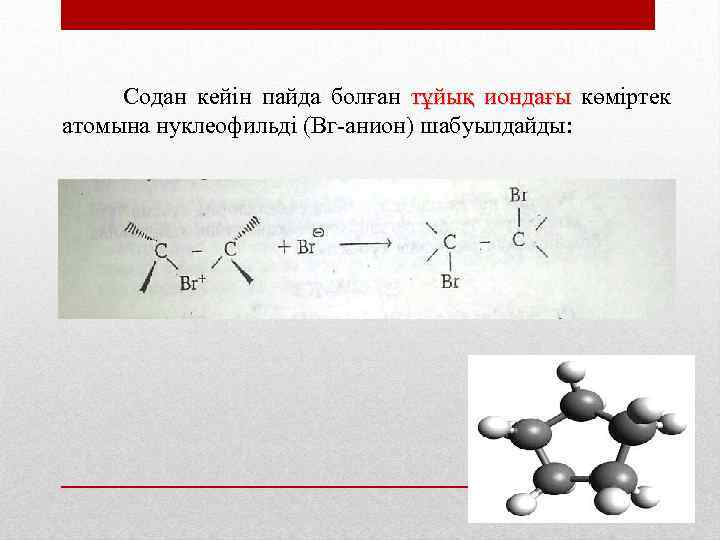
Содан кейін пайда болған тұйық иондағы көміртек атомына нуклеофильді (Вг анион) шабуылдайды:

Нуклеофиль (Вг анионы) тұйық ионды бұзып, көміртек атомымен байланыс түзіледі. Қос байланысқа HBr, H 2 SО 4, Н 2 О және басқа анорганикалық заттардың қосылуы жоғарыда көрсетілген механизмдермен жүреді. Бромның қосылуы (бром суының түссізденуі) қос байланысқа сапалы реакция болып саналады. Хлор, бром алкендерге бос радикалды механизм арқылы қосыла алады. Бұл реакциялар ионды қосылу реакцияларына қарағанда тез жүреді. Бірақ реакция жүру үшін инициатор керек. Реакцияның жалпы жүру тәртібі мына төмендегідей бо лады: Жарықтың әсерінен және жоғары температурада немесе пероксидтердің қатысуында бром молекуласы екі бром радикалына ыдырайды:

Жарықтың әсерінен және жоғары температурада немесе пероксидтердің қатысуында бром молекуласы екі бром радикалына ыдырайды: бром радикалына Жоғары температурада (300°C) пропилен хлормен әрекеттескенде аллилхлорид түзіледі. Себебі мұнда қосылу реакциясы емес, орынбасу реакциясы жүреді: реакциясы

3. Галогенсутектерімен қосылу реакциясы Пропилен хлорсутекпен әрекеттескенде алынатын негізгі өнім 2 хлор пропан болады, ал 1 хлорпропан өте аз мөлшерде түзіледі: 4. Гидратаииялау(су қосылу). Катализатордың (H 2 S 04, Zn. Cl 2 және т. б. ) қатысуымен алкендер су қосып алып, алкендер спирттер түзеді, Реакция Марковников ережесіне сәйкес жүреді:

Алкендерді күкірт қышқылды тәсілмен гидратациялаудың кейбір кемшіліктері бар (қондырғылардың коррозиясы, күкірт қышқылының шығындалуы және оның қиын регенерациялануы және т. б, ). Сол себептен Н 3 Р 04 (тасымалдаушыда) немесе А 12 О 3 катализаторын қолданып, тікелей гидратация жүргізеді:

5. Олефиндерге хлорлылау қышқылдың қосылуы Марковников ережесіне сәйкес жүреді, теріс зарядты гид роксил тобы көбінесе ең аз сутектенген көміртек атомына қосылады:

6. Олефиндердің тотығуы. Олефиндер оңай тотығады. Тотығу бағыты және пайда болатын өнімдер алкеннің құрылымына, тотықтырғыштарға және тотығу жағдайына байланысты: а) калий перманганатының сілтілік ортадағы ерітіндісі (Вагнер реакциясы) гликольдер береді: ә) ауадагы оттек күміс катализатордың қатысуында олефиндерді органикалық тотықтарға (эпоксидтерге) дейін тотықтырады:
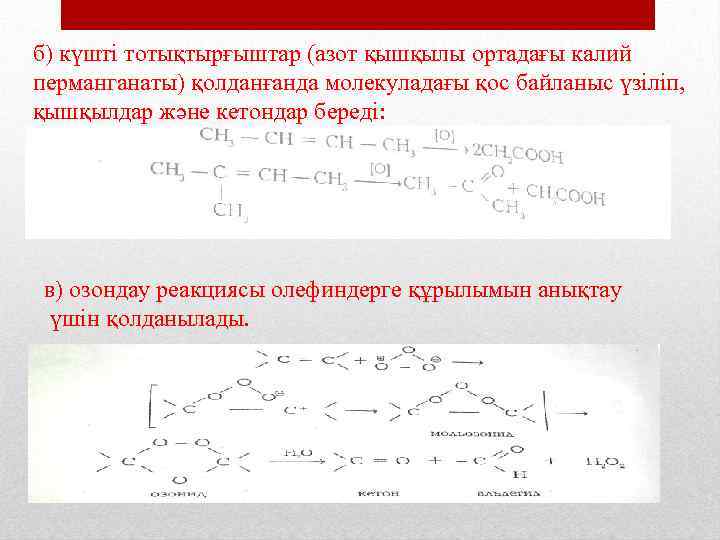
б) күшті тотықтырғыштар (азот қышқылы ортадағы калий перманганаты) қолданғанда молекуладағы қос байланыс үзіліп, қышқылдар және кетондар береді: в) озондау реакциясы олефиндерге құрылымын анықтау үшін қолданылады.