Жданкин А.Е._БХ-14м-6.pptx
- Количество слайдов: 29

Эти молекулы такие «аппетитные» …

Министерство образования и науки Украины Днепропетровский национальный университет им. Олеся Гончара Факультет биологии, экологии и медицины Кафедра биофизики и биохимии Металлоцены: понятие и физико -химические свойства Подготовил : студент гр. БХ-14 м-6 Жданкин А. Е. Днепропетровск-2015
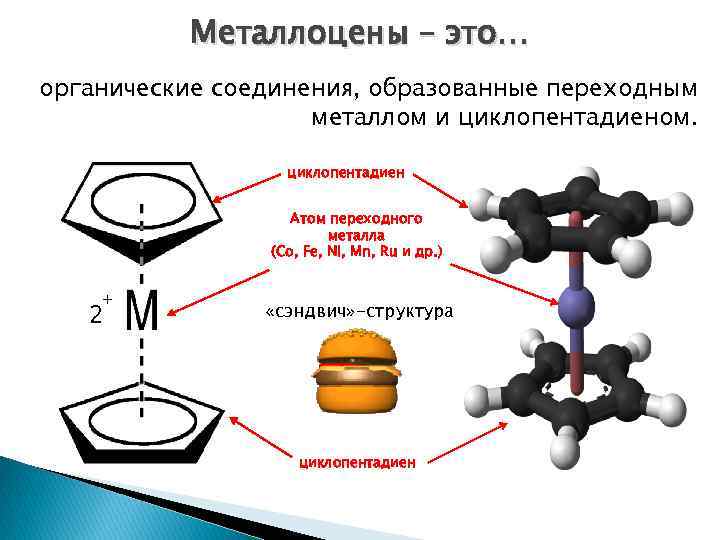
Металлоцены – это… органические соединения, образованные переходным металлом и циклопентадиеном. циклопентадиен Атом переходного металла (Со, Fe, Ni, Mn, Ru и др. ) + 2 «сэндвич» -структура циклопентадиен
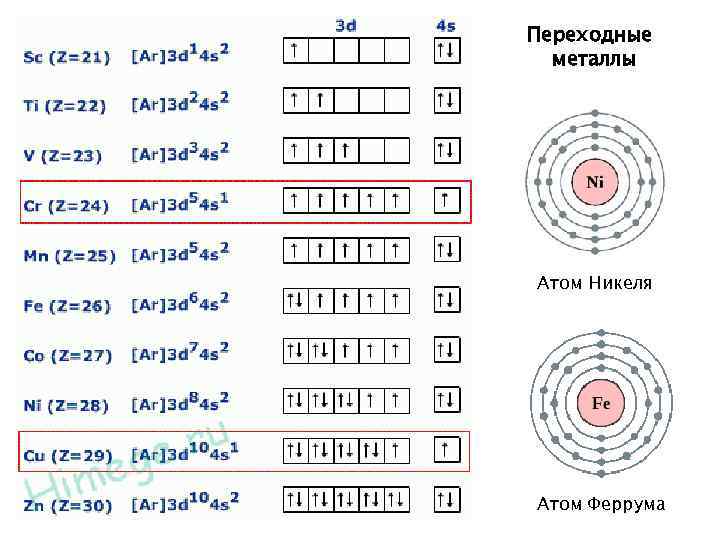
Переходные металлы Атом Никеля Атом Феррума

Немножко истории… В 1951 году Т. Кили и П. Посон, провели реакцию C 5 H 5 Mg. Br c хлоридом железа Fe. Cl 2 и получили совершенно новое, исключительно устойчивое жёлтооранжевое кристаллическое соединение, содержащее железо. Структура первого металлоцена - ферроцена - была установлена в 1952 году Р. Вудвордом и Дж. Уилкинсоном на основании его реакционной способности, и независимо от них — Э. Фишером на основании рентгеноструктурных данных. Обнаружено, что атом железа расположен посередине между двумя симметричными пятичленными кольцами C 5 H 5. Из-за сходства реакционной способности с бензолом, новое соединение было названо «ферроцен» (звуковая аналогия очевидна в английском языке: benzene — ferrocene). Вскоре предложен термин «металлоцены» .
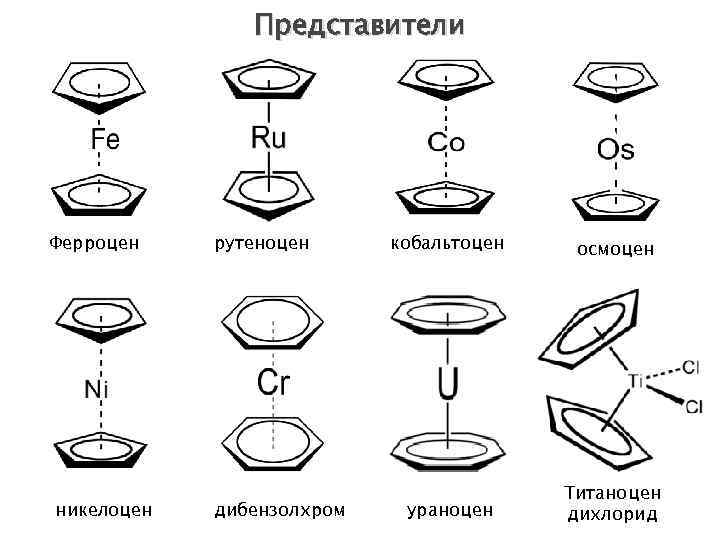
Представители Ферроцен никелоцен рутеноцен дибензолхром кобальтоцен осмоцен ураноцен Титаноцен дихлорид

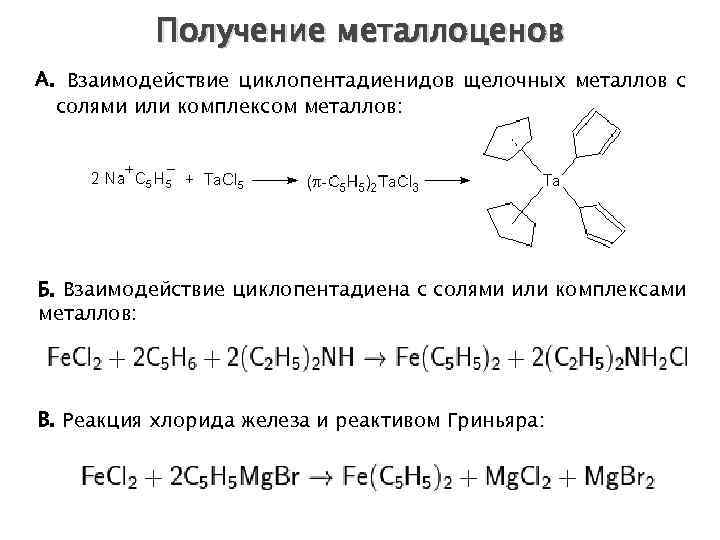
Получение металлоценов А. Взаимодействие циклопентадиенидов щелочных металлов с солями или комплексом металлов: Б. Взаимодействие циклопентадиена с солями или комплексами металлов: В. Реакция хлорида железа и реактивом Гриньяра:
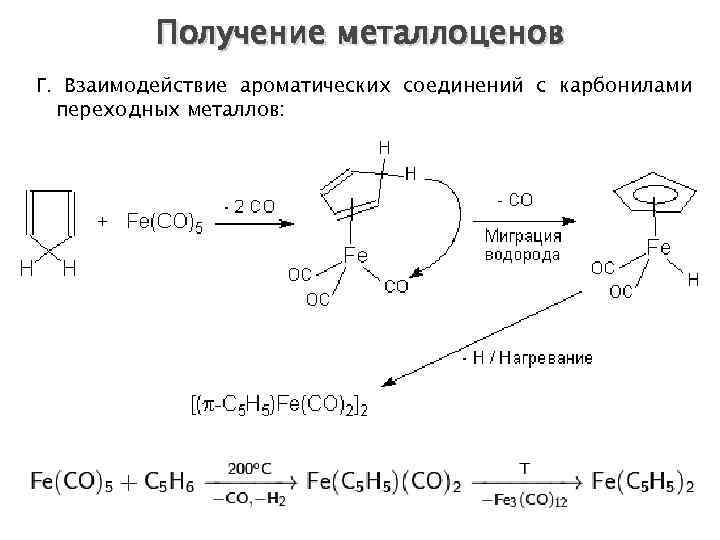
Получение металлоценов Г. Взаимодействие ароматических соединений с карбонилами переходных металлов:
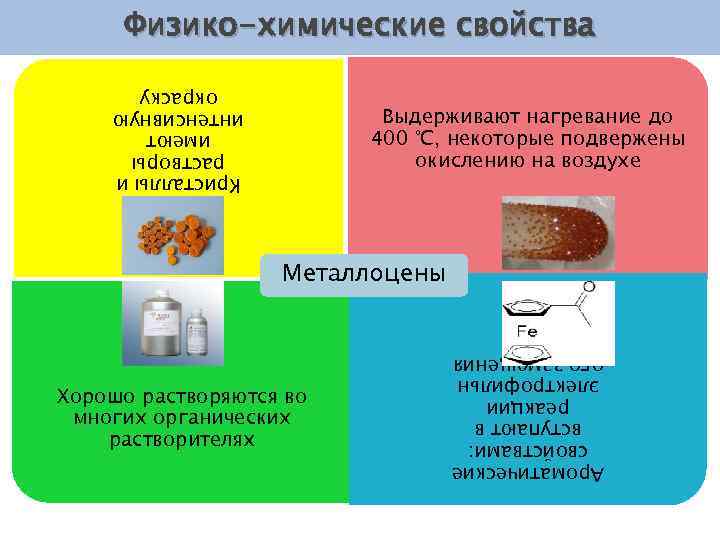
Физико-химические свойства Кристаллы и растворы имеют интенсивную окраску Выдерживают нагревание до 400 °C, некоторые подвержены окислению на воздухе Металлоцены Ароматические свойствами: вступают в реакции электрофильн ого замещения Хорошо растворяются во многих органических растворителях
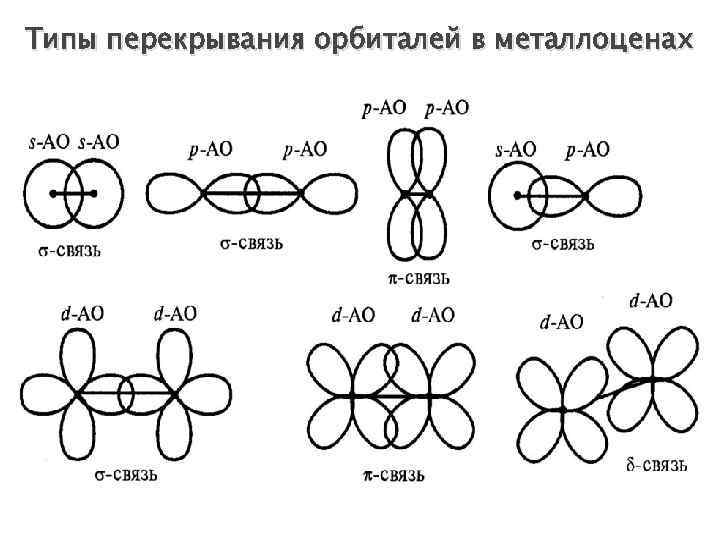
Типы перекрывания орбиталей в металлоценах
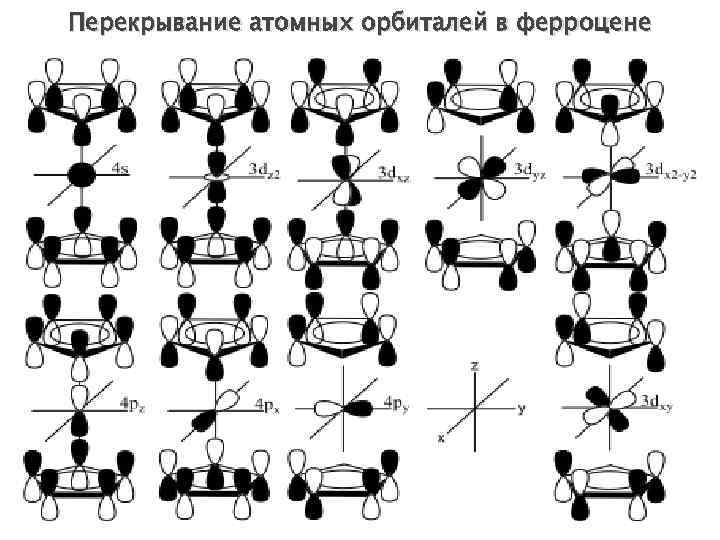
Перекрывание атомных орбиталей в ферроцене

Компьютерные модели перекрывания АО Fe и циклопентадиенильных радикалов в ферроцене
Bis(2 -pyrrolyl)methylferrocene
![catena-[Na ]2[1, 1 -Fc(4 -C 6 H 4 CO 2−)2]· 0. 6 H 2 catena-[Na ]2[1, 1 -Fc(4 -C 6 H 4 CO 2−)2]· 0. 6 H 2](https://present5.com/presentation/291476323_427617801/image-15.jpg)
catena-[Na ]2[1, 1 -Fc(4 -C 6 H 4 CO 2−)2]· 0. 6 H 2 O[1, 1 -Fc-=(η 5 -(C 5 H 4)2 Fe]
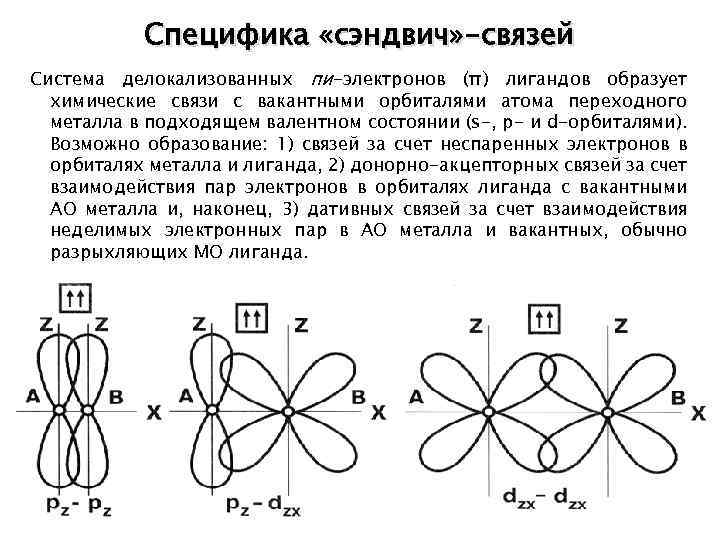
Специфика «сэндвич» -связей Система делокализованных пи-электронов (π) лигандов образует химические связи с вакантными орбиталями атома переходного металла в подходящем валентном состоянии (s-, р- и d-орбиталями). Возможно образование: 1) связей за счет неспаренных электронов в орбиталях металла и лиганда, 2) донорно-акцепторных связей за счет взаимодействия пар электронов в орбиталях лиганда с вакантными АО металла и, наконец, 3) дативных связей за счет взаимодействия неделимых электронных пар в АО металла и вакантных, обычно разрыхляющих МО лиганда.
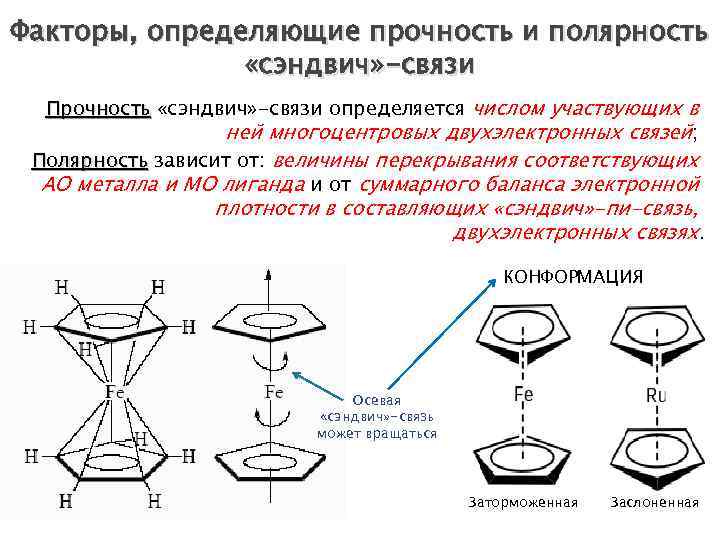
Факторы, определяющие прочность и полярность «сэндвич» -связи Прочность «сэндвич» -связи определяется числом участвующих в ней многоцентровых двухэлектронных связей; Полярность зависит от: величины перекрывания соответствующих АО металла и МО лиганда и от суммарного баланса электронной плотности в составляющих «сэндвич» -пи-связь, двухэлектронных связях. КОНФОРМАЦИЯ Осевая «сэндвич» -связь может вращаться Заторможенная Заслоненная

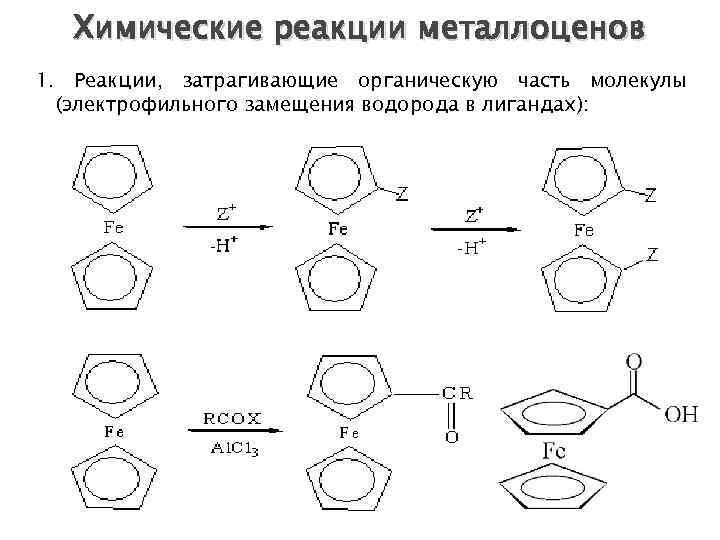
Химические реакции металлоценов 1. Реакции, затрагивающие органическую часть молекулы (электрофильного замещения водорода в лигандах):
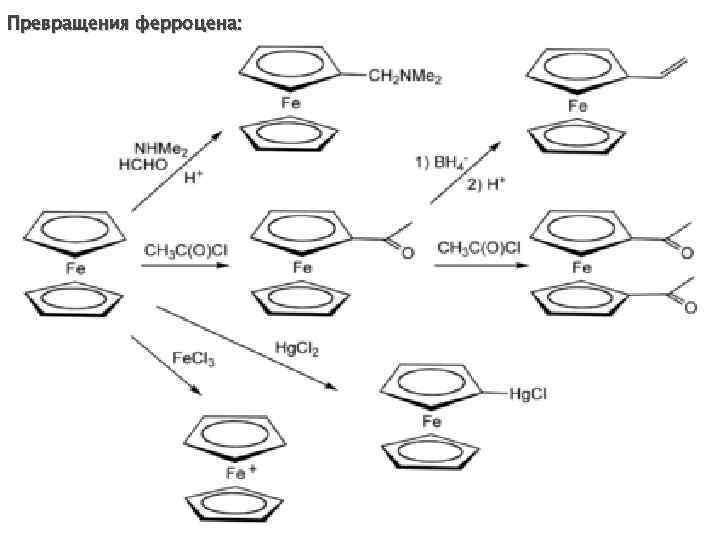
Превращения ферроцена:
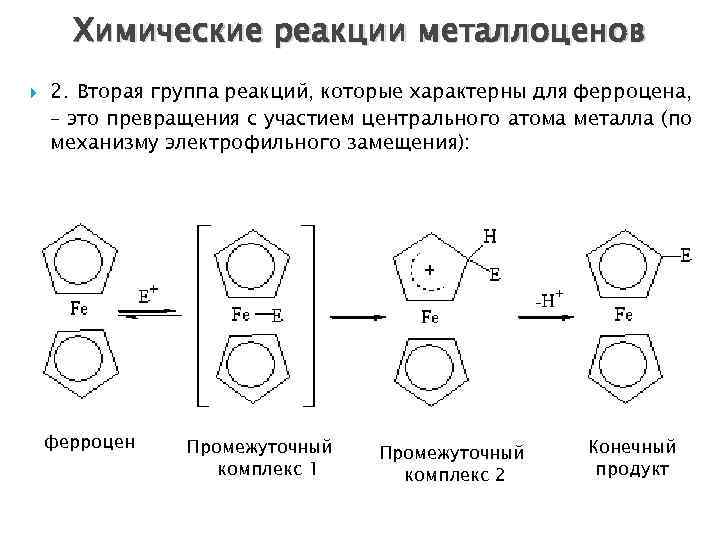
Химические реакции металлоценов 2. Вторая группа реакций, которые характерны для ферроцена, – это превращения с участием центрального атома металла (по механизму электрофильного замещения): ферроцен Промежуточный комплекс 1 Промежуточный комплекс 2 Конечный продукт
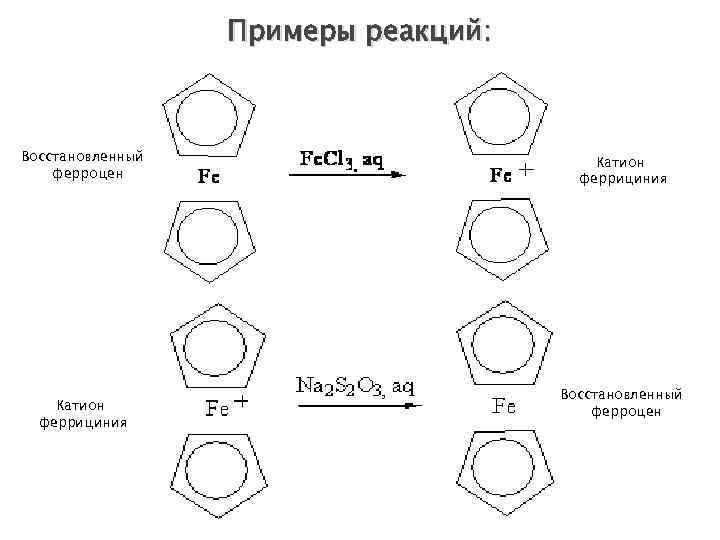
Примеры реакций: Восстановленный ферроцен Катион феррициния Восстановленный ферроцен
Применение металлоценов Лекарственные средства Промежуточные реагенты в органическом синтезе Катализаторы и сокатализаторы в различных гомогенных реакциях Присадки к топливам и маслам Фармакологические препараты
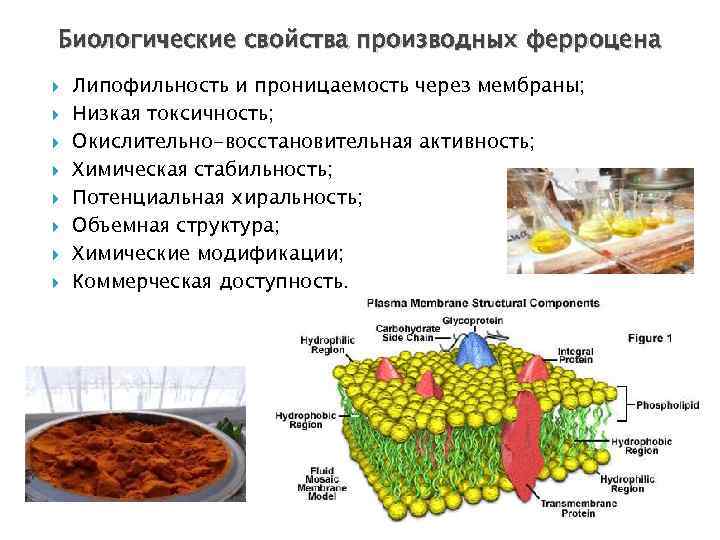
Биологические свойства производных ферроцена Липофильность и проницаемость через мембраны; Низкая токсичность; Окислительно-восстановительная активность; Химическая стабильность; Потенциальная хиральность; Объемная структура; Химические модификации; Коммерческая доступность.

Ferroceron (Ferroceronum) Ферроцерон железо-дефицитная анемия; озена; пародонтоз; аденома простаты; хронический простатит.
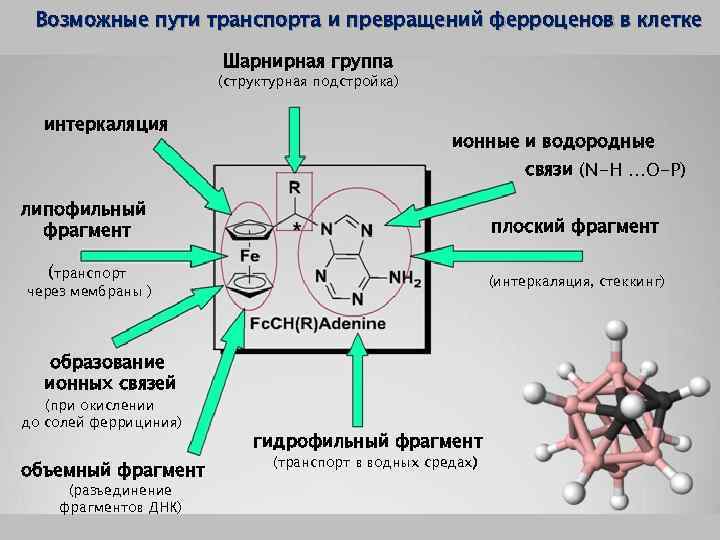
Возможные пути транспорта и превращений ферроценов в клетке Шарнирная группа (структурная подстройка) интеркаляция ионные и водородные связи (N-H …O-P) липофильный фрагмент плоский фрагмент (транспорт (интеркаляция, стеккинг) через мембраны ) образование ионных связей (при окислении до солей феррициния) объемный фрагмент (разъединение фрагментов ДНК) гидрофильный фрагмент (транспорт в водных средах)
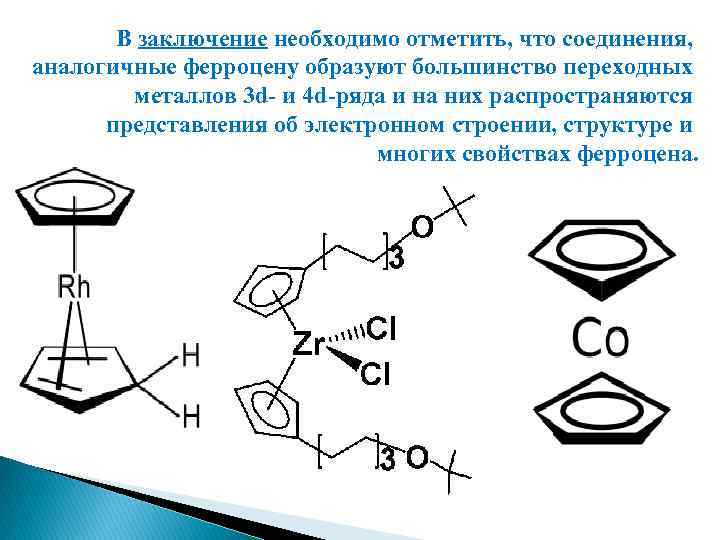
В заключение необходимо отметить, что соединения, аналогичные ферроцену образуют большинство переходных металлов 3 d- и 4 d-ряда и на них распространяются представления об электронном строении, структуре и многих свойствах ферроцена.


Жданкин А.Е._БХ-14м-6.pptx