Этапы разработки технологической схемы производства

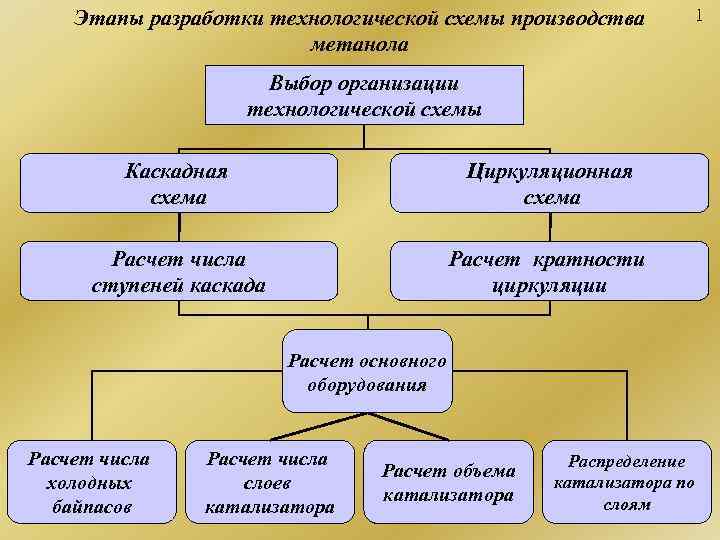
Этапы разработки технологической схемы производства 1 метанола Выбор организации технологической схемы Каскадная Циркуляционная схема схема Расчет числа Расчет кратности ступеней каскада циркуляции Расчет основного оборудования Расчет числа Распределение Расчет объема холодных слоев катализатора по катализатора слоям байпасов катализатора

2 Термодинамические закономерности процесса Основные реакции синтеза метанола: (1) (2) (3) Закон «действующих масс» для реакций (1) и (2): (4) (5) Функционал:
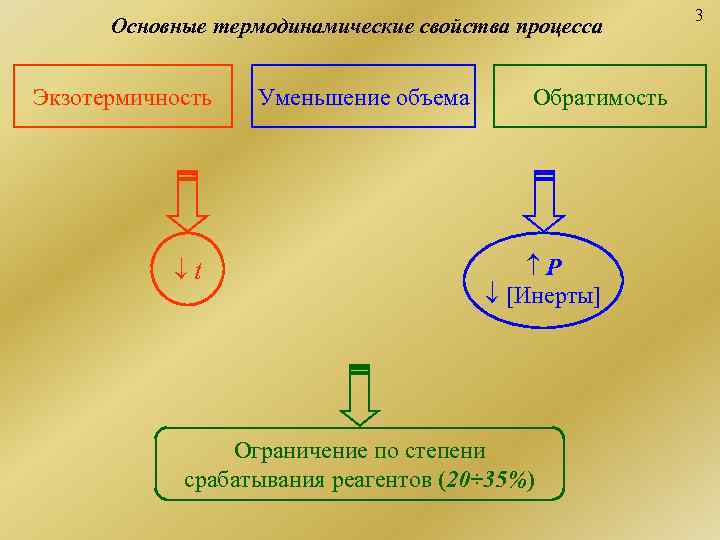
3 Основные термодинамические свойства процесса Экзотермичность Уменьшение объема Обратимость t P [Инерты] Ограничение по степени срабатывания реагентов (20÷ 35%)
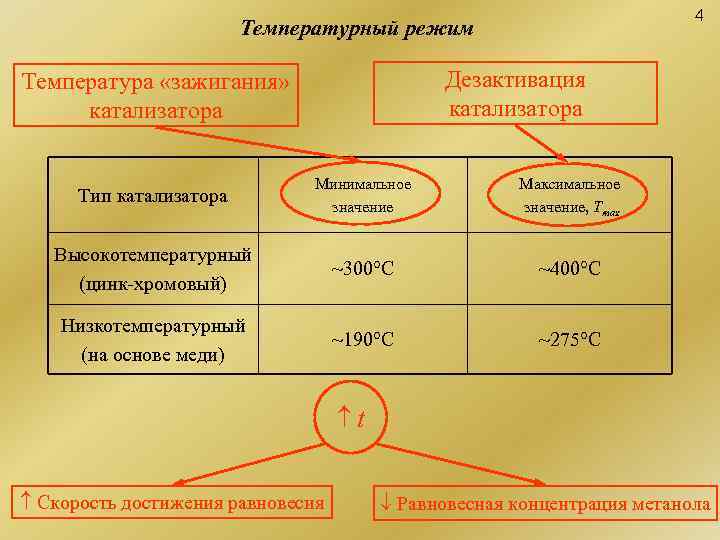
4 Температурный режим Температура «зажигания» Дезактивация катализатора Минимальное Максимальное Тип катализатора значение, Tmax Высокотемпературный ~300°C ~400°C (цинк-хромовый) Низкотемпературный ~190°С ~275°С (на основе меди) t Скорость достижения равновесия Равновесная концентрация метанола

5 Давление процесса Тип катализатора Давление, МПа Высокотемпературный 20, 0÷ 40, 0 (цинк-хромовый) Низкотемпературный 4, 9÷ 19, 6 (на основе меди) P + - Выход метанола Энергоемкость Степень превращения СО и СО 2 Выход высших спиртов и эфиров Выход парафинов Габариты оборудования
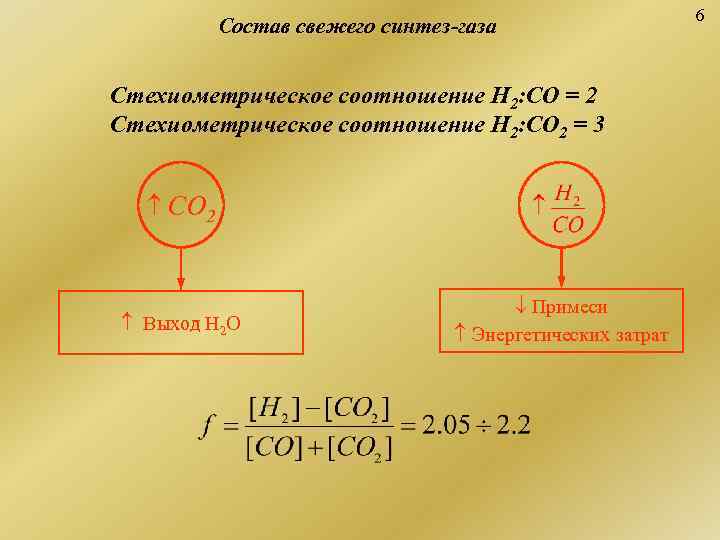
6 Состав свежего синтез-газа Стехиометрическое соотношение Н 2: СО = 2 Стехиометрическое соотношение Н 2: СО 2 = 3 СО 2 Примеси Выход Н 2 О Энергетических затрат
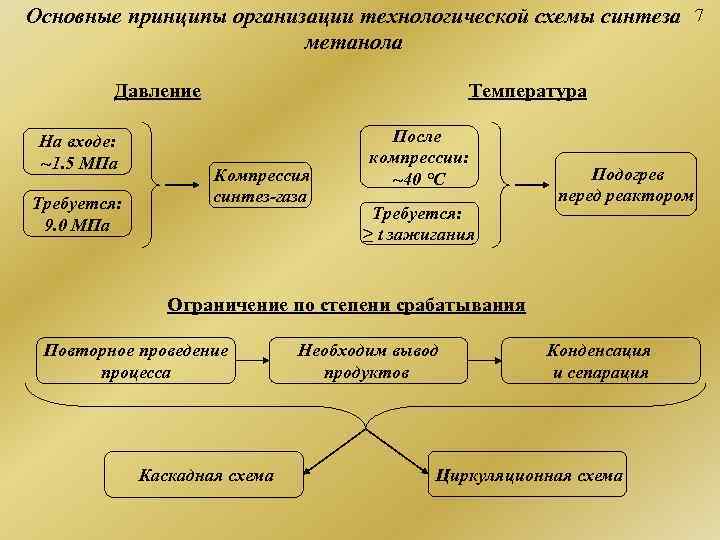
Основные принципы организации технологической схемы синтеза 7 метанола Давление Температура На входе: После ~1. 5 МПа компрессии: Компрессия ~40 °C Подогрев Требуется: синтез-газа перед реактором Требуется: 9. 0 МПа ≥ t зажигания Ограничение по степени срабатывания Повторное проведение Необходим вывод Конденсация процесса продуктов и сепарация Каскадная схема Циркуляционная схема
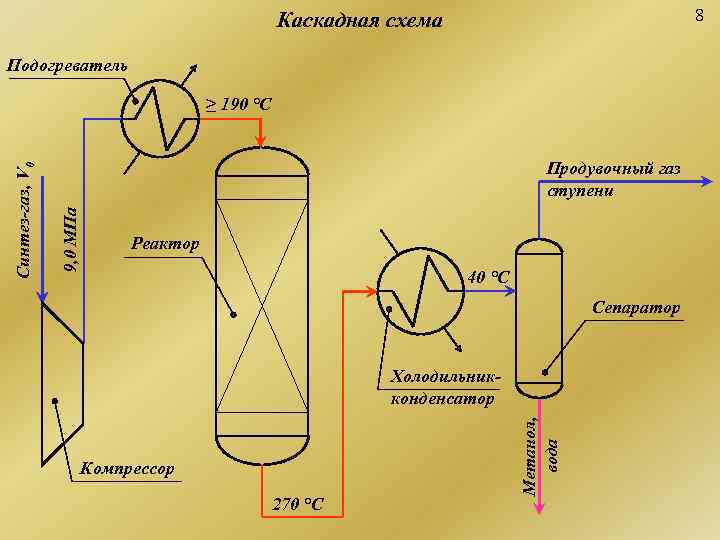
Каскадная схема 8 Подогреватель ≥ 190 °С Продувочный газ Синтез-газ, V 0 ступени 9, 0 МПа Реактор 40 °С Сепаратор Холодильник- конденсатор Метанол, вода Компрессор 270 °С
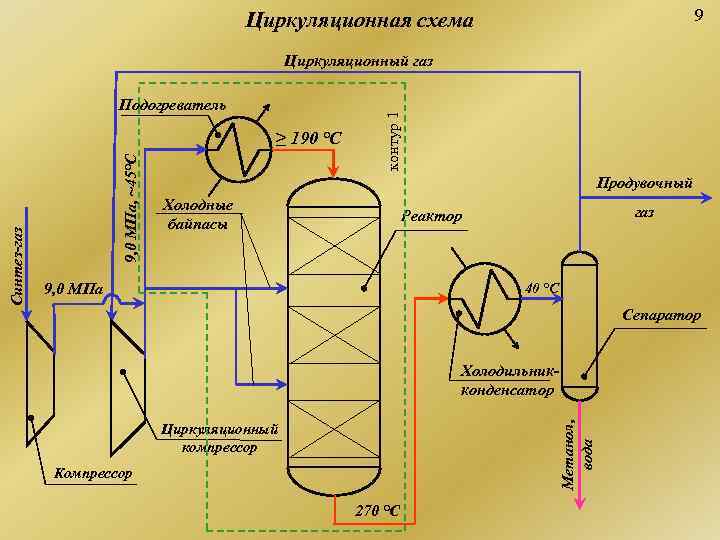
Циркуляционная схема 9 Циркуляционный газ Подогреватель контур 1 9, 0 МПа, ~45°С ≥ 190 °С Продувочный Холодные газ байпасы Реактор Синтез-газ 9, 0 МПа 40 °С Сепаратор Холодильник- конденсатор Метанол, Циркуляционный компрессор вода Компрессор 270 °С
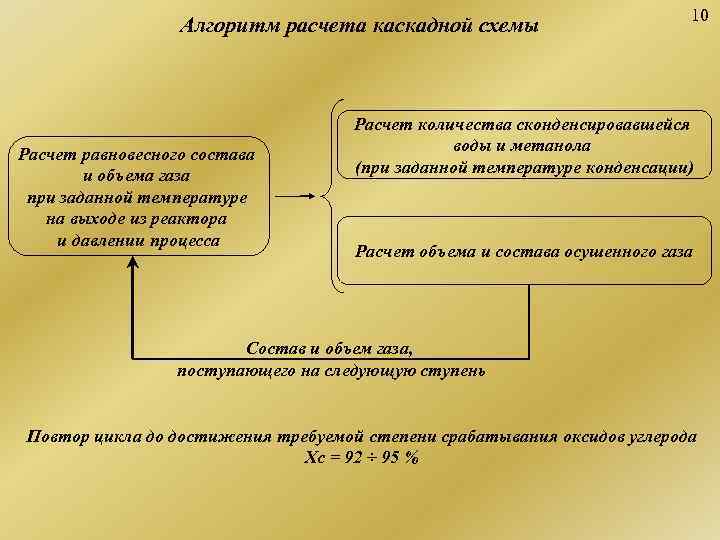
10 Алгоритм расчета каскадной схемы Расчет количества сконденсировавшейся Расчет равновесного состава воды и метанола и объема газа (при заданной температуре конденсации) при заданной температуре на выходе из реактора и давлении процесса Расчет объема и состава осушенного газа Состав и объем газа, поступающего на следующую ступень Повтор цикла до достижения требуемой степени срабатывания оксидов углерода Xc = 92 ÷ 95 %
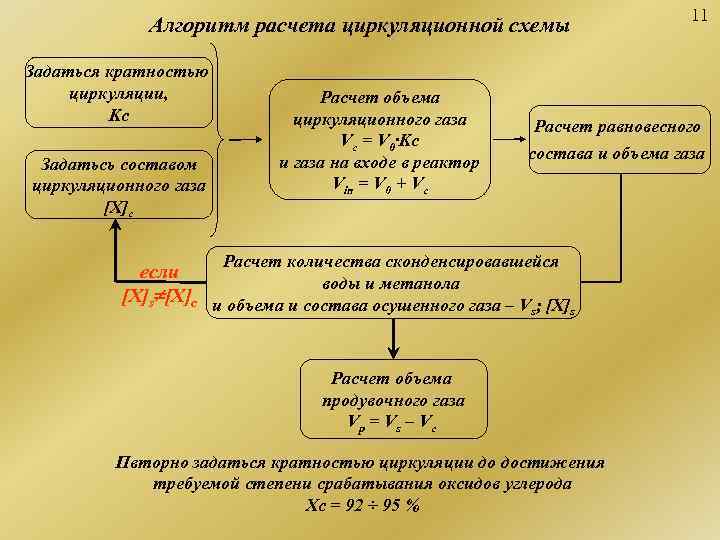
11 Алгоритм расчета циркуляционной схемы Задаться кратностью циркуляции, Расчет объема Kc циркуляционного газа Расчет равновесного Vс = V 0·Kc и газа на входе в реактор состава и объема газа Задатьсь составом циркуляционного газа Vin = V 0 + Vc [X]с Расчет количества сконденсировавшейся если воды и метанола [X]s [X]с и объема и состава осушенного газа – V ; [X] s s Расчет объема продувочного газа Vp = V s – Vс Пвторно задаться кратностью циркуляции до достижения требуемой степени срабатывания оксидов углерода Xc = 92 ÷ 95 %

Сравнение каскадной и циркуляционной схемы 12 f = 2. 154 ; p = 9. 0 МПа; t = 270 °C

Изменение капитальных затрат в зависимости от числа 13 ступеней каскада

Изменение эксплуатационных затрат в зависимости от 14 кратности циркуляции

15 Оптимизация капитальных и эксплуатационных затрат Оптимум

16 Расчет равновесного состава реакционного газа Закон «действующих масс» для реакций (1) и (2): (4) (5) где Pi – парциальное давление i-го компонента в равновесной газовой смеси Или: Требуется рассчитать (4. 1) (5. 1) где [Xi] – объемная доля i-го компонента в равновесной газовой смеси; P – давление равновесной смеси (давление синтеза).

17 Расчет равновесного состава реакционного газа Расчет значений констант равновесия при заданной температуре (уравнения Граафа): условие применимости р=5, 0÷ 9, 0 МПа; t=200÷ 300 o. C (6. 1) (6. 2) где Т – температура равновесной смеси, К; R – универсальная газовая постоянная, 8, 314 к. Дж/(кмоль*К).

18 Расчет равновесного состава реакционного газа Решение системы уравнений (4. 1) и (5. 1) путем выражения равновесных концентраций через степени образования «ключевых компонентов» Степень образования метанола – Ym Степень образования воды – Yw Количество образоваашегося метанола и воды, нм 3: VCH 3 OH = Ym·V 0 ; VH 2 O = Yw·V 0 ВНИМАНИЕ! Все объемы газов должны быть приведены к нормальным условиям: 0°С, 1 атм. Обозначается – нм 3

19 Расчет равновесного состава реакционного газа Обозначения: [Xi]0 – объемная доля i-го компонента в исходной газовой смеси; V 0 – объем исходной газовой смеси, нм 3; [Xi] – объемная доля i-го компонента в равновесной газовой смеси; VR – объем полученной равновесной газовой смеси, нм 3 Таким образом: (7) Объем i-го компонента в исходной газовой смеси, нм 3: (8) Объем i-го компонента в равновесной газовой смеси, нм 3: (9)

20 Расчет равновесного состава реакционного газа Принимаем: объем исходной газовой смеси V 0 = 1 нм 3 Тогда для исходной газовой смеси, состоящей из: CH 3 OH, H 2 O, CO 2, H 2, Инерты объем каждого компонента равен (нм 3):

21 Расчет равновесного состава реакционного газа Из стехиометрии реакций (1) и (2) объем каждого компонента в равновесной газовой смеси будет равен (нм 3):

Расчет равновесного состава реакционного газа 22 Объем равновесной газовой смеси, нм 3: =1 (10) Объемная доля компонетов в равновесной газовой смеси: уравнения закона «действующих масс» (4. 1) и (5. 1)

Расчет равновесного состава реакционного газа 23 Вид уравнений (4. 1) и (5. 1) с выражением равновесных концентраций через концентрации компонентов в исходной смеси и степени образования метанола и воды (4. 2) (6. 1) (6. 2) (5. 2) Ym, Yw Состав и объем равновесной смеси Степень превращения реагентов

24 Пример расчета первой ступени каскадной схемы Исходные данные 1. Температура синтеза: 270 о. С; 2. Давление синтеза: 9. 0 МПа; 3. Расход синтез-газа: 10000 нм 3/час; 4. Состав (%, об. ): CO – 10. 0; CO 2 – 16. 0; H 2 – 72. 0; CH 4 – 0. 6; N 2 – 1. 1; Ar – 0. 3 5. f = 2. 154 Результаты расчета 1. Кр1 = 0. 0006926; Кр2 = 0. 0163; Ym = 8. 792 %; Yw = 2. 786 %; 2. Равновесный газ: VR = 8241, 6 нм 3/час; 3. Состав равновесного газа (%, об. ): CO – 4, 846; CO 2 – 16, 034; H 2 – 62, 645; CH 3 OH – 10. 668; H 2 O – 3. 380; CH 4 – 0. 728; N 2 – 1. 335; Ar – 0. 364 Степень превращения суммы оксидов углерода в метанол: (11)

Расчет числа слоев катализатора и холодных байпасов 25 Qin; Gin; hin TAD [Xi]0 Условие адиабатичности: (12) Расчет адиабатической температуры: 1. Энтальпия газа, выходящего из реактора (равновесного газа) (13) 2. Тепловой поток газа, выходящего из реактора (14) 3. Энтальпии поступающего в реактор газа (15) Qout; Gout hout; Tout 4. Адиабатическая температура (16) Обозначения: Если: Q – тепловой поток, [ккал/час]; расчет окончен G – расход газа, [кг/час]; Если: h – энтальпия газа, [ккал/кг]; расчет числа слоев и байпасов TAD – адиабатическая температура
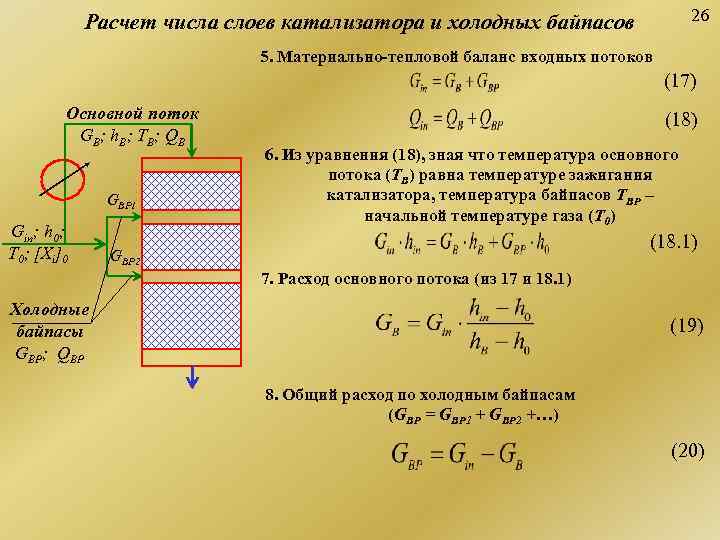
Расчет числа слоев катализатора и холодных байпасов 26 5. Материально-тепловой баланс входных потоков (17) Основной поток (18) GB; h. B; ТВ; QB 6. Из уравнения (18), зная что температура основного потока (TB) равна температуре зажигания GBP 1 катализатора, температура байпасов TBP – начальной температуре газа (T 0) Gin; h 0; (18. 1) T 0; [Xi]0 GBP 2 7. Расход основного потока (из 17 и 18. 1) Холодные байпасы (19) GBP; QBP 8. Общий расход по холодным байпасам (GBP = GBP 1 + GBP 2 +…) (20)

Расчет числа слоев катализатора и холодных байпасов 27 9. Расчет первого слоя: 9. 1 Зная TB , GB , [Xi]0 рассчитать QB (21) 9. 2 Задаться температурой Tout и провести расчет расхода Gout и равновесного состава газа на выходе из слоя [Xi]out 9. 3 Определить значение теплового потока, выходящего из слоя (22) 9. 4 Проверить выполнение условия адиабатичности (23) не выполняется Tout = Tmax; поправка на 9. 5 Проверить условие недостижение равновесия 10. Расчет расхода холодного байпаса после первого слоя GBP 1: подобрать расход таким образом, чтобы температура смеси (Gout + GBP 1) равнялась TB 11. Повтор расчета п. п. 9. 1 – 10 до GB = 0
Губкинский лекции метанол.ppt
- Количество слайдов: 27

