746d0c2114fb098e35c5cdd1a0dd8745.ppt
- Количество слайдов: 31

Если ты будешь любознательным, то будешь много знающим Сократ

Великий русский ученый Михаил Васильевич Ломоносов более двухсот лет назад определял некоторое вещество как «твердое, непрозрачное, светлое тело; которое на огне плавить и холодное ковать можно» . К какому веществу относятся эти свойства?

«Металлы»

Станция «Угадай -ка»

«Угадай-ка» 1. Пахать и строить, Все он может Если ему уголек В том поможет. 2. По прозванью инвалид Но крепок в деле И на вид инвалид 3. Богатырем его не зря назвали Друг железа Помощник стали 4. Металл красой своей пленил И первым в топку угодил

«Угадай-ка» 5. Металл зимой не прочен: Чума здоровье точит 7. Металл в соляхопора многих, А нас без них, Не носят ноги 6. «Живое серебро» И льется, И блестит, охотно С золотом дружит 8. От какого металла Нужно отрезать одну треть, Чтобы получить известную кость Животного или человека?

Станция «Мой дом»

1. Вещество, раствор или расплав которого проводит электрический ток. 2. Металл, который в середине века алхимики изображали в виде война. 3. Физическое свойство металлов, являющееся результатом отражения световых лучей от их поверхности. 4. Щелочной металл. 5. Физическое свойство металлов, связанное с их агрегатным состоянием. 6. Самый твёрдый металл. 7. Свойство металлов, которое лежит в основе их деления на лёгкие и тяжёлые. 8. Драгоценный металл VIIIВ группы. 9. Жидкий металл.

10. Самый тяжёлый металл. 11. Группа металлов, в которую не входят железо и его сплавы. 12. Металл, ставший причиной гибели целых племён (например, племени инков) 13. Положительно заряженный электрод. 14. Элемент, противоположный металлу по физическим и химическим свойствам. 15. Процесс самопроизвольного разрушения металлов и сплавов под действием внешних факторов. 16. Свойство веществ изменять форму под воздействием внешних факторов и сохранять принятую форму после прекращения этого воздействия. 17. Самый лёгкий металл. 18. Самый тугоплавкий металл.
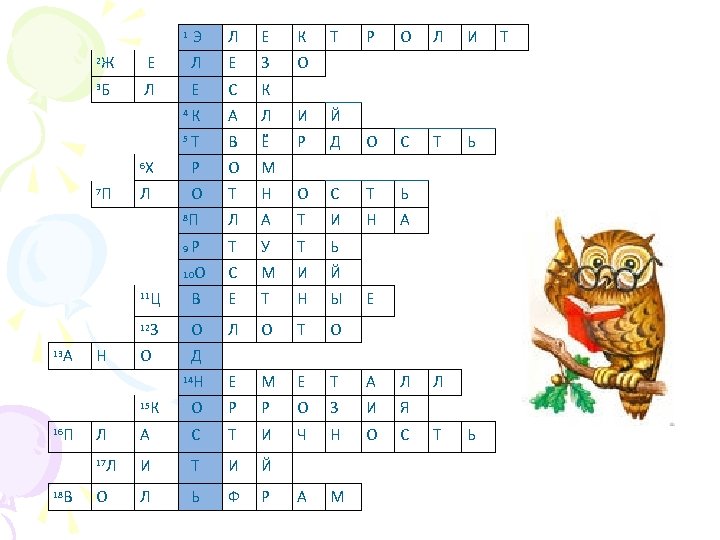
1 Э Л Е К О Ж Е Л Е З Б Л Е С Т Р О Л И К 2 3 Т 4 К А Л И Й 5 Т В Ё Р Д 6 Х Р О М Л О Т Н О С Т Ь П Л А Т И Н А Р Т У Т Ь О С М И Й Ц В Е Т Н Ы 12 З О Л О Т О О Д 14 Н Е М Е Т А Л 15 О Р Р О З И Я А С Т И Ч Н О С 17 И Т И Й О Л Ь Ф Р А М П 7 8 9 10 11 А 13 Н К П 16 Л Л В 18 О С Т Ь Е Л Т Ь

Станция «Мои друзья»

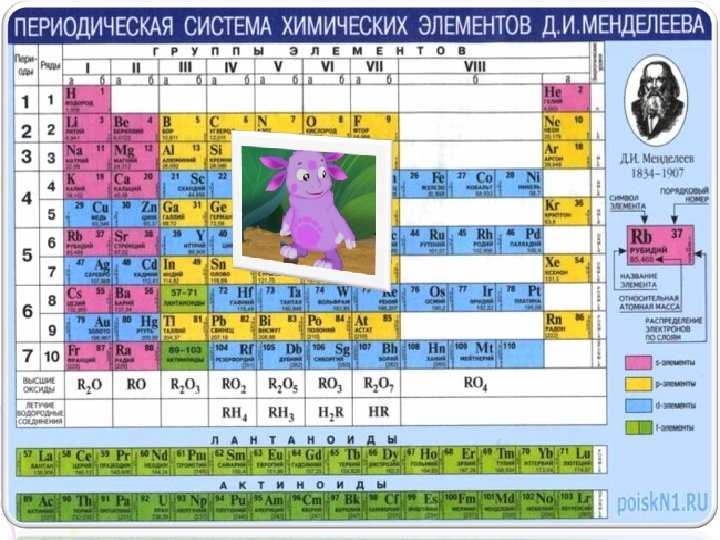

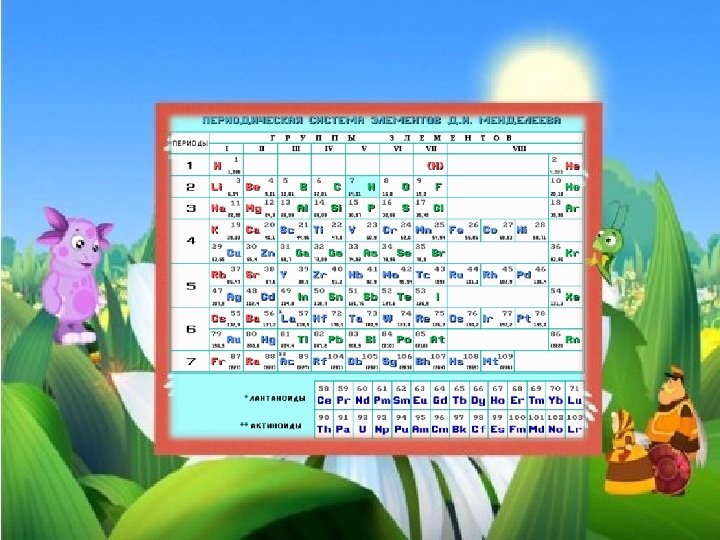

Na Np Cu Ra Sc Mn Ni Ti Ce Pa Ra Al Rb Cu Ga Cl Fe Al Sb Na Al Fe Hf Pa Na Al Li Fr Au Sr Br Ac Mg Si Cl In Cl

Щелочные металлы: • Li • Na • K • Rb • Cs • Fr

Химические свойства щелочных металлов

Щелочноземель ные металлы Be Mg Ca Sr Ba Ra

Физические свойства щелочноземельных металлов • Все щелочноземельные металлы — серые, твёрдые при комнатной температуре вещества. В отличие от щелочных металлов, они существенно более твёрдые, и ножом преимущественно не режутся (исключение — стронций). Плотность щелочноземельных металлов с порядковым номером растёт, хотя явно рост наблюдается только начиная с кальция, который самый лёгкий из них (ρ = 1, 55 г/см³), самый тяжёлый — радий, плотность которого примерно равна плотности железа.

• Алюми ний — элемент главной подгруппы третьей группы третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 13. Обозначается символом Al (лат. Aluminium). Относится к группе лёгких металлов. Наиболее распространённый металл и третий по распространённости (после кислорода и кремния) химический элемент в земной коре. • Легко реагирует с простыми веществами: • с кислородом: • 4 Al + 3 O 2 = 2 Al 2 O 3 • с галогенами: • 2 Al + 3 Br 2 = 2 Al. Br 3 • с другими неметаллами реагирует при нагревании: • с серой, образуя сульфид алюминия: • 2 Al + 3 S = Al 2 S 3 • с азотом, образуя нитрид алюминия: • 2 Al + N 2 = 2 Al. N • с углеродом, образуя карбид алюминия: • 4 Al + 3 С = Al 4 С 3

• Желе зо — элемент побочной подгруппы восьмой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 26. Обозначается символом Fe (лат. Ferrum). Один из самых распространённых в земной коре металлов (второе место после алюминия).

Физические свойства: 1. Пластичность 2. Электропроводность 3. Сверпроходимость 4. Теплопроводность 5. Металлический блеск


станция «Умельцы» Выполняя задания воспользуйтесь любой схемой А) металл оксид металла Б) металл соль В) металл пероксид металла Г) металл соль основание оксид соль металла оксид основание металла железная окалина основание соль оксид соль

станция «Логики» Решите задачу пользуясь алгоритмом

станция «Эрудит» выполни тест

Часть 1 Вариант – 1 А 1 Какая пара оксидов обладает основными и амфотерными свойствами соответственно: а) Са. О и Ва. О; в) Mg. O и Са. О б) Ва. О и Sr. O; г) Ва. О и Ве. О. А 2 При взаимодействии натрия с водой образуется а) пероксид натрия; б) хлорид натрия; в) гидроксид натрия и водород; г) гидроксид натрия. А 3 Какая формула соответствует гидроксиду и оксиду лития: а) Li. OH и Li 2 0; б) Li(OH)2 и Li 2 0; в) Li(OH)2 и Li. O; г) Li(ОН) 2 и Li 0. А 4 Электронная конфигурация атома ls 22 p 63 s 23 p 64 s 2. Это элемент: а) бериллий; б) кальций; в) магний; г) цинк. А 5 Какой объем водорода (н. у. ) может быть получен при растворении в воде 1, 4 г кальция? а) 6 б) 1 в) 4 г) 2 А 6 Укажите неизвестное соединение в цепочке превращений Al —> X —> Al(OH)3 а) Al 2 O 3 б) Al в) Al(OH)3 г) Al. Cl 3 Часть 2 С 1 Какая масса соли образуется при взаимодействии раствора гидроксида натрия с 139 г раствора фосфорной кислоты с массовой долей 10%? Часть 1 Вариант – 2 А 1 Какая пара оксидов обладает основными и амфотерными свойствами: а) Са. О и S 02; в) Ва. О и А 1203; б) Mg. O и Са. О; г) Ва и Ве. О. А 2 При взаимодействии калия с водой образуются: а) пероксид калия; б) хлорид калия и вода; в) гидроксид калия и водород; г) гидроксид калия. А 3 Какая формула соответствует гидроксиду и оксиду алюминия: а)Al. OH и Al 203 б)Al(OH)2 и Al 20; в)Al(OH)3 и Al 2 O 3; г)Al 2 O 3 и Al(OH)3 А 4 Электронная конфигурация атома ls 22 p 63 s 23 p 64 s 1. Это элемент: а) калий; б) кальций; в)магний; г) цинк. А 5 Какой объем водорода может быть получен при растворении в воде 4, 6 г натрия? а)22, 1 б)0, 22 в)2, 24 г)22, 4 А 6. Укажите неизвестное соединение в цепочке превращений К —> X —> KN 03. а)KОН б)K 2 О в)KC 1 г)K 2 SO 4 Часть 2 С 1 Какую массу осадка можно получить привзаимодействии 30 г 15%-ного раствора гидроксида натрия с раствором соли Fe. Cl 3?

Ответы 1 вариант А 1 А 2 А 3 А 4 А 5 А 6 С 1 - г в а б б г 23, 3 2 вариант А 1 А 2 А 3 А 4 А 5 А 6 С 1 - в в в а в б 4

Домашнее задание 1) § 8 – 14 (повторить) 2) Р/Т стр. 69 - 71 1 -й уровень « 3» 2 -й уровень « 4» 3 -й уровень « 5» 3) Составить и решить тест по теме: «Металлы»

Спасибо за урок
746d0c2114fb098e35c5cdd1a0dd8745.ppt