MOG-2.pptx
- Количество слайдов: 39
 Escherichia coli – модель для дослідження основних генетичних процесів на молекулярному рівні
Escherichia coli – модель для дослідження основних генетичних процесів на молекулярному рівні
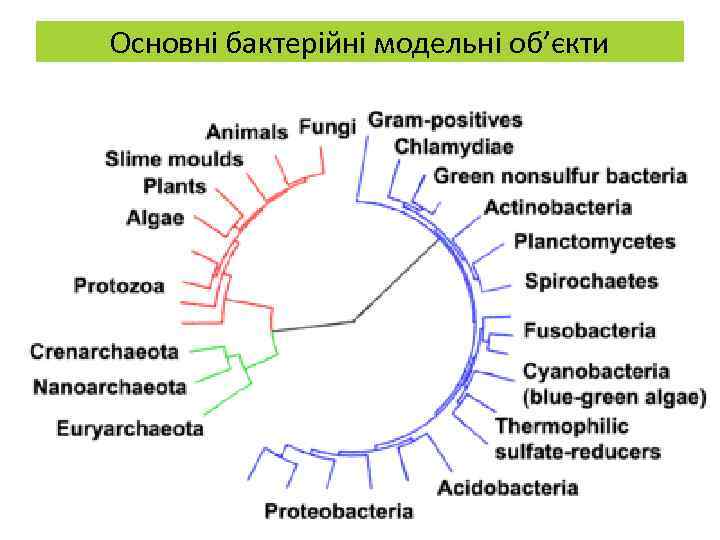 Основні бактерійні модельні об’єкти
Основні бактерійні модельні об’єкти
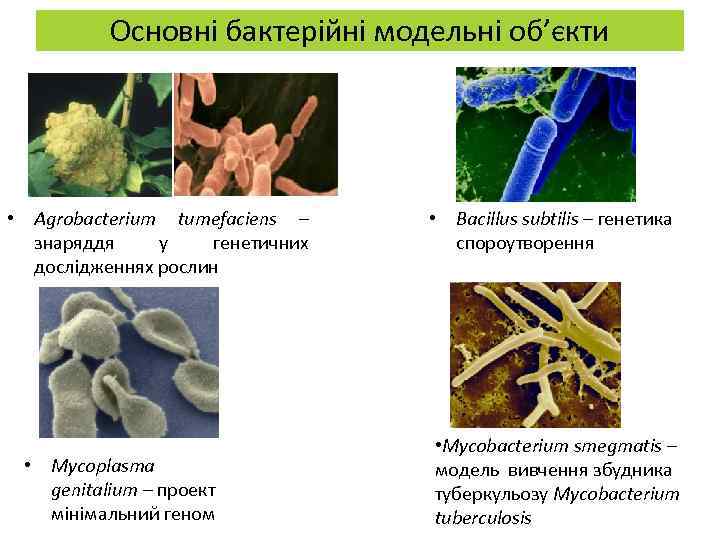 Основні бактерійні модельні об’єкти • Agrobacterium tumefaciens – знаряддя у генетичних дослідженнях рослин • Mycoplasma genitalium – проект мінімальний геном • Bacillus subtilis – генетика спороутворення • Mycobacterium smegmatis – модель вивчення збудника туберкульозу Mycobacterium tuberculosis
Основні бактерійні модельні об’єкти • Agrobacterium tumefaciens – знаряддя у генетичних дослідженнях рослин • Mycoplasma genitalium – проект мінімальний геном • Bacillus subtilis – генетика спороутворення • Mycobacterium smegmatis – модель вивчення збудника туберкульозу Mycobacterium tuberculosis
 Основні бактерійні модельні об’єкти • Myxococcus xanthus – генетика соціальної поведінки бактерій • Caulobacter crescentus – дослідження клітинної диференціації;
Основні бактерійні модельні об’єкти • Myxococcus xanthus – генетика соціальної поведінки бактерій • Caulobacter crescentus – дослідження клітинної диференціації;
 E. coli q. Escherichia coli (скорочено - E. сoli) кишкова паличка: q. Відкрита Теодором Ешеріхом (Theodor Escherich); сoli – “кишкова” (лат. ); q. Входить до складу мікрофлори кишківника теплокровних організмів; q. Більшість штамів не є патогенними; однак деякі серотипи патогенні і викликають серйозні харчові отруєння; q. Кілька наукових груп почали вивчати E. сoli q. Серотип – різноманітність мікроорганізмів серед одного виду за наявністю на поверхні клітини антигенів. q. Може тривалий час жити поза організмом господаря (тест на забруднення водойм) E. coli
E. coli q. Escherichia coli (скорочено - E. сoli) кишкова паличка: q. Відкрита Теодором Ешеріхом (Theodor Escherich); сoli – “кишкова” (лат. ); q. Входить до складу мікрофлори кишківника теплокровних організмів; q. Більшість штамів не є патогенними; однак деякі серотипи патогенні і викликають серйозні харчові отруєння; q. Кілька наукових груп почали вивчати E. сoli q. Серотип – різноманітність мікроорганізмів серед одного виду за наявністю на поверхні клітини антигенів. q. Може тривалий час жити поза організмом господаря (тест на забруднення водойм) E. coli
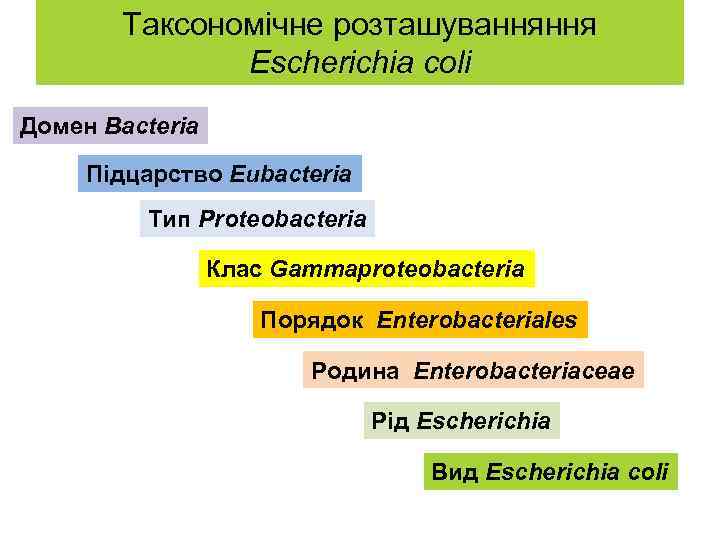 Таксономічне розташуванняння Escherichia coli Домен Bacteria Підцарство Eubacteria Тип Proteobacteria Клас Gammaproteobacteria Порядок Enterobacteriales Родина Enterobacteriaceae Рід Escherichia Вид Escherichia coli
Таксономічне розташуванняння Escherichia coli Домен Bacteria Підцарство Eubacteria Тип Proteobacteria Клас Gammaproteobacteria Порядок Enterobacteriales Родина Enterobacteriaceae Рід Escherichia Вид Escherichia coli
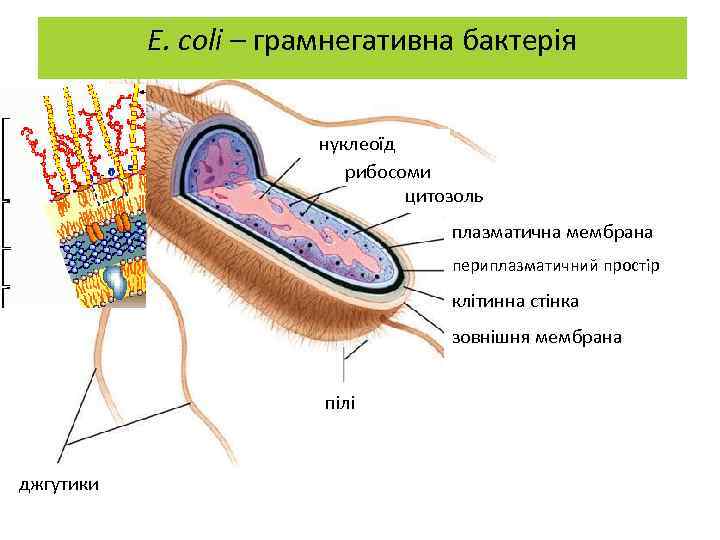 E. coli – грамнегативна бактерія нуклеоїд рибосоми цитозоль плазматична мембрана периплазматичний простір клітинна стінка зовнішня мембрана пілі джгутики
E. coli – грамнегативна бактерія нуклеоїд рибосоми цитозоль плазматична мембрана периплазматичний простір клітинна стінка зовнішня мембрана пілі джгутики
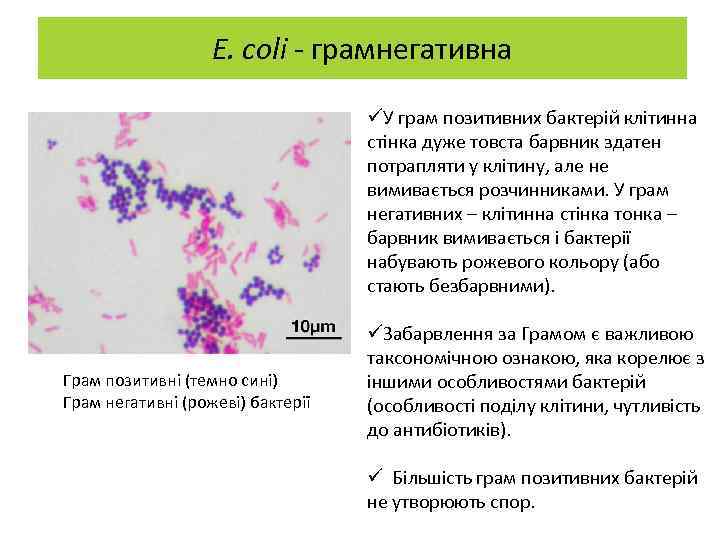 E. coli - грамнегативна üУ грам позитивних бактерій клітинна стінка дуже товста барвник здатен потрапляти у клітину, але не вимивається розчинниками. У грам негативних – клітинна стінка тонка – барвник вимивається і бактерії набувають рожевого кольору (або стають безбарвними). Грам позитивні (темно сині) Грам негативні (рожеві) бактерії üЗабарвлення за Грамом є важливою таксономічною ознакою, яка корелює з іншими особливостями бактерій (особливості поділу клітини, чутливість до антибіотиків). ü Більшість грам позитивних бактерій не утворюють спор.
E. coli - грамнегативна üУ грам позитивних бактерій клітинна стінка дуже товста барвник здатен потрапляти у клітину, але не вимивається розчинниками. У грам негативних – клітинна стінка тонка – барвник вимивається і бактерії набувають рожевого кольору (або стають безбарвними). Грам позитивні (темно сині) Грам негативні (рожеві) бактерії üЗабарвлення за Грамом є важливою таксономічною ознакою, яка корелює з іншими особливостями бактерій (особливості поділу клітини, чутливість до антибіотиків). ü Більшість грам позитивних бактерій не утворюють спор.
 Геном q. Геном – сукупність генетичної інформації, яку містить гаплоїдний набір хромосом живої клітини. Містить гени життєво необхідні для організму. q. Реплікація – процес синтезу другої копії ДНК (процес подвоєння ДНК), необхідний для передачі генетичної інформації від материнської клітини до дочірньої. q. Плазміда – позахромосомна молекула ДНК, що здатна до реплікації автономно, незалежно від хромосоми. Термін ввів Джошуа Ледерберг 1952 року.
Геном q. Геном – сукупність генетичної інформації, яку містить гаплоїдний набір хромосом живої клітини. Містить гени життєво необхідні для організму. q. Реплікація – процес синтезу другої копії ДНК (процес подвоєння ДНК), необхідний для передачі генетичної інформації від материнської клітини до дочірньої. q. Плазміда – позахромосомна молекула ДНК, що здатна до реплікації автономно, незалежно від хромосоми. Термін ввів Джошуа Ледерберг 1952 року.
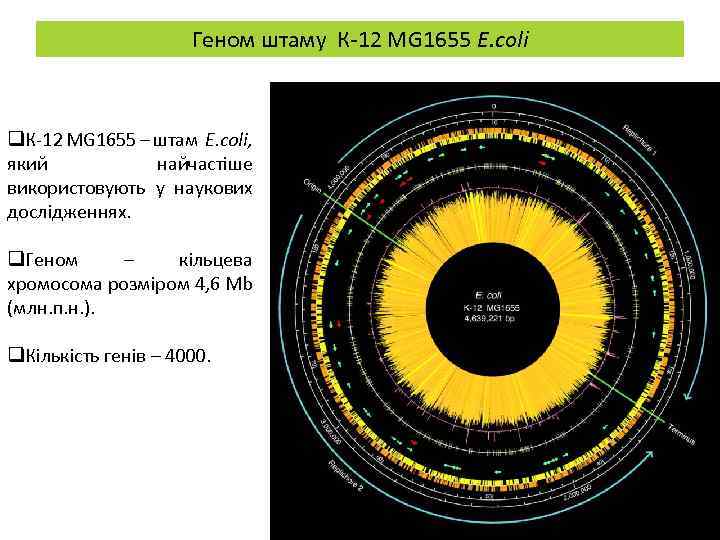 Геном штаму К-12 MG 1655 E. coli q. К-12 MG 1655 – штам E. coli, який найчастіше використовують у наукових дослідженнях. q. Геном – кільцева хромосома розміром 4, 6 Mb (млн. п. н. ). q. Кількість генів – 4000.
Геном штаму К-12 MG 1655 E. coli q. К-12 MG 1655 – штам E. coli, який найчастіше використовують у наукових дослідженнях. q. Геном – кільцева хромосома розміром 4, 6 Mb (млн. п. н. ). q. Кількість генів – 4000.
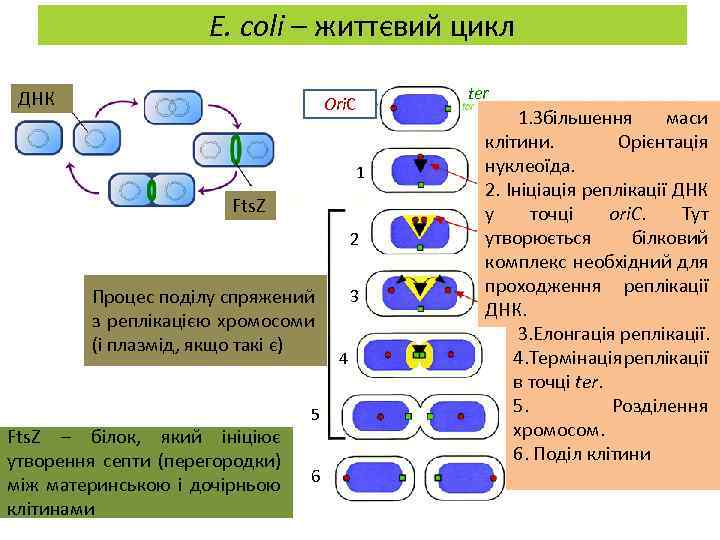 E. coli – життєвий цикл ДНК ter Ori. С 1 Fts. Z 2 Процес поділу спряжений з реплікацією хромосоми (і плазмід, якщо такі є) Fts. Z – білок, який ініціює утворення септи (перегородки) між материнською і дочірньою клітинами 5 6 3 4 1. Збільшення маси клітини. Орієнтація нуклеоїда. 2. Ініціація реплікації ДНК у точці ori. C. Тут утворюється білковий комплекс необхідний для проходження реплікації ДНК. 3. Елонгація реплікації. 4. Термінація реплікації в точці ter. 5. Розділення хромосом. 6. Поділ клітини
E. coli – життєвий цикл ДНК ter Ori. С 1 Fts. Z 2 Процес поділу спряжений з реплікацією хромосоми (і плазмід, якщо такі є) Fts. Z – білок, який ініціює утворення септи (перегородки) між материнською і дочірньою клітинами 5 6 3 4 1. Збільшення маси клітини. Орієнтація нуклеоїда. 2. Ініціація реплікації ДНК у точці ori. C. Тут утворюється білковий комплекс необхідний для проходження реплікації ДНК. 3. Елонгація реплікації. 4. Термінація реплікації в точці ter. 5. Розділення хромосом. 6. Поділ клітини
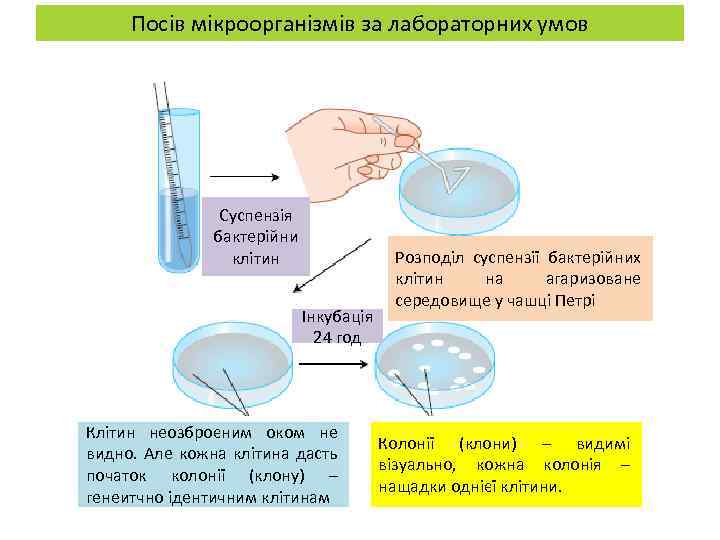 Посів мікроорганізмів за лабораторних умов Суспензія бактерійни клітин Інкубація 24 год Клітин неозброєним оком не видно. Але кожна клітина дасть початок колонії (клону) – генеитчно ідентичним клітинам Розподіл суспензії бактерійних клітин на агаризоване середовище у чашці Петрі Колонії (клони) – видимі візуально, кожна колонія – нащадки однієї клітини.
Посів мікроорганізмів за лабораторних умов Суспензія бактерійни клітин Інкубація 24 год Клітин неозброєним оком не видно. Але кожна клітина дасть початок колонії (клону) – генеитчно ідентичним клітинам Розподіл суспензії бактерійних клітин на агаризоване середовище у чашці Петрі Колонії (клони) – видимі візуально, кожна колонія – нащадки однієї клітини.
 E. coli – модельний об’єкт q. Легко отримати (кишкова мікрофлора людини) q. Простий одноклітинний організм, який можна культивувати за лабораторних умов без великих затрат. q. На твердому середовищі можна отримати окремі колонії. q. Наявність генетичних елементів, пов’язаних з E. coli: низка плазмід та бактеріофагів, транспозонів, які використовуються генетичних дослідженнях. q. Розмір - 1 мкм. q. Час генерації за оптимальних умов – 20 хвилин (в рідкому поживному середовищі – 30 хв). q. Одна хромосома. q. Розмножується поділом клітини. q. Можна отримати велику кількість клітин (велика вибірка) для дослідження генетичних закономірностей. q. Легко проводити скринінг рідкісних генетичних подій.
E. coli – модельний об’єкт q. Легко отримати (кишкова мікрофлора людини) q. Простий одноклітинний організм, який можна культивувати за лабораторних умов без великих затрат. q. На твердому середовищі можна отримати окремі колонії. q. Наявність генетичних елементів, пов’язаних з E. coli: низка плазмід та бактеріофагів, транспозонів, які використовуються генетичних дослідженнях. q. Розмір - 1 мкм. q. Час генерації за оптимальних умов – 20 хвилин (в рідкому поживному середовищі – 30 хв). q. Одна хромосома. q. Розмножується поділом клітини. q. Можна отримати велику кількість клітин (велика вибірка) для дослідження генетичних закономірностей. q. Легко проводити скринінг рідкісних генетичних подій.
 Перша еволюційна теорія 1809, Жан-Батист Ламарк Теорія вправлянь Мутації стимулює потреба Ч. Дарвін формально стояв на засадах ламаркізму, однак питання механізмів появи спадкової мінливості в його роботах не вивчалось
Перша еволюційна теорія 1809, Жан-Батист Ламарк Теорія вправлянь Мутації стимулює потреба Ч. Дарвін формально стояв на засадах ламаркізму, однак питання механізмів появи спадкової мінливості в його роботах не вивчалось
 E. coli – модельний об’єкт – флуктуаційний тест q Генетичне питання: поява спонтанних мутацій спричинена лише зовнішніми факторами чи з низькою частотою мутанти наявні у будь-якій популяції? q 1943 – Сальвадор Лурія і Макс Дельбрук – використовуючи чутливість E. coli до бактеріофага Т 1 довели випадковість спонтанних мутацій у бактерій. q. Бактеріофаг – вірус, що інфікує бактерію і спричиняє смерть клітини. q. E. coli чутлива до бактеріофага (фага) Т 1. q. Проаналізували появу мутації, яка б забезпечила стійкість до бактеріофага Т 1. Колонії, стійкі до фагової атаки виникали регулярно. Ці мутації – випадкові чи викликані виключно селективним середовищем (наявністю фага)? q. Селективне середовище – це середовище з таким складом, який дозволяє ріст лише мікроорганізмів з певними мутаціями.
E. coli – модельний об’єкт – флуктуаційний тест q Генетичне питання: поява спонтанних мутацій спричинена лише зовнішніми факторами чи з низькою частотою мутанти наявні у будь-якій популяції? q 1943 – Сальвадор Лурія і Макс Дельбрук – використовуючи чутливість E. coli до бактеріофага Т 1 довели випадковість спонтанних мутацій у бактерій. q. Бактеріофаг – вірус, що інфікує бактерію і спричиняє смерть клітини. q. E. coli чутлива до бактеріофага (фага) Т 1. q. Проаналізували появу мутації, яка б забезпечила стійкість до бактеріофага Т 1. Колонії, стійкі до фагової атаки виникали регулярно. Ці мутації – випадкові чи викликані виключно селективним середовищем (наявністю фага)? q. Селективне середовище – це середовище з таким складом, який дозволяє ріст лише мікроорганізмів з певними мутаціями.
 Флуктуаційний тест q Інокулювали 20 культур. Інкубували до густини 10 8 клітин на мілілітр середовища. З кожної культури відібрали зразок і посіяли на селективне середовище разом з фагом Т 1. q. На 11 чашках не було стійких до фага колоній. q. На 9 -ти чашках спостерігали появу стійких до фага колоній з такою частотою: - 1, 1, 3, 5, 5, 6, 35, 64 і 107 колоній на чашку.
Флуктуаційний тест q Інокулювали 20 культур. Інкубували до густини 10 8 клітин на мілілітр середовища. З кожної культури відібрали зразок і посіяли на селективне середовище разом з фагом Т 1. q. На 11 чашках не було стійких до фага колоній. q. На 9 -ти чашках спостерігали появу стійких до фага колоній з такою частотою: - 1, 1, 3, 5, 5, 6, 35, 64 і 107 колоній на чашку.
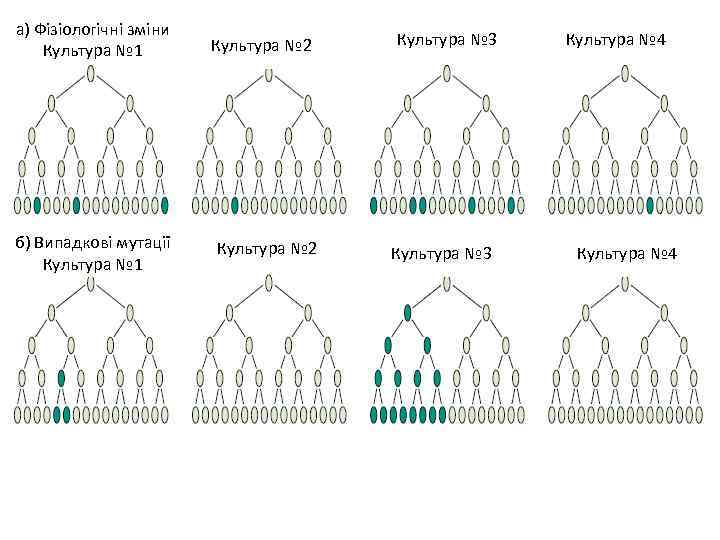 а) Фізіологічні зміни Культура № 1 б) Випадкові мутації Культура № 1 Культура № 2 Культура № 3 Культура № 4
а) Фізіологічні зміни Культура № 1 б) Випадкові мутації Культура № 1 Культура № 2 Культура № 3 Культура № 4
 Флуктуаційний тест q. Як це пояснити? q. Якби поява такої мутації була відповіддю на селективні умови, то мутанти виникали б з відносно однаковою частотою на різних чашках. q. Чому частота виникнення мутацій значно відрізняється у різних культур? q. Поява спонтанних мутацій – випадкове явище, незалежне від факторів зовнішнього середовища. q Чим швидше відбулася мутація, тим більше нащадків дала клітина з мутацією. q. Мутації, що відбулися на пізніх етапах розвитку культури закріпилися у меншої кількості клітин (менше часу на поділ). Макс Дельбрюк Сальвадор Лурія
Флуктуаційний тест q. Як це пояснити? q. Якби поява такої мутації була відповіддю на селективні умови, то мутанти виникали б з відносно однаковою частотою на різних чашках. q. Чому частота виникнення мутацій значно відрізняється у різних культур? q. Поява спонтанних мутацій – випадкове явище, незалежне від факторів зовнішнього середовища. q Чим швидше відбулася мутація, тим більше нащадків дала клітина з мутацією. q. Мутації, що відбулися на пізніх етапах розвитку культури закріпилися у меншої кількості клітин (менше часу на поділ). Макс Дельбрюк Сальвадор Лурія
 E. coli – модельний об’єкт вивчення регуляції експресії (активності транскрипції) генів q. Мікроорганізми відчувають умови середовища і реакцією на такі умови є репресія чи активація гена чи групи генів. q. Який механізм такої реакції? q. Моделлю для вивчення цього питання послугувала система метаболізму лактози Е. coli. q. При додаванні лактози у середовище рівень фермента β-галактозидази підвищується у 1000 разів. q. Що індукує лактоза ? Жак Моно Франсуа Жакоб Андре Львов
E. coli – модельний об’єкт вивчення регуляції експресії (активності транскрипції) генів q. Мікроорганізми відчувають умови середовища і реакцією на такі умови є репресія чи активація гена чи групи генів. q. Який механізм такої реакції? q. Моделлю для вивчення цього питання послугувала система метаболізму лактози Е. coli. q. При додаванні лактози у середовище рівень фермента β-галактозидази підвищується у 1000 разів. q. Що індукує лактоза ? Жак Моно Франсуа Жакоб Андре Львов
 E. coli – модельний об’єкт вивчення регуляції експресії (активності транскрипції) генів Експеримент: Припущення – лактоза індукує активацію білка-попередника βгалактозидази. Спростування: üДодаючи радіоактивно мічені амінокислоти, виявили, що вони активніше включаються у β-галактозидазу при додаванні галактози. üОкрім того, зростав рівень інших білків, зокрема пермеази. üОтримання та аналіз низки мутантних штамів з порушеною регуляцією засвоєння лактози дало змогу зробити висновок про генетичний механізм регуляції генів у прокаріот. üЯк індуктор, використали аналог лактози, який не розщеплювався βгалактозидазою: ізопропіл-D-тіогалактозид (IPTG).
E. coli – модельний об’єкт вивчення регуляції експресії (активності транскрипції) генів Експеримент: Припущення – лактоза індукує активацію білка-попередника βгалактозидази. Спростування: üДодаючи радіоактивно мічені амінокислоти, виявили, що вони активніше включаються у β-галактозидазу при додаванні галактози. üОкрім того, зростав рівень інших білків, зокрема пермеази. üОтримання та аналіз низки мутантних штамів з порушеною регуляцією засвоєння лактози дало змогу зробити висновок про генетичний механізм регуляції генів у прокаріот. üЯк індуктор, використали аналог лактози, який не розщеплювався βгалактозидазою: ізопропіл-D-тіогалактозид (IPTG).
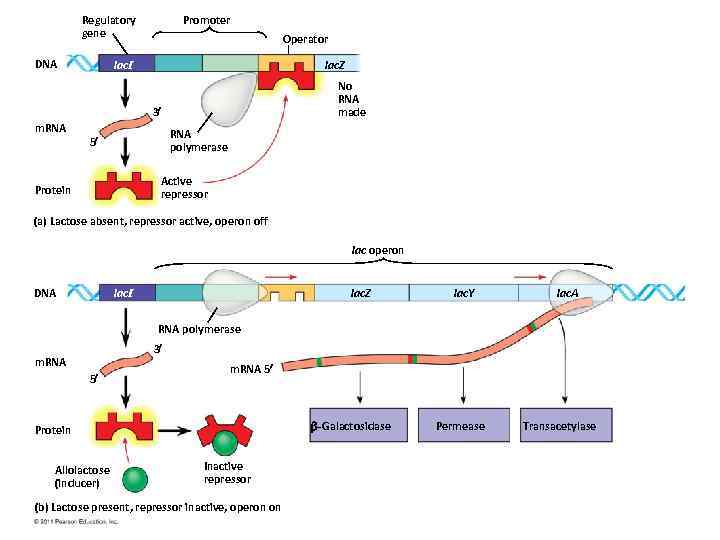 Regulatory gene DNA Promoter Operator lac. I lac. Z No RNA made 3 m. RNA polymerase 5 Active repressor Protein (a) Lactose absent, repressor active, operon off lac operon DNA lac. I lac. Z lac. Y lac. A RNA polymerase 3 m. RNA 5 -Galactosidase Protein Allolactose (inducer) Inactive repressor (b) Lactose present, repressor inactive, operon on Permease Transacetylase
Regulatory gene DNA Promoter Operator lac. I lac. Z No RNA made 3 m. RNA polymerase 5 Active repressor Protein (a) Lactose absent, repressor active, operon off lac operon DNA lac. I lac. Z lac. Y lac. A RNA polymerase 3 m. RNA 5 -Galactosidase Protein Allolactose (inducer) Inactive repressor (b) Lactose present, repressor inactive, operon on Permease Transacetylase
 Висновок: üлактоза впливає на рівень транскрипції гена, що кодує βгалактозидазу та генів, що контролюють транспорт її у клітину (пермеази). Транскрипція кількох генів регулюється одним механізмом. Для регуляції транскрипції гена/генів прокаріот необхідна наявність двох сайтів: Сайту зв’язування РНК-полімерази – промотор. Сайту зв’язування активатора або репресора – оператор. Послідовність ДНК, яка необхідна для ініціації транскрипції називається промотором, розміщена перед геном або низкою генів. Оперон – послідовність ДНК, що містить низку генів (кластер), експресія яких регулюється одним промотором.
Висновок: üлактоза впливає на рівень транскрипції гена, що кодує βгалактозидазу та генів, що контролюють транспорт її у клітину (пермеази). Транскрипція кількох генів регулюється одним механізмом. Для регуляції транскрипції гена/генів прокаріот необхідна наявність двох сайтів: Сайту зв’язування РНК-полімерази – промотор. Сайту зв’язування активатора або репресора – оператор. Послідовність ДНК, яка необхідна для ініціації транскрипції називається промотором, розміщена перед геном або низкою генів. Оперон – послідовність ДНК, що містить низку генів (кластер), експресія яких регулюється одним промотором.
 E. coli – модельний об’єкт вивчення регуляції експресії (активності транскрипції) генів Отримання та аналіз низки мутантних штамів з порушеною регуляцією засвоєння галактози дало змогу зробити висновок про генетичний механізм регуляції генів у прокаріот. Як індуктор, використали аналог галактози, який не розщеплювався βгалактозидазою: ізопропіл-D-тіогалактозид (IPTG). Для регуляції транскрипції гена прокаріот необхідна наявність двох сайтів: Сайту зв’язування РНК-полімерази – промотор. Сайту зв’язування активатора або репресора – оператор. Послідовність ДНК, яка необхідна для ініціації транскрипції називається промотором, розміщена перед геном або низкою генів. МWhen lactose is absent then there is very little Lac enzyme production (the operator has Lac repressor bound to it). When lactose is present but a preferred carbon source (like glucose) is also present then a small amount of enzyme is produced (Lac repressor is not bound to the operator).
E. coli – модельний об’єкт вивчення регуляції експресії (активності транскрипції) генів Отримання та аналіз низки мутантних штамів з порушеною регуляцією засвоєння галактози дало змогу зробити висновок про генетичний механізм регуляції генів у прокаріот. Як індуктор, використали аналог галактози, який не розщеплювався βгалактозидазою: ізопропіл-D-тіогалактозид (IPTG). Для регуляції транскрипції гена прокаріот необхідна наявність двох сайтів: Сайту зв’язування РНК-полімерази – промотор. Сайту зв’язування активатора або репресора – оператор. Послідовність ДНК, яка необхідна для ініціації транскрипції називається промотором, розміщена перед геном або низкою генів. МWhen lactose is absent then there is very little Lac enzyme production (the operator has Lac repressor bound to it). When lactose is present but a preferred carbon source (like glucose) is also present then a small amount of enzyme is produced (Lac repressor is not bound to the operator).
 E. coli – модельний об’єкт. Передача ДНК від однієї бактерійної клітини до іншої можлива за допомогою: ØКон’югації ØТрансформації ØТрансдукції
E. coli – модельний об’єкт. Передача ДНК від однієї бактерійної клітини до іншої можлива за допомогою: ØКон’югації ØТрансформації ØТрансдукції
 E. coli – модельний об’єкт – явище кон’югації. ØРезультатом статевого розмноження є передача нащадкам перекомбінованого та поєднаного генетичного матеріалу двох батьківських організмів. ØЧи є у бактерій аналогічне до статевого розмноження явище? Ø 1946 р – Джошуа Ледерберг і Едвард Тейтум – виявили подібне до статевого розмноження явище у бактерій. ØE. coli здатна синтезувати самостійно амінокислоти та вітаміни. ØПрацювали з двома мутантними штамами: штам А (ауксотроф за метіоніном і біотином), штам В (ауксотроф за треоніном, лейцином і тіаміном). Штам А: met- bio - thr + leu + thi + strain B: met + bio + thr - leu - thi – • Штами змішали разом і висіяли на чашку з мінімальним середовищем. • Невелика кількість клітин (1× 107) утворила колонії на мінімальному середовищі. Тобто набули рис штаму дикого типу.
E. coli – модельний об’єкт – явище кон’югації. ØРезультатом статевого розмноження є передача нащадкам перекомбінованого та поєднаного генетичного матеріалу двох батьківських організмів. ØЧи є у бактерій аналогічне до статевого розмноження явище? Ø 1946 р – Джошуа Ледерберг і Едвард Тейтум – виявили подібне до статевого розмноження явище у бактерій. ØE. coli здатна синтезувати самостійно амінокислоти та вітаміни. ØПрацювали з двома мутантними штамами: штам А (ауксотроф за метіоніном і біотином), штам В (ауксотроф за треоніном, лейцином і тіаміном). Штам А: met- bio - thr + leu + thi + strain B: met + bio + thr - leu - thi – • Штами змішали разом і висіяли на чашку з мінімальним середовищем. • Невелика кількість клітин (1× 107) утворила колонії на мінімальному середовищі. Тобто набули рис штаму дикого типу.
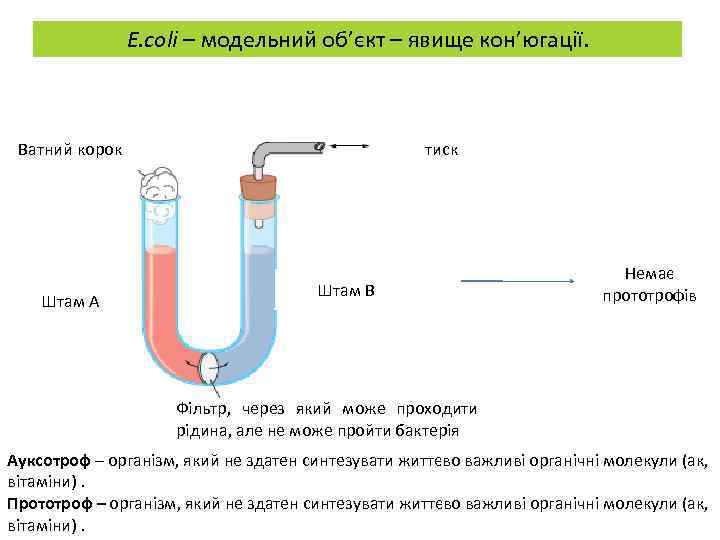 E. coli – модельний об’єкт – явище кон’югації. Ватний корок Штам А тиск Штам В Немає прототрофів Фільтр, через який може проходити рідина, але не може пройти бактерія Ауксотроф – організм, який не здатен синтезувати життєво важливі органічні молекули (ак, вітаміни). Прототроф – організм, який не здатен синтезувати життєво важливі органічні молекули (ак, вітаміни).
E. coli – модельний об’єкт – явище кон’югації. Ватний корок Штам А тиск Штам В Немає прототрофів Фільтр, через який може проходити рідина, але не може пройти бактерія Ауксотроф – організм, який не здатен синтезувати життєво важливі органічні молекули (ак, вітаміни). Прототроф – організм, який не здатен синтезувати життєво важливі органічні молекули (ак, вітаміни).
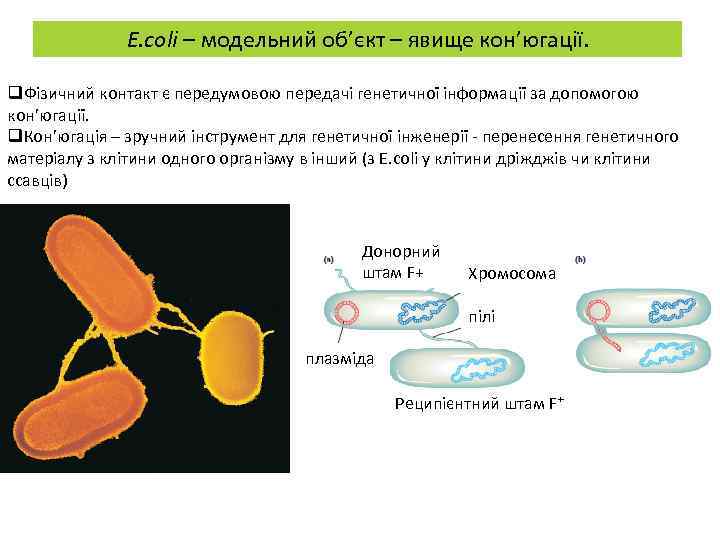 E. coli – модельний об’єкт – явище кон’югації. q. Фізичний контакт є передумовою передачі генетичної інформації за допомогою кон’югації. q. Кон’югація – зручний інструмент для генетичної інженерії - перенесення генетичного матеріалу з клітини одного організму в інший (з E. coli у клітини дріжджів чи клітини ссавців) Донорний штам F+ Хромосома пілі плазміда Реципієнтний штам F+
E. coli – модельний об’єкт – явище кон’югації. q. Фізичний контакт є передумовою передачі генетичної інформації за допомогою кон’югації. q. Кон’югація – зручний інструмент для генетичної інженерії - перенесення генетичного матеріалу з клітини одного організму в інший (з E. coli у клітини дріжджів чи клітини ссавців) Донорний штам F+ Хромосома пілі плазміда Реципієнтний штам F+
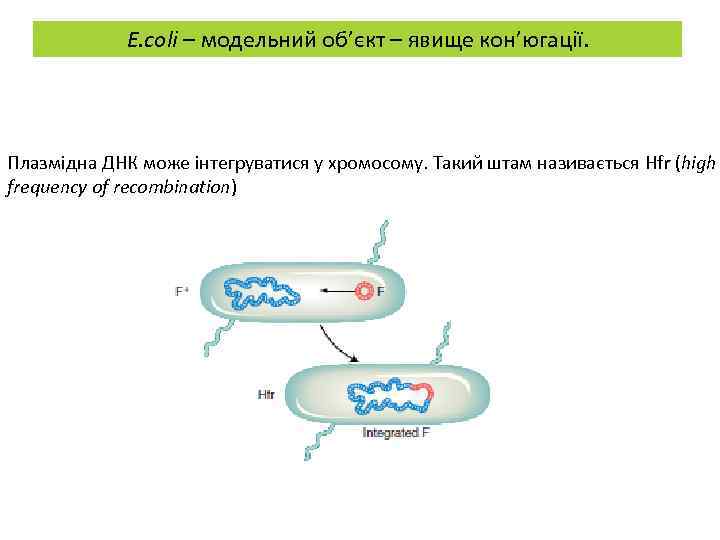 E. coli – модельний об’єкт – явище кон’югації. Плазмідна ДНК може інтегруватися у хромосому. Такий штам називається Hfr (high frequency of recombination)
E. coli – модельний об’єкт – явище кон’югації. Плазмідна ДНК може інтегруватися у хромосому. Такий штам називається Hfr (high frequency of recombination)
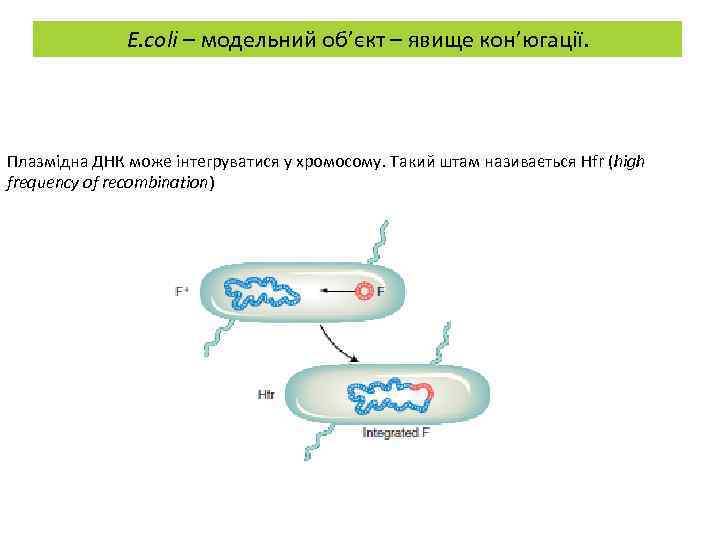 E. coli – модельний об’єкт – явище кон’югації. Плазмідна ДНК може інтегруватися у хромосому. Такий штам називається Hfr (high frequency of recombination)
E. coli – модельний об’єкт – явище кон’югації. Плазмідна ДНК може інтегруватися у хромосому. Такий штам називається Hfr (high frequency of recombination)
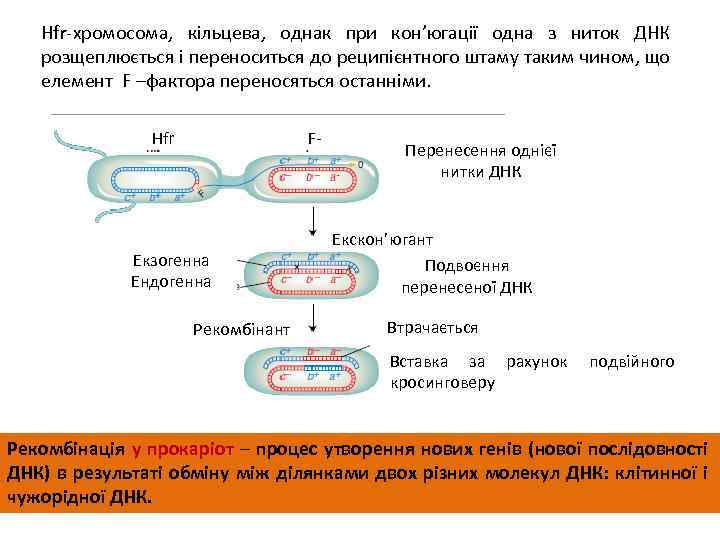 Hfr-хромосома, кільцева, однак при кон’югації одна з ниток ДНК розщеплюється і переноситься до реципієнтного штаму таким чином, що елемент F –фактора переносяться останніми. Hfr F- Екзогенна Ендогенна Рекомбінант Перенесення однієї нитки ДНК Екскон’югант Подвоєння перенесеної ДНК Втрачається Вставка за рахунок кросинговеру подвійного Рекомбінація у прокаріот – процес утворення нових генів (нової послідовності ДНК) в результаті обміну між ділянками двох різних молекул ДНК: клітинної і чужорідної ДНК.
Hfr-хромосома, кільцева, однак при кон’югації одна з ниток ДНК розщеплюється і переноситься до реципієнтного штаму таким чином, що елемент F –фактора переносяться останніми. Hfr F- Екзогенна Ендогенна Рекомбінант Перенесення однієї нитки ДНК Екскон’югант Подвоєння перенесеної ДНК Втрачається Вставка за рахунок кросинговеру подвійного Рекомбінація у прокаріот – процес утворення нових генів (нової послідовності ДНК) в результаті обміну між ділянками двох різних молекул ДНК: клітинної і чужорідної ДНК.
 E. coli – використання у генетичній інженерії. Клітини E. coli найчастіше використовують для: q. Конструювання рекомбінантних ДНК; q. Сайт-специфічної інактивації генів; q. Отримання рекомбінантних білків; q. Отримання у препаративних кількостях молекул білків (інсулін); q. Для цього використовують плазміди і штами E. coli з певним набором генів і мутацій, відповідно.
E. coli – використання у генетичній інженерії. Клітини E. coli найчастіше використовують для: q. Конструювання рекомбінантних ДНК; q. Сайт-специфічної інактивації генів; q. Отримання рекомбінантних білків; q. Отримання у препаративних кількостях молекул білків (інсулін); q. Для цього використовують плазміди і штами E. coli з певним набором генів і мутацій, відповідно.
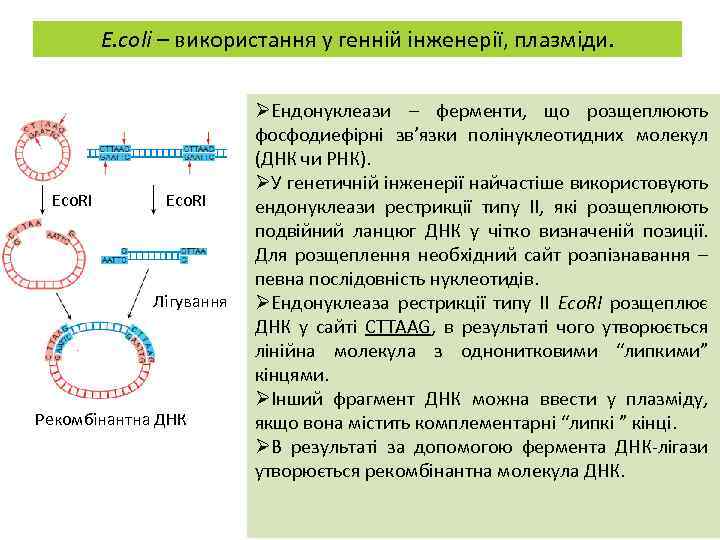 E. coli – використання у генній інженерії, плазміди. Eco. RI Лігування Рекомбінантна ДНК ØЕндонуклеази – ферменти, що розщеплюють фосфодиефірні зв’язки полінуклеотидних молекул (ДНК чи РНК). ØУ генетичній інженерії найчастіше використовують ендонуклеази рестрикції типу ІІ, які розщеплюють подвійний ланцюг ДНК у чітко визначеній позиції. Для розщеплення необхідний сайт розпізнавання – певна послідовність нуклеотидів. ØЕндонуклеаза рестрикції типу ІІ Eco. RI розщеплює ДНК у сайті CTTAAG, в результаті чого утворюється лінійна молекула з однонитковими “липкими” кінцями. ØІнший фрагмент ДНК можна ввести у плазміду, якщо вона містить комплементарні “липкі ” кінці. ØВ результаті за допомогою фермента ДНК-лігази утворюється рекомбінантна молекула ДНК.
E. coli – використання у генній інженерії, плазміди. Eco. RI Лігування Рекомбінантна ДНК ØЕндонуклеази – ферменти, що розщеплюють фосфодиефірні зв’язки полінуклеотидних молекул (ДНК чи РНК). ØУ генетичній інженерії найчастіше використовують ендонуклеази рестрикції типу ІІ, які розщеплюють подвійний ланцюг ДНК у чітко визначеній позиції. Для розщеплення необхідний сайт розпізнавання – певна послідовність нуклеотидів. ØЕндонуклеаза рестрикції типу ІІ Eco. RI розщеплює ДНК у сайті CTTAAG, в результаті чого утворюється лінійна молекула з однонитковими “липкими” кінцями. ØІнший фрагмент ДНК можна ввести у плазміду, якщо вона містить комплементарні “липкі ” кінці. ØВ результаті за допомогою фермента ДНК-лігази утворюється рекомбінантна молекула ДНК.
 E. coli – використання у генній інженерії, плазміди. q. Вектор – це плазміда, яку використовують у генетичній інженерії для конструювання рекомбінантної ДНК, експресії досліджуваних генів та переносу рекомбінантної ДНК з одного організму в інший. q. Основні складові вектора: полілінкер, селективні генетичні маркери, ділянка ori. q. Полілінкер або multiple cloning site (MCS) – це короткий сегмент ДНК, який містить сайти рестрикції (інколи понад 20). Кожен сайт рестрикції полілінкера, як правило, є унікальним у векторі. q. Селективні генетичні маркери – гени, які надають здатність мікроорганізму рости за певних селективних умов або засвоювати специфічний субстрат. qori - послідовність ДНК, необхідна для ініціації реплікації.
E. coli – використання у генній інженерії, плазміди. q. Вектор – це плазміда, яку використовують у генетичній інженерії для конструювання рекомбінантної ДНК, експресії досліджуваних генів та переносу рекомбінантної ДНК з одного організму в інший. q. Основні складові вектора: полілінкер, селективні генетичні маркери, ділянка ori. q. Полілінкер або multiple cloning site (MCS) – це короткий сегмент ДНК, який містить сайти рестрикції (інколи понад 20). Кожен сайт рестрикції полілінкера, як правило, є унікальним у векторі. q. Селективні генетичні маркери – гени, які надають здатність мікроорганізму рости за певних селективних умов або засвоювати специфічний субстрат. qori - послідовність ДНК, необхідна для ініціації реплікації.
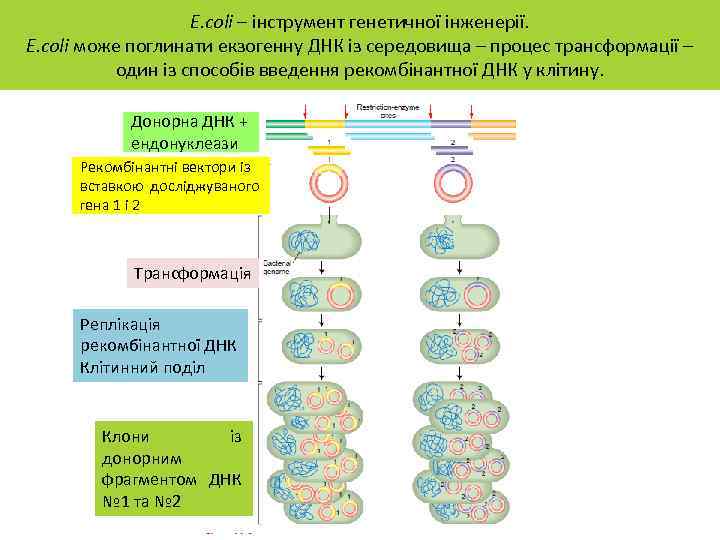 E. coli – інструмент генетичної інженерії. E. сoli може поглинати екзогенну ДНК із середовища – процес трансформації – один із способів введення рекомбінантної ДНК у клітину. Донорна ДНК + ендонуклеази Рекомбінантні вектори із вставкою досліджуваного гена 1 і 2 Трансформація Реплікація рекомбінантної ДНК Клітинний поділ Клони із донорним фрагментом ДНК № 1 та № 2
E. coli – інструмент генетичної інженерії. E. сoli може поглинати екзогенну ДНК із середовища – процес трансформації – один із способів введення рекомбінантної ДНК у клітину. Донорна ДНК + ендонуклеази Рекомбінантні вектори із вставкою досліджуваного гена 1 і 2 Трансформація Реплікація рекомбінантної ДНК Клітинний поділ Клони із донорним фрагментом ДНК № 1 та № 2
 Штами та плазміди E. coli, які використовують у лабораторних експериментах. XL 1 -Blue, DH 5α – штами E. coli для конструювання рекомбінантної ДНК: Генотип DH 5α: F- gyr. A 96 (Nalr) rec. A 1 rel. A 1 thi-1 hsd. R 17 (rk-mk+) gln. V 44 deo. R Δ(lac. ZYA-arg. F)U 169 [Φ 80 dΔ(lac. Z)M 15] gyr. A 96 – точкова мутація в гені субодиниці А ДНК-гірази – надає стійкості до налідиксової кислоти. rec. A 1 - відсутність гомологічної рекомбінації. rel. A 1 – втрата здатності синтезувати pp. Gpp у відповідь на ак голодування. end. A 1 – неактивний ген неспецифічної ендонуклеази І. З такого штаму отримують високої якості ДНК. thi-1 - ауксотроф за тіаміном. hsd. R 17 – мутація, що призвела до втрати здатності розщеплювати неметильовану ДНК, але вся ДНК клітини метилюється. gln. V 44 - A glutamine-inserting amber (UAG) suppressor t. RNA; required for growth of some phage vectors. Now called gln. V.
Штами та плазміди E. coli, які використовують у лабораторних експериментах. XL 1 -Blue, DH 5α – штами E. coli для конструювання рекомбінантної ДНК: Генотип DH 5α: F- gyr. A 96 (Nalr) rec. A 1 rel. A 1 thi-1 hsd. R 17 (rk-mk+) gln. V 44 deo. R Δ(lac. ZYA-arg. F)U 169 [Φ 80 dΔ(lac. Z)M 15] gyr. A 96 – точкова мутація в гені субодиниці А ДНК-гірази – надає стійкості до налідиксової кислоти. rec. A 1 - відсутність гомологічної рекомбінації. rel. A 1 – втрата здатності синтезувати pp. Gpp у відповідь на ак голодування. end. A 1 – неактивний ген неспецифічної ендонуклеази І. З такого штаму отримують високої якості ДНК. thi-1 - ауксотроф за тіаміном. hsd. R 17 – мутація, що призвела до втрати здатності розщеплювати неметильовану ДНК, але вся ДНК клітини метилюється. gln. V 44 - A glutamine-inserting amber (UAG) suppressor t. RNA; required for growth of some phage vectors. Now called gln. V.
 Приклади штамів та плазмід E. coli, які використовують у лабораторних експериментах. Штам K-12– лабораторний штам Е. coli, на базі якого сконструювали низку похідних штамів. K-12 MG 1655 Генотип: F- lambda- ilv. G- rfb-50 rph-1 ET 12567 (p. UZ 8002) – штам, який містить мутації у гені метилази. Чужерідні молекули ДНК не метилюються. Така ДНК не буде розщеплюватися ендонуклеазами. BL 21(DE 3) - E. coli B F– dcm omp. T hsd. S(r. B– m. B–) gal λ(DE 3): E. coli штам B, який містить похідну ДНК фага лямбда (DE 3) та мутації в генах протеаз. Штам сконструйований таким чином, що досліджуваний ген транскрибується лише після введення дослідником у середовище індуктора. Інактивація генів протеаз запобігає деградації білка, який потрібно отримати. Штам використовується для отримання та очистки гібридних молекул білка (білки інших мікроорганізмів, білки людини). Очищені білки можуть використовувати для подальших досліджень їхньої функції.
Приклади штамів та плазмід E. coli, які використовують у лабораторних експериментах. Штам K-12– лабораторний штам Е. coli, на базі якого сконструювали низку похідних штамів. K-12 MG 1655 Генотип: F- lambda- ilv. G- rfb-50 rph-1 ET 12567 (p. UZ 8002) – штам, який містить мутації у гені метилази. Чужерідні молекули ДНК не метилюються. Така ДНК не буде розщеплюватися ендонуклеазами. BL 21(DE 3) - E. coli B F– dcm omp. T hsd. S(r. B– m. B–) gal λ(DE 3): E. coli штам B, який містить похідну ДНК фага лямбда (DE 3) та мутації в генах протеаз. Штам сконструйований таким чином, що досліджуваний ген транскрибується лише після введення дослідником у середовище індуктора. Інактивація генів протеаз запобігає деградації білка, який потрібно отримати. Штам використовується для отримання та очистки гібридних молекул білка (білки інших мікроорганізмів, білки людини). Очищені білки можуть використовувати для подальших досліджень їхньої функції.
 Зберігання культур E. coli q. Основним завдання зберігання культур: ü підтримка життєдіяльності клітин; ü чистоти культури; üзапобігання появі мутацій. q. Фактори зберігання: üпідбір середовища і способу культивування; üпідбір фази росту культури на момент зберігання.
Зберігання культур E. coli q. Основним завдання зберігання культур: ü підтримка життєдіяльності клітин; ü чистоти культури; üзапобігання появі мутацій. q. Фактори зберігання: üпідбір середовища і способу культивування; üпідбір фази росту культури на момент зберігання.
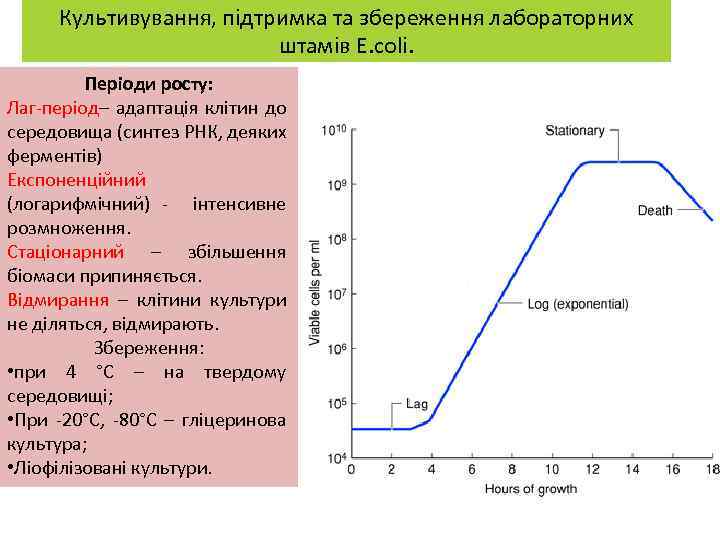 Культивування, підтримка та збереження лабораторних штамів E. coli. Періоди росту: Лаг-період– адаптація клітин до середовища (синтез РНК, деяких ферментів) Експоненційний (логарифмічний) - інтенсивне розмноження. Стаціонарний – збільшення біомаси припиняється. Відмирання – клітини культури не діляться, відмирають. Збереження: • при 4 °С – на твердому середовищі; • При -20°С, -80°С – гліцеринова культура; • Ліофілізовані культури.
Культивування, підтримка та збереження лабораторних штамів E. coli. Періоди росту: Лаг-період– адаптація клітин до середовища (синтез РНК, деяких ферментів) Експоненційний (логарифмічний) - інтенсивне розмноження. Стаціонарний – збільшення біомаси припиняється. Відмирання – клітини культури не діляться, відмирають. Збереження: • при 4 °С – на твердому середовищі; • При -20°С, -80°С – гліцеринова культура; • Ліофілізовані культури.
 Збереження лабораторних штамів E. coli. Центри збереження штамів E. coli: Keio collection – колекція мутантних штамів з інактивацією одного чи серії генів, при університеті Кейо (Японія). Coli Genetic Stock Center (CGSC) – колекція штамів дикого типу та мутантних штамів при Єльському університеті (США). National Bio. Resource Project (NBRP E. coli ) – колекція мутантних штамів, векторів і плазмід, Японія. American Type Culture Collection (ATCC)
Збереження лабораторних штамів E. coli. Центри збереження штамів E. coli: Keio collection – колекція мутантних штамів з інактивацією одного чи серії генів, при університеті Кейо (Японія). Coli Genetic Stock Center (CGSC) – колекція штамів дикого типу та мутантних штамів при Єльському університеті (США). National Bio. Resource Project (NBRP E. coli ) – колекція мутантних штамів, векторів і плазмід, Японія. American Type Culture Collection (ATCC)


