Антикоагулянты амстердам 2013.pptx
- Количество слайдов: 40
 ESC 2013 Аспирант кафедры профилактической и неотложной кардиологии Гаппоева З. К.
ESC 2013 Аспирант кафедры профилактической и неотложной кардиологии Гаппоева З. К.
 RE-ALIGN Безопасность применения новых антикоагулянтов (дабигатрана) у пациентов с механическими протезами сердца
RE-ALIGN Безопасность применения новых антикоагулянтов (дабигатрана) у пациентов с механическими протезами сердца
 RE-ALIGN: сравнение дабигатрана с варфарином у пациентов с механическими протезами клапанов сердца 2. 11. 2011 – 28. 11. 2012 гг. Рандомизированное исследование II фазы Участвовало 39 центров (10 стран)
RE-ALIGN: сравнение дабигатрана с варфарином у пациентов с механическими протезами клапанов сердца 2. 11. 2011 – 28. 11. 2012 гг. Рандомизированное исследование II фазы Участвовало 39 центров (10 стран)
 RE-ALIGN: цель исследования Определение дозы дабигатрана для больных с механическими протезами клапанов сердца
RE-ALIGN: цель исследования Определение дозы дабигатрана для больных с механическими протезами клапанов сердца
 RE-ALIGN: критерии включения Возраст с 18 до 75 лет Имплантация механического митрального, аортального или 2 клапанов сердца
RE-ALIGN: критерии включения Возраст с 18 до 75 лет Имплантация механического митрального, аортального или 2 клапанов сердца
 RE-ALIGN: критерии исключения Пациенты с повторным протезированием клапанов, протезированием корня аорты, восходящего отдела аорты Наличие биологического протеза Осложнения в ранний послеоперационный период Неконтролируемая артериальная гипертензия Геморрагические инсульты в анамнезе (в течение последних 6 месяцев) Активные формы гепатитов Клиренс креатинина меньше 40 мл/мин
RE-ALIGN: критерии исключения Пациенты с повторным протезированием клапанов, протезированием корня аорты, восходящего отдела аорты Наличие биологического протеза Осложнения в ранний послеоперационный период Неконтролируемая артериальная гипертензия Геморрагические инсульты в анамнезе (в течение последних 6 месяцев) Активные формы гепатитов Клиренс креатинина меньше 40 мл/мин
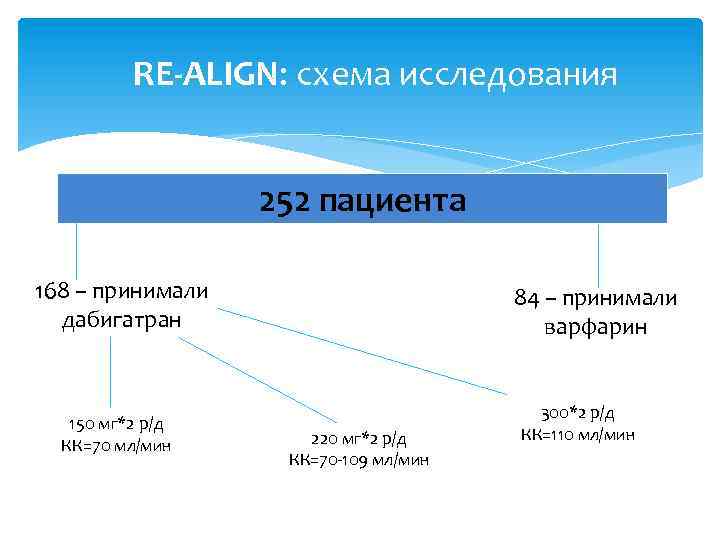 RE-ALIGN: схема исследования 252 пациента 168 – принимали дабигатран 150 мг*2 р/д КК=70 мл/мин 84 – принимали варфарин 220 мг*2 р/д КК=70 -109 мл/мин 300*2 р/д КК=110 мл/мин
RE-ALIGN: схема исследования 252 пациента 168 – принимали дабигатран 150 мг*2 р/д КК=70 мл/мин 84 – принимали варфарин 220 мг*2 р/д КК=70 -109 мл/мин 300*2 р/д КК=110 мл/мин
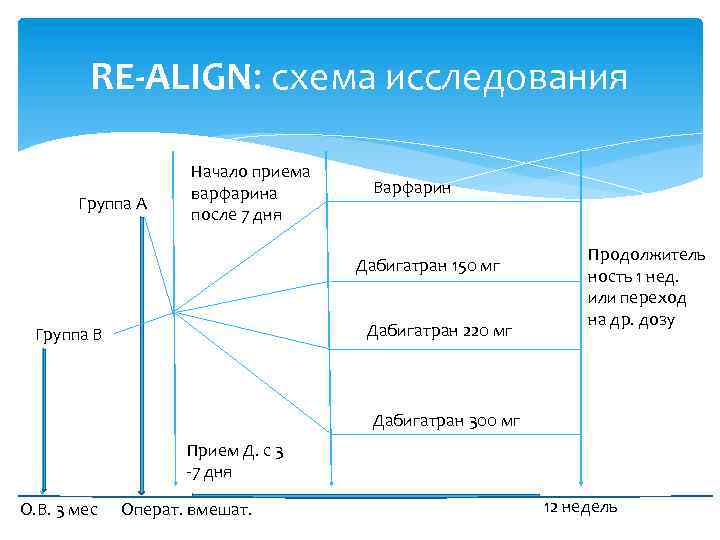 RE-ALIGN: схема исследования Группа А Начало приема варфарина после 7 дня Варфарин Дабигатран 150 мг Дабигатран 220 мг Группа В Продолжитель ность 1 нед. или переход на др. дозу Дабигатран 300 мг Прием Д. с 3 -7 дня О. В. 3 мес Операт. вмешат. 12 недель
RE-ALIGN: схема исследования Группа А Начало приема варфарина после 7 дня Варфарин Дабигатран 150 мг Дабигатран 220 мг Группа В Продолжитель ность 1 нед. или переход на др. дозу Дабигатран 300 мг Прием Д. с 3 -7 дня О. В. 3 мес Операт. вмешат. 12 недель
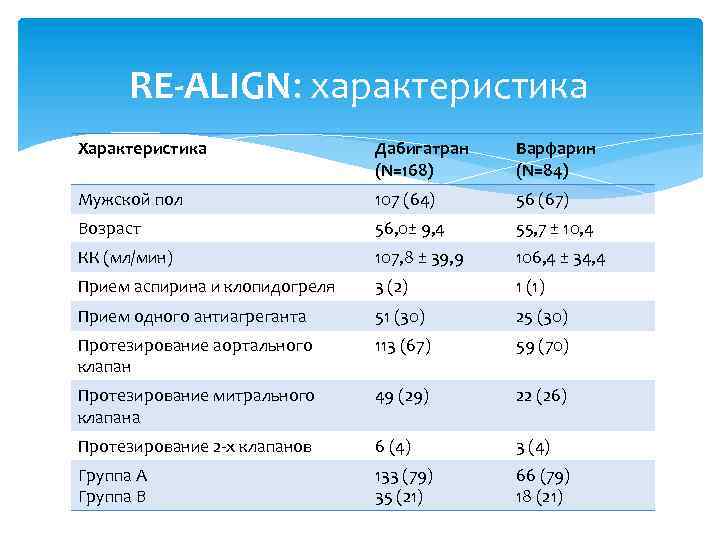 RE-ALIGN: характеристика Характеристика Дабигатран (N=168) Варфарин (N=84) Мужской пол 107 (64) 56 (67) Возраст 56, 0± 9, 4 55, 7 ± 10, 4 КК (мл/мин) 107, 8 ± 39, 9 106, 4 ± 34, 4 Прием аспирина и клопидогреля 3 (2) 1 (1) Прием одного антиагреганта 51 (30) 25 (30) Протезирование аортального клапан 113 (67) 59 (70) Протезирование митрального клапана 49 (29) 22 (26) Протезирование 2 -х клапанов 6 (4) 3 (4) Группа А Группа В 133 (79) 35 (21) 66 (79) 18 (21)
RE-ALIGN: характеристика Характеристика Дабигатран (N=168) Варфарин (N=84) Мужской пол 107 (64) 56 (67) Возраст 56, 0± 9, 4 55, 7 ± 10, 4 КК (мл/мин) 107, 8 ± 39, 9 106, 4 ± 34, 4 Прием аспирина и клопидогреля 3 (2) 1 (1) Прием одного антиагреганта 51 (30) 25 (30) Протезирование аортального клапан 113 (67) 59 (70) Протезирование митрального клапана 49 (29) 22 (26) Протезирование 2 -х клапанов 6 (4) 3 (4) Группа А Группа В 133 (79) 35 (21) 66 (79) 18 (21)
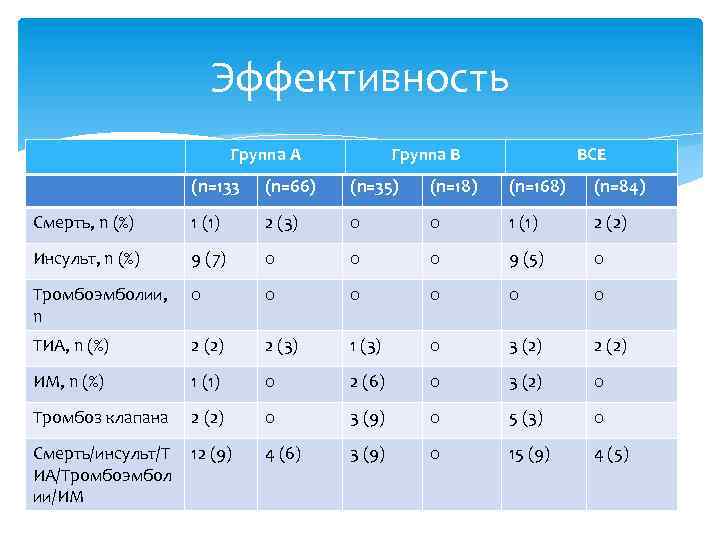 Эффективность Группа А Даб. Варф. (n=133 (n=66) Группа В Даб. Вар. (n=35) (n=18) Даб. (n=168) ВСЕ Вар. (n=84) Смерть, n (%) 1 (1) 2 (3) 0 0 1 (1) 2 (2) Инсульт, n (%) 9 (7) 0 0 0 9 (5) 0 Тромбоэмболии, n 0 0 0 ТИА, n (%) 2 (2) 2 (3) 1 (3) 0 3 (2) 2 (2) ИМ, n (%) 1 (1) 0 2 (6) 0 3 (2) 0 Тромбоз клапана 2 (2) 0 3 (9) 0 5 (3) 0 Смерть/инсульт/Т ИА/Тромбоэмбол ии/ИМ 12 (9) 4 (6) 3 (9) 0 15 (9) 4 (5)
Эффективность Группа А Даб. Варф. (n=133 (n=66) Группа В Даб. Вар. (n=35) (n=18) Даб. (n=168) ВСЕ Вар. (n=84) Смерть, n (%) 1 (1) 2 (3) 0 0 1 (1) 2 (2) Инсульт, n (%) 9 (7) 0 0 0 9 (5) 0 Тромбоэмболии, n 0 0 0 ТИА, n (%) 2 (2) 2 (3) 1 (3) 0 3 (2) 2 (2) ИМ, n (%) 1 (1) 0 2 (6) 0 3 (2) 0 Тромбоз клапана 2 (2) 0 3 (9) 0 5 (3) 0 Смерть/инсульт/Т ИА/Тромбоэмбол ии/ИМ 12 (9) 4 (6) 3 (9) 0 15 (9) 4 (5)
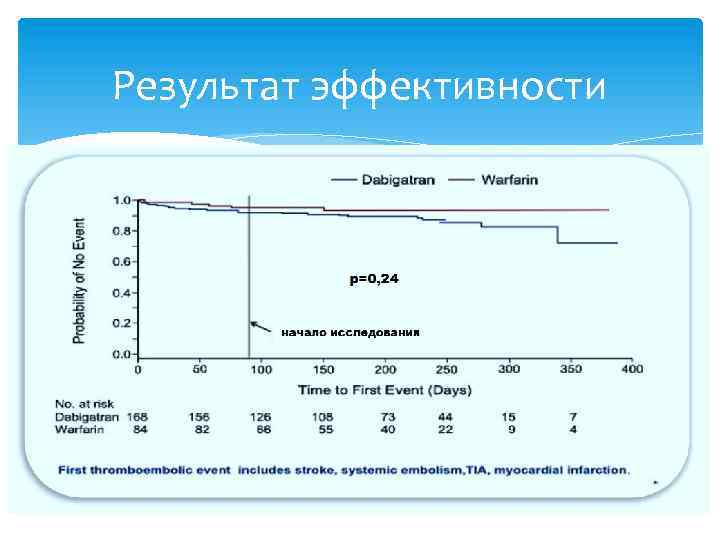 Результат эффективности
Результат эффективности
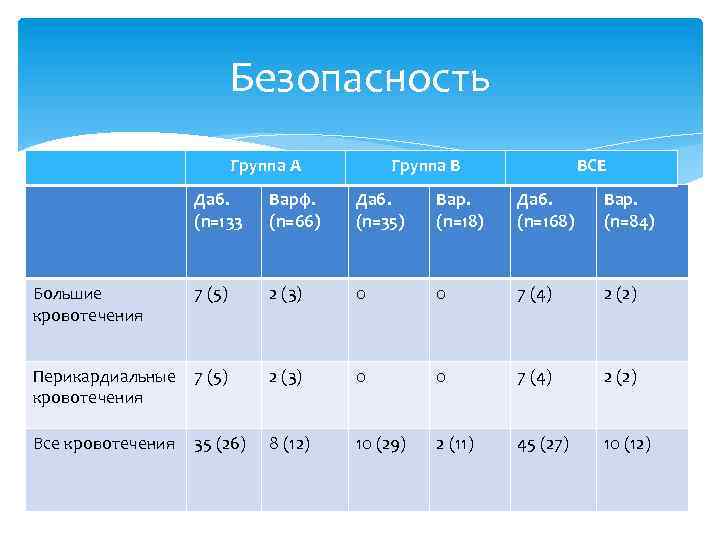 Безопасность Группа А Группа В ВСЕ Даб. (n=133 Варф. (n=66) Даб. (n=35) Вар. (n=18) Даб. (n=168) Вар. (n=84) Большие кровотечения 7 (5) 2 (3) 0 0 7 (4) 2 (2) Перикардиальные кровотечения 7 (5) 2 (3) 0 0 7 (4) 2 (2) Все кровотечения 35 (26) 8 (12) 10 (29) 2 (11) 45 (27) 10 (12)
Безопасность Группа А Группа В ВСЕ Даб. (n=133 Варф. (n=66) Даб. (n=35) Вар. (n=18) Даб. (n=168) Вар. (n=84) Большие кровотечения 7 (5) 2 (3) 0 0 7 (4) 2 (2) Перикардиальные кровотечения 7 (5) 2 (3) 0 0 7 (4) 2 (2) Все кровотечения 35 (26) 8 (12) 10 (29) 2 (11) 45 (27) 10 (12)
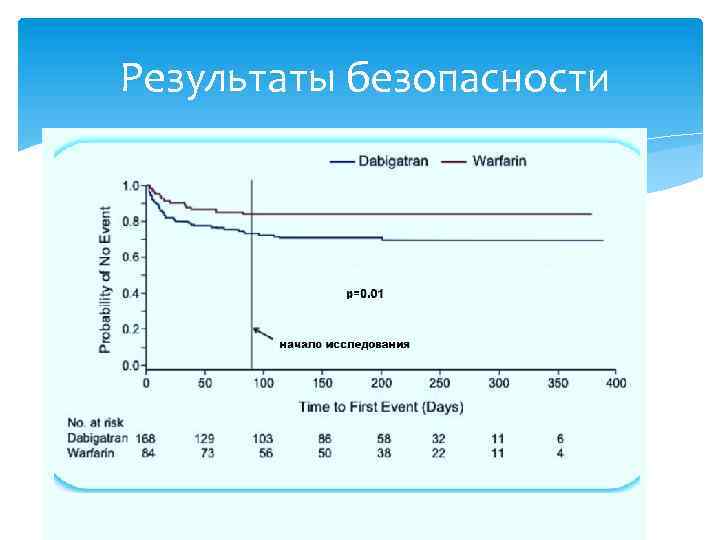 Результаты безопасности
Результаты безопасности
 Заключение RE-ALIGN – первое рандомизированное исследование, сравнивающее новый пероральный антикоагулянт с варфарином у пациентов с механическим клапаном Использование дабигатрана в качестве альтернативы варфарна для профилактики тромбоэмболических осложнений у больных с протезирование клапанов сердца (механическим протезом) нецелесообразно
Заключение RE-ALIGN – первое рандомизированное исследование, сравнивающее новый пероральный антикоагулянт с варфарином у пациентов с механическим клапаном Использование дабигатрана в качестве альтернативы варфарна для профилактики тромбоэмболических осложнений у больных с протезирование клапанов сердца (механическим протезом) нецелесообразно
 Hokusai-VTE Эффективность применения новых антикоагулянтов (эноксабан) для лечения венозных тромбоэмболий
Hokusai-VTE Эффективность применения новых антикоагулянтов (эноксабан) для лечения венозных тромбоэмболий
 Hokusai-VTE: сравнение эноксабана с варфарином для лечения симптоматической венозной тромбоэмболии Эноксабан – прямой ингибитор активированного Х фактора с быстрым началом действия способ применения: перорально 1 раз в день Коррекция дозы в зависимости от СКФ
Hokusai-VTE: сравнение эноксабана с варфарином для лечения симптоматической венозной тромбоэмболии Эноксабан – прямой ингибитор активированного Х фактора с быстрым началом действия способ применения: перорально 1 раз в день Коррекция дозы в зависимости от СКФ
 Hokusai-VTE: сравнение эноксабана с варфарином для лечения симптоматической венозной тромбоэмболии Рандомизированное, двойное слепое исследование январь 2010 г. - октябрь 2012 г. Включено 8292 пациента в 439 центрах в 37 странах
Hokusai-VTE: сравнение эноксабана с варфарином для лечения симптоматической венозной тромбоэмболии Рандомизированное, двойное слепое исследование январь 2010 г. - октябрь 2012 г. Включено 8292 пациента в 439 центрах в 37 странах
 Hokusai-VTE: цели исследования Оценить эффективность эноксабана, по сравнению с варфарином, для лечения симптоматической венозной тромбоэмболии Оценить преимущества эноксабана по сравнению с варфарином при лечении венозной тромбоэмболии
Hokusai-VTE: цели исследования Оценить эффективность эноксабана, по сравнению с варфарином, для лечения симптоматической венозной тромбоэмболии Оценить преимущества эноксабана по сравнению с варфарином при лечении венозной тромбоэмболии
 Hakusai-VTE: критерии включения Возраст: старше 18 лет Диагностированный острый, симптоматический тромбоз глубоких вен (подколенной, бедренной или подвздошной) Тромбоэмболия легочной артерии (с или без тромбоза глубоких вен)
Hakusai-VTE: критерии включения Возраст: старше 18 лет Диагностированный острый, симптоматический тромбоз глубоких вен (подколенной, бедренной или подвздошной) Тромбоэмболия легочной артерии (с или без тромбоза глубоких вен)
 Hakusai-VTE: критерии исключения Терапия гепарином более чем 48 часов Терапия варфарином, более чем одной дозы КК менее 30 мл/мин Онкологические заболевания в анамнезе Прием двойной антиагрегантной терапии
Hakusai-VTE: критерии исключения Терапия гепарином более чем 48 часов Терапия варфарином, более чем одной дозы КК менее 30 мл/мин Онкологические заболевания в анамнезе Прием двойной антиагрегантной терапии
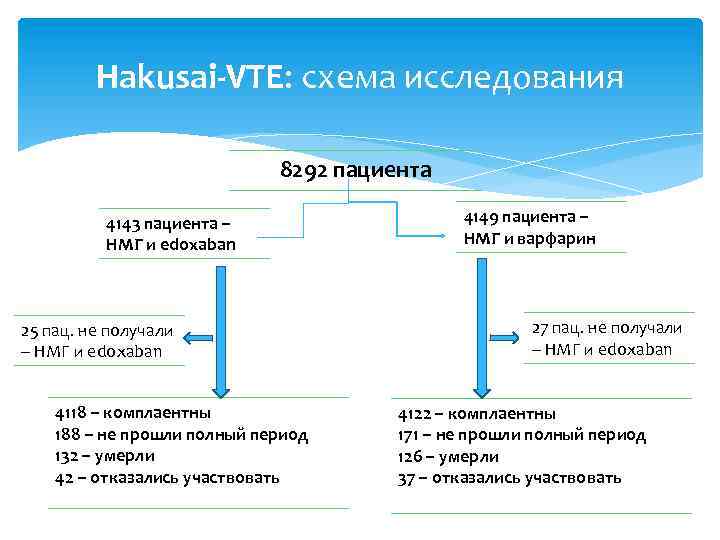 Hakusai-VTE: схема исследования 8292 пациента 4143 пациента – НМГ и edoxaban 25 пац. не получали – НМГ и edoxaban 4118 – комплаентны 188 – не прошли полный период 132 – умерли 42 – отказались участвовать 4149 пациента – НМГ и варфарин 27 пац. не получали – НМГ и edoxaban 4122 – комплаентны 171 – не прошли полный период 126 – умерли 37 – отказались участвовать
Hakusai-VTE: схема исследования 8292 пациента 4143 пациента – НМГ и edoxaban 25 пац. не получали – НМГ и edoxaban 4118 – комплаентны 188 – не прошли полный период 132 – умерли 42 – отказались участвовать 4149 пациента – НМГ и варфарин 27 пац. не получали – НМГ и edoxaban 4122 – комплаентны 171 – не прошли полный период 126 – умерли 37 – отказались участвовать
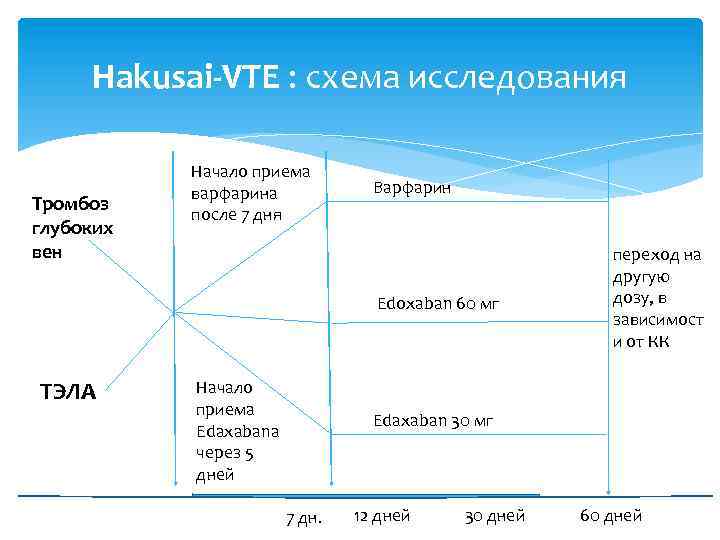 Hakusai-VTE : схема исследования Тромбоз глубоких вен Начало приема варфарина после 7 дня Варфарин Edoxaban 60 мг ТЭЛА Начало приема Edaxabana через 5 дней переход на другую дозу, в зависимост и от КК Edaxaban 30 мг 7 дн. 12 дней 30 дней 60 дней
Hakusai-VTE : схема исследования Тромбоз глубоких вен Начало приема варфарина после 7 дня Варфарин Edoxaban 60 мг ТЭЛА Начало приема Edaxabana через 5 дней переход на другую дозу, в зависимост и от КК Edaxaban 30 мг 7 дн. 12 дней 30 дней 60 дней
 Терапию продолжали в течение 12 месяцев 40% пациентов Больше 3 месяцев, но меньше 6 месяцев – 26% 3 месяца – 12% Больше 6 месяцев – 22% Среди пациентов, принимающих варфарин: TTR (в терапевтическом диапазоне) – 63, 5% МНО выше 3, 0 – 17, 6% МНО ниже 2, 0 – 18, 9%
Терапию продолжали в течение 12 месяцев 40% пациентов Больше 3 месяцев, но меньше 6 месяцев – 26% 3 месяца – 12% Больше 6 месяцев – 22% Среди пациентов, принимающих варфарин: TTR (в терапевтическом диапазоне) – 63, 5% МНО выше 3, 0 – 17, 6% МНО ниже 2, 0 – 18, 9%
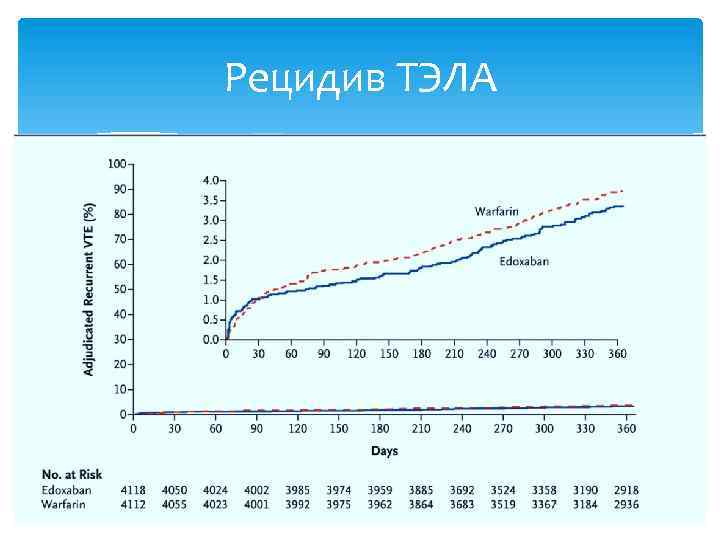 Рецидив ТЭЛА
Рецидив ТЭЛА
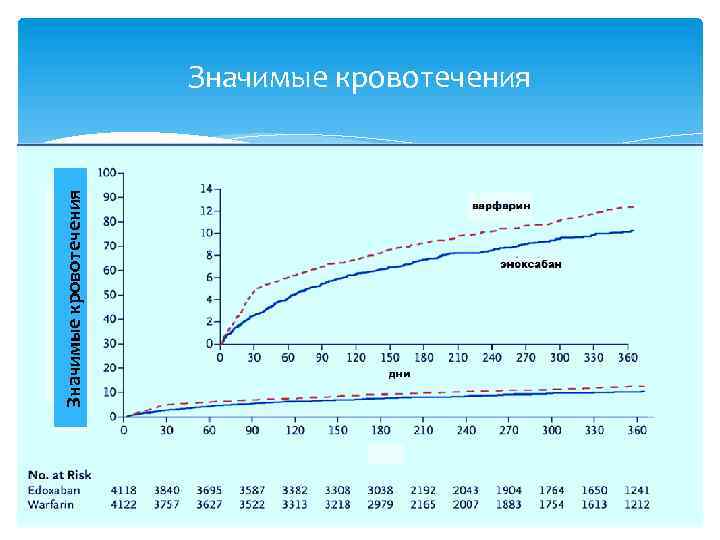 Значимые кровотечения
Значимые кровотечения
 Заключение Терапия эдоксабаном не хуже, чем терапия варфарином, для лечения больных с симптоматической венозной тромбоэмболией Лечение симптоматической венозной тромбоэмболии эдоксабаном более безопасно по сравнению с варфарином, так как вызывает меньшее количество кровотечений
Заключение Терапия эдоксабаном не хуже, чем терапия варфарином, для лечения больных с симптоматической венозной тромбоэмболией Лечение симптоматической венозной тромбоэмболии эдоксабаном более безопасно по сравнению с варфарином, так как вызывает меньшее количество кровотечений
 PEITHO Эффективность и безопасность тромболизиса (тенектеплазой) при лечении ТЭЛА, по сравнению с стандартной антикоагулянтной терапией
PEITHO Эффективность и безопасность тромболизиса (тенектеплазой) при лечении ТЭЛА, по сравнению с стандартной антикоагулянтной терапией
 PEITHO: Рандомизированное, двойное слепое, плацебоконтролируемое исследование Сроки проведения исследования: ноябрь 2007 г. по июль 2014 г. 3 фаза исследования
PEITHO: Рандомизированное, двойное слепое, плацебоконтролируемое исследование Сроки проведения исследования: ноябрь 2007 г. по июль 2014 г. 3 фаза исследования
 PEITHO: цель исследования Оценка эффективности тромболизиса (тенектеплаза), по сравнению с плацебо у пациентов с ТЭЛА Оценить безопасность тромболизиса (тенектеплазой) при лечении ТЭЛА
PEITHO: цель исследования Оценка эффективности тромболизиса (тенектеплаза), по сравнению с плацебо у пациентов с ТЭЛА Оценить безопасность тромболизиса (тенектеплазой) при лечении ТЭЛА
 PEITHO: критерии включения Возраст 18 лет и старше ТЭЛА (проявление первых симптомов не более 15 дней до рандомизации, диагностика с помощью МСКТ легких или ангиопульмонографии) Дисфункция правого желудочка (подтверждающееся Эхо. КГ или МСКТ грудной клетки, положительный тропониновый тест I или Т)
PEITHO: критерии включения Возраст 18 лет и старше ТЭЛА (проявление первых симптомов не более 15 дней до рандомизации, диагностика с помощью МСКТ легких или ангиопульмонографии) Дисфункция правого желудочка (подтверждающееся Эхо. КГ или МСКТ грудной клетки, положительный тропониновый тест I или Т)
 PEITHO: критерии исключения Высокий риск кровотечений Использование тромболитических препаратов в течение последних 4 дней Имплантация кава-фильтра или тромбоэктомия в течение предыдущих 4 суток Неконтролируемое АД Гиперчувствительность к тенектеплазе, альтеплазе или НМГ Нарушения коагуляции
PEITHO: критерии исключения Высокий риск кровотечений Использование тромболитических препаратов в течение последних 4 дней Имплантация кава-фильтра или тромбоэктомия в течение предыдущих 4 суток Неконтролируемое АД Гиперчувствительность к тенектеплазе, альтеплазе или НМГ Нарушения коагуляции
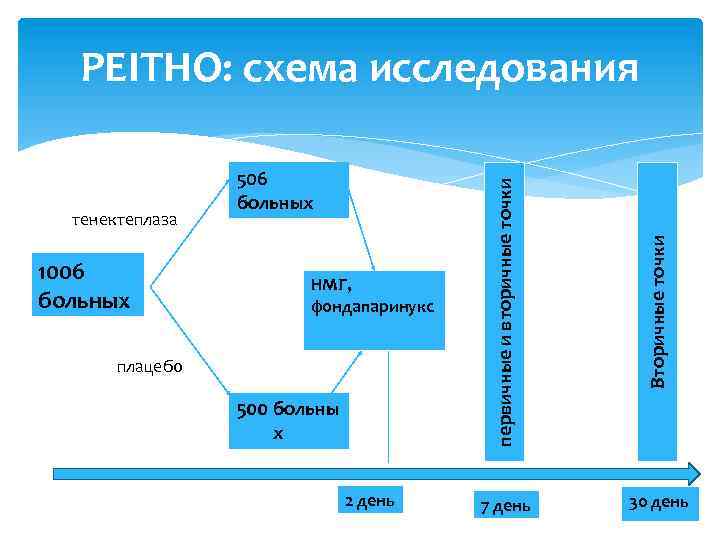 1006 больных НМГ, фондапаринукс плацебо 500 больны х 2 день Вторичные точки тенектеплаза 506 больных первичные и вторичные точки PEITHO: схема исследования 7 день 30 день
1006 больных НМГ, фондапаринукс плацебо 500 больны х 2 день Вторичные точки тенектеплаза 506 больных первичные и вторичные точки PEITHO: схема исследования 7 день 30 день
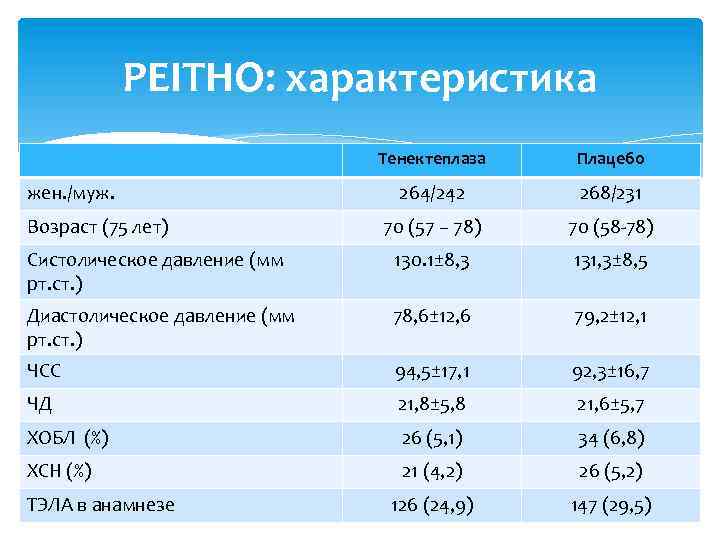 PEITHO: характеристика Тенектеплаза Плацебо 264/242 268/231 70 (57 – 78) 70 (58 -78) Систолическое давление (мм рт. ст. ) 130. 1± 8, 3 131, 3± 8, 5 Диастолическое давление (мм рт. ст. ) 78, 6± 12, 6 79, 2± 12, 1 ЧСС 94, 5± 17, 1 92, 3± 16, 7 ЧД 21, 8± 5, 8 21, 6± 5, 7 ХОБЛ (%) 26 (5, 1) 34 (6, 8) ХСН (%) 21 (4, 2) 26 (5, 2) 126 (24, 9) 147 (29, 5) жен. /муж. Возраст (75 лет) ТЭЛА в анамнезе
PEITHO: характеристика Тенектеплаза Плацебо 264/242 268/231 70 (57 – 78) 70 (58 -78) Систолическое давление (мм рт. ст. ) 130. 1± 8, 3 131, 3± 8, 5 Диастолическое давление (мм рт. ст. ) 78, 6± 12, 6 79, 2± 12, 1 ЧСС 94, 5± 17, 1 92, 3± 16, 7 ЧД 21, 8± 5, 8 21, 6± 5, 7 ХОБЛ (%) 26 (5, 1) 34 (6, 8) ХСН (%) 21 (4, 2) 26 (5, 2) 126 (24, 9) 147 (29, 5) жен. /муж. Возраст (75 лет) ТЭЛА в анамнезе
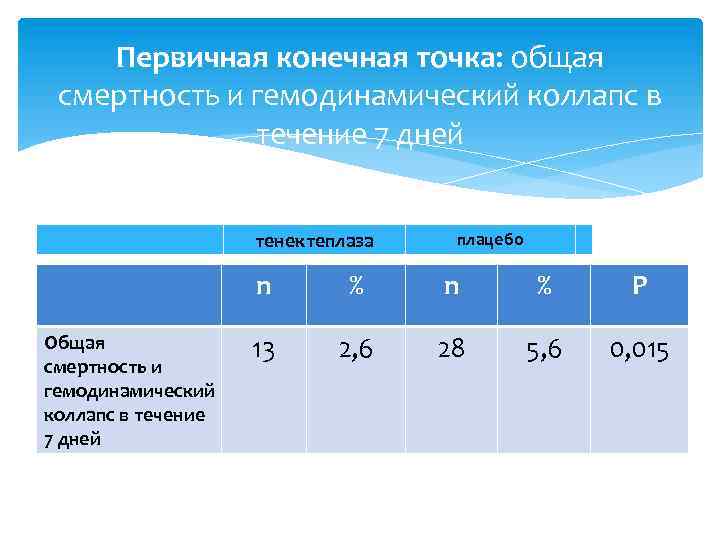 Первичная конечная точка: общая смертность и гемодинамический коллапс в течение 7 дней тенектеплаза плацебо n Общая смертность и гемодинамический коллапс в течение 7 дней % n % P 13 2, 6 28 5, 6 0, 015
Первичная конечная точка: общая смертность и гемодинамический коллапс в течение 7 дней тенектеплаза плацебо n Общая смертность и гемодинамический коллапс в течение 7 дней % n % P 13 2, 6 28 5, 6 0, 015
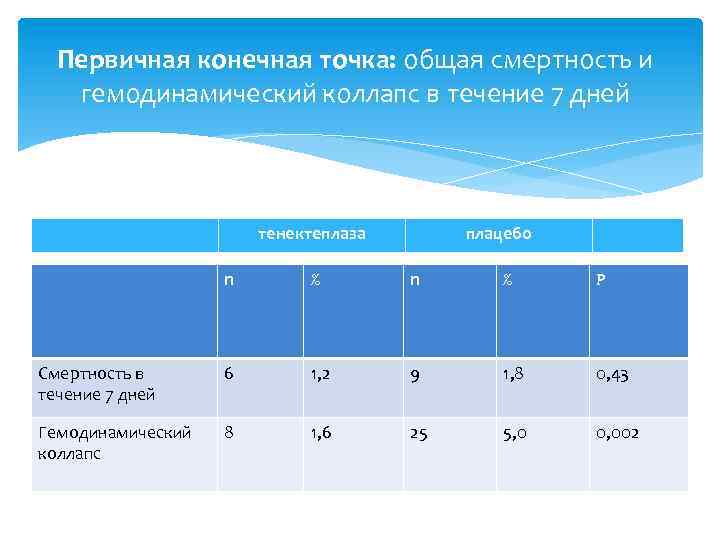 Первичная конечная точка: общая смертность и гемодинамический коллапс в течение 7 дней тенектеплаза плацебо n % Р Смертность в течение 7 дней 6 1, 2 9 1, 8 0, 43 Гемодинамический коллапс 8 1, 6 25 5, 0 0, 002
Первичная конечная точка: общая смертность и гемодинамический коллапс в течение 7 дней тенектеплаза плацебо n % Р Смертность в течение 7 дней 6 1, 2 9 1, 8 0, 43 Гемодинамический коллапс 8 1, 6 25 5, 0 0, 002
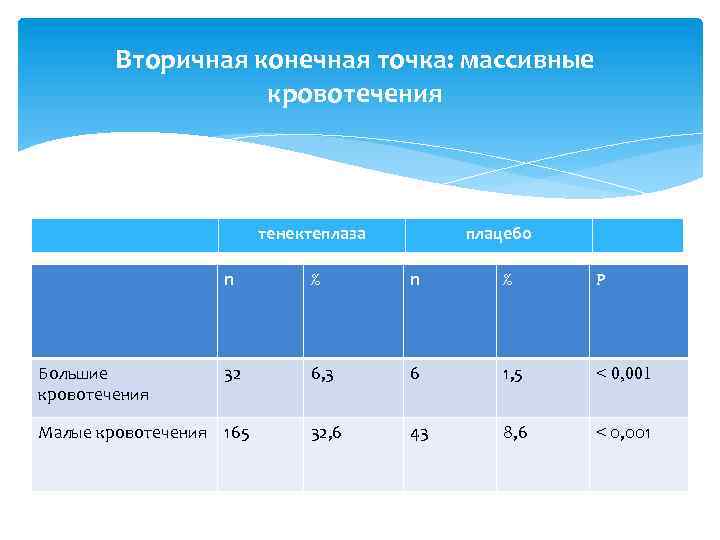 Вторичная конечная точка: массивные кровотечения тенектеплаза плацебо n Большие кровотечения % n % Р 32 6, 3 6 1, 5 ˂ 0, 001 32, 6 43 8, 6 ˂ 0, 001 Малые кровотечения 165
Вторичная конечная точка: массивные кровотечения тенектеплаза плацебо n Большие кровотечения % n % Р 32 6, 3 6 1, 5 ˂ 0, 001 32, 6 43 8, 6 ˂ 0, 001 Малые кровотечения 165
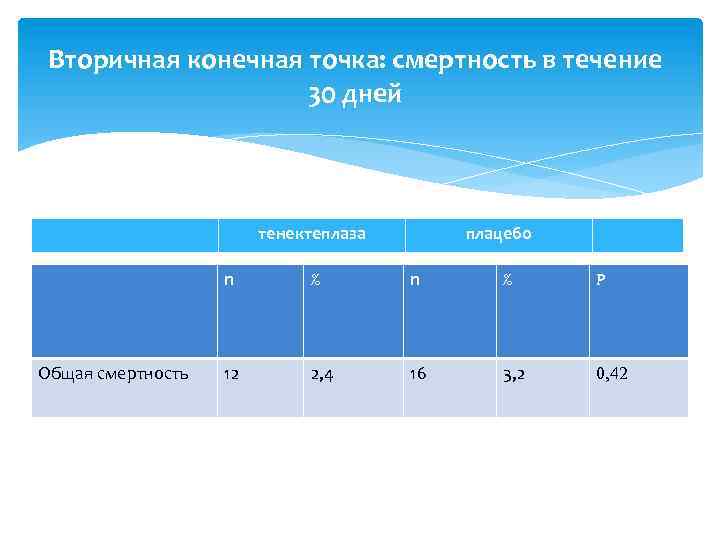 Вторичная конечная точка: смертность в течение 30 дней тенектеплаза плацебо n Общая смертность % n % Р 12 2, 4 16 3, 2 0, 42
Вторичная конечная точка: смертность в течение 30 дней тенектеплаза плацебо n Общая смертность % n % Р 12 2, 4 16 3, 2 0, 42
 Заключение: У пациентов со средним риском ТЭЛА тромболизис тенектеплазой эффективней плацебо Кровотечений в группе тенектеплазы больше
Заключение: У пациентов со средним риском ТЭЛА тромболизис тенектеплазой эффективней плацебо Кровотечений в группе тенектеплазы больше
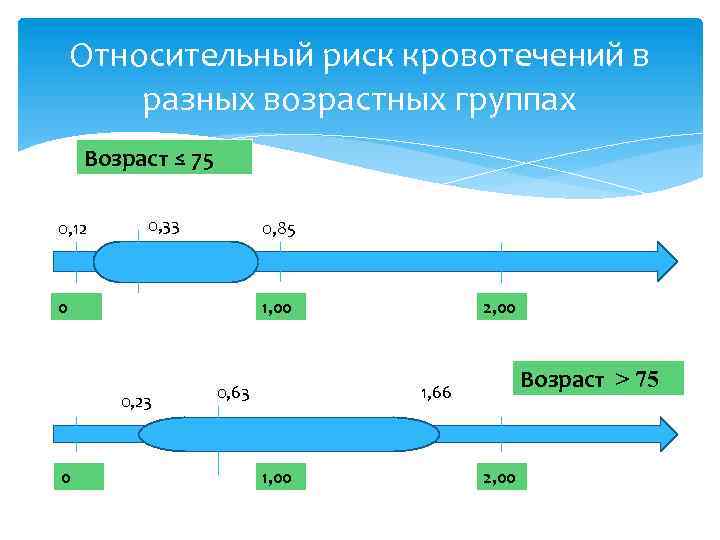 Относительный риск кровотечений в разных возрастных группах Возраст ≤ 75 0, 12 0, 33 0, 85 0 1, 00 0, 23 0 0, 63 2, 00 Возраст > 75 1, 66 1, 00 2, 00
Относительный риск кровотечений в разных возрастных группах Возраст ≤ 75 0, 12 0, 33 0, 85 0 1, 00 0, 23 0 0, 63 2, 00 Возраст > 75 1, 66 1, 00 2, 00
 Спасибо за внимание!
Спасибо за внимание!


