Лекция по стволовым клеткам 12 12 11.ppt
- Количество слайдов: 133


 Ernst Heinrich Philipp August Haeckel (1834 – 1919) 1868, 1871, 1877 – издания книги по эволюции многоклеточных Stemmbäume – эволюционные деревья Stammzelle – одноклеточный предок многоклеточных организмов
Ernst Heinrich Philipp August Haeckel (1834 – 1919) 1868, 1871, 1877 – издания книги по эволюции многоклеточных Stemmbäume – эволюционные деревья Stammzelle – одноклеточный предок многоклеточных организмов
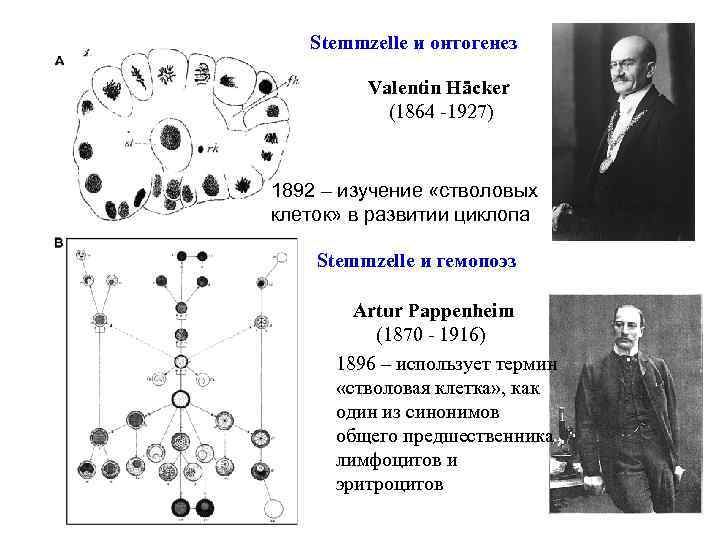 Stemmzelle и онтогенез Valentin Häcker (1864 -1927) 1892 – изучение «стволовых клеток» в развитии циклопа Stemmzelle и гемопоэз Artur Pappenheim (1870 - 1916) 1896 – использует термин «стволовая клетка» , как один из синонимов общего предшественника лимфоцитов и эритроцитов
Stemmzelle и онтогенез Valentin Häcker (1864 -1927) 1892 – изучение «стволовых клеток» в развитии циклопа Stemmzelle и гемопоэз Artur Pappenheim (1870 - 1916) 1896 – использует термин «стволовая клетка» , как один из синонимов общего предшественника лимфоцитов и эритроцитов
 Edmund Beecher Wilson (1856 – 1939) 1896 перевел термин «стволовая клетка» на английский язык
Edmund Beecher Wilson (1856 – 1939) 1896 перевел термин «стволовая клетка» на английский язык
 Stemmzelle и гемопоэз Клетка – предшественник лимфоцитов и эритроцитов Polyvalent large lymphocytes; lymphoidocytes; hemoblasts – A. Pappenheim True large lymphocytes – A. A. Maximow Nongranular undifferentiated lymphocytes – W. Dantschakoff Primery wandering cells – F. Saxer Hemato- or hemogones – S. Mollier, A. Pappenheim Hematocytoblasts – L. Zoja Стволовая клетка Aleksander Maximow 1908; Wera Dantschakoff 1908; Ernst Nuemann 1912
Stemmzelle и гемопоэз Клетка – предшественник лимфоцитов и эритроцитов Polyvalent large lymphocytes; lymphoidocytes; hemoblasts – A. Pappenheim True large lymphocytes – A. A. Maximow Nongranular undifferentiated lymphocytes – W. Dantschakoff Primery wandering cells – F. Saxer Hemato- or hemogones – S. Mollier, A. Pappenheim Hematocytoblasts – L. Zoja Стволовая клетка Aleksander Maximow 1908; Wera Dantschakoff 1908; Ernst Nuemann 1912
 Александрович Максимов (22 января (3 февраля) 1874, Санкт-Петербург – 4 декабря 1928, Чикаго) Активное внедрял метод тканевых культур в России, экспериментальнонаучно обосновал унитарную теорию кроветворения, ввел в науку понятие о стволовых клетках. Вот лишь немногие заслуги А. А. Максимова, на основе которых разрабатывается современная клеточная биология и регенеративная медицина не только в России, но и во всём мире.
Александрович Максимов (22 января (3 февраля) 1874, Санкт-Петербург – 4 декабря 1928, Чикаго) Активное внедрял метод тканевых культур в России, экспериментальнонаучно обосновал унитарную теорию кроветворения, ввел в науку понятие о стволовых клетках. Вот лишь немногие заслуги А. А. Максимова, на основе которых разрабатывается современная клеточная биология и регенеративная медицина не только в России, но и во всём мире.
 Первые экспериментальные доказательства существования стволовых клеток A direct measurement of the radiation sensitivity of normal mouse bone marrow cells. Till, J. E. , & Mc. Culloch, E. A. Radiation Res. 14, 213 -222 (1961) Cytological demonstration of the clonal nature of spleen colonies derived from transplanted mouse marrow cells. Becker, A. J. , Mc. Culloch, E. A. & Till, J. E. Nature 197, 452 -454 (1963) В начале 60 -х Э. Мак. Куллоч и Ж. Тилл обнаружили в костном мозге мыши самообновляемые клетки. В дальнейшем научные поиски в этом направлении привели в 1968 году к успешной трансплантации костного мозга, которая была выполнена доктором Робертом Гудом от здорового донорабрата к тяжело больному 5 -месячнему мальчику (брату-реципиенту) с тяжелым комбинированным иммунодефицитом. Robert Alan Good (May 21, 1922 – June 13, 2003)
Первые экспериментальные доказательства существования стволовых клеток A direct measurement of the radiation sensitivity of normal mouse bone marrow cells. Till, J. E. , & Mc. Culloch, E. A. Radiation Res. 14, 213 -222 (1961) Cytological demonstration of the clonal nature of spleen colonies derived from transplanted mouse marrow cells. Becker, A. J. , Mc. Culloch, E. A. & Till, J. E. Nature 197, 452 -454 (1963) В начале 60 -х Э. Мак. Куллоч и Ж. Тилл обнаружили в костном мозге мыши самообновляемые клетки. В дальнейшем научные поиски в этом направлении привели в 1968 году к успешной трансплантации костного мозга, которая была выполнена доктором Робертом Гудом от здорового донорабрата к тяжело больному 5 -месячнему мальчику (брату-реципиенту) с тяжелым комбинированным иммунодефицитом. Robert Alan Good (May 21, 1922 – June 13, 2003)

 Клод Бернар (12. 07. 1813 года, Сен. Жюльен – 10. 02. 1878 года, Париж) Французский физиолог и патолог, один из основоположников экспериментальной медицины и эндокринологии. Труды по иннервации сосудов, эндокринных желез, углеводному обмену, электрофизиологии. Ввел понятие о внутренней среде организма и концепцию гомеостаза.
Клод Бернар (12. 07. 1813 года, Сен. Жюльен – 10. 02. 1878 года, Париж) Французский физиолог и патолог, один из основоположников экспериментальной медицины и эндокринологии. Труды по иннервации сосудов, эндокринных желез, углеводному обмену, электрофизиологии. Ввел понятие о внутренней среде организма и концепцию гомеостаза.
 Вильгельм Ру (9. 06. 1850, Йена – 15. 09. 1924, Галле) Установил принцип культивирования тканей, извлек часть костного мозга из куриного эмбриона и держал его в теплом физрастворе в течение нескольких дней
Вильгельм Ру (9. 06. 1850, Йена – 15. 09. 1924, Галле) Установил принцип культивирования тканей, извлек часть костного мозга из куриного эмбриона и держал его в теплом физрастворе в течение нескольких дней
 Лео Лёб (21. 09. 1869, Майен, Пруссия - 28. 12. 1959, St. Louis, США) В 1897 г поддерживал в жизнеспособном состоянии клетки крови и соединительной ткани в пробирках с сывороткой и плазмой крови
Лео Лёб (21. 09. 1869, Майен, Пруссия - 28. 12. 1959, St. Louis, США) В 1897 г поддерживал в жизнеспособном состоянии клетки крови и соединительной ткани в пробирках с сывороткой и плазмой крови
 Росс Гаррисон (13. 01. 1870, Джермантаун, - 30. 09. 1959, Нью. Хейвен, штат Коннектикут) Одним из первых предложил метод культивирования изолированных тканей и впервые наблюдал рост нервного волокна вне организма.
Росс Гаррисон (13. 01. 1870, Джермантаун, - 30. 09. 1959, Нью. Хейвен, штат Коннектикут) Одним из первых предложил метод культивирования изолированных тканей и впервые наблюдал рост нервного волокна вне организма.
 Развитие методов культивирования in vitro ( конец 19 столетия – середина 20 столетия) Поддержание жизнеспособности тканей и клеток вне организма Арнольд – 1887 г. - наблюдение за поведением лейкоцитов лягушки 4 -5 дней в лимфе. Гаррисон – 1906 -1907 гг. - живые нервные клетки в лимфе лягушки Каррель – 1912 - 1917 гг. - ткани птиц и млекопиающих в плазме крови и с добавлением эмбриональных экстрактов Фишер – 1941 г. - диализованная плазма крови с добавлением разнообразных стимулирующих рост молекул Игл – 1955 г. - Первая синтетическая питательная среда
Развитие методов культивирования in vitro ( конец 19 столетия – середина 20 столетия) Поддержание жизнеспособности тканей и клеток вне организма Арнольд – 1887 г. - наблюдение за поведением лейкоцитов лягушки 4 -5 дней в лимфе. Гаррисон – 1906 -1907 гг. - живые нервные клетки в лимфе лягушки Каррель – 1912 - 1917 гг. - ткани птиц и млекопиающих в плазме крови и с добавлением эмбриональных экстрактов Фишер – 1941 г. - диализованная плазма крови с добавлением разнообразных стимулирующих рост молекул Игл – 1955 г. - Первая синтетическая питательная среда
 Получение клеточных линий и начало их широкого использования (40 -90 годы 20 столетия) для решения фундаментальных и прикладных проблем Ø Создание приборного обеспечения культивирования клеток Ø Постоянные клеточные линии Ø Создание и развитие коллекций клеточных культур Ø Исследования молекулярных механизмов регуляции клеточных функций Ø Разработки клеточных биотехнологий
Получение клеточных линий и начало их широкого использования (40 -90 годы 20 столетия) для решения фундаментальных и прикладных проблем Ø Создание приборного обеспечения культивирования клеток Ø Постоянные клеточные линии Ø Создание и развитие коллекций клеточных культур Ø Исследования молекулярных механизмов регуляции клеточных функций Ø Разработки клеточных биотехнологий
 Клеточная терапия и тканевая инженерия (конец 20 столетия по настоящее время) Ø Культивирование стволовых и прогениторных клеток Ø Заместительная клеточная терапия Ø Тканевая инженерия Ø Регенеративная медицина
Клеточная терапия и тканевая инженерия (конец 20 столетия по настоящее время) Ø Культивирование стволовых и прогениторных клеток Ø Заместительная клеточная терапия Ø Тканевая инженерия Ø Регенеративная медицина

 Культуральная лаборатории по работе с клеточным материалом
Культуральная лаборатории по работе с клеточным материалом
 Расходные материалы для культивирования клеток Сыворотки Среды Культуральный пластик Лабораторный пластик
Расходные материалы для культивирования клеток Сыворотки Среды Культуральный пластик Лабораторный пластик
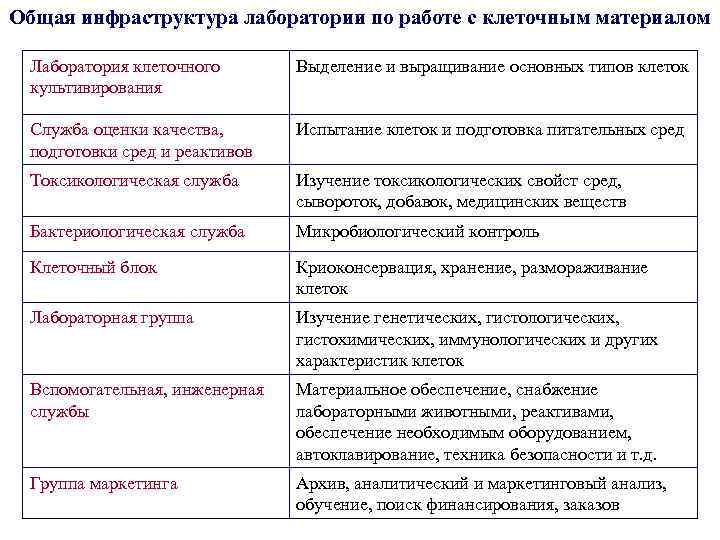 Общая инфраструктура лаборатории по работе с клеточным материалом Лаборатория клеточного культивирования Выделение и выращивание основных типов клеток Служба оценки качества, подготовки сред и реактивов Испытание клеток и подготовка питательных сред Токсикологическая служба Изучение токсикологических свойст сред, сывороток, добавок, медицинских веществ Бактериологическая служба Микробиологический контроль Клеточный блок Криоконсервация, хранение, размораживание клеток Лабораторная группа Изучение генетических, гистологических, гистохимических, иммунологических и других характеристик клеток Вспомогательная, инженерная службы Материальное обеспечение, снабжение лабораторными животными, реактивами, обеспечение необходимым оборудованием, автоклавирование, техника безопасности и т. д. Группа маркетинга Архив, аналитический и маркетинговый анализ, обучение, поиск финансирования, заказов
Общая инфраструктура лаборатории по работе с клеточным материалом Лаборатория клеточного культивирования Выделение и выращивание основных типов клеток Служба оценки качества, подготовки сред и реактивов Испытание клеток и подготовка питательных сред Токсикологическая служба Изучение токсикологических свойст сред, сывороток, добавок, медицинских веществ Бактериологическая служба Микробиологический контроль Клеточный блок Криоконсервация, хранение, размораживание клеток Лабораторная группа Изучение генетических, гистологических, гистохимических, иммунологических и других характеристик клеток Вспомогательная, инженерная службы Материальное обеспечение, снабжение лабораторными животными, реактивами, обеспечение необходимым оборудованием, автоклавирование, техника безопасности и т. д. Группа маркетинга Архив, аналитический и маркетинговый анализ, обучение, поиск финансирования, заказов
 1. Выделение 2. Сортировка 3. Культивирование • микробиологический и токсикологический контроль • размножение • стимуляция дифференцировки 4. Характеристика полученных культур 5. Криоконсервация 6. Трансплантация в поврежденную ткань
1. Выделение 2. Сортировка 3. Культивирование • микробиологический и токсикологический контроль • размножение • стимуляция дифференцировки 4. Характеристика полученных культур 5. Криоконсервация 6. Трансплантация в поврежденную ткань
 GMP (Good Manufacturing Practice) «Правила организации производства и контроля качества лекарственных средств (GMP)» 1998 «Правила производства и контроля качества лекарственных средств» 2000 г. (приказ Минздрава России и Минэкономики России о введении в действие стандарта отрасли ОСТ 42 -510 -98, ГОСТ Р 52249 -2009) GLP (Good Laboratory Practice) 1976 -1979 гг. «Правила доклинической оценки безопасности фармакологических средств (GLP)» 1991 г. (приказ министерства медицинской промышленности СССР за № 154 от 17. 05. 91, 3 В 64126 -91) «Правила лабораторной практики в Российской Федерации (GLP)» 2003 г. (приказ МЗ РФ от 19. 06. 2003 № 267 )
GMP (Good Manufacturing Practice) «Правила организации производства и контроля качества лекарственных средств (GMP)» 1998 «Правила производства и контроля качества лекарственных средств» 2000 г. (приказ Минздрава России и Минэкономики России о введении в действие стандарта отрасли ОСТ 42 -510 -98, ГОСТ Р 52249 -2009) GLP (Good Laboratory Practice) 1976 -1979 гг. «Правила доклинической оценки безопасности фармакологических средств (GLP)» 1991 г. (приказ министерства медицинской промышленности СССР за № 154 от 17. 05. 91, 3 В 64126 -91) «Правила лабораторной практики в Российской Федерации (GLP)» 2003 г. (приказ МЗ РФ от 19. 06. 2003 № 267 )
 Good Manufacturing Practice (GMP) Надлежащая производственная практика (1963 – наст. вр) • Первые официальные требования в США, 1963 год • В настоящее время более 40 стран имеют национальные требования по GMP • 1967 -1971 гг вопросы организации производства медикаментов (WHO) • Директивы ЕС о соответствии производств требованиям GMP
Good Manufacturing Practice (GMP) Надлежащая производственная практика (1963 – наст. вр) • Первые официальные требования в США, 1963 год • В настоящее время более 40 стран имеют национальные требования по GMP • 1967 -1971 гг вопросы организации производства медикаментов (WHO) • Директивы ЕС о соответствии производств требованиям GMP
 Сроки перехода на GMP • • США – 10 лет Чехия 6 -10 лет Венгрия – 2 года РФ – трижды откладывалось введение стандарта (01. 2014)
Сроки перехода на GMP • • США – 10 лет Чехия 6 -10 лет Венгрия – 2 года РФ – трижды откладывалось введение стандарта (01. 2014)

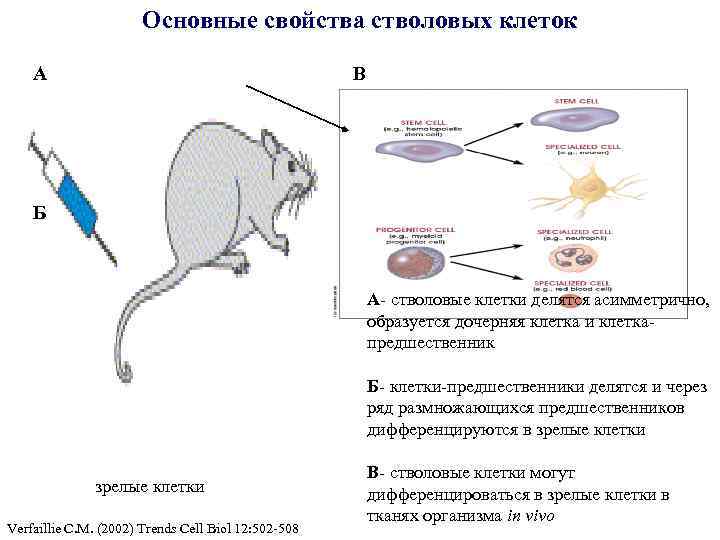 Основные свойства стволовых клеток А В Б А- стволовые клетки делятся асимметрично, образуется дочерняя клетка и клеткапредшественник Б- клетки-предшественники делятся и через ряд размножающихся предшественников дифференцируются в зрелые клетки Verfaillie C. M. (2002) Trends Cell Biol 12: 502 -508 В- стволовые клетки могут дифференцироваться в зрелые клетки в тканях организма in vivo
Основные свойства стволовых клеток А В Б А- стволовые клетки делятся асимметрично, образуется дочерняя клетка и клеткапредшественник Б- клетки-предшественники делятся и через ряд размножающихся предшественников дифференцируются в зрелые клетки Verfaillie C. M. (2002) Trends Cell Biol 12: 502 -508 В- стволовые клетки могут дифференцироваться в зрелые клетки в тканях организма in vivo
 Тканевые стволовые клетки • • Самоподдержание Клональность Асимметричное деление Мультипотентность Менее 1% в ткани Длинный клеточный цикл Редко делятся
Тканевые стволовые клетки • • Самоподдержание Клональность Асимметричное деление Мультипотентность Менее 1% в ткани Длинный клеточный цикл Редко делятся
 Прогениторные клетки-предшественники, потомки стволовых клеток • Нет самоподдержания • • • Не дают клонов Нет асимметричного деления Мультипотентность (±) Короткий клеточный цикл Часто делятся Большое количество пролиферирующих клеток
Прогениторные клетки-предшественники, потомки стволовых клеток • Нет самоподдержания • • • Не дают клонов Нет асимметричного деления Мультипотентность (±) Короткий клеточный цикл Часто делятся Большое количество пролиферирующих клеток
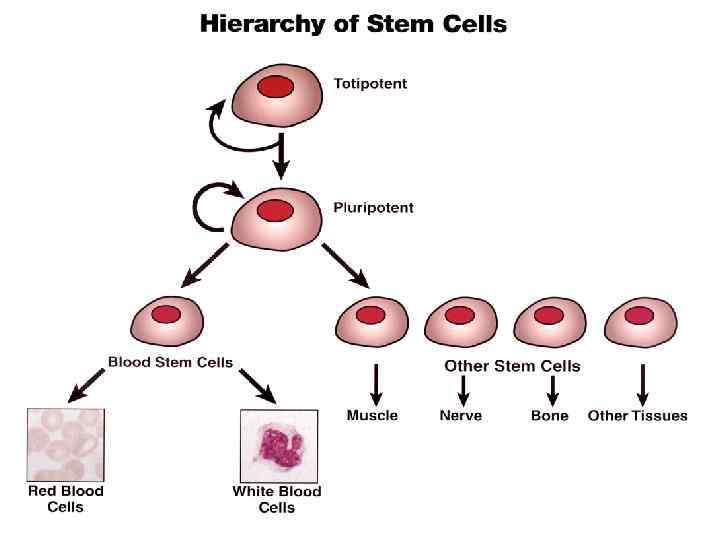
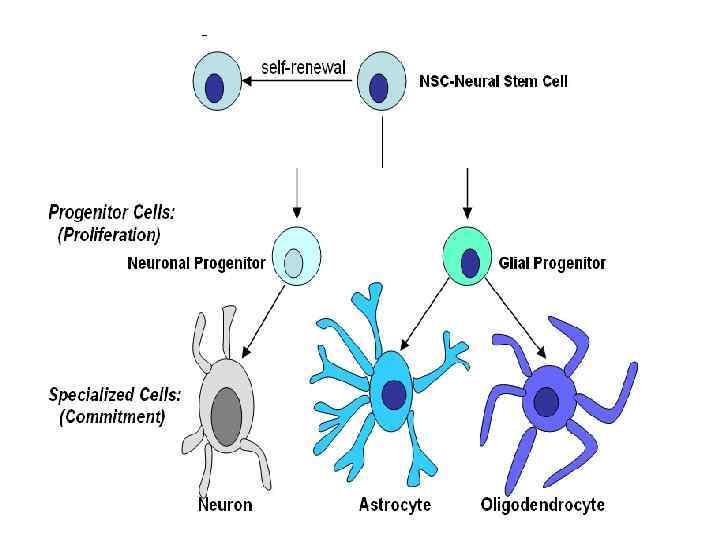
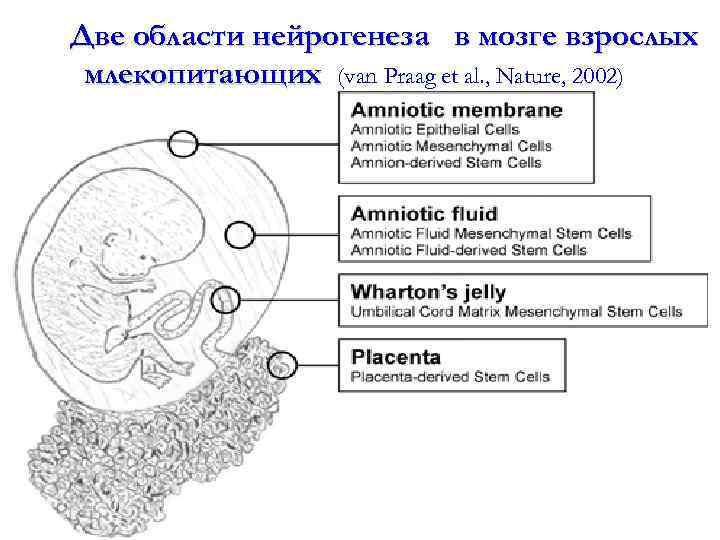 Две области нейрогенеза млекопитающих в мозге взрослых (van Praag et al. , Nature, 2002)
Две области нейрогенеза млекопитающих в мозге взрослых (van Praag et al. , Nature, 2002)
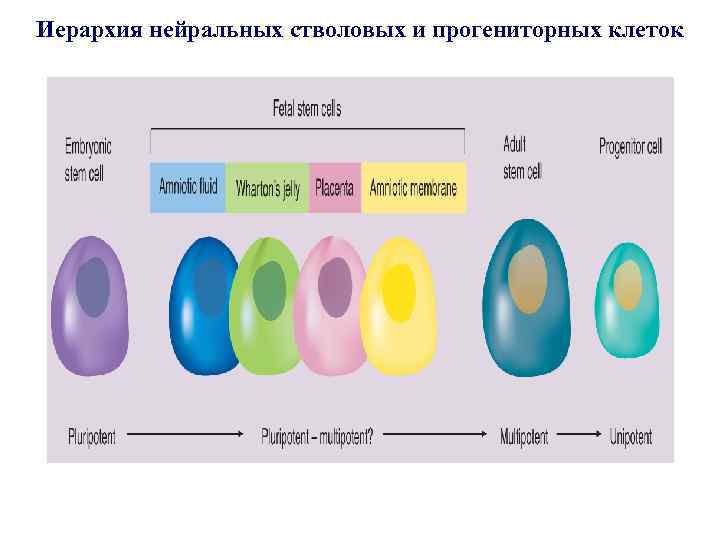 Иерархия нейральных стволовых и прогениторных клеток
Иерархия нейральных стволовых и прогениторных клеток
 Ниша стволовых клеток • Ниша – это группа тканевых клеток и внеклеточный матрикс, которые способны неограниченно долго поддерживать самовоспроизведение стволовых клеток и продукцию дочерних дифференцированных клеток in vivo (Spradling et al. , 2001). • Основная биологическая задача ниши – обеспечение жизнеспособности и самовоспроизведения стволовых клеток в течение длительного времени, в большей части случаев сравнимого с продолжительностью жизни организма.
Ниша стволовых клеток • Ниша – это группа тканевых клеток и внеклеточный матрикс, которые способны неограниченно долго поддерживать самовоспроизведение стволовых клеток и продукцию дочерних дифференцированных клеток in vivo (Spradling et al. , 2001). • Основная биологическая задача ниши – обеспечение жизнеспособности и самовоспроизведения стволовых клеток в течение длительного времени, в большей части случаев сравнимого с продолжительностью жизни организма.
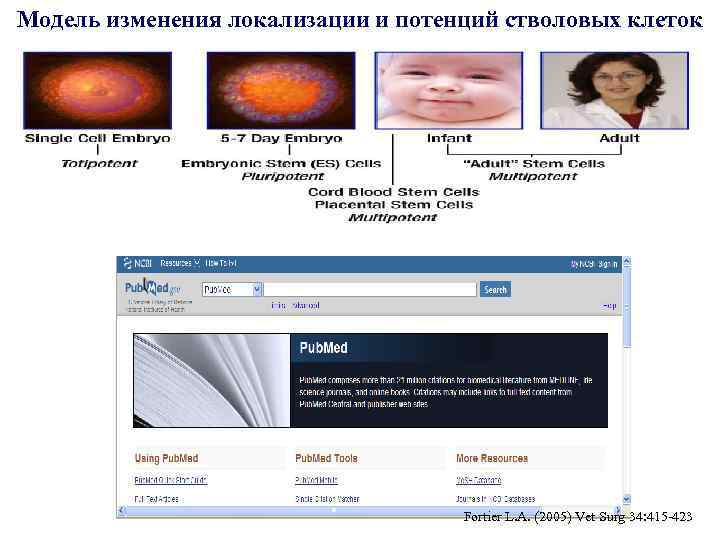 Модель изменения локализации и потенций стволовых клеток Fortier L. A. (2005) Vet Surg 34: 415 -423
Модель изменения локализации и потенций стволовых клеток Fortier L. A. (2005) Vet Surg 34: 415 -423
 Национальный центр биотехнологической информации США National Center for Biotechnological Information, NCBI предоставляет информацию о базах данных белковых доменов, ДНК (Gen. Bank) и РНК, базах данных статей научной литературы (Pub. Med) и таксономичной информации (Tax. Browser), обеспечивает поиск данных о конкретном биологическом виде (Taxonomy). Cодержит стандартные программы биоинформатики (BLAST). http: //www. ncbi. nlm. nih. gov/pubmed/
Национальный центр биотехнологической информации США National Center for Biotechnological Information, NCBI предоставляет информацию о базах данных белковых доменов, ДНК (Gen. Bank) и РНК, базах данных статей научной литературы (Pub. Med) и таксономичной информации (Tax. Browser), обеспечивает поиск данных о конкретном биологическом виде (Taxonomy). Cодержит стандартные программы биоинформатики (BLAST). http: //www. ncbi. nlm. nih. gov/pubmed/
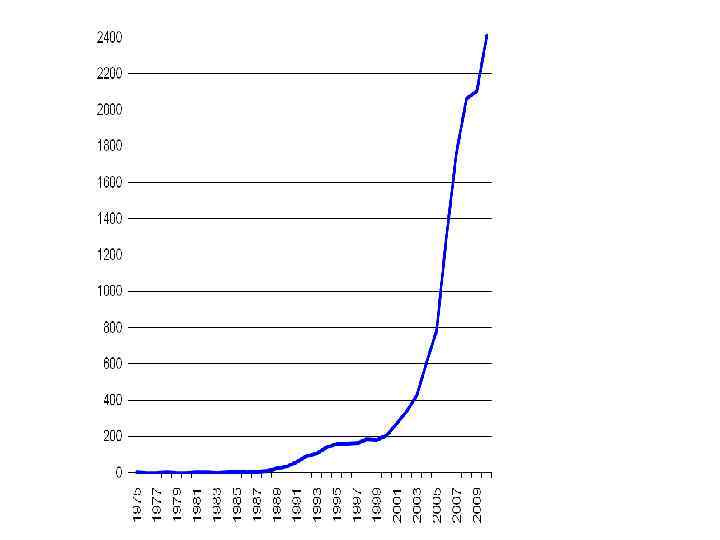
 Количество публикаций со словами «stem cells»
Количество публикаций со словами «stem cells»
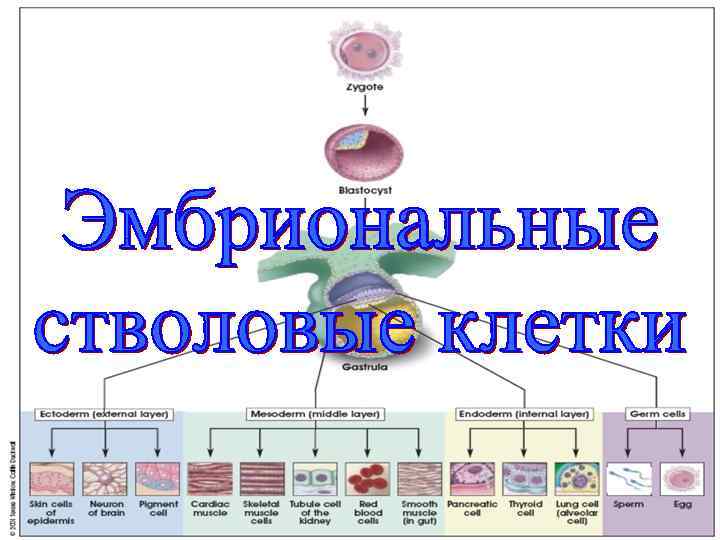
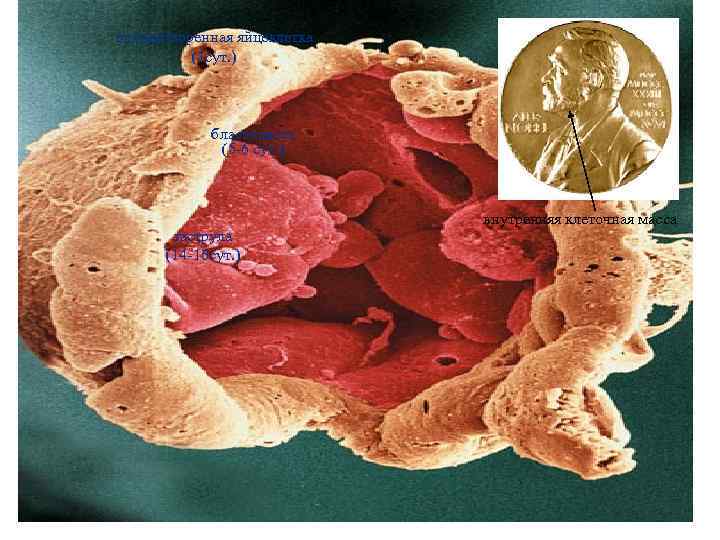 оплодотворенная яйцеклетка (1 сут. ) бластоциста (5 -6 сут. ) гаструла (14 -16 сут. ) внутренняя клеточная масса
оплодотворенная яйцеклетка (1 сут. ) бластоциста (5 -6 сут. ) гаструла (14 -16 сут. ) внутренняя клеточная масса
 1878 – первые попытки оплодотворения яйцеклеток млекопитающих вне организма 1959 – в США впервые методом ЭКО получено животное (кролик) 1960 -е – исследования тератокарцином. Получены клеточные линии 1968 - Edwards и Bavister провели первое оплодотворение яйцеклетки человека in vitro 1970 – получение химерной мыши путем инъекции EC в полость бластоцисты 1978 – родился первый ребенок ЭКО 1981 – Evans и Kaufman и Martin получили ЭСК мыши 1998 - Thomson и другие получили ЭСК человека
1878 – первые попытки оплодотворения яйцеклеток млекопитающих вне организма 1959 – в США впервые методом ЭКО получено животное (кролик) 1960 -е – исследования тератокарцином. Получены клеточные линии 1968 - Edwards и Bavister провели первое оплодотворение яйцеклетки человека in vitro 1970 – получение химерной мыши путем инъекции EC в полость бластоцисты 1978 – родился первый ребенок ЭКО 1981 – Evans и Kaufman и Martin получили ЭСК мыши 1998 - Thomson и другие получили ЭСК человека
 История открытия Мартин Эванс и Мэтью Кауфман Professor Gail R. Martin
История открытия Мартин Эванс и Мэтью Кауфман Professor Gail R. Martin
 Количество публикаций со словами «embryonic stem cells»
Количество публикаций со словами «embryonic stem cells»
 В 2007 году Нобелевская премия по физиологии и медицине за «открытие принципов введения специфических генных модификаций в организм мышей посредством эмбриональных стволовых клеток» , то есть за изобретение метода нокаута генов Марио Капеччи, Оливер Смитис и сэр Мартин Эванс
В 2007 году Нобелевская премия по физиологии и медицине за «открытие принципов введения специфических генных модификаций в организм мышей посредством эмбриональных стволовых клеток» , то есть за изобретение метода нокаута генов Марио Капеччи, Оливер Смитис и сэр Мартин Эванс
 Получение эмбриональных стволовых клеток
Получение эмбриональных стволовых клеток
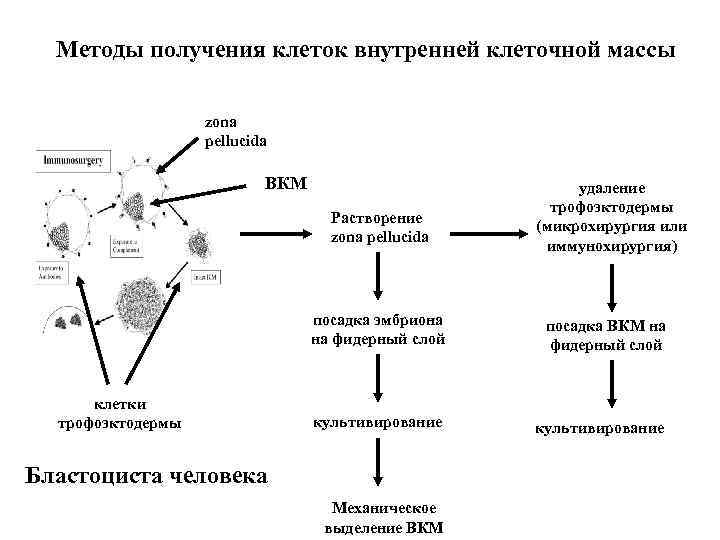 Методы получения клеток внутренней клеточной массы zona pellucida ВКМ Растворение zona pellucida посадка эмбриона на фидерный слой клетки трофоэктодермы культивирование Бластоциста человека Механическое выделение ВКМ удаление трофоэктодермы (микрохирургия или иммунохирургия) посадка ВКМ на фидерный слой культивирование
Методы получения клеток внутренней клеточной массы zona pellucida ВКМ Растворение zona pellucida посадка эмбриона на фидерный слой клетки трофоэктодермы культивирование Бластоциста человека Механическое выделение ВКМ удаление трофоэктодермы (микрохирургия или иммунохирургия) посадка ВКМ на фидерный слой культивирование
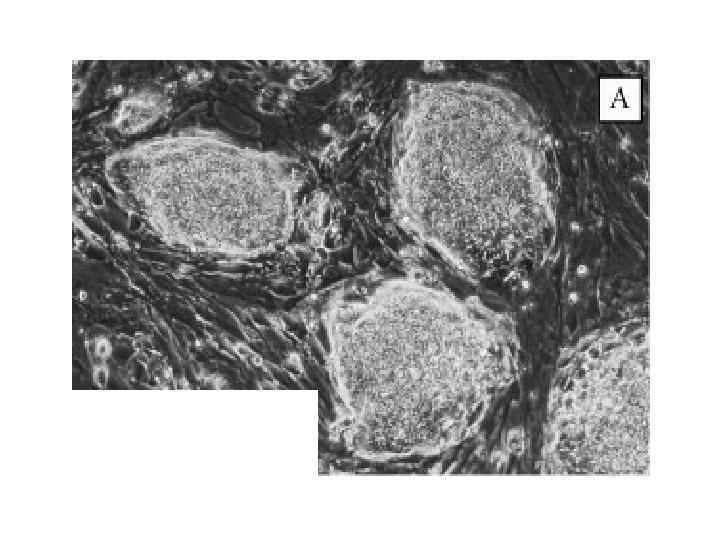
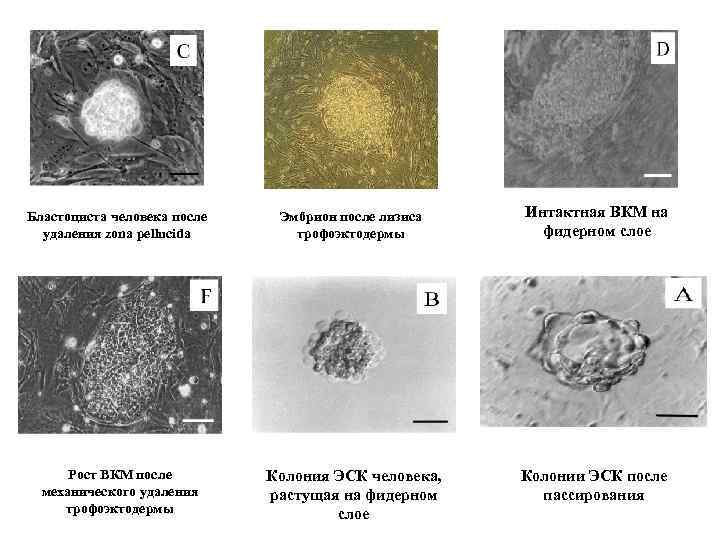 Бластоциста человека после удаления zona pellucida Эмбрион после лизиса трофоэктодермы Интактная ВКМ на фидерном слое Рост ВКМ после механического удаления трофоэктодермы Колония ЭСК человека, растущая на фидерном слое Колонии ЭСК после пассирования
Бластоциста человека после удаления zona pellucida Эмбрион после лизиса трофоэктодермы Интактная ВКМ на фидерном слое Рост ВКМ после механического удаления трофоэктодермы Колония ЭСК человека, растущая на фидерном слое Колонии ЭСК после пассирования
 Клеточные культуры ES Бластоциста
Клеточные культуры ES Бластоциста
 Условия культивирования ЭСК в недифференцированном состоянии: Сорбированная желатином или Матригелем поверхность Фидерный слой клеток мезенхимального происхождения (эмбриональные фибробласты) Leukemia inhibitory factor (LIF) – для ЭСК мыши Basic fibroblast growth factor (b. FGF) – для ЭСК человека
Условия культивирования ЭСК в недифференцированном состоянии: Сорбированная желатином или Матригелем поверхность Фидерный слой клеток мезенхимального происхождения (эмбриональные фибробласты) Leukemia inhibitory factor (LIF) – для ЭСК мыши Basic fibroblast growth factor (b. FGF) – для ЭСК человека
 Параметры, характеризующие линии ЭСК • Фенотип (морфология, экспрессия маркеров) • Плюрипотентность in vitro образование тератом получение химерных животных • Высокие темпы пролиферации • Кариотип и его стабильность
Параметры, характеризующие линии ЭСК • Фенотип (морфология, экспрессия маркеров) • Плюрипотентность in vitro образование тератом получение химерных животных • Высокие темпы пролиферации • Кариотип и его стабильность
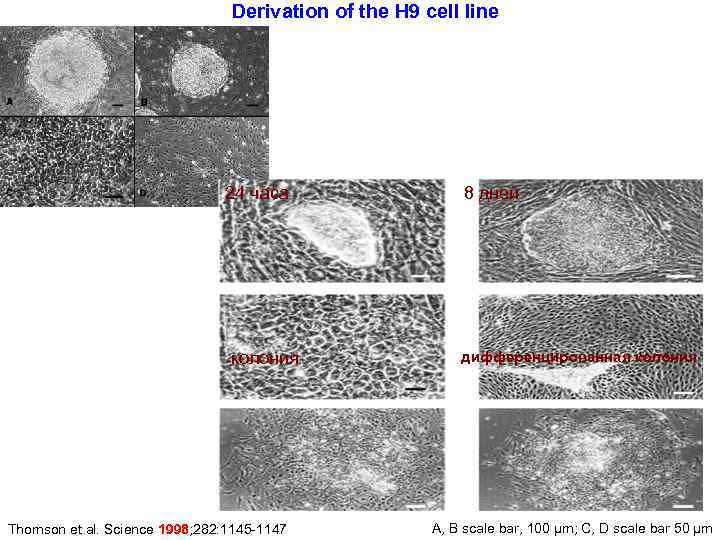 Derivation of the H 9 cell line 24 часа колония Thomson et al. Science 1998; 282: 1145 -1147 8 дней дифференцированная колония A, B scale bar, 100 μm; C, D scale bar 50 μm
Derivation of the H 9 cell line 24 часа колония Thomson et al. Science 1998; 282: 1145 -1147 8 дней дифференцированная колония A, B scale bar, 100 μm; C, D scale bar 50 μm
 Expression of cell surface markers by H 9 cells щелочная фосфатаза SSEA-3 TRA-1 -60 Thomson et al. Science 1998; 282: 1145 -1147 SSEA-1 SSEA-4 TRA-1 -81 Scale bar, 100 μm
Expression of cell surface markers by H 9 cells щелочная фосфатаза SSEA-3 TRA-1 -60 Thomson et al. Science 1998; 282: 1145 -1147 SSEA-1 SSEA-4 TRA-1 -81 Scale bar, 100 μm
 Phase contrast micrographs of human ES cells and their differentiated progeny ВКМ колония ЭСК спонтанная дифференцировка ЭСК нейронаяльные клетки в плотной культуре ЭСК Reubinoff et al. , Nat Biotechnol. 2000, 18
Phase contrast micrographs of human ES cells and their differentiated progeny ВКМ колония ЭСК спонтанная дифференцировка ЭСК нейронаяльные клетки в плотной культуре ЭСК Reubinoff et al. , Nat Biotechnol. 2000, 18
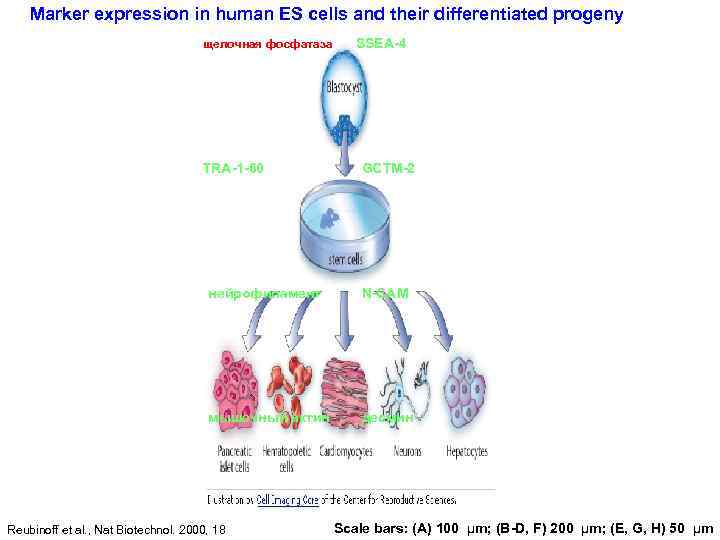 Marker expression in human ES cells and their differentiated progeny щелочная фосфатаза TRA-1 -60 SSEA-4 GCTM-2 нейрофиламент N-CAM мышечный актин десмин Reubinoff et al. , Nat Biotechnol. 2000, 18 Scale bars: (A) 100 μm; (B-D, F) 200 μm; (E, G, H) 50 μm
Marker expression in human ES cells and their differentiated progeny щелочная фосфатаза TRA-1 -60 SSEA-4 GCTM-2 нейрофиламент N-CAM мышечный актин десмин Reubinoff et al. , Nat Biotechnol. 2000, 18 Scale bars: (A) 100 μm; (B-D, F) 200 μm; (E, G, H) 50 μm
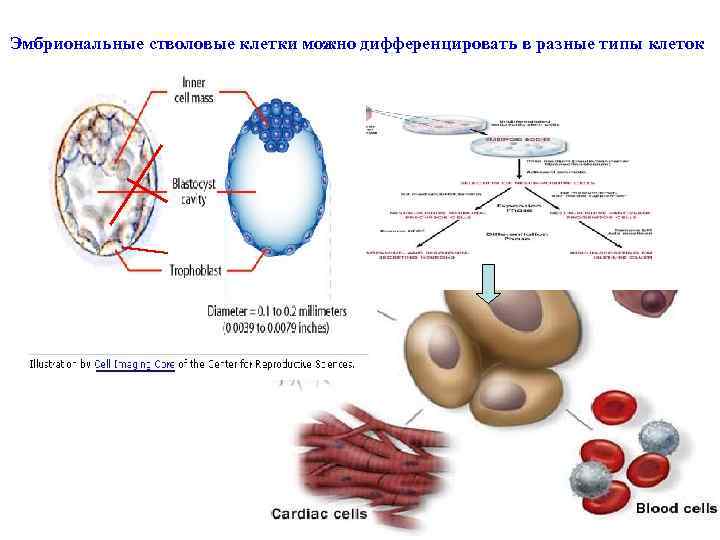 Эмбриональные стволовые клетки можно дифференцировать в разные типы клеток
Эмбриональные стволовые клетки можно дифференцировать в разные типы клеток
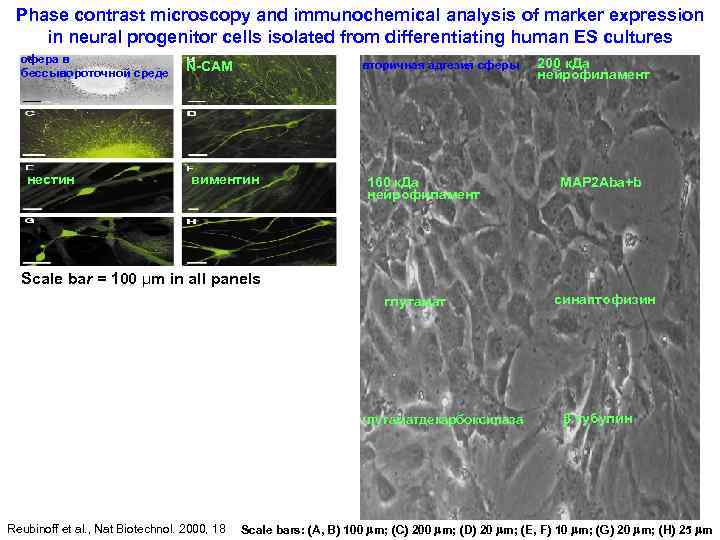 Phase contrast microscopy and immunochemical analysis of marker expression in neural progenitor cells isolated from differentiating human ES cultures сфера в бессывороточной среде нестин N-CAM вторичная адгезия сферы виментин 160 к. Да нейрофиламент 200 к. Да нейрофиламент MAP 2 Aba+b Scale bar = 100 μm in all panels глутаматдекарбоксилаза Reubinoff et al. , Nat Biotechnol. 2000, 18 синаптофизин тубулин Scale bars: (A, B) 100 m; (C) 200 m; (D) 20 m; (E, F) 10 m; (G) 20 m; (H) 25 m
Phase contrast microscopy and immunochemical analysis of marker expression in neural progenitor cells isolated from differentiating human ES cultures сфера в бессывороточной среде нестин N-CAM вторичная адгезия сферы виментин 160 к. Да нейрофиламент 200 к. Да нейрофиламент MAP 2 Aba+b Scale bar = 100 μm in all panels глутаматдекарбоксилаза Reubinoff et al. , Nat Biotechnol. 2000, 18 синаптофизин тубулин Scale bars: (A, B) 100 m; (C) 200 m; (D) 20 m; (E, F) 10 m; (G) 20 m; (H) 25 m
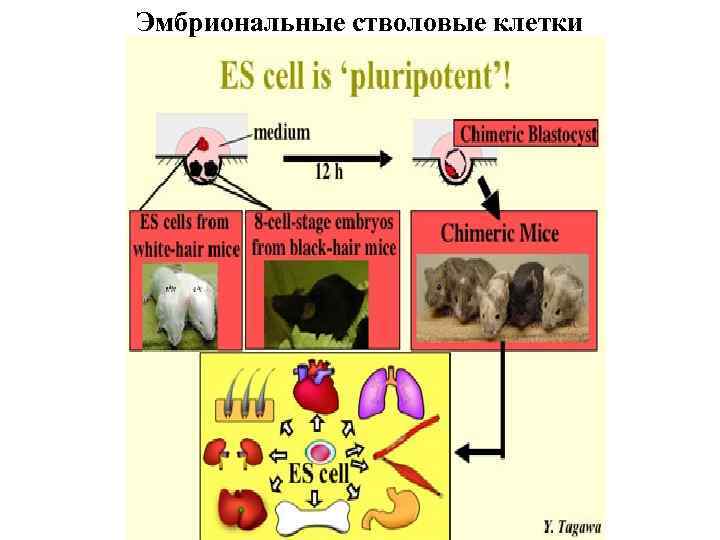 Эмбриональные стволовые клетки
Эмбриональные стволовые клетки
 Получение химерных животных при введении ЭСК в бластоцисту или морулу
Получение химерных животных при введении ЭСК в бластоцисту или морулу
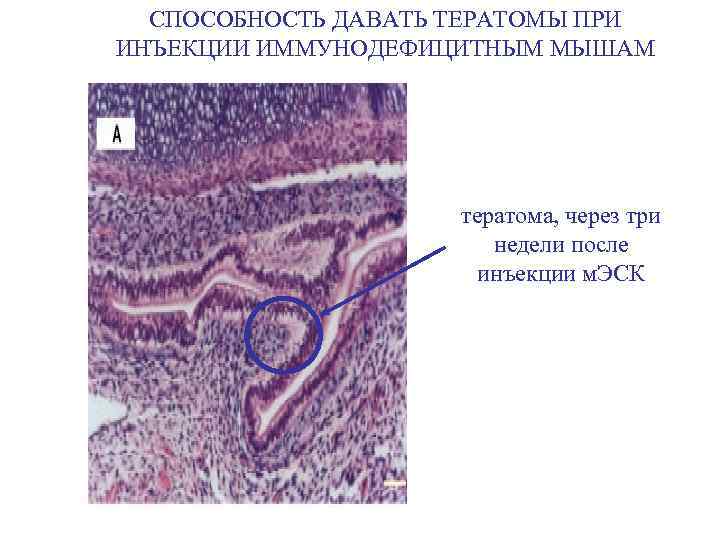 СПОСОБНОСТЬ ДАВАТЬ ТЕРАТОМЫ ПРИ ИНЪЕКЦИИ ИММУНОДЕФИЦИТНЫМ МЫШАМ тератома, через три недели после инъекции м. ЭСК
СПОСОБНОСТЬ ДАВАТЬ ТЕРАТОМЫ ПРИ ИНЪЕКЦИИ ИММУНОДЕФИЦИТНЫМ МЫШАМ тератома, через три недели после инъекции м. ЭСК
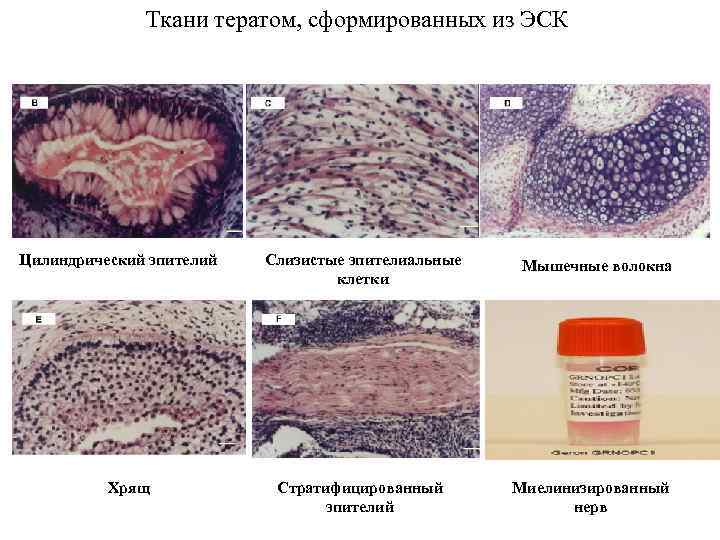 Ткани тератом, сформированных из ЭСК Цилиндрический эпителий Хрящ Слизистые эпителиальные клетки Мышечные волокна Стратифицированный эпителий Миелинизированный нерв
Ткани тератом, сформированных из ЭСК Цилиндрический эпителий Хрящ Слизистые эпителиальные клетки Мышечные волокна Стратифицированный эпителий Миелинизированный нерв
 Легко размножить Дифференцируются во все типы клеток ЭСК Отторгаются Могут давать опухоли
Легко размножить Дифференцируются во все типы клеток ЭСК Отторгаются Могут давать опухоли
 Необходимые предпосылки для использования ЭСК в регенеративной медицине • Контролируемая дифференцировка • Доказательство эффективности • Биобезопасность (риск образования тератом, перенос инфекционных агентов, отторжение) • Этические вопросы
Необходимые предпосылки для использования ЭСК в регенеративной медицине • Контролируемая дифференцировка • Доказательство эффективности • Биобезопасность (риск образования тератом, перенос инфекционных агентов, отторжение) • Этические вопросы
 Эмбриональные стволовые клетки стали потрясающей моделью для изучения широкого спектра биологических проблем, но, скорее всего, нескоро найдут широкое применение в клинике для заместительной клеточной терапии
Эмбриональные стволовые клетки стали потрясающей моделью для изучения широкого спектра биологических проблем, но, скорее всего, нескоро найдут широкое применение в клинике для заместительной клеточной терапии
 Geron Inc. Клинические испытания олигодендроцитов, полученных из ЭСК GRNOPC 1 Кардиомиоциты, инсулинпродуцирующие клетки, хондроциты
Geron Inc. Клинические испытания олигодендроцитов, полученных из ЭСК GRNOPC 1 Кардиомиоциты, инсулинпродуцирующие клетки, хондроциты
 FDA одобрило трансплантацию клеток сетчатки, полученных из эмбриональных стволовых клеток при макулодистрофии (2 клинических испытания) Исследования пройдут одновременно в нескольких клиниках на разных территориях США. Три первых пациента будут получать по 50 тысяч ЭСК с одной инъекцией, второй набор пациентов — по 100 тысяч, третий — по 200 тысяч. Испытания на животных дали положительные результаты. При самой маленькой дозе у животных наблюдались улучшения без каких-либо побочных эффектов. Иногда результаты были ошеломляющими. Достигалось стопроцентное восстановление зрения.
FDA одобрило трансплантацию клеток сетчатки, полученных из эмбриональных стволовых клеток при макулодистрофии (2 клинических испытания) Исследования пройдут одновременно в нескольких клиниках на разных территориях США. Три первых пациента будут получать по 50 тысяч ЭСК с одной инъекцией, второй набор пациентов — по 100 тысяч, третий — по 200 тысяч. Испытания на животных дали положительные результаты. При самой маленькой дозе у животных наблюдались улучшения без каких-либо побочных эффектов. Иногда результаты были ошеломляющими. Достигалось стопроцентное восстановление зрения.
 Индукция плюрипотентности в соматических клетках млекопитающих
Индукция плюрипотентности в соматических клетках млекопитающих
 Варианты репрограммирования клеточного ядра
Варианты репрограммирования клеточного ядра
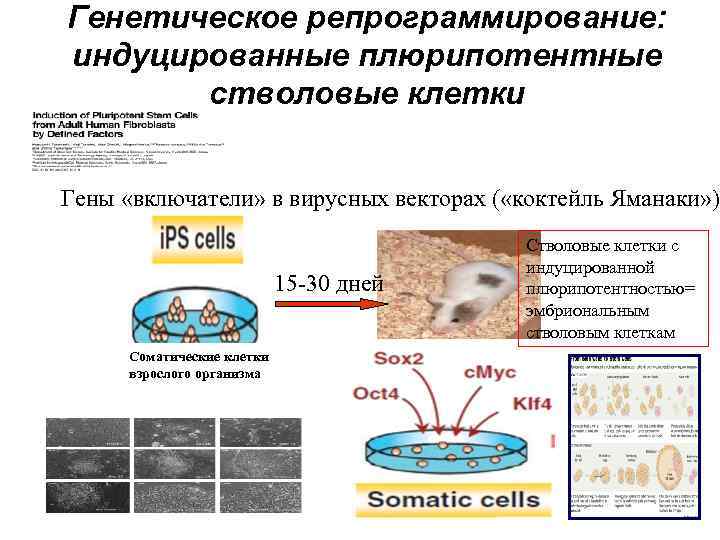 Генетическое репрограммирование: индуцированные плюрипотентные стволовые клетки Гены «включатели» в вирусных векторах ( «коктейль Яманаки» ) 15 -30 дней Соматические клетки взрослого организма Стволовые клетки с индуцированной плюрипотентностью= эмбриональным стволовым клеткам
Генетическое репрограммирование: индуцированные плюрипотентные стволовые клетки Гены «включатели» в вирусных векторах ( «коктейль Яманаки» ) 15 -30 дней Соматические клетки взрослого организма Стволовые клетки с индуцированной плюрипотентностью= эмбриональным стволовым клеткам
 Получение IPS клеток из фибробластов человека OCT 4, SOX 2, NANOG, LIN 28 Induction of Pluripotent Stem Cellsfrom Adult Human Fibroblasts by Defined Factors Kazutoshi Takahashi, Koji Tanabe, Mari Ohnuki, Megumi Narita, Tomoko Ichisaka, Kiichiro Tomoda, and Shinya Yamanaka. Cell. 2007 Nov 30; 131(5): 861 -72. Induced Pluripotent Stem Cell Lines Derived from Human Somatic Cells Junying Yu, Maxim A. Vodyanik, Kim Smuga-Otto, Jessica Antosiewicz-Bourget, Jennifer L. Frane, Shulan Tian, Jeff Nie, Gudrun A. Jonsdottir, Victor Ruotti, Ron Stewart, Igor I. Slukvin, James A. Thomson. Science. 2007 Dec 21; 318(5858): 1917 -20. Epub 2007 Nov 20
Получение IPS клеток из фибробластов человека OCT 4, SOX 2, NANOG, LIN 28 Induction of Pluripotent Stem Cellsfrom Adult Human Fibroblasts by Defined Factors Kazutoshi Takahashi, Koji Tanabe, Mari Ohnuki, Megumi Narita, Tomoko Ichisaka, Kiichiro Tomoda, and Shinya Yamanaka. Cell. 2007 Nov 30; 131(5): 861 -72. Induced Pluripotent Stem Cell Lines Derived from Human Somatic Cells Junying Yu, Maxim A. Vodyanik, Kim Smuga-Otto, Jessica Antosiewicz-Bourget, Jennifer L. Frane, Shulan Tian, Jeff Nie, Gudrun A. Jonsdottir, Victor Ruotti, Ron Stewart, Igor I. Slukvin, James A. Thomson. Science. 2007 Dec 21; 318(5858): 1917 -20. Epub 2007 Nov 20
 Индуцированные плюрипотентные клетки (i. PS cells) Индукция плюрипотентности в фибробластах с помощью ретровирусных конструкций, содержащих гены: - 4 фактора: Oct 3/4, Sox 2, c-Myc, Klf 4 (Takahashi et. аl. , 2006) Фибробласты мыши - 4 фактора: Oct 3/4, Sox 2, c-Myc, Klf 4 (Takahashi et. аl. , 2007) Фибробласты человека - 4 фактора: Oct 4, Sox 2, NANOG, LIN 28 (Junying Yu et. аl. , 2007) Фибробласты человека - 3 фактора: Oct 3/4, Sox 2, Klf 4 (Nakagava et. аl. , 2008) Фибробласты человека
Индуцированные плюрипотентные клетки (i. PS cells) Индукция плюрипотентности в фибробластах с помощью ретровирусных конструкций, содержащих гены: - 4 фактора: Oct 3/4, Sox 2, c-Myc, Klf 4 (Takahashi et. аl. , 2006) Фибробласты мыши - 4 фактора: Oct 3/4, Sox 2, c-Myc, Klf 4 (Takahashi et. аl. , 2007) Фибробласты человека - 4 фактора: Oct 4, Sox 2, NANOG, LIN 28 (Junying Yu et. аl. , 2007) Фибробласты человека - 3 фактора: Oct 3/4, Sox 2, Klf 4 (Nakagava et. аl. , 2008) Фибробласты человека
 Количество публикаций со словами «induced pluripotent stem cells»
Количество публикаций со словами «induced pluripotent stem cells»
 Клеточная терапия Получены b-клетки поджелудочной железы Generation of insulin-secreting islet-like clusters from human skin fibroblasts. Tateishi K, He J, Taranova O, Liang G, D'Alessio AC, Zhang Y.
Клеточная терапия Получены b-клетки поджелудочной железы Generation of insulin-secreting islet-like clusters from human skin fibroblasts. Tateishi K, He J, Taranova O, Liang G, D'Alessio AC, Zhang Y.
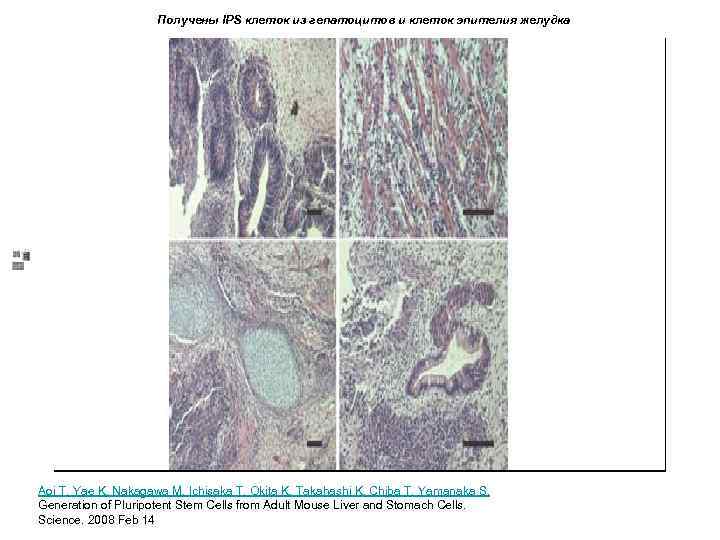 Получены IPS клеток из гепатоцитов и клеток эпителия желудка Aoi T, Yae K, Nakagawa M, Ichisaka T, Okita K, Takahashi K, Chiba T, Yamanaka S. Generation of Pluripotent Stem Cells from Adult Mouse Liver and Stomach Cells. Science. 2008 Feb 14
Получены IPS клеток из гепатоцитов и клеток эпителия желудка Aoi T, Yae K, Nakagawa M, Ichisaka T, Okita K, Takahashi K, Chiba T, Yamanaka S. Generation of Pluripotent Stem Cells from Adult Mouse Liver and Stomach Cells. Science. 2008 Feb 14
 Образование тератомы у иммунно-дефицитных мышей Гистологическая окраска гематоксилином и эозином
Образование тератомы у иммунно-дефицитных мышей Гистологическая окраска гематоксилином и эозином
 Первое терапевтическое использование костного мозга В 1896 Quine W. E. назначал экстракт костного мозга перорально для лечения лейкоза. В 1937 Schretzenmayer инъецировал свежий костный мозг внутримышечно для лечения паразитарной инфекции. В 1939 Osgood E. E. произвел внутривенную инфузию костного мозга для коррекции первичных расстройств костного мозга. В 1968 опубликованы первые сообщения об успешной трансплантации костного мозга в работе Gatti R. A. и Bach F. H.
Первое терапевтическое использование костного мозга В 1896 Quine W. E. назначал экстракт костного мозга перорально для лечения лейкоза. В 1937 Schretzenmayer инъецировал свежий костный мозг внутримышечно для лечения паразитарной инфекции. В 1939 Osgood E. E. произвел внутривенную инфузию костного мозга для коррекции первичных расстройств костного мозга. В 1968 опубликованы первые сообщения об успешной трансплантации костного мозга в работе Gatti R. A. и Bach F. H.
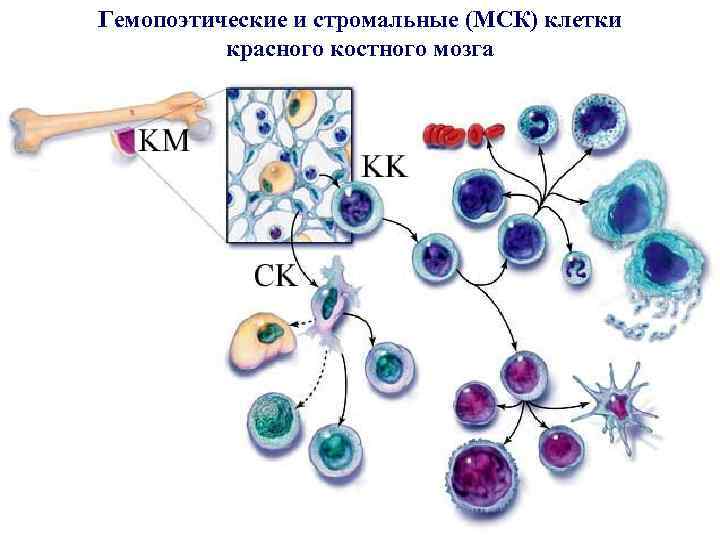 Гемопоэтические и стромальные (МСК) клетки красного костного мозга
Гемопоэтические и стромальные (МСК) клетки красного костного мозга
 Гематопоэтические СК А. Я. Фриденштейн (1924 -1998)
Гематопоэтические СК А. Я. Фриденштейн (1924 -1998)
 Терминология • Мезенхимальные или мезенхимные стволовые клетки костного мозга – МСК (mesenchymal stem/progenitor cells – MSCs – from bone marrow stroma) (Pittenger et al. , 2001) • Мультипотентные мезенхимные или мезенхимальные, стромальные клетки - ММСК (Кругляков и др. , 2004; Пулин и др. , 2008; Шалыгина и др. , 2009) • Стромальные клетки костного мозга СККМ (Bone marrow stromal cells -MSCs) (Sanchez-Ramos et al. , 2000) • Мультипотентные мезенхимные стромальные клетки костного мозга (Bone marrow mesenchymal stromal cells - BM-MSCs) (Ip et al. , 2007)
Терминология • Мезенхимальные или мезенхимные стволовые клетки костного мозга – МСК (mesenchymal stem/progenitor cells – MSCs – from bone marrow stroma) (Pittenger et al. , 2001) • Мультипотентные мезенхимные или мезенхимальные, стромальные клетки - ММСК (Кругляков и др. , 2004; Пулин и др. , 2008; Шалыгина и др. , 2009) • Стромальные клетки костного мозга СККМ (Bone marrow stromal cells -MSCs) (Sanchez-Ramos et al. , 2000) • Мультипотентные мезенхимные стромальные клетки костного мозга (Bone marrow mesenchymal stromal cells - BM-MSCs) (Ip et al. , 2007)
 Источники МСК • Строма костного мозга (0, 001% - 0, 01% ядросодержащих клеток) • Стромально-сосудистая фракция жировой ткани • Кожа • Фетальная печень • Плодные оболочки и плацента • Пупочный канатик • Амниотическая жидкость • Периферическая и пуповинная кровь • Пульпа молочных зубов
Источники МСК • Строма костного мозга (0, 001% - 0, 01% ядросодержащих клеток) • Стромально-сосудистая фракция жировой ткани • Кожа • Фетальная печень • Плодные оболочки и плацента • Пупочный канатик • Амниотическая жидкость • Периферическая и пуповинная кровь • Пульпа молочных зубов
 Современнные критерии определения МСК (требования комитета по мезенхимным и тканевым СК Международного общества клеточной терапии, 2006 г) 1. Адгезия к пластику при стандартных условиях культивирования 2. Фенотип Положительная экспрессия (>95%+) Отрицательная экспрессия (<2%+) CD 105 CD 73 CD 90 CD 45 CD 34 CD 14 или CD 11 b CD 79 a или CD 19 HLA-DR 3. Дифференцировка in vitro: остеобласты, хондроциты, адипоциты Dominici et al. , 2006
Современнные критерии определения МСК (требования комитета по мезенхимным и тканевым СК Международного общества клеточной терапии, 2006 г) 1. Адгезия к пластику при стандартных условиях культивирования 2. Фенотип Положительная экспрессия (>95%+) Отрицательная экспрессия (<2%+) CD 105 CD 73 CD 90 CD 45 CD 34 CD 14 или CD 11 b CD 79 a или CD 19 HLA-DR 3. Дифференцировка in vitro: остеобласты, хондроциты, адипоциты Dominici et al. , 2006
 Присутствующие на поверхности МСК антигены: • CD 73 – экто-5’-нуклеотидаза, выявлена на поверхности МСК, Т- и Влимфоцитов, на эндотелиальных клетках; • CD 105 – эндоглин, рецептор трансформирующего фактора роста-β (TGF-β), присутствует на поверхности макрофагов, эндотелия. фибробластов; • CD 90 (Thy-1) – член суперсемейства иммуноглобулинов на поверхности МСК должны отсутствовать следующие антигены: • CD 45 – маркер всех типов лейкоцитов; • CD 34 – маркер эндотелия и кроветворных предшественников; • CD 14 (CD 11 b) – маркер макрофагов и моноцитов; • CD 79α (CD 19) – маркер В-лимфоцитов; • HLA-DR – в отсутствии стимуляции интерфероном-γ (Dominici et al. , 2006; Паюшина, Старостин, Хрущов, 2009)
Присутствующие на поверхности МСК антигены: • CD 73 – экто-5’-нуклеотидаза, выявлена на поверхности МСК, Т- и Влимфоцитов, на эндотелиальных клетках; • CD 105 – эндоглин, рецептор трансформирующего фактора роста-β (TGF-β), присутствует на поверхности макрофагов, эндотелия. фибробластов; • CD 90 (Thy-1) – член суперсемейства иммуноглобулинов на поверхности МСК должны отсутствовать следующие антигены: • CD 45 – маркер всех типов лейкоцитов; • CD 34 – маркер эндотелия и кроветворных предшественников; • CD 14 (CD 11 b) – маркер макрофагов и моноцитов; • CD 79α (CD 19) – маркер В-лимфоцитов; • HLA-DR – в отсутствии стимуляции интерфероном-γ (Dominici et al. , 2006; Паюшина, Старостин, Хрущов, 2009)
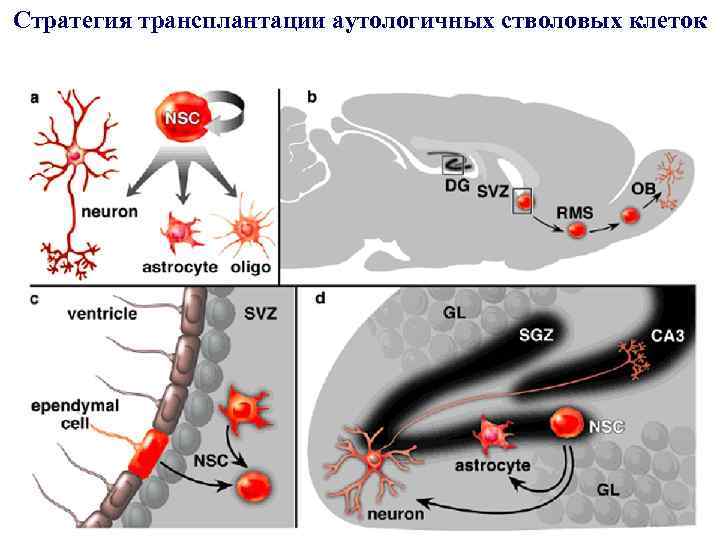 Стратегия трансплантации аутологичных стволовых клеток
Стратегия трансплантации аутологичных стволовых клеток
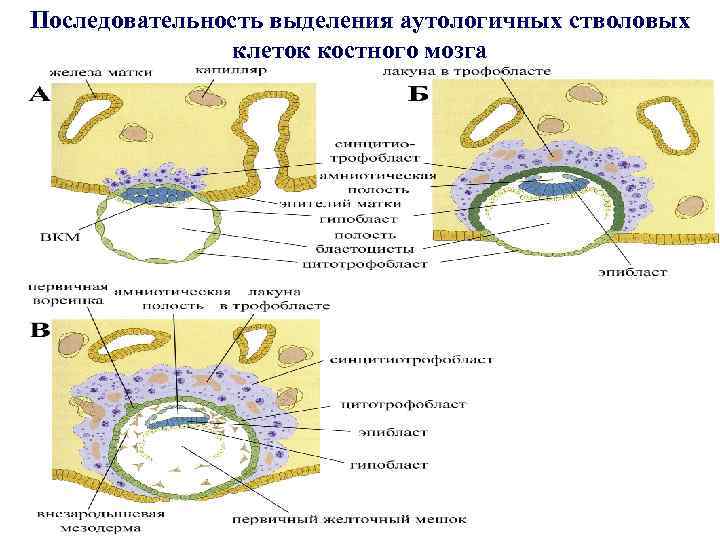 Последовательность выделения аутологичных стволовых клеток костного мозга
Последовательность выделения аутологичных стволовых клеток костного мозга

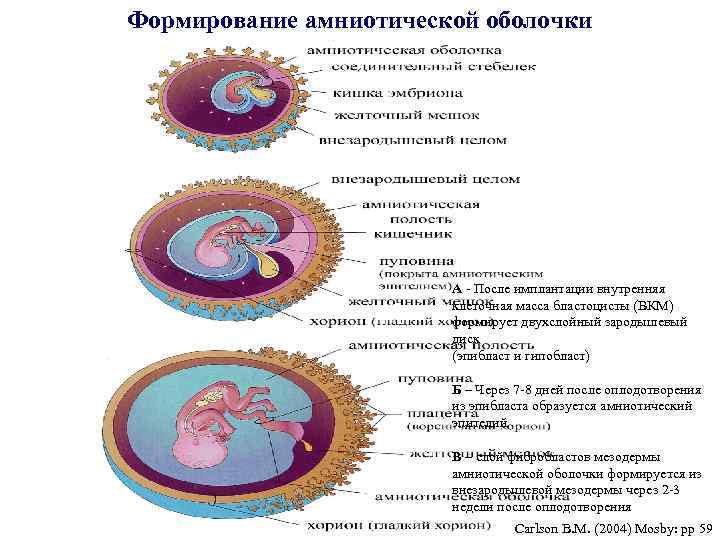 Формирование амниотической оболочки А - После имплантации внутренняя клеточная масса бластоцисты (ВКМ) формирует двухслойный зародышевый диск (эпибласт и гипобласт) Б – Через 7 -8 дней после оплодотворения из эпибласта образуется амниотический эпителий В – слой фибробластов мезодермы амниотической оболочки формируется из внезародышевой мезодермы через 2 -3 недели после оплодотворения Carlson B. M. (2004) Mosby: pp 59
Формирование амниотической оболочки А - После имплантации внутренняя клеточная масса бластоцисты (ВКМ) формирует двухслойный зародышевый диск (эпибласт и гипобласт) Б – Через 7 -8 дней после оплодотворения из эпибласта образуется амниотический эпителий В – слой фибробластов мезодермы амниотической оболочки формируется из внезародышевой мезодермы через 2 -3 недели после оплодотворения Carlson B. M. (2004) Mosby: pp 59
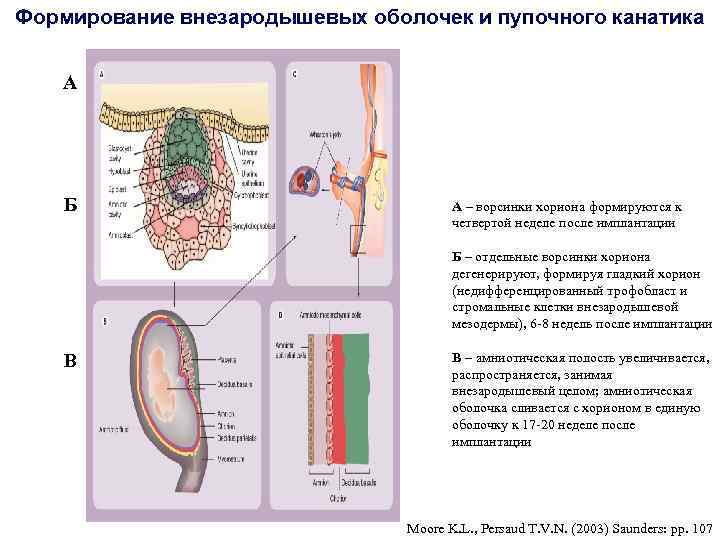 Формирование внезародышевых оболочек и пупочного канатика А Б А – ворсинки хориона формируются к четвертой неделе после имплантации Б – отдельные ворсинки хориона дегенерируют, формируя гладкий хорион (недифференцированный трофобласт и стромальные клетки внезародышевой мезодермы), 6 -8 недель после имплантации В В – амниотическая полость увеличивается, распространяется, занимая внезародышевый целом; амниотическая оболочка сливается с хорионом в единую оболочку к 17 -20 неделе после имплантации Moore K. L. , Persaud T. V. N. (2003) Saunders: pp. 107
Формирование внезародышевых оболочек и пупочного канатика А Б А – ворсинки хориона формируются к четвертой неделе после имплантации Б – отдельные ворсинки хориона дегенерируют, формируя гладкий хорион (недифференцированный трофобласт и стромальные клетки внезародышевой мезодермы), 6 -8 недель после имплантации В В – амниотическая полость увеличивается, распространяется, занимая внезародышевый целом; амниотическая оболочка сливается с хорионом в единую оболочку к 17 -20 неделе после имплантации Moore K. L. , Persaud T. V. N. (2003) Saunders: pp. 107
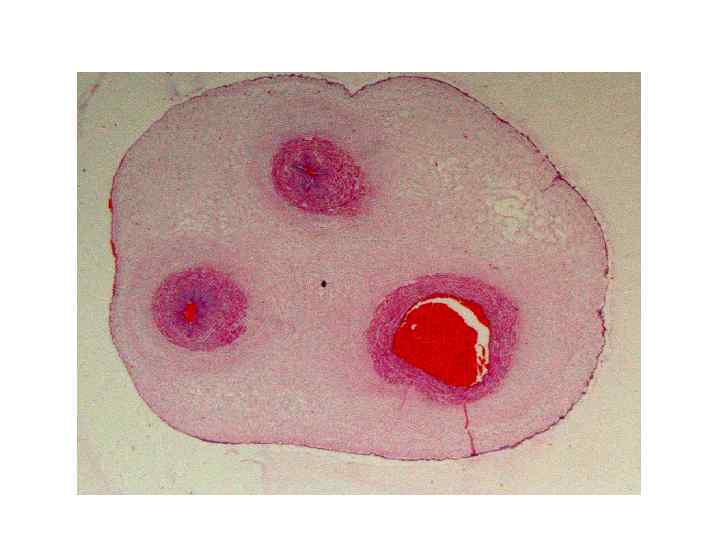
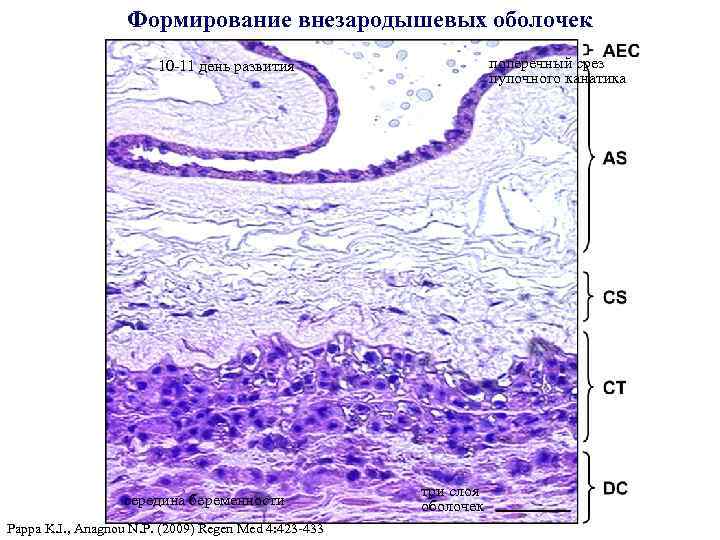 Формирование внезародышевых оболочек поперечный срез пупочного канатика 10 -11 день развития середина беременности Pappa K. I. , Anagnou N. P. (2009) Regen Med 4: 423 -433 три слоя оболочек
Формирование внезародышевых оболочек поперечный срез пупочного канатика 10 -11 день развития середина беременности Pappa K. I. , Anagnou N. P. (2009) Regen Med 4: 423 -433 три слоя оболочек
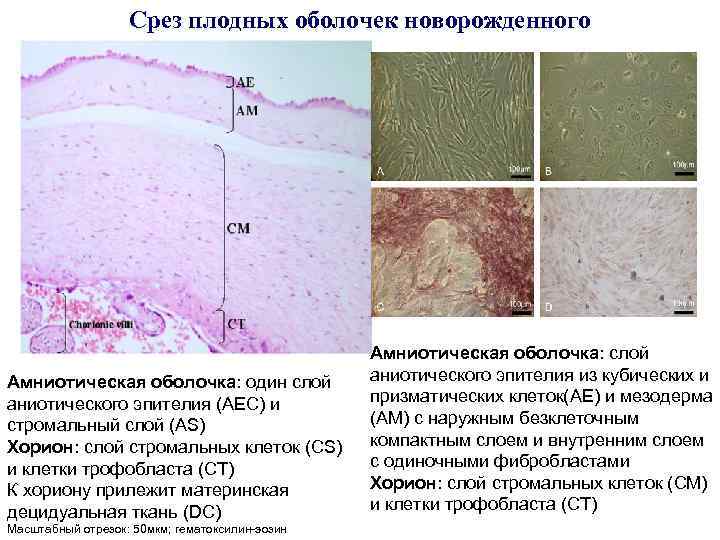 Срез плодных оболочек новорожденного Амниотическая оболочка: один слой аниотического эпителия (AEC) и стромальный слой (AS) Хорион: слой стромальных клеток (CS) и клетки трофобласта (CT) К хориону прилежит материнская децидуальная ткань (DC) Масштабный отрезок: 50 мкм; гематоксилин-эозин Амниотическая оболочка: слой аниотического эпителия из кубических и призматических клеток(AE) и мезодерма (AM) с наружным безклеточным компактным слоем и внутренним слоем с одиночными фибробластами Хорион: слой стромальных клеток (CM) и клетки трофобласта (CT)
Срез плодных оболочек новорожденного Амниотическая оболочка: один слой аниотического эпителия (AEC) и стромальный слой (AS) Хорион: слой стромальных клеток (CS) и клетки трофобласта (CT) К хориону прилежит материнская децидуальная ткань (DC) Масштабный отрезок: 50 мкм; гематоксилин-эозин Амниотическая оболочка: слой аниотического эпителия из кубических и призматических клеток(AE) и мезодерма (AM) с наружным безклеточным компактным слоем и внутренним слоем с одиночными фибробластами Хорион: слой стромальных клеток (CM) и клетки трофобласта (CT)
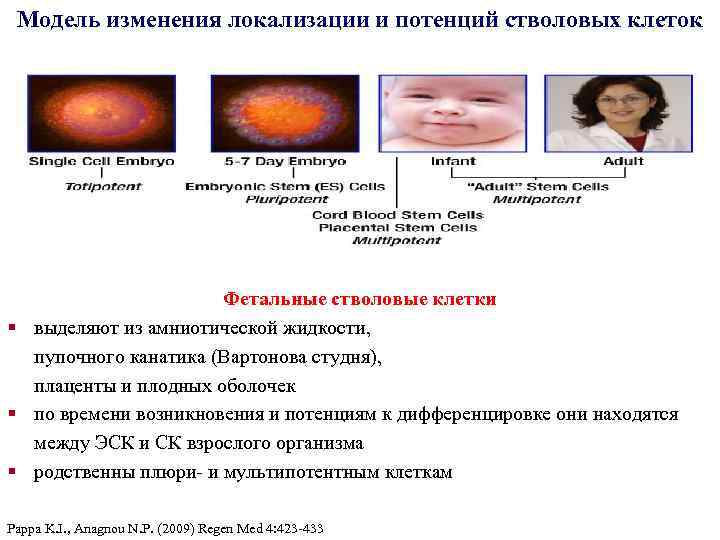 Модель изменения локализации и потенций стволовых клеток Фетальные стволовые клетки § выделяют из амниотической жидкости, пупочного канатика (Вартонова студня), плаценты и плодных оболочек § по времени возникновения и потенциям к дифференцировке они находятся между ЭСК и СК взрослого организма § родственны плюри- и мультипотентным клеткам Pappa K. I. , Anagnou N. P. (2009) Regen Med 4: 423 -433
Модель изменения локализации и потенций стволовых клеток Фетальные стволовые клетки § выделяют из амниотической жидкости, пупочного канатика (Вартонова студня), плаценты и плодных оболочек § по времени возникновения и потенциям к дифференцировке они находятся между ЭСК и СК взрослого организма § родственны плюри- и мультипотентным клеткам Pappa K. I. , Anagnou N. P. (2009) Regen Med 4: 423 -433
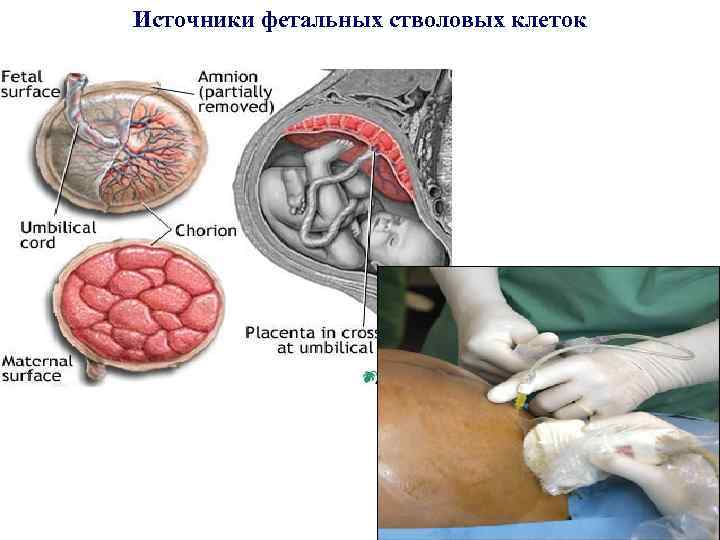 Источники фетальных стволовых клеток
Источники фетальных стволовых клеток

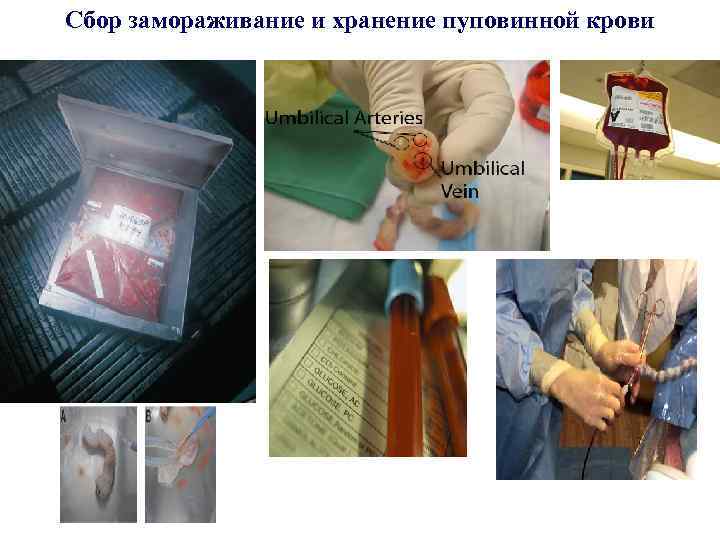 Сбор замораживание и хранение пуповинной крови
Сбор замораживание и хранение пуповинной крови
 Характеристика МСК-подобных клеток (0 -20%), полученных из пуповинной крови Параметр Характеристики Морфологические CD 34 -, CD 45 -, CD 14 -, CD 33 -, CD 49 -, CD 50 -, характеристики CD 62 -, CD 106 -, CD 117 -, CD 133 -, CD 135 Прикрепляются к пластику, CD 13+, CD 29+, CD 44+, CD 49+, CD 51+, CD 73+, CD 90/Thy 1+, CD 105/SH-2+, SH 3+, SH 4+, Дифференцирово Остеогенез, хондрогенез, адипогенез, чный потенциал нейрогенез (нейроны, олигодендроциты, астроциты), миогенез (миокард), гепатоциты (in vivo) Bieback K. et la. (2004) Stem Cells 22: 625 -634 Buzanska L. et al. (2002) J Cell Sci 115: 2131 -2138 Goodwin H. S. et al. (2001) Biol Blood Marrow Transplant 7: 581 -588 Kogler G. et al. (2004) J Exp Med 200: 123 -135 Lee O. K. et al. (2004) Blood 103: 1669 -1675
Характеристика МСК-подобных клеток (0 -20%), полученных из пуповинной крови Параметр Характеристики Морфологические CD 34 -, CD 45 -, CD 14 -, CD 33 -, CD 49 -, CD 50 -, характеристики CD 62 -, CD 106 -, CD 117 -, CD 133 -, CD 135 Прикрепляются к пластику, CD 13+, CD 29+, CD 44+, CD 49+, CD 51+, CD 73+, CD 90/Thy 1+, CD 105/SH-2+, SH 3+, SH 4+, Дифференцирово Остеогенез, хондрогенез, адипогенез, чный потенциал нейрогенез (нейроны, олигодендроциты, астроциты), миогенез (миокард), гепатоциты (in vivo) Bieback K. et la. (2004) Stem Cells 22: 625 -634 Buzanska L. et al. (2002) J Cell Sci 115: 2131 -2138 Goodwin H. S. et al. (2001) Biol Blood Marrow Transplant 7: 581 -588 Kogler G. et al. (2004) J Exp Med 200: 123 -135 Lee O. K. et al. (2004) Blood 103: 1669 -1675
 Банки пуповинной крови 1988 Элиан Глюкман в клинике святого Людовика в Париже впервые провела трансплантацию пуповинной крови ребенку с анемией Фанкони
Банки пуповинной крови 1988 Элиан Глюкман в клинике святого Людовика в Париже впервые провела трансплантацию пуповинной крови ребенку с анемией Фанкони
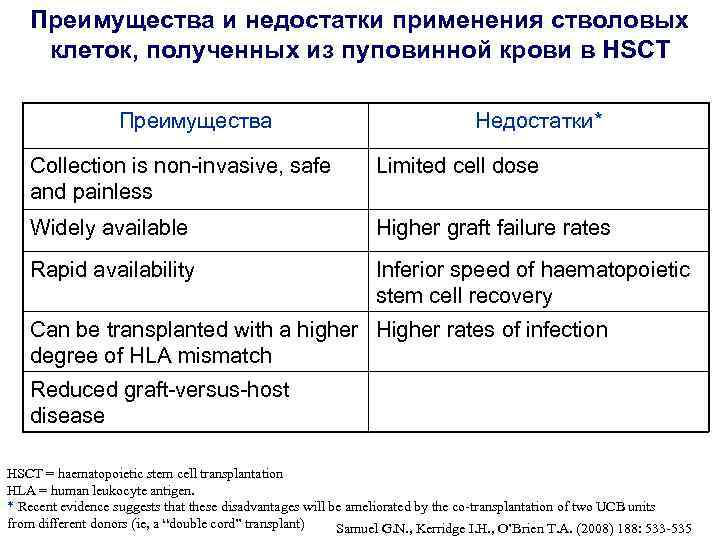 Преимущества и недостатки применения стволовых клеток, полученных из пуповинной крови в HSCT Преимущества Недостатки* Collection is non-invasive, safe and painless Limited cell dose Widely available Higher graft failure rates Rapid availability Inferior speed of haematopoietic stem cell recovery Can be transplanted with a higher Higher rates of infection degree of HLA mismatch Reduced graft-versus-host disease HSCT = haematopoietic stem cell transplantation HLA = human leukocyte antigen. * Recent evidence suggests that these disadvantages will be ameliorated by the co-transplantation of two UCB units from different donors (ie, a “double cord” transplant) Samuel G. N. , Kerridge I. H. , O’Brien T. A. (2008) 188: 533 -535
Преимущества и недостатки применения стволовых клеток, полученных из пуповинной крови в HSCT Преимущества Недостатки* Collection is non-invasive, safe and painless Limited cell dose Widely available Higher graft failure rates Rapid availability Inferior speed of haematopoietic stem cell recovery Can be transplanted with a higher Higher rates of infection degree of HLA mismatch Reduced graft-versus-host disease HSCT = haematopoietic stem cell transplantation HLA = human leukocyte antigen. * Recent evidence suggests that these disadvantages will be ameliorated by the co-transplantation of two UCB units from different donors (ie, a “double cord” transplant) Samuel G. N. , Kerridge I. H. , O’Brien T. A. (2008) 188: 533 -535

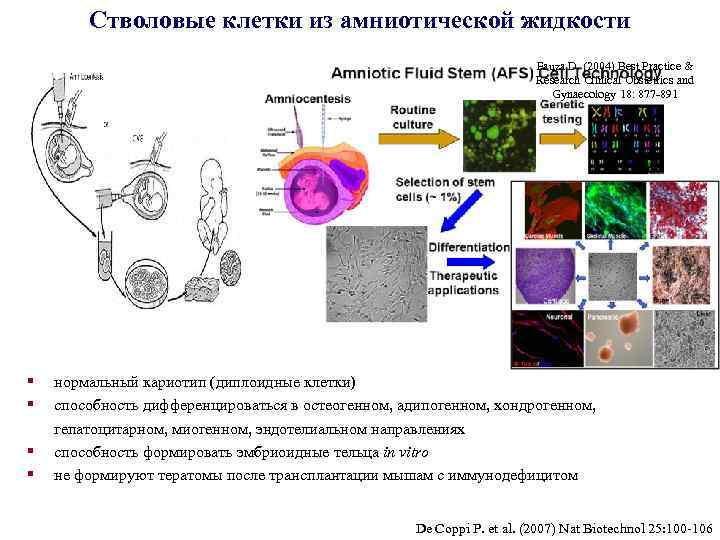 Стволовые клетки из амниотической жидкости Fauza D. (2004) Best Practice & Research Clinical Obstetrics and Gynaecology 18: 877 -891 § § нормальный кариотип (диплоидные клетки) способность дифференцироваться в остеогенном, адипогенном, хондрогенном, гепатоцитарном, миогенном, эндотелиальном направлениях способность формировать эмбриоидные тельца in vitro не формируют тератомы после трансплантации мышам с иммунодефицитом De Coppi P. et al. (2007) Nat Biotechnol 25: 100 -106
Стволовые клетки из амниотической жидкости Fauza D. (2004) Best Practice & Research Clinical Obstetrics and Gynaecology 18: 877 -891 § § нормальный кариотип (диплоидные клетки) способность дифференцироваться в остеогенном, адипогенном, хондрогенном, гепатоцитарном, миогенном, эндотелиальном направлениях способность формировать эмбриоидные тельца in vitro не формируют тератомы после трансплантации мышам с иммунодефицитом De Coppi P. et al. (2007) Nat Biotechnol 25: 100 -106

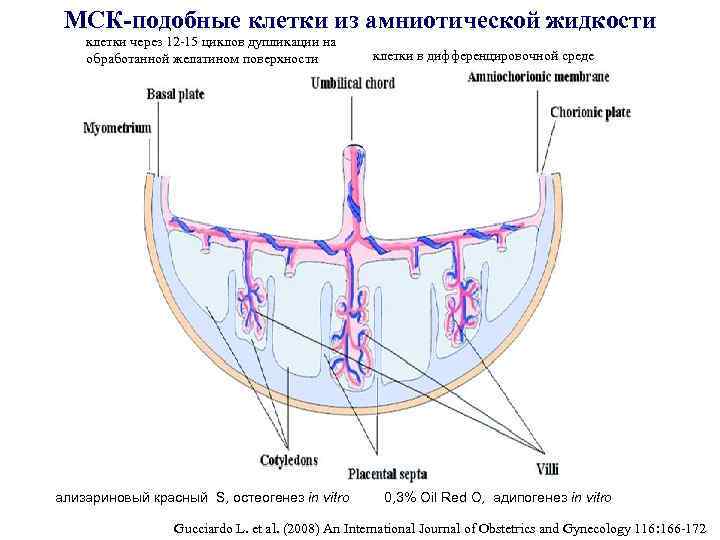 МСК-подобные клетки из амниотической жидкости клетки через 12 -15 циклов дупликации на обработанной желатином поверхности ализариновый красный S, остеогенез in vitro клетки в дифференцировочной среде 0, 3% Oil Red О, адипогенез in vitro Gucciardo L. et al. (2008) An International Journal of Obstetrics and Gynecology 116: 166 -172
МСК-подобные клетки из амниотической жидкости клетки через 12 -15 циклов дупликации на обработанной желатином поверхности ализариновый красный S, остеогенез in vitro клетки в дифференцировочной среде 0, 3% Oil Red О, адипогенез in vitro Gucciardo L. et al. (2008) An International Journal of Obstetrics and Gynecology 116: 166 -172
 Стволовые клетки из амниотической жидкости Клетки из амниотической жидкости в камере Горяева после выделения и центрифугирования, большинство окрашено трипановым синим (мертвые), много дебриса, живых клеток меньше 2% Увеличение х100
Стволовые клетки из амниотической жидкости Клетки из амниотической жидкости в камере Горяева после выделения и центрифугирования, большинство окрашено трипановым синим (мертвые), много дебриса, живых клеток меньше 2% Увеличение х100

 Выделение стволовых клеток из плаценты и плодных оболочек
Выделение стволовых клеток из плаценты и плодных оболочек
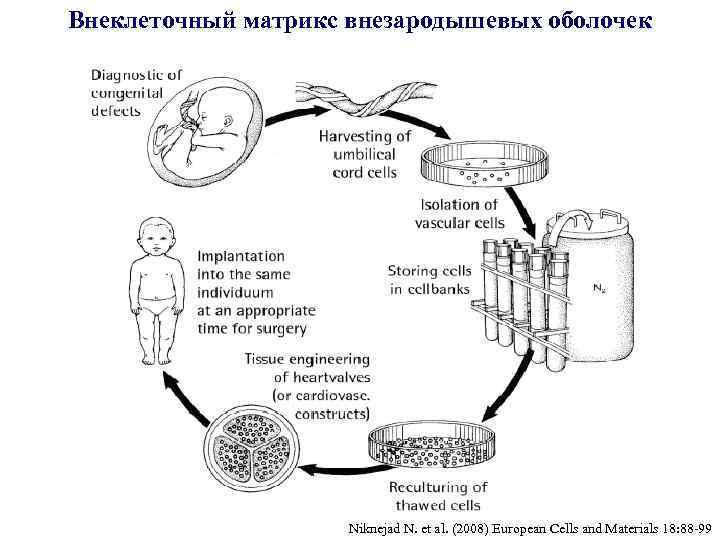 Внеклеточный матрикс внезародышевых оболочек Niknejad N. et al. (2008) European Cells and Materials 18: 88 -99
Внеклеточный матрикс внезародышевых оболочек Niknejad N. et al. (2008) European Cells and Materials 18: 88 -99
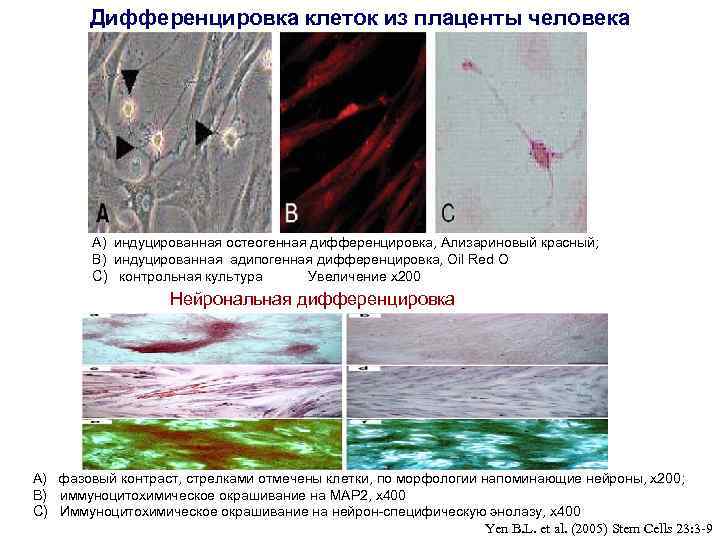 Дифференцировка клеток из плаценты человека A) индуцированная остеогенная дифференцировка, Ализариновый красный; B) индуцированная адипогенная дифференцировка, Oil Red O C) контрольная культура Увеличение х200 Нейрональная дифференцировка A) фазовый контраст, стрелками отмечены клетки, по морфологии напоминающие нейроны, х200; B) иммуноцитохимическое окрашивание на MAP 2, х400 C) Иммуноцитохимическое окрашивание на нейрон-специфическую энолазу, х400 Yen B. L. et al. (2005) Stem Cells 23: 3 -9
Дифференцировка клеток из плаценты человека A) индуцированная остеогенная дифференцировка, Ализариновый красный; B) индуцированная адипогенная дифференцировка, Oil Red O C) контрольная культура Увеличение х200 Нейрональная дифференцировка A) фазовый контраст, стрелками отмечены клетки, по морфологии напоминающие нейроны, х200; B) иммуноцитохимическое окрашивание на MAP 2, х400 C) Иммуноцитохимическое окрашивание на нейрон-специфическую энолазу, х400 Yen B. L. et al. (2005) Stem Cells 23: 3 -9
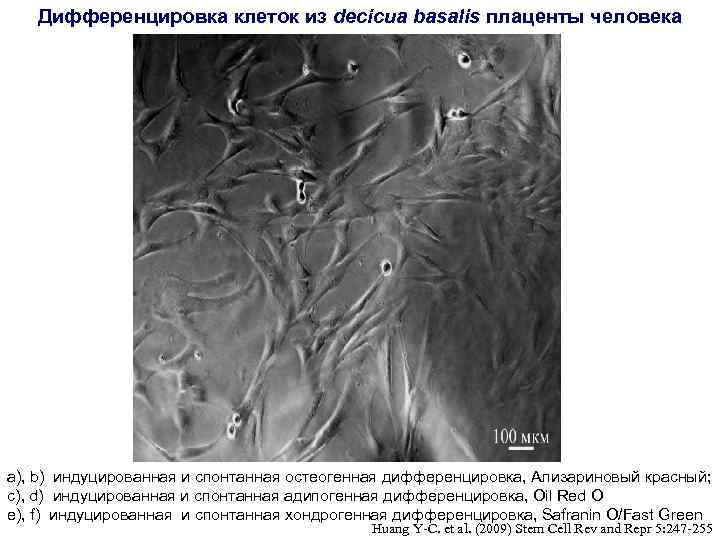 Дифференцировка клеток из decicua basalis плаценты человека a), b) индуцированная и спонтанная остеогенная дифференцировка, Ализариновый красный; c), d) индуцированная и спонтанная адипогенная дифференцировка, Oil Red O e), f) индуцированная и спонтанная хондрогенная дифференцировка, Safranin O/Fast Green Huang Y-C. et al. (2009) Stem Cell Rev and Repr 5: 247 -255
Дифференцировка клеток из decicua basalis плаценты человека a), b) индуцированная и спонтанная остеогенная дифференцировка, Ализариновый красный; c), d) индуцированная и спонтанная адипогенная дифференцировка, Oil Red O e), f) индуцированная и спонтанная хондрогенная дифференцировка, Safranin O/Fast Green Huang Y-C. et al. (2009) Stem Cell Rev and Repr 5: 247 -255
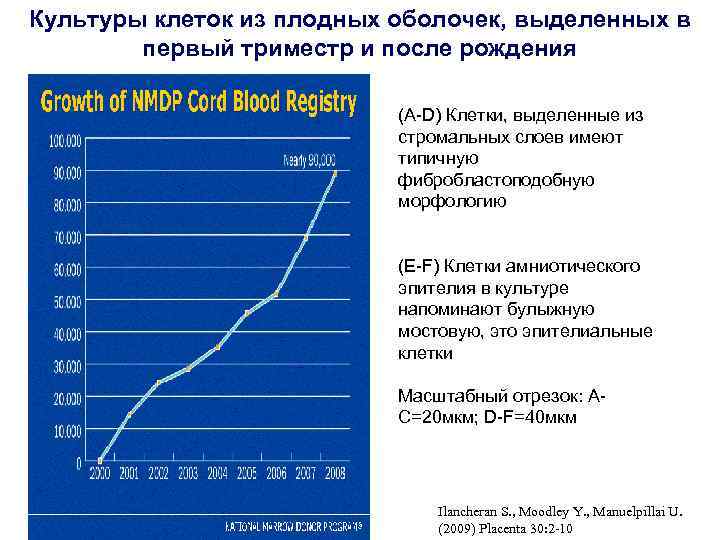 Культуры клеток из плодных оболочек, выделенных в первый триместр и после рождения (A-D) Клетки, выделенные из стромальных слоев имеют типичную фибробластоподобную морфологию (E-F) Клетки амниотического эпителия в культуре напоминают булыжную мостовую, это эпителиальные клетки Масштабный отрезок: AC=20 мкм; D-F=40 мкм Ilancheran S. , Moodley Y. , Manuelpillai U. (2009) Placenta 30: 2 -10
Культуры клеток из плодных оболочек, выделенных в первый триместр и после рождения (A-D) Клетки, выделенные из стромальных слоев имеют типичную фибробластоподобную морфологию (E-F) Клетки амниотического эпителия в культуре напоминают булыжную мостовую, это эпителиальные клетки Масштабный отрезок: AC=20 мкм; D-F=40 мкм Ilancheran S. , Moodley Y. , Manuelpillai U. (2009) Placenta 30: 2 -10
 Применение клеток пупочного канатика в медицине
Применение клеток пупочного канатика в медицине
 Исследования клеток пупочного канатика Структура пупочного канатика: 1. 2. 3. 4. 5. 6. амниотический эпителий; субамниотическая строма; межсосудистая строма (вартонов студень); околососудистая строма; кровеносные сосуды; эндотелиальная выстилка; 2 1 Sanmano et al. , 2005 5 3 6 4 Engraftment of umbilical cord epithelial cells in athymic mice: in an attempt to improve recostructed skin equivalents used as epithelial composite Baksh et al. , 2007 Human umbilical cord perivascular (HUCPV) cells: a source of mesenchymal progenitors Gasowska et al. , 2009 The influence of unfractionated and low-molecular weight heparins on the properties of human umbilical vein endothelial cells (HUVEC)
Исследования клеток пупочного канатика Структура пупочного канатика: 1. 2. 3. 4. 5. 6. амниотический эпителий; субамниотическая строма; межсосудистая строма (вартонов студень); околососудистая строма; кровеносные сосуды; эндотелиальная выстилка; 2 1 Sanmano et al. , 2005 5 3 6 4 Engraftment of umbilical cord epithelial cells in athymic mice: in an attempt to improve recostructed skin equivalents used as epithelial composite Baksh et al. , 2007 Human umbilical cord perivascular (HUCPV) cells: a source of mesenchymal progenitors Gasowska et al. , 2009 The influence of unfractionated and low-molecular weight heparins on the properties of human umbilical vein endothelial cells (HUVEC)
 клетки пупочного канатика in vitro клетки амниотического эпителия Sanmano B. , Mizoguchi M. , Suga U. , Ikeda S. , Ogawa H. Engraftment of umbilical cord epithelial cells in athymic mice: in an attempt to improve reconstructed skin equivalents used as epithelial composite // J Dermatol Sci. 2005; 37: 29 -39 периваскулярные клетки Sarugaser R. , Lickorish D. , Baksh D. , Hosseini M. M. , Davis J. E. Human umbilical cord perivascular (HUCPV) cells // Stem Cells 2005; 23: 220 -22 эндотелиальные клетки пупочной вены мультипотентные мезенхимальные стромальные клетки основного вещества Gasowska K, Naumnik B, Klejna K, Myśliwiec M. The influence of unfractionated and low-molecular weight heparins on the properties of human umbilical vein endothelial cells (HUVEC) // Folia Histoche Cytobiol. 2009; 47: 17 -23 Crampton S. P. , Davis J. , Hughes C. C. Isolation of human umbilical vein endothelial cells (HUVEC) // J Vis Exp 2007; 183 Baksh D, Yao R, Tuan RS. Comparison of proliferative and multilineage differentiation potential of human mesenchymal stem cells derived from umbilical cord and bone marrow// Stem Cells 2007; 25: 1384 – 1392 Wang H. S. , Hung S. C. , Peng S. T. , huang C. C. , Wei H. M. , Gug Y. J. , Fu Y. S. , Lai M. C. , Chen C. C. Mesenchymal stem cells in the Wharton's jelly of the human umbilical cord // Stem cells 2004; 22: 1330 -1337
клетки пупочного канатика in vitro клетки амниотического эпителия Sanmano B. , Mizoguchi M. , Suga U. , Ikeda S. , Ogawa H. Engraftment of umbilical cord epithelial cells in athymic mice: in an attempt to improve reconstructed skin equivalents used as epithelial composite // J Dermatol Sci. 2005; 37: 29 -39 периваскулярные клетки Sarugaser R. , Lickorish D. , Baksh D. , Hosseini M. M. , Davis J. E. Human umbilical cord perivascular (HUCPV) cells // Stem Cells 2005; 23: 220 -22 эндотелиальные клетки пупочной вены мультипотентные мезенхимальные стромальные клетки основного вещества Gasowska K, Naumnik B, Klejna K, Myśliwiec M. The influence of unfractionated and low-molecular weight heparins on the properties of human umbilical vein endothelial cells (HUVEC) // Folia Histoche Cytobiol. 2009; 47: 17 -23 Crampton S. P. , Davis J. , Hughes C. C. Isolation of human umbilical vein endothelial cells (HUVEC) // J Vis Exp 2007; 183 Baksh D, Yao R, Tuan RS. Comparison of proliferative and multilineage differentiation potential of human mesenchymal stem cells derived from umbilical cord and bone marrow// Stem Cells 2007; 25: 1384 – 1392 Wang H. S. , Hung S. C. , Peng S. T. , huang C. C. , Wei H. M. , Gug Y. J. , Fu Y. S. , Lai M. C. , Chen C. C. Mesenchymal stem cells in the Wharton's jelly of the human umbilical cord // Stem cells 2004; 22: 1330 -1337
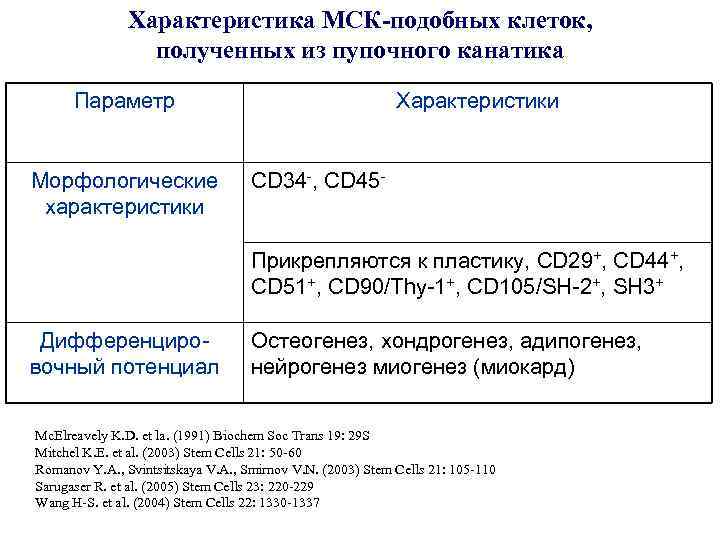 Характеристика МСК-подобных клеток, полученных из пупочного канатика Параметр Морфологические характеристики Характеристики CD 34 -, CD 45 - Прикрепляются к пластику, CD 29+, CD 44+, CD 51+, CD 90/Thy-1+, CD 105/SH-2+, SH 3+ Дифференцировочный потенциал Остеогенез, хондрогенез, адипогенез, нейрогенез миогенез (миокард) Mc. Elreavely K. D. et la. (1991) Biochem Soc Trans 19: 29 S Mitchel K. E. et al. (2003) Stem Cells 21: 50 -60 Romanov Y. A. , Svintsitskaya V. A. , Smirnov V. N. (2003) Stem Cells 21: 105 -110 Sarugaser R. et al. (2005) Stem Cells 23: 220 -229 Wang H-S. et al. (2004) Stem Cells 22: 1330 -1337
Характеристика МСК-подобных клеток, полученных из пупочного канатика Параметр Морфологические характеристики Характеристики CD 34 -, CD 45 - Прикрепляются к пластику, CD 29+, CD 44+, CD 51+, CD 90/Thy-1+, CD 105/SH-2+, SH 3+ Дифференцировочный потенциал Остеогенез, хондрогенез, адипогенез, нейрогенез миогенез (миокард) Mc. Elreavely K. D. et la. (1991) Biochem Soc Trans 19: 29 S Mitchel K. E. et al. (2003) Stem Cells 21: 50 -60 Romanov Y. A. , Svintsitskaya V. A. , Smirnov V. N. (2003) Stem Cells 21: 105 -110 Sarugaser R. et al. (2005) Stem Cells 23: 220 -229 Wang H-S. et al. (2004) Stem Cells 22: 1330 -1337
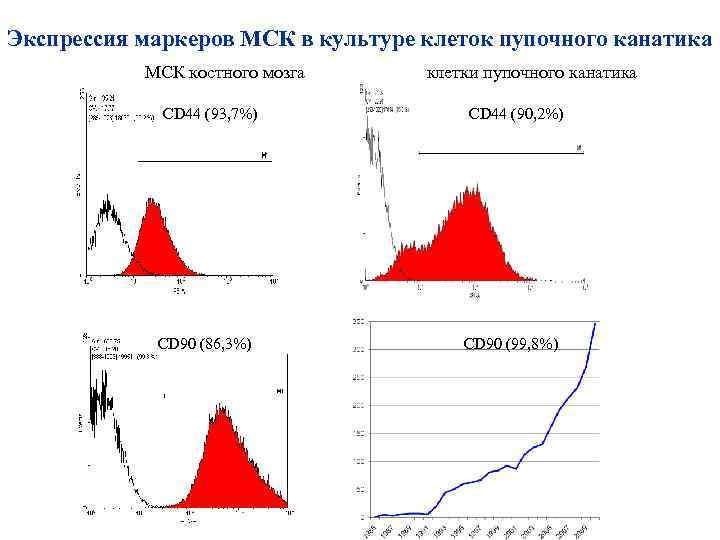 Экспрессия маркеров МСК в культуре клеток пупочного канатика МСК костного мозга СD 44 (93, 7%) СD 90 (86, 3%) клетки пупочного канатика СD 44 (90, 2%) СD 90 (99, 8%)
Экспрессия маркеров МСК в культуре клеток пупочного канатика МСК костного мозга СD 44 (93, 7%) СD 90 (86, 3%) клетки пупочного канатика СD 44 (90, 2%) СD 90 (99, 8%)
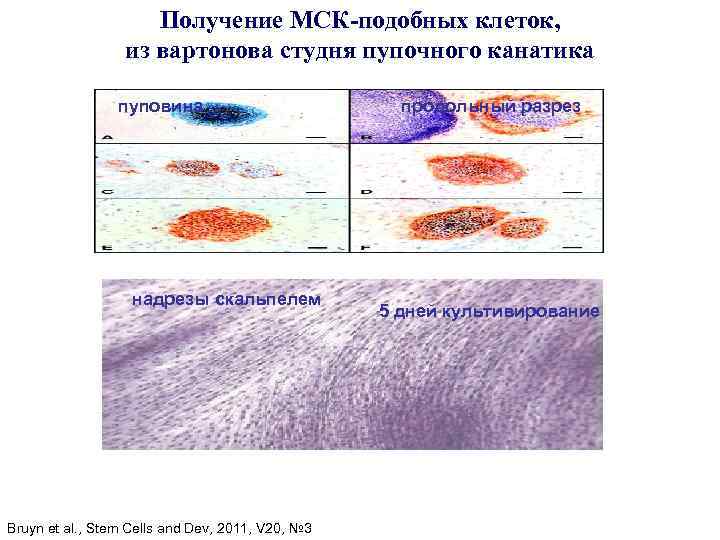 Получение МСК-подобных клеток, из вартонова студня пупочного канатика пуповина надрезы скальпелем Bruyn et al. , Stem Cells and Dev, 2011, V 20, № 3 продольный разрез 5 дней культивирование
Получение МСК-подобных клеток, из вартонова студня пупочного канатика пуповина надрезы скальпелем Bruyn et al. , Stem Cells and Dev, 2011, V 20, № 3 продольный разрез 5 дней культивирование
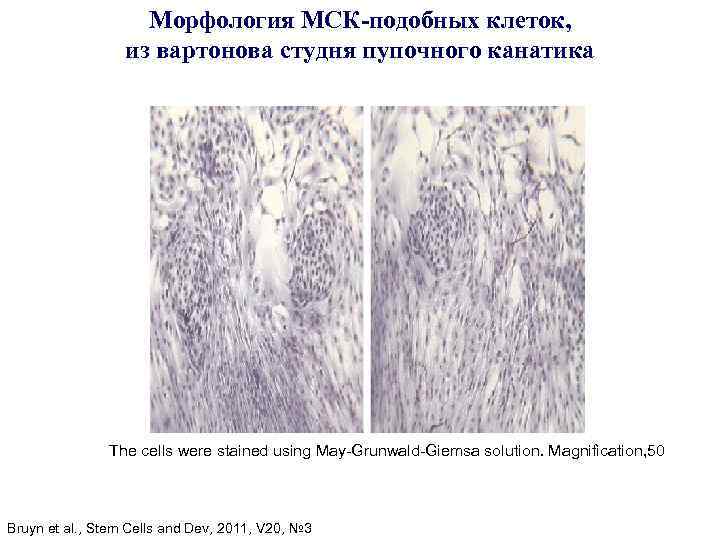 Морфология МСК-подобных клеток, из вартонова студня пупочного канатика The cells were stained using May-Grunwald-Giemsa solution. Magnification, 50 Bruyn et al. , Stem Cells and Dev, 2011, V 20, № 3
Морфология МСК-подобных клеток, из вартонова студня пупочного канатика The cells were stained using May-Grunwald-Giemsa solution. Magnification, 50 Bruyn et al. , Stem Cells and Dev, 2011, V 20, № 3
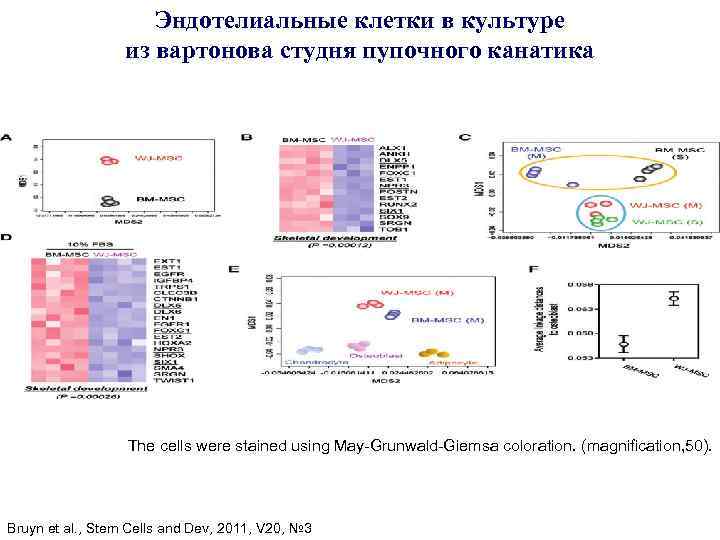 Эндотелиальные клетки в культуре из вартонова студня пупочного канатика The cells were stained using May-Grunwald-Giemsa coloration. (magnification, 50). Bruyn et al. , Stem Cells and Dev, 2011, V 20, № 3
Эндотелиальные клетки в культуре из вартонова студня пупочного канатика The cells were stained using May-Grunwald-Giemsa coloration. (magnification, 50). Bruyn et al. , Stem Cells and Dev, 2011, V 20, № 3
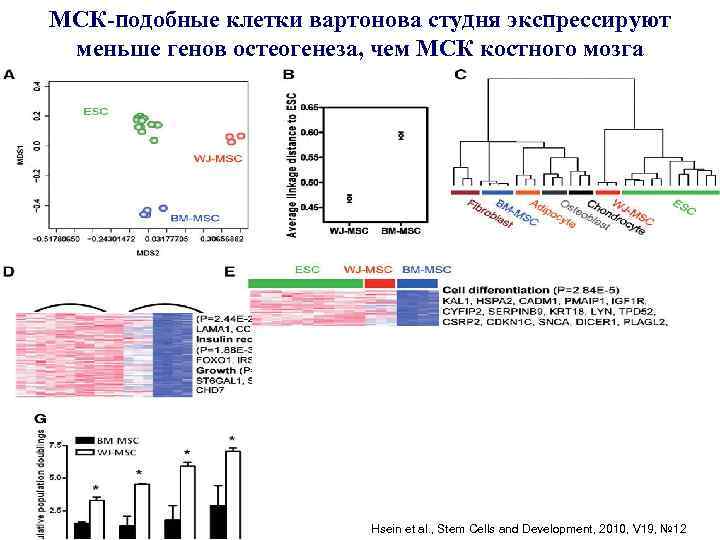 МСК-подобные клетки вартонова студня экспрессируют меньше генов остеогенеза, чем МСК костного мозга Hsein et al. , Stem Cells and Development, 2010, V 19, № 12
МСК-подобные клетки вартонова студня экспрессируют меньше генов остеогенеза, чем МСК костного мозга Hsein et al. , Stem Cells and Development, 2010, V 19, № 12
 Количество публикаций со словами «umbilical cord & stem cells»
Количество публикаций со словами «umbilical cord & stem cells»

 Первое успешное применение клеток 1819 г. Англия, Дж. Бланделл 1832 г. Ст. Петербург Акушер Андрей Вольф Первой обоснованной клеточной трансплантацией у человека следует считать переливание AB 0 -совместимой крови, впервые выполненное в 1907 году R. Ottenberg.
Первое успешное применение клеток 1819 г. Англия, Дж. Бланделл 1832 г. Ст. Петербург Акушер Андрей Вольф Первой обоснованной клеточной трансплантацией у человека следует считать переливание AB 0 -совместимой крови, впервые выполненное в 1907 году R. Ottenberg.
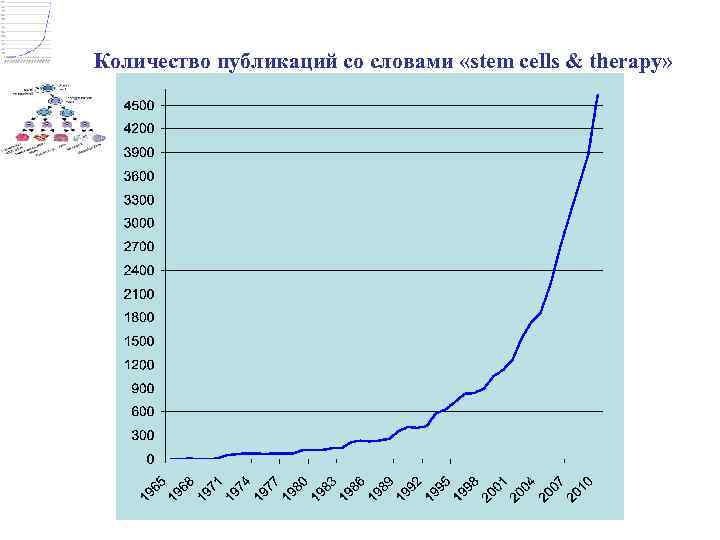 Количество публикаций со словами «stem cells & therapy»
Количество публикаций со словами «stem cells & therapy»
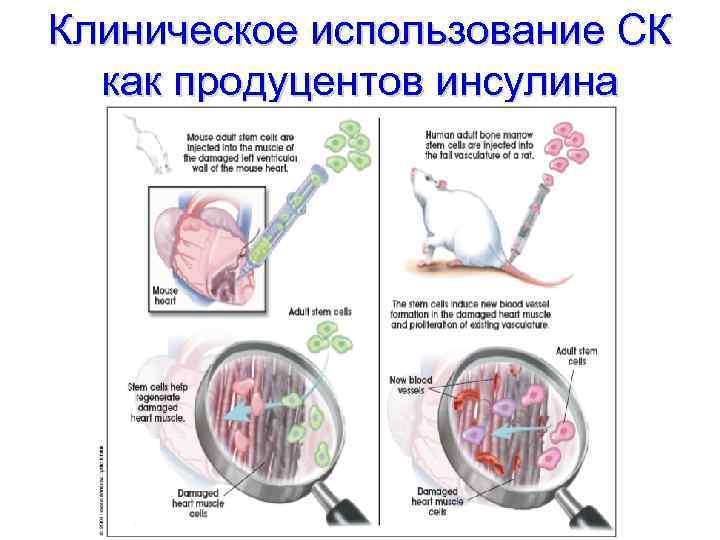 Клиническое использование СК как продуцентов инсулина
Клиническое использование СК как продуцентов инсулина
 Репарация дефектов сердца
Репарация дефектов сердца
 Регенеративная медицина — восстановление пораженной болезнью или повреждённой (травмированной) ткани с помощью активации эндогенных стволовых клеток или с помощью трансплантации клеток (клеточной терапии) – это создание живых полнофункциональных тканей для восстановления или замещения повреждённых тканей и/или органов (NIH Fact Sheet, 2006)
Регенеративная медицина — восстановление пораженной болезнью или повреждённой (травмированной) ткани с помощью активации эндогенных стволовых клеток или с помощью трансплантации клеток (клеточной терапии) – это создание живых полнофункциональных тканей для восстановления или замещения повреждённых тканей и/или органов (NIH Fact Sheet, 2006)
 В настоящее время стволовые клетки используются при лечении более 50 смертельно опасных заболеваний, среди них такие как:
В настоящее время стволовые клетки используются при лечении более 50 смертельно опасных заболеваний, среди них такие как:
 Клеточные продукты • Аутологичные – Без культивирования – С культивированием • Аллогенные – Без культивирования – С культивированием • Ксеногенные
Клеточные продукты • Аутологичные – Без культивирования – С культивированием • Аллогенные – Без культивирования – С культивированием • Ксеногенные
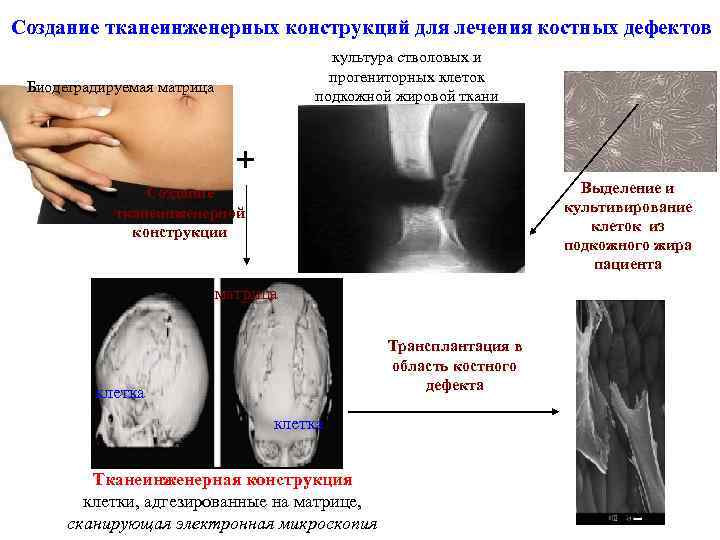 Cоздание тканеинженерных конструкций для лечения костных дефектов культура стволовых и прогениторных клеток подкожной жировой ткани Биодеградируемая матрица + Выделение и культивирование клеток из подкожного жира пациента Создание тканеинженерной конструкции матрица Трансплантация в область костного дефекта клетка Тканеинженерная конструкция клетки, адгезированные на матрице, сканирующая электронная микроскопия
Cоздание тканеинженерных конструкций для лечения костных дефектов культура стволовых и прогениторных клеток подкожной жировой ткани Биодеградируемая матрица + Выделение и культивирование клеток из подкожного жира пациента Создание тканеинженерной конструкции матрица Трансплантация в область костного дефекта клетка Тканеинженерная конструкция клетки, адгезированные на матрице, сканирующая электронная микроскопия
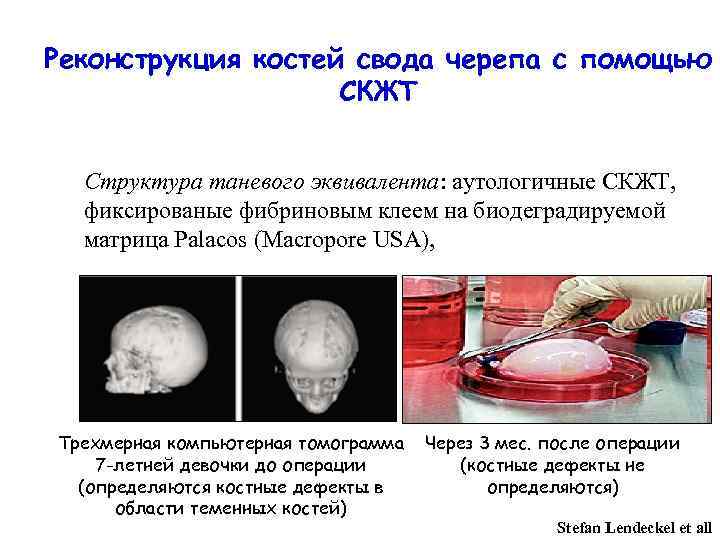 Реконструкция костей свода черепа с помощью СКЖТ Структура таневого эквивалента: аутологичные СКЖТ, фиксированые фибриновым клеем на биодеградируемой матрица Palacos (Macropore USA), Трехмерная компьютерная томограмма 7 -летней девочки до операции (определяются костные дефекты в области теменных костей) Через 3 мес. после операции (костные дефекты не определяются) Stefan Lendeckel et all
Реконструкция костей свода черепа с помощью СКЖТ Структура таневого эквивалента: аутологичные СКЖТ, фиксированые фибриновым клеем на биодеградируемой матрица Palacos (Macropore USA), Трехмерная компьютерная томограмма 7 -летней девочки до операции (определяются костные дефекты в области теменных костей) Через 3 мес. после операции (костные дефекты не определяются) Stefan Lendeckel et all
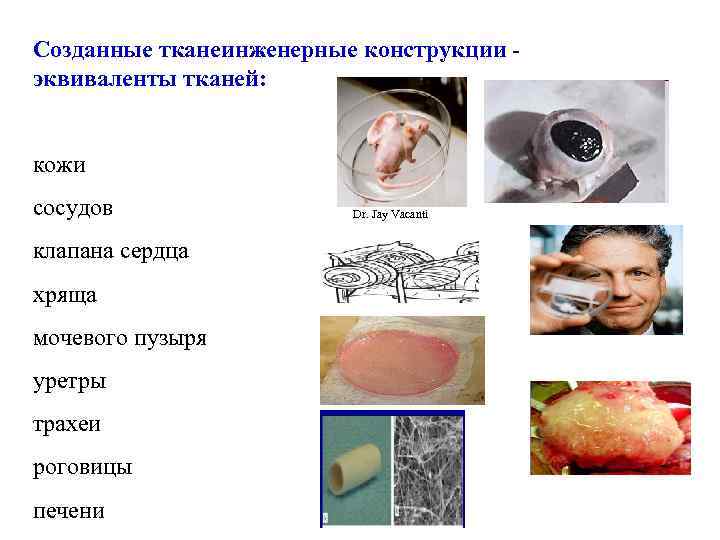 Созданные тканеинженерные конструкции - эквиваленты тканей: кожи сосудов клапана сердца хряща мочевого пузыря уретры трахеи роговицы печени Dr. Jay Vacanti
Созданные тканеинженерные конструкции - эквиваленты тканей: кожи сосудов клапана сердца хряща мочевого пузыря уретры трахеи роговицы печени Dr. Jay Vacanti
 Надежда медицины- терапия с использованием клеточных технологий • Дать организму новые стволовые клетки или клетки предшественники для регенерации • Использовать стволовые клетки для построения новых имплантируемых органов • Использовать потенциал стволовых клеток для органов ex vivo и отыграть время для восстановления или подходящего трансплантата НО: - Плохо умеем культивировать клетки in vitro - Нет подходящих материалов для биоинженерии - Не умеем обеспечить васкуляризацию доступно эффективно безопасно
Надежда медицины- терапия с использованием клеточных технологий • Дать организму новые стволовые клетки или клетки предшественники для регенерации • Использовать стволовые клетки для построения новых имплантируемых органов • Использовать потенциал стволовых клеток для органов ex vivo и отыграть время для восстановления или подходящего трансплантата НО: - Плохо умеем культивировать клетки in vitro - Нет подходящих материалов для биоинженерии - Не умеем обеспечить васкуляризацию доступно эффективно безопасно
 Активно развивающиеся клеточные технологии сместили интересы исследователей от больного к его изолированным клеткам в условиях культуры
Активно развивающиеся клеточные технологии сместили интересы исследователей от больного к его изолированным клеткам в условиях культуры