Энтропия(лекция)Саксонов(БТ31).ppt
- Количество слайдов: 22
 Энтропия. Второе начало термодинамики. Цикл Карно. Тепловые машины
Энтропия. Второе начало термодинамики. Цикл Карно. Тепловые машины
 Равновесное состояние термодинамической системы определяется постоянством значений макроскопических величин, характеризующих это состояние. Обратимым называют такой термодинамический процесс А→B, который, будучи проведен в обратном направлении, возвращает систему в исходное состояние, проходя через те же промежуточные состояния в обратной последовательности, а состояние тел вне термодинамической системы остались неизменными. P А Обратимый В V А В Квазистатический – процесс, в ходе которого система все время остается в состоянии равновесия. Круговой D C
Равновесное состояние термодинамической системы определяется постоянством значений макроскопических величин, характеризующих это состояние. Обратимым называют такой термодинамический процесс А→B, который, будучи проведен в обратном направлении, возвращает систему в исходное состояние, проходя через те же промежуточные состояния в обратной последовательности, а состояние тел вне термодинамической системы остались неизменными. P А Обратимый В V А В Квазистатический – процесс, в ходе которого система все время остается в состоянии равновесия. Круговой D C
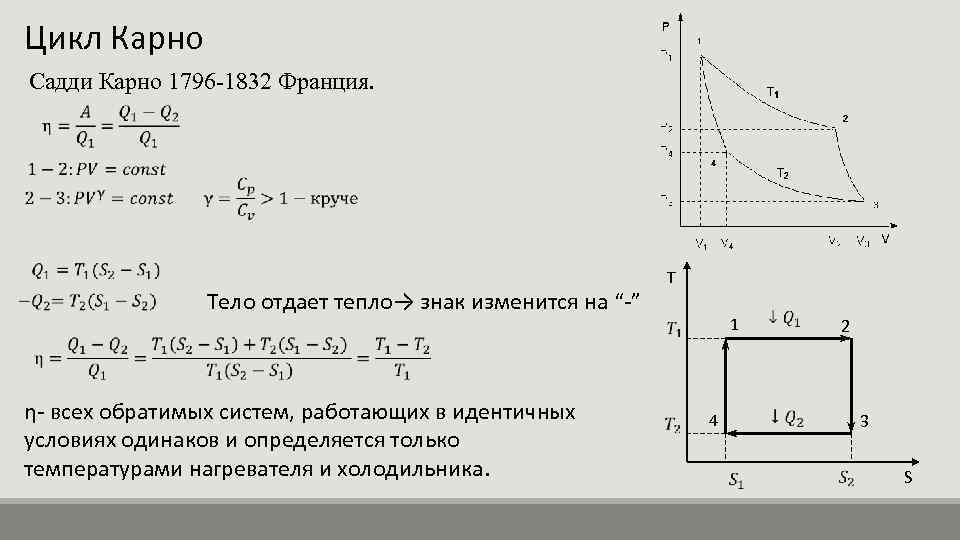 Цикл Карно Садди Карно 1796 -1832 Франция. Тело отдает тепло→ знак изменится на “-” η- всех обратимых систем, работающих в идентичных условиях одинаков и определяется только температурами нагревателя и холодильника. T 1 4 2 3 S
Цикл Карно Садди Карно 1796 -1832 Франция. Тело отдает тепло→ знак изменится на “-” η- всех обратимых систем, работающих в идентичных условиях одинаков и определяется только температурами нагревателя и холодильника. T 1 4 2 3 S
 При необратимом адиабатическом процессе энтропия возрастает η-любой необратимой машины всегда меньше, чем η обратимой, работающей в тех же условиях. Тепловая машина. 1 2 4 3
При необратимом адиабатическом процессе энтропия возрастает η-любой необратимой машины всегда меньше, чем η обратимой, работающей в тех же условиях. Тепловая машина. 1 2 4 3
 Предвестники 2 -ого начала термодинамики. Нельзя ли построить периодически действующую тепловую машину без холодильника? . Q 2=0 => такая машина превращала бы в работу всю теплоту, заимствованную от нагревателя. Закон сохранения энергии здесь не нарушается. Тогда представляется возможность создания вечного двигателя 2 -го рода (перпетуум мобиле 2 -го рода) => Заимствуем тепло из «неограниченного» (из океана, атмосферы, недров Земли) источника и превращаем его в работу. … тепло и вечный двигатель => Вильгельм Оствальд (1853 -1932 гг. )
Предвестники 2 -ого начала термодинамики. Нельзя ли построить периодически действующую тепловую машину без холодильника? . Q 2=0 => такая машина превращала бы в работу всю теплоту, заимствованную от нагревателя. Закон сохранения энергии здесь не нарушается. Тогда представляется возможность создания вечного двигателя 2 -го рода (перпетуум мобиле 2 -го рода) => Заимствуем тепло из «неограниченного» (из океана, атмосферы, недров Земли) источника и превращаем его в работу. … тепло и вечный двигатель => Вильгельм Оствальд (1853 -1932 гг. )
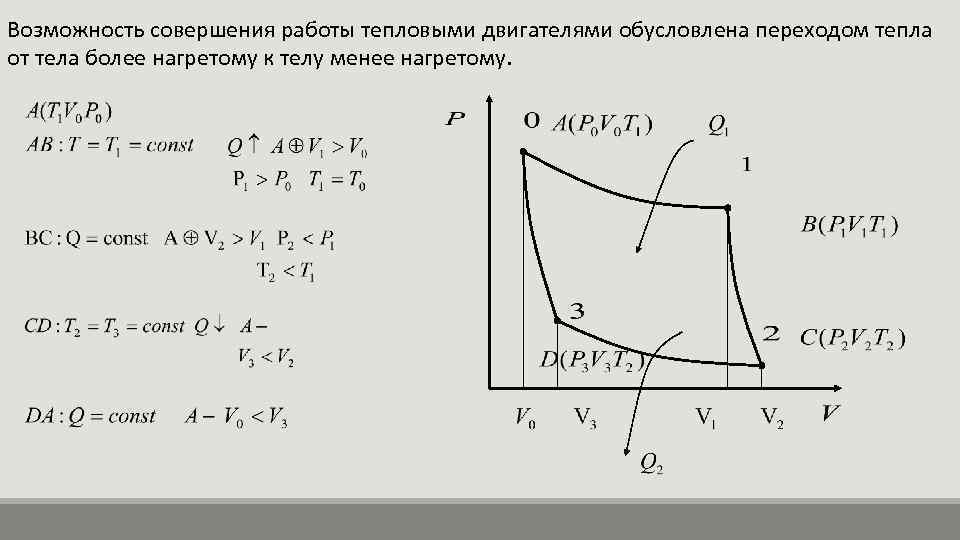 Возможность совершения работы тепловыми двигателями обусловлена переходом тепла от тела более нагретому к телу менее нагретому.
Возможность совершения работы тепловыми двигателями обусловлена переходом тепла от тела более нагретому к телу менее нагретому.
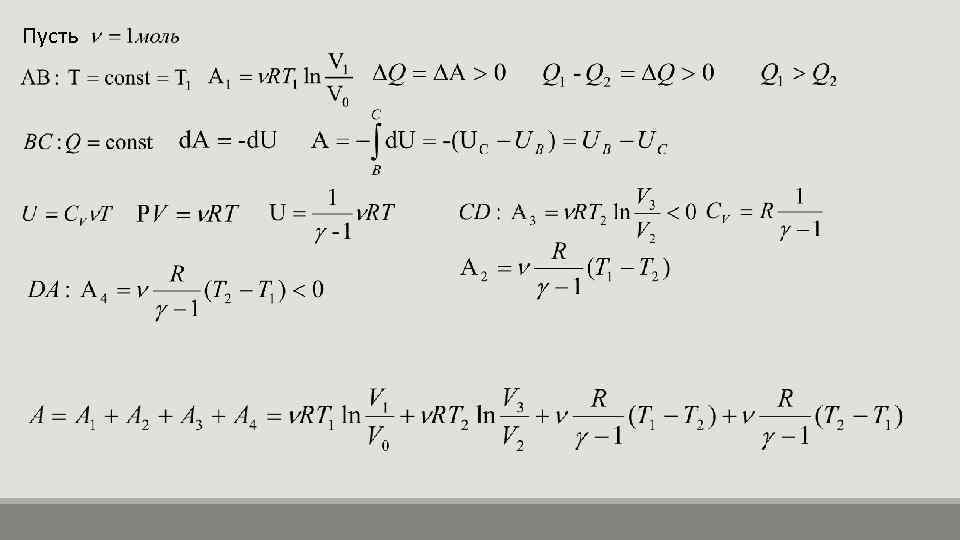 Пусть
Пусть

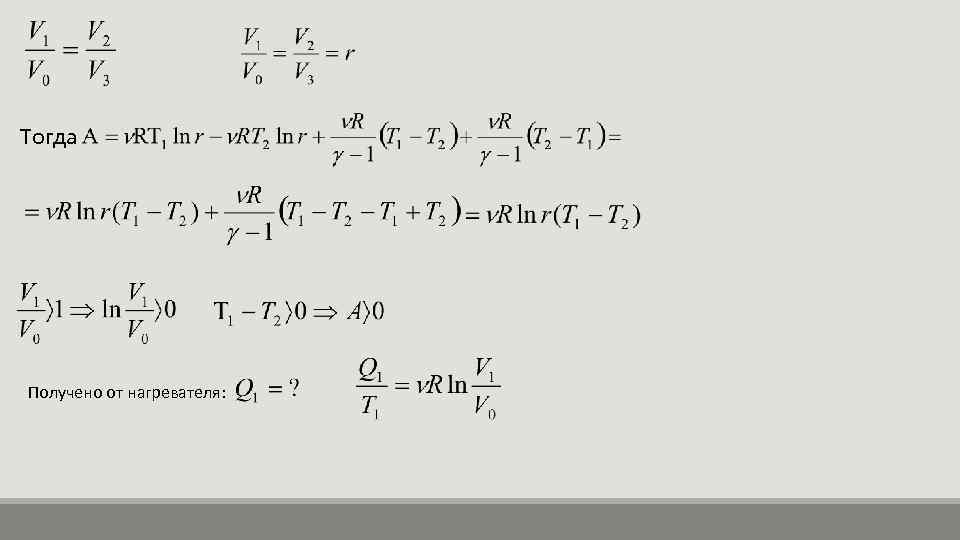 Тогда Получено от нагревателя:
Тогда Получено от нагревателя:
 Передано холодильнику: Преобразовано в работу:
Передано холодильнику: Преобразовано в работу:
 Энтропия , а для -приведенная теплота, является Но отношение функцией состояния системы - энтропия, где S- параметр состояния(как и P, V, T) В замкнутой или изолированной системе при протекании любого обратимого процесса энтропия остается неизменной
Энтропия , а для -приведенная теплота, является Но отношение функцией состояния системы - энтропия, где S- параметр состояния(как и P, V, T) В замкнутой или изолированной системе при протекании любого обратимого процесса энтропия остается неизменной
 При протекании в замкнутой термодинамической системе необратимого процесса, энтропия системы возрастает, достигая своего максимума в состоянии равновесия системы. Если , то какие либо изменения в системе без внешнего воздействия невозможны. - для обратимого процесса - для необратимого процесса Энтропия-мера отклонения реального процесса от идеального.
При протекании в замкнутой термодинамической системе необратимого процесса, энтропия системы возрастает, достигая своего максимума в состоянии равновесия системы. Если , то какие либо изменения в системе без внешнего воздействия невозможны. - для обратимого процесса - для необратимого процесса Энтропия-мера отклонения реального процесса от идеального.
 I-начало: II-начало: В замкнутой или изолированной системе при протекании необратим процесса энтропия системы возрастает, достигая своего максимума в состоянии равновесия системы. Если система находится в состоянии равновесия то какие либо изменения в системе без внешнего воздействия невозможны. Энтропия замкнутой системы может только возрастать. 1. Устанавливает наличие в природе фундаментальной асимметрии – однонаправленность всех самопроизвольно происходящих в природе процессов. 2. Количество энергии в замкнутых системах сохраняется, но распределение энергии меняется необратимым образом. III-начало: Если Т→ 0, то S→ 0, т. е. невозможно охладить вещество до температуры абсолютного нуля.
I-начало: II-начало: В замкнутой или изолированной системе при протекании необратим процесса энтропия системы возрастает, достигая своего максимума в состоянии равновесия системы. Если система находится в состоянии равновесия то какие либо изменения в системе без внешнего воздействия невозможны. Энтропия замкнутой системы может только возрастать. 1. Устанавливает наличие в природе фундаментальной асимметрии – однонаправленность всех самопроизвольно происходящих в природе процессов. 2. Количество энергии в замкнутых системах сохраняется, но распределение энергии меняется необратимым образом. III-начало: Если Т→ 0, то S→ 0, т. е. невозможно охладить вещество до температуры абсолютного нуля.
 Увеличение энтропии при теплопередаче. Необратимые процессы в замкнутой системе всегда сопровождаются возрастанием энтропии.
Увеличение энтропии при теплопередаче. Необратимые процессы в замкнутой системе всегда сопровождаются возрастанием энтропии.
 - МАЛО! У реальных <22% Тепло, заимствованное у источника, не может быть целиком преобразовано в работу. Различные формулировки II-начала термодинамики. 1. Вильям Томсон ↔ лорд Кельвин 1851. «Невозможен круговой процесс единственным результатом которого было бы производство работы за счет охлаждения теплового резервуара. » Невозможен круговой процесс, единственным результатом которого было бы производство работы за счет уменьшения внутренней энергии теплового резервуара.
- МАЛО! У реальных <22% Тепло, заимствованное у источника, не может быть целиком преобразовано в работу. Различные формулировки II-начала термодинамики. 1. Вильям Томсон ↔ лорд Кельвин 1851. «Невозможен круговой процесс единственным результатом которого было бы производство работы за счет охлаждения теплового резервуара. » Невозможен круговой процесс, единственным результатом которого было бы производство работы за счет уменьшения внутренней энергии теплового резервуара.
 2. Клаузиус (1822 – 1888) в 1850 “ Теплота не может самопроизвольно переходить от тела менее нагретого к телу более нагретому. ” Вообще “она” возможна. Но она невозможна при условии, что во всех остальных телах не произошло никаких изменений. Холодильник, но процесс не самопроизвольный, а сопровождается работой электрического мотора. 3. т. Нернста: энтропия любого тела стремится к нулю при Т → 0 Обратимый процесс - процесс, при котором система переходит из состояния А в В и возможно вернуть ее хотя бы одним способом в исходное состояние А и при том так, чтобы во всех остальных телах не произошло никаких изменений.
2. Клаузиус (1822 – 1888) в 1850 “ Теплота не может самопроизвольно переходить от тела менее нагретого к телу более нагретому. ” Вообще “она” возможна. Но она невозможна при условии, что во всех остальных телах не произошло никаких изменений. Холодильник, но процесс не самопроизвольный, а сопровождается работой электрического мотора. 3. т. Нернста: энтропия любого тела стремится к нулю при Т → 0 Обратимый процесс - процесс, при котором система переходит из состояния А в В и возможно вернуть ее хотя бы одним способом в исходное состояние А и при том так, чтобы во всех остальных телах не произошло никаких изменений.
 Второе начало термодинамики. Направление термодинамических процессов в изолированной системе → к состояниям, вероятность которых максимальна : --Теплопередача => выравнивание температур. --Диффузия => однородный газ не может собраться в одной половинке сосуда. Энтропия. Статистический вес - число различных микросостояний, посредством которых осуществляется данное макросостояние w; Все макросостояния равновесны => вероятность макросостояния пропорциональна его статистическому весу. – энтропия – характеризует вероятность состояния термодинамической системы.
Второе начало термодинамики. Направление термодинамических процессов в изолированной системе → к состояниям, вероятность которых максимальна : --Теплопередача => выравнивание температур. --Диффузия => однородный газ не может собраться в одной половинке сосуда. Энтропия. Статистический вес - число различных микросостояний, посредством которых осуществляется данное макросостояние w; Все макросостояния равновесны => вероятность макросостояния пропорциональна его статистическому весу. – энтропия – характеризует вероятность состояния термодинамической системы.
 Энтропия идеального газа.
Энтропия идеального газа.
 Необратимый - процесс, обратный к которому маловероятен - диффузия/газ сосредоточился в половине сосуда. В случае обратимого процесса в неизолированной системе энтропия может как возрастать, так и убывать.
Необратимый - процесс, обратный к которому маловероятен - диффузия/газ сосредоточился в половине сосуда. В случае обратимого процесса в неизолированной системе энтропия может как возрастать, так и убывать.
 Энтропия идеального газа. Для случая диффузии газа из половины сосуда в весь сосуд:
Энтропия идеального газа. Для случая диффузии газа из половины сосуда в весь сосуд:
 Невозможность вечного двигателя 2 -ого рода. Молекулы сами собрались в ½ части сосуда и , затем, за счет подводимого тепла изотермически расширяясь совершают работу : Вроде бы все хорошо, если бы молекулы действительно циклически собирались самопроизвольно в ½ части объема сосуда. А вот у тепловой машины энтропия возрастает! но т. к. , то
Невозможность вечного двигателя 2 -ого рода. Молекулы сами собрались в ½ части сосуда и , затем, за счет подводимого тепла изотермически расширяясь совершают работу : Вроде бы все хорошо, если бы молекулы действительно циклически собирались самопроизвольно в ½ части объема сосуда. А вот у тепловой машины энтропия возрастает! но т. к. , то
 Связь энтропии с вероятностью. Всякий процесс в природе протекает так, что система переходит в состояние, вероятность которого больше. Если система находится в состоянии с данной энтропией, то с подавляющей вероятностью следует ожидать, что она перейдет в состояние с большей энтропией, т. е. что наиболее вероятным изменением энтропии является ее возрастание. Но возможны и процессы с уменьшением энтропии – флуктуации ω в среднем росте.
Связь энтропии с вероятностью. Всякий процесс в природе протекает так, что система переходит в состояние, вероятность которого больше. Если система находится в состоянии с данной энтропией, то с подавляющей вероятностью следует ожидать, что она перейдет в состояние с большей энтропией, т. е. что наиболее вероятным изменением энтропии является ее возрастание. Но возможны и процессы с уменьшением энтропии – флуктуации ω в среднем росте.


