влияние температуры на скор р-ции,.ppt
- Количество слайдов: 16
 Энтропия и ее изменение при различных процессах • Количественной мерой беспорядка (хаотичности, неупорядоченности) системы является энтропия S. – Энтропия всегда возрастает (ΔS > 0) при переходе системы из более упорядоченного состояния в менее упорядоченное: при переходе вещества из кристаллического состояния в жидкое и из жидкого в газообразное, при повышении температуры, при растворении и диссоциации кристаллического вещества и т. д. – При переходе системы из менее упорядоченного состояния в более упорядоченное энтропия системы уменьшается (ΔS < 0), например при конденсации, кристаллизации, понижении температуры и т. д. • В термодинамике изменение энтропии связано с теплотой выражением: d. S = δQ/T или ΔS=ΔH / T
Энтропия и ее изменение при различных процессах • Количественной мерой беспорядка (хаотичности, неупорядоченности) системы является энтропия S. – Энтропия всегда возрастает (ΔS > 0) при переходе системы из более упорядоченного состояния в менее упорядоченное: при переходе вещества из кристаллического состояния в жидкое и из жидкого в газообразное, при повышении температуры, при растворении и диссоциации кристаллического вещества и т. д. – При переходе системы из менее упорядоченного состояния в более упорядоченное энтропия системы уменьшается (ΔS < 0), например при конденсации, кристаллизации, понижении температуры и т. д. • В термодинамике изменение энтропии связано с теплотой выражением: d. S = δQ/T или ΔS=ΔH / T
 Изменение энтропии Стандартная энтропия 1 моль обозначается S 0298, это справочная величина, измеряется в Дж/(К*моль) Например, стандартная энтропия – льда……………. . S 0298 = 39, 7 Дж/(К*моль); – воды……………. S 0298 = 70, 08 Дж/(К*моль); – водяного пара…. . S 0298 = 188, 72 Дж/(К*моль), т. е. энтропия возрастает – степень беспорядка вещества в газообразном состоянии больше. – У графита S 0298 = 5, 74 Дж/(К*моль), у алмаза S 0298 = 2, 36 Дж/(К*моль), так как у веществ с аморфной структурой энтропия больше, чем с кристаллической.
Изменение энтропии Стандартная энтропия 1 моль обозначается S 0298, это справочная величина, измеряется в Дж/(К*моль) Например, стандартная энтропия – льда……………. . S 0298 = 39, 7 Дж/(К*моль); – воды……………. S 0298 = 70, 08 Дж/(К*моль); – водяного пара…. . S 0298 = 188, 72 Дж/(К*моль), т. е. энтропия возрастает – степень беспорядка вещества в газообразном состоянии больше. – У графита S 0298 = 5, 74 Дж/(К*моль), у алмаза S 0298 = 2, 36 Дж/(К*моль), так как у веществ с аморфной структурой энтропия больше, чем с кристаллической.
 Реакции с изменением энтропии – С увеличением энтропии (ΔS > 0) протекают также реакции: – 2 Н 2 О(г) = 2 Н 2(г) + О 2(г) – 2 Н 2 О 2(ж)= 2 Н 2 О(ж) + О 2(г) – Са. СО 3(к) = Са. О(к) + СО 2(г) , ΔS 0298 = 160, 48 Дж/К В реакции образования аммиака – N 2(г) + 3 H 2(г) = 2 NH 3(г) ; ΔS 0298 = - 103, 1 Дж/К Объем системы уменьшается, поэтому и энтропия понижается (ΔS < 0). С уменьшением энтропии (ΔS < 0) протекают реакции: – 3 H 2(г) + N 2(г) = 2 NH 3(г) – 2 H 2(г) + О 2(г) = 2 H 2 O(ж)
Реакции с изменением энтропии – С увеличением энтропии (ΔS > 0) протекают также реакции: – 2 Н 2 О(г) = 2 Н 2(г) + О 2(г) – 2 Н 2 О 2(ж)= 2 Н 2 О(ж) + О 2(г) – Са. СО 3(к) = Са. О(к) + СО 2(г) , ΔS 0298 = 160, 48 Дж/К В реакции образования аммиака – N 2(г) + 3 H 2(г) = 2 NH 3(г) ; ΔS 0298 = - 103, 1 Дж/К Объем системы уменьшается, поэтому и энтропия понижается (ΔS < 0). С уменьшением энтропии (ΔS < 0) протекают реакции: – 3 H 2(г) + N 2(г) = 2 NH 3(г) – 2 H 2(г) + О 2(г) = 2 H 2 O(ж)
 Пример расчета энтропии Рассчитайте и объясните изменение энтропии для процесса 2 SO 2(г) + O 2(г) = 2 SO 2(г) Решение. Выпишем из Прил. значения стандартных энтропий веществ соединение SO 2(г) SO 3 г) S 0 , Дж/(К·моль 248, 1 205, 04 256, 23 Согласно следствию из закона Гесса, ΔS 0 = 2 S 0 SO 3(г) – ( 2 S 0 SO 2(г) + S 0 O 2(г) ) = 2 · 256, 23 – (2 · 248, 1 + 205, 04) = - 188, 78 Дж/К. Так как ΔS < 0, энтропия уменьшается вследствии уменьшения объема системы, т. е. уменьшения числа молей газообразных веществ (в левой части 3 моль газообразных веществ, в правой – 2 моль).
Пример расчета энтропии Рассчитайте и объясните изменение энтропии для процесса 2 SO 2(г) + O 2(г) = 2 SO 2(г) Решение. Выпишем из Прил. значения стандартных энтропий веществ соединение SO 2(г) SO 3 г) S 0 , Дж/(К·моль 248, 1 205, 04 256, 23 Согласно следствию из закона Гесса, ΔS 0 = 2 S 0 SO 3(г) – ( 2 S 0 SO 2(г) + S 0 O 2(г) ) = 2 · 256, 23 – (2 · 248, 1 + 205, 04) = - 188, 78 Дж/К. Так как ΔS < 0, энтропия уменьшается вследствии уменьшения объема системы, т. е. уменьшения числа молей газообразных веществ (в левой части 3 моль газообразных веществ, в правой – 2 моль).
 Энергия Гиббса
Энергия Гиббса
 Направление протекания хим. р-ции – Если ΔG < 0, реакция может протекать самопроизвольно в прямом направлении. – Если энергия Гиббса ΔG > 0, реакция самопроизвольно в прямом направлении протекать не может. – Если ΔG=0, система находится в состоянии химического равновесия, энтальпийный и энтропийный факторы равны (ΔH = T * ΔS ). Температура, при которой ΔG = 0, называется температурой начала реакции: T = ΔH /ΔS. При этой температуре и прямая и обратная реакция равновероятны.
Направление протекания хим. р-ции – Если ΔG < 0, реакция может протекать самопроизвольно в прямом направлении. – Если энергия Гиббса ΔG > 0, реакция самопроизвольно в прямом направлении протекать не может. – Если ΔG=0, система находится в состоянии химического равновесия, энтальпийный и энтропийный факторы равны (ΔH = T * ΔS ). Температура, при которой ΔG = 0, называется температурой начала реакции: T = ΔH /ΔS. При этой температуре и прямая и обратная реакция равновероятны.
 Пример расчета ΔG Исходя из значений ΔH 0 и ΔS 0 рассчитайте ΔG 0 реакции Сu 2 S(к) + 2 O 2(г) = 2 Cu. O(к) + SO 2(г) Укажите возможность ее протекания в стандартных условиях в закрытой системе. Решение: Изменение свободной энергии Гиббса в химической реакции при стандартных условиях ( Т = 298 К, Р = 101325 Па ) рассчитывается по уравнению ΔG 0 = ΔH 0 – T *ΔS 0. Тепловой эффект химической реакции ΔH 0 = - 545, 5 к. Дж (см. расчет выше). Изменение энтропии в химической реакции ΔS 0 = -9, 1 Дж/К (см. расчет выше). Изменение свободной энергии Гиббса в химической реакции ΔG 0 = ΔH 0 - T·ΔS 0 = - 545, 5 – [298 (9, 1)10 -3] = -548, 21 к. Дж. Так как ΔG 0 < 0, следовательно, в стандартных условиях самопроизвольное протекание данной химической реакции в прямом направлении возможно.
Пример расчета ΔG Исходя из значений ΔH 0 и ΔS 0 рассчитайте ΔG 0 реакции Сu 2 S(к) + 2 O 2(г) = 2 Cu. O(к) + SO 2(г) Укажите возможность ее протекания в стандартных условиях в закрытой системе. Решение: Изменение свободной энергии Гиббса в химической реакции при стандартных условиях ( Т = 298 К, Р = 101325 Па ) рассчитывается по уравнению ΔG 0 = ΔH 0 – T *ΔS 0. Тепловой эффект химической реакции ΔH 0 = - 545, 5 к. Дж (см. расчет выше). Изменение энтропии в химической реакции ΔS 0 = -9, 1 Дж/К (см. расчет выше). Изменение свободной энергии Гиббса в химической реакции ΔG 0 = ΔH 0 - T·ΔS 0 = - 545, 5 – [298 (9, 1)10 -3] = -548, 21 к. Дж. Так как ΔG 0 < 0, следовательно, в стандартных условиях самопроизвольное протекание данной химической реакции в прямом направлении возможно.
 Химическая кинетика - это учение о скоростях и механизмах химических реакций – Гомогенная химическая реакция протекает в гомогенной системе (в пределах одной фазы). Гомогенные реакции идут во всем объеме системы. Например, при взаимодействии серной кислоты и тиосульфата натрия образуется сера, которая вызывает помутнение во всем объеме раствора: H 2 SO 4 + Na 2 S 2 O 3 = Na 2 SO 4 + H 2 O + SO 2 + S – Гетерогенная химическая реакция протекает между веществами, образующими гетерогенную систему. Такие вещества образуют различные фазы, поэтому реакция идет на поверхности раздела фаз. Например, растворение металла в кислоте идет на поверхности металла: Fe +2 HCl = Fe. Cl 2 + H 2
Химическая кинетика - это учение о скоростях и механизмах химических реакций – Гомогенная химическая реакция протекает в гомогенной системе (в пределах одной фазы). Гомогенные реакции идут во всем объеме системы. Например, при взаимодействии серной кислоты и тиосульфата натрия образуется сера, которая вызывает помутнение во всем объеме раствора: H 2 SO 4 + Na 2 S 2 O 3 = Na 2 SO 4 + H 2 O + SO 2 + S – Гетерогенная химическая реакция протекает между веществами, образующими гетерогенную систему. Такие вещества образуют различные фазы, поэтому реакция идет на поверхности раздела фаз. Например, растворение металла в кислоте идет на поверхности металла: Fe +2 HCl = Fe. Cl 2 + H 2
 Скорость химической реакции - изменение концентрации одного из исходных веществ или конечных продуктов в единицу времени. Скорость гомогенной и скорость гетерогенной реакции определяются различно: - для гомогенной реакции скорость рассчитывается через количество вещества, вступившего в реакцию или образовавшегося при реакции в единицу времени в единице объема: рассчитывается =dc/d и измеряется в моль л∙с. - для гетерогенной реакции скорость рассчитывается по выражению = dc/S∙d и измеряется в моль м 2∙с. Скорость реакции может быть измерена также по изменению объема выделяющегося газа, изменению количества образующегося осадка, вязкости раствора, его оптической плотности, р. Н раствора, электропроводности и др.
Скорость химической реакции - изменение концентрации одного из исходных веществ или конечных продуктов в единицу времени. Скорость гомогенной и скорость гетерогенной реакции определяются различно: - для гомогенной реакции скорость рассчитывается через количество вещества, вступившего в реакцию или образовавшегося при реакции в единицу времени в единице объема: рассчитывается =dc/d и измеряется в моль л∙с. - для гетерогенной реакции скорость рассчитывается по выражению = dc/S∙d и измеряется в моль м 2∙с. Скорость реакции может быть измерена также по изменению объема выделяющегося газа, изменению количества образующегося осадка, вязкости раствора, его оптической плотности, р. Н раствора, электропроводности и др.
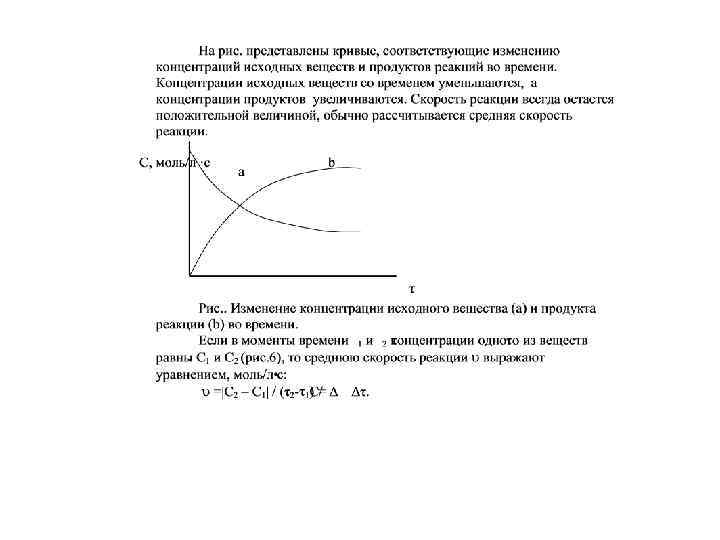
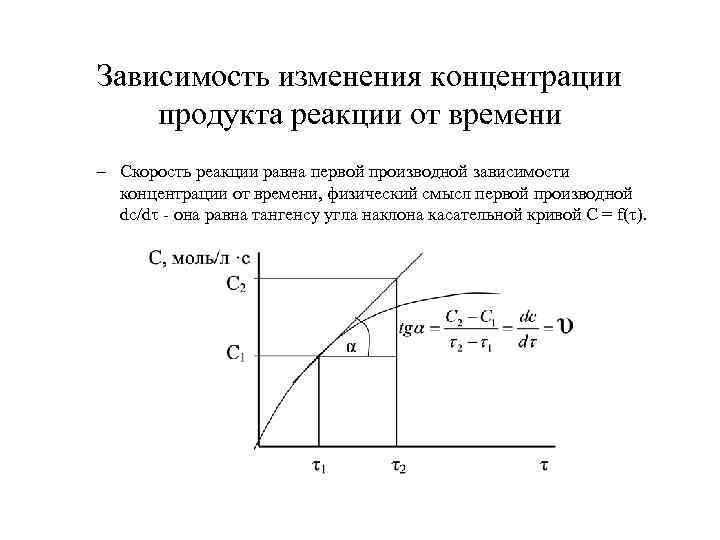 Зависимость изменения концентрации продукта реакции от времени – Скорость реакции равна первой производной зависимости концентрации от времени, физический смысл первой производной dc/d - она равна тангенсу угла наклона касательной кривой С = f(τ).
Зависимость изменения концентрации продукта реакции от времени – Скорость реакции равна первой производной зависимости концентрации от времени, физический смысл первой производной dc/d - она равна тангенсу угла наклона касательной кривой С = f(τ).
 Факторы, влияющие на скорость химической реакции • • • природа реагирующих веществ; условия протекания реакции; концентрация С; температура t; присутствие катализаторов; др. факторы(давление - для газовых р-ций, измельчение - для твердых веществ, радиоактивное облучение и т. д. )
Факторы, влияющие на скорость химической реакции • • • природа реагирующих веществ; условия протекания реакции; концентрация С; температура t; присутствие катализаторов; др. факторы(давление - для газовых р-ций, измельчение - для твердых веществ, радиоактивное облучение и т. д. )
 Зависимость скорости реакции от концентрации реагирующих веществ Закон действия масс (закон действующих масс), сформулирован К. Гульдбергом и П. Ваге, 1867 г. : скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ. Так скорость реакции А + В = С = k·СА·Св , или = k [A] · [B], где СА , Св , [A] , [B] – молярные концентрации веществ А и В, k - коэффициент пропорциональности, константа скорости данной реакции, численно равна скорости реакции при концентрациях равных 1 мольл. Скорость реакции 2 А + В = А 2 В протекает путем тройного столкновения: А + В = А 2 В в соответствии с законом действия масс можно записать: = k · СА· Св = k ·с. А 2· св или = k · [A]2 ·[B]
Зависимость скорости реакции от концентрации реагирующих веществ Закон действия масс (закон действующих масс), сформулирован К. Гульдбергом и П. Ваге, 1867 г. : скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ. Так скорость реакции А + В = С = k·СА·Св , или = k [A] · [B], где СА , Св , [A] , [B] – молярные концентрации веществ А и В, k - коэффициент пропорциональности, константа скорости данной реакции, численно равна скорости реакции при концентрациях равных 1 мольл. Скорость реакции 2 А + В = А 2 В протекает путем тройного столкновения: А + В = А 2 В в соответствии с законом действия масс можно записать: = k · СА· Св = k ·с. А 2· св или = k · [A]2 ·[B]
 Пример: Написать выражение скорости реакции окисления оксида азота (II): 2 NO(г) + O 2(г) = 2 NO 2(г) Как изменится скорость этой реакции, если концентрацию NO увеличить в два раза? Решение: В соответствии с законом действия масс скорость реакции: = k·с. NO 2 ·с. O 2 или = k·[NO]2· [O 2] После увеличения концентрации газа NO в два раза его новую концентрацию можно записать: [NO]' = [2 NO], тогда выражение скорости реакции принимает вид: ' = k·с'NO 2 ·с. O 2 или ' = k ·[NO]'2·[O 2] = k ·[2 NO]2 ·[O 2] = 4 k· [NO]2 · [O 2] = 4 то есть скорость химической реакции возросла в 4 раза.
Пример: Написать выражение скорости реакции окисления оксида азота (II): 2 NO(г) + O 2(г) = 2 NO 2(г) Как изменится скорость этой реакции, если концентрацию NO увеличить в два раза? Решение: В соответствии с законом действия масс скорость реакции: = k·с. NO 2 ·с. O 2 или = k·[NO]2· [O 2] После увеличения концентрации газа NO в два раза его новую концентрацию можно записать: [NO]' = [2 NO], тогда выражение скорости реакции принимает вид: ' = k·с'NO 2 ·с. O 2 или ' = k ·[NO]'2·[O 2] = k ·[2 NO]2 ·[O 2] = 4 k· [NO]2 · [O 2] = 4 то есть скорость химической реакции возросла в 4 раза.
 Зависимость скорости реакции от температуры определяется правилом Вант-Гоффа: При повышении температуры на каждые 100 С скорость большинства реакций увеличивается в 2 -4 раза. Математически зависимость скорости реакции от температуры выражается правилом Вант-Гоффа: (t 2) = (t 1) γ(t 2 -t 1)/10 где (t 2) и (t 1) – скорости химической реакции при температурах t 2 и t 1 соответственно, γ - температурный коэффициент скорости реакции. Физический смысл γ - показывает, во сколько раз возрастает скорость данной реакции при повышении температуры системы на 100 С. Для большинства реакций температурный коэффициент лежит в пределах от 2 до 4.
Зависимость скорости реакции от температуры определяется правилом Вант-Гоффа: При повышении температуры на каждые 100 С скорость большинства реакций увеличивается в 2 -4 раза. Математически зависимость скорости реакции от температуры выражается правилом Вант-Гоффа: (t 2) = (t 1) γ(t 2 -t 1)/10 где (t 2) и (t 1) – скорости химической реакции при температурах t 2 и t 1 соответственно, γ - температурный коэффициент скорости реакции. Физический смысл γ - показывает, во сколько раз возрастает скорость данной реакции при повышении температуры системы на 100 С. Для большинства реакций температурный коэффициент лежит в пределах от 2 до 4.



