12 Энтропия.pptx
- Количество слайдов: 51
 ЭНТРОПИЯ 1
ЭНТРОПИЯ 1
 ЭНТРОПИЯ Принцип существования энтропии В середине XIX века было сделано существенное открытие, касающееся обратимых термодинамических процессов. Оказалось, что наряду с внутренней энергией у тела имеется еще одна замеча тельная функция состояния – энтропия. Также, как и внутренняя энергия, энтропия определяется с точностью до произвольной по стоянной. Опыт дает значение приращения энтропии. 2
ЭНТРОПИЯ Принцип существования энтропии В середине XIX века было сделано существенное открытие, касающееся обратимых термодинамических процессов. Оказалось, что наряду с внутренней энергией у тела имеется еще одна замеча тельная функция состояния – энтропия. Также, как и внутренняя энергия, энтропия определяется с точностью до произвольной по стоянной. Опыт дает значение приращения энтропии. 2
 ЭНТРОПИЯ Принцип существования энтропии • 3
ЭНТРОПИЯ Принцип существования энтропии • 3
 ЭНТРОПИЯ Принцип существования энтропии Утверждение о существовании функции, дифференциал которой есть DQ /T, носит название принципа существования энтропии и является одним из важнейших законов природы. В частности, оно является существенной частью второго начала термодинамики, о чем мы еще поговорим. Открытие этого принципа, как и всего второго начала термодинамики, связано, прежде всего, с именами Карно и Клаузиуса. 4
ЭНТРОПИЯ Принцип существования энтропии Утверждение о существовании функции, дифференциал которой есть DQ /T, носит название принципа существования энтропии и является одним из важнейших законов природы. В частности, оно является существенной частью второго начала термодинамики, о чем мы еще поговорим. Открытие этого принципа, как и всего второго начала термодинамики, связано, прежде всего, с именами Карно и Клаузиуса. 4
 ЭНТРОПИЯ Принцип существования энтропии • 5
ЭНТРОПИЯ Принцип существования энтропии • 5
 ЭНТРОПИЯ Принцип существования энтропии • 6
ЭНТРОПИЯ Принцип существования энтропии • 6
 ЭНТРОПИЯ Принцип существования энтропии • 7
ЭНТРОПИЯ Принцип существования энтропии • 7
 ЭНТРОПИЯ Принцип существования энтропии За нуль энтропии может быть принято значение энтропии любого состояния (кипящей воды, плавящегося льда). Однако в некоторых случаях принимают за нуль значение энтропии вещества при аб солютном нуле температуры. Для этого, впрочем, имеются некоторые теоретические основания (теорема Нернста), на которых мы оста навливаться не будем. Приняв S = 0 при Т = 0, энтропию вещества при температуре Т можно найти по формуле 8
ЭНТРОПИЯ Принцип существования энтропии За нуль энтропии может быть принято значение энтропии любого состояния (кипящей воды, плавящегося льда). Однако в некоторых случаях принимают за нуль значение энтропии вещества при аб солютном нуле температуры. Для этого, впрочем, имеются некоторые теоретические основания (теорема Нернста), на которых мы оста навливаться не будем. Приняв S = 0 при Т = 0, энтропию вещества при температуре Т можно найти по формуле 8
 ЭНТРОПИЯ Принцип существования энтропии • 9
ЭНТРОПИЯ Принцип существования энтропии • 9
 ЭНТРОПИЯ Принцип существования энтропии • 10
ЭНТРОПИЯ Принцип существования энтропии • 10
 ЭНТРОПИЯ Принцип существования энтропии • 11
ЭНТРОПИЯ Принцип существования энтропии • 11
 ЭНТРОПИЯ Принцип возрастания энтропии Как уже говорилось, обратимых процессов, строго говоря, не существует, хотя с точностью, доступной опыту, можно осуществить множество процессов, практически неотличимых от обратимых. Имеются, однако, примеры процессов, которые всегда односторонни и уже поэтому никоим образом не могут быть обращены. Так, на пример, газ может расшириться сам по себе, но не может сжиматься без приложения внешних сил. 12
ЭНТРОПИЯ Принцип возрастания энтропии Как уже говорилось, обратимых процессов, строго говоря, не существует, хотя с точностью, доступной опыту, можно осуществить множество процессов, практически неотличимых от обратимых. Имеются, однако, примеры процессов, которые всегда односторонни и уже поэтому никоим образом не могут быть обращены. Так, на пример, газ может расшириться сам по себе, но не может сжиматься без приложения внешних сил. 12
 ЭНТРОПИЯ Принцип возрастания энтропии Тепло может самопроизвольно пере ходить от горячего тела к холодному и только при затрате работы (например, электроэнергии) может переходить от холодного тела к более нагретому. При трении кинетическая энергия макроскопического движения всегда превращается во внутреннюю энергию, но никогда не происходит самопроизвольный обратный процесс. 13
ЭНТРОПИЯ Принцип возрастания энтропии Тепло может самопроизвольно пере ходить от горячего тела к холодному и только при затрате работы (например, электроэнергии) может переходить от холодного тела к более нагретому. При трении кинетическая энергия макроскопического движения всегда превращается во внутреннюю энергию, но никогда не происходит самопроизвольный обратный процесс. 13
 ЭНТРОПИЯ Принцип возрастания энтропии Не обратимость сех остальных процессов в в конечном счете связана с тем, что в каждом из них в той или иной степени присутствует один из перечисленных односторонних процессов. В реальных процессах невозможно избежать ни самопроизвольных расширений, ни тре ния, ни теплового рассеяния. Нет ли какого нибудь общего признака у всех перечисленных односторонних процессов? 14
ЭНТРОПИЯ Принцип возрастания энтропии Не обратимость сех остальных процессов в в конечном счете связана с тем, что в каждом из них в той или иной степени присутствует один из перечисленных односторонних процессов. В реальных процессах невозможно избежать ни самопроизвольных расширений, ни тре ния, ни теплового рассеяния. Нет ли какого нибудь общего признака у всех перечисленных односторонних процессов? 14
 ЭНТРОПИЯ Принцип возрастания энтропии • 15
ЭНТРОПИЯ Принцип возрастания энтропии • 15
 ЭНТРОПИЯ Принцип возрастания энтропии • 16
ЭНТРОПИЯ Принцип возрастания энтропии • 16
 ЭНТРОПИЯ Принцип возрастания энтропии • 17
ЭНТРОПИЯ Принцип возрастания энтропии • 17
 ЭНТРОПИЯ Принцип возрастания энтропии Нетрудно понять, какое значение имеет этот вывод для всех необратимых процессов. Так каждый необратимый процесс со провождается односторонними явлениями, идущими с повышением энтропии, то прирост энтропии в необратимом процессе будет завы шен против того прироста, который имел бы место при обратимом переходе. Пусть DQ — тепло, полученное телом при температуре Т в интересующем нас необратимом процессе. 18
ЭНТРОПИЯ Принцип возрастания энтропии Нетрудно понять, какое значение имеет этот вывод для всех необратимых процессов. Так каждый необратимый процесс со провождается односторонними явлениями, идущими с повышением энтропии, то прирост энтропии в необратимом процессе будет завы шен против того прироста, который имел бы место при обратимом переходе. Пусть DQ — тепло, полученное телом при температуре Т в интересующем нас необратимом процессе. 18
 ЭНТРОПИЯ Принцип возрастания энтропии • 19
ЭНТРОПИЯ Принцип возрастания энтропии • 19
 ЭНТРОПИЯ Принцип возрастания энтропии • 20
ЭНТРОПИЯ Принцип возрастания энтропии • 20
 ЭНТРОПИЯ Принцип возрастания энтропии • 21
ЭНТРОПИЯ Принцип возрастания энтропии • 21
 ЭНТРОПИЯ Принцип возрастания энтропии Далее будет показано, что процессы молекулярного упорядоче ния связаны с уменьшением энтропии. Живой организм из неупоря доченной системы малых молекул, получаемых в процессах пита ния и дыхания, конструирует высокоорганизованные постройки – биологические макромолекулы. При этом энтропия орга низма падает. 22
ЭНТРОПИЯ Принцип возрастания энтропии Далее будет показано, что процессы молекулярного упорядоче ния связаны с уменьшением энтропии. Живой организм из неупоря доченной системы малых молекул, получаемых в процессах пита ния и дыхания, конструирует высокоорганизованные постройки – биологические макромолекулы. При этом энтропия орга низма падает. 22
 ЭНТРОПИЯ Принцип возрастания энтропии • 23
ЭНТРОПИЯ Принцип возрастания энтропии • 23
 ЭНТРОПИЯ Принцип возрастания энтропии Можно сказать, что жизнедеятельность организма состоит в пропускании через себя потока энтропии вещества. При этом энтропия вещества, входящего в организм, меньше энтропии, отдавае мой среде, — организм деградирует продукты питания. 24
ЭНТРОПИЯ Принцип возрастания энтропии Можно сказать, что жизнедеятельность организма состоит в пропускании через себя потока энтропии вещества. При этом энтропия вещества, входящего в организм, меньше энтропии, отдавае мой среде, — организм деградирует продукты питания. 24
 ЭНТРОПИЯ Принцип действия тепловой машины Тепловая машина превращает тепло в работу, иначе говоря, забирает тепло от одних тел и передает его другим телам в форме механической работы. Для того чтобы осуществить это превращение, надо располагать двумя различно нагретыми телами, между которы ми возможен теплообмен. Для краткости будем называть более горячее тело нагревателем, а более холодное — холодильником. 25
ЭНТРОПИЯ Принцип действия тепловой машины Тепловая машина превращает тепло в работу, иначе говоря, забирает тепло от одних тел и передает его другим телам в форме механической работы. Для того чтобы осуществить это превращение, надо располагать двумя различно нагретыми телами, между которы ми возможен теплообмен. Для краткости будем называть более горячее тело нагревателем, а более холодное — холодильником. 25
 ЭНТРОПИЯ Принцип действия тепловой машины При наличии таких двух тел процесс превращения тепла в работу рисуется следующим образом: способное расшириться тело (рабочее тело) приводится в контакт с нагревателем. Тепло Q 1 отбирается от нагревателя и затрачивается на работу расширения А 1 которая отдается окружающим телам. Далее рабочее тело при водится в контакт с холодильником, которому оно отдает тепло Q 2 за счет работы А 2, совершаемой внешними силами над рабочим телом. 26
ЭНТРОПИЯ Принцип действия тепловой машины При наличии таких двух тел процесс превращения тепла в работу рисуется следующим образом: способное расшириться тело (рабочее тело) приводится в контакт с нагревателем. Тепло Q 1 отбирается от нагревателя и затрачивается на работу расширения А 1 которая отдается окружающим телам. Далее рабочее тело при водится в контакт с холодильником, которому оно отдает тепло Q 2 за счет работы А 2, совершаемой внешними силами над рабочим телом. 26
 ЭНТРОПИЯ Принцип действия тепловой машины Чтобы получить непрерывно действующую те о ую машину, необходимо закончить такт пл в сжатия в той точке, в которой начался такт расширения; короче говоря, процесс должен быть ци и е им. Рабочее тело по проведении кл ч ск каждого цикла возвращается в исходное состояние. Закон сохранения энергии требует поэтому, чтобы энер гия, полученная от окружающих тел, равнялась энергии, пере данной окружающим телам. От среды получено: тепло Q 1 при расширении и работа А 2 при сжатии рабочего 27
ЭНТРОПИЯ Принцип действия тепловой машины Чтобы получить непрерывно действующую те о ую машину, необходимо закончить такт пл в сжатия в той точке, в которой начался такт расширения; короче говоря, процесс должен быть ци и е им. Рабочее тело по проведении кл ч ск каждого цикла возвращается в исходное состояние. Закон сохранения энергии требует поэтому, чтобы энер гия, полученная от окружающих тел, равнялась энергии, пере данной окружающим телам. От среды получено: тепло Q 1 при расширении и работа А 2 при сжатии рабочего 27
 ЭНТРОПИЯ Принцип действия тепловой машины Среде отдано: ра бота 1 при расширении тела и А тепло Q 2 при сжатии. Следовательно, Q 1 + A 2 = Q 2 + A 1, или А 1 – A 2=Q 1 – Q 2. При проведении цикла по часовой стрелке работа сжатия меньше работы расширения. По этому последнее равенство выражает тот простой факт, что чистая работа, переданная рабочим телом внешней среде, равна разности теплот, полученной от нагревателя и отданной холодильнику. 28
ЭНТРОПИЯ Принцип действия тепловой машины Среде отдано: ра бота 1 при расширении тела и А тепло Q 2 при сжатии. Следовательно, Q 1 + A 2 = Q 2 + A 1, или А 1 – A 2=Q 1 – Q 2. При проведении цикла по часовой стрелке работа сжатия меньше работы расширения. По этому последнее равенство выражает тот простой факт, что чистая работа, переданная рабочим телом внешней среде, равна разности теплот, полученной от нагревателя и отданной холодильнику. 28
 ЭНТРОПИЯ Принцип действия тепловой машины • 29
ЭНТРОПИЯ Принцип действия тепловой машины • 29
 ЭНТРОПИЯ Принцип действия тепловой машины Нагревателем служит паровой котел или, в двигателях внутреннего сгорания, горючая смесь. Те же три системы являются необходимыми и для холодильной машины, в которой цикл протекает в обратную сторону. Принцип работы этой машины заключается в следующем: расширение рабочего тела производится тогда, когда оно находится в контакте с холо дильником. Этим холодное тело охлаждается еще больше, что и является задачей холодильной машины. 30
ЭНТРОПИЯ Принцип действия тепловой машины Нагревателем служит паровой котел или, в двигателях внутреннего сгорания, горючая смесь. Те же три системы являются необходимыми и для холодильной машины, в которой цикл протекает в обратную сторону. Принцип работы этой машины заключается в следующем: расширение рабочего тела производится тогда, когда оно находится в контакте с холо дильником. Этим холодное тело охлаждается еще больше, что и является задачей холодильной машины. 30
 ЭНТРОПИЯ Принцип действия тепловой машины Далее, чтобы цикл стал воз можным, нужно произвести сжатие рабочего тела и передать тепло, полученное от холодильника. Это выполняется при контакте ра бочего тела с нагревателем. Таким образом, более горячее тело на гревается еще больше. «Противоестественный» переход тепла от те ла менее нагретого к телу более нагретому «оплачивается» работой. 31
ЭНТРОПИЯ Принцип действия тепловой машины Далее, чтобы цикл стал воз можным, нужно произвести сжатие рабочего тела и передать тепло, полученное от холодильника. Это выполняется при контакте ра бочего тела с нагревателем. Таким образом, более горячее тело на гревается еще больше. «Противоестественный» переход тепла от те ла менее нагретого к телу более нагретому «оплачивается» работой. 31
 ЭНТРОПИЯ Принцип действия тепловой машины Действительно, при совершении цикла против часовой стрелки ра венство энергии, переданной среде, и энергии, отнятой от среды (т. е. Q 1+A 2 = Q 2 + A 1 или Q 2 – Q 1 = – (A 1 – A 2), где мы по прежнему индекс 1 относим к части процесса, протекающей при контакте с более горячим телом), имеет следующий смысл: количество тепла, отнятое от системы, должно быть скомпенсировано равным количе ством механической работы. 32
ЭНТРОПИЯ Принцип действия тепловой машины Действительно, при совершении цикла против часовой стрелки ра венство энергии, переданной среде, и энергии, отнятой от среды (т. е. Q 1+A 2 = Q 2 + A 1 или Q 2 – Q 1 = – (A 1 – A 2), где мы по прежнему индекс 1 относим к части процесса, протекающей при контакте с более горячим телом), имеет следующий смысл: количество тепла, отнятое от системы, должно быть скомпенсировано равным количе ством механической работы. 32
 ЭНТРОПИЯ Принцип действия тепловой машины • 33
ЭНТРОПИЯ Принцип действия тепловой машины • 33
 ЭНТРОПИЯ Принцип действия тепловой машины • 34
ЭНТРОПИЯ Принцип действия тепловой машины • 34
 ЭНТРОПИЯ Принцип действия тепловой машины Подсчитывая значения этих интегралов для конкретных процессов, можно в ряде случаев довольно просто найти значение максимального коэффициента по лезного действия того или иного цикла тепловой машины. 35
ЭНТРОПИЯ Принцип действия тепловой машины Подсчитывая значения этих интегралов для конкретных процессов, можно в ряде случаев довольно просто найти значение максимального коэффициента по лезного действия того или иного цикла тепловой машины. 35
 ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. Сейчас мы задаемся целью найти выражение предельно большого коэффициента полезного действия тепловой машины, достижимого для идеальной машины, работающей без потерь на обратимом цикле. Прежде всего рассмотрим теоретический четырехтактный цикл Карно, изображенный на 36 рисунке.
ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. Сейчас мы задаемся целью найти выражение предельно большого коэффициента полезного действия тепловой машины, достижимого для идеальной машины, работающей без потерь на обратимом цикле. Прежде всего рассмотрим теоретический четырехтактный цикл Карно, изображенный на 36 рисунке.
 ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. Цикл Карно состоит из двух изотерм (для температур T 1 и Т 2) и двух адиабат. Первым тактом процесса пусть будет изотермическое расширение от состояния 1 к состоянию 2 – рабочее тело находится в контакте с нагревателем, имеющим температуру Т 1, и процесс проводится весьма медленно. 37
ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. Цикл Карно состоит из двух изотерм (для температур T 1 и Т 2) и двух адиабат. Первым тактом процесса пусть будет изотермическое расширение от состояния 1 к состоянию 2 – рабочее тело находится в контакте с нагревателем, имеющим температуру Т 1, и процесс проводится весьма медленно. 37
 ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. По достижении состояния 2 контакт с нагревателем нарушается, тело теплоизолируется и ему предоставляется возмож ность дополнительно расшириться. Работа производится за счет внутренней энергии и температура тела пусть падает до Т 2. Начиная с этой точки (состояние 3) на чинается двухтактное 38 сжатие.
ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. По достижении состояния 2 контакт с нагревателем нарушается, тело теплоизолируется и ему предоставляется возмож ность дополнительно расшириться. Работа производится за счет внутренней энергии и температура тела пусть падает до Т 2. Начиная с этой точки (состояние 3) на чинается двухтактное 38 сжатие.
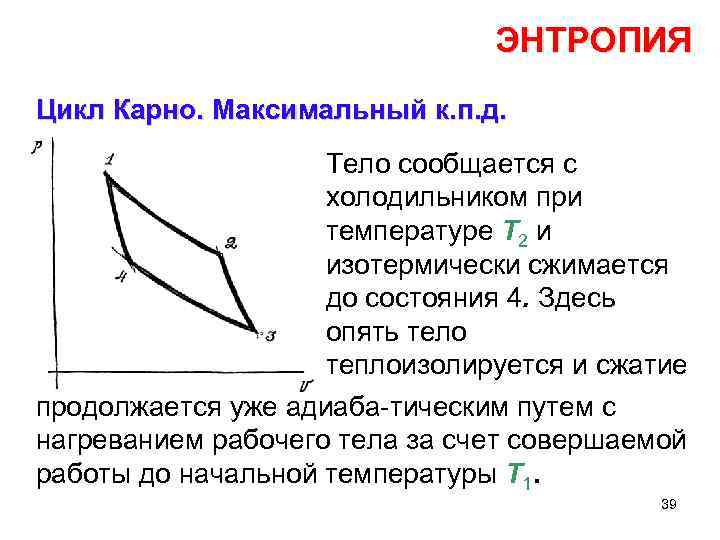 ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. Тело сообщается с холодильником при температуре Т 2 и изотермически сжимается до состояния 4. Здесь опять тело теплоизолируется и сжатие продолжается уже адиаба тическим путем с нагреванием рабочего тела за счет совершаемой работы до начальной температуры Т 1. 39
ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. Тело сообщается с холодильником при температуре Т 2 и изотермически сжимается до состояния 4. Здесь опять тело теплоизолируется и сжатие продолжается уже адиаба тическим путем с нагреванием рабочего тела за счет совершаемой работы до начальной температуры Т 1. 39
 ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. Адиабатические процессы в цикле Карно носят вспомогательный характер: они помогают перейти с одной изотермы на другую. В энер гетическом балансе эти процессы не участвуют, так как работа ади абатического расширения v(T 1 c —Т 2) и работа сжатия cv(T 2 – Т 1) компенсируют друга. 40
ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. Адиабатические процессы в цикле Карно носят вспомогательный характер: они помогают перейти с одной изотермы на другую. В энер гетическом балансе эти процессы не участвуют, так как работа ади абатического расширения v(T 1 c —Т 2) и работа сжатия cv(T 2 – Т 1) компенсируют друга. 40
 ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. • 41
ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. • 41
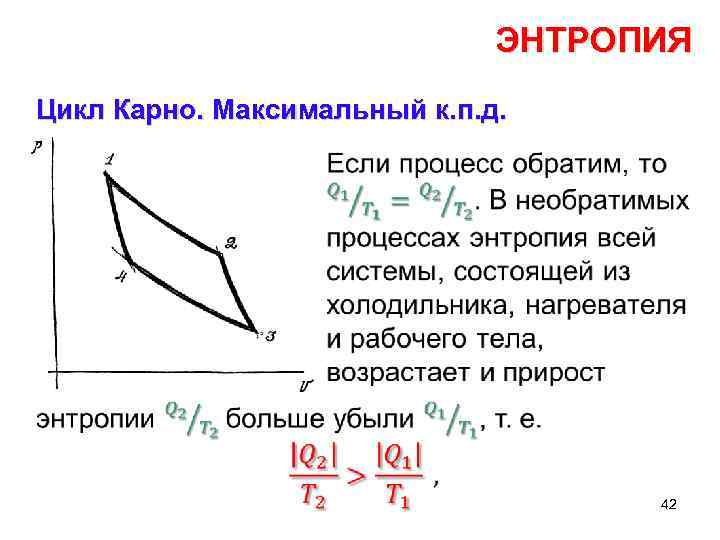 ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. • 42
ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. • 42
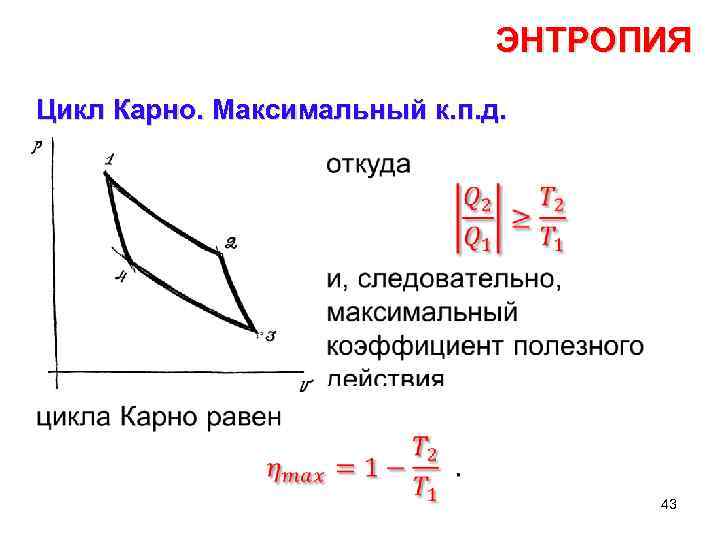 ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. • 43
ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. • 43
 ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. К. п. д. цикла определяется температурами холодиль ника и нагревателя. Чем больше перепад темпера туры, тем выше к. п. д. машины. Нетрудно видеть, что коэффи циент олезно п го действия цикла Карно дает оптимальное значение к. п. д. Нет лучшего цикла, чем цикл Карно. 44
ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. К. п. д. цикла определяется температурами холодиль ника и нагревателя. Чем больше перепад темпера туры, тем выше к. п. д. машины. Нетрудно видеть, что коэффи циент олезно п го действия цикла Карно дает оптимальное значение к. п. д. Нет лучшего цикла, чем цикл Карно. 44
 ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. Формула максимального к. п. д. показывает причину низкого к. п. д. паровых машин. При T 2 = 300 К и T 1 = 400 К к. п. д. равен 25%. Однако это – максималь ный к. п. д. , он достижим для идеальной машины, работающей обра тимо без каких бы то ни было потерь энергии. Не приходится удив ляться, что в реальных паровых 45 машинах к. п. д. ниже 10%.
ЭНТРОПИЯ Цикл Карно. Максимальный к. п. д. Формула максимального к. п. д. показывает причину низкого к. п. д. паровых машин. При T 2 = 300 К и T 1 = 400 К к. п. д. равен 25%. Однако это – максималь ный к. п. д. , он достижим для идеальной машины, работающей обра тимо без каких бы то ни было потерь энергии. Не приходится удив ляться, что в реальных паровых 45 машинах к. п. д. ниже 10%.
 ЭНТРОПИЯ Второе начало термодинамики Как уже было сказано, второе начало термодинамики состоит в утверждении, что энтропия в теплоизолированной системе возра стает. Это утверждение может показаться несколько абстрактным. Кроме того, приведенная формулировка не соответствует истори ческому развитию идей. Имея в виду огромную значимость этого закона природы, надо кратко остановиться на других существующих формулировках второго начала термодинамики и показать их экви валентность приведенной выше. 46
ЭНТРОПИЯ Второе начало термодинамики Как уже было сказано, второе начало термодинамики состоит в утверждении, что энтропия в теплоизолированной системе возра стает. Это утверждение может показаться несколько абстрактным. Кроме того, приведенная формулировка не соответствует истори ческому развитию идей. Имея в виду огромную значимость этого закона природы, надо кратко остановиться на других существующих формулировках второго начала термодинамики и показать их экви валентность приведенной выше. 46
 ЭНТРОПИЯ Второе начало термодинамики Исторически второе начало термодинамики вошло в науку в виде постулата Томсона о невоз можности создания вечного двигателя второго рода. Вечным двигателем первого рода называ Вечным двигателем первого рода ют машину, создающую работу «из ничего» , т. е. машину, работа которой нару шает первое начало термодинамики. Вечным двигателем второго рода называют такой двигатель, который рода производит работу при помощи периодически действующей машины за счет одного лишь отнятия теплоты от окружающей среды. 47
ЭНТРОПИЯ Второе начало термодинамики Исторически второе начало термодинамики вошло в науку в виде постулата Томсона о невоз можности создания вечного двигателя второго рода. Вечным двигателем первого рода называ Вечным двигателем первого рода ют машину, создающую работу «из ничего» , т. е. машину, работа которой нару шает первое начало термодинамики. Вечным двигателем второго рода называют такой двигатель, который рода производит работу при помощи периодически действующей машины за счет одного лишь отнятия теплоты от окружающей среды. 47
 ЭНТРОПИЯ Второе начало термодинамики Такой двигатель, будь он возможен, был бы практически вечным, так как запас энергии в ок ружающей среде почти безграничен и охлаждение, скажем, воды оке анов на один градус дало бы непредставимо огромную энергию. Масса воды в мировом океане по порядку величины составляет ~1018 т. При охлаждении всей этой массы воды лишь на 1° выдели лось бы 1021 ккал = 4, 18 1024 Дж тепла, что эквивалентно полному сжиганию 1014 т угля. 48
ЭНТРОПИЯ Второе начало термодинамики Такой двигатель, будь он возможен, был бы практически вечным, так как запас энергии в ок ружающей среде почти безграничен и охлаждение, скажем, воды оке анов на один градус дало бы непредставимо огромную энергию. Масса воды в мировом океане по порядку величины составляет ~1018 т. При охлаждении всей этой массы воды лишь на 1° выдели лось бы 1021 ккал = 4, 18 1024 Дж тепла, что эквивалентно полному сжиганию 1014 т угля. 48
 ЭНТРОПИЯ Второе начало термодинамики Железнодорожный состав, нагруженный этим количеством угля, растянулся бы на расстояние ~1010 км, что по порядку величины совпадает с размерами солнечной системы! Вечный двигатель второго рода – это тепловая машина, рабо тающая с нагревателем, но без холодильника. Такая машина могла бы проработать один такт — газ, находящийся в сосуде с поршнем, мог бы расшириться, но на этом работа двигателя и закончилась бы, так как 49 для продолжения действия машины тепло,
ЭНТРОПИЯ Второе начало термодинамики Железнодорожный состав, нагруженный этим количеством угля, растянулся бы на расстояние ~1010 км, что по порядку величины совпадает с размерами солнечной системы! Вечный двигатель второго рода – это тепловая машина, рабо тающая с нагревателем, но без холодильника. Такая машина могла бы проработать один такт — газ, находящийся в сосуде с поршнем, мог бы расшириться, но на этом работа двигателя и закончилась бы, так как 49 для продолжения действия машины тепло,
 ЭНТРОПИЯ Второе начало термодинамики полученное газом, необходимо передать холодильнику. Формально невозможность вечного двигателя второго рода видна из формулы максимального к. п. д. При отсутствии теплового перепада (Т 2 =Т 1) максимальное значение к. п. д. равно нулю. Невозможно осуществить периодически действующий вечный двигатель, комбинируя изотермическое расширение с адиабатиче ским процессом сжатия. Такой процесс невозможен, даже если бы удалось его сделать обратимым. 50
ЭНТРОПИЯ Второе начало термодинамики полученное газом, необходимо передать холодильнику. Формально невозможность вечного двигателя второго рода видна из формулы максимального к. п. д. При отсутствии теплового перепада (Т 2 =Т 1) максимальное значение к. п. д. равно нулю. Невозможно осуществить периодически действующий вечный двигатель, комбинируя изотермическое расширение с адиабатиче ским процессом сжатия. Такой процесс невозможен, даже если бы удалось его сделать обратимым. 50
 ЭНТРОПИЯ Второе начало термодинамики При изотермическом расширении рабочего тела энтропия падает. Значит, процесс сжатия должен приводить к возрастанию энтропии. Но этого не может сде лать адиабатический процесс, так как он проходит при постоянной энтропии. Вполне соответствует приведенной здесь формулировке второго на чала термодинамики также постулат Клаузиуса, который состоит в Клаузиуса утверждении о невозможности перехода тепла от менее нагретого тела к более нагретому без компенсации. Процесс, противоречащий постулату Клаузиуса, протекает с уменьшением энтропии. 51
ЭНТРОПИЯ Второе начало термодинамики При изотермическом расширении рабочего тела энтропия падает. Значит, процесс сжатия должен приводить к возрастанию энтропии. Но этого не может сде лать адиабатический процесс, так как он проходит при постоянной энтропии. Вполне соответствует приведенной здесь формулировке второго на чала термодинамики также постулат Клаузиуса, который состоит в Клаузиуса утверждении о невозможности перехода тепла от менее нагретого тела к более нагретому без компенсации. Процесс, противоречащий постулату Клаузиуса, протекает с уменьшением энтропии. 51


