Энергия Гиббса(Батыршин Р.А. 430151).ppt
- Количество слайдов: 12

Энергия Гиббса. Влияние температуры на направление течения реакций. Выполнил: студент гр. 430151 Батыршин Р. А. Проверила: Исхакова И. О.

Энергия Гиббса. Энергия Гиббса— это термодинамический потенциал , показывающая изменение энергии в ходе химической реакции и дающая таким образом ответ на вопрос о принципиальной возможности протекания химической реакции. Эта функция получила название в честь великого американского физика Д. У. Гиббса (1839— 1903), который вывел эту функцию, а затем использовал в термодинамических работах.

Энергия Гиббса характеризует ту часть полной энергии системы, которая может быть превращена в работу в изобарноизотермическом (или в изохорноизотермическом) процессе (так называемая полезная работа, совершаемая системой). Она так же является функцией состояния системы, их абсолютные значения не поддаются вычислению.
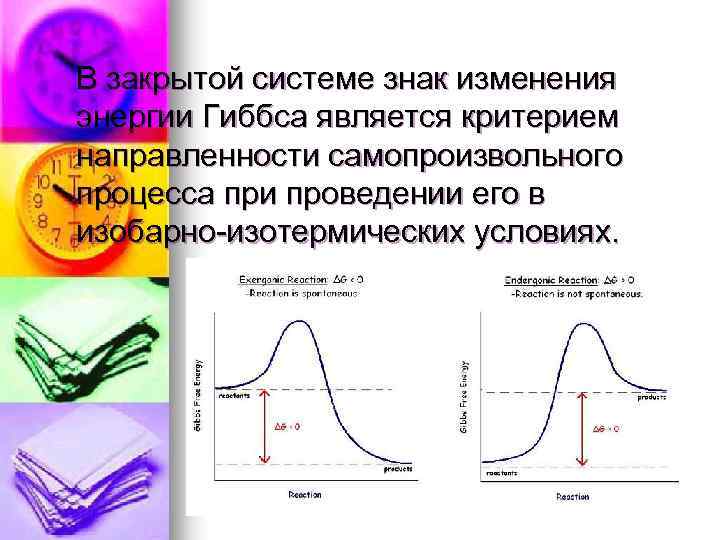
В закрытой системе знак изменения энергии Гиббса является критерием направленности самопроизвольного процесса при проведении его в изобарно-изотермических условиях.

- при ΔG = 0 система находится в состоянии термодинамического равновесия; - при ΔG < 0 процесс самопроизвольно протекает в прямом направлении, т. е. термодинамически возможен; - при ΔG > 0 самопроизвольно протекает только обратный процесс , прямой процесс термодинамически невозможен.

Стандартную энергию Гиббса химической реакции при Т = 298 К можно рассчитать двумя способами: используя уравнение Гиббса-Гельмгольца : Или через стандартные табличные данные:

Расчёт энергии Гиббса реакции, выраженной уравнением 4 NH 3(г) + 5 O 2(г) = = 4 NO(г) + 6 H 2 O(г), при температуре 298 К. Согласно условию, реакция протекает при практически реальных значениях давления и температуры. • ∆Н(298) = - 904, 8 к. Дж = - 904800 Дж. • ∆S(298). = 179, 77 Дж/К. Получаем: ∆G(298) = ∆H(298) – 298 X∆S(298) = - 904800 – 298⋅179, 77= - 958371, 46 Дж = - 958, 373 к. Дж. Полученное отрицательное значение энергии Гиббса реакции ∆G(298) указывает на то, что данная реакция в рассматриваемых условиях может протекать самопроизвольно.

Влияние температуры на направление реакции По формуле зависимости энергии Гиббса от энтропии, энтальпии и температуры очевидно, что влияние температуры определяется знаком и величиной энтропии.

1)Для реакции, протекающей с увеличением энтропии (ΔS > 0), повышение температуры уменьшает энергию Гиббса. Это есть благоприятствует протеканию процесса.

2) Для реакции, протекающей с уменьшением энтропии (ΔS < 0), с повышением температуры препятствует протеканию процесса. Это приводит к тому, что некоторые вещества при определенных температурах образуют одни соединения, а при других температурах - другие.

3) Процессы, протекающие с уменьшением энтальпии (ΔН < 0) и увеличением энтропии (ΔS > 0), практически необратимы. Вне зависимости от температуры, энергия Гиббса будет здесь отрицательной.

Конец
Энергия Гиббса(Батыршин Р.А. 430151).ppt