4_ENERGETIChES_OBMEN-2016_pptkaz.ppt
- Количество слайдов: 91
 ЭНЕРГИЯ АЛМАСУЫ. ATФ
ЭНЕРГИЯ АЛМАСУЫ. ATФ
 ДӘРІС ЖОСПАРЫ: ü Энергия алмасуы туралы түсінік. ü Энергия алмасуының сатылары. ü Көмірсулар (К), липидтер (Л) және белоктардың (Б) арнайы жолдармен ыдырауы. ü Үш карбон қышқылдарының циклі (Кребс циклі).
ДӘРІС ЖОСПАРЫ: ü Энергия алмасуы туралы түсінік. ü Энергия алмасуының сатылары. ü Көмірсулар (К), липидтер (Л) және белоктардың (Б) арнайы жолдармен ыдырауы. ü Үш карбон қышқылдарының циклі (Кребс циклі).
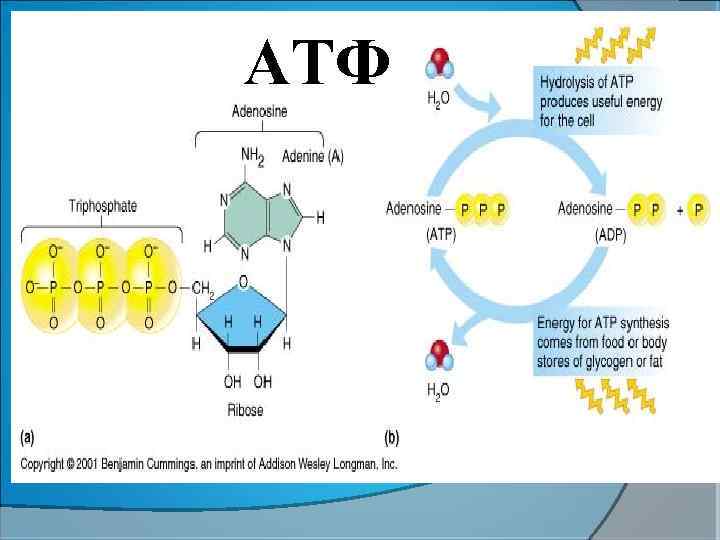 ATФ
ATФ
 ЭНЕРГИЯ АЛМАСУЫ ( ЭА)− ЭНЕРГЕТИКАЛЫҚ МАТЕРИАЛДАРДЫҢ (К, Л, Б) АҒЗАДА ТОТЫҒЫП ЭНЕРГИЯ БӨЛУІ Н/Е БЕЛГІЛІ БІР ҚОСЫЛЫС ТҮРІНДЕ СИНТЕЗДЕЛІП ЭНЕРГИЯНЫ САҚТАУЫ Ж/Е ОНЫ ТІРШІЛІК ҚАЖЕТІНЕ ПАЙДАЛАНУЫ.
ЭНЕРГИЯ АЛМАСУЫ ( ЭА)− ЭНЕРГЕТИКАЛЫҚ МАТЕРИАЛДАРДЫҢ (К, Л, Б) АҒЗАДА ТОТЫҒЫП ЭНЕРГИЯ БӨЛУІ Н/Е БЕЛГІЛІ БІР ҚОСЫЛЫС ТҮРІНДЕ СИНТЕЗДЕЛІП ЭНЕРГИЯНЫ САҚТАУЫ Ж/Е ОНЫ ТІРШІЛІК ҚАЖЕТІНЕ ПАЙДАЛАНУЫ.
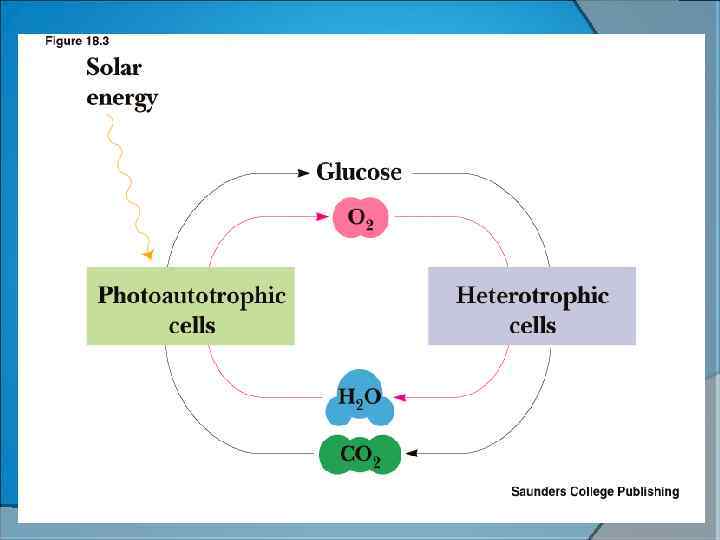
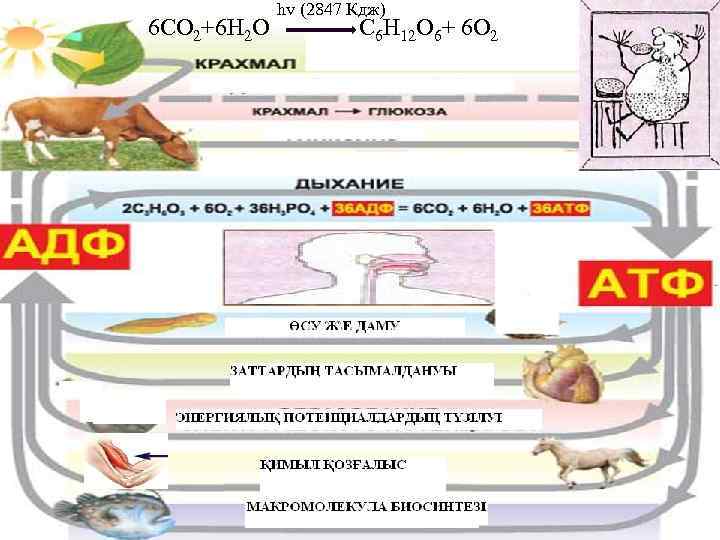 hv (2847 Кдж) 6 СО 2+6 Н 2 О С 6 Н 12 О 6+ 6 О 2
hv (2847 Кдж) 6 СО 2+6 Н 2 О С 6 Н 12 О 6+ 6 О 2
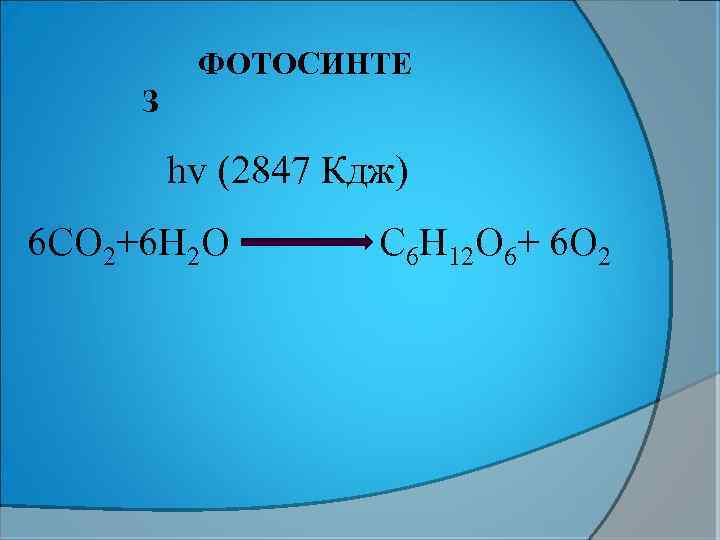 ФОТОСИНТЕ З hv (2847 Кдж) 6 СО 2+6 Н 2 О С 6 Н 12 О 6+ 6 О 2
ФОТОСИНТЕ З hv (2847 Кдж) 6 СО 2+6 Н 2 О С 6 Н 12 О 6+ 6 О 2
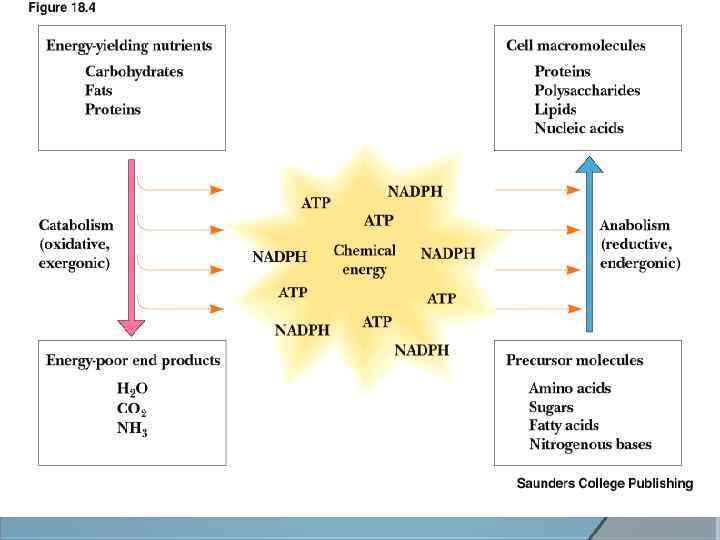
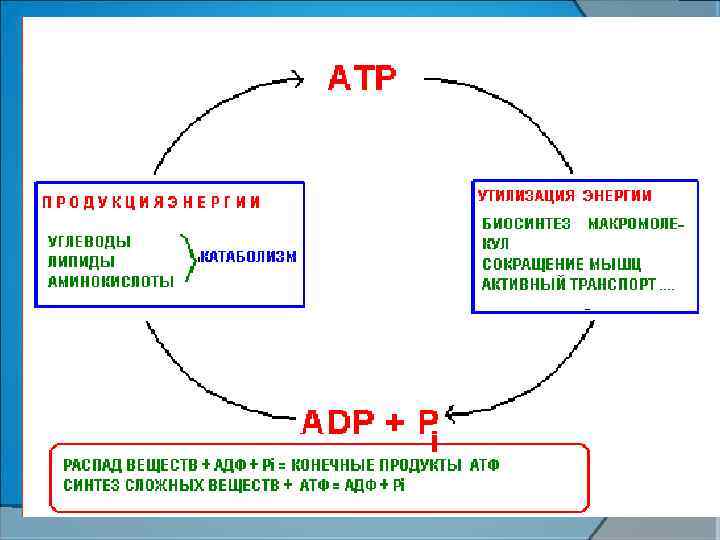
 Mechanisms of ATP generation 1. Substrate-level phosphorylation ○ Transferring high-energy phosphate group from an intermediate directly to ADP 2. Oxidative phosphorylation ○ Remove electrons and pass them through electron transport chain to oxygen Copyright 2009, John Wiley & Sons, Inc.
Mechanisms of ATP generation 1. Substrate-level phosphorylation ○ Transferring high-energy phosphate group from an intermediate directly to ADP 2. Oxidative phosphorylation ○ Remove electrons and pass them through electron transport chain to oxygen Copyright 2009, John Wiley & Sons, Inc.
 АТФ ағзада 2 процесте түзіледі: 1) тотығудан фосфорлану; 2) субстраттан фосфорлану.
АТФ ағзада 2 процесте түзіледі: 1) тотығудан фосфорлану; 2) субстраттан фосфорлану.
 Энергия алмасуы 4 сатыдан тұрады: 1. КҮРДЕЛІ ЗАТТАРДЫҢ АРНАЙЫ ЖОЛДАРМЕН ЫДЫРАП ОРТАҚ ӨНІМ АКТИВТІ СІРКЕ ҚЫШҚЫЛЫН (Ацетил-Ко. А) ТҮЗУІ. 2. ҮШ КАРБОН ҚЫШҚЫЛДАРЫНЫҢ ЦИКЛІ (ҮКЦ) 3. БИОЛОГИЯЛЫҚ ТОТЫҒУ (БТ) 4. ТОТЫҒУДАН ФОСФОРЛАНУ (ТФ)
Энергия алмасуы 4 сатыдан тұрады: 1. КҮРДЕЛІ ЗАТТАРДЫҢ АРНАЙЫ ЖОЛДАРМЕН ЫДЫРАП ОРТАҚ ӨНІМ АКТИВТІ СІРКЕ ҚЫШҚЫЛЫН (Ацетил-Ко. А) ТҮЗУІ. 2. ҮШ КАРБОН ҚЫШҚЫЛДАРЫНЫҢ ЦИКЛІ (ҮКЦ) 3. БИОЛОГИЯЛЫҚ ТОТЫҒУ (БТ) 4. ТОТЫҒУДАН ФОСФОРЛАНУ (ТФ)
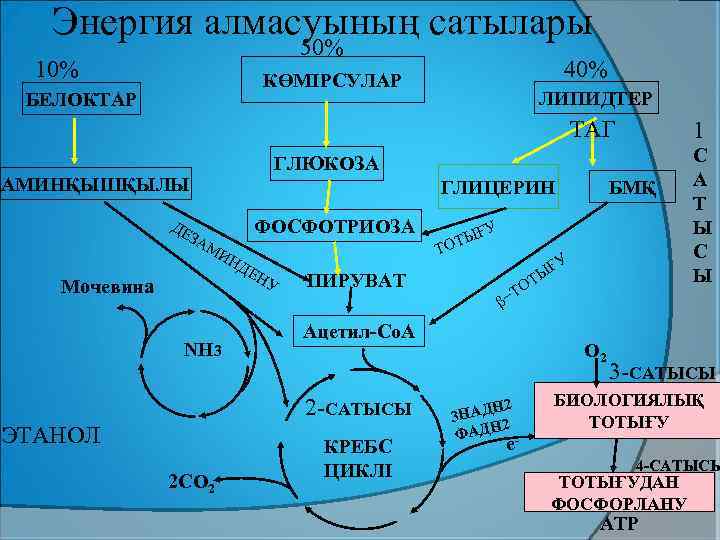 Энергия алмасуының сатылары 50% 10% 40% КӨМІРСУЛАР БЕЛОКТАР ЛИПИДТЕР ТАГ ГЛЮКОЗА АМИНҚЫШҚЫЛЫ ДЕ 1 ГЛИЦЕРИН ФОСФОТРИОЗА ЗА МИ НД Мочевина ΝΗ 3 ЕН У ПИРУВАТ ЭТАНОЛ 2 CO 2 ҒУ Ы ТОТ ҒУ β− Ы ОТ Т Ацетил-Co. A 2 -САТЫСЫ КРЕБС ЦИКЛІ БМҚ O 2 Н 2 3 НАД 2 ФАДН - С А Т Ы С Ы 3 -САТЫСЫ БИОЛОГИЯЛЫҚ ТОТЫҒУ e 4 -САТЫСЫ ТОТЫҒУДАН ФОСФОРЛАНУ ATP
Энергия алмасуының сатылары 50% 10% 40% КӨМІРСУЛАР БЕЛОКТАР ЛИПИДТЕР ТАГ ГЛЮКОЗА АМИНҚЫШҚЫЛЫ ДЕ 1 ГЛИЦЕРИН ФОСФОТРИОЗА ЗА МИ НД Мочевина ΝΗ 3 ЕН У ПИРУВАТ ЭТАНОЛ 2 CO 2 ҒУ Ы ТОТ ҒУ β− Ы ОТ Т Ацетил-Co. A 2 -САТЫСЫ КРЕБС ЦИКЛІ БМҚ O 2 Н 2 3 НАД 2 ФАДН - С А Т Ы С Ы 3 -САТЫСЫ БИОЛОГИЯЛЫҚ ТОТЫҒУ e 4 -САТЫСЫ ТОТЫҒУДАН ФОСФОРЛАНУ ATP
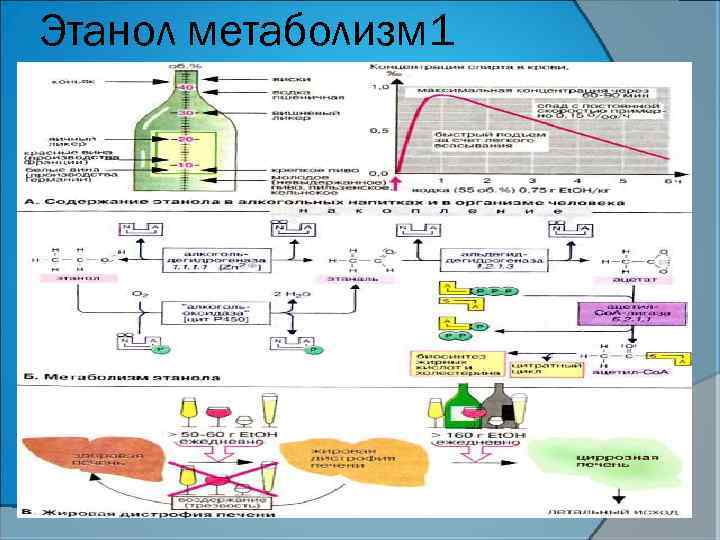 Этанол метаболизм 1
Этанол метаболизм 1
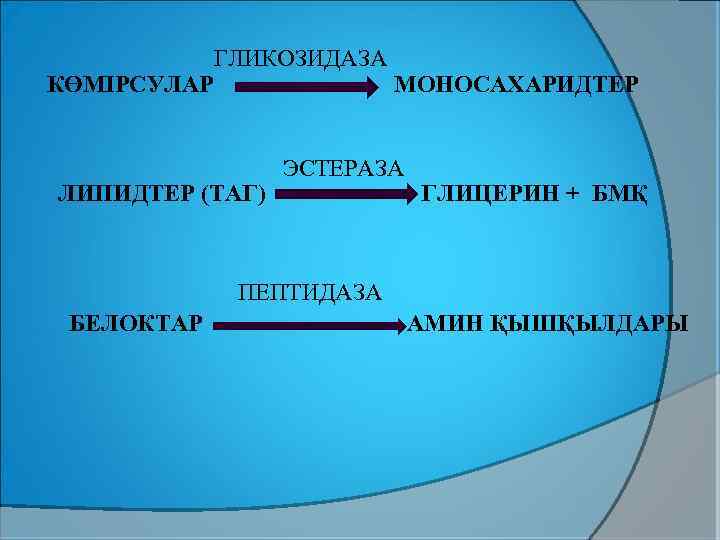 ГЛИКОЗИДАЗА КӨМІРСУЛАР МОНОСАХАРИДТЕР ЛИПИДТЕР (ТАГ) ЭСТЕРАЗА ГЛИЦЕРИН + БМҚ ПЕПТИДАЗА БЕЛОКТАР АМИН ҚЫШҚЫЛДАРЫ
ГЛИКОЗИДАЗА КӨМІРСУЛАР МОНОСАХАРИДТЕР ЛИПИДТЕР (ТАГ) ЭСТЕРАЗА ГЛИЦЕРИН + БМҚ ПЕПТИДАЗА БЕЛОКТАР АМИН ҚЫШҚЫЛДАРЫ
 Глюкоза тотыққанда, ПЖҚ түзіледі. ПЖҚ тотығудан декарбоксилденіп АСҚ пайда болады. Аминқышқылдар дезаминденіп ПЖҚ немесе АСҚ түзіледі. Липидтер ыдырағанда глицерин мен БМҚ түзіледі. Глицерин тотығып фосфотриозалар арқылы ПЖҚ-ға ол тотығудан декарбоксилденіп АСҚ түзіледі, ал БМҚ β-тотығуға ұшырағанда АСҚ түзіледі.
Глюкоза тотыққанда, ПЖҚ түзіледі. ПЖҚ тотығудан декарбоксилденіп АСҚ пайда болады. Аминқышқылдар дезаминденіп ПЖҚ немесе АСҚ түзіледі. Липидтер ыдырағанда глицерин мен БМҚ түзіледі. Глицерин тотығып фосфотриозалар арқылы ПЖҚ-ға ол тотығудан декарбоксилденіп АСҚ түзіледі, ал БМҚ β-тотығуға ұшырағанда АСҚ түзіледі.
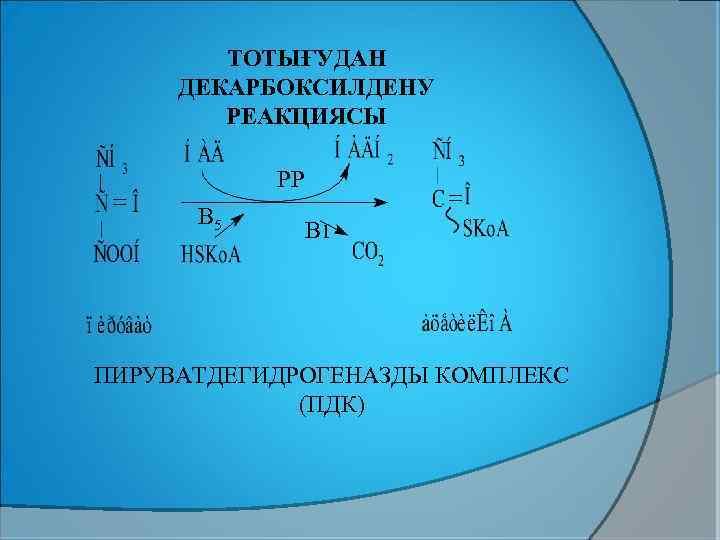 ТОТЫҒУДАН ДЕКАРБОКСИЛДЕНУ РЕАКЦИЯСЫ РР В 5 В 1 ПИРУВАТДЕГИДРОГЕНАЗДЫ КОМПЛЕКС (ПДК)
ТОТЫҒУДАН ДЕКАРБОКСИЛДЕНУ РЕАКЦИЯСЫ РР В 5 В 1 ПИРУВАТДЕГИДРОГЕНАЗДЫ КОМПЛЕКС (ПДК)
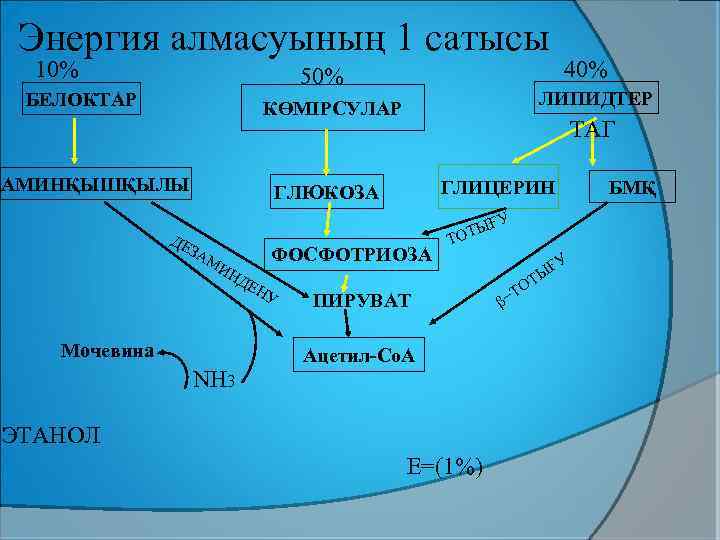 Энергия алмасуының 1 сатысы 10% 50% БЕЛОКТАР ЛИПИДТЕР КӨМІРСУЛАР АМИНҚЫШҚЫЛЫ 40% ТАГ ГЛИЦЕРИН ГЛЮКОЗА ДЕ ҒУ ЗА МИ НД Мочевина NН 3 ФОСФОТРИОЗА ЕН У Ы ТОТ ПИРУВАТ Ацетил-Co. A ЭТАНОЛ Е=(1%) ҒУ β− Ы ОТ Т БМҚ
Энергия алмасуының 1 сатысы 10% 50% БЕЛОКТАР ЛИПИДТЕР КӨМІРСУЛАР АМИНҚЫШҚЫЛЫ 40% ТАГ ГЛИЦЕРИН ГЛЮКОЗА ДЕ ҒУ ЗА МИ НД Мочевина NН 3 ФОСФОТРИОЗА ЕН У Ы ТОТ ПИРУВАТ Ацетил-Co. A ЭТАНОЛ Е=(1%) ҒУ β− Ы ОТ Т БМҚ
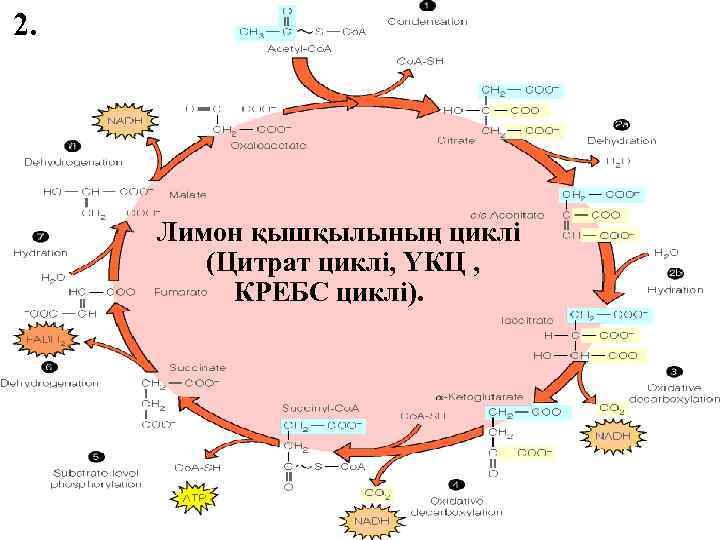 2. Лимон қышқылының циклі (Цитрат циклі, ҮКЦ , КРЕБС циклі).
2. Лимон қышқылының циклі (Цитрат циклі, ҮКЦ , КРЕБС циклі).
 АМЕРИКАЛЫҚ БИОХИМИК ГАНС КРЕБС 1953 ЖЫЛЫ НОБЕЛЬ СЫЙЛЫҒЫН АЛДЫ.
АМЕРИКАЛЫҚ БИОХИМИК ГАНС КРЕБС 1953 ЖЫЛЫ НОБЕЛЬ СЫЙЛЫҒЫН АЛДЫ.
 ҮКЦ МАҢЫЗЫ: 1. ҮКЦ −КӨМІРСУЛАР , ЛИПИДТЕР, БЕЛОКТАР ЫДЫРАҒАНДА ТҮЗІЛГЕН АКТИВТІ СІРКЕ ҚЫШҚЫЛЫН (АСҚ) 2 СО 2−ГЕ ДЕЙІН ТОТЫҚТЫРАДЫ. 2. ПЛАСТИКАЛЫҚ ҚЫЗМЕТ АТҚАРАДЫ.
ҮКЦ МАҢЫЗЫ: 1. ҮКЦ −КӨМІРСУЛАР , ЛИПИДТЕР, БЕЛОКТАР ЫДЫРАҒАНДА ТҮЗІЛГЕН АКТИВТІ СІРКЕ ҚЫШҚЫЛЫН (АСҚ) 2 СО 2−ГЕ ДЕЙІН ТОТЫҚТЫРАДЫ. 2. ПЛАСТИКАЛЫҚ ҚЫЗМЕТ АТҚАРАДЫ.
 vҮКЦ− НІҢ АРАЛЫҚ ӨНІМДЕРІ: ГЛЮКОНЕОГЕНЕЗ , ЛИПОГЕНЕЗ, АМИН ҚЫШҚЫЛДАРЫНЫҢ МЕТАБОЛИЗМІНЕ ПАЙДАЛАНЫЛУЫ МҮМКІН.
vҮКЦ− НІҢ АРАЛЫҚ ӨНІМДЕРІ: ГЛЮКОНЕОГЕНЕЗ , ЛИПОГЕНЕЗ, АМИН ҚЫШҚЫЛДАРЫНЫҢ МЕТАБОЛИЗМІНЕ ПАЙДАЛАНЫЛУЫ МҮМКІН.
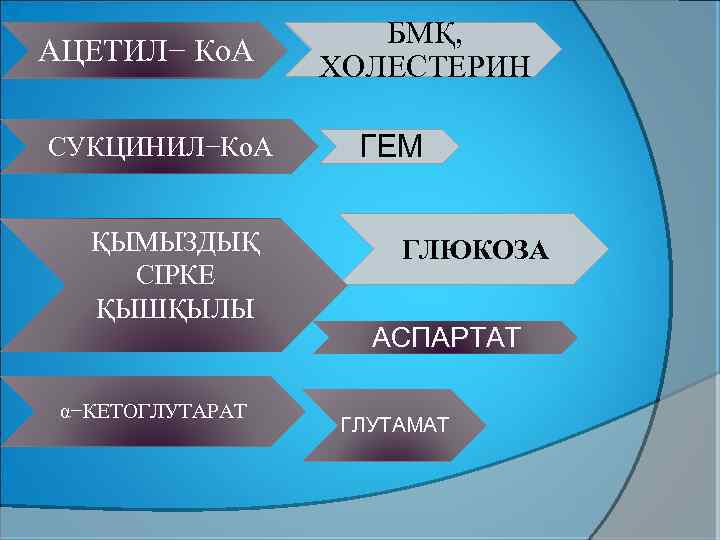 АЦЕТИЛ− Ко. А СУКЦИНИЛ−Ко. А ҚЫМЫЗДЫҚ СІРКЕ ҚЫШҚЫЛЫ α−КЕТОГЛУТАРАТ БМҚ, ХОЛЕСТЕРИН ГЕМ ГЛЮКОЗА АСПАРТАТ ГЛУТАМАТ
АЦЕТИЛ− Ко. А СУКЦИНИЛ−Ко. А ҚЫМЫЗДЫҚ СІРКЕ ҚЫШҚЫЛЫ α−КЕТОГЛУТАРАТ БМҚ, ХОЛЕСТЕРИН ГЕМ ГЛЮКОЗА АСПАРТАТ ГЛУТАМАТ
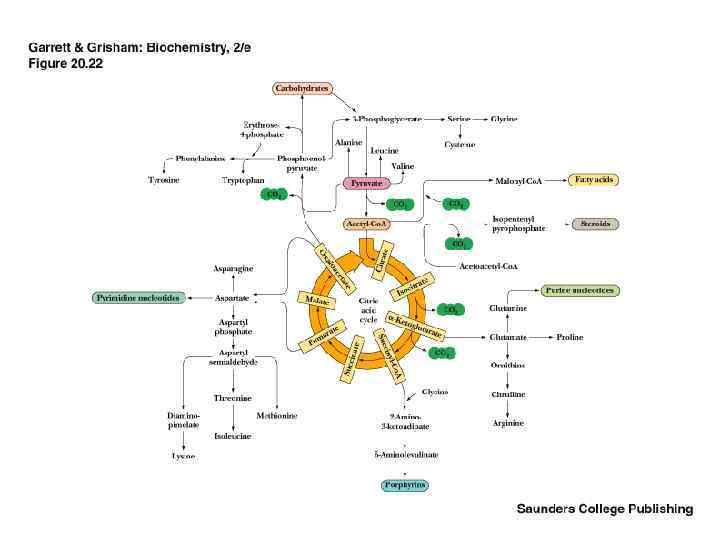
 3. БАРЛЫҚ АЛМАСУ ПРОЦЕСТЕРІН (К, Л, Б) БІР−БІРІМЕН БАЙЛАНЫСТЫРАДЫ. 4. СУТЕГІНІҢ КӨЗІ. АСҚ ТОТЫҒУЫНДА ТҮЗІЛГЕН ЭНЕРГИЯ АКТИВТІ СУТЕГІ ТҮРІНДЕ ( НАДН 2, ФАДН 2) САҚТАЛАДЫ.
3. БАРЛЫҚ АЛМАСУ ПРОЦЕСТЕРІН (К, Л, Б) БІР−БІРІМЕН БАЙЛАНЫСТЫРАДЫ. 4. СУТЕГІНІҢ КӨЗІ. АСҚ ТОТЫҒУЫНДА ТҮЗІЛГЕН ЭНЕРГИЯ АКТИВТІ СУТЕГІ ТҮРІНДЕ ( НАДН 2, ФАДН 2) САҚТАЛАДЫ.
 КРЕБС ЦИКЛІНІҢ ЕРЕКШЕЛІГІ: 1 2 • РЕАКЦИЯ БІР БАҒЫТҚА ТЕК АСҚ ТОТЫҒУЫНА БАҒЫТТАЛҒАН. • ПРОЦЕСС ҚАЙТЫМСЫЗ , ЦИКЛДІ. • ҮКЦ РЕАКЦИЯЛАРЫ ҮШІН ТІКЕЛЕЙ ОТТЕК ҚАЖЕТ ЕМЕС. БІРАҚ ҮКЦ− ДА ТОТЫҚСЫЗДАНҒАН ДЕГИДРОГЕНАЗАЛАР (НАД 2, ФАДН 2 )БИОЛОГИЯЛЫҚ ТОТЫҒУ ТІЗБЕГІНДЕ ТОТЫҒУ ҮШІН ОТТЕК ҚАЖЕТ. ҮКЦ−АЭРОБТЫ ПРОЦЕСС.
КРЕБС ЦИКЛІНІҢ ЕРЕКШЕЛІГІ: 1 2 • РЕАКЦИЯ БІР БАҒЫТҚА ТЕК АСҚ ТОТЫҒУЫНА БАҒЫТТАЛҒАН. • ПРОЦЕСС ҚАЙТЫМСЫЗ , ЦИКЛДІ. • ҮКЦ РЕАКЦИЯЛАРЫ ҮШІН ТІКЕЛЕЙ ОТТЕК ҚАЖЕТ ЕМЕС. БІРАҚ ҮКЦ− ДА ТОТЫҚСЫЗДАНҒАН ДЕГИДРОГЕНАЗАЛАР (НАД 2, ФАДН 2 )БИОЛОГИЯЛЫҚ ТОТЫҒУ ТІЗБЕГІНДЕ ТОТЫҒУ ҮШІН ОТТЕК ҚАЖЕТ. ҮКЦ−АЭРОБТЫ ПРОЦЕСС.
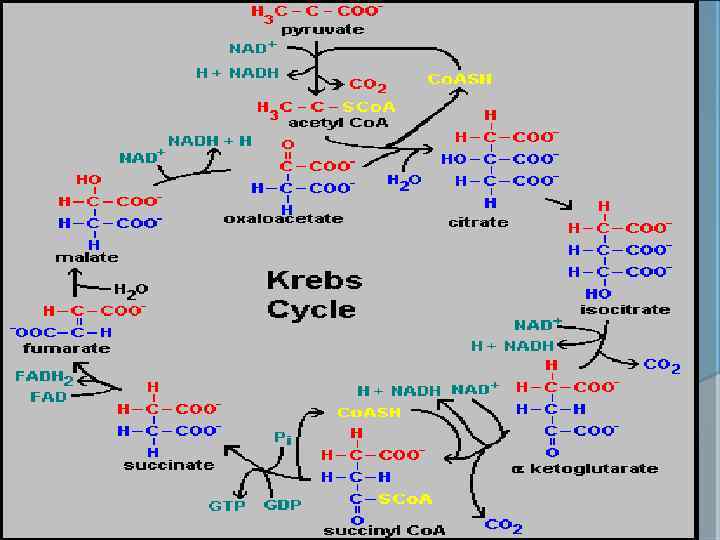
 ҮКЦ РЕАКЦИЯЛАРЫ ЖҮРУІ ҮШІН: АСҚ, ҚСҚ ЖЕТКІЛІКТІ БОЛУЫ КЕРЕК ТОТЫҚСЫЗДАНҒАН ДЕГИДРОГЕНАЗАЛАР НАДН 2, ФАДН 2 ТОТЫҒЫП ТҰРУЫ КЕРЕК ОТТЕК ҚАЖЕТ
ҮКЦ РЕАКЦИЯЛАРЫ ЖҮРУІ ҮШІН: АСҚ, ҚСҚ ЖЕТКІЛІКТІ БОЛУЫ КЕРЕК ТОТЫҚСЫЗДАНҒАН ДЕГИДРОГЕНАЗАЛАР НАДН 2, ФАДН 2 ТОТЫҒЫП ТҰРУЫ КЕРЕК ОТТЕК ҚАЖЕТ
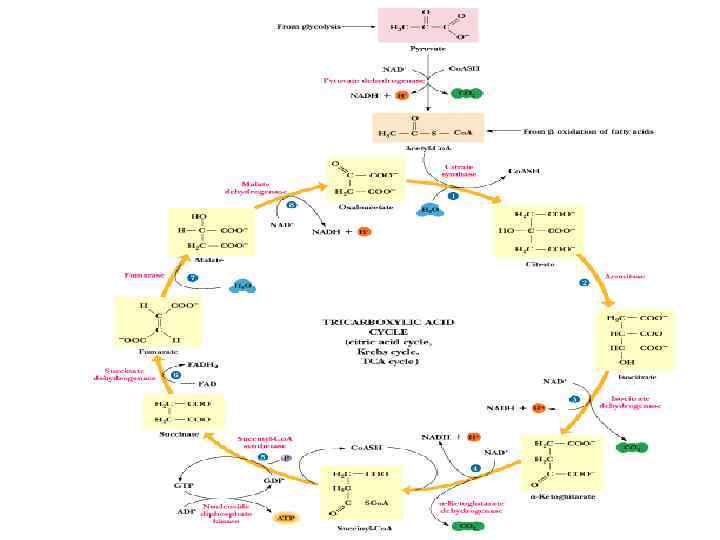
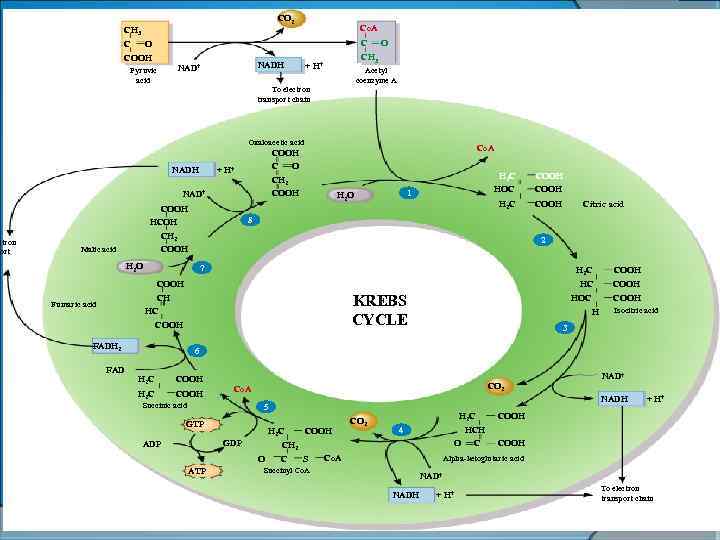
 ҮКЦ реакциялары митохондрия матриксасында жүреді, 10 реакциядан тұрады.
ҮКЦ реакциялары митохондрия матриксасында жүреді, 10 реакциядан тұрады.
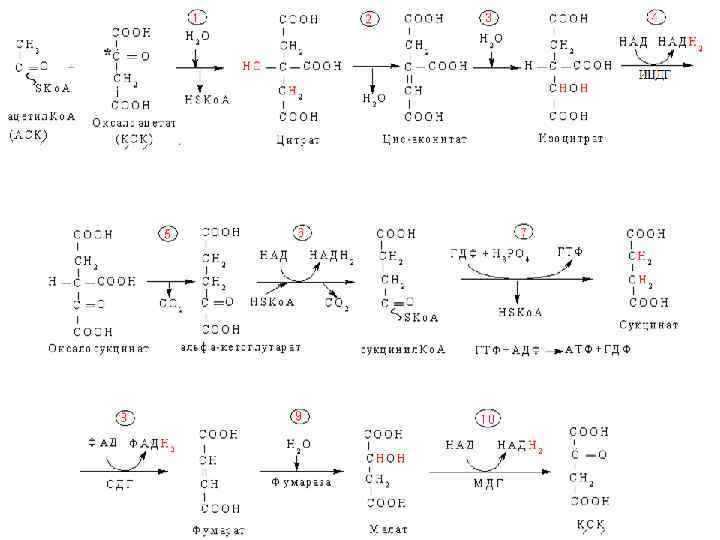
 1 -реакция. Ацетил-Ко. А цитратсинтаза әсерінен Қымыздық сірке қышқылымен ҚСҚ конденсацияланып цитрат (лимон қышқылы) түзеді.
1 -реакция. Ацетил-Ко. А цитратсинтаза әсерінен Қымыздық сірке қышқылымен ҚСҚ конденсацияланып цитрат (лимон қышқылы) түзеді.
 2. Цитрат аконитаза қатысуымен дегидратацияланып цис- аконитатқа айналады.
2. Цитрат аконитаза қатысуымен дегидратацияланып цис- аконитатқа айналады.
 4. 1−ші тотығу-тотықсыздану р/сы. Изоцитратдегидрогеназа (ИЦДГ әсерінен изоцитрат Қымыздық янтарь қышқылына (оксалосукцинат) тотығады(дегидрлену). НАДН 2 -ге тотықсызданады.
4. 1−ші тотығу-тотықсыздану р/сы. Изоцитратдегидрогеназа (ИЦДГ әсерінен изоцитрат Қымыздық янтарь қышқылына (оксалосукцинат) тотығады(дегидрлену). НАДН 2 -ге тотықсызданады.
 5. Декарбоксилдену реакциясы ҚЯҚ декарбоксилденіп -кетоглутарат, СО 2 түзеді
5. Декарбоксилдену реакциясы ҚЯҚ декарбоксилденіп -кетоглутарат, СО 2 түзеді
 6. 2−ші тотығу-тотықсыздану рсы. -кетоглутарат тотығудан декарбоксилденіп жоғары энергиялық қосылыс сукцинил. Ко. А, НАДН 2, СО 2 түзеді. -кетоглутаратдегидрогеназды комплекс қатысады
6. 2−ші тотығу-тотықсыздану рсы. -кетоглутарат тотығудан декарбоксилденіп жоғары энергиялық қосылыс сукцинил. Ко. А, НАДН 2, СО 2 түзеді. -кетоглутаратдегидрогеназды комплекс қатысады
 7. Субстраттан фосфорлану реакциясы. Сукцинаттиокиназа әсерінен Сукцинил-Ко. А-дағы макроэргиялық байланыс үзіліп Сукцинат (янтарь қышқылы) түзіледі. Бөлінген энергия арқылы ГДФ пен НЗРО 4 – тен ГТФ түзіледі
7. Субстраттан фосфорлану реакциясы. Сукцинаттиокиназа әсерінен Сукцинил-Ко. А-дағы макроэргиялық байланыс үзіліп Сукцинат (янтарь қышқылы) түзіледі. Бөлінген энергия арқылы ГДФ пен НЗРО 4 – тен ГТФ түзіледі
 Түзілген ГТФ нуклеозиддифосфат− киназа көмегімен АТФ-ке айналады: ГТФ + АДФ → АТФ + ГДФ
Түзілген ГТФ нуклеозиддифосфат− киназа көмегімен АТФ-ке айналады: ГТФ + АДФ → АТФ + ГДФ
 8. 3−ші тотығу-тотықсыздану рсы. ФАД−тәуелді сукцинатдегидрогеназа (СДГ) әсерінен Сукцинаттан фумарат және тотықсызданған ФАДН 2 түзіледі.
8. 3−ші тотығу-тотықсыздану рсы. ФАД−тәуелді сукцинатдегидрогеназа (СДГ) әсерінен Сукцинаттан фумарат және тотықсызданған ФАДН 2 түзіледі.
 9. Фумараза фумаратты гидратациялап малат түзіледі.
9. Фумараза фумаратты гидратациялап малат түзіледі.
 10. 4−ші тотығу-тотықсыздану р/сы. НАД−тәуелді малатдегидрогеназа (МДГ) әсерінен Малаттан ҚСҚ және НАДН 2 түзіледі.
10. 4−ші тотығу-тотықсыздану р/сы. НАД−тәуелді малатдегидрогеназа (МДГ) әсерінен Малаттан ҚСҚ және НАДН 2 түзіледі.
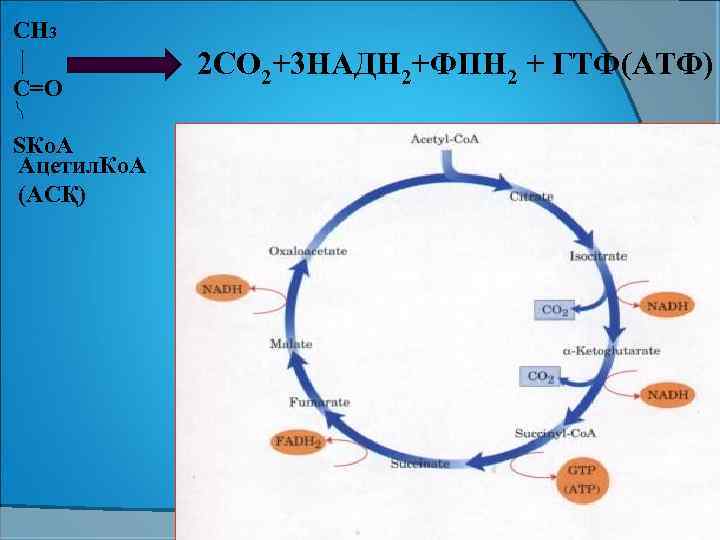 СН 3 С=О SКо. А Ацетил. Ко. А (АСҚ) 2 СО 2+3 НАДН 2+ФПН 2 + ГТФ(АТФ)
СН 3 С=О SКо. А Ацетил. Ко. А (АСҚ) 2 СО 2+3 НАДН 2+ФПН 2 + ГТФ(АТФ)
 ҮКЦ−де: Ø 2 ДЕКАРБОКСИЛДЕНУ, Ø 4 ТОТЫҒУ−ТОТЫҚСЫЗДАНУ, Ø 1 СУБСТРАТТАН ФОСФОРЛАНУ РЕАКЦИЯСЫ ЖҮРЕДІ.
ҮКЦ−де: Ø 2 ДЕКАРБОКСИЛДЕНУ, Ø 4 ТОТЫҒУ−ТОТЫҚСЫЗДАНУ, Ø 1 СУБСТРАТТАН ФОСФОРЛАНУ РЕАКЦИЯСЫ ЖҮРЕДІ.
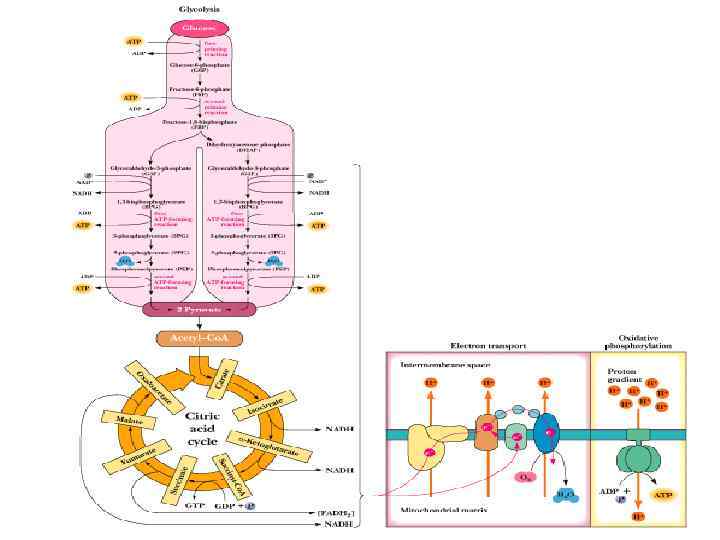
 ctron ort CO 2 CH 3 C O COOH Co. A C OO C NADH NAD+ Pyruvic acid CO 2 CH 33 CH NADH+ +H Acetyl coenzyme A A coenzyme acid To electron transport chain transport Oxaloacetic acid NADH + H+ CH H 2 O FAD H 2 C H 2 C COOH HC COOH 2 HOC COOH H Isocitric acid 3 GTP GDP ADP 5 H 2 C GDP CH CO 22 CO H 2 C COOH CH 2 Co. A C O S Co. A 2 O Succinyl Co. A ATP CO 2 H 2 C COOH H 2 C 4 HCH 4 NAD+ NADH + H+ CO 2 Co. A Succinic acid 5 ATP COOH 6 FAD COOH H 2 C COOH H CCo. A COOH ADP H 2 C HC HOC COOH KREBS CYCLE COOH Succinic acid Citric acid 2 7 FADH 2 6 H 2 C COOH Citric COOH H 2 C acid 2 COOH CH HC COOH FADH 2 HOC COOH HOC 1 CH 2 COOH 7 H 2 O COOH CH Fumaric acid HC Fumaric acid 1 COOH 8 HCOH 2 To electron COOH Malic acidtransport Malic acid chain Co. A H 2 C COOHH 2 C CH 2 COOH H 2 O O H 2 NAD+ COOH HCOH Co. A COOH C O NADH + H+ COOH HCH O C COOHC O COOH Alpha-ketoglutaric acid NAD+ NADH + H+ To electron transport chain
ctron ort CO 2 CH 3 C O COOH Co. A C OO C NADH NAD+ Pyruvic acid CO 2 CH 33 CH NADH+ +H Acetyl coenzyme A A coenzyme acid To electron transport chain transport Oxaloacetic acid NADH + H+ CH H 2 O FAD H 2 C H 2 C COOH HC COOH 2 HOC COOH H Isocitric acid 3 GTP GDP ADP 5 H 2 C GDP CH CO 22 CO H 2 C COOH CH 2 Co. A C O S Co. A 2 O Succinyl Co. A ATP CO 2 H 2 C COOH H 2 C 4 HCH 4 NAD+ NADH + H+ CO 2 Co. A Succinic acid 5 ATP COOH 6 FAD COOH H 2 C COOH H CCo. A COOH ADP H 2 C HC HOC COOH KREBS CYCLE COOH Succinic acid Citric acid 2 7 FADH 2 6 H 2 C COOH Citric COOH H 2 C acid 2 COOH CH HC COOH FADH 2 HOC COOH HOC 1 CH 2 COOH 7 H 2 O COOH CH Fumaric acid HC Fumaric acid 1 COOH 8 HCOH 2 To electron COOH Malic acidtransport Malic acid chain Co. A H 2 C COOHH 2 C CH 2 COOH H 2 O O H 2 NAD+ COOH HCOH Co. A COOH C O NADH + H+ COOH HCH O C COOHC O COOH Alpha-ketoglutaric acid NAD+ NADH + H+ To electron transport chain
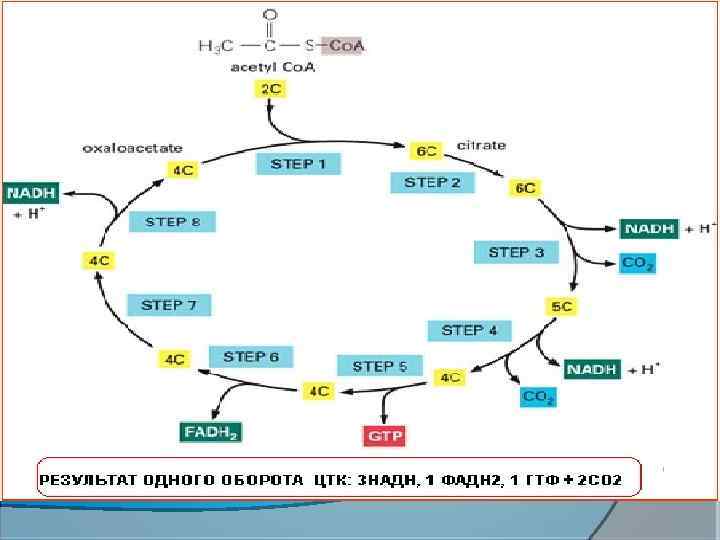
 Regulation of the TCA Cycle Again, 3 reactions are the key sites Citrate synthase - ATP, цитрат, NADH and succinyl-Co. A inhibit Isocitrate dehydrogenase - ATP and NADH inhibit, Са + 2 ADP and NAD+ activate · -Ketoglutarate dehydrogenase - NADH and succinyl-Co. A inhibit, Са + 2 , AMP activatе Also note pyruvate dehydrogenase: ATP, NADH, acetyl-Co. A inhibit, NAD+, Co. A activate
Regulation of the TCA Cycle Again, 3 reactions are the key sites Citrate synthase - ATP, цитрат, NADH and succinyl-Co. A inhibit Isocitrate dehydrogenase - ATP and NADH inhibit, Са + 2 ADP and NAD+ activate · -Ketoglutarate dehydrogenase - NADH and succinyl-Co. A inhibit, Са + 2 , AMP activatе Also note pyruvate dehydrogenase: ATP, NADH, acetyl-Co. A inhibit, NAD+, Co. A activate
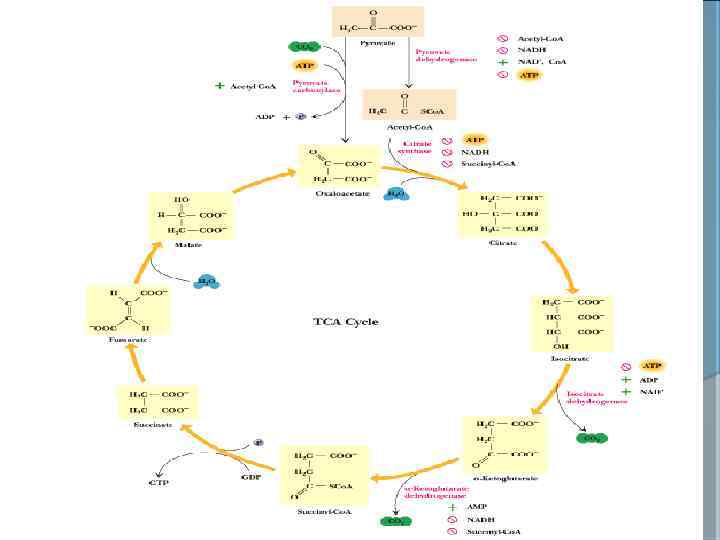
 3 САТЫ. БИОЛОГИЯЛЫҚ ТОТЫҒУ (БТ ) БТ— ЖАСУША МИТОХОНДРИЯСЫНДА ӨТЕТІН ТОТЫҒУ–ТОТЫҚСЫЗДАНУ (Т-Т) РЕАКЦИЯЛАРЫНЫҢ ЖИЫНЫ. Т-Т РЕАКЦИЯЛАРЫНЫҢ ЖИЫНЫН= ЭЛЕКТРОНДАРДЫҢ ТАСЫМАЛДАНУ ТІЗБЕГІ = ТЫНЫС АЛУ ТІЗБЕГІ= ТІНДІК ТЫНЫС АЛУ ДЕПТЕ АТАЙДЫ.
3 САТЫ. БИОЛОГИЯЛЫҚ ТОТЫҒУ (БТ ) БТ— ЖАСУША МИТОХОНДРИЯСЫНДА ӨТЕТІН ТОТЫҒУ–ТОТЫҚСЫЗДАНУ (Т-Т) РЕАКЦИЯЛАРЫНЫҢ ЖИЫНЫ. Т-Т РЕАКЦИЯЛАРЫНЫҢ ЖИЫНЫН= ЭЛЕКТРОНДАРДЫҢ ТАСЫМАЛДАНУ ТІЗБЕГІ = ТЫНЫС АЛУ ТІЗБЕГІ= ТІНДІК ТЫНЫС АЛУ ДЕПТЕ АТАЙДЫ.
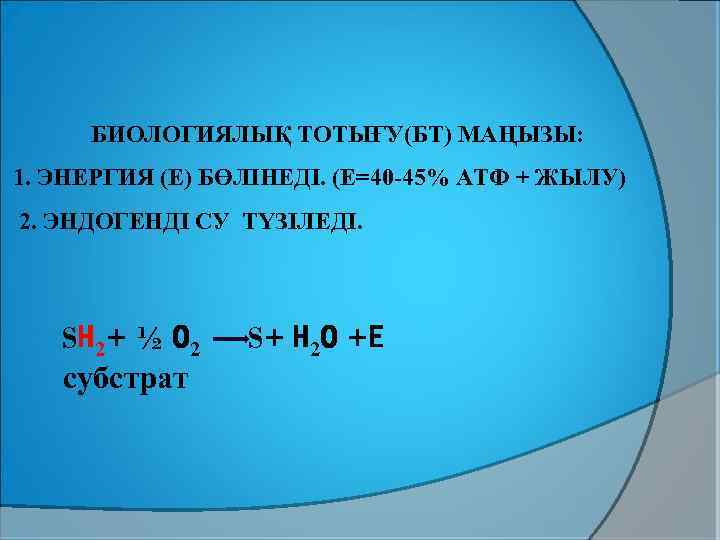 БИОЛОГИЯЛЫҚ ТОТЫҒУ(БТ) МАҢЫЗЫ: 1. ЭНЕРГИЯ (Е) БӨЛІНЕДІ. (Е=40 -45% АТФ + ЖЫЛУ) 2. ЭНДОГЕНДІ СУ ТҮЗІЛЕДІ. SН 2+ ½ О 2 субстрат S+ Н 2 О +Е
БИОЛОГИЯЛЫҚ ТОТЫҒУ(БТ) МАҢЫЗЫ: 1. ЭНЕРГИЯ (Е) БӨЛІНЕДІ. (Е=40 -45% АТФ + ЖЫЛУ) 2. ЭНДОГЕНДІ СУ ТҮЗІЛЕДІ. SН 2+ ½ О 2 субстрат S+ Н 2 О +Е
 БТ ОКСИДОРЕДУКТАЗАЛАР ҚАТЫСУЫМЕН МИТОХОНДРИЯДА ЖҮРЕДІ: 11 РЕАКЦИЯДАН ТҰРАДЫ.
БТ ОКСИДОРЕДУКТАЗАЛАР ҚАТЫСУЫМЕН МИТОХОНДРИЯДА ЖҮРЕДІ: 11 РЕАКЦИЯДАН ТҰРАДЫ.
 SН 2 БТ тізбегіндегі ферменттердің орналасу тәртібі неге тәуелді? ПФ(НАД) (ФП (ФМН) Ко. Q Цхb с1 с а а 3 О 2. ТОТЫҒУ–ТОТЫҚСЫЗДАНУ потенциалының өсуіне байланысты.
SН 2 БТ тізбегіндегі ферменттердің орналасу тәртібі неге тәуелді? ПФ(НАД) (ФП (ФМН) Ко. Q Цхb с1 с а а 3 О 2. ТОТЫҒУ–ТОТЫҚСЫЗДАНУ потенциалының өсуіне байланысты.
 Е , В Н/ Н 2 -0. 41 НАДНАДН 2 -0, 32 ФМНФМНН 2 -0, 22 Ко. QКо. QН 2 +0, 04 Цхв (Fe 3+Fe 2+) +0, 07 с1 (Fe 3+Fe 2+ +0, 23 c (Fe 3+Fe 2+) +0, 25 а (Fe 3+Fe 2+ ) +0, 29 а 3 (Fe 3+Fe 2+ ) +0, 55 ½ О 2 +0, 82 SН 2 НАДН 2 ФПН 2 Ко. QН 2 b c 1 c a a 3 О 2
Е , В Н/ Н 2 -0. 41 НАДНАДН 2 -0, 32 ФМНФМНН 2 -0, 22 Ко. QКо. QН 2 +0, 04 Цхв (Fe 3+Fe 2+) +0, 07 с1 (Fe 3+Fe 2+ +0, 23 c (Fe 3+Fe 2+) +0, 25 а (Fe 3+Fe 2+ ) +0, 29 а 3 (Fe 3+Fe 2+ ) +0, 55 ½ О 2 +0, 82 SН 2 НАДН 2 ФПН 2 Ко. QН 2 b c 1 c a a 3 О 2
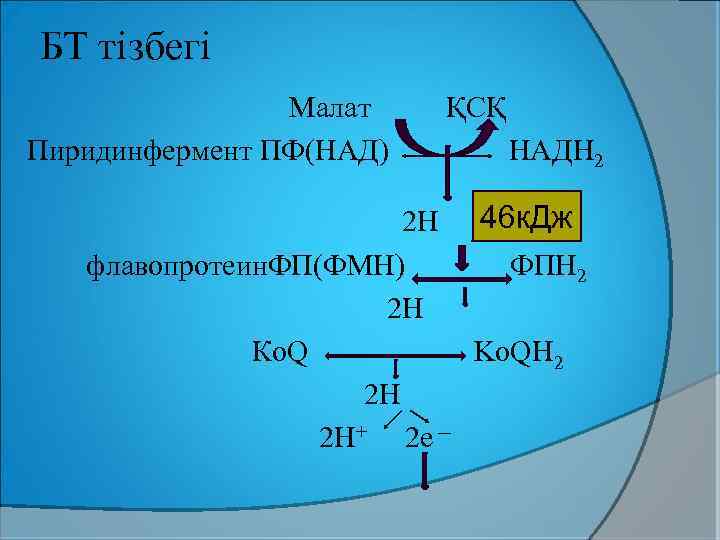 БТ тізбегі Малат ҚСҚ Пиридинфермент ПФ(НАД) НАДН 2 2 Н 46 к. Дж флавопротеин. ФП(ФМН) ФПН 2 2 Н Ко. Q Ko. QН 2 2 Н+ 2 е
БТ тізбегі Малат ҚСҚ Пиридинфермент ПФ(НАД) НАДН 2 2 Н 46 к. Дж флавопротеин. ФП(ФМН) ФПН 2 2 Н Ко. Q Ko. QН 2 2 Н+ 2 е
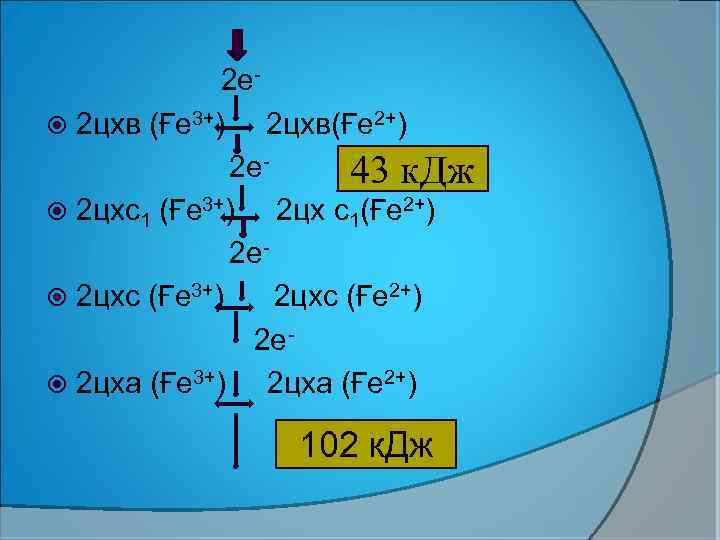 2 е 2 цхв (Ғе 3+) 2 цхв(Ғе 2+) 2 е 43 к. Дж 2 цхс1 (Ғе 3+) 2 цх с1(Ғе 2+) 2 е 2 цхс (Ғе 3+) 2 цхс (Ғе 2+) 2 е 2 цха (Ғе 3+) 2 цха (Ғе 2+) 102 к. Дж
2 е 2 цхв (Ғе 3+) 2 цхв(Ғе 2+) 2 е 43 к. Дж 2 цхс1 (Ғе 3+) 2 цх с1(Ғе 2+) 2 е 2 цхс (Ғе 3+) 2 цхс (Ғе 2+) 2 е 2 цха (Ғе 3+) 2 цха (Ғе 2+) 102 к. Дж
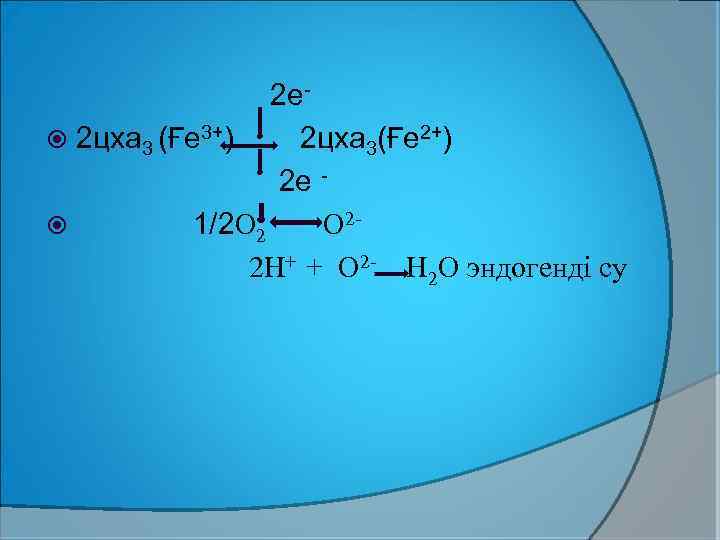 2 е 2 цха 3 (Ғе 3+) 2 цха 3(Ғе 2+) 2 е 1/2 О 2 2 Н+ + О 2 - Н 2 О эндогенді су
2 е 2 цха 3 (Ғе 3+) 2 цха 3(Ғе 2+) 2 е 1/2 О 2 2 Н+ + О 2 - Н 2 О эндогенді су
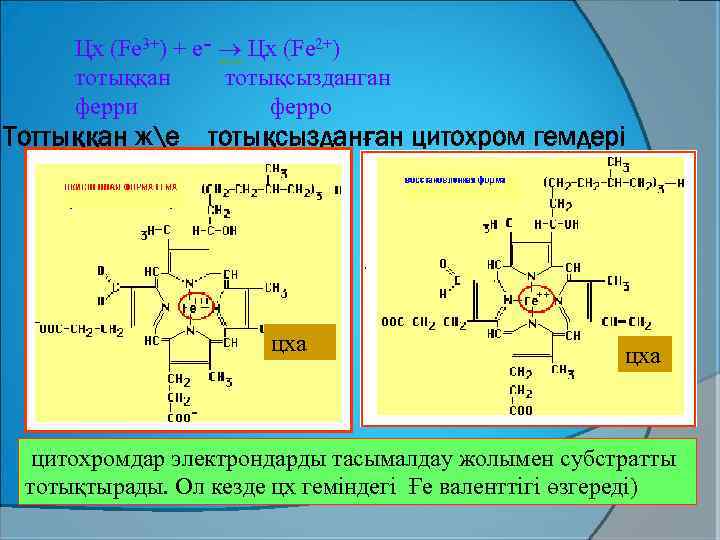 Цх (Fe 3+) + e ־ Цх (Fe 2+) тотыққан тотықсызданган ферри ферро Тоттыққан же тотықсызданған цитохром гемдері цха цитохромдар электрондарды тасымалдау жолымен субстратты тотықтырады. Ол кезде цх геміндегі Ғе валенттігі өзгереді)
Цх (Fe 3+) + e ־ Цх (Fe 2+) тотыққан тотықсызданган ферри ферро Тоттыққан же тотықсызданған цитохром гемдері цха цитохромдар электрондарды тасымалдау жолымен субстратты тотықтырады. Ол кезде цх геміндегі Ғе валенттігі өзгереді)
 Қорытынды: БТ-ның 3 нүктесінде сатысында АТФ түзуге жеткілікті энергия бөлінеді. Осы сатылар БТ мен ТФның қабысу нүктелері деп аталады, олар: 2, 6, 9 және 10 сатылар. 1. 2 пункт−НАДН 2 -нің ФП(ФМН)–мен тотығуы 46 к. Дж 2. 6 пункт- Ферро Цхв тотығуы- 43 к. Дж. 3. (9, 10 пункт) -Цитохромоксидазаның тотығуы 102 к. Дж.
Қорытынды: БТ-ның 3 нүктесінде сатысында АТФ түзуге жеткілікті энергия бөлінеді. Осы сатылар БТ мен ТФның қабысу нүктелері деп аталады, олар: 2, 6, 9 және 10 сатылар. 1. 2 пункт−НАДН 2 -нің ФП(ФМН)–мен тотығуы 46 к. Дж 2. 6 пункт- Ферро Цхв тотығуы- 43 к. Дж. 3. (9, 10 пункт) -Цитохромоксидазаның тотығуы 102 к. Дж.
 ЭНЕРГИЯ АЛМАСУЫНЫҢ 4 САТЫСЫ: ТОТЫҒУДАН ФОСФОРЛАНУ (ТФ). ТФ − БИОЛОГИЯЛЫҚ ТОТЫҒУ ЭНЕРГИЯСЫН ПАЙДАЛАНЫП АДФ ПЕН БЕЙОРГАНИКАЛЫҚ ФОСФАТТАН АТФ ТҮЗУ ПРОЦЕСІ. +БТ энергия АДФ + Н 3 РО 4 АТФ + Н 2 О АТФ-СИНТАЗА
ЭНЕРГИЯ АЛМАСУЫНЫҢ 4 САТЫСЫ: ТОТЫҒУДАН ФОСФОРЛАНУ (ТФ). ТФ − БИОЛОГИЯЛЫҚ ТОТЫҒУ ЭНЕРГИЯСЫН ПАЙДАЛАНЫП АДФ ПЕН БЕЙОРГАНИКАЛЫҚ ФОСФАТТАН АТФ ТҮЗУ ПРОЦЕСІ. +БТ энергия АДФ + Н 3 РО 4 АТФ + Н 2 О АТФ-СИНТАЗА
 БТ тізбегінде электрондар НАДН 2 -ден О 2 -ке тасымалданғанда матрикстен мембранааралық кеңістікке шамамен 6 протон шығарылады. Ішкі мембрананың сыртқы жағы - оң, ал ішкі жағы теріс зарядталады. Ішкі мембранада пайда болған электрохимиялық потенциал энергиясы протондардың матрикске АТФ-синтазаның иондық каналдары арқылы қайтуына әсер етеді, яғни АТФ түзіледі. Мембрана аралық кеңістікке протондардың тасымалдануы ЭТТ-нің I, III, IV комплекстері орналасқан бөлімдерде жүретіндіктен бұл бөлімдер тыныс алу мен тотығудан фосфорланудың қабысу нүктелері деп аталады.
БТ тізбегінде электрондар НАДН 2 -ден О 2 -ке тасымалданғанда матрикстен мембранааралық кеңістікке шамамен 6 протон шығарылады. Ішкі мембрананың сыртқы жағы - оң, ал ішкі жағы теріс зарядталады. Ішкі мембранада пайда болған электрохимиялық потенциал энергиясы протондардың матрикске АТФ-синтазаның иондық каналдары арқылы қайтуына әсер етеді, яғни АТФ түзіледі. Мембрана аралық кеңістікке протондардың тасымалдануы ЭТТ-нің I, III, IV комплекстері орналасқан бөлімдерде жүретіндіктен бұл бөлімдер тыныс алу мен тотығудан фосфорланудың қабысу нүктелері деп аталады.
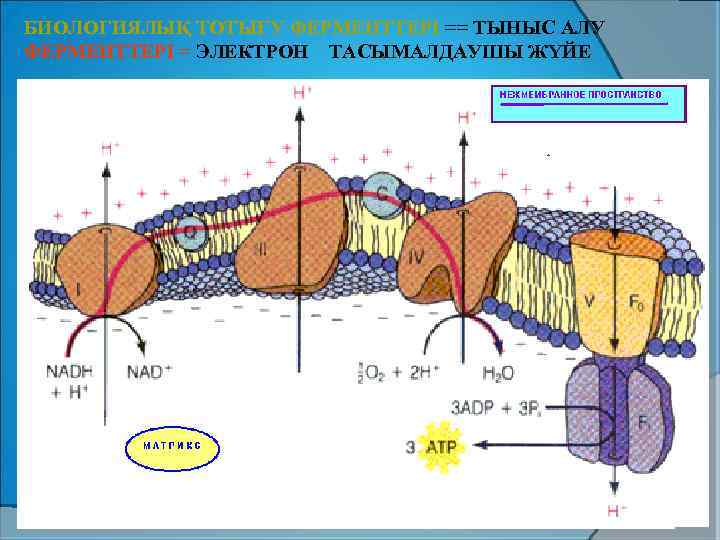 БИОЛОГИЯЛЫҚ ТОТЫҒУ ФЕРМЕНТТЕРІ == ТЫНЫС АЛУ ФЕРМЕНТТЕРІ = ЭЛЕКТРОН ТАСЫМАЛДАУШЫ ЖҮЙЕ
БИОЛОГИЯЛЫҚ ТОТЫҒУ ФЕРМЕНТТЕРІ == ТЫНЫС АЛУ ФЕРМЕНТТЕРІ = ЭЛЕКТРОН ТАСЫМАЛДАУШЫ ЖҮЙЕ
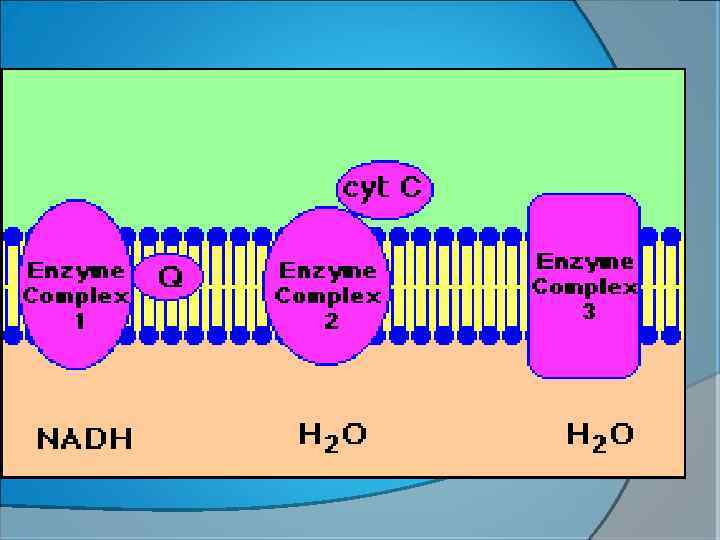
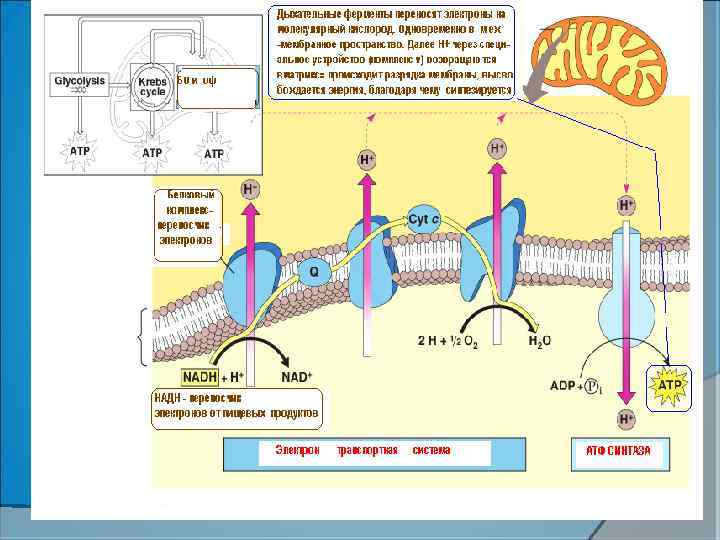
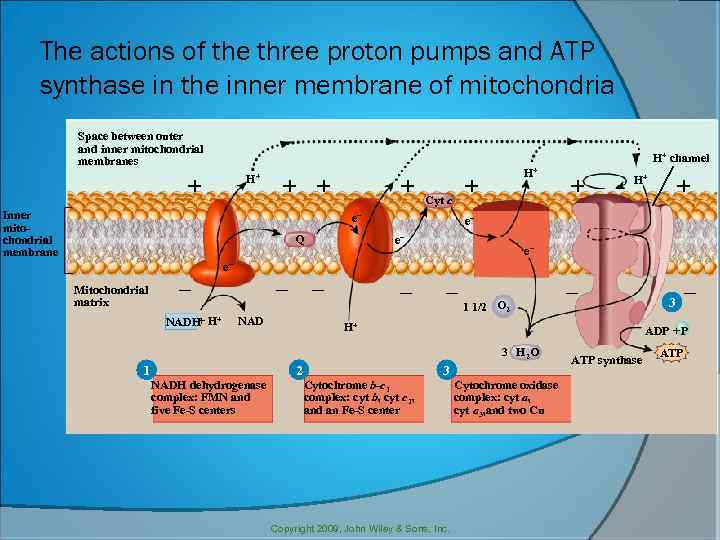 The actions of the three proton pumps and ATP synthase in the inner membrane of mitochondria Space between outer and inner mitochondrial membranes H+ channel H+ + Inner mitochondrial membrane + Cyt c e– Q H+ + H+ e– e– Mitochondrial matrix – + NADH H+ – – NAD – – 1 1/2 O 2 H+ 2 NADH dehydrogenase complex: FMN and five Fe-S centers 3 – ADP + P 3 H 2 O 1 – 3 Cytochrome b-c 1 complex: cyt b, cyt c 1, and an Fe-S center Copyright 2009, John Wiley & Sons, Inc. Cytochrome oxidase complex: cyt a, cyt a 3, and two Cu ATP synthase ATP
The actions of the three proton pumps and ATP synthase in the inner membrane of mitochondria Space between outer and inner mitochondrial membranes H+ channel H+ + Inner mitochondrial membrane + Cyt c e– Q H+ + H+ e– e– Mitochondrial matrix – + NADH H+ – – NAD – – 1 1/2 O 2 H+ 2 NADH dehydrogenase complex: FMN and five Fe-S centers 3 – ADP + P 3 H 2 O 1 – 3 Cytochrome b-c 1 complex: cyt b, cyt c 1, and an Fe-S center Copyright 2009, John Wiley & Sons, Inc. Cytochrome oxidase complex: cyt a, cyt a 3, and two Cu ATP synthase ATP
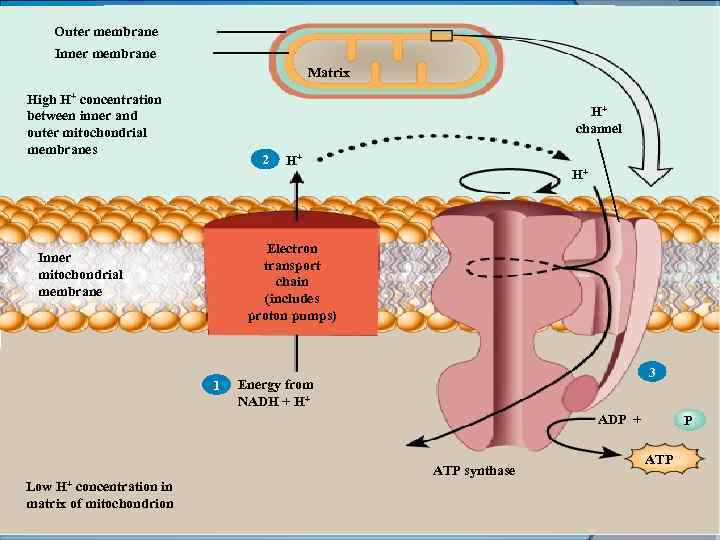 Outer membrane Inner membrane Matrix High H+ concentration High H between inner and outer mitochondrial outer membranes Inner mitochondrial membrane 1 H+ channel 2 2 H+ H+ H+ channel H+ H+ Electron transport chain (includes proton pumps) 3 Energy from 1 Energy NADH + H+ NADH ADP + ATP synthase Low H+ concentration in Low H+ matrix of mitochondrion matrix of P ATP
Outer membrane Inner membrane Matrix High H+ concentration High H between inner and outer mitochondrial outer membranes Inner mitochondrial membrane 1 H+ channel 2 2 H+ H+ H+ channel H+ H+ Electron transport chain (includes proton pumps) 3 Energy from 1 Energy NADH + H+ NADH ADP + ATP synthase Low H+ concentration in Low H+ matrix of mitochondrion matrix of P ATP
 Р/О−ТОТЫҒУДАН ФОСФОРЛАНУ КОЭФФИЦИЕНТІ. Р/О − АТФ ־ ТІ ТҮЗУГЕ КЕТКЕН БЕЙОРГАНИКАЛЫҚ ФОСФАТТЫҢ МОЛЬ САНЫН КӨРСЕТЕДІ (СІҢІРІЛГЕН ОТТЕКТІҢ БІР АТОМЫНА ЕСЕПТЕГЕНДЕ). Н/Е ТҮЗІЛГЕН АТФ-тің МОЛЬ САНЫН КӨРСЕТЕДІ. Р/О = 2 н/е 3
Р/О−ТОТЫҒУДАН ФОСФОРЛАНУ КОЭФФИЦИЕНТІ. Р/О − АТФ ־ ТІ ТҮЗУГЕ КЕТКЕН БЕЙОРГАНИКАЛЫҚ ФОСФАТТЫҢ МОЛЬ САНЫН КӨРСЕТЕДІ (СІҢІРІЛГЕН ОТТЕКТІҢ БІР АТОМЫНА ЕСЕПТЕГЕНДЕ). Н/Е ТҮЗІЛГЕН АТФ-тің МОЛЬ САНЫН КӨРСЕТЕДІ. Р/О = 2 н/е 3
 ЕГЕР СУБСТРАТ ПИРИДИН ФЕРМЕНТІ ПФ(НАД) АРҚЫЛЫ ТОТЫҚСА: Р/О = 3; себебі бұл кезде бөлінген энергия 3 АТФ түзуге жеткілікті. НАДН 2−ден О 2 −ке тасымалданатын протондар мен электрондар 3 қабысу нүктесін басып өтеді. НАДН 2 3 АТФ ЕГЕР СУБСТРАТ ФЛАВОПРОТЕИД ФП( ФАД) АРҚЫЛЫ ТОТЫҚСА: Р/О =2; ФПН 2 2 АТФ
ЕГЕР СУБСТРАТ ПИРИДИН ФЕРМЕНТІ ПФ(НАД) АРҚЫЛЫ ТОТЫҚСА: Р/О = 3; себебі бұл кезде бөлінген энергия 3 АТФ түзуге жеткілікті. НАДН 2−ден О 2 −ке тасымалданатын протондар мен электрондар 3 қабысу нүктесін басып өтеді. НАДН 2 3 АТФ ЕГЕР СУБСТРАТ ФЛАВОПРОТЕИД ФП( ФАД) АРҚЫЛЫ ТОТЫҚСА: Р/О =2; ФПН 2 2 АТФ
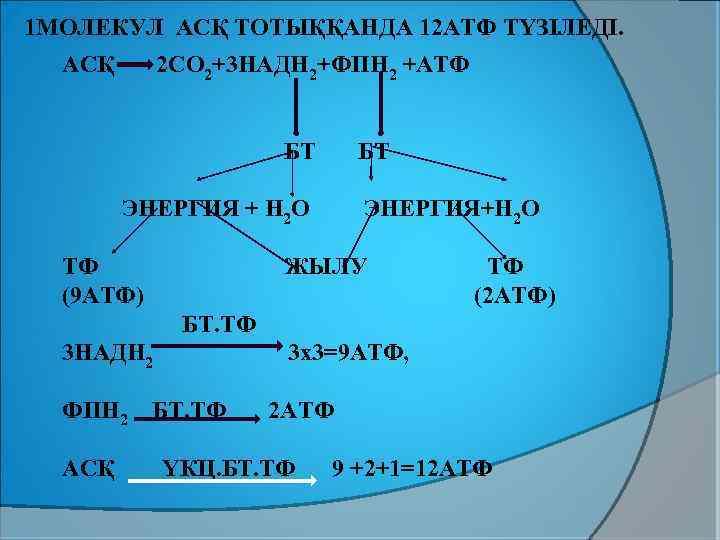 1 МОЛЕКУЛ АСҚ ТОТЫҚҚАНДА 12 АТФ ТҮЗІЛЕДІ. АСҚ 2 СО 2+3 НАДН 2+ФПН 2 +АТФ БТ БТ ЭНЕРГИЯ + Н 2 О ТФ (9 АТФ) ЭНЕРГИЯ+Н 2 О ЖЫЛУ ТФ (2 АТФ) БТ. ТФ 3 НАДН 2 3 х3=9 АТФ, ФПН 2 БТ. ТФ АСҚ 2 АТФ ҮКЦ. БТ. ТФ 9 +2+1=12 АТФ
1 МОЛЕКУЛ АСҚ ТОТЫҚҚАНДА 12 АТФ ТҮЗІЛЕДІ. АСҚ 2 СО 2+3 НАДН 2+ФПН 2 +АТФ БТ БТ ЭНЕРГИЯ + Н 2 О ТФ (9 АТФ) ЭНЕРГИЯ+Н 2 О ЖЫЛУ ТФ (2 АТФ) БТ. ТФ 3 НАДН 2 3 х3=9 АТФ, ФПН 2 БТ. ТФ АСҚ 2 АТФ ҮКЦ. БТ. ТФ 9 +2+1=12 АТФ
 Ферменттік ансамбль. БТ тізбегіне қатысатын ферменттер митохондрияның ішкі мембранасымен берік байланысқан, сызықты түрде орналаспайды, олар 4 комплекске (тыныс алу ансамблі) бірігіп электрондар мен протондарды тасымалдайды: I-комплекс ФП ФМН ; ол – НАДН 2 - ні тотықтырады; II -комплекс ФП ФАД ; ол органикалық қышқылдарды (сукцинат) тотықтырады , өздері ФАДН 2 -ге тотықсызданады; III -комплекс Цхb - Цхс1; Олар. Ко. QН 2 -ден электрондарды қосып алып ферро формаға айналады. IV -комплекс цитохромоксидаза (2 Цха+4 Цха 3 +6 Сu) н/е Цха мен Цх а 3 ; олар электрондарды ферро Цхс –дан О 2 –ке тасымалдайды.
Ферменттік ансамбль. БТ тізбегіне қатысатын ферменттер митохондрияның ішкі мембранасымен берік байланысқан, сызықты түрде орналаспайды, олар 4 комплекске (тыныс алу ансамблі) бірігіп электрондар мен протондарды тасымалдайды: I-комплекс ФП ФМН ; ол – НАДН 2 - ні тотықтырады; II -комплекс ФП ФАД ; ол органикалық қышқылдарды (сукцинат) тотықтырады , өздері ФАДН 2 -ге тотықсызданады; III -комплекс Цхb - Цхс1; Олар. Ко. QН 2 -ден электрондарды қосып алып ферро формаға айналады. IV -комплекс цитохромоксидаза (2 Цха+4 Цха 3 +6 Сu) н/е Цха мен Цх а 3 ; олар электрондарды ферро Цхс –дан О 2 –ке тасымалдайды.
 I ж/е II комплекс Ко. Q арқылы III – комплекспен байланысады, ал III ж/е IV–комплекс Цхс арқылы бірімен байланысады. Ко. Q мен Цхс тыныс алу комплексінің құрамына кірмейді.
I ж/е II комплекс Ко. Q арқылы III – комплекспен байланысады, ал III ж/е IV–комплекс Цхс арқылы бірімен байланысады. Ко. Q мен Цхс тыныс алу комплексінің құрамына кірмейді.
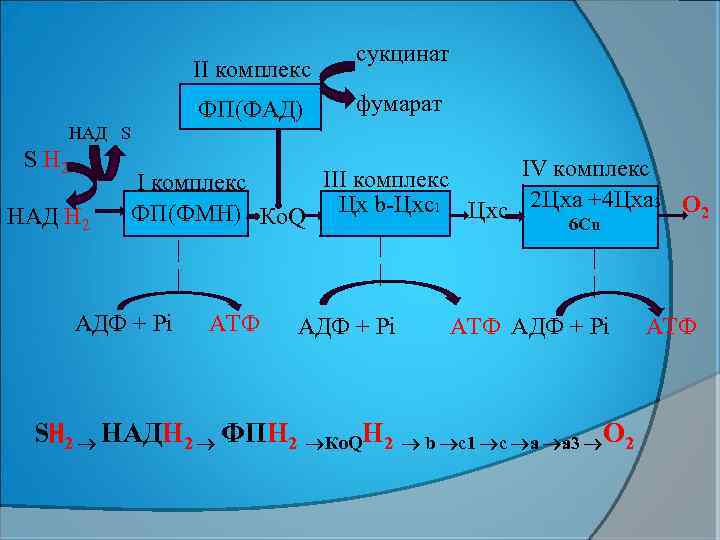 II комплекс ФП(ФАД) сукцинат фумарат НАД S S Н 2 НАД Н 2 IV комплекс III комплекс Цх b-Цхс1 Цхс 2 Цха +4 Цха 3 О 2 ФП(ФМН) Ко. Q 6 Сu | | | АДФ + Рi АТФ АДФ + Рi АТФ SН 2 НАДН 2 ФПН 2 Ко. QН 2 b c 1 c a a 3 О 2
II комплекс ФП(ФАД) сукцинат фумарат НАД S S Н 2 НАД Н 2 IV комплекс III комплекс Цх b-Цхс1 Цхс 2 Цха +4 Цха 3 О 2 ФП(ФМН) Ко. Q 6 Сu | | | АДФ + Рi АТФ АДФ + Рi АТФ SН 2 НАДН 2 ФПН 2 Ко. QН 2 b c 1 c a a 3 О 2
 БТ МЕН ТФ ӨЗАРА ТЫҒЫЗ БАЙЛАНЫСТЫ. БТ ЖЫЛДАМДЫҒЫН ТФ БАҚЫЛАЙДЫ, МҰНЫ ТЫНЫС АЛУДЫ БАҚЫЛАУ ДЕЙДІ. ЕГЕР: АДФ , АЛ АТФ БОЛСА− БТ ЖЫЛДАМДЫҒЫ ; АДФ , АЛ АТФ БОЛСА − БТ ЖЫЛДАМДЫҒЫ .
БТ МЕН ТФ ӨЗАРА ТЫҒЫЗ БАЙЛАНЫСТЫ. БТ ЖЫЛДАМДЫҒЫН ТФ БАҚЫЛАЙДЫ, МҰНЫ ТЫНЫС АЛУДЫ БАҚЫЛАУ ДЕЙДІ. ЕГЕР: АДФ , АЛ АТФ БОЛСА− БТ ЖЫЛДАМДЫҒЫ ; АДФ , АЛ АТФ БОЛСА − БТ ЖЫЛДАМДЫҒЫ .
 ЭНЕРГИЯ АЛМАСУЫ САТЫЛАРЫ БІР-БІРІМЕН ТЫҒЫЗ БАЙЛАНЫСТЫ. 1 -2 САТЫСЫ: АСҚ АРҚЫЛЫ БАЙЛАНЫСАДЫ. 1 САТЫДА ТҮЗІЛГЕН АСҚ 2 САТЫ ҮКЦ- де ТОТЫҒАДЫ. 2 -3 САТЫСЫ: ҮКЦ- де. ТОТЫҚСЫЗДАНҒАН ДЕГИДРОГЕНАЗАЛАР (НАДН 2 , ФАДН 2)АРҚЫЛЫ; НАДН 2 , ФАДН 2 тек БТ-да оксидоредуктазалар қатысуымен тотығады. 3 -4 САТЫСЫ: БТ ЭНЕРГИЯСЫ АРҚЫЛЫ. ТФ-да АДФ ПЕН ФОСФОР ҚЫШҚЫЛЫНАН БТ ЭНЕРГИЯСЫН ПАЙДАЛАНЫП АТФ ТҮЗІЛЕДІ.
ЭНЕРГИЯ АЛМАСУЫ САТЫЛАРЫ БІР-БІРІМЕН ТЫҒЫЗ БАЙЛАНЫСТЫ. 1 -2 САТЫСЫ: АСҚ АРҚЫЛЫ БАЙЛАНЫСАДЫ. 1 САТЫДА ТҮЗІЛГЕН АСҚ 2 САТЫ ҮКЦ- де ТОТЫҒАДЫ. 2 -3 САТЫСЫ: ҮКЦ- де. ТОТЫҚСЫЗДАНҒАН ДЕГИДРОГЕНАЗАЛАР (НАДН 2 , ФАДН 2)АРҚЫЛЫ; НАДН 2 , ФАДН 2 тек БТ-да оксидоредуктазалар қатысуымен тотығады. 3 -4 САТЫСЫ: БТ ЭНЕРГИЯСЫ АРҚЫЛЫ. ТФ-да АДФ ПЕН ФОСФОР ҚЫШҚЫЛЫНАН БТ ЭНЕРГИЯСЫН ПАЙДАЛАНЫП АТФ ТҮЗІЛЕДІ.
 ГИПОЭНЕРГЕТИКАЛЫҚ КҮЙ ־ АТФ СИНТЕЗІНІҢ ТӨМЕНДЕУІ: v. АШТЫҚ v. О 2 v. ЖАСУШАНЫ ОТТЕКПЕН ҚАМТАМАСЫ ЕТЕТІН ЖҮРЕК ־ ҚАН ТАМЫРЛАРЫ МЕН ТЫНЫС АЛУЖҮЙЕСІНІҢ БҰЗЫЛУЫ v. АНЕМИЯ v. ГИПОВИТАМИНОЗ
ГИПОЭНЕРГЕТИКАЛЫҚ КҮЙ ־ АТФ СИНТЕЗІНІҢ ТӨМЕНДЕУІ: v. АШТЫҚ v. О 2 v. ЖАСУШАНЫ ОТТЕКПЕН ҚАМТАМАСЫ ЕТЕТІН ЖҮРЕК ־ ҚАН ТАМЫРЛАРЫ МЕН ТЫНЫС АЛУЖҮЙЕСІНІҢ БҰЗЫЛУЫ v. АНЕМИЯ v. ГИПОВИТАМИНОЗ
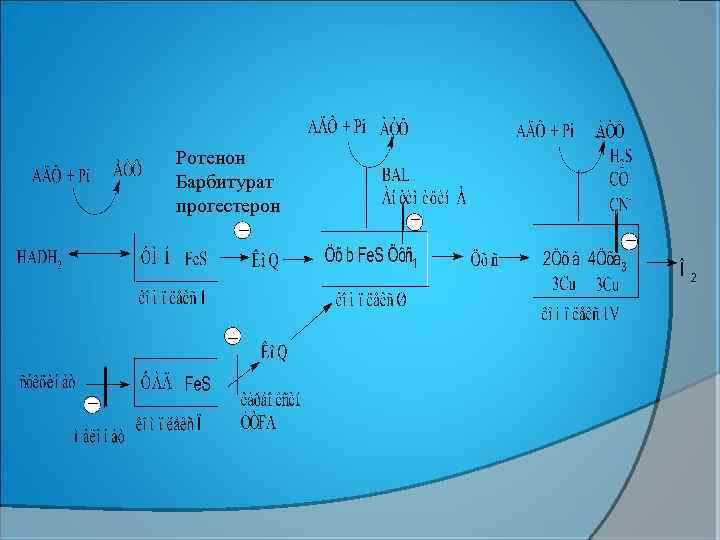 Ротенон Барбитурат прогестерон
Ротенон Барбитурат прогестерон
 БТ ИНГИБИТОРЛАРЫ НАДН-ДЕГИДРОГЕНАЗА ИНГИБИТОРЛАРЫ: РОТЕНОН, БАРБИТУРАТТАР (ВЕНОНАЛ, ГЕКСЕНАЛ, НЕМБУТАЛ, АМИТАЛ); ЦХв −с ИНГИБИТОРЛАРЫ- АНТИМИЦИН А; ЦИТОХРОМОКСИДАЗА ИНГИБИТОРЛАРЫ- ЦИАНИДТЕР(СN), УГАРНЫЙ ГАЗ (СО), Н 2 S.
БТ ИНГИБИТОРЛАРЫ НАДН-ДЕГИДРОГЕНАЗА ИНГИБИТОРЛАРЫ: РОТЕНОН, БАРБИТУРАТТАР (ВЕНОНАЛ, ГЕКСЕНАЛ, НЕМБУТАЛ, АМИТАЛ); ЦХв −с ИНГИБИТОРЛАРЫ- АНТИМИЦИН А; ЦИТОХРОМОКСИДАЗА ИНГИБИТОРЛАРЫ- ЦИАНИДТЕР(СN), УГАРНЫЙ ГАЗ (СО), Н 2 S.
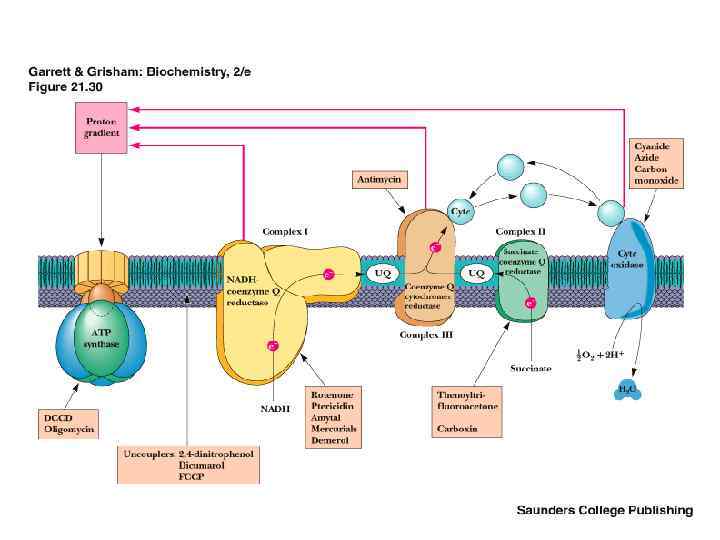
 АТФ түзілу үшін: 1 - митохондрия мембранасының өткізгіштігі қалыпты болуы керек; 2 - мембранада потенциалдың айырымы болуы керек.
АТФ түзілу үшін: 1 - митохондрия мембранасының өткізгіштігі қалыпты болуы керек; 2 - мембранада потенциалдың айырымы болуы керек.
 БТ МЕН ТФ АЖЫРАТУШЫ ЗАТТАРЫ КЕЙБІР ЛИПОФИЛЬДІ ПРОТОНОФОРЛАР МИТОХОНДРИЯ МЕМБРАНАСЫНЫҢ ӨТКІЗГІШТІГІН БҰЗЫП ПРОТОНДАРДЫ ПРОТОНДЫҚ НАСОС АРҚЫЛЫ ЕМЕС МИТОХОНДРИЯ МЕМБРАНАСЫ АРҚЫЛЫ МАТРИКСКЕ ТАСЫМАЛДАЙДЫ. ОНДА БТ МЕН ТФ АРАСЫНДАҒЫ БАЙЛАНЫСТАР ҮЗІЛІП , БІРІНЕН АЖЫРАЙДЫ. БҰЛ КЕЗДЕ БТ ЖҮРЕ БЕРЕДІ, БІРАҚ БӨЛІНГЕН ЭНЕРГИЯ ЖЫЛУ ТҮРІНДЕ ТАРАЛЫП, АТФ СИНТЕЗІ ТӨМЕНДЕЙДІ. ДЕНЕ ТЕМПЕРАТУРАСЫ ЖОҒАРЛАЙДЫ. Р/О КОЭФФИЦИЕНТІ ТӨМЕНДЕЙДІ.
БТ МЕН ТФ АЖЫРАТУШЫ ЗАТТАРЫ КЕЙБІР ЛИПОФИЛЬДІ ПРОТОНОФОРЛАР МИТОХОНДРИЯ МЕМБРАНАСЫНЫҢ ӨТКІЗГІШТІГІН БҰЗЫП ПРОТОНДАРДЫ ПРОТОНДЫҚ НАСОС АРҚЫЛЫ ЕМЕС МИТОХОНДРИЯ МЕМБРАНАСЫ АРҚЫЛЫ МАТРИКСКЕ ТАСЫМАЛДАЙДЫ. ОНДА БТ МЕН ТФ АРАСЫНДАҒЫ БАЙЛАНЫСТАР ҮЗІЛІП , БІРІНЕН АЖЫРАЙДЫ. БҰЛ КЕЗДЕ БТ ЖҮРЕ БЕРЕДІ, БІРАҚ БӨЛІНГЕН ЭНЕРГИЯ ЖЫЛУ ТҮРІНДЕ ТАРАЛЫП, АТФ СИНТЕЗІ ТӨМЕНДЕЙДІ. ДЕНЕ ТЕМПЕРАТУРАСЫ ЖОҒАРЛАЙДЫ. Р/О КОЭФФИЦИЕНТІ ТӨМЕНДЕЙДІ.
 ЭКЗОГЕНДІ АЖЫРАТҚЫШТАР− 2, 4 -ДИНИТРОФЕНОЛ, ДИКУМАРОЛ, СТРЕПТОМИЦИН; ЭНДОГЕНДІ АЖЫРАТҚЫШТАР−МАЙ ҚЫШҚЫЛДАРЫ, ҚАЛҚАНША БЕЗІНІҢ ГОРМОНЫ ־ ТИРОКСИН, ӨТ ПИГМЕНТІ ־ БИЛИРУБИН, ТЕРМОГЕНИН БЕЛОГЫ. ФОСФОРЛАНУДЫҢ ТЕЖЕГІШТЕРІ−ОЛИГОМИЦИН. АТФСИНТЕТАЗА ӘСЕРІН ТЕЖЕЙДІ.
ЭКЗОГЕНДІ АЖЫРАТҚЫШТАР− 2, 4 -ДИНИТРОФЕНОЛ, ДИКУМАРОЛ, СТРЕПТОМИЦИН; ЭНДОГЕНДІ АЖЫРАТҚЫШТАР−МАЙ ҚЫШҚЫЛДАРЫ, ҚАЛҚАНША БЕЗІНІҢ ГОРМОНЫ ־ ТИРОКСИН, ӨТ ПИГМЕНТІ ־ БИЛИРУБИН, ТЕРМОГЕНИН БЕЛОГЫ. ФОСФОРЛАНУДЫҢ ТЕЖЕГІШТЕРІ−ОЛИГОМИЦИН. АТФСИНТЕТАЗА ӘСЕРІН ТЕЖЕЙДІ.
 ӘДЕБИЕТТЕР: Негізгі: • Биохимия. Под ред. проф. Е. С. Северина, А. Я. Николаева, М. , 2014 ж. • Т. Ш. Шарманов, С. М. Плешкова «Метаболические основы питания с курсом общей биохимии» , Алматы, 1998 г. • «Медицинская биохимия» , Астана, 2001 г. • В. Дж. Маршал «Клиническая биохимия» , 2000 г. Қосымша: 1. Б. Гринстейн, А. Гринстейн «Наглядная биохимия» , 2000 г. 2. Т. Т. Березов, Б. Ф. Коровкин «Биологическая химия» , 2005 г. 3. Д. Г. Кнорре, С. Д. Мызина «Биологическая химия» , Москва, 2002 г. 4. Р. Марри, Д. Греннер «Биохимия человека» , I-II том, 1993 г. 5. А. Ш. Зайчик, Л. Г. Чурилов «Основы патохимии» , Москва, 2001 г. 6. Полосухина Т. Я. , Аблаев Н. Р. «Материалы к курсу биологической химии» , 1977 – С. 3, 30 -33, 47 -49, 59 -62. 7. Бышевский А. Ш. , Терсенов О. А. «Биохимия для врача» , 1994 – С. 34 -54, 75, 95, 108, 214 -216, 224, 249. 8. Н. Р. Аблаев Биохимия в схемах и рисунках, Алматы 2005 г. 9. Биохимия. Краткий курс с упражнениями и задачами. Под ред. проф. Е. С. Северина, А. Я. Николаева, М. , 2002 г.
ӘДЕБИЕТТЕР: Негізгі: • Биохимия. Под ред. проф. Е. С. Северина, А. Я. Николаева, М. , 2014 ж. • Т. Ш. Шарманов, С. М. Плешкова «Метаболические основы питания с курсом общей биохимии» , Алматы, 1998 г. • «Медицинская биохимия» , Астана, 2001 г. • В. Дж. Маршал «Клиническая биохимия» , 2000 г. Қосымша: 1. Б. Гринстейн, А. Гринстейн «Наглядная биохимия» , 2000 г. 2. Т. Т. Березов, Б. Ф. Коровкин «Биологическая химия» , 2005 г. 3. Д. Г. Кнорре, С. Д. Мызина «Биологическая химия» , Москва, 2002 г. 4. Р. Марри, Д. Греннер «Биохимия человека» , I-II том, 1993 г. 5. А. Ш. Зайчик, Л. Г. Чурилов «Основы патохимии» , Москва, 2001 г. 6. Полосухина Т. Я. , Аблаев Н. Р. «Материалы к курсу биологической химии» , 1977 – С. 3, 30 -33, 47 -49, 59 -62. 7. Бышевский А. Ш. , Терсенов О. А. «Биохимия для врача» , 1994 – С. 34 -54, 75, 95, 108, 214 -216, 224, 249. 8. Н. Р. Аблаев Биохимия в схемах и рисунках, Алматы 2005 г. 9. Биохимия. Краткий курс с упражнениями и задачами. Под ред. проф. Е. С. Северина, А. Я. Николаева, М. , 2002 г.
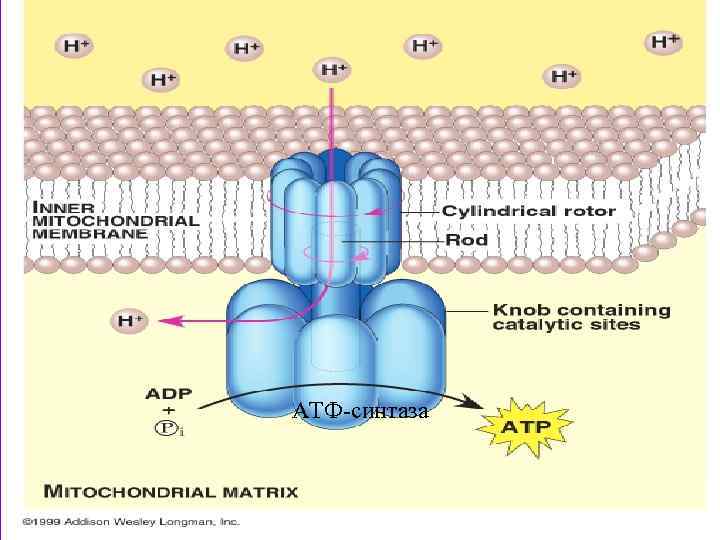 АТФ-синтаза
АТФ-синтаза
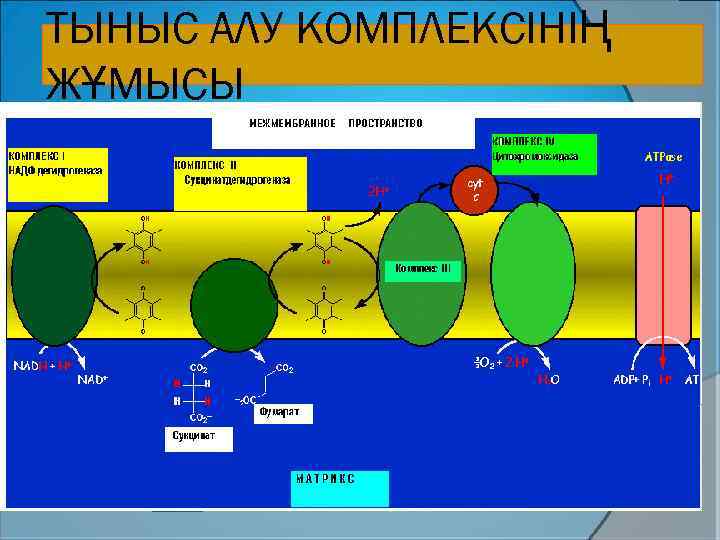 ТЫНЫС АЛУ КОМПЛЕКСІНІҢ ЖҰМЫСЫ
ТЫНЫС АЛУ КОМПЛЕКСІНІҢ ЖҰМЫСЫ
 НАЗАРЛАРЫҢЫЗҒА РАХМЕТ!
НАЗАРЛАРЫҢЫЗҒА РАХМЕТ!
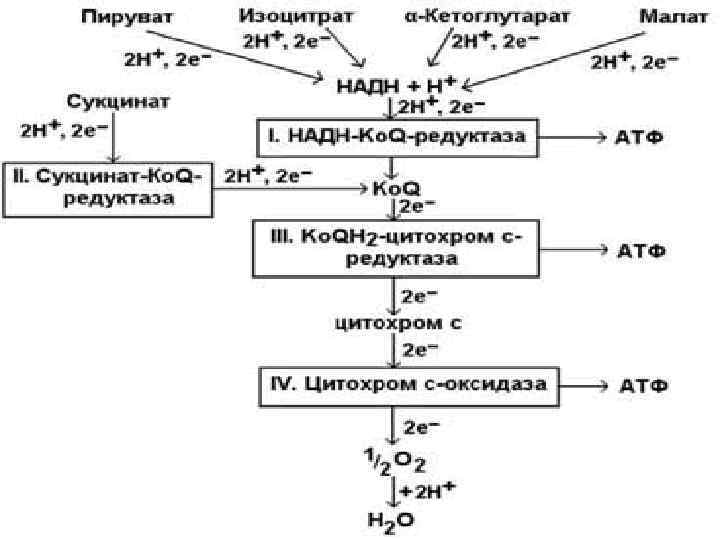
 В цепь биологического окисления или тканевого дыхания вступают в основном НАДН 2, который получается в результате бета-окисления жирных кислот, окислительного дезаминтрования аминокислот, окислительного декарбоксилирования пировиноградной кислоты и, особенно, в цикле трикарбоновых кислот. Все указанные процессы протекают в митохондриях. Ферменты тканевого дыхания размещаются во внутренней мембране митохондрий и образуют так называемые дыхательные комплексы, или дыхательные ансамбли. Таких дыхательных комплексов 4, пятым комплексом является АТФ-синтаза, превращающая энергию разрядки во внутренней мембране в макроэргическую связь АТФ. Состав ДК, последовательность и характер их функционирования показаны на следующей схеме: При работе дыхательных комплексов I, III и IV освобождается энергия, которой достаточно для образования АТФ из АДФ и фосфата АДФ + Н 3 РО 4 + Е. Б. О АТФ + Н 2 О
В цепь биологического окисления или тканевого дыхания вступают в основном НАДН 2, который получается в результате бета-окисления жирных кислот, окислительного дезаминтрования аминокислот, окислительного декарбоксилирования пировиноградной кислоты и, особенно, в цикле трикарбоновых кислот. Все указанные процессы протекают в митохондриях. Ферменты тканевого дыхания размещаются во внутренней мембране митохондрий и образуют так называемые дыхательные комплексы, или дыхательные ансамбли. Таких дыхательных комплексов 4, пятым комплексом является АТФ-синтаза, превращающая энергию разрядки во внутренней мембране в макроэргическую связь АТФ. Состав ДК, последовательность и характер их функционирования показаны на следующей схеме: При работе дыхательных комплексов I, III и IV освобождается энергия, которой достаточно для образования АТФ из АДФ и фосфата АДФ + Н 3 РО 4 + Е. Б. О АТФ + Н 2 О
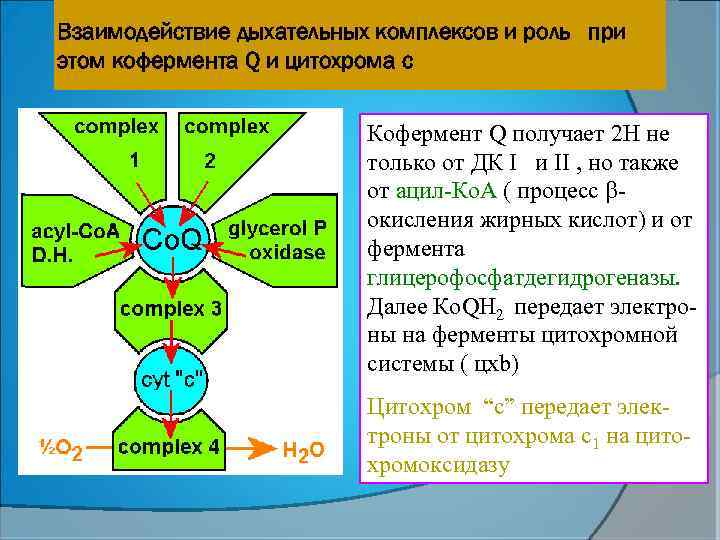 Взаимодействие дыхательных комплексов и роль при этом кофермента Q и цитохрома с Кофермент Q получает 2 Н не только от ДК I и II , но также от ацил-Ко. А ( процесс окисления жирных кислот) и от фермента глицерофосфатдегидрогеназы. Далее Ко. QH 2 передает электроны на ферменты цитохромной системы ( цхb) Цитохром “с” передает электроны от цитохрома c 1 на цитохромоксидазу
Взаимодействие дыхательных комплексов и роль при этом кофермента Q и цитохрома с Кофермент Q получает 2 Н не только от ДК I и II , но также от ацил-Ко. А ( процесс окисления жирных кислот) и от фермента глицерофосфатдегидрогеназы. Далее Ко. QH 2 передает электроны на ферменты цитохромной системы ( цхb) Цитохром “с” передает электроны от цитохрома c 1 на цитохромоксидазу
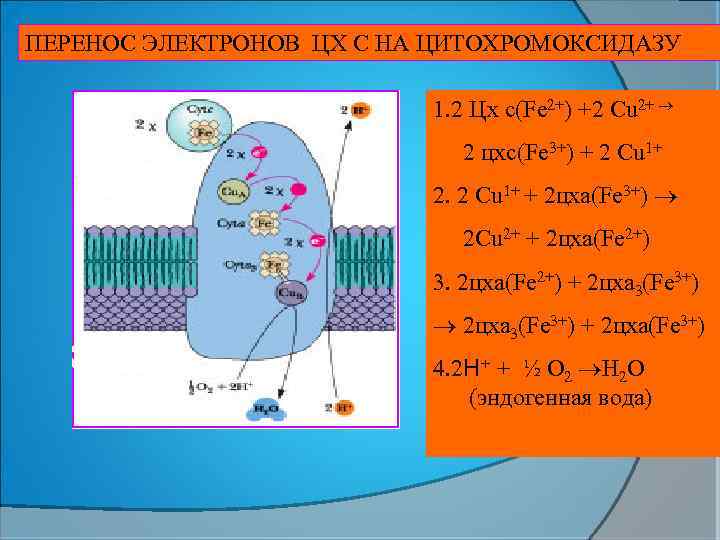 ПЕРЕНОС ЭЛЕКТРОНОВ ЦХ С НА ЦИТОХРОМОКСИДАЗУ 1. 2 Цх с(Fe 2+) +2 Cu 2+ 2 цхс(Fe 3+) + 2 Cu 1+ 2. 2 Cu 1+ + 2 цха(Fe 3+) 2 Сu 2+ + 2 цха(Fe 2+) 3. 2 цха(Fe 2+) + 2 цха 3(Fe 3+) + 2 цха(Fe 3+) 4. 2 Н+ + ½ O 2 H 2 O (эндогенная вода)
ПЕРЕНОС ЭЛЕКТРОНОВ ЦХ С НА ЦИТОХРОМОКСИДАЗУ 1. 2 Цх с(Fe 2+) +2 Cu 2+ 2 цхс(Fe 3+) + 2 Cu 1+ 2. 2 Cu 1+ + 2 цха(Fe 3+) 2 Сu 2+ + 2 цха(Fe 2+) 3. 2 цха(Fe 2+) + 2 цха 3(Fe 3+) + 2 цха(Fe 3+) 4. 2 Н+ + ½ O 2 H 2 O (эндогенная вода)
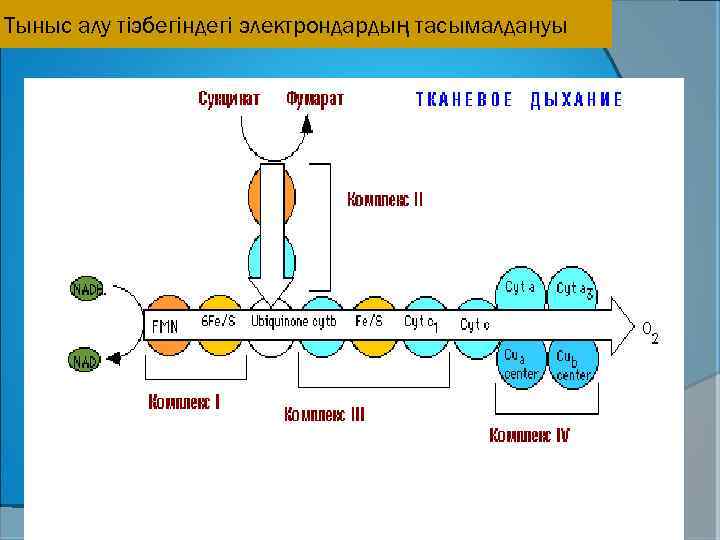 Тыныс алу тіэбегіндегі электрондардың тасымалдануы
Тыныс алу тіэбегіндегі электрондардың тасымалдануы
 ӘДЕБИЕТТЕР: Негізгі: • Т. Ш. Шарманов, С. М. Плешкова «Метаболические основы питания с курсом общей биохимии» , Алматы, 1998 г. • С. Тапбергенов «Медицинская биохимия» , Астана, 2001 г. • С. Сеитов «Биохимия» , Алматы, 2001 г. • В. Дж. Маршал «Клиническая биохимия» , 2000 г. Қосымша: 1. Б. Гринстейн, А. Гринстейн «Наглядная биохимия» , 2000 г. 2. Т. Т. Березов, Б. Ф. Коровкин «Биологическая химия» , 2005 г. 3. Д. Г. Кнорре, С. Д. Мызина «Биологическая химия» , Москва, 2002 г. 4. Р. Марри, Д. Греннер «Биохимия человека» , I-II том, 1993 г. 5. А. Ш. Зайчик, Л. Г. Чурилов «Основы патохимии» , Москва, 2001 г. 6. Полосухина Т. Я. , Аблаев Н. Р. «Материалы к курсу биологической химии» , 1977 – С. 3, 30 -33, 47 -49, 59 -62. 7. Бышевский А. Ш. , Терсенов О. А. «Биохимия для врача» , 1994 – С. 34 -54, 75, 95, 108, 214 -216, 224, 249. 8. Н. Р. Аблаев Биохимия в схемах и рисунках, Алматы 2005 г. 9. Биохимия. Краткий курс с упражнениями и задачами. Под ред. проф. Е. С. Северина, А. Я. Николаева, М. , 2002 г. 1. ҚОРЫТЫНДЫ СҰРАҚТАР: 2. 1. Энергия алмасуының сатылары. 3. 2. Көмірсулар, липидтердің және белоктардың арнайы жолдармен ыдырауына сипаттама. 4. 3. Үш карбон қышқылдарының цикліне сипаттама. 5. 4. ҮКЦ реакциялары және оған қатысатын негізгі ферменттер.
ӘДЕБИЕТТЕР: Негізгі: • Т. Ш. Шарманов, С. М. Плешкова «Метаболические основы питания с курсом общей биохимии» , Алматы, 1998 г. • С. Тапбергенов «Медицинская биохимия» , Астана, 2001 г. • С. Сеитов «Биохимия» , Алматы, 2001 г. • В. Дж. Маршал «Клиническая биохимия» , 2000 г. Қосымша: 1. Б. Гринстейн, А. Гринстейн «Наглядная биохимия» , 2000 г. 2. Т. Т. Березов, Б. Ф. Коровкин «Биологическая химия» , 2005 г. 3. Д. Г. Кнорре, С. Д. Мызина «Биологическая химия» , Москва, 2002 г. 4. Р. Марри, Д. Греннер «Биохимия человека» , I-II том, 1993 г. 5. А. Ш. Зайчик, Л. Г. Чурилов «Основы патохимии» , Москва, 2001 г. 6. Полосухина Т. Я. , Аблаев Н. Р. «Материалы к курсу биологической химии» , 1977 – С. 3, 30 -33, 47 -49, 59 -62. 7. Бышевский А. Ш. , Терсенов О. А. «Биохимия для врача» , 1994 – С. 34 -54, 75, 95, 108, 214 -216, 224, 249. 8. Н. Р. Аблаев Биохимия в схемах и рисунках, Алматы 2005 г. 9. Биохимия. Краткий курс с упражнениями и задачами. Под ред. проф. Е. С. Северина, А. Я. Николаева, М. , 2002 г. 1. ҚОРЫТЫНДЫ СҰРАҚТАР: 2. 1. Энергия алмасуының сатылары. 3. 2. Көмірсулар, липидтердің және белоктардың арнайы жолдармен ыдырауына сипаттама. 4. 3. Үш карбон қышқылдарының цикліне сипаттама. 5. 4. ҮКЦ реакциялары және оған қатысатын негізгі ферменттер.
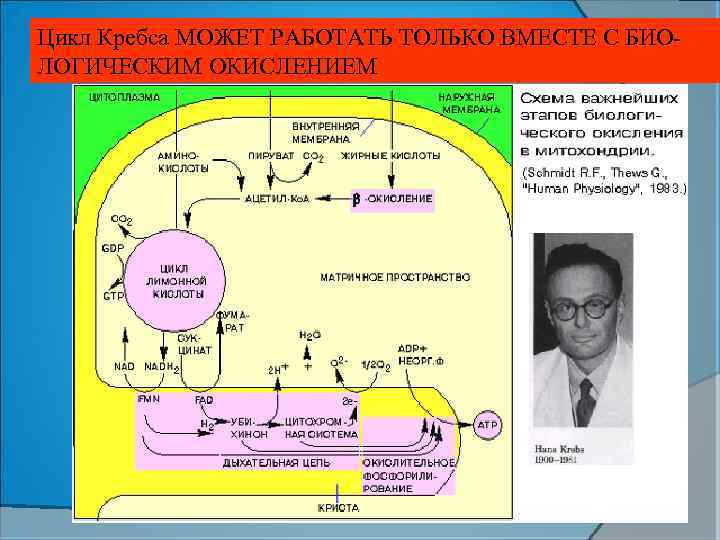 Цикл Кребса МОЖЕТ РАБОТАТЬ ТОЛЬКО ВМЕСТЕ С БИО- ЛОГИЧЕСКИМ ОКИСЛЕНИЕМ Схема важнейших этапов биоокисления
Цикл Кребса МОЖЕТ РАБОТАТЬ ТОЛЬКО ВМЕСТЕ С БИО- ЛОГИЧЕСКИМ ОКИСЛЕНИЕМ Схема важнейших этапов биоокисления


