лекция 5 - энергетика хим. процессов.ppt
- Количество слайдов: 24
 Энергетика химических реакций 1
Энергетика химических реакций 1
 Термодинамика система - открытая - закрытая - изолированная 2
Термодинамика система - открытая - закрытая - изолированная 2
![Тепловая энергия Q, [Дж] Параметры состояния: P, T, V, состав системы 3 Тепловая энергия Q, [Дж] Параметры состояния: P, T, V, состав системы 3](https://present5.com/presentation/43238305_452878220/image-3.jpg) Тепловая энергия Q, [Дж] Параметры состояния: P, T, V, состав системы 3
Тепловая энергия Q, [Дж] Параметры состояния: P, T, V, состав системы 3
 Функции состояния: Внутренняя энергия U, Энтальпия H, Энтропия S, Энергия Гиббса (изобарноизотермический потенциал) G. 4
Функции состояния: Внутренняя энергия U, Энтальпия H, Энтропия S, Энергия Гиббса (изобарноизотермический потенциал) G. 4
 Первый закон термодинамики Q = U + A U = U 2 – U 1, U 2 и U 1 – внутренняя энергия системы в состоянии 2 и 1 соответственно. A = p(V 2–V 1) = p△V 5
Первый закон термодинамики Q = U + A U = U 2 – U 1, U 2 и U 1 – внутренняя энергия системы в состоянии 2 и 1 соответственно. A = p(V 2–V 1) = p△V 5
 Изохорный процесс: V=const, V = 0, А = 0, тогда QV = U Изобарный процесс: Р=const V = V 2 – V 1, А = р V Qp = U + р V Qp = (U 2 + р. V 2) – (U 1 + р. V 1) 6
Изохорный процесс: V=const, V = 0, А = 0, тогда QV = U Изобарный процесс: Р=const V = V 2 – V 1, А = р V Qp = U + р V Qp = (U 2 + р. V 2) – (U 1 + р. V 1) 6
 H = U + р. V, Отсюда: Qp = Н 2 – Н 1 = Н Энтальпия, H [к. Дж/моль] H 0 – эндотермический процесс H 0 – экзотермический процесс 7
H = U + р. V, Отсюда: Qp = Н 2 – Н 1 = Н Энтальпия, H [к. Дж/моль] H 0 – эндотермический процесс H 0 – экзотермический процесс 7
![H обр или f. H 298 , [к. Дж/моль] H 2(г) + 1/2 H обр или f. H 298 , [к. Дж/моль] H 2(г) + 1/2](https://present5.com/presentation/43238305_452878220/image-8.jpg) H обр или f. H 298 , [к. Дж/моль] H 2(г) + 1/2 О 2(г) H 2 O(ж); при 25 С и 101 к. Па r. H = – 285, 84 к. Дж r. Н 0, реакция экзотермическая 8
H обр или f. H 298 , [к. Дж/моль] H 2(г) + 1/2 О 2(г) H 2 O(ж); при 25 С и 101 к. Па r. H = – 285, 84 к. Дж r. Н 0, реакция экзотермическая 8
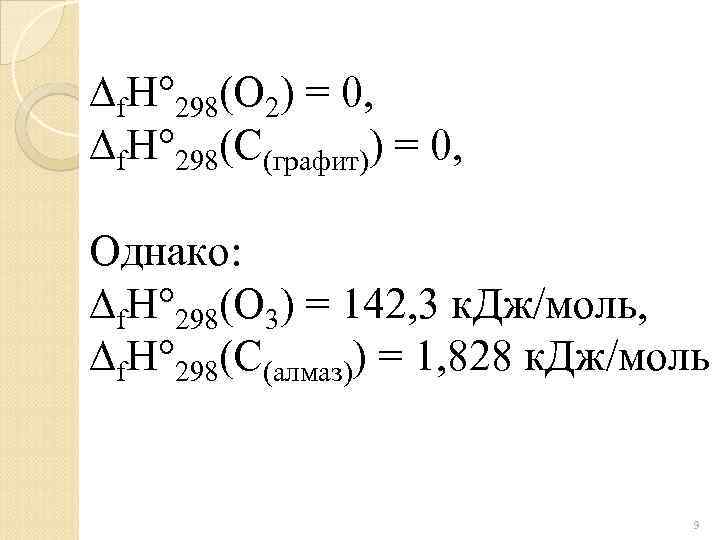 f. H 298(O 2) = 0, f. H 298(C(графит)) = 0, Однако: f. H 298(O 3) = 142, 3 к. Дж/моль, f. H 298(C(алмаз)) = 1, 828 к. Дж/моль 9
f. H 298(O 2) = 0, f. H 298(C(графит)) = 0, Однако: f. H 298(O 3) = 142, 3 к. Дж/моль, f. H 298(C(алмаз)) = 1, 828 к. Дж/моль 9
 Закон Лавуазье-Лапласа 1/2 H 2 (г) + 1/2 Сl 2(г) HCl(г); r. H 298(HCl) = – 92 к. Дж HCl(г) 1/2 H 2 (г) + 1/2 Сl 2(г); r. H 298 = +92 к. Дж 10
Закон Лавуазье-Лапласа 1/2 H 2 (г) + 1/2 Сl 2(г) HCl(г); r. H 298(HCl) = – 92 к. Дж HCl(г) 1/2 H 2 (г) + 1/2 Сl 2(г); r. H 298 = +92 к. Дж 10
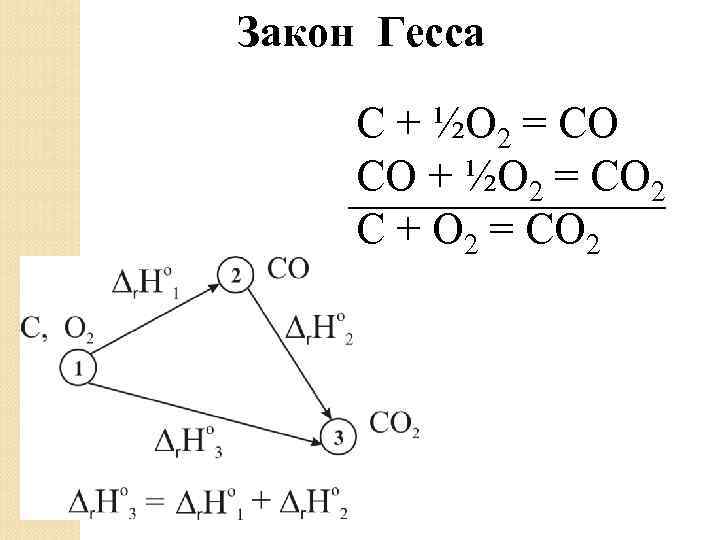 Закон Гесса C + ½O 2 = CO CO + ½O 2 = CO 2 C + O 2 = CO 2
Закон Гесса C + ½O 2 = CO CO + ½O 2 = CO 2 C + O 2 = CO 2
 Следствие из закона Гесса: H = Для реакции в общем виде: а. А + b. B c. C + d. D H = [c Hобр(C) + d Hобр(D)] – – [a Hобр(A) + b Hобр(B)] 12
Следствие из закона Гесса: H = Для реакции в общем виде: а. А + b. B c. C + d. D H = [c Hобр(C) + d Hобр(D)] – – [a Hобр(A) + b Hобр(B)] 12
 Пример: Вычислить тепловой эффект реакции горения бензола по стандартным энтальпиям образования f. H 298 С 6 Н 6(ж) + 7/2 О 2(г) = 6 СО 2(г) + 3 Н 2 О(ж) 40, 6 0 – 394, 7 – 286 Воспользуемся следствием из закона Гесса: r. H = 6 H (СО 2(г)) + 3 H ( Н 2 О(ж)) – H ( С 6 Н 6(ж)), r. H = 6(– 394, 7) +3 (– 286) – (+ 40, 6) = – 3186, 8 к. Дж.
Пример: Вычислить тепловой эффект реакции горения бензола по стандартным энтальпиям образования f. H 298 С 6 Н 6(ж) + 7/2 О 2(г) = 6 СО 2(г) + 3 Н 2 О(ж) 40, 6 0 – 394, 7 – 286 Воспользуемся следствием из закона Гесса: r. H = 6 H (СО 2(г)) + 3 H ( Н 2 О(ж)) – H ( С 6 Н 6(ж)), r. H = 6(– 394, 7) +3 (– 286) – (+ 40, 6) = – 3186, 8 к. Дж.
![Энтропия, S [Дж/(моль К)] Процессы, для которых S 0: 1) расширение газов; 2) Sтв Энтропия, S [Дж/(моль К)] Процессы, для которых S 0: 1) расширение газов; 2) Sтв](https://present5.com/presentation/43238305_452878220/image-14.jpg) Энтропия, S [Дж/(моль К)] Процессы, для которых S 0: 1) расширение газов; 2) Sтв Sжид Sгаз SН 2 О(пар) = 183 Дж/(моль К) SН 2 О(жидк. ) = 69 Дж/(моль К) SН 2 О(лед) = 43, 89 Дж/(моль К) 3) растворение кристаллических веществ. SCo(алмаз) = 2, 38 Дж/моль К SCo(графит) = 5, 74 Дж/моль К
Энтропия, S [Дж/(моль К)] Процессы, для которых S 0: 1) расширение газов; 2) Sтв Sжид Sгаз SН 2 О(пар) = 183 Дж/(моль К) SН 2 О(жидк. ) = 69 Дж/(моль К) SН 2 О(лед) = 43, 89 Дж/(моль К) 3) растворение кристаллических веществ. SCo(алмаз) = 2, 38 Дж/моль К SCo(графит) = 5, 74 Дж/моль К
 Процессы, для которых S 0: 1) сжатие газов; 2) конденсация и кристаллизация веществ. Рассчитывается по следствию из закона Гесса: S =
Процессы, для которых S 0: 1) сжатие газов; 2) конденсация и кристаллизация веществ. Рассчитывается по следствию из закона Гесса: S =
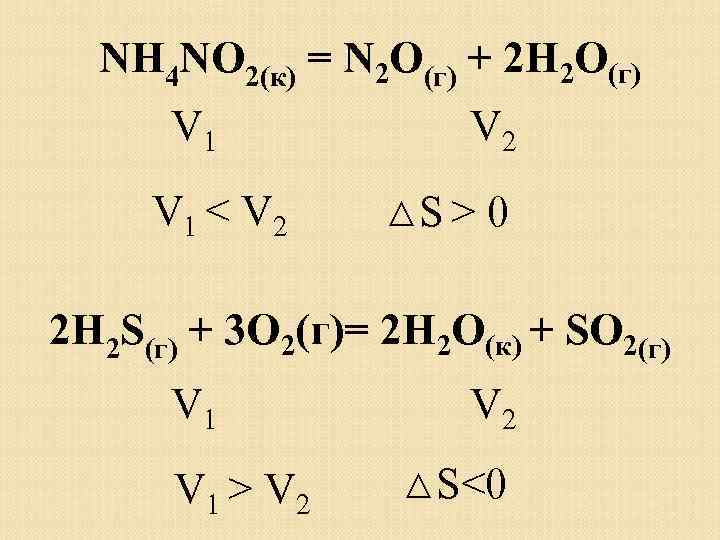 NH 4 NO 2(к) = N 2 О(г) + 2 H 2 О(г) V 1 < V 2 △S > 0 2 H 2 S(г) + 3 O 2(г)= 2 H 2 О(к) + SО 2(г) V 1 > V 2 △S<0
NH 4 NO 2(к) = N 2 О(г) + 2 H 2 О(г) V 1 < V 2 △S > 0 2 H 2 S(г) + 3 O 2(г)= 2 H 2 О(к) + SО 2(г) V 1 > V 2 △S<0
![Энергия Гиббса, G, [к. Дж/моль] G = Н – Т S Энергия Гиббса, G, [к. Дж/моль] G = Н – Т S](https://present5.com/presentation/43238305_452878220/image-17.jpg) Энергия Гиббса, G, [к. Дж/моль] G = Н – Т S
Энергия Гиббса, G, [к. Дж/моль] G = Н – Т S
 G 0 – процесс термодинамически возможен (реакция идет самопроизвольно); G 0 – процесс термодинамически невозможен (реакция не идет); G = 0 – система находится в состоянии химического равновесия.
G 0 – процесс термодинамически возможен (реакция идет самопроизвольно); G 0 – процесс термодинамически невозможен (реакция не идет); G = 0 – система находится в состоянии химического равновесия.
 Возможность протекания реакции G = Н – Т S Реакция экзотермическая Н 0, S > 0, то всегда G 0, т. е. реакция протекает при всех t. Н < 0, S < 0, то реакция протекает при низких t (т. е. должно выполняться условие │ H│>│T S│) ( G 0).
Возможность протекания реакции G = Н – Т S Реакция экзотермическая Н 0, S > 0, то всегда G 0, т. е. реакция протекает при всех t. Н < 0, S < 0, то реакция протекает при низких t (т. е. должно выполняться условие │ H│>│T S│) ( G 0).
 G = Н – Т S Реакция эндотермическая Н > 0, S < 0, то всегда G > 0 , т. е. реакция не протекает. Н > 0, S > 0, то реакция протекает при высоких t (т. е. должно выполняться условие │ H│<│T S│) ( G 0).
G = Н – Т S Реакция эндотермическая Н > 0, S < 0, то всегда G > 0 , т. е. реакция не протекает. Н > 0, S > 0, то реакция протекает при высоких t (т. е. должно выполняться условие │ H│<│T S│) ( G 0).
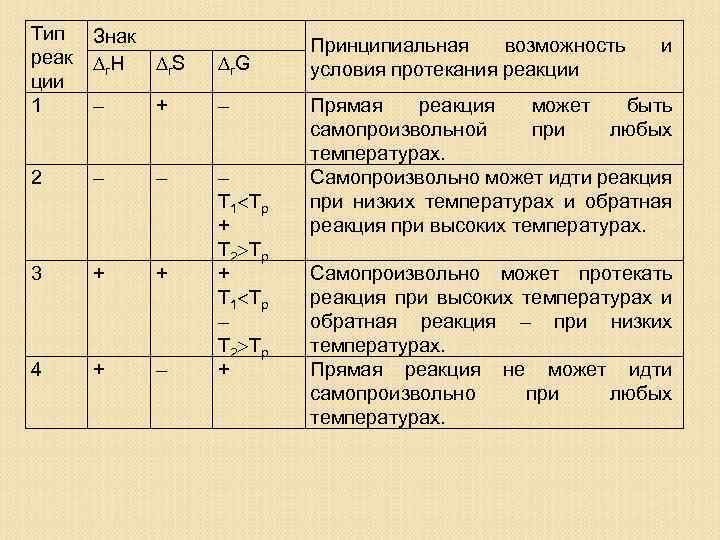 Тип реак ции 1 Знак r. Н r. S r. G – + – 2 – – 3 + + 4 + – – Т 1 Тр + Т 2 Тр + Т 1 Тр – Т 2 Тр + Принципиальная возможность условия протекания реакции и Прямая реакция может быть самопроизвольной при любых температурах. Самопроизвольно может идти реакция при низких температурах и обратная реакция при высоких температурах. Самопроизвольно может протекать реакция при высоких температурах и обратная реакция – при низких температурах. Прямая реакция не может идти самопроизвольно при любых температурах.
Тип реак ции 1 Знак r. Н r. S r. G – + – 2 – – 3 + + 4 + – – Т 1 Тр + Т 2 Тр + Т 1 Тр – Т 2 Тр + Принципиальная возможность условия протекания реакции и Прямая реакция может быть самопроизвольной при любых температурах. Самопроизвольно может идти реакция при низких температурах и обратная реакция при высоких температурах. Самопроизвольно может протекать реакция при высоких температурах и обратная реакция – при низких температурах. Прямая реакция не может идти самопроизвольно при любых температурах.
 NH 3(г) + HCl(г) = NH 4 Сl(к) при 298 К r. Н = ? r. S = ? r. G = ? Выписываем из справочных данных: Вещество NH 3(г) Н , к. Дж/моль – 46, 19 S , Дж/моль К 192, 50 HCl(г) NH 4 Сl(к) – 92, 3 – 315, 39 186, 7 94, 56
NH 3(г) + HCl(г) = NH 4 Сl(к) при 298 К r. Н = ? r. S = ? r. G = ? Выписываем из справочных данных: Вещество NH 3(г) Н , к. Дж/моль – 46, 19 S , Дж/моль К 192, 50 HCl(г) NH 4 Сl(к) – 92, 3 – 315, 39 186, 7 94, 56
 Из з-на Гесса энтальпия реакции: r. Н = Н (NH 4 Сl(к)) – Н (NH 3(г)) – Н (HCl(г)) = – 315, 39 – (– 46, 19 – 92, 3) = – 176, 9 к. Дж. Изменение энтропии реакции: r. S = S (NH 4 Сl(к)) – S (NH 3(г)) – S (HCl(г)) = = 94, 56 – 192, 50 – 186, 70 = – 284, 64 Дж/моль К. Используем ур-е Гиббса: r. G = r. Н – Т r. S r. G = – 176, 9 + 284, 64 10– 3 303 = – 90, 55 к. Дж. r. G 0, реакция идет
Из з-на Гесса энтальпия реакции: r. Н = Н (NH 4 Сl(к)) – Н (NH 3(г)) – Н (HCl(г)) = – 315, 39 – (– 46, 19 – 92, 3) = – 176, 9 к. Дж. Изменение энтропии реакции: r. S = S (NH 4 Сl(к)) – S (NH 3(г)) – S (HCl(г)) = = 94, 56 – 192, 50 – 186, 70 = – 284, 64 Дж/моль К. Используем ур-е Гиббса: r. G = r. Н – Т r. S r. G = – 176, 9 + 284, 64 10– 3 303 = – 90, 55 к. Дж. r. G 0, реакция идет
 Энтальпия сгорания этана f. Hо 298 = -1560 к. Дж/моль Вычислить энтальпию образования этана C 2 H 6(г) + 31/2 O 2(г) = 2 CO 2(г) + 3 H 2 O(ж) Х 0 -393, 5 -286, 2 r. Hо 298= 2 f. Hо 298 CO 2 + 3 f. Hо 298 H 2 O – - f. Hо 298(C 2 H 6) -1560 = 2(-393, 5) + 3(-286, 2)-X X = -85, 6 к. Дж/моль 24
Энтальпия сгорания этана f. Hо 298 = -1560 к. Дж/моль Вычислить энтальпию образования этана C 2 H 6(г) + 31/2 O 2(г) = 2 CO 2(г) + 3 H 2 O(ж) Х 0 -393, 5 -286, 2 r. Hо 298= 2 f. Hо 298 CO 2 + 3 f. Hо 298 H 2 O – - f. Hо 298(C 2 H 6) -1560 = 2(-393, 5) + 3(-286, 2)-X X = -85, 6 к. Дж/моль 24


