Л.1_ендо_рег_КЦ.ppt
- Количество слайдов: 27
 ЕНДОГЕННА РЕГУЛЯЦІЯ КЛІТИННОГО ЦИКЛУ 1. Дослідження L. Hartwell із США в 1970 -1971 рр. - клітини пекарських дріжджів. Він ввів поняття «контрольна точка» - чекпоінт (checkpoint), які розташовані в кінцях G 1, G 2 і М фаз. 2. PM Nurse продовжив розпочаті дослідження клітинного циклу, використовуючи клітини дріжджів іншого типу -в середині 70 -х рр. . відкрив в клітинах цих дріжджів ген сдс2, який грає ключову функцію в регуляції переходу від G 2 до М. У 1987 р. він виділив такий же ген у людини - СDK 1, його продукт білок - циклін -залежна протеїнкіназа, активність якого залежить від зворотного фосфорилювання. За відкриття циклінів та циклін-залежних кіназ в 2001 р Leland H. Hartwell, R. Timothy Hunt і Paul M. Nurse отримали Нобелівську Премію в галузі Медицини і Фізіології
ЕНДОГЕННА РЕГУЛЯЦІЯ КЛІТИННОГО ЦИКЛУ 1. Дослідження L. Hartwell із США в 1970 -1971 рр. - клітини пекарських дріжджів. Він ввів поняття «контрольна точка» - чекпоінт (checkpoint), які розташовані в кінцях G 1, G 2 і М фаз. 2. PM Nurse продовжив розпочаті дослідження клітинного циклу, використовуючи клітини дріжджів іншого типу -в середині 70 -х рр. . відкрив в клітинах цих дріжджів ген сдс2, який грає ключову функцію в регуляції переходу від G 2 до М. У 1987 р. він виділив такий же ген у людини - СDK 1, його продукт білок - циклін -залежна протеїнкіназа, активність якого залежить від зворотного фосфорилювання. За відкриття циклінів та циклін-залежних кіназ в 2001 р Leland H. Hartwell, R. Timothy Hunt і Paul M. Nurse отримали Нобелівську Премію в галузі Медицини і Фізіології
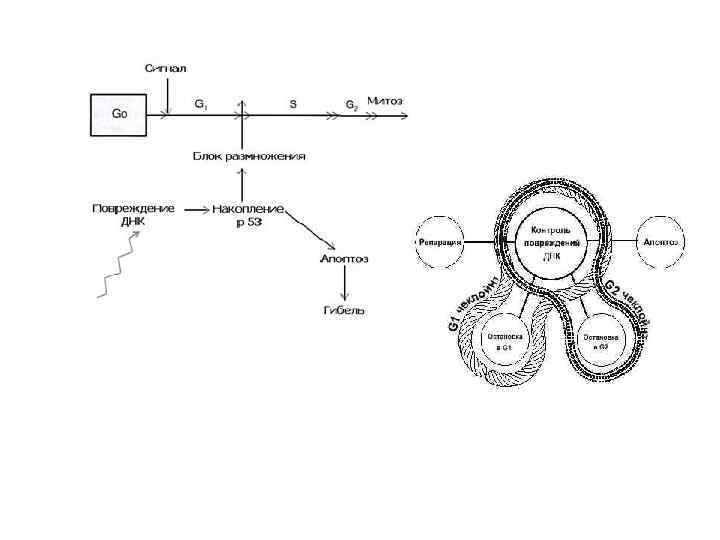
 При вивченні ендогенної регуляції клітинного циклу було використано результати досліджень трьох груп експериментів: - експерименти, які стосуються злиття клітин - вивчення поділу бластомерів - дослідження мутантів (це в основному стосується клітин-дріждів).
При вивченні ендогенної регуляції клітинного циклу було використано результати досліджень трьох груп експериментів: - експерименти, які стосуються злиття клітин - вивчення поділу бластомерів - дослідження мутантів (це в основному стосується клітин-дріждів).
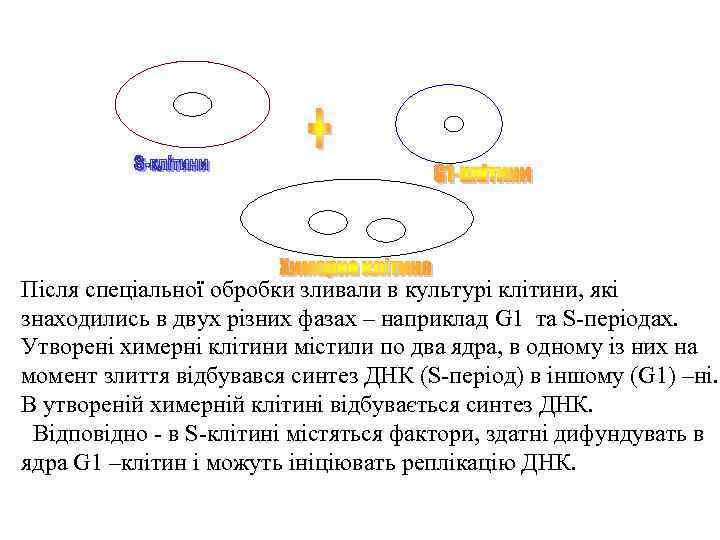 Після спеціальної обробки зливали в культурі клітини, які знаходились в двух різних фазах – наприклад G 1 та S-періодах. Утворені химерні клітини містили по два ядра, в одному із них на момент злиття відбувався синтез ДНК (S-період) в іншому (G 1) –ні. В утвореній химерній клітині відбувається синтез ДНК. Відповідно - в S-клітині містяться фактори, здатні дифундувать в ядра G 1 –клітин і можуть ініціювать реплікацію ДНК.
Після спеціальної обробки зливали в культурі клітини, які знаходились в двух різних фазах – наприклад G 1 та S-періодах. Утворені химерні клітини містили по два ядра, в одному із них на момент злиття відбувався синтез ДНК (S-період) в іншому (G 1) –ні. В утвореній химерній клітині відбувається синтез ДНК. Відповідно - в S-клітині містяться фактори, здатні дифундувать в ядра G 1 –клітин і можуть ініціювать реплікацію ДНК.
 2. Дослідження поділу бластомерів. Для цього було використано гігантські яйцеклітини амфібій та морських їжаків, а також утворені із них зародки на ранніх стадіях розвитку. Як відомо, на цих стадіях інтенсивно відбувається мітотичний поділ – всі клітини при цьому діляться одночасно. Все це дозволяє використовувати цей біологічний матеріал для отримання біохімічних білкових факторів, відповідальних за мітоз. Після очистки відповідних субстанцій їх вводять в фракцію ооцитів, які знаходяться в самому початку мейозу. Якщо в отриманому зразку містяться фактори, що запускають поділ, ооцити із стану спокою вступають в мейотичний поділ і перетворюються в яйцеклітину
2. Дослідження поділу бластомерів. Для цього було використано гігантські яйцеклітини амфібій та морських їжаків, а також утворені із них зародки на ранніх стадіях розвитку. Як відомо, на цих стадіях інтенсивно відбувається мітотичний поділ – всі клітини при цьому діляться одночасно. Все це дозволяє використовувати цей біологічний матеріал для отримання біохімічних білкових факторів, відповідальних за мітоз. Після очистки відповідних субстанцій їх вводять в фракцію ооцитів, які знаходяться в самому початку мейозу. Якщо в отриманому зразку містяться фактори, що запускають поділ, ооцити із стану спокою вступають в мейотичний поділ і перетворюються в яйцеклітину
 3. Дослідження дріжджевих клітин - мутантів. Для зручності в цих експериментах використовують дріжджі, в вегетативній фазі життєдіяльності їх клітини гаплоїдні (містять по одній копії генів), що полегшує виявлення мутацій, які можна індукувати різними способами: опроміненням, нагріванням, хімічними агентами. Подібні мутації порушують клітинний цикл, при якому змінююються розміри клітин. А)при мутаціях cdc (cell-division-cycle цикл поділу клітин) мутаціях йде блокування поділу клітин, що призводить до їх постійного росту без почкування – формуються гігантські клітини Б). крихітні мутації wee-поділ відбувається до того, як клітина встигла достатньо подовжитись – в результаті утворюються клітини дуже малої довжини. В обох випадках ушкоджуються різні гени, для ідентифікації яких поступають наступним чином: -виділяють ДНК із нормальних клітин -фрагментують її за допомогою рестриктаз -включають отримані фрагменти нормальної ДНК в склад різних плазмід -вводять плазміди із досліджуваним фрагментом в мутантні клітини Якщо мутація рецесивна, а введений фрагмент ДНК містить “правильну” версію мутованого гену, то клітинний цикл нормалізується і утворюється колонія клітин звичайного розміру. Таким чином можно досліджувати роль кожного із генів в регуляції клітинного циклу.
3. Дослідження дріжджевих клітин - мутантів. Для зручності в цих експериментах використовують дріжджі, в вегетативній фазі життєдіяльності їх клітини гаплоїдні (містять по одній копії генів), що полегшує виявлення мутацій, які можна індукувати різними способами: опроміненням, нагріванням, хімічними агентами. Подібні мутації порушують клітинний цикл, при якому змінююються розміри клітин. А)при мутаціях cdc (cell-division-cycle цикл поділу клітин) мутаціях йде блокування поділу клітин, що призводить до їх постійного росту без почкування – формуються гігантські клітини Б). крихітні мутації wee-поділ відбувається до того, як клітина встигла достатньо подовжитись – в результаті утворюються клітини дуже малої довжини. В обох випадках ушкоджуються різні гени, для ідентифікації яких поступають наступним чином: -виділяють ДНК із нормальних клітин -фрагментують її за допомогою рестриктаз -включають отримані фрагменти нормальної ДНК в склад різних плазмід -вводять плазміди із досліджуваним фрагментом в мутантні клітини Якщо мутація рецесивна, а введений фрагмент ДНК містить “правильну” версію мутованого гену, то клітинний цикл нормалізується і утворюється колонія клітин звичайного розміру. Таким чином можно досліджувати роль кожного із генів в регуляції клітинного циклу.
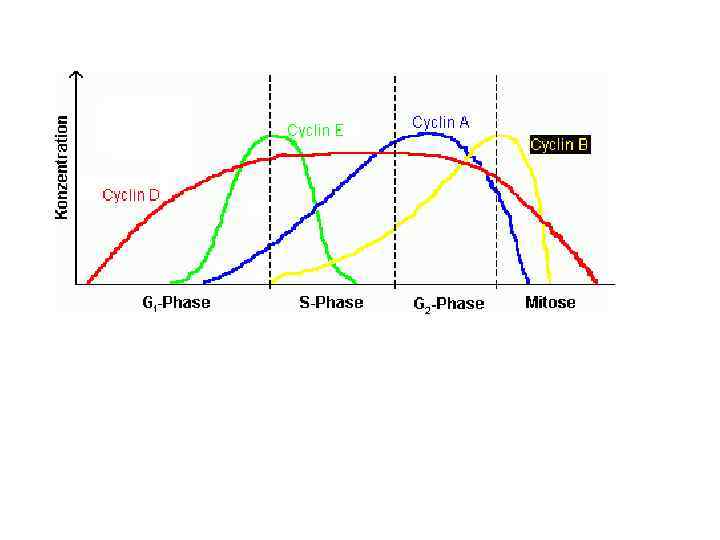
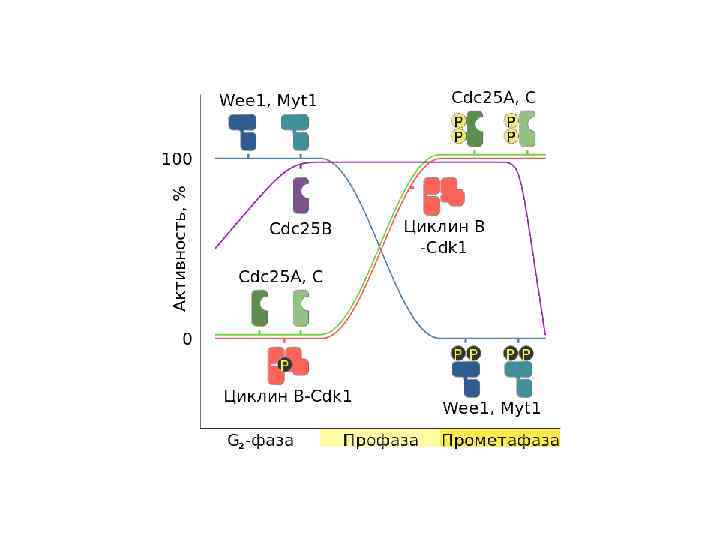
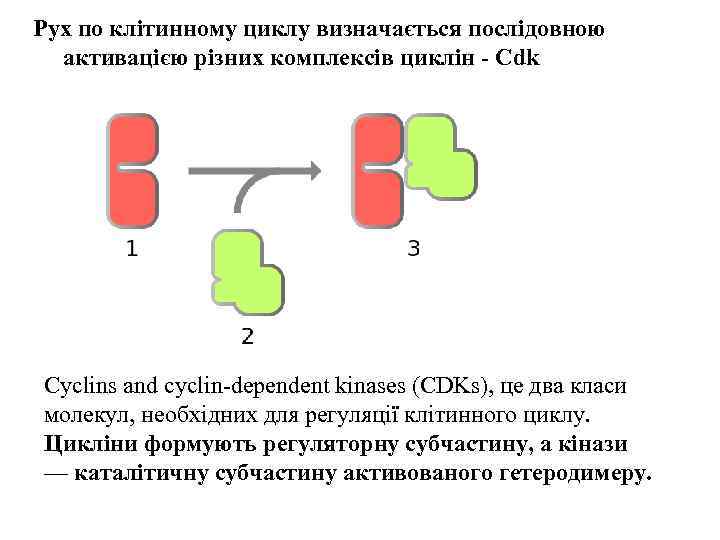 Рух по клітинному циклу визначається послідовною активацією різних комплексів циклін - Cdk Cyclins and cyclin-dependent kinases (CDKs), це два класи молекул, необхідних для регуляції клітинного циклу. Цикліни формують регуляторну субчастину, а кінази — каталітичну субчастину активованого гетеродимеру.
Рух по клітинному циклу визначається послідовною активацією різних комплексів циклін - Cdk Cyclins and cyclin-dependent kinases (CDKs), це два класи молекул, необхідних для регуляції клітинного циклу. Цикліни формують регуляторну субчастину, а кінази — каталітичну субчастину активованого гетеродимеру.
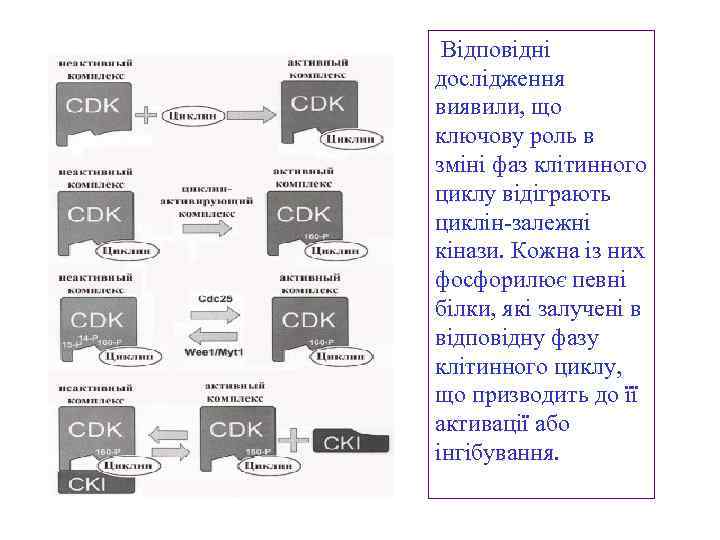 Відповідні дослідження виявили, що ключову роль в зміні фаз клітинного циклу відіграють циклін-залежні кінази. Кожна із них фосфорилює певні білки, які залучені в відповідну фазу клітинного циклу, що призводить до її активації або інгібування.
Відповідні дослідження виявили, що ключову роль в зміні фаз клітинного циклу відіграють циклін-залежні кінази. Кожна із них фосфорилює певні білки, які залучені в відповідну фазу клітинного циклу, що призводить до її активації або інгібування.
 • Циклінзалежні кінази (Cdk) - високоспецифічні протеїнкінази, що фосфорилюють певні білки різних фаз клітинного циклу і таким чином активують або інгібують їх. • Cdk функціонує в комплексі з цикліном, який не лише активує кіназу, а й визначає її субстратну специфічність. • Циклін-Cdk – гетеродимерний комплекс, в якому циклін відіграє роль регуляторної (активаторної) субодиниці, а Cdk – каталітичної.
• Циклінзалежні кінази (Cdk) - високоспецифічні протеїнкінази, що фосфорилюють певні білки різних фаз клітинного циклу і таким чином активують або інгібують їх. • Cdk функціонує в комплексі з цикліном, який не лише активує кіназу, а й визначає її субстратну специфічність. • Циклін-Cdk – гетеродимерний комплекс, в якому циклін відіграє роль регуляторної (активаторної) субодиниці, а Cdk – каталітичної.
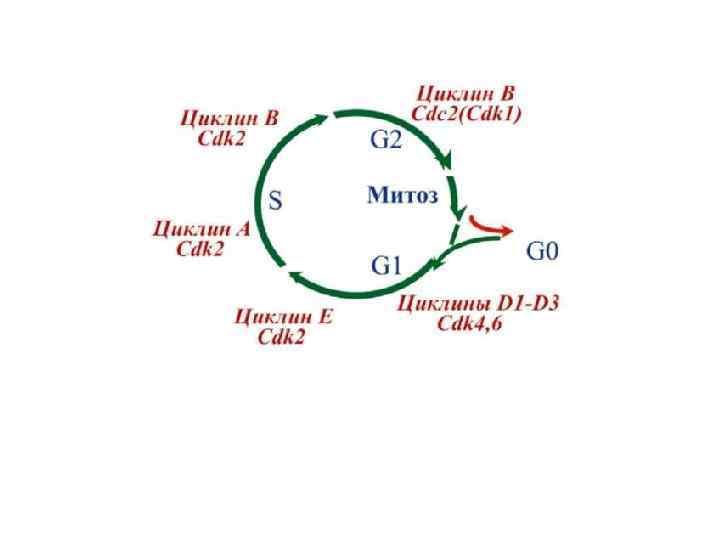
 РЕГУЛЯЦІЯ ЕКСПРЕСІЇ ГЕНІВ CDKS • Комплекси G 1 -періоду (циклін D– Cdk 4, 6 та циклін Е–Cdk 2), окрім інших різноманітних впливів, запускають транскрипцію гену Cdk 1. Зв’язування активаторної субодиниці – цикліну. Зв’язування інгібіторної субодиниці. Інгібіторами Cdk є білки двох родин – INK 4 (p 15, p 16) та КІР 1 (р21, р27, р57), які перешкоджають активації Cdks. Фосфорилювання/дефосфорилювання Cdks специфічними кіназами/фосфатазами, що призводить до їх активації чи інгібування.
РЕГУЛЯЦІЯ ЕКСПРЕСІЇ ГЕНІВ CDKS • Комплекси G 1 -періоду (циклін D– Cdk 4, 6 та циклін Е–Cdk 2), окрім інших різноманітних впливів, запускають транскрипцію гену Cdk 1. Зв’язування активаторної субодиниці – цикліну. Зв’язування інгібіторної субодиниці. Інгібіторами Cdk є білки двох родин – INK 4 (p 15, p 16) та КІР 1 (р21, р27, р57), які перешкоджають активації Cdks. Фосфорилювання/дефосфорилювання Cdks специфічними кіназами/фосфатазами, що призводить до їх активації чи інгібування.
 РЕГУЛЯЦІЯ СИНТЕЗУ ТА РОЗПАДУ АКТИВАТОРІВ ТА ІНГІБІТОРІВ CDKS • Синтез циклінів: кінцевою мішенню дії мітогенних факторів часто є ген цикліну D. • Розпад циклінів: убіквітинзалежний протеоліз. Циклін В–Cdk 1 (MPF) фосфорилює певні білки і стимулює вхід клітини в мітоз, але для завершення мітозу рівень MPF має зменшитись. Це забезпечується наступним чином: під час метафази мітозу MPF фосфорилює, окрім інших білків, фактор APC (anaphase-promoting complex) – убіквітинлігазу, специфічну до MPF. АРС швидко приєднує молекули убіквітину до цикліну В, який після цього швидко руйнується в протеосомі. • Синтез інгібіторів Cdks: в деяких регуляторних шляхах білки родини Smad стимулюють синтез р15, р21 та інших інгібіторів, в результаті чого поділи припиняються.
РЕГУЛЯЦІЯ СИНТЕЗУ ТА РОЗПАДУ АКТИВАТОРІВ ТА ІНГІБІТОРІВ CDKS • Синтез циклінів: кінцевою мішенню дії мітогенних факторів часто є ген цикліну D. • Розпад циклінів: убіквітинзалежний протеоліз. Циклін В–Cdk 1 (MPF) фосфорилює певні білки і стимулює вхід клітини в мітоз, але для завершення мітозу рівень MPF має зменшитись. Це забезпечується наступним чином: під час метафази мітозу MPF фосфорилює, окрім інших білків, фактор APC (anaphase-promoting complex) – убіквітинлігазу, специфічну до MPF. АРС швидко приєднує молекули убіквітину до цикліну В, який після цього швидко руйнується в протеосомі. • Синтез інгібіторів Cdks: в деяких регуляторних шляхах білки родини Smad стимулюють синтез р15, р21 та інших інгібіторів, в результаті чого поділи припиняються.
 РЕЗУЛЬТАТ ВПЛИВУ МІТОГЕНІВ: • Підвищення вмісту в клітині цикліну D та Cdk 4, Cdk 6. • Зниження вмісту інгібіторів Cdks. • Дефосфорилювання і підвищення активності Cdk 4, Cdk 6, а також Cdk 2. ØВсе це забезпечує накопичення в клітині активних комплексів циклін D–Cdk 4, 6. Вони починають готувати клітину до поділу.
РЕЗУЛЬТАТ ВПЛИВУ МІТОГЕНІВ: • Підвищення вмісту в клітині цикліну D та Cdk 4, Cdk 6. • Зниження вмісту інгібіторів Cdks. • Дефосфорилювання і підвищення активності Cdk 4, Cdk 6, а також Cdk 2. ØВсе це забезпечує накопичення в клітині активних комплексів циклін D–Cdk 4, 6. Вони починають готувати клітину до поділу.
 ДІЯ АНТИМІТОГЕНІВ • TNFα через сигнальні шляхи сфінгозину та РКС інгібує каскад МАРК, в результаті чого в клітині знижується кількість активних комплексів циклін D–Cdk 4, 6 і поділи припиняються. Водночас через інші сигнальні шляхи TNFα ініціює апоптоз. • TGFβ-рецептор фосфорилює і активує Smad 2 та Smad 3, після чого вони приєднують Smad 4 і дифундують в ядро, щоб активувати експресію генів інгібіторів Cdks (p 15, p 21). Накопичення цих інгібіторів призводить до зупинки проліферації.
ДІЯ АНТИМІТОГЕНІВ • TNFα через сигнальні шляхи сфінгозину та РКС інгібує каскад МАРК, в результаті чого в клітині знижується кількість активних комплексів циклін D–Cdk 4, 6 і поділи припиняються. Водночас через інші сигнальні шляхи TNFα ініціює апоптоз. • TGFβ-рецептор фосфорилює і активує Smad 2 та Smad 3, після чого вони приєднують Smad 4 і дифундують в ядро, щоб активувати експресію генів інгібіторів Cdks (p 15, p 21). Накопичення цих інгібіторів призводить до зупинки проліферації.
 РОЛЬ ПОЗАКЛІТИННОГО МАТРИКСУ • Більшість клітин можуть ділитися, тільки будучи прикріпленими до позаклітинного матриксу (базальної мембрани, колагенових волокон, поверхні флакона тощо). • Інформація про такий зв’язок надходить від інтегринів через тирозинкінази FAK та Src. Субстратом Src є адапторний білок SHC, який передає сигнал на каскад МАРК паралельно з сигналом від рецепторів факторів росту. ØТобто для вступу в мітотичний цикл необхідні як сигнал про прикріплення до субстрату, так і мітогенна стимуляція, причому в неприкріпленій клітині активація мітозу блокується.
РОЛЬ ПОЗАКЛІТИННОГО МАТРИКСУ • Більшість клітин можуть ділитися, тільки будучи прикріпленими до позаклітинного матриксу (базальної мембрани, колагенових волокон, поверхні флакона тощо). • Інформація про такий зв’язок надходить від інтегринів через тирозинкінази FAK та Src. Субстратом Src є адапторний білок SHC, який передає сигнал на каскад МАРК паралельно з сигналом від рецепторів факторів росту. ØТобто для вступу в мітотичний цикл необхідні як сигнал про прикріплення до субстрату, так і мітогенна стимуляція, причому в неприкріпленій клітині активація мітозу блокується.
 КОНТАКТНЕ ГАЛЬМУВАННЯ ПРОЛІФЕРАЦІЇ • При контакті з навколишніми клітинами проліферація припиняється. • Сигнал про міжклітинний контакт надходить від адгезивних білків кадгеринів. При взаємодії з іншою клітиною кадгерин набуває здатності зв’язувати білок β-катенін. У вільній формі β-катенін утворює активний комплекс із транскрипційним фактором Tcf 4, який мігрує в ядро і в кінцевому результаті стимулює експресію генів цикліну D та білка Мус (останній активує експресію фосфатази, яка дефосфорилює і активує Cdk 4). • При міжклітинній взаємодії β-катенін зв’язується з кадгерином, і поділи припиняються.
КОНТАКТНЕ ГАЛЬМУВАННЯ ПРОЛІФЕРАЦІЇ • При контакті з навколишніми клітинами проліферація припиняється. • Сигнал про міжклітинний контакт надходить від адгезивних білків кадгеринів. При взаємодії з іншою клітиною кадгерин набуває здатності зв’язувати білок β-катенін. У вільній формі β-катенін утворює активний комплекс із транскрипційним фактором Tcf 4, який мігрує в ядро і в кінцевому результаті стимулює експресію генів цикліну D та білка Мус (останній активує експресію фосфатази, яка дефосфорилює і активує Cdk 4). • При міжклітинній взаємодії β-катенін зв’язується з кадгерином, і поділи припиняються.
 СИГНАЛЬНІ ШЛЯХИ CDKS: ВИСНОВКИ • Для того, щоб розпочався клітинний цикл, необхідне утворення певного комплексу транскрипційних факторів, що активують експресію генів ранньої відповіді. • Цей комплекс містить β-катенін та фактор Tcf 4 (коли немає міжклітинних контактів), а також фактори, що активуються через каскад МАРК (його повноцінне функціонування можливе при дії ростового фактора та за умови прикріплення клітини до матриксу). • Отже, для вступу в мітотичний цикл необхідне виконання трьох умов: o відсутність міжклітинних контактів o прикріплення клітини до субстрату o позаклітинний стимул (ростовий фактор)
СИГНАЛЬНІ ШЛЯХИ CDKS: ВИСНОВКИ • Для того, щоб розпочався клітинний цикл, необхідне утворення певного комплексу транскрипційних факторів, що активують експресію генів ранньої відповіді. • Цей комплекс містить β-катенін та фактор Tcf 4 (коли немає міжклітинних контактів), а також фактори, що активуються через каскад МАРК (його повноцінне функціонування можливе при дії ростового фактора та за умови прикріплення клітини до матриксу). • Отже, для вступу в мітотичний цикл необхідне виконання трьох умов: o відсутність міжклітинних контактів o прикріплення клітини до субстрату o позаклітинний стимул (ростовий фактор)
 ЗАГАЛЬНИЙ ПРИНЦИП ПЕРЕБІГУ ЦИКЛУ • Комплекс циклін–Сdk чергової стадії циклу забезпечує: o інактивацію комплексу попередньої стадії o стимуляцію подій поточної стадії o утворення або активацію комплексів наступної стадії Ø Тобто діє своєрідний ланцюговий механізм, в якому кожна стадія процесу готує умови для наступної стадії, причому після проходу точки рестрикції процес іде незалежно від зовнішніх стимулів.
ЗАГАЛЬНИЙ ПРИНЦИП ПЕРЕБІГУ ЦИКЛУ • Комплекс циклін–Сdk чергової стадії циклу забезпечує: o інактивацію комплексу попередньої стадії o стимуляцію подій поточної стадії o утворення або активацію комплексів наступної стадії Ø Тобто діє своєрідний ланцюговий механізм, в якому кожна стадія процесу готує умови для наступної стадії, причому після проходу точки рестрикції процес іде незалежно від зовнішніх стимулів.
 МЕХАНІЗМ ДІЇ КОМПЛЕКСІВ G 1 -ПЕРІОДУ. АКТИВАЦІЯ PRB • Комплекси циклін D–Cdk 4, 6 фосфорилюють білок p. Rb та подібні до нього білки р105 та р130. • Білок p. Rb в нефосфорильованому стані інгібує транскрипційні фактори E 2 F i DP. Після фосфорилювання p. Rb дисоціює, а комплекс E 2 F-DP активується і набуває здатності стимулювати експресію цілого ряду генів, серед них: o гени циклінів Е, А та Cdk 1, 2 o гени самих факторів E 2 F (позитивний зворотний зв’язок, самопідтримання процесу) o гени ключових ферментів синтезу ДНК (підготовка до S-періоду) o гени наступних транскрипційних факторів, що стимулють в кінці G 1 -періоду синтез цикліну В
МЕХАНІЗМ ДІЇ КОМПЛЕКСІВ G 1 -ПЕРІОДУ. АКТИВАЦІЯ PRB • Комплекси циклін D–Cdk 4, 6 фосфорилюють білок p. Rb та подібні до нього білки р105 та р130. • Білок p. Rb в нефосфорильованому стані інгібує транскрипційні фактори E 2 F i DP. Після фосфорилювання p. Rb дисоціює, а комплекс E 2 F-DP активується і набуває здатності стимулювати експресію цілого ряду генів, серед них: o гени циклінів Е, А та Cdk 1, 2 o гени самих факторів E 2 F (позитивний зворотний зв’язок, самопідтримання процесу) o гени ключових ферментів синтезу ДНК (підготовка до S-періоду) o гени наступних транскрипційних факторів, що стимулють в кінці G 1 -періоду синтез цикліну В
 МЕХАНІЗМ ДІЇ КОМПЛЕКСІВ G 1 -ПЕРІОДУ • Фосфорилювання та інактивація АРС (anaphase promoting factor) – убіквітинлігази, яка стимулює швидкий протеоліз цикліну В. Як наслідок, рівень цикліну В продовжує зростати до метафази мітозу. • Фосфорилювання та інактивація інгібіторів комплексів циклін A–Cdk 2 та циклін В–Cdk 2. звільнені від інгібуючого впливу комплекси вводять клітину в S-період.
МЕХАНІЗМ ДІЇ КОМПЛЕКСІВ G 1 -ПЕРІОДУ • Фосфорилювання та інактивація АРС (anaphase promoting factor) – убіквітинлігази, яка стимулює швидкий протеоліз цикліну В. Як наслідок, рівень цикліну В продовжує зростати до метафази мітозу. • Фосфорилювання та інактивація інгібіторів комплексів циклін A–Cdk 2 та циклін В–Cdk 2. звільнені від інгібуючого впливу комплекси вводять клітину в S-період.
 МЕХАНІЗМ ДІЇ КОМПЛЕКСІВ S- ТА G 2 -ПЕРІОДІВ (ЦИКЛІН А–CDK 2, ЦИКЛІН B–CDK 1, 2) • контроль одноразової реплікацї ДНК • утворення компонентів MPF (mitosispromoting factor) – цикліну В та Cdk 1 • гальмування активності цього комплексу і запобігання передчасному входу клітини в мітоз
МЕХАНІЗМ ДІЇ КОМПЛЕКСІВ S- ТА G 2 -ПЕРІОДІВ (ЦИКЛІН А–CDK 2, ЦИКЛІН B–CDK 1, 2) • контроль одноразової реплікацї ДНК • утворення компонентів MPF (mitosispromoting factor) – цикліну В та Cdk 1 • гальмування активності цього комплексу і запобігання передчасному входу клітини в мітоз
 ПРОФАЗА ТА МЕТАФАЗА МІТОЗУ: МЕХАНІЗМ ДІЇ MPF (ЦИКЛІН В–CDK 1) • Конденсація хромосом. MPF фосфорилює гістон Н 1 та білки SMS (structural maintanance of chromosomes) з утворенням компактних метафазних хромосом. • Розпад ядерної оболонки. MPF фосфорилює білки ядерної ламіни, що призводить до їх дисоціації, при цьому ядерна мембрана розпадається на дрібні везикули. • Формування веретена поділу. MPF фосфорилює тубулін з утворенням мікротрубочок веретена. • Затримка передчасної цитотомії. MPF фосфорилює легкі ланцюги міозину, що запобігає їх взаємодії з актином і утворенню кільця до того моменту, поки
ПРОФАЗА ТА МЕТАФАЗА МІТОЗУ: МЕХАНІЗМ ДІЇ MPF (ЦИКЛІН В–CDK 1) • Конденсація хромосом. MPF фосфорилює гістон Н 1 та білки SMS (structural maintanance of chromosomes) з утворенням компактних метафазних хромосом. • Розпад ядерної оболонки. MPF фосфорилює білки ядерної ламіни, що призводить до їх дисоціації, при цьому ядерна мембрана розпадається на дрібні везикули. • Формування веретена поділу. MPF фосфорилює тубулін з утворенням мікротрубочок веретена. • Затримка передчасної цитотомії. MPF фосфорилює легкі ланцюги міозину, що запобігає їх взаємодії з актином і утворенню кільця до того моменту, поки
 АНАФАЗА І ТЕЛОФАЗА МІТОЗУ: ДІЯ АРС І ПРОТЕЇНФОСФАТАЗ АРС (убіквітинлігаза, що сприяє швидкому протеолізу ряду білків, в тому числі і MPF) фосфорилюється і активується MPF в метафазі мітозу. • Маркує до протеолізу білки-інгібітори анафази, що входять до складу центромерних комплексів, які утримують сестринські хроматиди від розходження. • Маркує до протеолізу MPF в пізній анафазі. Після цього фосфатази дефосфорилюють білки, що були фосфорильовані MPF в метафазі. Це призводить до відновлення ядерної оболонки, деконденсації
АНАФАЗА І ТЕЛОФАЗА МІТОЗУ: ДІЯ АРС І ПРОТЕЇНФОСФАТАЗ АРС (убіквітинлігаза, що сприяє швидкому протеолізу ряду білків, в тому числі і MPF) фосфорилюється і активується MPF в метафазі мітозу. • Маркує до протеолізу білки-інгібітори анафази, що входять до складу центромерних комплексів, які утримують сестринські хроматиди від розходження. • Маркує до протеолізу MPF в пізній анафазі. Після цього фосфатази дефосфорилюють білки, що були фосфорильовані MPF в метафазі. Це призводить до відновлення ядерної оболонки, деконденсації
 ВИСНОВКИ • Клітинний цикл – складний самопідтримуваний процес, який після запуску регулюється внутрішньоклітинними факторами незалежно від мітогенних стимулів. • Головними факторами, які регулюють перебіг клітинного циклу, є цикліни та циклінзалежні кінази, які в комплексі фосфорилюють певні білки-мішені, активуючи або інактивуючи їх. • Завдяки складній системі позитивних та негативних зворотних зв’язків фази мітозу відбуваються строго послідовно, оскільки ефекторні молекули кожної фази створюють умови для переходу до наступної.
ВИСНОВКИ • Клітинний цикл – складний самопідтримуваний процес, який після запуску регулюється внутрішньоклітинними факторами незалежно від мітогенних стимулів. • Головними факторами, які регулюють перебіг клітинного циклу, є цикліни та циклінзалежні кінази, які в комплексі фосфорилюють певні білки-мішені, активуючи або інактивуючи їх. • Завдяки складній системі позитивних та негативних зворотних зв’язків фази мітозу відбуваються строго послідовно, оскільки ефекторні молекули кожної фази створюють умови для переходу до наступної.
 1 Роль циклінів в регуляції клітинного циклу. 2 Механізми активації та інгібування циклінів. 3 Циклін-залежні кінази та їх роль в регуляції активності циклінів 4 Регуляція синтезу та розпаду активаторів та інгібіторів циклінзалежних кіназ 5 Циклін D в регуляції клітин проліферативного пулу нормальних та трансформованих клітин. 6 Механізми регуляції активності циклінів на різних фазах клітинного циклу. 7 Циклічність активації та інактивації комплексів циклінівциклінзалежних кіназ. 8 Аутокринна регуляція клітинного циклу в нормі та за патологічних станів 9 Рецептори з тирозинкіназною активністю в екзогенній регуляції клітинного циклу. 10 Яку роль відіграють протеїни двох родин – INK 4 (p 15, p 16) та КІР 1 (р21, р27, р57) в регуляції клітинного циклу? 11 За яким механізмом відбувається розпад циклінів? 12 Яку роль в регуляції клітинного циклу відіграє каскад МАРК? 13 Механізми паракринного впливу на клітинний цикл.
1 Роль циклінів в регуляції клітинного циклу. 2 Механізми активації та інгібування циклінів. 3 Циклін-залежні кінази та їх роль в регуляції активності циклінів 4 Регуляція синтезу та розпаду активаторів та інгібіторів циклінзалежних кіназ 5 Циклін D в регуляції клітин проліферативного пулу нормальних та трансформованих клітин. 6 Механізми регуляції активності циклінів на різних фазах клітинного циклу. 7 Циклічність активації та інактивації комплексів циклінівциклінзалежних кіназ. 8 Аутокринна регуляція клітинного циклу в нормі та за патологічних станів 9 Рецептори з тирозинкіназною активністю в екзогенній регуляції клітинного циклу. 10 Яку роль відіграють протеїни двох родин – INK 4 (p 15, p 16) та КІР 1 (р21, р27, р57) в регуляції клітинного циклу? 11 За яким механізмом відбувається розпад циклінів? 12 Яку роль в регуляції клітинного циклу відіграє каскад МАРК? 13 Механізми паракринного впливу на клітинний цикл.


