Элементы химической кинетики Науку, изучающую механизмы химических





















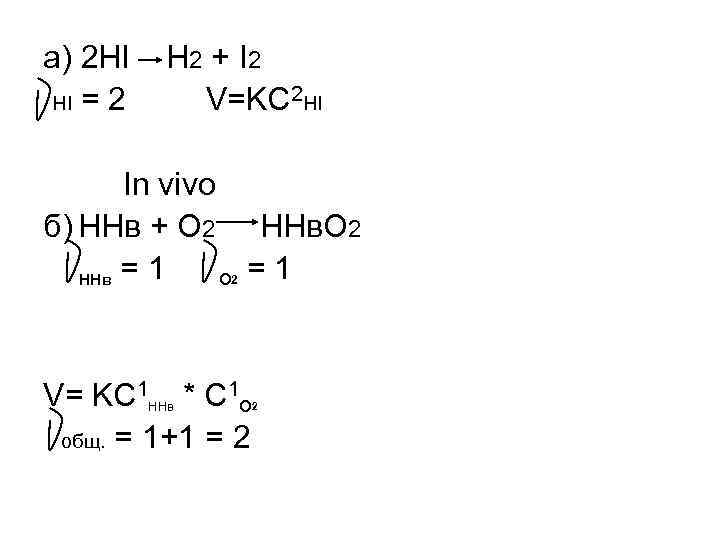





![Еа – называют энергетическим барьером Еа необходима для возникновения переходного комплекса [А---В---С] Комплекс Еа – называют энергетическим барьером Еа необходима для возникновения переходного комплекса [А---В---С] Комплекс](https://present5.com/presentation/3/18788323_135633963.pdf-img/18788323_135633963.pdf-30.jpg)
















Элементы химической кинетики.ppt
- Количество слайдов: 49
 Элементы химической кинетики
Элементы химической кинетики
 Науку, изучающую механизмы химических реакций и скорость их протекания называют кинетикой.
Науку, изучающую механизмы химических реакций и скорость их протекания называют кинетикой.
 Химические процессы совершаются с различной скоростью. In vivo Процесс передачи нервного импульса протекает за сотые доли секунды. Процессы усвоения пищи требует нескольких часов. Процессы старения длятся десятилетиями.
Химические процессы совершаются с различной скоростью. In vivo Процесс передачи нервного импульса протекает за сотые доли секунды. Процессы усвоения пищи требует нескольких часов. Процессы старения длятся десятилетиями.
 Классификация химических реакций 1. По агрегатному состоянию: Гомогенные реакции. Протекают по всему объёму системы. Реагенты находятся в одном агрегатном состоянии. NO 2(г) + O 2(г) 2 NO(г) ННв + O 2 ННв. O 2 В одной клеточной жидкости.
Классификация химических реакций 1. По агрегатному состоянию: Гомогенные реакции. Протекают по всему объёму системы. Реагенты находятся в одном агрегатном состоянии. NO 2(г) + O 2(г) 2 NO(г) ННв + O 2 ННв. O 2 В одной клеточной жидкости.
 Гетерогенные реакции. Протекают на поверхности раздела. Реагенты находятся в разных агрегатных состояниях. Zn(т) + 2 HCl(ж) Zn. Cl 2 + H 2 (Me + к-та) In vivo – реакции на мембранах. (окисление глюкозы).
Гетерогенные реакции. Протекают на поверхности раздела. Реагенты находятся в разных агрегатных состояниях. Zn(т) + 2 HCl(ж) Zn. Cl 2 + H 2 (Me + к-та) In vivo – реакции на мембранах. (окисление глюкозы).
 2. По сложности: Простые реакции (элементарные) (Протекают в одну стадию) O 2 + O O 3 Сложные реакции (Протекают в 2 или более стадий, каждая из которых является простой) Свет СH 4 + Cl 2 CH 3 Cl + HCl
2. По сложности: Простые реакции (элементарные) (Протекают в одну стадию) O 2 + O O 3 Сложные реакции (Протекают в 2 или более стадий, каждая из которых является простой) Свет СH 4 + Cl 2 CH 3 Cl + HCl
 По молекулярности: Молекулярность – число молекул участвующих в элементарной реакции. Мономолекулярные реакции (участвует в реакции одна молекула) A B A B+C + - Na. Cl Na + Cl SO 2 Cl 2 SO 2 + Cl 2
По молекулярности: Молекулярность – число молекул участвующих в элементарной реакции. Мономолекулярные реакции (участвует в реакции одна молекула) A B A B+C + - Na. Cl Na + Cl SO 2 Cl 2 SO 2 + Cl 2
 Бимолекулярные реакции (участвуют 2 молекулы) A + B AB 2 A B H 2 + I 2 2 HI ННв + О 2 ННв. О 2
Бимолекулярные реакции (участвуют 2 молекулы) A + B AB 2 A B H 2 + I 2 2 HI ННв + О 2 ННв. О 2
 Тримолекулярные реакции (участвуют три молекулы) Встречаются редко А + 2 В С 2 NO + O 2 2 NO 2
Тримолекулярные реакции (участвуют три молекулы) Встречаются редко А + 2 В С 2 NO + O 2 2 NO 2
 Скорость химических реакций Определяется изменением концентрации реагирующих веществ или продуктов реакиции в единицу времени. _ + C 2 – C 1 Vср = t 2 – t 1 (моль/л*с) C- молярная концентрация (-) скорость измеряют по реагентам (+) скорость измеряют по продуктам реакции Скорость реакции величина положительная
Скорость химических реакций Определяется изменением концентрации реагирующих веществ или продуктов реакиции в единицу времени. _ + C 2 – C 1 Vср = t 2 – t 1 (моль/л*с) C- молярная концентрация (-) скорость измеряют по реагентам (+) скорость измеряют по продуктам реакции Скорость реакции величина положительная
 Скорость реакции за бесконечно малый промежуток времени называют «истинной» скоростью. + dc _ Vист = dt
Скорость реакции за бесконечно малый промежуток времени называют «истинной» скоростью. + dc _ Vист = dt
 Факторы влияющие на скорость гомогенных реакций 1. Влияние природы реагирующих веществ. Реакция между молекулами протекают медленно H 2 + O 2 H 2 O Между ионами и радикалами быстро. H+ + OH- H 2 O H + Cl HCl
Факторы влияющие на скорость гомогенных реакций 1. Влияние природы реагирующих веществ. Реакция между молекулами протекают медленно H 2 + O 2 H 2 O Между ионами и радикалами быстро. H+ + OH- H 2 O H + Cl HCl
 2. Влияние концентрации реагентов. С, число частиц в объёме, число столкновений реагирующих частиц, Vреакции.
2. Влияние концентрации реагентов. С, число частиц в объёме, число столкновений реагирующих частиц, Vреакции.
 Количественно зависимость V от Среаг. выражается 3 ДМ Скорость простой гомогенной реакции при t=const пропорциональна произведению концентраций реагирующих веществ в степени их стехиометрических коэффициентов. a. A + в. B d. D + c. C а в V = KC (A) C (В) Кинетическое уравнение Где C(A) и C(B) – молярные концентрации реагентов.
Количественно зависимость V от Среаг. выражается 3 ДМ Скорость простой гомогенной реакции при t=const пропорциональна произведению концентраций реагирующих веществ в степени их стехиометрических коэффициентов. a. A + в. B d. D + c. C а в V = KC (A) C (В) Кинетическое уравнение Где C(A) и C(B) – молярные концентрации реагентов.
 K – константа скорости реакции. Константа зависит от: -температуры -природы реагирующих веществ Константа не зависит от: -концентрации реагентов Значение K численно равно Vр-ции, если СА = СВ = 1 моль/л K – определяют экспериментально.
K – константа скорости реакции. Константа зависит от: -температуры -природы реагирующих веществ Константа не зависит от: -концентрации реагентов Значение K численно равно Vр-ции, если СА = СВ = 1 моль/л K – определяют экспериментально.
 а - порядок реакции по реагенту А ( A) в – порядок реакции по реагенту В ( B) а + в = общий порядок реакции Сумма показателей степеней в кинетическом уравнении называется порядком реакции. Для простых реакций показатели порядка по реагентам равны стехиометрическим коэффицентам.
а - порядок реакции по реагенту А ( A) в – порядок реакции по реагенту В ( B) а + в = общий порядок реакции Сумма показателей степеней в кинетическом уравнении называется порядком реакции. Для простых реакций показатели порядка по реагентам равны стехиометрическим коэффицентам.
 Порядок реакции по реагенту определяет зависимость Vр-ции от Среаг. Различают реакции 0 , 1 , 2 – порядка (по реагенту). Общий порядок ( ) может быть равным 3 и 4. Дробный порядок указывает на сложный механизм р-ции.
Порядок реакции по реагенту определяет зависимость Vр-ции от Среаг. Различают реакции 0 , 1 , 2 – порядка (по реагенту). Общий порядок ( ) может быть равным 3 и 4. Дробный порядок указывает на сложный механизм р-ции.
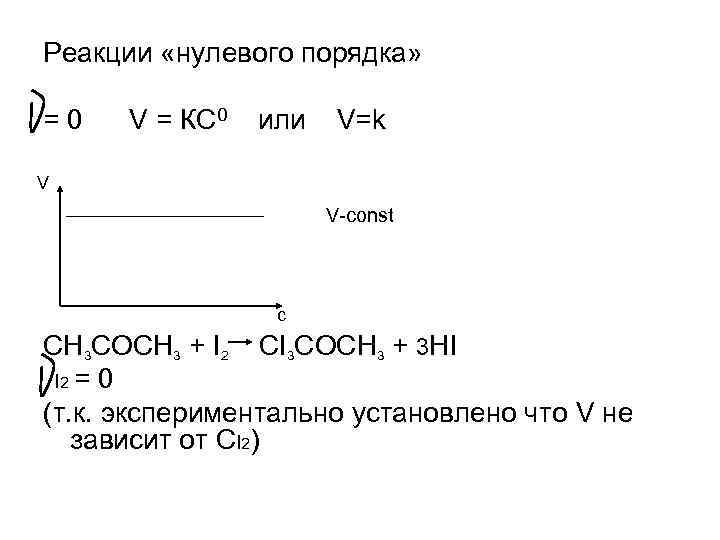
 Реакции «нулевого порядка» =0 V = КС 0 или V=k V V-const с CH 3 CОCH 3 + I 2 CI 3 COCH 3 + 3 HI I 2 = 0 (т. к. экспериментально установлено что V не зависит от CI 2)
Реакции «нулевого порядка» =0 V = КС 0 или V=k V V-const с CH 3 CОCH 3 + I 2 CI 3 COCH 3 + 3 HI I 2 = 0 (т. к. экспериментально установлено что V не зависит от CI 2)
 In vivo Ферментативные реакции, идущие при высокой Сs s=0 кинет. ур-е V=KCs 0
In vivo Ферментативные реакции, идущие при высокой Сs s=0 кинет. ур-е V=KCs 0
 Реакции «первого» порядка =1 V=KC 1 v Зависимость V от С Прямопропор- циональная c C в 2, 4 раза, V в 2, 4 раза
Реакции «первого» порядка =1 V=KC 1 v Зависимость V от С Прямопропор- циональная c C в 2, 4 раза, V в 2, 4 раза
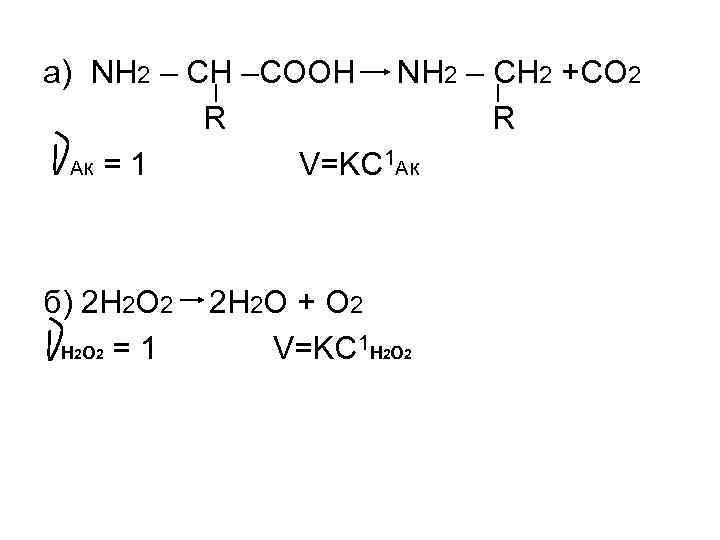
 a) NH 2 – CH –COOH NH 2 – CH 2 +CO 2 R Ак = 1 V=KC 1 Ак б) 2 H 2 O 2 2 H 2 O + O 2 H 2 O 2 = 1 V=KC 1 H 2 O 2
a) NH 2 – CH –COOH NH 2 – CH 2 +CO 2 R Ак = 1 V=KC 1 Ак б) 2 H 2 O 2 2 H 2 O + O 2 H 2 O 2 = 1 V=KC 1 H 2 O 2
 Реакции «второго» порядка =2 V=KC 2 V C Зависимость V от С квадратичная С в 2 раза V в 4 раза
Реакции «второго» порядка =2 V=KC 2 V C Зависимость V от С квадратичная С в 2 раза V в 4 раза
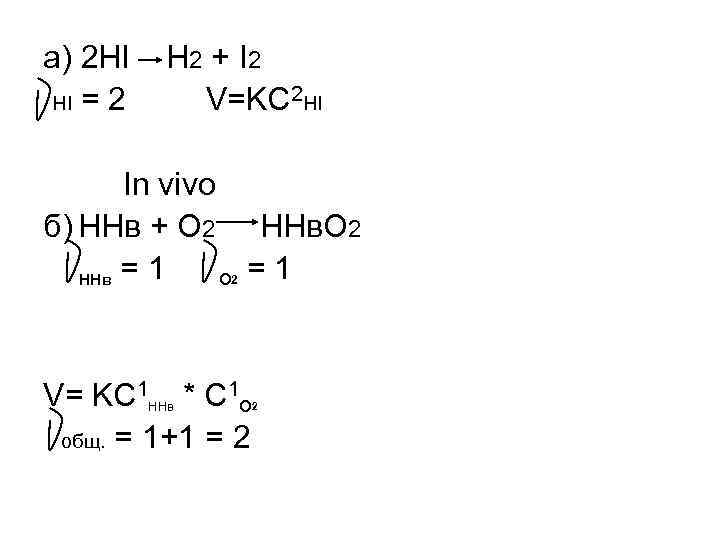 a) 2 HI H 2 + I 2 HI = 2 V=KC 2 HI In vivo б) ННв + О 2 ННв. О 2 ННв = 1 2 О = 1 V= KC 1 ННв * С 1 О 2 общ. = 1+1 = 2
a) 2 HI H 2 + I 2 HI = 2 V=KC 2 HI In vivo б) ННв + О 2 ННв. О 2 ННв = 1 2 О = 1 V= KC 1 ННв * С 1 О 2 общ. = 1+1 = 2
 Vр-ции и (порядок реакции) для сложных реакций определяют по самой медленной (лимитирующей) стадии. 2 N 2 O 5 4 NO +O 2 1. N 2 O 5 N 2 O 3 + O 2 (медл) 2. N 2 O 5 + N 2 O 3 4 NO 2 (быстро) V= KC 1 N 2 O 5 =1 общ. =1
Vр-ции и (порядок реакции) для сложных реакций определяют по самой медленной (лимитирующей) стадии. 2 N 2 O 5 4 NO +O 2 1. N 2 O 5 N 2 O 3 + O 2 (медл) 2. N 2 O 5 + N 2 O 3 4 NO 2 (быстро) V= KC 1 N 2 O 5 =1 общ. =1
 Порядок реакции определяют экспериментально по: С реагентов К (константе скорости реакции) t ½ (времени полупревращения) Промежуток времени, в течении которого начальная концентрация реагента в 2 раза, т. е. на ½ , называется временем полупревращения. (полупериодом) Если =1 t ½ = 0. 69 / k =2 t ½ = 1 / C 0 K
Порядок реакции определяют экспериментально по: С реагентов К (константе скорости реакции) t ½ (времени полупревращения) Промежуток времени, в течении которого начальная концентрация реагента в 2 раза, т. е. на ½ , называется временем полупревращения. (полупериодом) Если =1 t ½ = 0. 69 / k =2 t ½ = 1 / C 0 K
 Влияние температуры При t V, К Правило Вант – Гоффа: При T на каждые 10 К скорость химических реакций увеличивается в 2 -4 раза T 2 - T 1 V 2 = V 1 · 10 T 2 – T 1 K 2 = K 1 · 10
Влияние температуры При t V, К Правило Вант – Гоффа: При T на каждые 10 К скорость химических реакций увеличивается в 2 -4 раза T 2 - T 1 V 2 = V 1 · 10 T 2 – T 1 K 2 = K 1 · 10
 где - температурный коэффициент показывает во сколько раз увеличивается Vр-ции при t на каждые 10 к ; V 1; V 2 – скорости реакций при температуре T 1 и Т 2 = 2 – 4 для химических реакций = 7 – 9 для ферментативных реакций Tтела человека даже на 1 С сильно сказывается на его самочувствии.
где - температурный коэффициент показывает во сколько раз увеличивается Vр-ции при t на каждые 10 к ; V 1; V 2 – скорости реакций при температуре T 1 и Т 2 = 2 – 4 для химических реакций = 7 – 9 для ферментативных реакций Tтела человека даже на 1 С сильно сказывается на его самочувствии.
 Влияние T на V объясняет теория переходного комплекса: - к химическому взаимодействию приводят только столкновения частиц, обладающих Е, необходимой для данного взаимодействия (Еа) - при соударении частицы должны быть определённым образом сориентированы.
Влияние T на V объясняет теория переходного комплекса: - к химическому взаимодействию приводят только столкновения частиц, обладающих Е, необходимой для данного взаимодействия (Еа) - при соударении частицы должны быть определённым образом сориентированы.
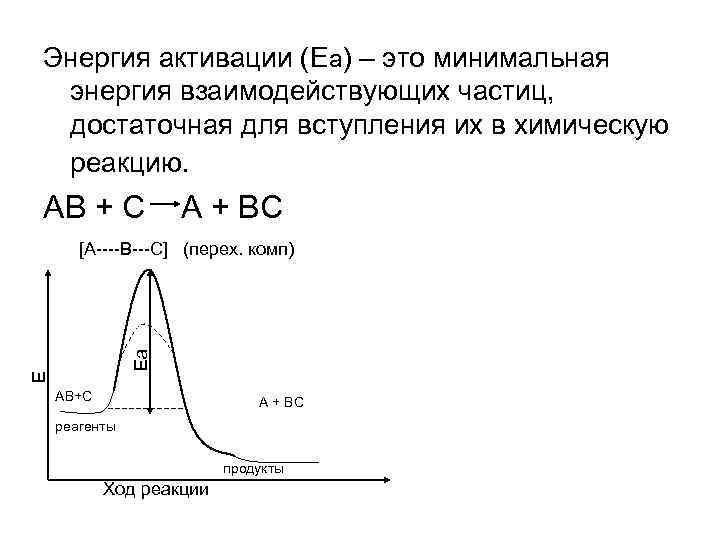
 Энергия активации (Еа) – это минимальная энергия взаимодействующих частиц, достаточная для вступления их в химическую реакцию. AB + C A + BC [A----B---C] (перех. комп) Еа Е АВ+С А + ВС реагенты продукты Ход реакции
Энергия активации (Еа) – это минимальная энергия взаимодействующих частиц, достаточная для вступления их в химическую реакцию. AB + C A + BC [A----B---C] (перех. комп) Еа Е АВ+С А + ВС реагенты продукты Ход реакции
![>Еа – называют энергетическим барьером Еа необходима для возникновения переходного комплекса [А---В---С] Комплекс >Еа – называют энергетическим барьером Еа необходима для возникновения переходного комплекса [А---В---С] Комплекс](https://present5.com/presentation/3/18788323_135633963.pdf-img/18788323_135633963.pdf-30.jpg) Еа – называют энергетическим барьером Еа необходима для возникновения переходного комплекса [А---В---С] Комплекс неустойчив вследствие высокой Еа и быстро распадается, образуя продукты реакции. Источники активации: -t - излучение - действия быстрых частиц (ядерный распад)
Еа – называют энергетическим барьером Еа необходима для возникновения переходного комплекса [А---В---С] Комплекс неустойчив вследствие высокой Еа и быстро распадается, образуя продукты реакции. Источники активации: -t - излучение - действия быстрых частиц (ядерный распад)
 Еа связана с К уравнением Аррениуса : К = A * e –Ea/RT где К – константа скорости реакции А – коэффициент Аррениуса (учитывает число столкновений частиц) Еа – энергия активации е – основание натурального логарифма R = 8. 31 дж/моль * к - универсальная газовая постоянная Чем Еа тем V, K.
Еа связана с К уравнением Аррениуса : К = A * e –Ea/RT где К – константа скорости реакции А – коэффициент Аррениуса (учитывает число столкновений частиц) Еа – энергия активации е – основание натурального логарифма R = 8. 31 дж/моль * к - универсальная газовая постоянная Чем Еа тем V, K.
 Значение Ea рассчитывают по уравнению: T 1*T 2 КТ 2 Ea = 2. 3 R T 2 -T 1 lg КТ 1 Еа (х. реак. ) 40 – 200 к. Дж/моль Высокое значение Еа делает невозможным многие реакции N 2 + O 2 + H 2 O HNO 3 78% 21% воздух Все живые ткани бы погибли.
Значение Ea рассчитывают по уравнению: T 1*T 2 КТ 2 Ea = 2. 3 R T 2 -T 1 lg КТ 1 Еа (х. реак. ) 40 – 200 к. Дж/моль Высокое значение Еа делает невозможным многие реакции N 2 + O 2 + H 2 O HNO 3 78% 21% воздух Все живые ткани бы погибли.
 Влияние катализатора Вещества, которые ускоряют хим. реакции, активно участвуют в них, но сами в итоге не расходуются называются катализаторами. (Pt, Ni, Mn. O 2, Al. Cl 3) Катализатор: -изменяет механизм реакции -создает др. путь реакции с Еа -способствует ориентации частиц - ∆S (переходн. процесса)
Влияние катализатора Вещества, которые ускоряют хим. реакции, активно участвуют в них, но сами в итоге не расходуются называются катализаторами. (Pt, Ni, Mn. O 2, Al. Cl 3) Катализатор: -изменяет механизм реакции -создает др. путь реакции с Еа -способствует ориентации частиц - ∆S (переходн. процесса)
 Катализ- явление ускорения хим. реакций в присутствии катализатора. (+) катализ - V (-) катализ-V (ингибирование) Гетерогенный катализ kt и реакционная смесь в разных фазах (kt – твёрдый , реакция протекает на его поверхности) Vзависит Sповерхность катализатора Mn. O 2 H 2 O 2 2 H 2 O + O 2
Катализ- явление ускорения хим. реакций в присутствии катализатора. (+) катализ - V (-) катализ-V (ингибирование) Гетерогенный катализ kt и реакционная смесь в разных фазах (kt – твёрдый , реакция протекает на его поверхности) Vзависит Sповерхность катализатора Mn. O 2 H 2 O 2 2 H 2 O + O 2
 Гомогенный катализ kt и реакционная смесь в одной фазе H 2 O 2 Cu 2 H 2 O + O 2 2+ Механизм гомогенного катализа Кат A+B C Еа. I 1) A + Кат [А * Кат] Еа. II 2) [А * Кат] + В С + Кат
Гомогенный катализ kt и реакционная смесь в одной фазе H 2 O 2 Cu 2 H 2 O + O 2 2+ Механизм гомогенного катализа Кат A+B C Еа. I 1) A + Кат [А * Кат] Еа. II 2) [А * Кат] + В С + Кат
 Ферментативный катализ Катализаторы – ферменты (энзимы) каталаза H 2 O 2 Ф 2 H 2 O + O 2 Большинство реакций in vivo идут в присутствии биокатализаторов. (10 тыс. реакций катализируют 2 тыс. ферм. )
Ферментативный катализ Катализаторы – ферменты (энзимы) каталаза H 2 O 2 Ф 2 H 2 O + O 2 Большинство реакций in vivo идут в присутствии биокатализаторов. (10 тыс. реакций катализируют 2 тыс. ферм. )
 Отличие ферментов от химических kt 1. сложное строение апофермент (белок) ф кофермент (небелковая часть) + + (витамины, гормоны НАД, ФАД )
Отличие ферментов от химических kt 1. сложное строение апофермент (белок) ф кофермент (небелковая часть) + + (витамины, гормоны НАД, ФАД )
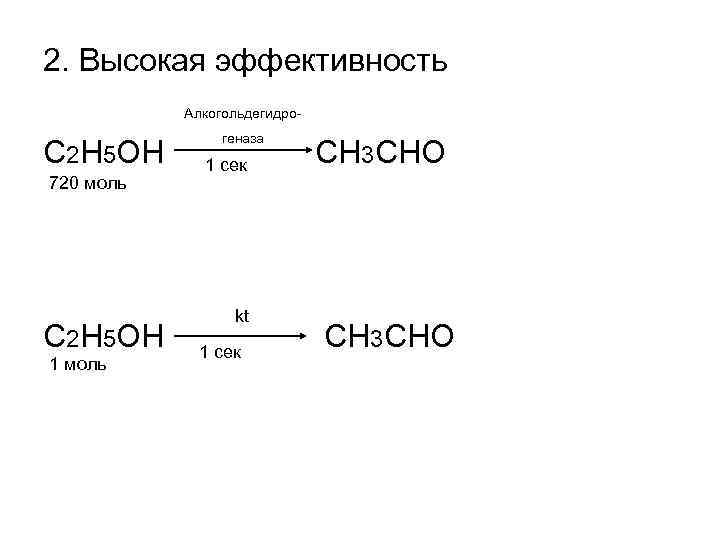
 2. Высокая эффективность Алкогольдегидро- геназа С 2 H 5 OH 1 сек CH 3 CHO 720 моль kt C 2 H 5 OH 1 сек CH 3 CHO 1 моль
2. Высокая эффективность Алкогольдегидро- геназа С 2 H 5 OH 1 сек CH 3 CHO 720 моль kt C 2 H 5 OH 1 сек CH 3 CHO 1 моль
 3. Высокая специфичность- способность изменять V одной или нескольких реакций и не влиять на многие др. , протекающие в клетке. Амилаза (фермент слюны)- катализирует гидролиз крахмала. Карбоангидраза – обратимую гидратацию. CO 2 + H 2 O H 2 CO 3
3. Высокая специфичность- способность изменять V одной или нескольких реакций и не влиять на многие др. , протекающие в клетке. Амилаза (фермент слюны)- катализирует гидролиз крахмала. Карбоангидраза – обратимую гидратацию. CO 2 + H 2 O H 2 CO 3
 4. Высокая молекулярная активность – число молекул субстрата, претерпевающих превращение под действием 1 молекулы ф, в течении 1 мин. Карбоангидраза – 32 млн. оборотов Каталаза - 5 млн. оборотов
4. Высокая молекулярная активность – число молекул субстрата, претерпевающих превращение под действием 1 молекулы ф, в течении 1 мин. Карбоангидраза – 32 млн. оборотов Каталаза - 5 млн. оборотов
 Активность ф проявляется при определённом значении p. H. Аргиназа 10 – 10. 2 р. Н Пепсин 1 – 2 р. Н В узком интервале t (10 – 60) Наивысшая активность 36 – 40 С При t < 10 С – сгущение крови, кристаллизация. При t > 60 C денатурация белка 5. Инактивация фермента (хим. кt практически не изменяет активность)
Активность ф проявляется при определённом значении p. H. Аргиназа 10 – 10. 2 р. Н Пепсин 1 – 2 р. Н В узком интервале t (10 – 60) Наивысшая активность 36 – 40 С При t < 10 С – сгущение крови, кристаллизация. При t > 60 C денатурация белка 5. Инактивация фермента (хим. кt практически не изменяет активность)
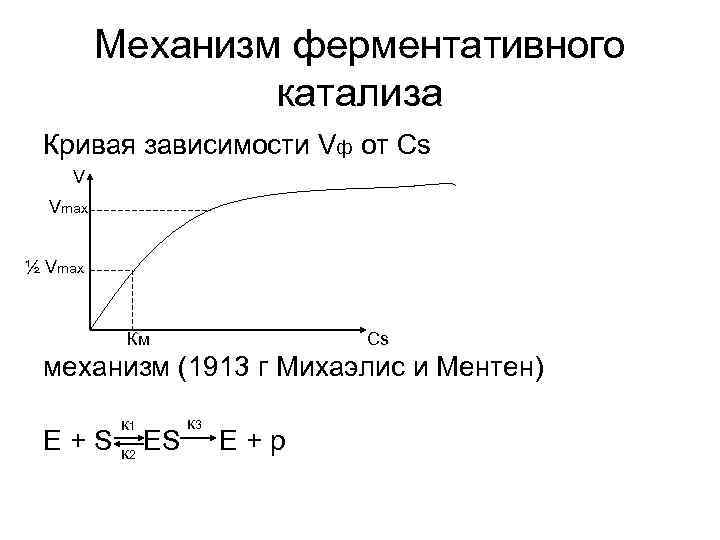
 Механизм ферментативного катализа Кривая зависимости Vф от Cs V Vmax ½ Vmax Км Cs механизм (1913 г Михаэлис и Ментен) к 1 к 3 E+S к 2 ES E+р
Механизм ферментативного катализа Кривая зависимости Vф от Cs V Vmax ½ Vmax Км Cs механизм (1913 г Михаэлис и Ментен) к 1 к 3 E+S к 2 ES E+р
 Формула для расчёта скорости Vф = Vmax * Cs KM + Cs где Cs – концентрация субстрата KM - константа Михаэлиса KM = Cs, если V = ½ Vmax зависит от t, p. H, от природы S
Формула для расчёта скорости Vф = Vmax * Cs KM + Cs где Cs – концентрация субстрата KM - константа Михаэлиса KM = Cs, если V = ½ Vmax зависит от t, p. H, от природы S
 При низких Cs: Cs << KM Vф = Vmax * Cs KM Vф II Cs (прямопропорц. ) s=1 На кривой - это начальный участок. Прямая с tg угла наклона V/Км
При низких Cs: Cs << KM Vф = Vmax * Cs KM Vф II Cs (прямопропорц. ) s=1 На кривой - это начальный участок. Прямая с tg угла наклона V/Км
 При высоких Cs: Сs>> KM Vф = Vmax (V не зависит от Cs) s=0 на графике – прямая параллельная оси х.
При высоких Cs: Сs>> KM Vф = Vmax (V не зависит от Cs) s=0 на графике – прямая параллельная оси х.
 Фармакокинетика Изучает скорость действия и выведения из организма лекарств. Путь лекарства в организме: желудок 1 кровь 2 моча тж Кв тк Ке тм 1 ст. Всасывание лекарства из желудка в кровь 2 ст. Выведение лекарства из крови в мочу
Фармакокинетика Изучает скорость действия и выведения из организма лекарств. Путь лекарства в организме: желудок 1 кровь 2 моча тж Кв тк Ке тм 1 ст. Всасывание лекарства из желудка в кровь 2 ст. Выведение лекарства из крови в мочу
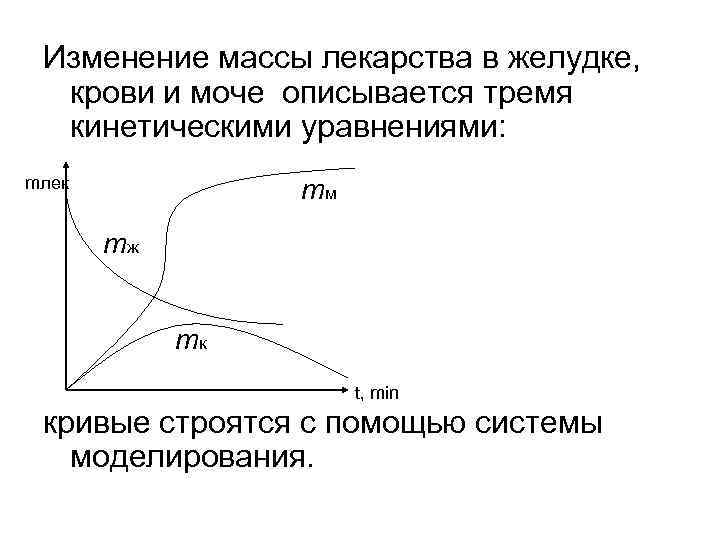
 Изменение массы лекарства в желудке, крови и моче описывается тремя кинетическими уравнениями: mлек тм тж тк t, min кривые строятся с помощью системы моделирования.
Изменение массы лекарства в желудке, крови и моче описывается тремя кинетическими уравнениями: mлек тм тж тк t, min кривые строятся с помощью системы моделирования.
 Простой моделью организма является сосуд, Cсосуда = Vжидк. орг. + Vлекар. ≈ 7, 5 л V выведения лекарства выражают кинетическим уравнением первого порядка ( =1) dт V= dt = - Keт (вместо концентрации используют массу) Ke – константа элиминирования
Простой моделью организма является сосуд, Cсосуда = Vжидк. орг. + Vлекар. ≈ 7, 5 л V выведения лекарства выражают кинетическим уравнением первого порядка ( =1) dт V= dt = - Keт (вместо концентрации используют массу) Ke – константа элиминирования
 Решая это уравнение определяют Ke и полупериод выведения лекарства t ½ = 0. 69 / Ke ( =1) зная полупериод, устанавливают дозировку и интервал приема лекарств t ½ (пенициллин) = 1, 5 час прием через 3 часа t ½ (сульфалена) = 80 час. прием 1 раз в неделю
Решая это уравнение определяют Ke и полупериод выведения лекарства t ½ = 0. 69 / Ke ( =1) зная полупериод, устанавливают дозировку и интервал приема лекарств t ½ (пенициллин) = 1, 5 час прием через 3 часа t ½ (сульфалена) = 80 час. прием 1 раз в неделю

