Элементы подгруппы титана.ppt
- Количество слайдов: 18
 Элементы подгруппы титана Ti Zr Hf
Элементы подгруппы титана Ti Zr Hf
 Открытие • • • Цирконий был открыт в 1789 г. , титан — в 1791 г. Открытие гафния последовало лишь в 1923 г. До 1795 г. элемент № 22 назывался «менакином» . Так назвал его в 1791 г. английский химик и минералог Уильям Грегор, открывший новый элемент в минерале менаканите (не ищите это название в современных минералогических справочниках – менаканит тоже переименован, сейчас он называется ильменитом). Спустя четыре года после открытия Грегора немецкий химик Мартин Клапрот обнаружил новый химический элемент в другом минерале – рутиле – и в честь царицы эльфов Титании (германская мифология) назвал его титаном. Венгерский химик Д. Хевеши и голландский физик Д. Костер систематически исследовали минералы циркония методом рентгеноспектрального анализа и в 1922 обнаружили элемент № 72, назвав его Г. по месту открытия — городу Копенгагену (позднелат. hafnia). Дьёрдь (Георг) Хевеши - венгерский химик, почётный академик Венгерской АН, лауреат Нобелевской премии по химии (1943 г. ) Мартин-Генрих Клапрот немецкий химик, член Берлинской Академии наук (с 1788 г. ), иностранный почетный член Петербургской АН (с 1805 г. ). Открыл уран и цирконий (1789 г. ), титан (1795 г. ). Независимо от И. Я. Берцелиуса и шведского химика В. Г. Хизингера открыл церий (1803 г. ).
Открытие • • • Цирконий был открыт в 1789 г. , титан — в 1791 г. Открытие гафния последовало лишь в 1923 г. До 1795 г. элемент № 22 назывался «менакином» . Так назвал его в 1791 г. английский химик и минералог Уильям Грегор, открывший новый элемент в минерале менаканите (не ищите это название в современных минералогических справочниках – менаканит тоже переименован, сейчас он называется ильменитом). Спустя четыре года после открытия Грегора немецкий химик Мартин Клапрот обнаружил новый химический элемент в другом минерале – рутиле – и в честь царицы эльфов Титании (германская мифология) назвал его титаном. Венгерский химик Д. Хевеши и голландский физик Д. Костер систематически исследовали минералы циркония методом рентгеноспектрального анализа и в 1922 обнаружили элемент № 72, назвав его Г. по месту открытия — городу Копенгагену (позднелат. hafnia). Дьёрдь (Георг) Хевеши - венгерский химик, почётный академик Венгерской АН, лауреат Нобелевской премии по химии (1943 г. ) Мартин-Генрих Клапрот немецкий химик, член Берлинской Академии наук (с 1788 г. ), иностранный почетный член Петербургской АН (с 1805 г. ). Открыл уран и цирконий (1789 г. ), титан (1795 г. ). Независимо от И. Я. Берцелиуса и шведского химика В. Г. Хизингера открыл церий (1803 г. ).
 По другой версии название элемента происходит от титанов, могучих сыновей богини земли – Геи (греческая мифология).
По другой версии название элемента происходит от титанов, могучих сыновей богини земли – Геи (греческая мифология).
 Нахождение в природе • На долю титана приходится около 0, 2% от общего числа атомов земной коры, т. е. он является одним из весьма распространенных в природе элементов. Доля циркония составляет 3 · 10– 3% и гафния – 5 · 10– 5%. • Хотя содержание в земной коре даже гафния больше, чем, например, иода или ртути, однако и титан и его аналоги ещё сравнительно плохо освоены практикой и иногда трактуются как “редкие” элементы. Обусловлено это их распылённостью, вследствие чего пригодные для промышленной разработки месторождения встречаются лишь в немногих местах земного шара. Другой важной причиной является трудность выделения рассматриваемых элементов из их природных соединений. • Титан встречается в минералах ильменит (Fe. Ti. O 3) и рутил (Ti. O 2). Значительные количества титана содержат также некоторые железные руды, в частности уральские титаномагнетиты. Цирконий встречается главным образом в виде минералов цирконила (Zr. Si. O 4) и бадделеита (Zr. O 2). Для гафния отдельные минералы пока не найдены. В виде примеси (порядка 1 атом. %) он всегда содержится в рудах Zr. • Ничтожные количества титана постоянно содержатся в организмах растений и животных, но его биологическая роль не ясна. Титан и его аналоги не токсичны.
Нахождение в природе • На долю титана приходится около 0, 2% от общего числа атомов земной коры, т. е. он является одним из весьма распространенных в природе элементов. Доля циркония составляет 3 · 10– 3% и гафния – 5 · 10– 5%. • Хотя содержание в земной коре даже гафния больше, чем, например, иода или ртути, однако и титан и его аналоги ещё сравнительно плохо освоены практикой и иногда трактуются как “редкие” элементы. Обусловлено это их распылённостью, вследствие чего пригодные для промышленной разработки месторождения встречаются лишь в немногих местах земного шара. Другой важной причиной является трудность выделения рассматриваемых элементов из их природных соединений. • Титан встречается в минералах ильменит (Fe. Ti. O 3) и рутил (Ti. O 2). Значительные количества титана содержат также некоторые железные руды, в частности уральские титаномагнетиты. Цирконий встречается главным образом в виде минералов цирконила (Zr. Si. O 4) и бадделеита (Zr. O 2). Для гафния отдельные минералы пока не найдены. В виде примеси (порядка 1 атом. %) он всегда содержится в рудах Zr. • Ничтожные количества титана постоянно содержатся в организмах растений и животных, но его биологическая роль не ясна. Титан и его аналоги не токсичны.
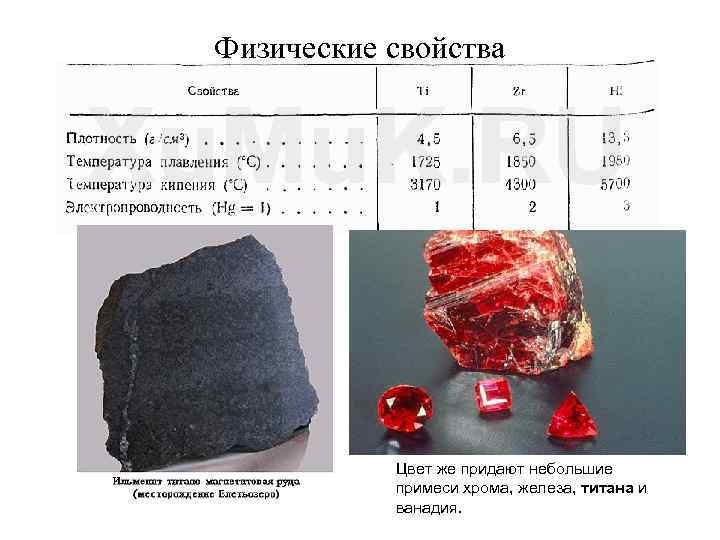 Физические свойства Цвет же придают небольшие примеси хрома, железа, титана и ванадия.
Физические свойства Цвет же придают небольшие примеси хрома, железа, титана и ванадия.
 Получение Ti Металлы подгруппы Ti получают: • металлотермическим восстановлением тетрахлоридов MCl 4 или гексафторосолей в вакууме или атмосфере инертного газа (Ar, He) • термической диссоциацией тетраиодидов • электролизом расплавленных в смеси с KCl солей K 2[MF 6]. Очистка сырого металла осуществляется по методу Ван-Аркела и де Бура, заключающейся в термической диссоциации MI 4, полученного действием паров I 2 на сырой металл. Fe. Ti. O 3 (концентрат ильменита) + H 2 SO 4, конц. → Ti. OSO 4 + Fe. SO 4 + H 2 O При выпаривании в вакууме из раствора выпадает Fe. SO 4· 7 H 2 O. При дальнейшем кипячении раствора Ti. OSO 4 и последующем разбавлении выпадает осадок H 2 Ti. O 3, который при прокаливании дает двуокись титана: Ti. OSO 4 + 2 H 2 O → H 2 Ti. O 3 + H 2 SO 4 H 2 Ti. O 3 →→ Ti. O 2 + H 2 O. Очистку двуокиси проводят по схеме: Ti. O 2 + C + 2 Cl 2 = Ti. Cl 4 + CO 2 Ti. Cl 4 + Mg (Na, Na. H) →→ Ti + Mg. Cl 2 (Na. Cl, HCl) – в вакууме или атмосфере H 2.
Получение Ti Металлы подгруппы Ti получают: • металлотермическим восстановлением тетрахлоридов MCl 4 или гексафторосолей в вакууме или атмосфере инертного газа (Ar, He) • термической диссоциацией тетраиодидов • электролизом расплавленных в смеси с KCl солей K 2[MF 6]. Очистка сырого металла осуществляется по методу Ван-Аркела и де Бура, заключающейся в термической диссоциации MI 4, полученного действием паров I 2 на сырой металл. Fe. Ti. O 3 (концентрат ильменита) + H 2 SO 4, конц. → Ti. OSO 4 + Fe. SO 4 + H 2 O При выпаривании в вакууме из раствора выпадает Fe. SO 4· 7 H 2 O. При дальнейшем кипячении раствора Ti. OSO 4 и последующем разбавлении выпадает осадок H 2 Ti. O 3, который при прокаливании дает двуокись титана: Ti. OSO 4 + 2 H 2 O → H 2 Ti. O 3 + H 2 SO 4 H 2 Ti. O 3 →→ Ti. O 2 + H 2 O. Очистку двуокиси проводят по схеме: Ti. O 2 + C + 2 Cl 2 = Ti. Cl 4 + CO 2 Ti. Cl 4 + Mg (Na, Na. H) →→ Ti + Mg. Cl 2 (Na. Cl, HCl) – в вакууме или атмосфере H 2.
 Получение Zr • Zr (Zr. O 2) получают методом сплавления концентрата циркона с Na. OH Zr. Si. O 4 + 4 Na. OH → Na 2 Zr. O 3 + Na 2 Si. O 3 + H 2 O Плав растворяют в горяч. воде, при этом в осадок выпадает гидратированная двуокись Zr, очистка которой проводится путем растворения в соляной кислоте с последующим осаждением аммиаком Na 2 Zr. O 3 →→ Zr. O 2·n. H 2 O↓ →→Zr. OCl 2 →→ Zr. O 2·n. H 2 O↓ • Спеканием циркона с K 2[Si. F 6] получают смесь гексафторосолей Zr и Hf Zr. Si. O 4 + K 2[Si. F 6] = K 2[Zr. F 6] + 2 Si. O 2 Hf. Si. O 4 + K 2[Si. F 6] = K 2[Hf. F 6] + 2 Si. O 2 которую разделяют методом дробной кристаллизации. Действием аммиака на K 2[Zr. F 6] получают Zr. O 2·n. H 2 O, которую затем прокаливают. Другой способ получения металлич. Zr состоит в электролизе расплава (K 2[Zr. F 6] + KCl) в атмосфере аргона (800ºС).
Получение Zr • Zr (Zr. O 2) получают методом сплавления концентрата циркона с Na. OH Zr. Si. O 4 + 4 Na. OH → Na 2 Zr. O 3 + Na 2 Si. O 3 + H 2 O Плав растворяют в горяч. воде, при этом в осадок выпадает гидратированная двуокись Zr, очистка которой проводится путем растворения в соляной кислоте с последующим осаждением аммиаком Na 2 Zr. O 3 →→ Zr. O 2·n. H 2 O↓ →→Zr. OCl 2 →→ Zr. O 2·n. H 2 O↓ • Спеканием циркона с K 2[Si. F 6] получают смесь гексафторосолей Zr и Hf Zr. Si. O 4 + K 2[Si. F 6] = K 2[Zr. F 6] + 2 Si. O 2 Hf. Si. O 4 + K 2[Si. F 6] = K 2[Hf. F 6] + 2 Si. O 2 которую разделяют методом дробной кристаллизации. Действием аммиака на K 2[Zr. F 6] получают Zr. O 2·n. H 2 O, которую затем прокаливают. Другой способ получения металлич. Zr состоит в электролизе расплава (K 2[Zr. F 6] + KCl) в атмосфере аргона (800ºС).
 Химические свойства Ti • С химической т. з. металлы подгруппы Ti не активны, устойчивы на воздухе или в воде при н. у. При повышенной tº становятся очень активными по отношению к O 2, Hal 2, S, N 2, C, B: M + O 2, Hal 2, S, N 2, C, B = MO 2, MHal 4, MN, MC, MB 2 • Металлический Ti разлагает воду при кипячении Ti + 4 H 2 O → H 4 Ti. O 4 + 2 H 2 • Ti растворяется в царской водке, расплавах щелочей и конц. HF, HCl, H 2 SO 4 Ti + HNO 3 + HCl = H 2[Ti. Cl 6] + NO + H 2 O Ti + HCl = Ti. Cl 3 +H 2 Ti + H 2 SO 4, разб. = Ti 2(SO 4)3 + H 2 Ti + H 2 SO 4, конц. = Ti(SO 4)2 или Ti. OSO 4+ SO 2 + H 2 O • При действии конц. HNO 3 Ti превращается в метатитановую кислоту H 2 Ti. O 3·H 2 O↓ Ti + HNO 3, конц. = H 2 Ti. O 3 + NO • По отношению к большинству агрессивных сред Ti проявляет коррозионную устойчивость.
Химические свойства Ti • С химической т. з. металлы подгруппы Ti не активны, устойчивы на воздухе или в воде при н. у. При повышенной tº становятся очень активными по отношению к O 2, Hal 2, S, N 2, C, B: M + O 2, Hal 2, S, N 2, C, B = MO 2, MHal 4, MN, MC, MB 2 • Металлический Ti разлагает воду при кипячении Ti + 4 H 2 O → H 4 Ti. O 4 + 2 H 2 • Ti растворяется в царской водке, расплавах щелочей и конц. HF, HCl, H 2 SO 4 Ti + HNO 3 + HCl = H 2[Ti. Cl 6] + NO + H 2 O Ti + HCl = Ti. Cl 3 +H 2 Ti + H 2 SO 4, разб. = Ti 2(SO 4)3 + H 2 Ti + H 2 SO 4, конц. = Ti(SO 4)2 или Ti. OSO 4+ SO 2 + H 2 O • При действии конц. HNO 3 Ti превращается в метатитановую кислоту H 2 Ti. O 3·H 2 O↓ Ti + HNO 3, конц. = H 2 Ti. O 3 + NO • По отношению к большинству агрессивных сред Ti проявляет коррозионную устойчивость.
 Химические свойства Zr и Hf • Металлические Zr и Hf не взаимодействуют с H 2 O, хлорной водой, разб. кислотами, конц. HCl и HNO 3. Они растворяются только в расплавах щелочей, KHF 2 и царской водке M + 4 Na. OH → Na 4 MO 4 + 2 H 2 M + 4 KHF = K 2[MF 6] + 2 KF + 2 H 2 M + HNO 3 + HCl = H 2[MCl 6] + NO + H 2 O или MCl 4
Химические свойства Zr и Hf • Металлические Zr и Hf не взаимодействуют с H 2 O, хлорной водой, разб. кислотами, конц. HCl и HNO 3. Они растворяются только в расплавах щелочей, KHF 2 и царской водке M + 4 Na. OH → Na 4 MO 4 + 2 H 2 M + 4 KHF = K 2[MF 6] + 2 KF + 2 H 2 M + HNO 3 + HCl = H 2[MCl 6] + NO + H 2 O или MCl 4
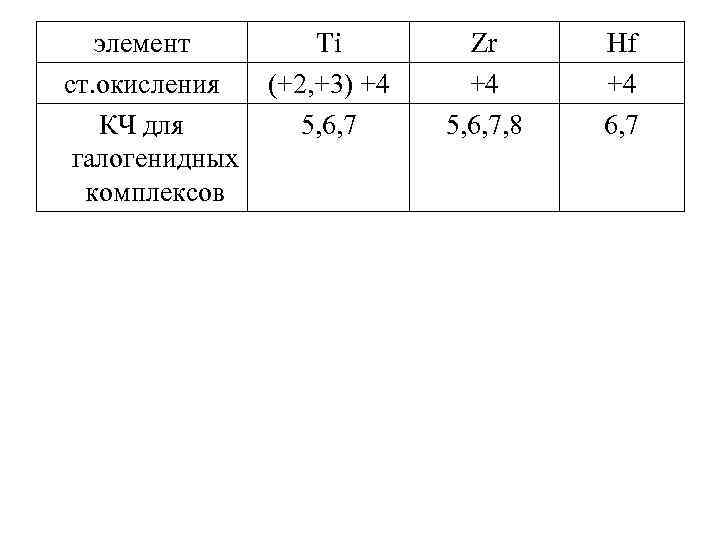 элемент Ti ст. окисления (+2, +3) +4 КЧ для 5, 6, 7 галогенидных комплексов Zr +4 5, 6, 7, 8 Hf +4 6, 7
элемент Ti ст. окисления (+2, +3) +4 КЧ для 5, 6, 7 галогенидных комплексов Zr +4 5, 6, 7, 8 Hf +4 6, 7
 • При сжигании металлов подгруппы Ti в кислороде или прокаливании соединений H 4 MO 4 (M(OH)4) образуются устойчивые, тугоплавкие, плохо растворимые в воде и разб. кислотах и щелочах двуокиси MO 2. M →→→ MO 2 ←←← H 4 MO 4 • Двуокиси MO 2 растворяются при нагревании в конц. H 2 SO 4 и в расплавленных щелочах. Сплавлением MO 2 со щелочами получают соли составов Na 2 MO 3 и Na 4 MO 4, которые, переходя в раствор, полностью гидролизуются: Na 4 Zr. O 4 + 4 H 2 O = Zr(OH)4 + 4 Na. OH • Ti. O 2 обладает слабо кислыми свойствами, а Zr. O 2 и Hf. O 2 – слабо основными. В ряду H 4 Ti. O 4 - Zr(OH)4 - Hf(OH)4 , которые представляют собой белые гелевидные осадки MO 2· 2 H 2 O, плохо растворимые в воде, отмечается уменьшение кислотных и усиление основных свойств, а также появляется способность растворяться в сильных кислотах.
• При сжигании металлов подгруппы Ti в кислороде или прокаливании соединений H 4 MO 4 (M(OH)4) образуются устойчивые, тугоплавкие, плохо растворимые в воде и разб. кислотах и щелочах двуокиси MO 2. M →→→ MO 2 ←←← H 4 MO 4 • Двуокиси MO 2 растворяются при нагревании в конц. H 2 SO 4 и в расплавленных щелочах. Сплавлением MO 2 со щелочами получают соли составов Na 2 MO 3 и Na 4 MO 4, которые, переходя в раствор, полностью гидролизуются: Na 4 Zr. O 4 + 4 H 2 O = Zr(OH)4 + 4 Na. OH • Ti. O 2 обладает слабо кислыми свойствами, а Zr. O 2 и Hf. O 2 – слабо основными. В ряду H 4 Ti. O 4 - Zr(OH)4 - Hf(OH)4 , которые представляют собой белые гелевидные осадки MO 2· 2 H 2 O, плохо растворимые в воде, отмечается уменьшение кислотных и усиление основных свойств, а также появляется способность растворяться в сильных кислотах.
 • Тетрагалогениды MHal 4, растворяясь в воде, гидролизуются. Действием теплой воды на тетрафториды MF 4 получают кислоты состава H 2[MOF 4] Ti. F 4 + H 2 O = H 2[Ti. OF 4] • При гидролизе растворимых солей Ti, Zr и Hf образуются соли титанила Ti. O 2+, цирконила Zr. O 2+ и гафнила Hf. O 2+, а при более глубоком гидролизе солей Ti - H 4 Ti. O 4(H 2 Ti. O 3·H 2 O). Действием H 2 O 2 на соединения M(IV) в присутствии щелочей получают пероксосоединения. При действии на соли титанила перекиси водорода (в кислой или нейтр. средах) образуется монопероксоортотитановая кислота желтого(оранжевого) цвета Ti. OSO 4 + H 2 O 2 + H 2 O = H 4 Ti. O 5 + H 2 SO 4
• Тетрагалогениды MHal 4, растворяясь в воде, гидролизуются. Действием теплой воды на тетрафториды MF 4 получают кислоты состава H 2[MOF 4] Ti. F 4 + H 2 O = H 2[Ti. OF 4] • При гидролизе растворимых солей Ti, Zr и Hf образуются соли титанила Ti. O 2+, цирконила Zr. O 2+ и гафнила Hf. O 2+, а при более глубоком гидролизе солей Ti - H 4 Ti. O 4(H 2 Ti. O 3·H 2 O). Действием H 2 O 2 на соединения M(IV) в присутствии щелочей получают пероксосоединения. При действии на соли титанила перекиси водорода (в кислой или нейтр. средах) образуется монопероксоортотитановая кислота желтого(оранжевого) цвета Ti. OSO 4 + H 2 O 2 + H 2 O = H 4 Ti. O 5 + H 2 SO 4
 Соединения Ti(II, III) • Хлориды Ti(II) и Ti(III) получают восстановлением Ti. Cl 4 водородом при повышенной tº Ti. Cl 4 + H 2 →→ Ti. Cl 3 →→ Ti. Cl 2 • Растворением металлического Ti в конц. HCl или восстановлением Ti. Cl 4 атомарным водородом (Zn + HCl) получают фиолетовый раствор, из которого выделяют кристаллогидрат Ti. Cl 3· 6 H 2 O. Соединения Ti(III) являются более сильными восстановителями, чем соли Sn(II), поэтому водные растворы Ti. Cl 3 хранят в атмосфере H 2 или CO 2, защищая от действия O 2 Ti. Cl 3 + H 2 O = Ti. O 2 + HCl + H 2 Ti. Cl 3 + O 2 + H 2 O = Ti. OCl 2 + HCl • Соединения Ti(III) восстанавливают соли Au(III), Hg(II), Fe(III), Cu(II): Ti. Cl 3 + Au. Cl 3(Hg. Cl 2, Fe. Cl 3, Cu. Cl 2) = Ti. Cl 4 + Au(Hg 2 Cl 2, Fe. Cl 2, Cu. Cl) • Ti. Cl 3 + KMn. O 4 + H 2 SO 4 = Ti. OCl 2 + Mn. SO 4 + K 2 SO 4 + H 2 O • При повышенной tº Ti. Cl 3 диспропорционирует на хлориды Ti(II) и Ti(IV): 2 Ti. Cl 3 →→ Ti. Cl 2 + Ti. Cl 4
Соединения Ti(II, III) • Хлориды Ti(II) и Ti(III) получают восстановлением Ti. Cl 4 водородом при повышенной tº Ti. Cl 4 + H 2 →→ Ti. Cl 3 →→ Ti. Cl 2 • Растворением металлического Ti в конц. HCl или восстановлением Ti. Cl 4 атомарным водородом (Zn + HCl) получают фиолетовый раствор, из которого выделяют кристаллогидрат Ti. Cl 3· 6 H 2 O. Соединения Ti(III) являются более сильными восстановителями, чем соли Sn(II), поэтому водные растворы Ti. Cl 3 хранят в атмосфере H 2 или CO 2, защищая от действия O 2 Ti. Cl 3 + H 2 O = Ti. O 2 + HCl + H 2 Ti. Cl 3 + O 2 + H 2 O = Ti. OCl 2 + HCl • Соединения Ti(III) восстанавливают соли Au(III), Hg(II), Fe(III), Cu(II): Ti. Cl 3 + Au. Cl 3(Hg. Cl 2, Fe. Cl 3, Cu. Cl 2) = Ti. Cl 4 + Au(Hg 2 Cl 2, Fe. Cl 2, Cu. Cl) • Ti. Cl 3 + KMn. O 4 + H 2 SO 4 = Ti. OCl 2 + Mn. SO 4 + K 2 SO 4 + H 2 O • При повышенной tº Ti. Cl 3 диспропорционирует на хлориды Ti(II) и Ti(IV): 2 Ti. Cl 3 →→ Ti. Cl 2 + Ti. Cl 4
 Применение Ti, Zr, Hf • • Практическое значение Ti и Zr особенно велико для металлургии специальных сталей. Оба металла используются и в качестве самостоятельных конструктивных материалов. Их соединения находят применение в различных отраслях промышленности. Гафний и его соединения пока почти не используются. Добавка к стали уже 0, 1% титана придаёт ей твёрдость и эластичность, что делает такую сталь очень хорошим материалом для изготовления рельсов, вагонных осей и колёс и т. д. Введением в сталь уже 0, 1% Zr сильно повышает её твёрдость и вязкость, что особенно ценно для изготовления броневых плит и щитов. Как Тi, так и Zr нередко вводят также в различные сплавы Сu и Al. Как конструкционный материал титан имеет очень благоприятное отношение прочности к массе в сочетании с высокой термической и коррозионной стойкостью. Он используется в самолетостроении. Цирконий (освобожденный от примеси гафния) является одним из важнейших конструкционных материалов при сооружении атомных реакторов. Гафний находит использование главным образом в электронной технике (катоды телевизионных трубок и др. ) и ядерной энергетике (как поглотитель нейтронов).
Применение Ti, Zr, Hf • • Практическое значение Ti и Zr особенно велико для металлургии специальных сталей. Оба металла используются и в качестве самостоятельных конструктивных материалов. Их соединения находят применение в различных отраслях промышленности. Гафний и его соединения пока почти не используются. Добавка к стали уже 0, 1% титана придаёт ей твёрдость и эластичность, что делает такую сталь очень хорошим материалом для изготовления рельсов, вагонных осей и колёс и т. д. Введением в сталь уже 0, 1% Zr сильно повышает её твёрдость и вязкость, что особенно ценно для изготовления броневых плит и щитов. Как Тi, так и Zr нередко вводят также в различные сплавы Сu и Al. Как конструкционный материал титан имеет очень благоприятное отношение прочности к массе в сочетании с высокой термической и коррозионной стойкостью. Он используется в самолетостроении. Цирконий (освобожденный от примеси гафния) является одним из важнейших конструкционных материалов при сооружении атомных реакторов. Гафний находит использование главным образом в электронной технике (катоды телевизионных трубок и др. ) и ядерной энергетике (как поглотитель нейтронов).






