Lect_2_.PPT
- Количество слайдов: 47
 Элементы кристаллохимии. Для описания атомного строения кристалла в кристаллохимии прибегают к приему разбиения полной картины на отдельные фрагменты. Наибольшую роль при таком разбиении структуры придают непосредственному, ближайшему координационному окружению каждой из атомных частиц. Этот подход использует два основных понятия - координационный координационное число. полиэдр и 1
Элементы кристаллохимии. Для описания атомного строения кристалла в кристаллохимии прибегают к приему разбиения полной картины на отдельные фрагменты. Наибольшую роль при таком разбиении структуры придают непосредственному, ближайшему координационному окружению каждой из атомных частиц. Этот подход использует два основных понятия - координационный координационное число. полиэдр и 1
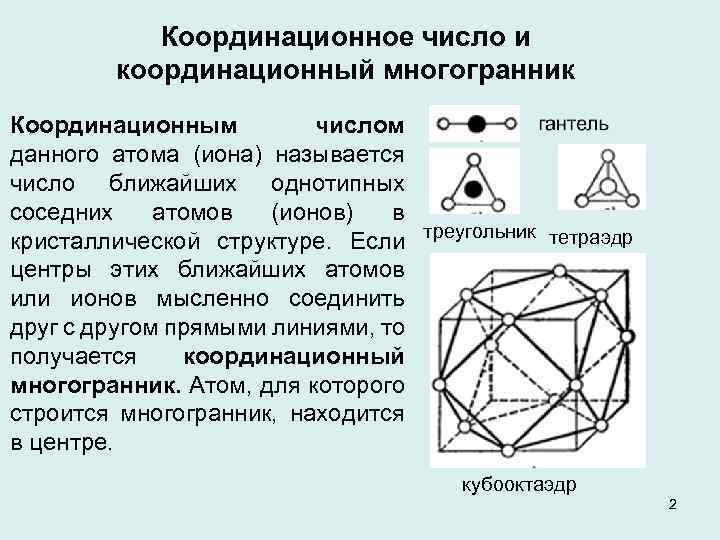 Координационное число и координационный многогранник Координационным числом данного атома (иона) называется число ближайших однотипных соседних атомов (ионов) в кристаллической структуре. Если треугольник тетраэдр центры этих ближайших атомов или ионов мысленно соединить друг с другом прямыми линиями, то получается координационный многогранник. Атом, для которого строится многогранник, находится в центре. кубооктаэдр 2
Координационное число и координационный многогранник Координационным числом данного атома (иона) называется число ближайших однотипных соседних атомов (ионов) в кристаллической структуре. Если треугольник тетраэдр центры этих ближайших атомов или ионов мысленно соединить друг с другом прямыми линиями, то получается координационный многогранник. Атом, для которого строится многогранник, находится в центре. кубооктаэдр 2
 Кристаллографические направления и плоскости в кристаллической решетке Кристаллографические направления - характерные прямые линии, выходящие из точки отсчета, вдоль которых в кристаллической решетке располагаются атомы. Точками отсчета, могут служить вершины куба, а кристаллографическими направлениями - его ребра и диагонали, а также диагонали граней. Для определения индекса какого-либо направления необходимо найти индекс ближайшего к данной точке отсчета атома, находящегося на данном направлении. Например, индекс ближайшего атома вдоль оси ОХ обозначается цифрами 100. . 3
Кристаллографические направления и плоскости в кристаллической решетке Кристаллографические направления - характерные прямые линии, выходящие из точки отсчета, вдоль которых в кристаллической решетке располагаются атомы. Точками отсчета, могут служить вершины куба, а кристаллографическими направлениями - его ребра и диагонали, а также диагонали граней. Для определения индекса какого-либо направления необходимо найти индекс ближайшего к данной точке отсчета атома, находящегося на данном направлении. Например, индекс ближайшего атома вдоль оси ОХ обозначается цифрами 100. . 3
![Индексы направления ОХ и параллельных ему направлений обозначаются [100]. Эти цифры представляют собой координаты Индексы направления ОХ и параллельных ему направлений обозначаются [100]. Эти цифры представляют собой координаты](https://present5.com/presentation/1015967_132154887/image-4.jpg) Индексы направления ОХ и параллельных ему направлений обозначаются [100]. Эти цифры представляют собой координаты атома относительно точки О, выраженные через количество параметров ячейки вдоль осей OX, OY и OZ. Направления OY и OZ обозначаются [010] и [001]. Кристаллографические направления вдоль диагоналей граней XOZ, XOY и YOZ обозначают [101], [110] и [011]. Индекс направления вдоль диагонали куба - [111]. 4
Индексы направления ОХ и параллельных ему направлений обозначаются [100]. Эти цифры представляют собой координаты атома относительно точки О, выраженные через количество параметров ячейки вдоль осей OX, OY и OZ. Направления OY и OZ обозначаются [010] и [001]. Кристаллографические направления вдоль диагоналей граней XOZ, XOY и YOZ обозначают [101], [110] и [011]. Индекс направления вдоль диагонали куба - [111]. 4
 Кристаллографическими плоскостями являются, например, плоскости граней кубов, а также их различные диагональные плоскости вместе с находящимися на них атомами. Для ГПУ-решеток кристаллографическими плоскостями могут быть плоскости оснований. Индексы кристаллографической плоскости выражаются через параметры решетки, например (001), (010) и (100) и записываются в отличие от индексов направлений в круглых скобках. 5
Кристаллографическими плоскостями являются, например, плоскости граней кубов, а также их различные диагональные плоскости вместе с находящимися на них атомами. Для ГПУ-решеток кристаллографическими плоскостями могут быть плоскости оснований. Индексы кристаллографической плоскости выражаются через параметры решетки, например (001), (010) и (100) и записываются в отличие от индексов направлений в круглых скобках. 5
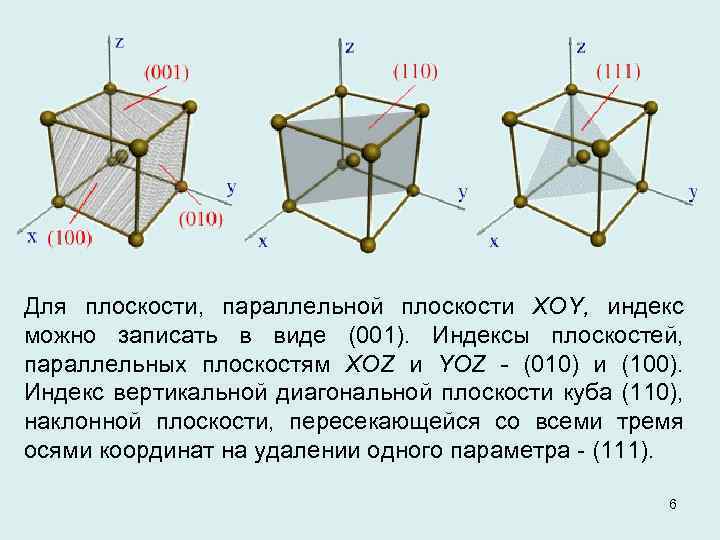 Для плоскости, параллельной плоскости XOY, индекс можно записать в виде (001). Индексы плоскостей, параллельных плоскостям XOZ и YOZ - (010) и (100). Индекс вертикальной диагональной плоскости куба (110), наклонной плоскости, пересекающейся со всеми тремя осями координат на удалении одного параметра - (111). 6
Для плоскости, параллельной плоскости XOY, индекс можно записать в виде (001). Индексы плоскостей, параллельных плоскостям XOZ и YOZ - (010) и (100). Индекс вертикальной диагональной плоскости куба (110), наклонной плоскости, пересекающейся со всеми тремя осями координат на удалении одного параметра - (111). 6
 Плотнейшие упаковки Минимум потенциальной энергии кристаллической структуры является условием ее устойчивости. Одним из факторов, уменьшающих потенциальную энергию, является максимальное сближение структурных единиц, их плотнейшая упаковка. Тенденция к осуществлению плотнейшей упаковки свойственна всем типам кристаллических структур, но сильнее всего она выражена в металлических и ионных структурах, где связи не направлены, атомы или ионы можно считать сферическими. Шары касаются друга, заполняя большую часть пространства. Между ними имеются промежутки (пустоты), в которых могут размещаться меньшие шары других сортов. Значение координационного числа должно быть максимальным. 7
Плотнейшие упаковки Минимум потенциальной энергии кристаллической структуры является условием ее устойчивости. Одним из факторов, уменьшающих потенциальную энергию, является максимальное сближение структурных единиц, их плотнейшая упаковка. Тенденция к осуществлению плотнейшей упаковки свойственна всем типам кристаллических структур, но сильнее всего она выражена в металлических и ионных структурах, где связи не направлены, атомы или ионы можно считать сферическими. Шары касаются друга, заполняя большую часть пространства. Между ними имеются промежутки (пустоты), в которых могут размещаться меньшие шары других сортов. Значение координационного числа должно быть максимальным. 7
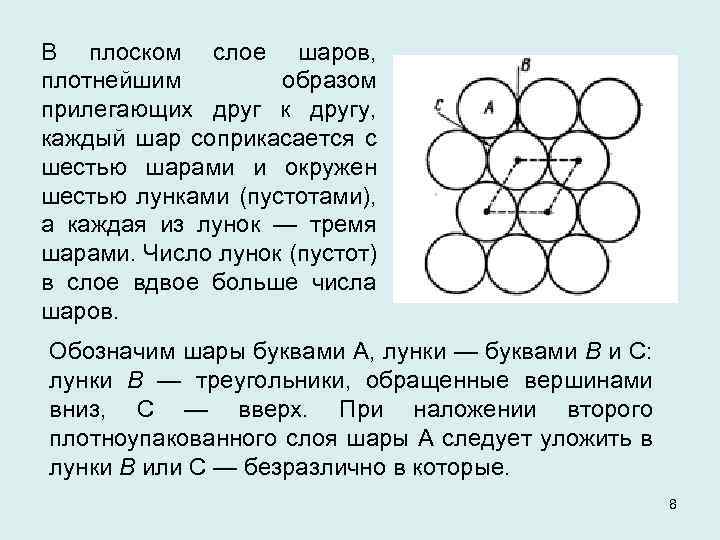 В плоском слое шаров, плотнейшим образом прилегающих друг к другу, каждый шар соприкасается с шестью шарами и окружен шестью лунками (пустотами), а каждая из лунок — тремя шарами. Число лунок (пустот) в слое вдвое больше числа шаров. Обозначим шары буквами А, лунки — буквами В и С: лунки В — треугольники, обращенные вершинами вниз, С — вверх. При наложении второго плотноупакованного слоя шары А следует уложить в лунки В или С — безразлично в которые. 8
В плоском слое шаров, плотнейшим образом прилегающих друг к другу, каждый шар соприкасается с шестью шарами и окружен шестью лунками (пустотами), а каждая из лунок — тремя шарами. Число лунок (пустот) в слое вдвое больше числа шаров. Обозначим шары буквами А, лунки — буквами В и С: лунки В — треугольники, обращенные вершинами вниз, С — вверх. При наложении второго плотноупакованного слоя шары А следует уложить в лунки В или С — безразлично в которые. 8
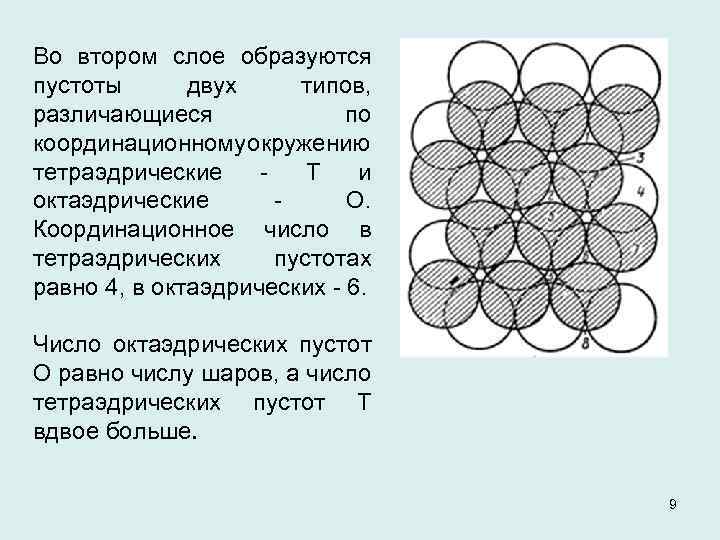 Во втором слое образуются пустоты двух типов, различающиеся по координационному кружению о тетраэдрические - Т и октаэдрические - О. Координационное число в тетраэдрических пустотах равно 4, в октаэдрических - 6. Число октаэдрических пустот О равно числу шаров, а число тетраэдрических пустот Т вдвое больше. 9
Во втором слое образуются пустоты двух типов, различающиеся по координационному кружению о тетраэдрические - Т и октаэдрические - О. Координационное число в тетраэдрических пустотах равно 4, в октаэдрических - 6. Число октаэдрических пустот О равно числу шаров, а число тетраэдрических пустот Т вдвое больше. 9
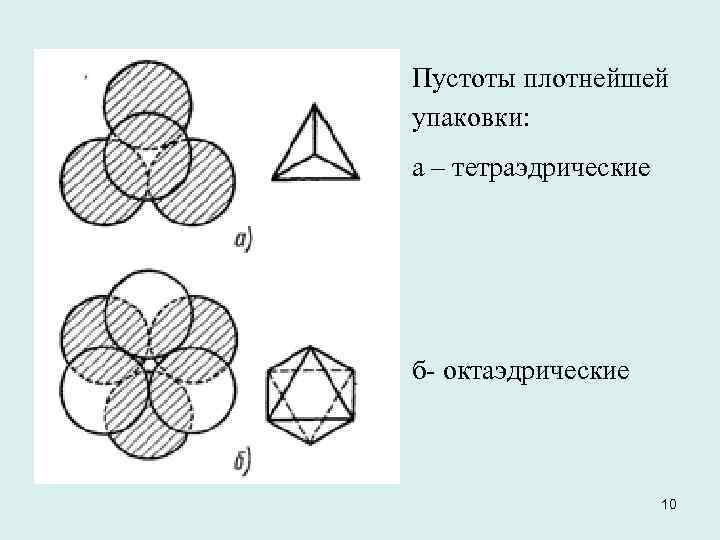 Пустоты плотнейшей упаковки: а – тетраэдрические б- октаэдрические 10
Пустоты плотнейшей упаковки: а – тетраэдрические б- октаэдрические 10
 Шары третьего слоя можно укладывать двояким путем: - в лунки Т, каждый шар слоя III находится над шаром слоя I. Третий слой повторяет укладку первого, получаем упаковку. . . АВАВАВ. . . ; - в лунки О, слой III не повторяет слоя I, получаем упаковку. . . АВСАВС. . Слои можно укладывать, получая любое чередование Однако плотнейшими упаковками оказываются только две: двухслойная . . . АВАВАВ. . . и трехслойная . . . АВСАВСАВС. . В обеих этих упаковках коэффициент компактности К=74, 05%, т. е. шары занимают около 3/4 объема. В ионных соединениях, как правило, анионы образуют плотнейшую упаковку, а катионы размещаются в пустотах. 11
Шары третьего слоя можно укладывать двояким путем: - в лунки Т, каждый шар слоя III находится над шаром слоя I. Третий слой повторяет укладку первого, получаем упаковку. . . АВАВАВ. . . ; - в лунки О, слой III не повторяет слоя I, получаем упаковку. . . АВСАВС. . Слои можно укладывать, получая любое чередование Однако плотнейшими упаковками оказываются только две: двухслойная . . . АВАВАВ. . . и трехслойная . . . АВСАВСАВС. . В обеих этих упаковках коэффициент компактности К=74, 05%, т. е. шары занимают около 3/4 объема. В ионных соединениях, как правило, анионы образуют плотнейшую упаковку, а катионы размещаются в пустотах. 11
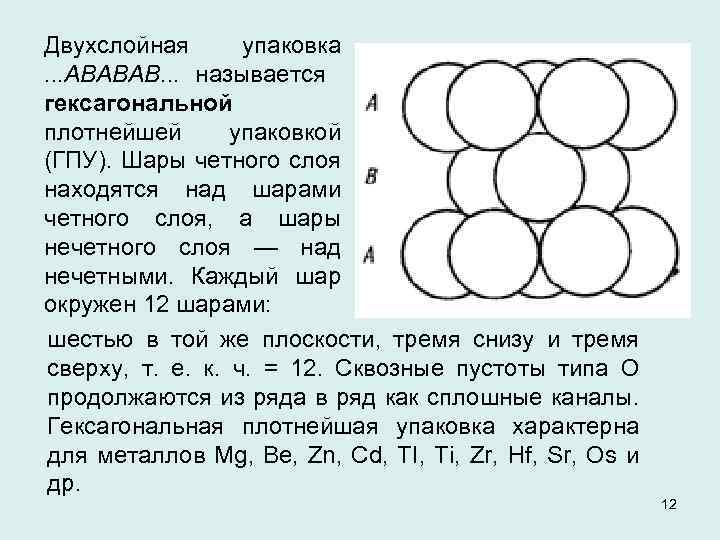 Двухслойная упаковка . . . АВАВАВ. . . называется гексагональной плотнейшей упаковкой (ГПУ). Шары четного слоя находятся над шарами четного слоя, а шары нечетного слоя — над нечетными. Каждый шар окружен 12 шарами: шестью в той же плоскости, тремя снизу и тремя сверху, т. е. к. ч. = 12. Сквозные пустоты типа О продолжаются из ряда в ряд как сплошные каналы. Гексагональная плотнейшая упаковка характерна для металлов Mg, Be, Zn, Cd, TI, Ti, Zr, Hf, Sr, Os и др. 12
Двухслойная упаковка . . . АВАВАВ. . . называется гексагональной плотнейшей упаковкой (ГПУ). Шары четного слоя находятся над шарами четного слоя, а шары нечетного слоя — над нечетными. Каждый шар окружен 12 шарами: шестью в той же плоскости, тремя снизу и тремя сверху, т. е. к. ч. = 12. Сквозные пустоты типа О продолжаются из ряда в ряд как сплошные каналы. Гексагональная плотнейшая упаковка характерна для металлов Mg, Be, Zn, Cd, TI, Ti, Zr, Hf, Sr, Os и др. 12
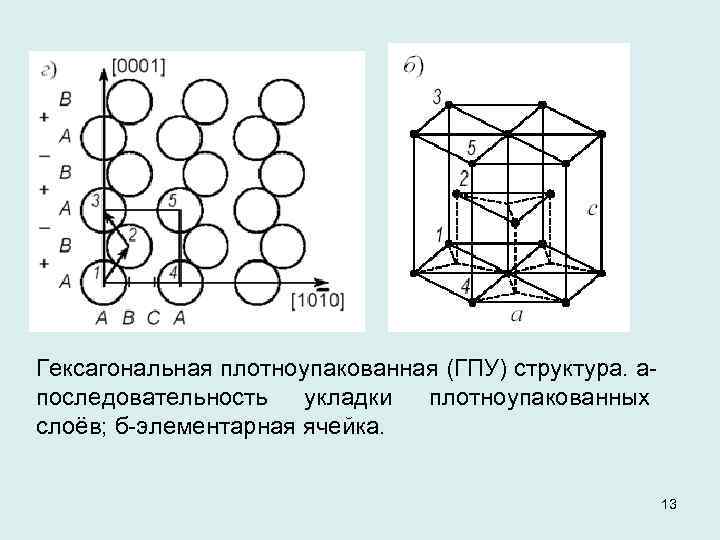 Гексагональная плотноупакованная (ГПУ) структура. апоследовательность укладки плотноупакованных слоёв; б-элементарная ячейка. 13
Гексагональная плотноупакованная (ГПУ) структура. апоследовательность укладки плотноупакованных слоёв; б-элементарная ячейка. 13
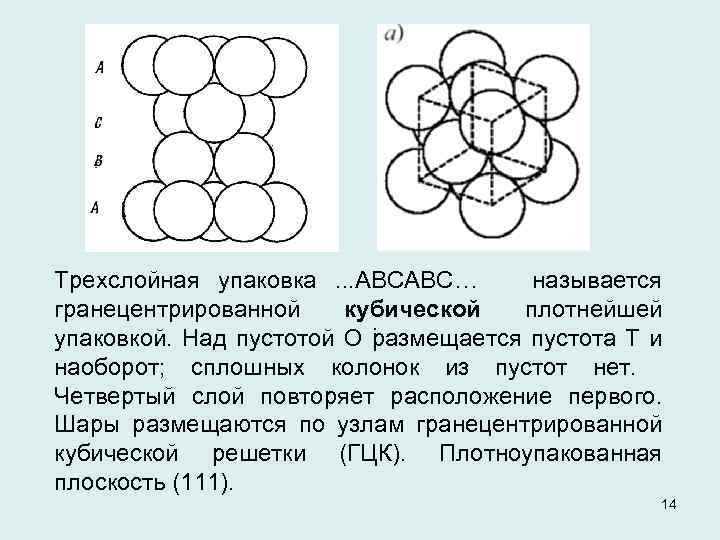 Трехслойная упаковка . . . АВСАВС… называется гранецентрированной кубической плотнейшей . упаковкой. Над пустотой О размещается пустота Т и наоборот; сплошных колонок из пустот нет. Четвертый слой повторяет расположение первого. Шары размещаются по узлам гранецентрированной кубической решетки (ГЦК). Плотноупакованная плоскость (111). 14
Трехслойная упаковка . . . АВСАВС… называется гранецентрированной кубической плотнейшей . упаковкой. Над пустотой О размещается пустота Т и наоборот; сплошных колонок из пустот нет. Четвертый слой повторяет расположение первого. Шары размещаются по узлам гранецентрированной кубической решетки (ГЦК). Плотноупакованная плоскость (111). 14
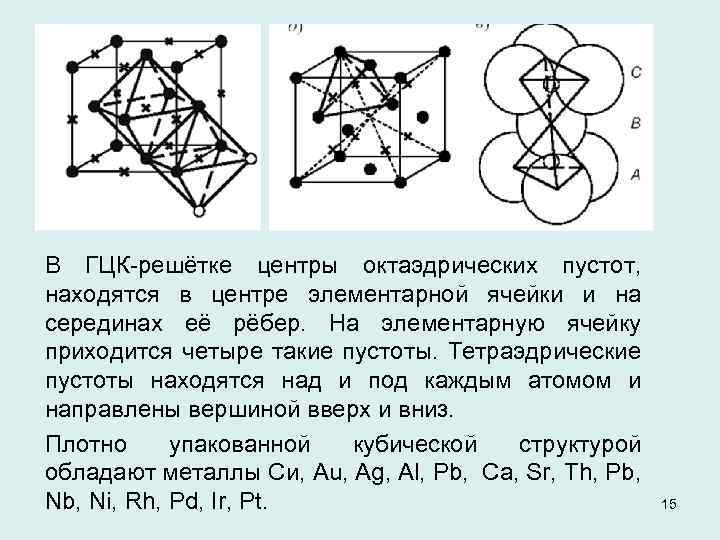 В ГЦК-решётке центры октаэдрических пустот, находятся в центре элементарной ячейки и на серединах её рёбер. На элементарную ячейку приходится четыре такие пустоты. Тетраэдрические пустоты находятся над и под каждым атомом и направлены вершиной вверх и вниз. Плотно упакованной кубической структурой обладают металлы Си, Аu, Ag, Al, Pb, Са, Sr, Th, Pb, Nb, Ni, Rh, Pd, Ir, Pt. 15
В ГЦК-решётке центры октаэдрических пустот, находятся в центре элементарной ячейки и на серединах её рёбер. На элементарную ячейку приходится четыре такие пустоты. Тетраэдрические пустоты находятся над и под каждым атомом и направлены вершиной вверх и вниз. Плотно упакованной кубической структурой обладают металлы Си, Аu, Ag, Al, Pb, Са, Sr, Th, Pb, Nb, Ni, Rh, Pd, Ir, Pt. 15
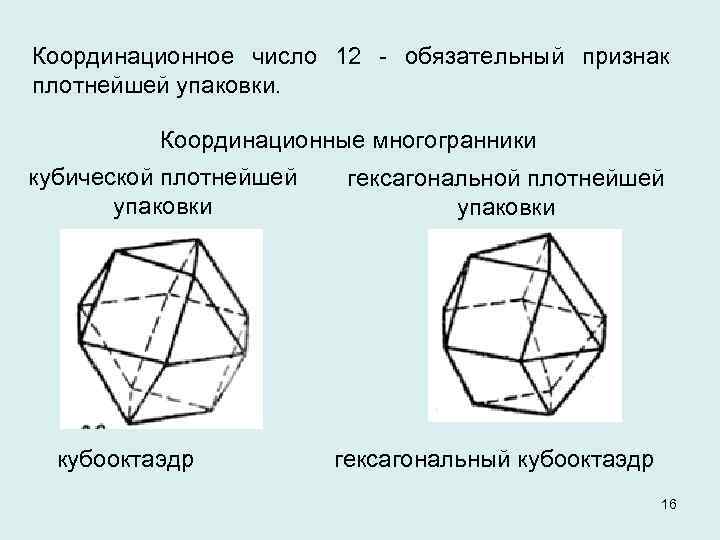 Координационное число 12 - обязательный признак плотнейшей упаковки. Координационные многогранники кубической плотнейшей упаковки гексагональной плотнейшей упаковки кубооктаэдр гексагональный кубооктаэдр 16
Координационное число 12 - обязательный признак плотнейшей упаковки. Координационные многогранники кубической плотнейшей упаковки гексагональной плотнейшей упаковки кубооктаэдр гексагональный кубооктаэдр 16
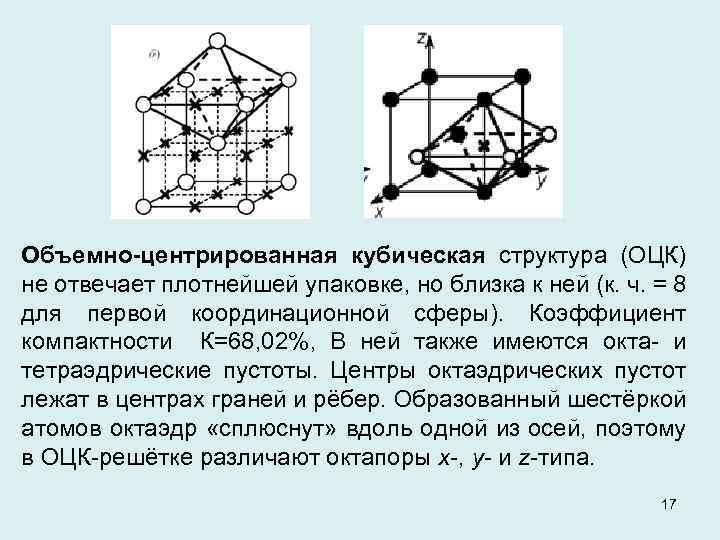 Объемно-центрированная кубическая структура (ОЦК) не отвечает плотнейшей упаковке, но близка к ней (к. ч. = 8 для первой координационной сферы). Коэффициент компактности К=68, 02%, В ней также имеются окта- и тетраэдрические пустоты. Центры октаэдрических пустот лежат в центрах граней и рёбер. Образованный шестёркой атомов октаэдр «сплюснут» вдоль одной из осей, поэтому в ОЦК-решётке различают октапоры x-, y- и z-типа. 17
Объемно-центрированная кубическая структура (ОЦК) не отвечает плотнейшей упаковке, но близка к ней (к. ч. = 8 для первой координационной сферы). Коэффициент компактности К=68, 02%, В ней также имеются окта- и тетраэдрические пустоты. Центры октаэдрических пустот лежат в центрах граней и рёбер. Образованный шестёркой атомов октаэдр «сплюснут» вдоль одной из осей, поэтому в ОЦК-решётке различают октапоры x-, y- и z-типа. 17
![На каждый атом в ОЦК-решётке приходится по шесть тетраэдрических пустот. Плотноупакованное направление – [111], На каждый атом в ОЦК-решётке приходится по шесть тетраэдрических пустот. Плотноупакованное направление – [111],](https://present5.com/presentation/1015967_132154887/image-18.jpg) На каждый атом в ОЦК-решётке приходится по шесть тетраэдрических пустот. Плотноупакованное направление – [111], плотноупакованной плоскости нет. 18
На каждый атом в ОЦК-решётке приходится по шесть тетраэдрических пустот. Плотноупакованное направление – [111], плотноупакованной плоскости нет. 18
 Описание кристаллических структур с помощью концепции плотнейших упаковок шаров одинакового размера более всего адекватно для кристаллов типичных металлов или благородных газов, в которых химические связи (металлическая и ван-дер-ваальсова) ненаправленны и ненасыщаемы. Большинство типичных металлов кристаллизуется либо в кубической (например, Сu), либо в гексагональной (например, Мg), либо в обеих этих упаковках (например, Со), либо образуют более многослойные упаковки (например, структура Lа описывается четырехслойной плотнейшей упаковкой). В твердом Не - гексагональная плотнейшая упаковка атомов, а в кристаллах остальных инертных газов - кубическая. 19
Описание кристаллических структур с помощью концепции плотнейших упаковок шаров одинакового размера более всего адекватно для кристаллов типичных металлов или благородных газов, в которых химические связи (металлическая и ван-дер-ваальсова) ненаправленны и ненасыщаемы. Большинство типичных металлов кристаллизуется либо в кубической (например, Сu), либо в гексагональной (например, Мg), либо в обеих этих упаковках (например, Со), либо образуют более многослойные упаковки (например, структура Lа описывается четырехслойной плотнейшей упаковкой). В твердом Не - гексагональная плотнейшая упаковка атомов, а в кристаллах остальных инертных газов - кубическая. 19
 Свойство ненаправленности в пространстве имеет также типично ионная связь. принцип плотнейшей упаковки остается справедливым и для ионных соединений. Однако, в этом случае приходится иметь дело с «шарами» разных зарядов и размеров. Если предположить, что более крупные «шары» , которые обычно описывают отрицательно заряженные частицы (анионы), образуют плотнейшую упаковку, то более мелкие «шары» (обычно катионы) окажутся в пустотах этой упаковки. При наложении плотнейших слоев друг на друга образуются два главных типа пустот - тетраэдрические и октаэдрические. Это отвечает наиболее распространенным ближайшим окружениям катионов в существенно ионных неорганических кристаллах, в том числе в кристаллах комплексных соединений. 20
Свойство ненаправленности в пространстве имеет также типично ионная связь. принцип плотнейшей упаковки остается справедливым и для ионных соединений. Однако, в этом случае приходится иметь дело с «шарами» разных зарядов и размеров. Если предположить, что более крупные «шары» , которые обычно описывают отрицательно заряженные частицы (анионы), образуют плотнейшую упаковку, то более мелкие «шары» (обычно катионы) окажутся в пустотах этой упаковки. При наложении плотнейших слоев друг на друга образуются два главных типа пустот - тетраэдрические и октаэдрические. Это отвечает наиболее распространенным ближайшим окружениям катионов в существенно ионных неорганических кристаллах, в том числе в кристаллах комплексных соединений. 20
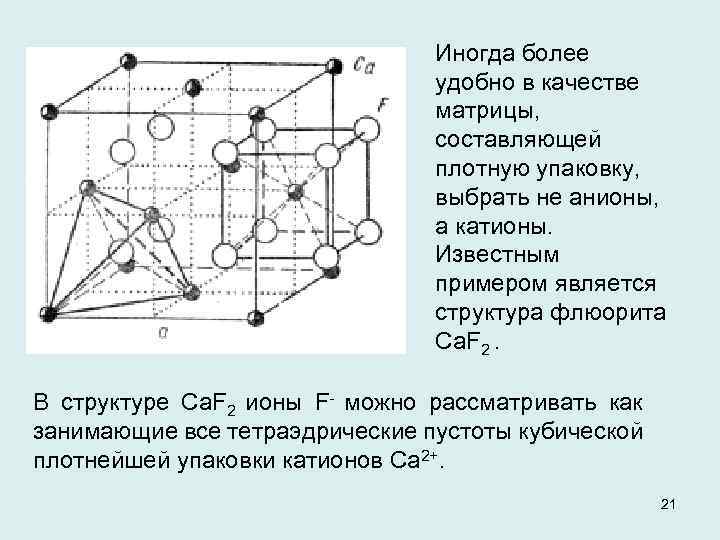 Иногда более удобно в качестве матрицы, составляющей плотную упаковку, выбрать не анионы, а катионы. Известным примером является структура флюорита Са. F 2. В структуре Са. F 2 ионы F- можно рассматривать как занимающие все тетраэдрические пустоты кубической плотнейшей упаковки катионов Са 2+. 21
Иногда более удобно в качестве матрицы, составляющей плотную упаковку, выбрать не анионы, а катионы. Известным примером является структура флюорита Са. F 2. В структуре Са. F 2 ионы F- можно рассматривать как занимающие все тетраэдрические пустоты кубической плотнейшей упаковки катионов Са 2+. 21
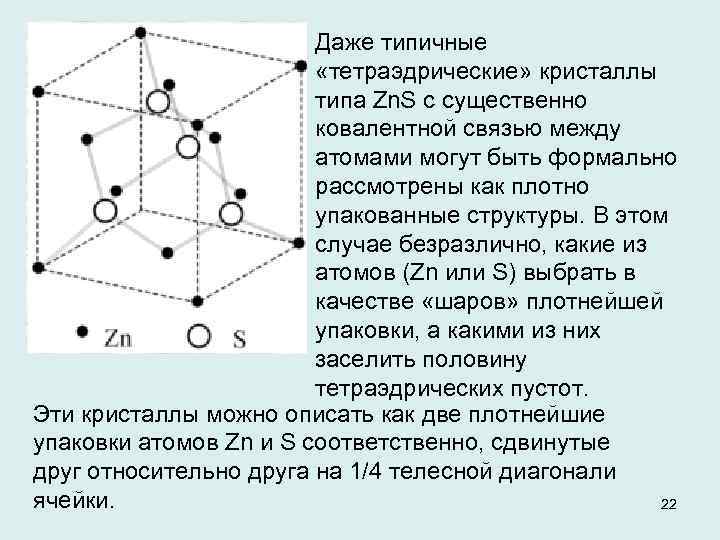 Даже типичные «тетраэдрические» кристаллы типа Zn. S с существенно ковалентной связью между атомами могут быть формально рассмотрены как плотно упакованные структуры. В этом случае безразлично, какие из атомов (Zn или S) выбрать в качестве «шаров» плотнейшей упаковки, а какими из них заселить половину тетраэдрических пустот. Эти кристаллы можно описать как две плотнейшие упаковки атомов Zn и S соответственно, сдвинутые друг относительно друга на 1/4 телесной диагонали ячейки. 22
Даже типичные «тетраэдрические» кристаллы типа Zn. S с существенно ковалентной связью между атомами могут быть формально рассмотрены как плотно упакованные структуры. В этом случае безразлично, какие из атомов (Zn или S) выбрать в качестве «шаров» плотнейшей упаковки, а какими из них заселить половину тетраэдрических пустот. Эти кристаллы можно описать как две плотнейшие упаковки атомов Zn и S соответственно, сдвинутые друг относительно друга на 1/4 телесной диагонали ячейки. 22
 Основные типы структур металлов Принцип плотнейшей упаковки играет важную роль в определении типа кристаллических структур различных классов веществ. Он лежит в основе установления конфигурации частиц в тех случаях, когда между частицами действуют ненасыщенные и ненаправленные связи. В этих условиях энергетически более выгодным оказывается образование структуры с возможно большими координационными числами. 23
Основные типы структур металлов Принцип плотнейшей упаковки играет важную роль в определении типа кристаллических структур различных классов веществ. Он лежит в основе установления конфигурации частиц в тех случаях, когда между частицами действуют ненасыщенные и ненаправленные связи. В этих условиях энергетически более выгодным оказывается образование структуры с возможно большими координационными числами. 23
 Все металлы являются кристаллическими телами, имеющими определенный тип кристаллической решетки, состоящей из малоподвижных положительно заряженных ионов, между которыми движутся свободные электроны. В кристаллах с металлической связью обобществляются валентные электроны в пределах всего кристалла. При этом наиболее вероятным становится образование структур типа плотных шаровых упаковок. Металлы имеют относительно сложные типы кубических решеток – объемно-центрированная (ОЦК) и гранецентрированная (ГЦК) кубические решетки. 24
Все металлы являются кристаллическими телами, имеющими определенный тип кристаллической решетки, состоящей из малоподвижных положительно заряженных ионов, между которыми движутся свободные электроны. В кристаллах с металлической связью обобществляются валентные электроны в пределах всего кристалла. При этом наиболее вероятным становится образование структур типа плотных шаровых упаковок. Металлы имеют относительно сложные типы кубических решеток – объемно-центрированная (ОЦК) и гранецентрированная (ГЦК) кубические решетки. 24
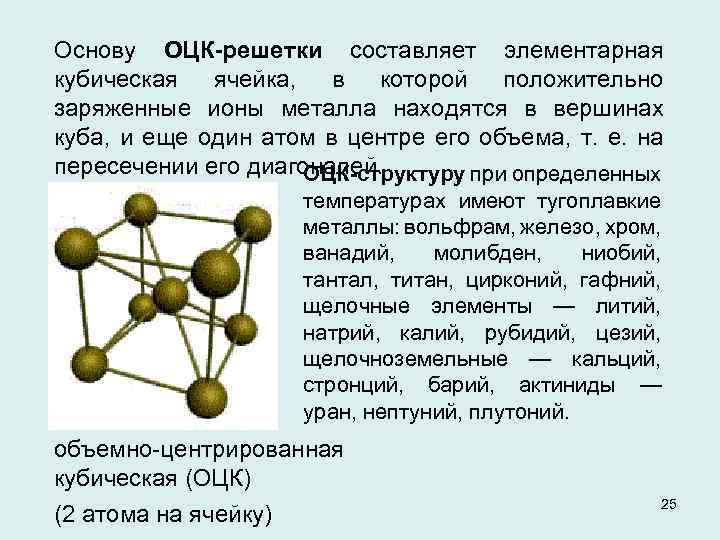 Основу ОЦК-решетки составляет элементарная кубическая ячейка, в которой положительно заряженные ионы металла находятся в вершинах куба, и еще один атом в центре его объема, т. е. на пересечении его диагоналей. ОЦК-структуру при определенных температурах имеют тугоплавкие металлы: вольфрам, железо, хром, ванадий, молибден, ниобий, тантал, титан, цирконий, гафний, щелочные элементы — литий, натрий, калий, рубидий, цезий, щелочноземельные — кальций, стронций, барий, актиниды — уран, нептуний, плутоний. объемно-центрированная кубическая (ОЦК) (2 атома на ячейку) 25
Основу ОЦК-решетки составляет элементарная кубическая ячейка, в которой положительно заряженные ионы металла находятся в вершинах куба, и еще один атом в центре его объема, т. е. на пересечении его диагоналей. ОЦК-структуру при определенных температурах имеют тугоплавкие металлы: вольфрам, железо, хром, ванадий, молибден, ниобий, тантал, титан, цирконий, гафний, щелочные элементы — литий, натрий, калий, рубидий, цезий, щелочноземельные — кальций, стронций, барий, актиниды — уран, нептуний, плутоний. объемно-центрированная кубическая (ОЦК) (2 атома на ячейку) 25
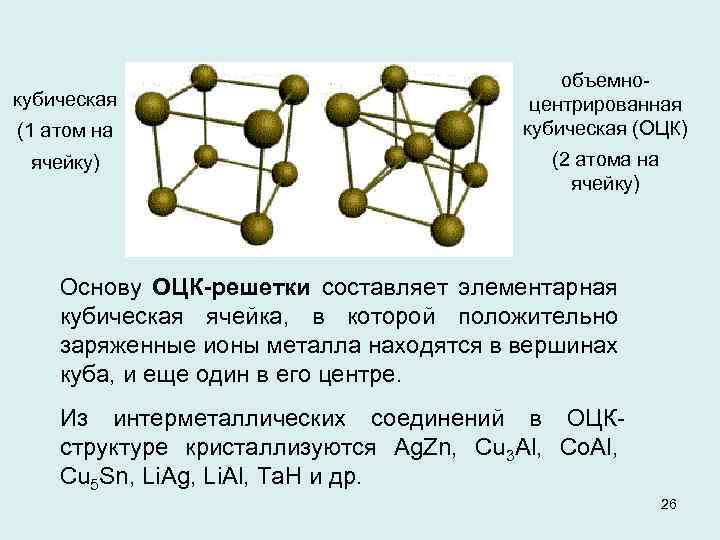 кубическая (1 атом на ячейку) объемноцентрированная кубическая (ОЦК) (2 атома на ячейку) Основу ОЦК-решетки составляет элементарная кубическая ячейка, в которой положительно заряженные ионы металла находятся в вершинах куба, и еще один в его центре. Из интерметаллических соединений в ОЦКструктуре кристаллизуются Ag. Zn, Cu 3 Al, Co. Al, Cu 5 Sn, Li. Ag, Li. Al, Ta. H и др. 26
кубическая (1 атом на ячейку) объемноцентрированная кубическая (ОЦК) (2 атома на ячейку) Основу ОЦК-решетки составляет элементарная кубическая ячейка, в которой положительно заряженные ионы металла находятся в вершинах куба, и еще один в его центре. Из интерметаллических соединений в ОЦКструктуре кристаллизуются Ag. Zn, Cu 3 Al, Co. Al, Cu 5 Sn, Li. Ag, Li. Al, Ta. H и др. 26
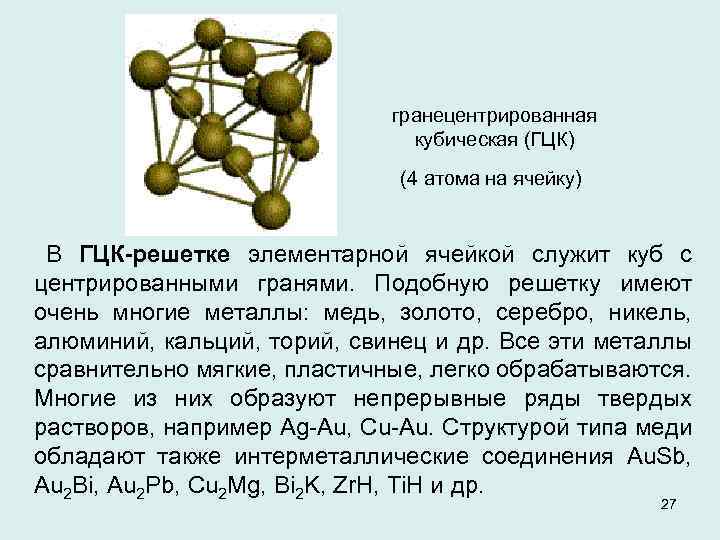 гранецентрированная кубическая (ГЦК) (4 атома на ячейку) В ГЦК-решетке элементарной ячейкой служит куб с центрированными гранями. Подобную решетку имеют очень многие металлы: медь, золото, серебро, никель, алюминий, кальций, торий, свинец и др. Все эти металлы сравнительно мягкие, пластичные, легко обрабатываются. Многие из них образуют непрерывные ряды твердых растворов, например Ag-Au, Cu-Au. Структурой типа меди обладают также интерметаллические соединения Au. Sb, Au 2 Bi, Au 2 Pb, Cu 2 Mg, Bi 2 K, Zr. H, Ti. H и др. 27
гранецентрированная кубическая (ГЦК) (4 атома на ячейку) В ГЦК-решетке элементарной ячейкой служит куб с центрированными гранями. Подобную решетку имеют очень многие металлы: медь, золото, серебро, никель, алюминий, кальций, торий, свинец и др. Все эти металлы сравнительно мягкие, пластичные, легко обрабатываются. Многие из них образуют непрерывные ряды твердых растворов, например Ag-Au, Cu-Au. Структурой типа меди обладают также интерметаллические соединения Au. Sb, Au 2 Bi, Au 2 Pb, Cu 2 Mg, Bi 2 K, Zr. H, Ti. H и др. 27
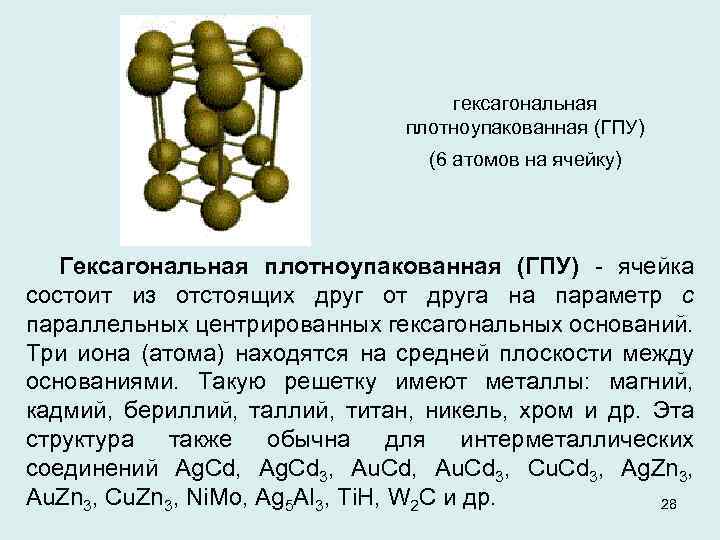 гексагональная плотноупакованная (ГПУ) (6 атомов на ячейку) Гексагональная плотноупакованная (ГПУ) - ячейка состоит из отстоящих друг от друга на параметр с параллельных центрированных гексагональных оснований. Три иона (атома) находятся на средней плоскости между основаниями. Такую решетку имеют металлы: магний, кадмий, бериллий, таллий, титан, никель, хром и др. Эта структура также обычна для интерметаллических соединений Ag. Cd, Ag. Cd 3, Au. Cd 3, Cu. Cd 3, Ag. Zn 3, Au. Zn 3, Cu. Zn 3, Ni. Mo, Ag 5 Al 3, Ti. H, W 2 C и др. 28
гексагональная плотноупакованная (ГПУ) (6 атомов на ячейку) Гексагональная плотноупакованная (ГПУ) - ячейка состоит из отстоящих друг от друга на параметр с параллельных центрированных гексагональных оснований. Три иона (атома) находятся на средней плоскости между основаниями. Такую решетку имеют металлы: магний, кадмий, бериллий, таллий, титан, никель, хром и др. Эта структура также обычна для интерметаллических соединений Ag. Cd, Ag. Cd 3, Au. Cd 3, Cu. Cd 3, Ag. Zn 3, Au. Zn 3, Cu. Zn 3, Ni. Mo, Ag 5 Al 3, Ti. H, W 2 C и др. 28
 Важной характеристикой кристаллической решетки является компактность или степень заполнения ее объема атомами. Она определяется такими показателями как параметр решетки, число атомов в элементарной ячейке, координационное число и плотность упаковки. Параметр решетки - расстояние между атомами по ребру элементарной ячейки. Параметры кубических решеток характеризуются длиной ребра куба и обозначаются буквой а. Гексагональной решетки - стороной шестигранника а и высотой призмы с. При с/а = 1, 633 решетка называется гексагональной плотноупакованной. Некоторые металлы имеют гексагональную решетку с менее плотной упаковкой атомов (с/а > 1, 633): для цинка с/а = 1, 86, для кадмия с/а = 1, 88. 29
Важной характеристикой кристаллической решетки является компактность или степень заполнения ее объема атомами. Она определяется такими показателями как параметр решетки, число атомов в элементарной ячейке, координационное число и плотность упаковки. Параметр решетки - расстояние между атомами по ребру элементарной ячейки. Параметры кубических решеток характеризуются длиной ребра куба и обозначаются буквой а. Гексагональной решетки - стороной шестигранника а и высотой призмы с. При с/а = 1, 633 решетка называется гексагональной плотноупакованной. Некоторые металлы имеют гексагональную решетку с менее плотной упаковкой атомов (с/а > 1, 633): для цинка с/а = 1, 86, для кадмия с/а = 1, 88. 29
 Число атомов в ОЦК- и ГЦК-ячейках 2 и 4, соответственно. Плотность упаковки - отношение суммарного объема, занимаемого атомами в ячейке, к ее полному объему ( ГЦК и ГПУ – 74%, ОЦК - 68%). Координационное число - количество ближайших соседей данного атома. Для ОЦК решетки КЧ=8, для ГЦК КЧ=12, для ГПУ КЧ=12. В плотнейших шаровых упаковках встречаются КЧ-12 (координационный многогранник – кубооктаэдр), 6 (октаэдр), 4 (тетраэдр), 3 (треугольник), 2 (гантель). 30
Число атомов в ОЦК- и ГЦК-ячейках 2 и 4, соответственно. Плотность упаковки - отношение суммарного объема, занимаемого атомами в ячейке, к ее полному объему ( ГЦК и ГПУ – 74%, ОЦК - 68%). Координационное число - количество ближайших соседей данного атома. Для ОЦК решетки КЧ=8, для ГЦК КЧ=12, для ГПУ КЧ=12. В плотнейших шаровых упаковках встречаются КЧ-12 (координационный многогранник – кубооктаэдр), 6 (октаэдр), 4 (тетраэдр), 3 (треугольник), 2 (гантель). 30
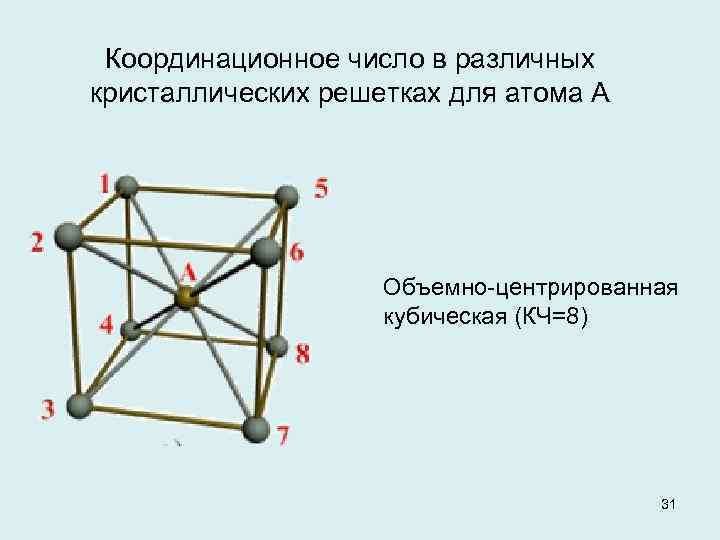 Координационное число в различных кристаллических решетках для атома А Объемно-центрированная кубическая (КЧ=8) 31
Координационное число в различных кристаллических решетках для атома А Объемно-центрированная кубическая (КЧ=8) 31
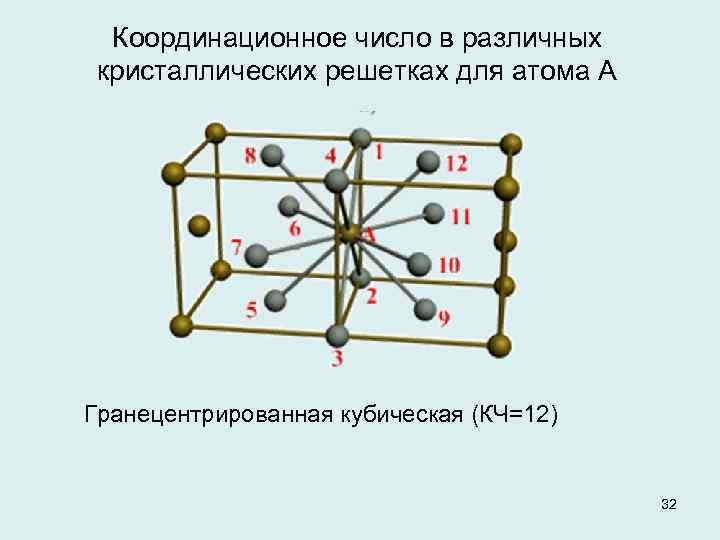 Координационное число в различных кристаллических решетках для атома А Гранецентрированная кубическая (КЧ=12) 32
Координационное число в различных кристаллических решетках для атома А Гранецентрированная кубическая (КЧ=12) 32
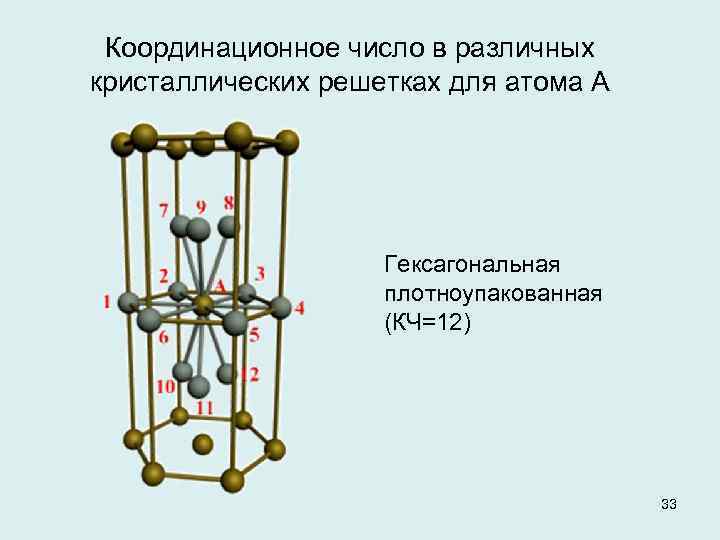 Координационное число в различных кристаллических решетках для атома А Гексагональная плотноупакованная (КЧ=12) 33
Координационное число в различных кристаллических решетках для атома А Гексагональная плотноупакованная (КЧ=12) 33
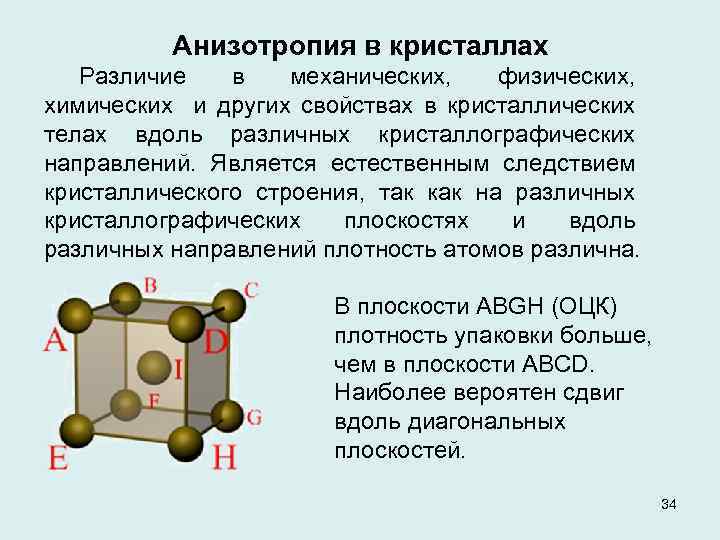 Анизотропия в кристаллах Различие в механических, физических, химических и других свойствах в кристаллических телах вдоль различных кристаллографических направлений. Является естественным следствием кристаллического строения, так как на различных кристаллографических плоскостях и вдоль различных направлений плотность атомов различна. В плоскости ABGH (ОЦК) плотность упаковки больше, чем в плоскости ABСD. Наиболее вероятен сдвиг вдоль диагональных плоскостей. 34
Анизотропия в кристаллах Различие в механических, физических, химических и других свойствах в кристаллических телах вдоль различных кристаллографических направлений. Является естественным следствием кристаллического строения, так как на различных кристаллографических плоскостях и вдоль различных направлений плотность атомов различна. В плоскости ABGH (ОЦК) плотность упаковки больше, чем в плоскости ABСD. Наиболее вероятен сдвиг вдоль диагональных плоскостей. 34
 Примеры кристаллических структур металлов Структура кристалла − это конкретное расположение частиц в пространстве. Описывая структуру, необходимо указать вид и размер частиц, а также расстояния между ними. Если вещества кристаллизуются в сходных друг с другом решетках, то говорят, что они относятся к одному структурному типу. У кристаллов, принадлежащих к одному структурному типу, элементарные ячейки одинаковы с точностью до подобия. Известно, что почти 80 % металлов кристаллизуются в объемно- и гранецентрированных кубических, а также в гексагональных плотноупакованных решетках. 35
Примеры кристаллических структур металлов Структура кристалла − это конкретное расположение частиц в пространстве. Описывая структуру, необходимо указать вид и размер частиц, а также расстояния между ними. Если вещества кристаллизуются в сходных друг с другом решетках, то говорят, что они относятся к одному структурному типу. У кристаллов, принадлежащих к одному структурному типу, элементарные ячейки одинаковы с точностью до подобия. Известно, что почти 80 % металлов кристаллизуются в объемно- и гранецентрированных кубических, а также в гексагональных плотноупакованных решетках. 35
 Структура вольфрама характеризуется объемноцентрированной кубической ячейкой — ОЦК. Атомы располагаются по вершинам и в центре ячейки, т. е. на ячейку приходится два атома. Пространственная группа Im 3 m. Плоскости зеркального отражения проходят параллельно грани элементарной ячейки и диагоналям граней. Структура не является плотнейшей упаковкой атомов. Наиболее плотноупакованные плоскости (110). Коэффициент компактности 0, 68, т. к. на каждый атом приходится по три октаэдрических и по шесть тетраэдрических пустот, тогда как в плотнейших ГЦК и ГПУ упаковках — по одной октаэдрической и по две тетраэдрических пустоты. Большее число пустот обеспечивает «рыхлость» структуры и более легкое 36 вхождение примесей.
Структура вольфрама характеризуется объемноцентрированной кубической ячейкой — ОЦК. Атомы располагаются по вершинам и в центре ячейки, т. е. на ячейку приходится два атома. Пространственная группа Im 3 m. Плоскости зеркального отражения проходят параллельно грани элементарной ячейки и диагоналям граней. Структура не является плотнейшей упаковкой атомов. Наиболее плотноупакованные плоскости (110). Коэффициент компактности 0, 68, т. к. на каждый атом приходится по три октаэдрических и по шесть тетраэдрических пустот, тогда как в плотнейших ГЦК и ГПУ упаковках — по одной октаэдрической и по две тетраэдрических пустоты. Большее число пустот обеспечивает «рыхлость» структуры и более легкое 36 вхождение примесей.
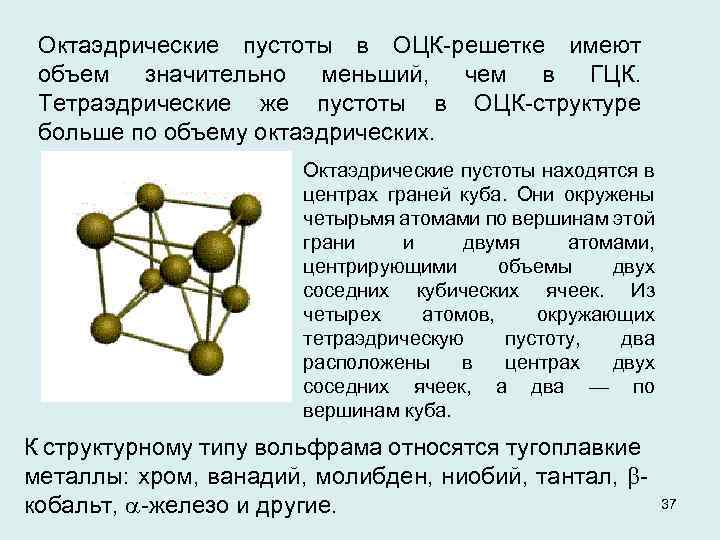 Октаэдрические пустоты в ОЦК-решетке имеют объем значительно меньший, чем в ГЦК. Тетраэдрические же пустоты в ОЦК-структуре больше по объему октаэдрических. Октаэдрические пустоты находятся в центрах граней куба. Они окружены четырьмя атомами по вершинам этой грани и двумя атомами, центрирующими объемы двух соседних кубических ячеек. Из четырех атомов, окружающих тетраэдрическую пустоту, два расположены в центрах двух соседних ячеек, а два — по вершинам куба. К структурному типу вольфрама относятся тугоплавкие металлы: хром, ванадий, молибден, ниобий, тантал, кобальт, -железо и другие. 37
Октаэдрические пустоты в ОЦК-решетке имеют объем значительно меньший, чем в ГЦК. Тетраэдрические же пустоты в ОЦК-структуре больше по объему октаэдрических. Октаэдрические пустоты находятся в центрах граней куба. Они окружены четырьмя атомами по вершинам этой грани и двумя атомами, центрирующими объемы двух соседних кубических ячеек. Из четырех атомов, окружающих тетраэдрическую пустоту, два расположены в центрах двух соседних ячеек, а два — по вершинам куба. К структурному типу вольфрама относятся тугоплавкие металлы: хром, ванадий, молибден, ниобий, тантал, кобальт, -железо и другие. 37
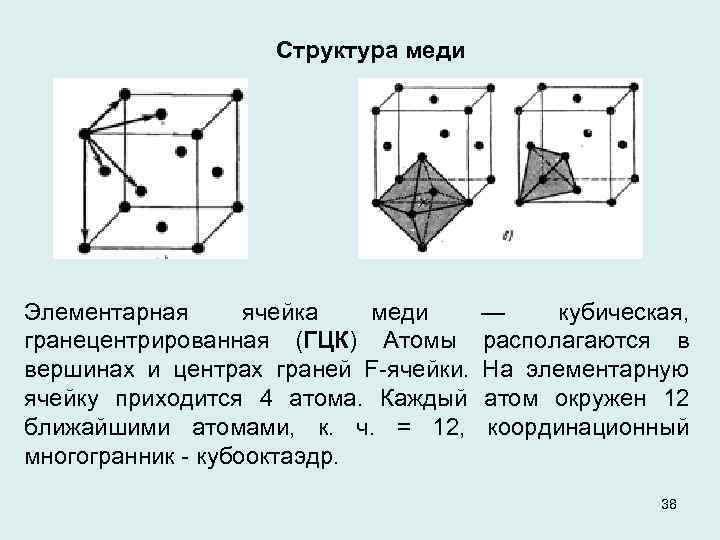 Структура меди Элементарная ячейка меди — кубическая, гранецентрированная (ГЦК) Атомы располагаются в вершинах и центрах граней F-ячейки. На элементарную ячейку приходится 4 атома. Каждый атом окружен 12 ближайшими атомами, к. ч. = 12, координационный многогранник - кубооктаэдр. 38
Структура меди Элементарная ячейка меди — кубическая, гранецентрированная (ГЦК) Атомы располагаются в вершинах и центрах граней F-ячейки. На элементарную ячейку приходится 4 атома. Каждый атом окружен 12 ближайшими атомами, к. ч. = 12, координационный многогранник - кубооктаэдр. 38
 Пространственная группа F m 3 m. Плоскости зеркального отражения m проходят параллельно грани элементарной ячейки и диагоналям граней. Плотнейшая упаковка — кубическая, трехслойная АВСАВС. . . К структурному типу меди относятся, например, золото, серебро, никель, алюминий, кальций, свинец, -кобальт и др. Все эти металлы сравнительно мягкие, пластичные, легко обрабатываются. Структурой типа меди обладают некоторые твердые растворы, например твердый раствор меди в золоте (Cu−Au), а также многие так называемые интерметаллические соединения (Au. Sb, Zr. H, Ti. H и т. д. ). 39
Пространственная группа F m 3 m. Плоскости зеркального отражения m проходят параллельно грани элементарной ячейки и диагоналям граней. Плотнейшая упаковка — кубическая, трехслойная АВСАВС. . . К структурному типу меди относятся, например, золото, серебро, никель, алюминий, кальций, свинец, -кобальт и др. Все эти металлы сравнительно мягкие, пластичные, легко обрабатываются. Структурой типа меди обладают некоторые твердые растворы, например твердый раствор меди в золоте (Cu−Au), а также многие так называемые интерметаллические соединения (Au. Sb, Zr. H, Ti. H и т. д. ). 39
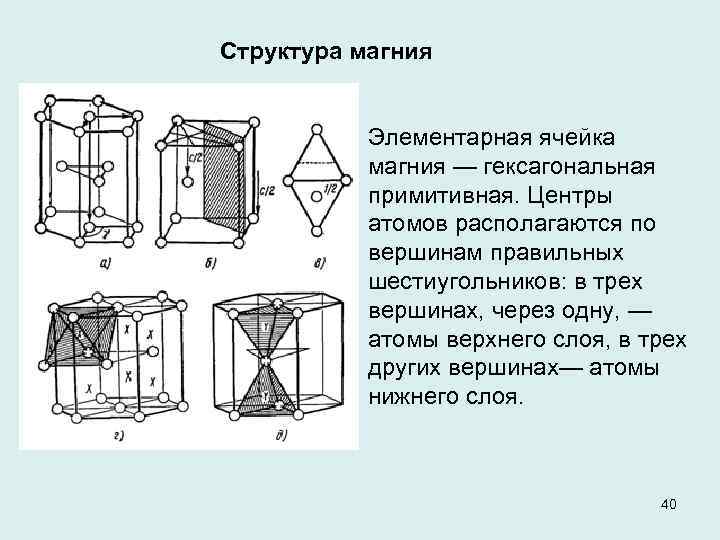 Структура магния Элементарная ячейка магния — гексагональная примитивная. Центры атомов располагаются по вершинам правильных шестиугольников: в трех вершинах, через одну, — атомы верхнего слоя, в трех других вершинах— атомы нижнего слоя. 40
Структура магния Элементарная ячейка магния — гексагональная примитивная. Центры атомов располагаются по вершинам правильных шестиугольников: в трех вершинах, через одну, — атомы верхнего слоя, в трех других вершинах— атомы нижнего слоя. 40
 Элементарную ячейку можно разделить плоскостью на две тригональные призмы. В центре одной из призм расположен атом, другая «не заселена» , «заселенные» и пустые призмы чередуются между собой. На элементарную ячейку приходится два атома магния. Каждый атом окружен 12 ближайшими атомами: 6 в том же слое и 3 в соседних слоях сверху и снизу. КЧ = 12, что служит признаком плотнейшей упаковки. Координационный многогранник — гексагональный аналог кубооктаэдра. Плотные слои – плоскости базиса (000). Упаковка гексагональная, АВАВ. . двухслойная . . . 41
Элементарную ячейку можно разделить плоскостью на две тригональные призмы. В центре одной из призм расположен атом, другая «не заселена» , «заселенные» и пустые призмы чередуются между собой. На элементарную ячейку приходится два атома магния. Каждый атом окружен 12 ближайшими атомами: 6 в том же слое и 3 в соседних слоях сверху и снизу. КЧ = 12, что служит признаком плотнейшей упаковки. Координационный многогранник — гексагональный аналог кубооктаэдра. Плотные слои – плоскости базиса (000). Упаковка гексагональная, АВАВ. . двухслойная . . . 41
 Пространственная группа магния Р бз/ттс. Через центры правильных шестиугольников перпендикулярно слоям проходит ось 63, a перпендикулярно ей — плоскость зеркального отражения m, совпадающая с горизонтальными слоями атомов. В направлении длинной диагонали ромба, представляющего грань ячейки, перпендикулярную оси 63, также проходит плоскость зеркального отражения m. Параллельно короткой диагонали ромба через ось симметрии 63 проходит плоскость скользящего отражения с. К структурному типу относятся, например кадмий, бериллий, таллий, титан, никель и др. , интерметаллические соединения, Ag. Cd, Au. Cd, Cu. Cd 3 и т. д. 42
Пространственная группа магния Р бз/ттс. Через центры правильных шестиугольников перпендикулярно слоям проходит ось 63, a перпендикулярно ей — плоскость зеркального отражения m, совпадающая с горизонтальными слоями атомов. В направлении длинной диагонали ромба, представляющего грань ячейки, перпендикулярную оси 63, также проходит плоскость зеркального отражения m. Параллельно короткой диагонали ромба через ось симметрии 63 проходит плоскость скользящего отражения с. К структурному типу относятся, например кадмий, бериллий, таллий, титан, никель и др. , интерметаллические соединения, Ag. Cd, Au. Cd, Cu. Cd 3 и т. д. 42
 Применения теории плотнейших упаковок Свойство ненаправленности в пространстве имеет также типично ионная связь, хотя в этом случае приходится иметь дело с «шарами» разных зарядов и размеров. Если предположить, что более крупные «шары» , которые обычно описывают отрицательно заряженные частицы (анионы), образуют плотнейшую упаковку, то более мелкие «шары» (обычно катионы) окажутся в пустотах этой упаковки. При наложении плотнейших слоев друг на друга образуются два главных типа пустот - тетраэдрические и октаэдрические. На каждый шар приходится две тетраэдрические и одна октаэдрическая пустоты. 43
Применения теории плотнейших упаковок Свойство ненаправленности в пространстве имеет также типично ионная связь, хотя в этом случае приходится иметь дело с «шарами» разных зарядов и размеров. Если предположить, что более крупные «шары» , которые обычно описывают отрицательно заряженные частицы (анионы), образуют плотнейшую упаковку, то более мелкие «шары» (обычно катионы) окажутся в пустотах этой упаковки. При наложении плотнейших слоев друг на друга образуются два главных типа пустот - тетраэдрические и октаэдрические. На каждый шар приходится две тетраэдрические и одна октаэдрическая пустоты. 43
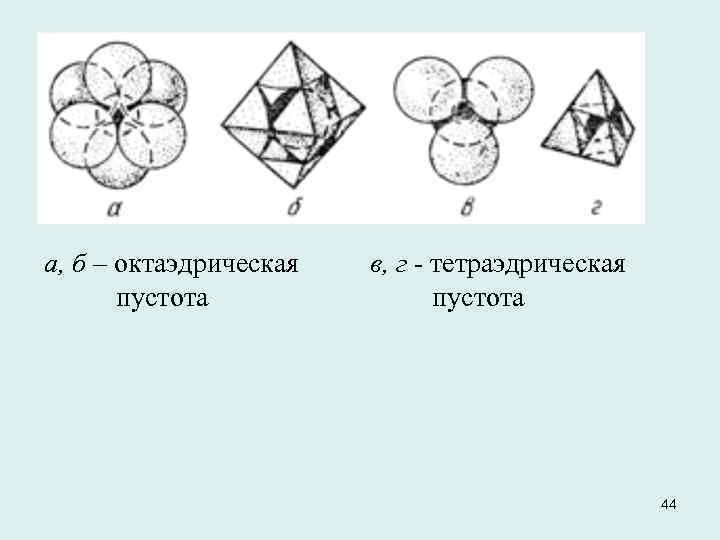 а, б – октаэдрическая в, г - тетраэдрическая пустота пустота 44
а, б – октаэдрическая в, г - тетраэдрическая пустота пустота 44
 Рамки применения теории плотнейших упаковок сильно расширяются благодаря тому, что наиболее распространенные ближайшие окружения катионов в существенно ионных неорганических кристаллах, в том числе в кристаллах комплексных соединений, октаэдрическое и тетраэдрическое. Можно считать, что чаще всего катионы попадают либо в тетраэдрические, либо в октаэдрические пустоты плотнейшей упаковки анионов. В ряде случаев более удобно в качестве матрицы, составляющей плотную упаковку, выбрать не анионы, а катионы. Известным примером является структура флюорита Са. F 2 , в которой ионы F- можно рассматривать как занимающие все тетраэдрические пустоты кубической плотнейшей упаковки катионов Са 2+. 45
Рамки применения теории плотнейших упаковок сильно расширяются благодаря тому, что наиболее распространенные ближайшие окружения катионов в существенно ионных неорганических кристаллах, в том числе в кристаллах комплексных соединений, октаэдрическое и тетраэдрическое. Можно считать, что чаще всего катионы попадают либо в тетраэдрические, либо в октаэдрические пустоты плотнейшей упаковки анионов. В ряде случаев более удобно в качестве матрицы, составляющей плотную упаковку, выбрать не анионы, а катионы. Известным примером является структура флюорита Са. F 2 , в которой ионы F- можно рассматривать как занимающие все тетраэдрические пустоты кубической плотнейшей упаковки катионов Са 2+. 45
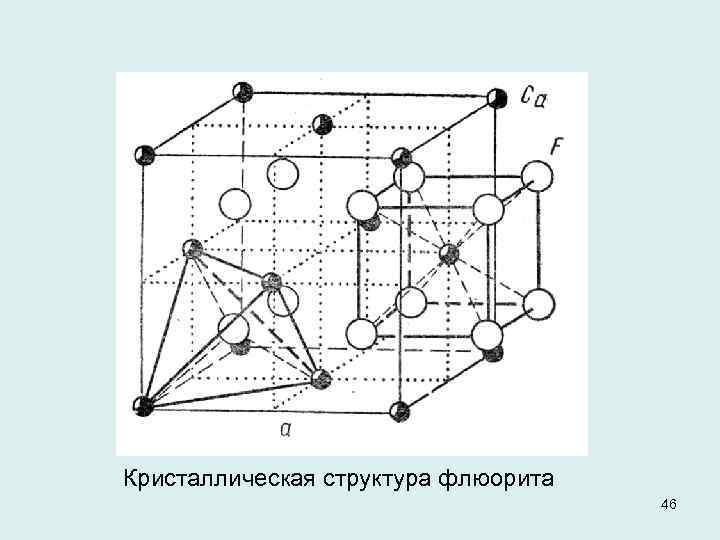 Кристаллическая структура флюорита 46
Кристаллическая структура флюорита 46
 Типичные «тетраэдрические» кристаллы типа Zn. S с существенно ковалентной связью между атомами могут быть формально рассмотрены как плотно упакованные структуры. В этом случае безразлично, какие из атомов (Zn или S) выбрать в качестве «шаров» плотнейшей упаковки, а какими из них заселить половину тетраэдрических пустот. С равным успехом эти кристаллы можно описать как две плотнейшие упаковки атомов Zn и S соответственно, сдвинутые друг относительно друга на 1/4 телесной диагонали ячейки Бравэ. Принципы теории плотнейших упаковок в большинстве случаев скорее представляют собой полезную основу для формального описания кристаллической структуры, чем отражают реальную картину строения кристалла. 47
Типичные «тетраэдрические» кристаллы типа Zn. S с существенно ковалентной связью между атомами могут быть формально рассмотрены как плотно упакованные структуры. В этом случае безразлично, какие из атомов (Zn или S) выбрать в качестве «шаров» плотнейшей упаковки, а какими из них заселить половину тетраэдрических пустот. С равным успехом эти кристаллы можно описать как две плотнейшие упаковки атомов Zn и S соответственно, сдвинутые друг относительно друга на 1/4 телесной диагонали ячейки Бравэ. Принципы теории плотнейших упаковок в большинстве случаев скорее представляют собой полезную основу для формального описания кристаллической структуры, чем отражают реальную картину строения кристалла. 47


