презентация химия.pptx
- Количество слайдов: 29

Элементы II Б группы: цинк, кадмий, ртуть. Сопоставление электронных конфигураций, величин радиусов, энергий ионизации атомов элементов подгруппы цинка и подгруппы щелочноземельных элементов, характерные степени окисления, координационные числа. Получение, физические и химические свойства цинка, кадмия, ртути. Сравнение строения и свойств соединений в степени окисления (II) (оксиды, гидроксиды, галогениды). Строение и диспропорционирование соединений Hg 22+. Комплексные соединения: аммиакаты, галогениды, цианиды, тиоцианаты. Применение цинка, кадмия, ртути и их соединений.

Положения в периодической системе: q Ртуть расположена в 12 группе Периодической системы химических элементов Д. И. Менделеева. В шестом периоде ртуть является последним d элементом, его валентные электроны 5 d 106 s 2. В образовании химических связей участвуют только электроны внешнего энергетического уровня, поскольку конфигурация d 10 является очень устойчивой. В соединениях для ртути характерны степени окисления +1 и +2.
![Важнейшие свойства ртути: q q q Электронная конфигурация [Hg] 4 f 14 5 d Важнейшие свойства ртути: q q q Электронная конфигурация [Hg] 4 f 14 5 d](https://present5.com/presentation/39614796_85876644/image-3.jpg)
Важнейшие свойства ртути: q q q Электронная конфигурация [Hg] 4 f 14 5 d 10 6 s 2 Радиус атома 0, 157 нм Энергия ионизации (10, 43) (э. В) Степени окисления +2, +1 Электродный потенциал Hg ←Hg 2+ 0, 854 В Атомный номер 80 Атомная масса 200, 59 Плотность г/см³ 13, 52 Температура плавления °С 38, 9 Температура кипения °С 357 Электроотрицательность 1, 9

q q q Физические свойства ртути: Ртуть при нормальных условиях — серебристо белая блестящая жидкость, которая заметно испаряется уже при комнатной температуре, пары ртути ядовиты! Единственный металл, находящийся при комнатной температуре в жидком состоянии, ведь температура плавления ртути = 38, 89 °С, то есть, чтобы перевести элемент в твердое состояние, его необходимо заморозить. Температура кипения ртути также невелика, начинает кипеть при 356, 58 °С. В твердом состоянии она представляет собой серебристо синеватый металл обладающий хорошей ковкостью и эластичностью, напоминающий по внешнему виду свинец. Поэтому, если залить ртуть в форму, имеющую очертания молотка, а затем быстро охладить до затвердевания, например, жидким азотом, то таким ртутным молотком можно с успехом забить гвоздь в доску, только делать это необходимо быстро, ведь такой инструмент весьма недолговечен и может растаять на глазах. В своем обычном состоянии ртуть — в 13, 6 раза тяжелее воды в ней будут тонуть лишь некоторые тяжелые тугоплавкие металлы, зато железный болт, например, будет плавать на поверхности ртутной ванны. Однако, в связи с тем, что ртуть весьма ядовита и она не выводиться из организма человека, вышеприведенные эксперименты можно проводить лишь в специально оборудованных научных лабораториях.
![Группировка [Hg 2]2+ Для ртути характерно состояние окисления +1, которое сводится к образованию группировки Группировка [Hg 2]2+ Для ртути характерно состояние окисления +1, которое сводится к образованию группировки](https://present5.com/presentation/39614796_85876644/image-5.jpg)
Группировка [Hg 2]2+ Для ртути характерно состояние окисления +1, которое сводится к образованию группировки [Hg 2]2+ содержащей связь Hg —Hg; предположение о существовании в жидкой ртути «псевдомолекул» [Hg]2 хорошо объясняет ее легкоплавкость и летучесть. Однако пар над металлической ртутью состоит из одноатомных молекул.

Химические свойства ртути: 1. Взаимодействие с неметаллами q Выше 300°С окисляется кислородом, образуя оксид ртути (II) красного цвета : 2 Hg + O 2 = 2 Hg. O. Эта реакция обратима: при нагревании выше 340 °C оксид разлагается до простых веществ : ртути и кислорода. q Очень легко взаимодействует с серой с образованием сульфида ртути (II): Hg + S = Hg. S. q При нормальных условиях реагирует с галогенами: Hg + Cl 2 = Hg. Cl 2. q При нагревании – с фосфором, образуя фосфид: 3 Hg + 2 P = Hg 3 P 2. q С водородом, азотом, бором, кремнием, углеродом ртуть не взаимодействует. 2. Взаимодействие с кислотами q В электрохимическом ряду напряжений металлов ртуть находится после водорода; с водой, щелочами и неокисляющими кислотами не взаимодействует. q Растворяется в разбавленной и концентрированной азотной кислоте и концентрированной серной кислоте, образуя соли ртути и продукты восстановления кислот: Hg + 4 HNO 3 (конц. ) = Hg(NO 3)2 + 2 NO 2 + 2 H 2 O, 6 Hg + 8 HNO 3 (разб. ) = 3 Hg 2(NO 3)2 + 2 NO + 4 H 2 O, Hg + 2 H 2 SO 4 = Hg. SO 4 + SO 2 + 2 H 2 O; q при избытке ртути возможно образование сульфата ртути (I): 2 Hg + 2 H 2 SO 4 = Hg 2 SO 4 + SO 2 + 2 H 2 O. q ртуть растворяется в царской водке: 3 Hg + 2 HNO 3 + 6 HCl=3 Hg. Cl 2 + 2 NO+ 4 H 2 O 3. Взаимодействие с солями q Ртуть взаимодействует с солями ртути (II) с образованием солей ртути (I): Hg + Hg(NO 3)2 = Hg 2(NO 3)2, Hg + Hg. Cl 2 = Hg 2 Cl 2. q Другие металлы, из за малой активности, вытеснять из растворов не может.

Получение ртути: q Ртутное месторождение Монте Амьята в Италии разрабатывается со времен Древнего Рима. Причина столь ранней известности ртути в том, что добываемая там киноварь (сульфид ртути Hg. S) легко разлагается при нагревании на воздухе при 700– 800 °С с образованием металлической ртути: Hg. S + 02 = Нg + S 02. q Ртуть также можно получить при восстановлении её из сульфида более активным металлом: Hg. S + Fe = Hg + Fe. S. q При воздействии восстановителей соединения восстанавливаются до металлической ртути: Hg 2 Cl 2 + SO 2 + 2 H 2 O = H 2 SO 4 + Hg + 2 HCl.

Оксиды ртути Физические свойства v оксида ртути (I) Hg 2 O Черные кристаллы с плотностью 9, 8 г/см 3. Неустойчив и легко разлагается под действием света или тепла на Hg. O и металлическую ртуть. Hg 2 O плохо растворим в воде (ПР =1, 6· 10 23). q Получение Hg 2 O не удалось получить, так как он на свету мгновенно распадается (диспропорционирует) на оксид ртути (II) и метал лическую ртуть давая осадок черного цвета. Hg 2(NO 3)2 + 2 Na. OH = Hg 2 O + H 2 O + 2 Na. NO 3. Hg 2(NO 3)2 + 2 Na. OH => Hg. O + Hg + Н 2 O + 2 Na. NO 3. q

q Физические свойства v Оксид ртути (II) Hg. O Образует две кристаллические модификации : красный кристаллический или желтый аморфный порошок , цвет зависит от размера кристаллов: при размерах до 4 мкм цвет оксида желтый, выше 8 мкм – красный. Желтая до 4 мкм, красная выше 8 мкм. Для желтого Hg. O: плотность = 11, 03 г/см 3 , а для красного Hg. O: плотность = 11, 14 г/см 3. Hg. O слабое основание. Желтая форма химически более активна, разлагается при 332 °С, а красная форма разлагается около 500 °С, при нагревании чернеет, но приобретает прежний цвет при охлаждении. Желтая модификация при нагревании краснеет. Hg. O плохо растворим в воде.

q Получение оксида ртути (II) Hg. O Красный оксид ртути получают нагреванием ртути до 350 °C или пиролизом нитрата ртути. 2 Hg + O 2 → 2 Hg. O 2 Hg(NO 3)2 → 2 Hg. O + 4 NO 2↑ + O 2↑ v Жёлтый оксид получают осаждением солей ртути(II) щелочами, например: Hg. S + 2 Na. OH → Hg. O + Na 2 S + H 2 O↑ Hg(NO 3)2 + 2 Na. OH = Hg. O↓ + 2 Na. NO 3 + H 2 O. Разница в цвете объясняется размером частиц, обе формы имеют одинаковую структуру — цепь линейных звеньев состава O Hg O соединённых под углом 108°. v

Химические свойства ртути: q Оксид ртути (II) обладает только основными свойствами, растворяется в кислотах: Hg. O + 2 HNO 3 = Hg(NO 3)2 + H 2 O. q Оксид ртути (II) взаимодействует с растворами галогенидов ЩЭ с выделением соответствующей щелочи. Hg. O + 4 KI + Н 2 О = K 2[Hg. I 4] + 2 KOH.

Гидроксиды ртути q Металл ртуть — один из немногих металлов, не образующих гидроксидов. Гидроксид ртути (II) уже при попытке его выделения отщепляет воду, превращаясь в оксид ртути: Hg(NO 3)2+2 Na. OH=Hg. O+Н 2 О+2 Na. NO 3.
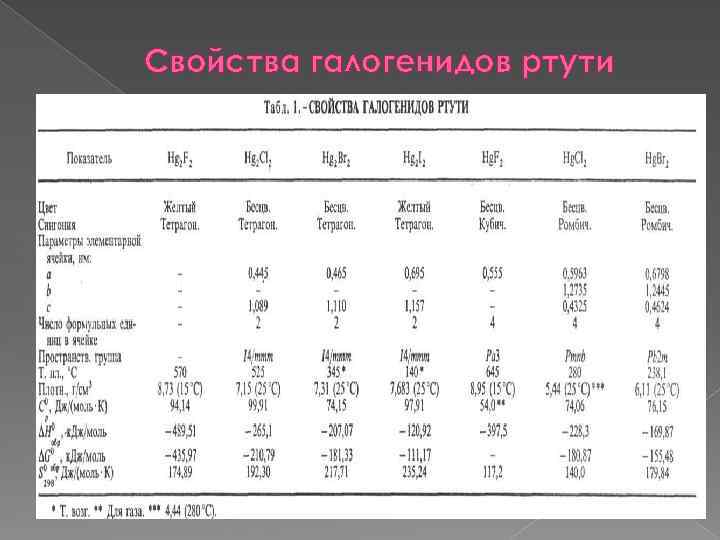
Свойства галогенидов ртути

Физические свойства Моногалогениды Hg 2 X 2, где X = Сl, Вr, I, малорастворимы в воде, не растворимы в органических растворителях. Особенность в химическом поведении Hg 2 X 2 способность ионов к диспропорционированию: Hg 2+ + Hg 0, в растворе равновесие сдвигается вправо в присутствие избытка ионов Сl , Вr , а также лигандов, с которыми ион Hg 2+ образует прочные комплексы (ОН , S 2 , CN , I , амины, алкилсульфиды); q Дигалогениды Hg. X 2 растворимы в воде и органических растворителях, в отличие от большинства других солей в водных растворах практически не диссоциируются. В водных растворах в присутствие избытка MX, где М = Na, К, Rb, образуют хорошо растворимые комплексы M 2[Hg. X 4]. q

q Физические свойства Hg 2 Сl 2 (Каломель): Белый порошок, без вкуса и запаха, нерастворим в воде, спирте, этаноле, эфире , растворяется в бензоле, пиридине. При действии аммиака чернеет. Почернение происходит вследствие выделения мелкодисперсной ртути. Плотность =7160 кг/м 3, испаряется без плавления; температура возгонки = 383, 7 °C. q Получение Hg 2 Сl 2: v с помощью реакций ионного обмена, например осаждением хлоридом калия из раствора нитрата диртути в разбавленной азотной кислоте v взаимодействием хлорида ртути 2 и металлической ртути при высокой температуре

v q Химические свойства. Hg 2 Сl 2: свойства Хлорид диртути (+2) не реагирует со щелочами. Окисляется до соединений ртути(II): v в горячей концентрированной серной кислоте v в горячей концентрированной азотной кислоте v Восстанавливается до металлической ртути сильными восстановителями, например хлоридом олова(II) в соляной кислоте: v Под действием хлора каломель окисляется с образованием сулемы: q v Дисмутирует на металлическую ртуть и соединения ртути(II): в разбавленных кислотах (медленно) или при нагревании выше 400 °C v в растворе аммиака образуется так называемый белый неплавкий преципитат При температуре возгонки в газовой фазе частично разлагается с образованием хлорида ртути(I):

Применение Hg 2 Сl 2 q Хлорид диртути (+2) используется для изготовления каломельного электрода сравнения, как антисептик, в качестве катализатора, для синтеза ртутьорганических соединений

q. Физические свойства Hg 2 F 2 Фторид диртути (+2) при нормальных условиях — твёрдое вещество светло жёлтого цвета малорастворимое в воде (несколько лучше, чем Хлорид диртути (+2)). Плавится без разложения при 570 °C. Не образует кристаллогидратов. q Получение: v Фторид диртути(2+) может быть получен путём реакций ионного обмена, например осаждением фторидом калия из раствора нитрата диртути(2+) в разбавленной азотной кислоте:

Химические свойства Hg 2 F 2 v Фторид диртути (2+) легко подвергается дисмутации с образованием металлической ртути и соединений ртути(II) в различных условиях: на свету (медленно) v в горячей воде v в разбавленной соляной кислоте v в концентрированной щёлочи v в растворе аммиака q v Фторид диртути(2+) может быть полностью окислен до соединений ртути(II) различными сильными окислителями, например: концентрированной серной кислотой v газообразным хлором v фторидом нитрозила q

Применение Hg 2 F 2 q Фторид диртути (2+) находит применение при изготовлении электродов сравнения.

q. Физические свойства Hg 2 Br 2 Бромид диртути (2+) при нормальных условиях — твёрдое вещество светло жёлтого цвета нерастворимое в воде, этаноле, ацетоне. Возгоняется при 345 °C. Не образует кристаллогидратов. q Получение Hg 2 Br 2: v взаимодействием бромида ртути(II) и металлической ртути при высокой температуре v с помощью реакций ионного обмена, например осаждением бромидом калия из раствора нитрата диртути(2+) в разбавленной азотной кислоте v анодным растворением ртути в бромомоводородной кислоте на аноде на катоде

Химические свойства Hg 2 Br 2 Бромид диртути (2+) не реагирует с соляной кислотой, щелочами, гидратом аммиака. v с концентрированной азотной кислотой v v с горячей концентрированной серной кислотой v с концентрированным раствором бромида калия v На свету медленно разлагается на бромид ртути(II) и металлическую ртуть:

Применение Hg 2 Br 2 q Бромид диртути (2+) применяют как компонент электролитов при рафинировании металлической ртути, для электрохимических экспериментов, для синтеза ртутьорганических соединений.

q. Физические свойства Hg 2 I 2 Иодид диртути (2+) при нормальных условиях — твёрдое легколетучее вещество жёлтого цвета, нерастворимое в воде этаноле, эфире, растворимое в касторовом масле. Не образует кристаллогидратов. q Получение Hg 2 I 2 v с помощью реакций ионного обмена, например осаждением иодидом калия из раствора нитрата диртути(2+) в разбавленной азотной кислоте v взаимодействием металлической ртути с иодом в этаноле (иодид диртути(2+) выпадает в осадок)

Химические свойства Hg 2 I 2 Иодид диртути (2+) не реагирует с щелочами, раствором аммиака, разбавленными кислотами v с концентрированной азотной кислотой v v с горячей концентрированной серной кислотой v с концентрированным раствором иодида калия v На свету разлагается на иодид ртути(II) и металлическую ртуть:

Применение Hg 2 I 2 q Иодид диртути (2+) применяется при изготовлении люминесцентных ламп (газоразрядный источник света, в котором видимый свет излучается в основном люминофором, который, в свою очередь, светится под воздействием ультрафиолетового излучения разряда)

Физические свойства Hg. Cl 2 q Сулема Hg. Cl 2 – бесцветное кристаллическое вещество, плотность 5, 44 г/см 3, температура плавления 277°С, плохо растворима в воде. q Получение Hg. CI 2 (сулема) – образуется при нагревании смеси сульфата ртути (II) с хлоридом натрия: Hg. SO 4 + 2 Na. Cl = Hg. Cl 2 + Na 2 SO 4 q под действием окислителей соединения легко переходят в производные Hg 2+: Hg 2 Cl 2 + Cl 2 = 2 Hg. Cl 2

q. Комплексные соединения: q v v v Для ртути (II) характерно образование устойчивых комплексных соединений: При растворении солей в воде, при взаимодействии оксида с кислотами образуются устойчивые аквакомплексы типа [Hg(H 2 O)4]2+ Устойчивые аммиакаты получаются при действии избытка водного раствора аммиака на растворы солей в присутствии солей аммония: Hg(NO 3)2 + 4 NH 3 = [Hg(NH 3)4](NO 3)2 Очень прочные цианидные комплексы образуются при действии на растворы солей ртути (II) основного цианида, образующийся в начале осадок Hg(CN)2 растворяется с образованием тетрационoмеркурата (II) калия: Hg(NO 3)2 + 2 KCN = Hg(CN)2 + 2 KNO 3 Hg(CN)2 + 2 KCN = K 2[Hg(CN)4] Устойчивы комплексы ртути (II) с галоген и сульфид ионами. Нерастворимый в воде йодид ртути (II) легко растворяется в йодиде калия с образованием тетрайодомеркурата (II) калия : Hg(NO 3)2 + 2 KI = Hg. I 2 + 2 KNO 3; Hg. I 2 + 2 KI = K 2[Hg. I 4] Киноварь легко растворяется в сульфиде калия, образуя дисульфидомеркурат (II) калия: Hg. S + K 2 S = K 2[Hg. S 2]. Для ртути (I) образование устойчивых комплексных соединений не характерно.

q. Применение ртути и её соединений: q q q Металлическая ртуть используется для изготовления катодов при электрохимическом получении едких щелочей и хлора, в производстве люминесцентных ламп, термометров, барометров, манометров и других измерительных приборов. Каломель применяется для изготовления каломельных электродов в электрохимии и в медицине, в качестве легкого слабительного. Сулема применяется для дезинфекции и для протравливания семян, используется в медицине. Фульмиат ртути (II) – взрывчатое вещество, используется в капсюлях патронов и снарядов в качестве детонаторов. Соли ртути (II) используют в качестве катализаторов в органическом синтезе.
презентация химия.pptx