Элементы V группы.ppt
- Количество слайдов: 18

Элементы главной подгруппы V группы Общая характеристика … 2 S 22 P 3 -3; -2; -1; 0; (+1); (+2); +3; (+4); +5 … 3 S 23 P 3 -3; (-2); 0; (+2); +3; (+4); +5 … 4 S 24 P 3 -3; 0; +3; +5 … 5 S 25 P 3 -3; 0; +3; +5 … 6 S 26 P 3 0; +3; (+5) В скобках – неустойчивые степени окисления
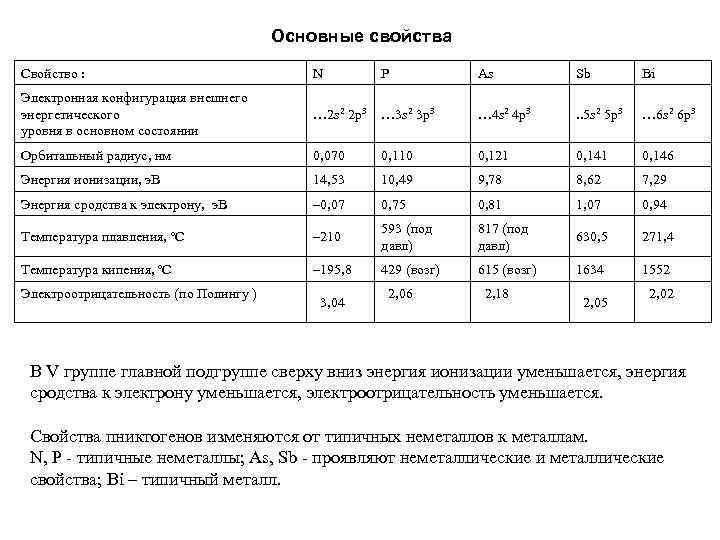
Основные свойства Свойство : N Электронная конфигурация внешнего энергетического уровня в основном состоянии As Sb Bi … 2 s 2 2 p 3 … 3 s 2 3 p 3 … 4 s 2 4 p 3 . . 5 s 2 5 p 3 … 6 s 2 6 p 3 Орбитальный радиус, нм 0, 070 0, 110 0, 121 0, 146 Энергия ионизации, э. В 14, 53 10, 49 9, 78 8, 62 7, 29 Энергия сродства к электрону, э. В – 0, 07 0, 75 0, 81 1, 07 0, 94 Температура плавления, ºС – 210 593 (под давл) 817 (под давл) 630, 5 271, 4 Температура кипения, ºС – 195, 8 429 (возг) 615 (возг) 1634 1552 2, 06 2, 18 Электроотрицательность (по Полингу ) 3, 04 P 2, 05 2, 02 В V группе главной подгруппе сверху вниз энергия ионизации уменьшается, энергия сродства к электрону уменьшается, электроотрицательность уменьшается. Свойства пниктогенов изменяются от типичных неметаллов к металлам. N, P - типичные неметаллы; As, Sb - проявляют неметаллические и металлические свойства; Bi – типичный металл.

Температуры плавления и кипения веществ с ковалентной связью зависят от величины энергии межмолекулярного взаимодействия. С ростом радиуса атомов межмолекулярное взаимодействие усиливается, что приводит к росту температур плавления и кипения от азота до мышьяка. В металлических кристаллах – наоборот, с увеличением радиуса атомов ослабевает межатомное взаимодействие. Понижение температуры плавления в ряду As – Sb – Bi обусловлено увеличением доли металлической связи. Висмут – один из самых легкоплавких металлов. N 2 As P Sb Bi
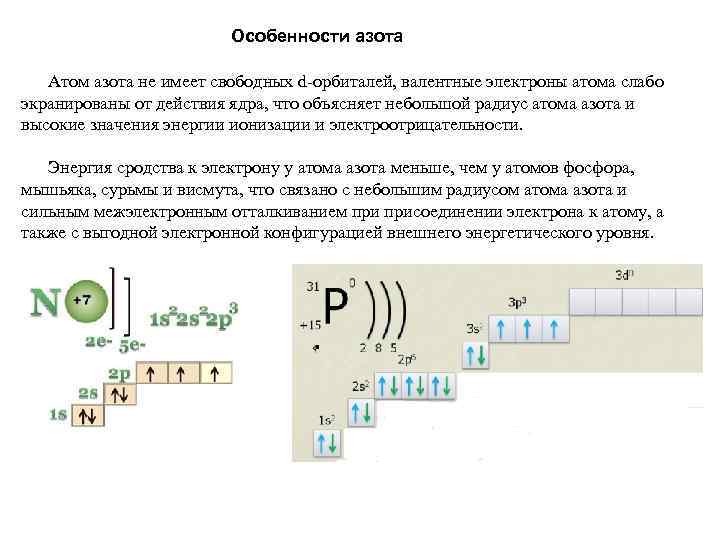
Особенности азота Атом азота не имеет свободных d-орбиталей, валентные электроны атома слабо экранированы от действия ядра, что объясняет небольшой радиус атома азота и высокие значения энергии ионизации и электроотрицательности. Энергия сродства к электрону у атома азота меньше, чем у атомов фосфора, мышьяка, сурьмы и висмута, что связано с небольшим радиусом атома азота и сильным межэлектронным отталкиванием присоединении электрона к атому, а также с выгодной электронной конфигурацией внешнего энергетического уровня.

Характерная валентность N – 3, 4 P, As, Sb, Bi – 3, 4, 5, 6 Азот пятивалентным быть не может – максимальная его валентность равна четырем, т. к. наивысшая валентность равна числу орбиталей на внешнем уровне – у азота их четыре, следовательно, число ковалентных связей тоже четыре. У фосфора и всех последующих элементов подгруппы имеется d-подуровень, куда может промотироваться электрон с s– подуровня, и валентность будет равна пяти. Эти атомы могут также акцептировать электронные пары на пустые d -орбитали, что расширяет их валентные возможности.
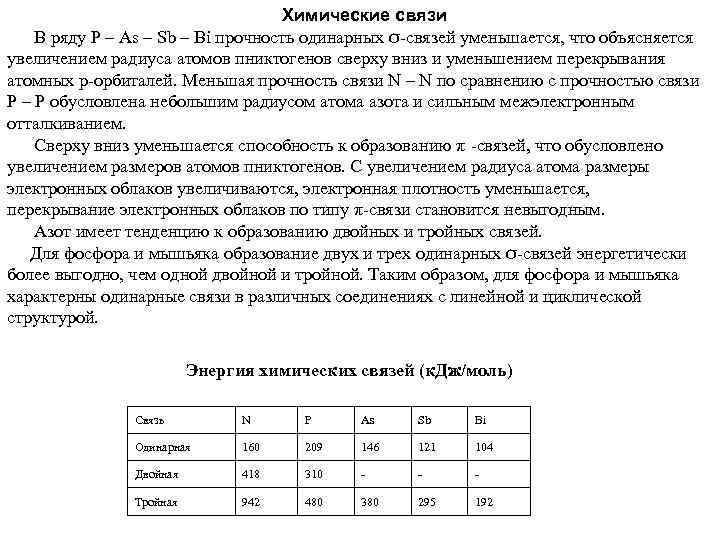
Химические связи В ряду P – As – Sb – Bi прочность одинарных σ-связей уменьшается, что объясняется увеличением радиуса атомов пниктогенов сверху вниз и уменьшением перекрывания атомных р-орбиталей. Меньшая прочность связи N – N по сравнению с прочностью связи Р – Р обусловлена небольшим радиусом атома азота и сильным межэлектронным отталкиванием. Сверху вниз уменьшается способность к образованию π -связей, что обусловлено увеличением размеров атомов пниктогенов. С увеличением радиуса атома размеры электронных облаков увеличиваются, электронная плотность уменьшается, перекрывание электронных облаков по типу π-связи становится невыгодным. Азот имеет тенденцию к образованию двойных и тройных связей. Для фосфора и мышьяка образование двух и трех одинарных σ-связей энергетически более выгодно, чем одной двойной и тройной. Таким образом, для фосфора и мышьяка характерны одинарные связи в различных соединениях с линейной и циклической структурой. Энергия химических связей (к. Дж/моль) Связь N P As Sb Bi Одинарная 160 209 146 121 104 Двойная 418 310 - - - Тройная 942 480 380 295 192
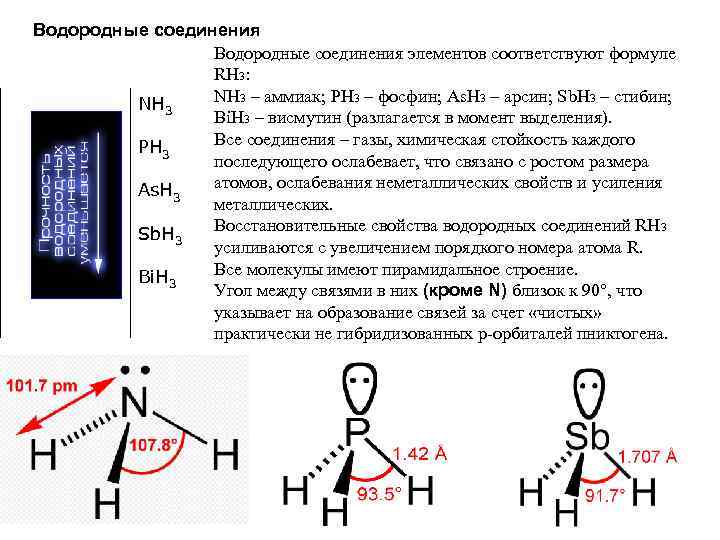
Водородные соединения элементов соответствуют формуле RН 3: NН 3 – аммиак; РН 3 – фосфин; As. Н 3 – арсин; Sb. Н 3 – стибин; NH 3 Bi. Н 3 – висмутин (разлагается в момент выделения). Все соединения – газы, химическая стойкость каждого PH 3 последующего ослабевает, что связано с ростом размера атомов, ослабевания неметаллических свойств и усиления As. H 3 металлических. Восстановительные свойства водородных соединений RH 3 Sb. H 3 усиливаются с увеличением порядкого номера атома R. Все молекулы имеют пирамидальное строение. Bi. H 3 Угол между связями в них (кроме N) близок к 90°, что указывает на образование связей за счет «чистых» практически не гибридизованных р-орбиталей пниктогена.

Характерные оксиды Э 2 O 3 и Э 2 О 5 +3 +5 N 2 O 3 – кислотный P 2 O 3 – слабокислотный N 2 O 5 – кислотный P 2 O 5 – кислотный As 2 O 3 - амфотерный с преобладанием кислотных свойств As 2 O 5 – кислотный Sb 2 O 3 - амфотерный с преобладанием основных свойств Sb 2 O 5 – плохо растворим в воде, слабокислотный Bi 2 O 3 - основный окcид Bi 2 O 5 – нет точных данных о существовании

Проявление вторичной периодичности в главной подгруппе V группы Устойчивость различных степеней окисления и окислительная способность соединений элементов VА группы изменяется сверху вниз немонотонно, это называют вторичной периодичностью. Например, высшая степень окисления +5 наиболее устойчива для фосфора и сурьмы. Вторичная периодичность является следствием действия сразу нескольких факторов: -увеличение размеров атомов (и размеров орбиталей) сверху вниз; - кайносимметрия 2 р-орбитали у азота; - кайносимметрия 3 d-орбитали у мышьяка, и последствия d-сжатия в IV периоде; - 4 d-орбиталь гораздо более объемная, чем 3 d-орбиталь, поэтому сильно экранирует 5 s-электроны, следовательно Sb легко отдает все 5 электронов и для нее устойчива с. о. +5; - в VI периоде появляются 4 f-орбитали, компактные, кайносимметричные; 6 sэлектроны проникают под двойной экран 5 d и 4 f, поэтому степень окисления +5 у висмута трудно реализуется, для него характерна с. о. +3, а висмутаты (+5) – сильные окислители.

Элементы побочной подгруппы V группы Общая характеристика ).
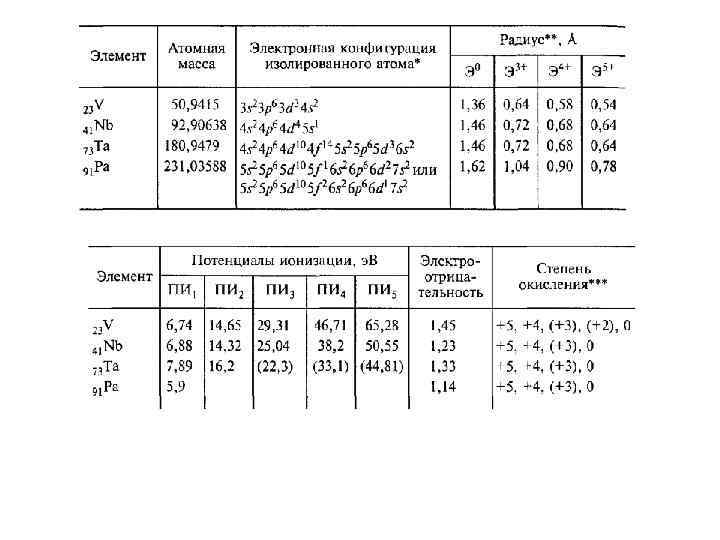


Типичные гомо- и гетероатомные соединения элементов VB-группы


Оксиды Высшие оксиды обладают кислотными свойствами.

Схема кислотно-основного равновесия, иллюстрирующая амфотерность ванадиевой кислоты

Получение металлов из руд Хлорирующий обжиг: V

Разделение смесей ниобия и тантала
Элементы V группы.ppt