 Элементы 5 -А группы Азот и его свойства • Общая характеристика элементов 5 -А группы • Азот • Свойства азота • Соединения азота • Получение и применение азота 1
Элементы 5 -А группы Азот и его свойства • Общая характеристика элементов 5 -А группы • Азот • Свойства азота • Соединения азота • Получение и применение азота 1
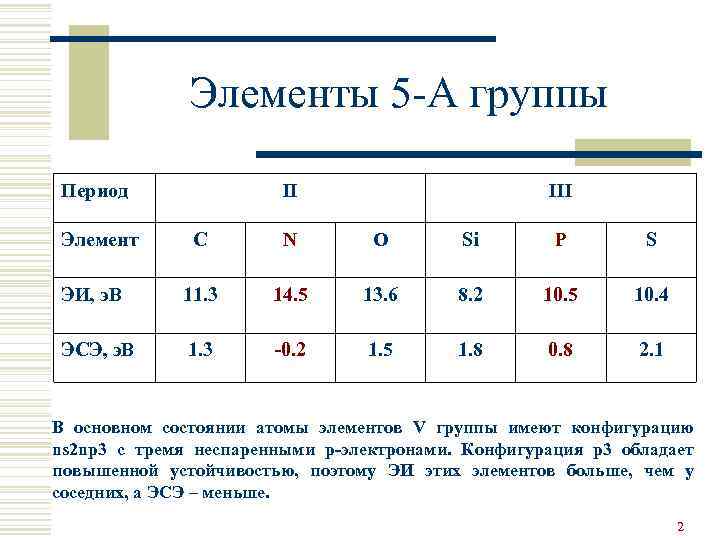 Элементы 5 -А группы Период Элемент II III C N O Si P S ЭИ, э. В 11. 3 14. 5 13. 6 8. 2 10. 5 10. 4 ЭСЭ, э. В 1. 3 -0. 2 1. 5 1. 8 0. 8 2. 1 В основном состоянии атомы элементов V группы имеют конфигурацию ns 2 np 3 с тремя неспаренными р-электронами. Конфигурация р3 обладает повышенной устойчивостью, поэтому ЭИ этих элементов больше, чем у соседних, а ЭСЭ – меньше. 2
Элементы 5 -А группы Период Элемент II III C N O Si P S ЭИ, э. В 11. 3 14. 5 13. 6 8. 2 10. 5 10. 4 ЭСЭ, э. В 1. 3 -0. 2 1. 5 1. 8 0. 8 2. 1 В основном состоянии атомы элементов V группы имеют конфигурацию ns 2 np 3 с тремя неспаренными р-электронами. Конфигурация р3 обладает повышенной устойчивостью, поэтому ЭИ этих элементов больше, чем у соседних, а ЭСЭ – меньше. 2
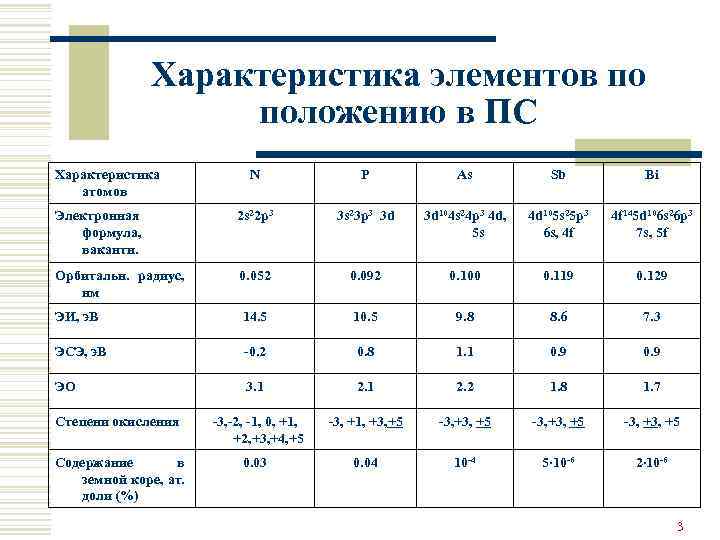 Характеристика элементов по положению в ПС Характеристика атомов N P As Sb Bi Электронная формула, вакантн. 2 s 22 p 3 3 s 23 p 3 3 d 3 d 104 s 24 p 3 4 d, 5 s 4 d 105 s 25 p 3 6 s, 4 f 4 f 145 d 106 s 26 p 3 7 s, 5 f Орбитальн. радиус, нм 0. 052 0. 092 0. 100 0. 119 0. 129 ЭИ, э. В 14. 5 10. 5 9. 8 8. 6 7. 3 ЭСЭ, э. В -0. 2 0. 8 1. 1 0. 9 ЭО 3. 1 2. 2 1. 8 1. 7 Степени окисления ‑ 3, ‑ 2, -1, 0, +1, +2, +3, +4, +5 -3, +1, +3, +5 -3, +5 Содержание в земной коре, ат. доли (%) 0. 03 0. 04 10 -4 5∙ 10 -6 2∙ 10 -6 3
Характеристика элементов по положению в ПС Характеристика атомов N P As Sb Bi Электронная формула, вакантн. 2 s 22 p 3 3 s 23 p 3 3 d 3 d 104 s 24 p 3 4 d, 5 s 4 d 105 s 25 p 3 6 s, 4 f 4 f 145 d 106 s 26 p 3 7 s, 5 f Орбитальн. радиус, нм 0. 052 0. 092 0. 100 0. 119 0. 129 ЭИ, э. В 14. 5 10. 5 9. 8 8. 6 7. 3 ЭСЭ, э. В -0. 2 0. 8 1. 1 0. 9 ЭО 3. 1 2. 2 1. 8 1. 7 Степени окисления ‑ 3, ‑ 2, -1, 0, +1, +2, +3, +4, +5 -3, +1, +3, +5 -3, +5 Содержание в земной коре, ат. доли (%) 0. 03 0. 04 10 -4 5∙ 10 -6 2∙ 10 -6 3
 Азот 4
Азот 4
 Открытие азота w Даниель Резерфорд – 1772 г. w Одновременно: Д. Пристли, Г. Кавендиш w Исследование свойств – А. Л. Лавуазье, раньше Д. Резерфорда w Азот – «безжизненный» w Азот – элемент жизни (В. И. Вернадский) 5
Открытие азота w Даниель Резерфорд – 1772 г. w Одновременно: Д. Пристли, Г. Кавендиш w Исследование свойств – А. Л. Лавуазье, раньше Д. Резерфорда w Азот – «безжизненный» w Азот – элемент жизни (В. И. Вернадский) 5
 Азот в природе w В литосфере – 0, 01%, в атмосфере – 75, 6% w Возникает и сейчас, выделяется с вулканическими газами w 8 изотопов – 12 -19, стабильных – 2, 14 -15 w В свободном состоянии – в атмосфере w В связанном – аммиак – во Вселенной w Появился на Земле, когда кислород стал окислять аммиак: 4 NH 3 + 3 O 2 = 2 N 2 + 6 H 2 O 6
Азот в природе w В литосфере – 0, 01%, в атмосфере – 75, 6% w Возникает и сейчас, выделяется с вулканическими газами w 8 изотопов – 12 -19, стабильных – 2, 14 -15 w В свободном состоянии – в атмосфере w В связанном – аммиак – во Вселенной w Появился на Земле, когда кислород стал окислять аммиак: 4 NH 3 + 3 O 2 = 2 N 2 + 6 H 2 O 6
 Простое вещество w N 2 - газ, бц, бз, бвк, плохо растворим в воде, при 00 С в 1 л воды растворяется 24 мл азота, при резкой смене давления выделяется в виде пузырьков w Молекулярная масса – 28 w tпл = -2100 С – кристаллы, похожие на лед w tкип. = -1950 С – бесцветная жидкость 7
Простое вещество w N 2 - газ, бц, бз, бвк, плохо растворим в воде, при 00 С в 1 л воды растворяется 24 мл азота, при резкой смене давления выделяется в виде пузырьков w Молекулярная масса – 28 w tпл = -2100 С – кристаллы, похожие на лед w tкип. = -1950 С – бесцветная жидкость 7
 Превращения азота w Молекула устойчива, возможно атомарное состояние – 90 -120 км над Землей w Атомарный азот отличается по свойствам, активен w При пропускании разряда – N 3, - золотистый газ, при замерзании – голубой, частицы подобны озону 8
Превращения азота w Молекула устойчива, возможно атомарное состояние – 90 -120 км над Землей w Атомарный азот отличается по свойствам, активен w При пропускании разряда – N 3, - золотистый газ, при замерзании – голубой, частицы подобны озону 8
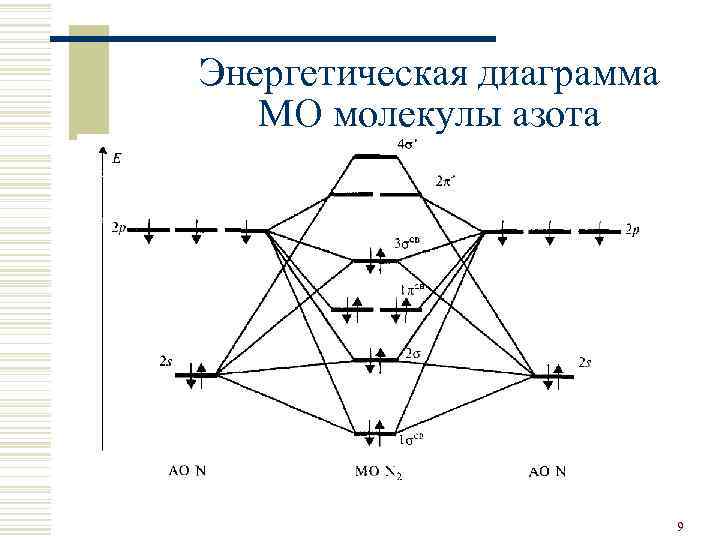 Энергетическая диаграмма МО молекулы азота 9
Энергетическая диаграмма МО молекулы азота 9
 Молекула азота w Связь тройная - 1σ и 2π связи w Молекула прочная, неполярна, термическая диссоциация возможна при 30000 С – 0, 1% w Неспаренные электроны отсутствуют w Молекула линейная w Активирование – перевод в атомарное состояние 10
Молекула азота w Связь тройная - 1σ и 2π связи w Молекула прочная, неполярна, термическая диссоциация возможна при 30000 С – 0, 1% w Неспаренные электроны отсутствуют w Молекула линейная w Активирование – перевод в атомарное состояние 10
 Химические свойства w 1. С металлами при нагревании 3 Mg +N 2 = Mg 3 N 2 – 4500 С 2 Ti + N 2 = 2 Ti. N – 8000 С 2 Al + N 2 = 2 Al. N - 9000 C w 2. С водородом на катализаторе N 2 + 3 H 2 = 2 NH 3 (процесс Боша-Габера) w 3. С кислородом в электрическом разряде N 2 + O 2 = 2 NO w 4. С комплексами переходных металлов [Ru(NH 3)5]Cl 3 + N 2 + Zn/Hg =[Ru(NH 3)5(N 2)]Cl 2 + Zn. Cl 2 + Hg + H 2 O w При обычных условиях: 6 Li + N 2 = 2 Li 3 N 11
Химические свойства w 1. С металлами при нагревании 3 Mg +N 2 = Mg 3 N 2 – 4500 С 2 Ti + N 2 = 2 Ti. N – 8000 С 2 Al + N 2 = 2 Al. N - 9000 C w 2. С водородом на катализаторе N 2 + 3 H 2 = 2 NH 3 (процесс Боша-Габера) w 3. С кислородом в электрическом разряде N 2 + O 2 = 2 NO w 4. С комплексами переходных металлов [Ru(NH 3)5]Cl 3 + N 2 + Zn/Hg =[Ru(NH 3)5(N 2)]Cl 2 + Zn. Cl 2 + Hg + H 2 O w При обычных условиях: 6 Li + N 2 = 2 Li 3 N 11
 С кислородом… w w Ежегодно – три с лишним миллиарда молний Мощность отдельных разрядов – 200 млн. квт Воздух нагревается до 20 тыс. градусов Оксид азота (II) не распадается, быстро охлаждается и доокисляется: 2 NO + O 2 = 2 NO 2 w NO 2 подхватывается атмосферной влагой: 3 NO 2 + Н 2 О = 2 НNO 3 + NО 12
С кислородом… w w Ежегодно – три с лишним миллиарда молний Мощность отдельных разрядов – 200 млн. квт Воздух нагревается до 20 тыс. градусов Оксид азота (II) не распадается, быстро охлаждается и доокисляется: 2 NO + O 2 = 2 NO 2 w NO 2 подхватывается атмосферной влагой: 3 NO 2 + Н 2 О = 2 НNO 3 + NО 12
 Соединения азота w 1. 2. w w w В степени окисления – 3: Гидрид – аммиак NH 3 Нитриды: основные - Nа 3 N + 3 Н 2 О = 3 Nа. ОН + NН 3 амфотерные – Al. N, с водой не реагирует кислотные - Cl 3 N + 3 Н 2 О = 3 НCl. О + NН 3 13
Соединения азота w 1. 2. w w w В степени окисления – 3: Гидрид – аммиак NH 3 Нитриды: основные - Nа 3 N + 3 Н 2 О = 3 Nа. ОН + NН 3 амфотерные – Al. N, с водой не реагирует кислотные - Cl 3 N + 3 Н 2 О = 3 НCl. О + NН 3 13
 Соединения азота w В степени окисления – 2: w w Пернитриды – аналогично пероксидам гидразин, или диамид – N 2 H 4 N 2 H 2 – диимид, неустойчив, имеет производные органических соединений w В степени окисления – 1: w Гидроксиламин - NH 2 ОН ? Азотистоводородная кислота – HN 3 14
Соединения азота w В степени окисления – 2: w w Пернитриды – аналогично пероксидам гидразин, или диамид – N 2 H 4 N 2 H 2 – диимид, неустойчив, имеет производные органических соединений w В степени окисления – 1: w Гидроксиламин - NH 2 ОН ? Азотистоводородная кислота – HN 3 14
 Кислородсодержащие соединения азота w В оксидах реализуются все положительные степени окисления w Некоторым оксидам соответствуют кислоты w Существуют кислородсодержащие ионы азота w Может образовывать кислородсодержащие радикалы w В кислородсодержащих соединениях валентности и степени окисления могут не совпадать 15
Кислородсодержащие соединения азота w В оксидах реализуются все положительные степени окисления w Некоторым оксидам соответствуют кислоты w Существуют кислородсодержащие ионы азота w Может образовывать кислородсодержащие радикалы w В кислородсодержащих соединениях валентности и степени окисления могут не совпадать 15
 Аммиак 16
Аммиак 16
 Гидразин 17
Гидразин 17
 Гидразин 18
Гидразин 18
 Окислительно-восстановительные свойства гидразина Восстановительные свойства: Окислительные свойства: 19
Окислительно-восстановительные свойства гидразина Восстановительные свойства: Окислительные свойства: 19
 Гидроксиламин 20
Гидроксиламин 20
 Окислительно-восстановительные свойства гидроксиламина 21
Окислительно-восстановительные свойства гидроксиламина 21
 Азотистоводородная кислота и азиды 22
Азотистоводородная кислота и азиды 22
 Азиды 23
Азиды 23
 Получение азота w В промышленности – из воздуха w В лаборатории можно получить разложением нитрида натрия и нитрита аммония: w 2 Nа 3 N = 6 Nа + N 2 w NH 4 NО 2 = N 2 + 2 Н 2 О 24
Получение азота w В промышленности – из воздуха w В лаборатории можно получить разложением нитрида натрия и нитрита аммония: w 2 Nа 3 N = 6 Nа + N 2 w NH 4 NО 2 = N 2 + 2 Н 2 О 24
 Применение азота w Создание инертной атмосферы w Синтез аммиака w Охлаждение w Аммиак – производство азотной кислоты и органический синтез w Гидразин - растворитель 25
Применение азота w Создание инертной атмосферы w Синтез аммиака w Охлаждение w Аммиак – производство азотной кислоты и органический синтез w Гидразин - растворитель 25
 Спасибо за внимание! 26
Спасибо за внимание! 26


