медь.pptx
- Количество слайдов: 15

Элементы 1 Б группы: медь, серебро, золото. Сопоставление электронных конфигураций, величин радиусов, энергии ионизации, характерных степеней окисления и координационных чисел атомов элементов I A и I Б групп. Физические, химические свойства, получение и применение простых веществ. Сопоставление строения и свойств однотипных соединений (оксиды, гидроксиды, галогениды) элементов I A и I Б групп со степенями окисления (I). Особенности соединений Cu (II). Комплексные соединения (аммиакаты, цианиды, галогениды): координационные числа, зависимость формы координационного полиэдра от электронной конфигурации центрального атома и природы лиганда. Строение и свойства соединений элементов Сu, Ag, Аu в высших степенях окисления. Высокотемпературные сверхпроводники на основе сложных оксидов меди.

Характеристика элементов IБ группы. ●Сравнительно малая химическая активность элементов подгруппы меди объясняется двумя причинами: Во-первых, ярко выраженным в их атомах эффектом проникновения s-электронов внутрь непосредственно подстилающих (n-1)d-оболочек. Во-вторых, в результате d-контракции и совместной d- и fконтракций(золото) радиусы их атомов значительно меньше радиусов атомов щелочных металлов R(K)>R(Cu) R(Rb)>R(Ag) R(Cs)>R(Au). ●В результате металлы подгруппы меди характеризуются несравненно большими значениями первого ионизационного потенциала, ОЭО, сродства к электрону, чем щелочные металлы.

Cu-медь. Общая характеристика. ●Элемент медь расположен в IV периоде и IБ группе, атомный номер 29, относительная атомная масса 63, 546. ●Электронная конфигурация меди в основном состоянии 1 s 22 p 63 s 23 p 63 d 104 s 1 ( в атоме меди наблюдается «проскок» электрона с 4 s-подуровня на 3 dподуровень ). ●Следовательно, в атоме меди третий энергетический уровень полностью заполнен электронами. Поскольку в степени окисления +2 медь имеет не полностью заполненный энергетический 3 d-подуровень( 3 d 9), она, подобно железу и хрому, относится к семейству dэлементов.
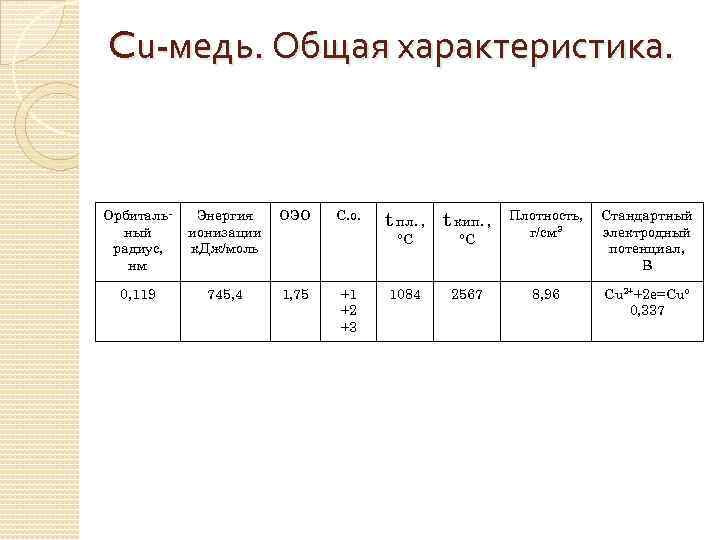
Cu-медь. Общая характеристика. Орбитальный радиус, нм Энергия ионизации к. Дж/моль ОЭО 0, 119 745, 4 1, 75 С. о. t пл. , t кип. , °С +1 +2 +3 °С 1084 2567 Плотность, г/см 3 Стандартный электродный потенциал, В 8, 96 Cu 2++2 e=Cu° 0, 337

Cu-медь. Общая характеристика. ●В природе медь встречается в виде соединений(чаще): Cu 2 S - медный блеск, Cu. Fe. S 2 - медный колчедан, Cu 2 O - куприт, Cu 2(OH)2 CO 3 - малахит, и в виде простого вещества( самородная медь).

Физические свойства меди. ●Простое вещество медь – металл красного цвета, ковкий, обладает прекрасной тепло- и электропроводностью ( уступает серебру), малая твердость, но легко устраняется добавлением других металлов. Медь относится к группе тяжелых тугоплавких металлов. ●Кристаллическая медь имеет кубическую гранецентрированную решетку. ●Химическая активность меди не велика. В ряду стандартных электродных потенциалов медь расположена за водородом, поэтому наиболее эффективно медь окисляется не водородом, а анионом кислот-окислителей (HNO 3 , H 2 SO 4(конц. )). Разбавленные растворы кислотнеокислителей, щелочей(в отсутствие окислителей) на медь не действуют.

Физические свойства меди. ●Вследствие окисления на воздухе в присутствии углекислого газа медные изделия со временем покрываются зеленым налетом карбоната гидроксомеди (II) (Cu. OH)2 CO 3.

Химические свойства меди. ●При температуре красного каления медь реагирует с кислородом с образованием оксида меди (II), а при более высокой температуре –оксид меди(I). 2 Cu + O 2 = 2 Cu. O (черный) - оксид меди (II) 4 Cu + O 2 = 2 Cu 2 O (красный) - оксид меди(I) ●С галогенами медь реагирует при нагревании, во всех случаях кроме йода образуются галогениды меди (II). Cu + Cl 2 = Cu. Cl 2 2 Cu + I 2 = 2 Cu. I ●При нагревании медь реагирует с серой, состав продукта зависит от температуры, как в случае с кислородом. Cu + S = Cu. S (сульфид меди (II)) 2 Cu + S = Cu 2 S (сульфид меди(I)) ●C азотом, водородом, углеродом медь не реагирует. ●С фосфором и кремнием реагирует при нагревании. 2 Cu + P = Cu 2 P ( а также Сu 3 P 2, Cu 3 P) 2 Cu + Si = Cu 2 Si ( а также соединения другого состава)

Химические свойства меди. ●Медь хорошо растворяется в азотной и серной концентрированной кислотах. Cu + 4 HNO 3(>60%) = Cu(NO 3)3 + 2 NO 2 + 2 H 2 O ( t° ) 3 Cu + 8 HNO 3(40%) = 3 Cu(NO 3)3 + 2 NO + 4 H 2 O ( t° ) Cu + 2 H 2 SO 4(конц. ) = Cu. SO 4 + SO 2 + 2 H 2 O ●C разбавленными галогеноводородными кислотами медь не реагирует, однако растворяется в их концентрированных растворах. 2 Cu + 4 HCl(конц. ) = H 2 + 2 H[Cu. Cl 2] (дихлорокупрат (I) водорода) ●При нагревании медь реагирует с сероводородом. 2 Сu + H 2 S = Cu 2 S + H 2 ●При обычной температуре медь окисляется оксидом азота(IV), а при нагревании оксидом азота (II). 2 Cu + NO 2 = Cu 2 O + NO 4 Cu + 2 NO = Cu 2 O + N 2 ●Нагретая до красного каления, медь реагирует с аммиаком, образуя нитриды меди (I). 6 Cu + 2 NH 3 = 2 Cu 3 N + 3 H 2

Химические свойства меди. ●Медь вытесняет менее активные металлы из водных растворов солей. Cu + 2 Ag. NO 3 = Cu(NO 3)2 + 2 Ag ●В растворимое состояние медь можно перевести с помощью водного раствора Fe. Cl 3, поскольку ионы Fe 3+ окисляют металлическую медь. Cu + 2 Fe. Cl 3 = Cu. Cl 2 + 2 Fe. Cl 2 ●В присутствии кислорода медь растворяется в конц. водных растворах аммиака с образованием ярко-синего тетраамминового комплекса. 2 Cu + 8 NH 3· H 2 O + O 2 = 6 H 2 O + 2[Cu(NH 3)4](OH)2 (гидроксид тетрааммин меди (II))

Получение меди. ●В промышленности медь чаще всего получают из сульфидных руд, в которых содержание меди невелико. С этой целью руду флотацией и обжигом вначале обогащают, а затем сплавляют окисленную медь с сульфидом меди (I). Cu 2 S + 2 Cu 2 O = 6 Cu + SO 2 Полученную таким образом медь подвергают очистке методом электролиза. ●Медные руды растворяют в разбавленных растворах аммиака, Fe 2(SO 4)3 или H 2 SO 4. Cu 2 S + 2 Fe 2(SO 4)3 = 4 Fe. SO 4 + 2 Cu. SO 4 + S Из полученных растворов медь выделяют электролизом или вытесняют железом Cu. SO 4 + Fe = Cu + Fe. SO 4 В процессе электролиза анод растворяется Сu° - 2 e = Cu 2+ и медь оседает на катоде Cu 2+ +2 e = Cu° таким способом получают медь высокой степени чистоты.

Применение меди. ●В следствие высокой тепло- и электропроводности медь в больших количествах используется для изготовления электрических проводов, кабелей, котлов, перегонных кубов и т. д. ●Самое разнообразное применение находят сплавы меди. Латунь(содержит до 45% цинка) используется для изготовления радиаторов, деталей часовых механизмов, в судостроении. Медноникелевые сплавы применяются в энергетической промышленности, судостроении, для изготовления термопар. Основное назначение бронзы(содержит олово и алюминий) – изготовление колов и статуй. Cu 2 O – в качестве выпрямителя переменного тока. Cu. O – как окислитель в лабораторной технике, в производстве стекла и эмалей, как зеленый и синий краситель. Cu. SO 4 – как осушитель. Cu. SO 4 · 5 H 2 O – для борьбы с вредителями с/х, при пропитке древесины для предотвращения гниения. (Cu. OH)2 CO 3 – для изготовления синих и зеленых красок, как поделочный камень( в виде малахита).

Cu 2 O ●Твердое вещество красного цвета, в природе встречается в виде минерала куприта. ●Оксид практически не растворим в воде, обладает слабовыраженными амфотерными свойствами( преобладают основные), растворяется в кислотах и концентрированных растворах щелочей при нагревании. Cu 2 O + 4 HCl = 2 H[Cu. Cl 2] + H 2 O Cu 2 O + H 2 SO 4 = Cu. SO 4 + H 2 O + Cu Cu 2 O + 2 Na. OH(конц. ) + H 2 O = 2 Na[Cu(OH)2] (дигидроксокупрат(I) натрия) ●Оксид хорошо растворяется в водных растворах аммиака с образованием комплексных соединений (аммиакатов), координационное число Cu равно 2. Cu 2 O + 4 NH 3 + H 2 O = 2[Cu(NH 3)2]OH (гидроксид диаммин меди (I)) ●Cu 2 O + H 2 = 2 Cu + H 2 O (t°) ●Cu 2 O + CO = 2 Cu + CO 2 (t°) ● 2 Cu 2 O + 2 Al = 6 Cu + Al 2 O 3 (t°) ● 2 Cu 2 O + O 2 = 4 Cu. O (t°) ● 2 Cu 2 O = 4 Cu + O 2 (t°) ●Cu 2 O можно получить, обрабатывая при слабом нагревании глюкозу свежеполученным гидроксидом меди(II). 2 Сu(OH)2+C 6 H 12 O 6=CH 2 OH-(CHOH)4 -COOH+Cu 2 O +2 H 2 O (t°)

Cu. O ●Твердое вещество черного цвета, плохо растворяется в воде, встречается в природе в виде минерала мелаконита. ●Оксид обладает слабовыраженными амфотерными свойствами( преобладают основные), хорошо растворяется в кислотах, а в щелочах только при сплавлении. Cu. O + H 2 SO 4 (разб. ) = Cu. SO 4 + H 2 O (t°) Cu. O + 2 KOH = H 2 O + K 2 Cu. O 2 (купрат калия) (t°) ●Оксид образует комплексные соединения, координационное число 4. Cu. O + 4 NH 3 + H 2 O = [Cu(NH 3)4](OH)2 ( гидроксид тетрааммин меди (II)) ●Cu. O + CO = Cu + CO 2 (t°) ●Cu. O + C = Cu + CO (t°) ● 4 Cu. O = 2 Cu 2 O + O 2 (t°) ●Получение при нагревании 2 Сu+O 2=2 Cu. O Cu(OH)2=Cu. O+H 2 O 2 Cu(NO 3)2=2 Cu. O+4 NO 2 +O 2

медь.pptx