 Елементи V-А групи Лекція № 3 курсу «Загальна та неорганічна хімія»
Елементи V-А групи Лекція № 3 курсу «Загальна та неорганічна хімія»
 Нітроген N, Фосфор Р, Арсен As, Стибій Sb, Бісмут Ві
Нітроген N, Фосфор Р, Арсен As, Стибій Sb, Бісмут Ві

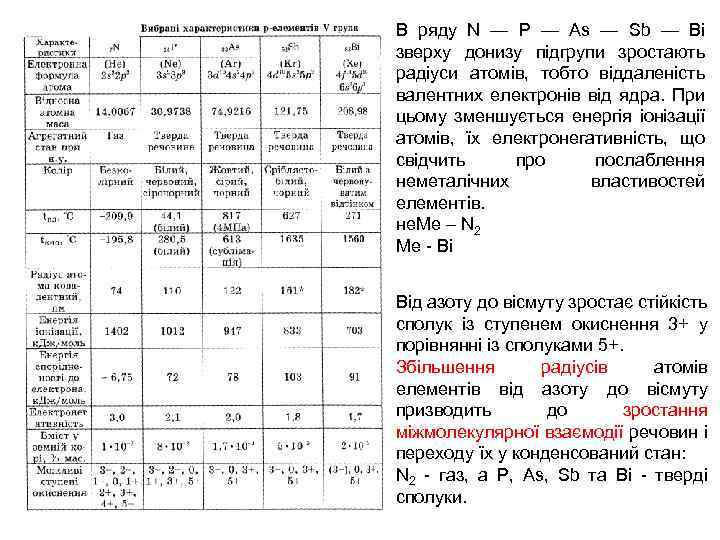 В ряду N — Р — Аs — Sb — Ві зверху донизу підгрупи зростають радіуси атомів, тобто віддаленість валентних електронів від ядра. При цьому зменшується енергія іонізації атомів, їх електронегативність, що свідчить про послаблення неметалічних властивостей елементів. не. Ме – N 2 Ме - Bi Від азоту до вісмуту зростає стійкість сполук із ступенем окиснення 3+ у порівнянні із сполуками 5+. Збільшення радіусів атомів елементів від азоту до вісмуту призводить до зростання міжмолекулярної взаємодії речовин і переходу їх у конденсований стан: N 2 - газ, а Р, Аs, Sb та Ві - тверді сполуки.
В ряду N — Р — Аs — Sb — Ві зверху донизу підгрупи зростають радіуси атомів, тобто віддаленість валентних електронів від ядра. При цьому зменшується енергія іонізації атомів, їх електронегативність, що свідчить про послаблення неметалічних властивостей елементів. не. Ме – N 2 Ме - Bi Від азоту до вісмуту зростає стійкість сполук із ступенем окиснення 3+ у порівнянні із сполуками 5+. Збільшення радіусів атомів елементів від азоту до вісмуту призводить до зростання міжмолекулярної взаємодії речовин і переходу їх у конденсований стан: N 2 - газ, а Р, Аs, Sb та Ві - тверді сполуки.
 Поширення та роль елементів V-А групи у природі Азот - в біосфері знаходиться у вільному стані (повітря), а також у складі великої кількості неорганічних і органічних сполук. Природні родовища мінеральних сполук азоту представлені нітратами — Nа. NO 3 (чилійська селітра) та КNО 3 (індійська селітра). Фосфор належить до поширених у природі хімічних елементів. Внаслідок своєї високої хімічної активності у вільному стані не зустрічається. Входить до складу близько двохсот мінералів:
Поширення та роль елементів V-А групи у природі Азот - в біосфері знаходиться у вільному стані (повітря), а також у складі великої кількості неорганічних і органічних сполук. Природні родовища мінеральних сполук азоту представлені нітратами — Nа. NO 3 (чилійська селітра) та КNО 3 (індійська селітра). Фосфор належить до поширених у природі хімічних елементів. Внаслідок своєї високої хімічної активності у вільному стані не зустрічається. Входить до складу близько двохсот мінералів:
 Миш'як (арсен), сурма (стибій) і вісмут (бісмут) мало поширені у природі і знаходяться в земній корі майже виключно в окис-неному стані, у вигляді сульфідів. Лише вісмут інколи зустрічається у вільному стані. Однак незважаючи на незначний вміст цих елементів в земній корі, арсен входить до складу більш як 200 мінералів, стибій — 100, вісмут — 70 мінералів. Основне промислове значення мають: арсенопірит Fе. Аs. S, головний компонент миш'якового колчедану; стибніт Sb 2 S 3 (антимоніт), основа сурмяного блиску; бісмутиніт Ві 2 S 3, основа вісмутового блиску.
Миш'як (арсен), сурма (стибій) і вісмут (бісмут) мало поширені у природі і знаходяться в земній корі майже виключно в окис-неному стані, у вигляді сульфідів. Лише вісмут інколи зустрічається у вільному стані. Однак незважаючи на незначний вміст цих елементів в земній корі, арсен входить до складу більш як 200 мінералів, стибій — 100, вісмут — 70 мінералів. Основне промислове значення мають: арсенопірит Fе. Аs. S, головний компонент миш'якового колчедану; стибніт Sb 2 S 3 (антимоніт), основа сурмяного блиску; бісмутиніт Ві 2 S 3, основа вісмутового блиску.
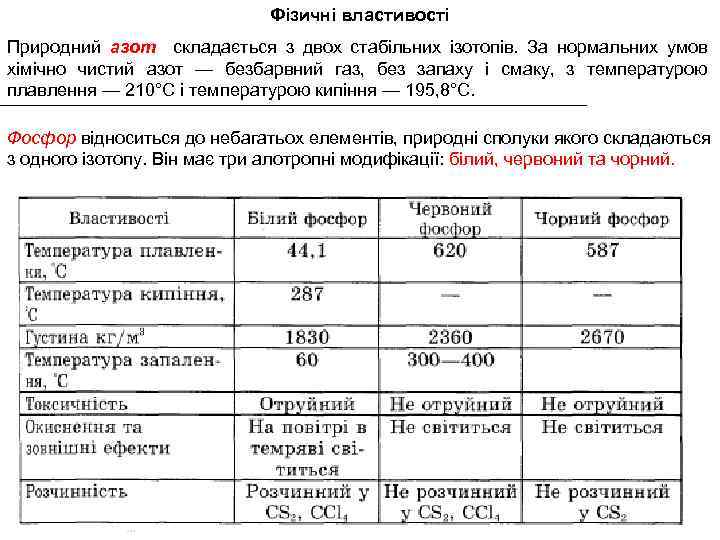 Фізичні властивості Природний азот складається з двох стабільних ізотопів. За нормальних умов хімічно чистий азот — безбарвний газ, без запаху і смаку, з температурою плавлення — 210°С і температурою кипіння — 195, 8°С. Фосфор відноситься до небагатьох елементів, природні сполуки якого складаються з одного ізотопу. Він має три алотропні модифікації: білий, червоний та чорний.
Фізичні властивості Природний азот складається з двох стабільних ізотопів. За нормальних умов хімічно чистий азот — безбарвний газ, без запаху і смаку, з температурою плавлення — 210°С і температурою кипіння — 195, 8°С. Фосфор відноситься до небагатьох елементів, природні сполуки якого складаються з одного ізотопу. Він має три алотропні модифікації: білий, червоний та чорний.
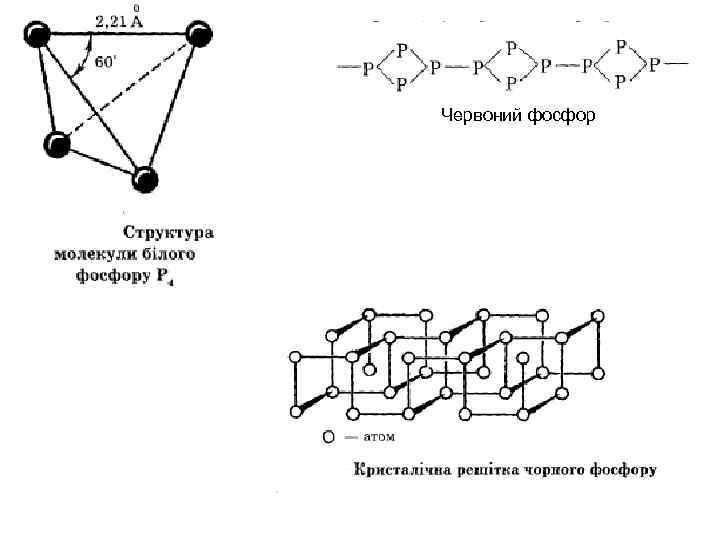 Червоний фосфор
Червоний фосфор
 Арсен і вісмут у природі є моноізотопними елементами Арсен має декілька алотропних модифікацій. Його пара безбарвна, до температури 800°С містить молекули As 4, в інтервалі 800 — 1700°С — суміш молекул As 4 та As 2, понад 1700°С — тільки молекули As 2. Жовтий миш'як As 4 — прозорі м'які кристали. Жовтий миш'як ізоморфний білому фосфору. Мало стійкий, під дією світла або слабкого нагрівання легко переходить у металічну модифікацію — сірий миш'як. Сірий миш'як - має металічну електропровідність, яка складає близько 4% електропровідності срібла. При сублімації в струмені водню утворюється чорний миш'як він стійкий, не окиснюється на повітрі; за температури понад 270 С переходить у сірий миш'як.
Арсен і вісмут у природі є моноізотопними елементами Арсен має декілька алотропних модифікацій. Його пара безбарвна, до температури 800°С містить молекули As 4, в інтервалі 800 — 1700°С — суміш молекул As 4 та As 2, понад 1700°С — тільки молекули As 2. Жовтий миш'як As 4 — прозорі м'які кристали. Жовтий миш'як ізоморфний білому фосфору. Мало стійкий, під дією світла або слабкого нагрівання легко переходить у металічну модифікацію — сірий миш'як. Сірий миш'як - має металічну електропровідність, яка складає близько 4% електропровідності срібла. При сублімації в струмені водню утворюється чорний миш'як він стійкий, не окиснюється на повітрі; за температури понад 270 С переходить у сірий миш'як.
 Основні способи одержання елементів р-елементів V групи N 2 Промислове одержання азоту засновано на ректифікації зрідженого повітря, яке практично складається з двох компонентів: азоту — 78, 2% і кисню — 21, 0%. Оскільки азот має нижчу температуру зрідження (-195, 8 °С), ніж кисень (-183, 0 °С), то при нагріванні рідкого повітря у газоподібний стан спочатку переходить азот, а кисень залишається рідким. У лабораторних умовах невеликі кількості азоту можна одержати трьома способами. 1. Розкладанням суміші нітриту натрію з хлоридом амонію (фактично нітриту амонію): 2. Розкладанням дихромату амонію: 3. Термічним окисненням аміаку оксидом міді (II):
Основні способи одержання елементів р-елементів V групи N 2 Промислове одержання азоту засновано на ректифікації зрідженого повітря, яке практично складається з двох компонентів: азоту — 78, 2% і кисню — 21, 0%. Оскільки азот має нижчу температуру зрідження (-195, 8 °С), ніж кисень (-183, 0 °С), то при нагріванні рідкого повітря у газоподібний стан спочатку переходить азот, а кисень залишається рідким. У лабораторних умовах невеликі кількості азоту можна одержати трьома способами. 1. Розкладанням суміші нітриту натрію з хлоридом амонію (фактично нітриту амонію): 2. Розкладанням дихромату амонію: 3. Термічним окисненням аміаку оксидом міді (II):
 Фосфор одержують із апатиту або фосфориту. Пару фосфору конденсують при різкому охолодженні водою у вигляді білого фосфору. Наведена технологія одержання фосфору на сьогоднішній день є загальноприйнятою у хімічній промисловості всіх країн світу. Арсен одержують відновленням As 2 O 3, який утворюється внаслідок окиснюючого випалу руд деревним вугіллям або коксом: Термічним розкладом арсенопіриту: Способи одержання стибію та бісмуту подібні до вищенаведеного:
Фосфор одержують із апатиту або фосфориту. Пару фосфору конденсують при різкому охолодженні водою у вигляді білого фосфору. Наведена технологія одержання фосфору на сьогоднішній день є загальноприйнятою у хімічній промисловості всіх країн світу. Арсен одержують відновленням As 2 O 3, який утворюється внаслідок окиснюючого випалу руд деревним вугіллям або коксом: Термічним розкладом арсенопіриту: Способи одержання стибію та бісмуту подібні до вищенаведеного:
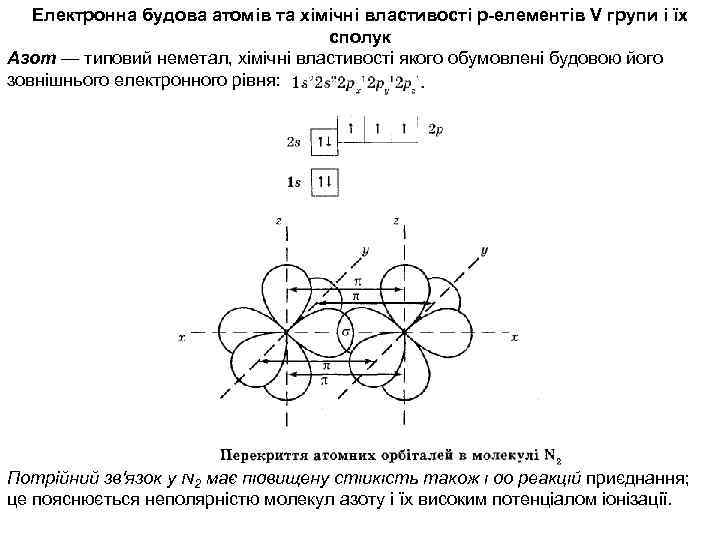 Електронна будова атомів та хімічні властивості р-елементів V групи і їх сполук Азот — типовий неметал, хімічні властивості якого обумовлені будовою його зовнішнього електронного рівня: Потрійний зв'язок у N 2 має підвищену стійкість також і до реакцій приєднання; це пояснюється неполярністю молекул азоту і їх високим потенціалом іонізації.
Електронна будова атомів та хімічні властивості р-елементів V групи і їх сполук Азот — типовий неметал, хімічні властивості якого обумовлені будовою його зовнішнього електронного рівня: Потрійний зв'язок у N 2 має підвищену стійкість також і до реакцій приєднання; це пояснюється неполярністю молекул азоту і їх високим потенціалом іонізації.
 Хімічні властивості При звичайних умовах азот взаємодіє тільки з літієм і не реагує з жодним іншим металом або неметалом: За високих температур, у присутності каталізаторів активність азоту зростає і він може виявляти як окиснюючі, так і відновлюючі властивості (останні тільки по відношенню до фтору і кисню). Найвища активність азоту досягається у плазмі електричного розряду.
Хімічні властивості При звичайних умовах азот взаємодіє тільки з літієм і не реагує з жодним іншим металом або неметалом: За високих температур, у присутності каталізаторів активність азоту зростає і він може виявляти як окиснюючі, так і відновлюючі властивості (останні тільки по відношенню до фтору і кисню). Найвища активність азоту досягається у плазмі електричного розряду.
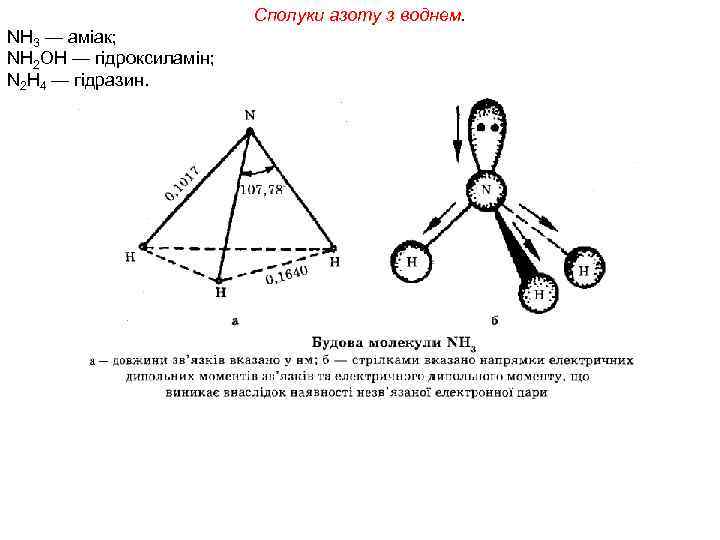 Сполуки азоту з воднем. NH 3 — аміак; NH 2 OH — гідроксиламін; N 2 H 4 — гідразин.
Сполуки азоту з воднем. NH 3 — аміак; NH 2 OH — гідроксиламін; N 2 H 4 — гідразин.
 Аміак — безбарвний газ з характерним різким запахом у два рази легший за повітря. При температурі - 33°С зріджується, а при - 78°С переходить у твердий стан. Аміак добре розчиняється у воді: в одному об'ємі води при 0°С розчиняється 1200 об'ємів аміаку, а при 20°С — 700 об'ємів. Концентрований розчин містить 25 мас. % NH 3. У медицині та ветеринарії застосовують 10% розчин аміаку під назвою нашатирний спирт.
Аміак — безбарвний газ з характерним різким запахом у два рази легший за повітря. При температурі - 33°С зріджується, а при - 78°С переходить у твердий стан. Аміак добре розчиняється у воді: в одному об'ємі води при 0°С розчиняється 1200 об'ємів аміаку, а при 20°С — 700 об'ємів. Концентрований розчин містить 25 мас. % NH 3. У медицині та ветеринарії застосовують 10% розчин аміаку під назвою нашатирний спирт.
 Одержання аміаку На початку XX ст. майже одночасно було розроблено два промислових способи фіксації атмосферного азоту — синтезу аміаку. 1. Ціанамідний спосіб (1904 р. ) заснований на взаємодії, при 1000°С, карбіду кальцію з азотом, і наступним розкладанням ціанаміду кальцію водяною парою: 2 2. У 1913 p. було впроваджено метод прямого синтезу аміаку із азоту і водню (Ф. Габер, Німеччина): У лабораторних умовах аміак одержують шляхом нагрівання солей амонію із лугами:
Одержання аміаку На початку XX ст. майже одночасно було розроблено два промислових способи фіксації атмосферного азоту — синтезу аміаку. 1. Ціанамідний спосіб (1904 р. ) заснований на взаємодії, при 1000°С, карбіду кальцію з азотом, і наступним розкладанням ціанаміду кальцію водяною парою: 2 2. У 1913 p. було впроваджено метод прямого синтезу аміаку із азоту і водню (Ф. Габер, Німеччина): У лабораторних умовах аміак одержують шляхом нагрівання солей амонію із лугами:
 Хімічні властивості аміаку. Для аміаку характерні реакції трьох типів — приєднання, заміщення і окиснення. 1. Найбільш характерні для аміаку реакції приєднання До реакцій приєднання аміаку можна також віднести реакції комплексоутворення, у яких функції лігандів виконують молекули аміаку:
Хімічні властивості аміаку. Для аміаку характерні реакції трьох типів — приєднання, заміщення і окиснення. 1. Найбільш характерні для аміаку реакції приєднання До реакцій приєднання аміаку можна також віднести реакції комплексоутворення, у яких функції лігандів виконують молекули аміаку:
 2. В молекулі аміаку атоми водню здатні заміщуватися на метал. Якщо заміщується один атом водню утворюється сполука, яка має назву амід: Аміак, як протонний розчинник Якщо в молекулі аміаку заміщується два атома водню на метал утворюється сполука, що має назву імід: При заміщенні трьох атомів водню в аміаку на метал утворюються сполуки, які називаються нітридами. Нітриди утворюються при прожарюванні амідів: Аміди, іміди та нітриди лужних і лужноземельних металів — активно гідролізують Сильний окисник N+3
2. В молекулі аміаку атоми водню здатні заміщуватися на метал. Якщо заміщується один атом водню утворюється сполука, яка має назву амід: Аміак, як протонний розчинник Якщо в молекулі аміаку заміщується два атома водню на метал утворюється сполука, що має назву імід: При заміщенні трьох атомів водню в аміаку на метал утворюються сполуки, які називаються нітридами. Нітриди утворюються при прожарюванні амідів: Аміди, іміди та нітриди лужних і лужноземельних металів — активно гідролізують Сильний окисник N+3
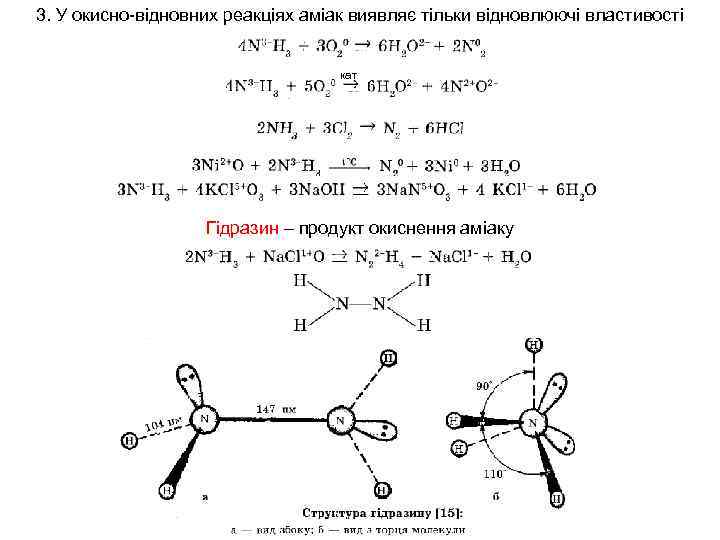 3. У окисно-відновних реакціях аміак виявляє тільки відновлюючі властивості кат Гідразин – продукт окиснення аміаку
3. У окисно-відновних реакціях аміак виявляє тільки відновлюючі властивості кат Гідразин – продукт окиснення аміаку
 Гідразин - проявляє відновні властивості
Гідразин - проявляє відновні властивості
 Гідразин Слабка двоосновна основа
Гідразин Слабка двоосновна основа
 Гдроксиламін Добування Проявляє як відновні так і окисні властивості
Гдроксиламін Добування Проявляє як відновні так і окисні властивості
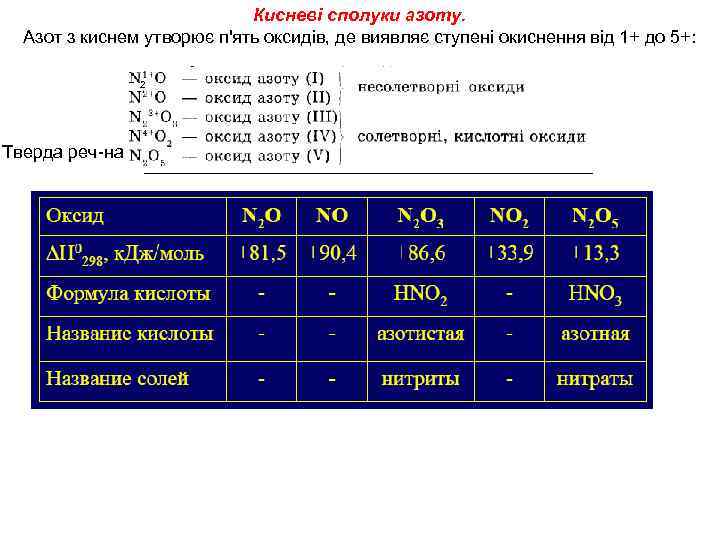 Кисневі сполуки азоту. Азот з киснем утворює п'ять оксидів, де виявляє ступені окиснення від 1+ до 5+: 2 Тверда реч-на
Кисневі сполуки азоту. Азот з киснем утворює п'ять оксидів, де виявляє ступені окиснення від 1+ до 5+: 2 Тверда реч-на
 Оксид азоту (І). Електронна будова молекули N 2 О: Одержання Властивості При температурі вище 700°С оксид азоту (І) розкладається на окремі елементи:
Оксид азоту (І). Електронна будова молекули N 2 О: Одержання Властивості При температурі вище 700°С оксид азоту (І) розкладається на окремі елементи:
 Оксид азоту (II). Електронна будова NO — єдиний з усіх оксидів азоту, який можна одержати безпосередньо з елементів в електричних розрядах або при нагріванні суміші азоту і кисню до температур 2500— 3000°С: Одержання розв. к-а Властивості Проявляє як відновні так і окисні властивості
Оксид азоту (II). Електронна будова NO — єдиний з усіх оксидів азоту, який можна одержати безпосередньо з елементів в електричних розрядах або при нагріванні суміші азоту і кисню до температур 2500— 3000°С: Одержання розв. к-а Властивості Проявляє як відновні так і окисні властивості
 Наявність неподілених пар електронів біля атомів азоту і кисню у молекулі NО надає їй електронно-донорних властивостей. Оксид азоту (III). Електронна будова Добування Властивості Азотиста кислота слабка (К = 4 • 10 -5), існує лише у розведених розчинах при низьких температурах. Солі азотистої кислоти — нітрити більш стійкі і за звичайних умов існують у кристалічному вигляді (KNО 2, Na. NО 2).
Наявність неподілених пар електронів біля атомів азоту і кисню у молекулі NО надає їй електронно-донорних властивостей. Оксид азоту (III). Електронна будова Добування Властивості Азотиста кислота слабка (К = 4 • 10 -5), існує лише у розведених розчинах при низьких температурах. Солі азотистої кислоти — нітрити більш стійкі і за звичайних умов існують у кристалічному вигляді (KNО 2, Na. NО 2).
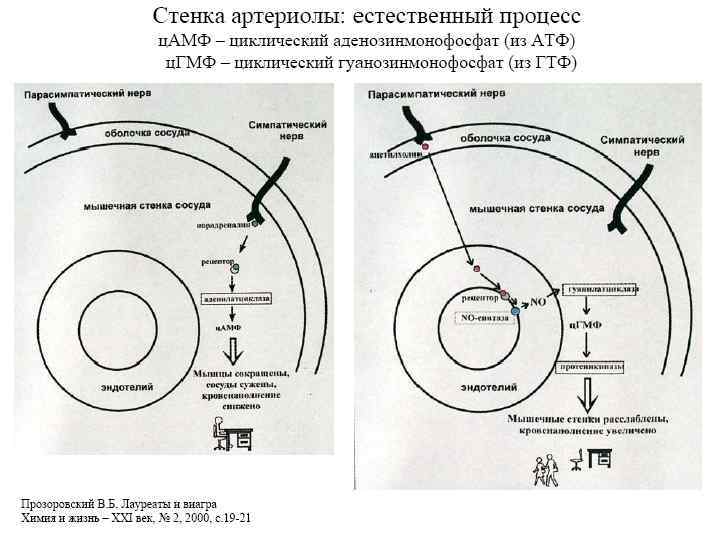
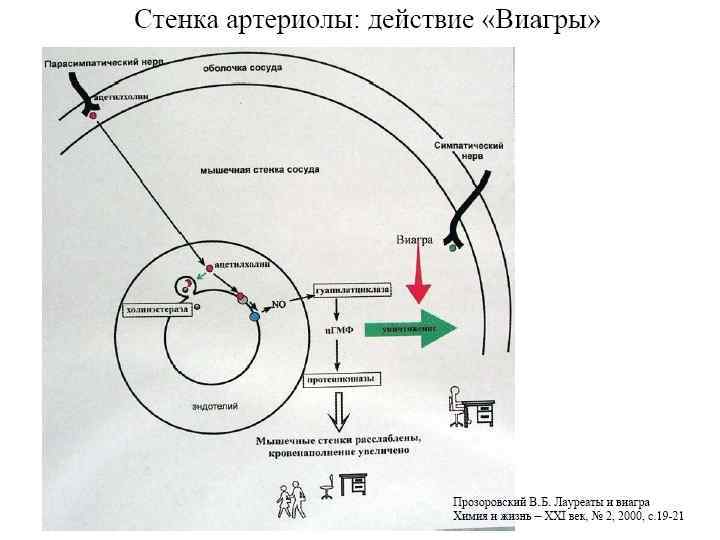
 Проявляє як відновні так і окисні властивості Із солей азотистої кислоти найбільше значення має нітрит натрію Na. NО 2
Проявляє як відновні так і окисні властивості Із солей азотистої кислоти найбільше значення має нітрит натрію Na. NО 2


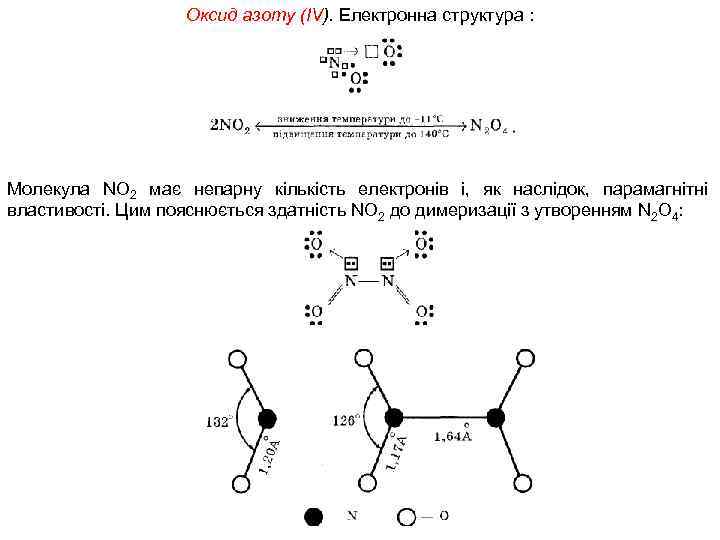 Оксид азоту (IV). Електронна структура : Молекула NО 2 має непарну кількість електронів і, як наслідок, парамагнітні властивості. Цим пояснюється здатність NО 2 до димеризації з утворенням N 2 О 4:
Оксид азоту (IV). Електронна структура : Молекула NО 2 має непарну кількість електронів і, як наслідок, парамагнітні властивості. Цим пояснюється здатність NО 2 до димеризації з утворенням N 2 О 4:
 Одержання оксиду азоту (IV). 1. Окисненням оксиду азоту (II) киснем (при звичайних умовах): 2. Розкладанням при нагріванні нітратів малоактивних металів: 3. Дією концентрованої азотної кислоти на малоактивні метали: Оксид азоту (IV) можна розглядати як ангідрид двох кислот: азотної і азотистої. Реакції взаємодії NО 2 з водою і лугами свідчать про те, що NО 2 може виявляти властивості як відновника, так і окисника. окиснююча функція для NО 2 більш характерна.
Одержання оксиду азоту (IV). 1. Окисненням оксиду азоту (II) киснем (при звичайних умовах): 2. Розкладанням при нагріванні нітратів малоактивних металів: 3. Дією концентрованої азотної кислоти на малоактивні метали: Оксид азоту (IV) можна розглядати як ангідрид двох кислот: азотної і азотистої. Реакції взаємодії NО 2 з водою і лугами свідчать про те, що NО 2 може виявляти властивості як відновника, так і окисника. окиснююча функція для NО 2 більш характерна.
 Оксид азоту (V). Електронна структура Одержують оксид азоту (V) шляхом дегідратації азотної кислоти за допомогою оксиду фосфору (V): або при окисненні оксиду азоту (IV) озоном: N 2 О 5 — біла кристалічна речовина, легко розкладається на оксид азоту (IV) і кисень: N 2 О 5 — сильний окисник. Оксид азоту (V) — кислотний оксид, ангідрид азотної кислоти. При взаємодії з водою утворює азотну кислоту, а в реакціях з основами — солі азотної кислоти — нітрати.
Оксид азоту (V). Електронна структура Одержують оксид азоту (V) шляхом дегідратації азотної кислоти за допомогою оксиду фосфору (V): або при окисненні оксиду азоту (IV) озоном: N 2 О 5 — біла кристалічна речовина, легко розкладається на оксид азоту (IV) і кисень: N 2 О 5 — сильний окисник. Оксид азоту (V) — кислотний оксид, ангідрид азотної кислоти. При взаємодії з водою утворює азотну кислоту, а в реакціях з основами — солі азотної кислоти — нітрати.
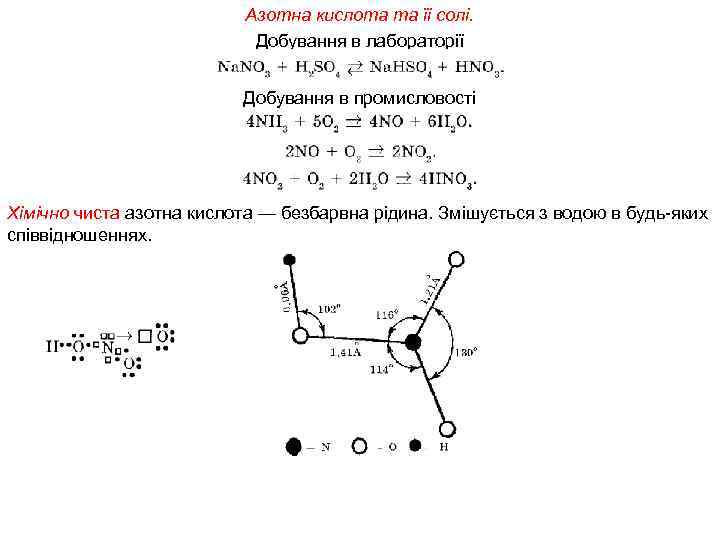 Азотна кислота та їі солі. Добування в лабораторії Добування в промисловості Хімічно чиста азотна кислота — безбарвна рідина. Змішується з водою в будь-яких співвідношеннях.
Азотна кислота та їі солі. Добування в лабораторії Добування в промисловості Хімічно чиста азотна кислота — безбарвна рідина. Змішується з водою в будь-яких співвідношеннях.
 Продуктом реакції за участю азотної кислоти не може бути вільний водень. Азотна кислота здатна окиснювати як метали, так і неметали.
Продуктом реакції за участю азотної кислоти не може бути вільний водень. Азотна кислота здатна окиснювати як метали, так і неметали.
 Найбільшу окиснюючу дію виявляє суміш концентрованих азотної і хлористоводневої кислот в об'ємному співвідношенні 1: 3 (царська водка). Вона розчиняє такі метали, як золото і платина. Окиснює складні речовини
Найбільшу окиснюючу дію виявляє суміш концентрованих азотної і хлористоводневої кислот в об'ємному співвідношенні 1: 3 (царська водка). Вона розчиняє такі метали, як золото і платина. Окиснює складні речовини
 Солі азотної кислоти (нітрати) тверді кристалічні речовини, білого кольору, розчинні у воді. Солі лужних та лужноземельних металів називаються селітрами: Na. NО 3 — чилійська селітра; KNО 3 — індійська селітра; Ca(NО 3)2 — норвезька селітра; NH 4 N 03 — аміачна селітра;
Солі азотної кислоти (нітрати) тверді кристалічні речовини, білого кольору, розчинні у воді. Солі лужних та лужноземельних металів називаються селітрами: Na. NО 3 — чилійська селітра; KNО 3 — індійська селітра; Ca(NО 3)2 — норвезька селітра; NH 4 N 03 — аміачна селітра;
 При нагріванні нітрати розкладаються за різними схемами. 1. Нітрати металів, розміщених у ряду активності металів лівіше магнію, перетворюються у нітрити з виділенням кисню: 2. Нітрати металів, розміщених у ряду активності між магнієм та міддю, розкладаються з утворенням оксидів металів, азоту (IV) та кисню: 3. Нітрати малоактивних металів, розміщених в ряду активності правіше міді, розкладаються на вільний метал, оксид азоту (IV) та кисень:
При нагріванні нітрати розкладаються за різними схемами. 1. Нітрати металів, розміщених у ряду активності металів лівіше магнію, перетворюються у нітрити з виділенням кисню: 2. Нітрати металів, розміщених у ряду активності між магнієм та міддю, розкладаються з утворенням оксидів металів, азоту (IV) та кисню: 3. Нітрати малоактивних металів, розміщених в ряду активності правіше міді, розкладаються на вільний метал, оксид азоту (IV) та кисень:
 Фосфор знаходячись у головній підгрупі V групи періодичної системи елементів, є електронним аналогом азоту. Вона полягає в тому, що фосфор може існувати у двох станах — нормальному і збудженому. Серед усіх алотропних модифікацій найбільш хімічно активним є білий фосфор. При нагріванні фосфор окиснює майже всі метали, утворюючи сполуки, що мають назву фосфіди: Іонно-ковалентні фосфіди — солеподібні речовини, легко розкладаються водою: При нагріванні фосфор взаємодіє з галогенами. В залежності від умов реакції, утворюються похідні трьох- і п'ятивалентного фосфору
Фосфор знаходячись у головній підгрупі V групи періодичної системи елементів, є електронним аналогом азоту. Вона полягає в тому, що фосфор може існувати у двох станах — нормальному і збудженому. Серед усіх алотропних модифікацій найбільш хімічно активним є білий фосфор. При нагріванні фосфор окиснює майже всі метали, утворюючи сполуки, що мають назву фосфіди: Іонно-ковалентні фосфіди — солеподібні речовини, легко розкладаються водою: При нагріванні фосфор взаємодіє з галогенами. В залежності від умов реакції, утворюються похідні трьох- і п'ятивалентного фосфору
 Галогеніди фосфору здатні гідролізуватися: При нагріванні фосфор взаємодіє з сіркою, утворюючи сульфід фосфору (III), а при надлишку сірки — сульфід фосфору (V): З воднем фосфор безпосередньо не взаємодіє, але утворює дві леткі сполуки: газоподібний при звичайній температурі фосфористий водень — фосфін РН 3 (аналог NH 3) і рідкий — дифосфін Р 2 Н 4 (аналог N 2 H 4).
Галогеніди фосфору здатні гідролізуватися: При нагріванні фосфор взаємодіє з сіркою, утворюючи сульфід фосфору (III), а при надлишку сірки — сульфід фосфору (V): З воднем фосфор безпосередньо не взаємодіє, але утворює дві леткі сполуки: газоподібний при звичайній температурі фосфористий водень — фосфін РН 3 (аналог NH 3) і рідкий — дифосфін Р 2 Н 4 (аналог N 2 H 4).
 Фосфін одержують дією сильних кислот на фосфіди активних металів: або внаслідок гідролізу фосфідів лужних та лужноземельних металів: Фосфін — безбарвний отруйний газ. Температура плавлення — 132, 5°С, кипіння — 87, 5°С. Подібно до аміаку фосфін взаємодіє з сильними кислотами, утворюючи солі фосфонію: Властивості Фосфін — сильний відновник. На повітрі він самозаймається і окиснюється до ортофосфорної кислоти: З розчинів солей важких металів фосфін відновлює вільні метали:
Фосфін одержують дією сильних кислот на фосфіди активних металів: або внаслідок гідролізу фосфідів лужних та лужноземельних металів: Фосфін — безбарвний отруйний газ. Температура плавлення — 132, 5°С, кипіння — 87, 5°С. Подібно до аміаку фосфін взаємодіє з сильними кислотами, утворюючи солі фосфонію: Властивості Фосфін — сильний відновник. На повітрі він самозаймається і окиснюється до ортофосфорної кислоти: З розчинів солей важких металів фосфін відновлює вільні метали:
 Дифосфін Р 2 Н 4 утворюється як побічний продукт у реакціях одержання фосфіну. Він також виявляє сильні відновні властивості. На повітрі згоряє з утворенням Н 3 РО 4. У розчинах окиснюється до ортофосфорної кислоти: Кисневі сполуки фосфору. У процесі диспропорціонування фосфору у розчинах лугів, поряд з фосфіном, утворюються солі фосфорнува-тистої кислоти — гіпофосфіти, у яких фосфор має ступінь окиснення 1+. Фосфорнуватиста кислота — безбарвна кристалічна речовина. Ця кислота не має ангідриду, досить сильна незважаючи на наявність трьох атомів водню, одноосновна.
Дифосфін Р 2 Н 4 утворюється як побічний продукт у реакціях одержання фосфіну. Він також виявляє сильні відновні властивості. На повітрі згоряє з утворенням Н 3 РО 4. У розчинах окиснюється до ортофосфорної кислоти: Кисневі сполуки фосфору. У процесі диспропорціонування фосфору у розчинах лугів, поряд з фосфіном, утворюються солі фосфорнува-тистої кислоти — гіпофосфіти, у яких фосфор має ступінь окиснення 1+. Фосфорнуватиста кислота — безбарвна кристалічна речовина. Ця кислота не має ангідриду, досить сильна незважаючи на наявність трьох атомів водню, одноосновна.
 Ступінь окиснення фосфору у складі фосфорнуватистої кислоти має проміжне значення (1+) – проявляє і окисні, і відновні властивості. Відновні властивості фосфорнуватистої кислоти та її солей виявлені значно сильніше, ніж окисні. Вони відновлюють у розчинах метали з їх солей: та окиснюються галогенами, киснем та іншими окисниками:
Ступінь окиснення фосфору у складі фосфорнуватистої кислоти має проміжне значення (1+) – проявляє і окисні, і відновні властивості. Відновні властивості фосфорнуватистої кислоти та її солей виявлені значно сильніше, ніж окисні. Вони відновлюють у розчинах метали з їх солей: та окиснюються галогенами, киснем та іншими окисниками:
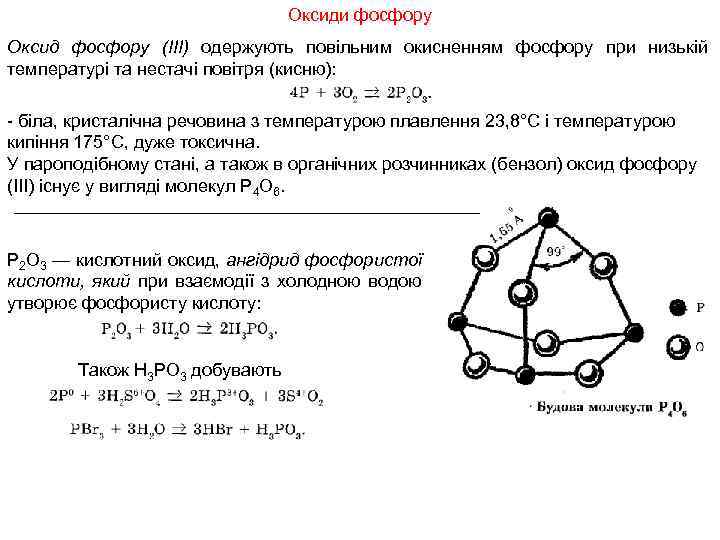 Оксиди фосфору Оксид фосфору (III) одержують повільним окисненням фосфору при низькій температурі та нестачі повітря (кисню): - біла, кристалічна речовина з температурою плавлення 23, 8°С і температурою кипіння 175°С, дуже токсична. У пароподібному стані, а також в органічних розчинниках (бензол) оксид фосфору (III) існує у вигляді молекул Р 4 О 6. Р 2 О 3 — кислотний оксид, ангідрид фосфористої кислоти, який при взаємодії з холодною водою утворює фосфористу кислоту: Також Н 3 РО 3 добувають
Оксиди фосфору Оксид фосфору (III) одержують повільним окисненням фосфору при низькій температурі та нестачі повітря (кисню): - біла, кристалічна речовина з температурою плавлення 23, 8°С і температурою кипіння 175°С, дуже токсична. У пароподібному стані, а також в органічних розчинниках (бензол) оксид фосфору (III) існує у вигляді молекул Р 4 О 6. Р 2 О 3 — кислотний оксид, ангідрид фосфористої кислоти, який при взаємодії з холодною водою утворює фосфористу кислоту: Також Н 3 РО 3 добувають
 Фосфориста кислота — безбарвна, кристалічна речовина; легко розчиняється у воді. Для фосфористої кислоти відомі дві таутомерні форми: Валентні орбіталі атома кислотоутворювача перебувають у стані sp 3 -гібридизації, а атом водню, що безпосередньо сполучений з атомом фосфору, не здатний заміщуватися на метал. Двохосновна кислота
Фосфориста кислота — безбарвна, кристалічна речовина; легко розчиняється у воді. Для фосфористої кислоти відомі дві таутомерні форми: Валентні орбіталі атома кислотоутворювача перебувають у стані sp 3 -гібридизації, а атом водню, що безпосередньо сполучений з атомом фосфору, не здатний заміщуватися на метал. Двохосновна кислота
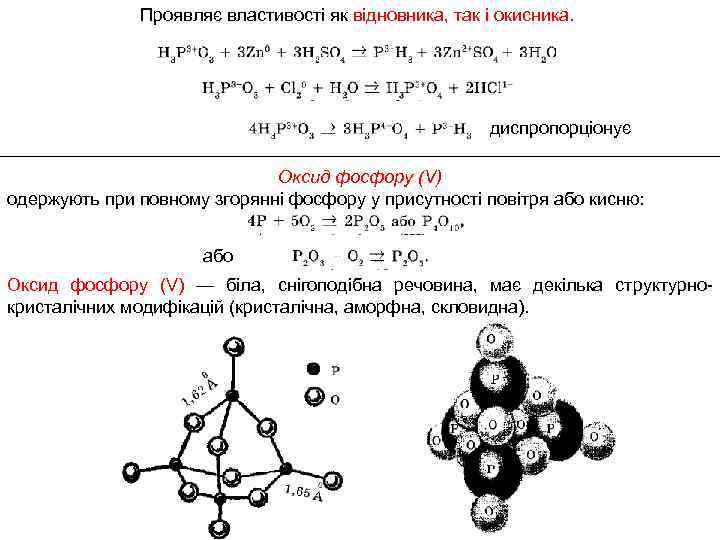 Проявляє властивості як відновника, так і окисника. диспропорціонує Оксид фосфору (V) одержують при повному згорянні фосфору у присутності повітря або кисню: або Оксид фосфору (V) — біла, снігоподібна речовина, має декілька структурнокристалічних модифікацій (кристалічна, аморфна, скловидна).
Проявляє властивості як відновника, так і окисника. диспропорціонує Оксид фосфору (V) одержують при повному згорянні фосфору у присутності повітря або кисню: або Оксид фосфору (V) — біла, снігоподібна речовина, має декілька структурнокристалічних модифікацій (кристалічна, аморфна, скловидна).
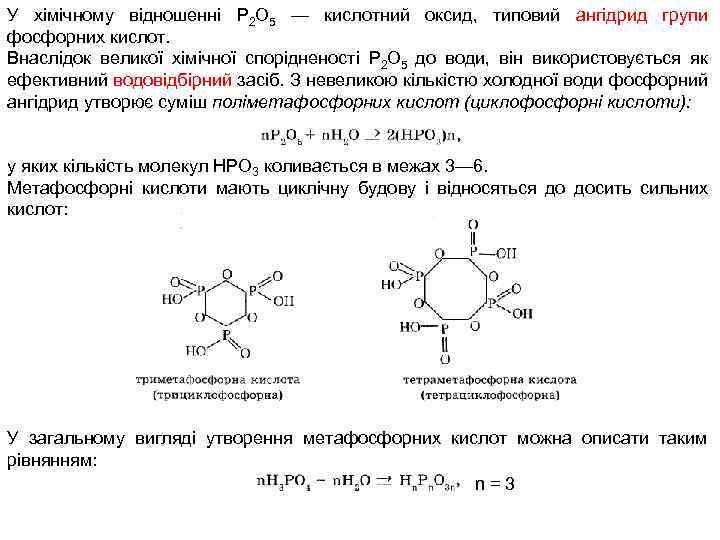 У хімічному відношенні Р 2 О 5 — кислотний оксид, типовий ангідрид групи фосфорних кислот. Внаслідок великої хімічної спорідненості Р 2 О 5 до води, він використовується як ефективний водовідбірний засіб. З невеликою кількістю холодної води фосфорний ангідрид утворює суміш поліметафосфорних кислот (циклофосфорні кислоти): у яких кількість молекул НРО 3 коливається в межах 3— 6. Метафосфорні кислоти мають циклічну будову і відносяться до досить сильних кислот: У загальному вигляді утворення метафосфорних кислот можна описати таким рівнянням: n=3
У хімічному відношенні Р 2 О 5 — кислотний оксид, типовий ангідрид групи фосфорних кислот. Внаслідок великої хімічної спорідненості Р 2 О 5 до води, він використовується як ефективний водовідбірний засіб. З невеликою кількістю холодної води фосфорний ангідрид утворює суміш поліметафосфорних кислот (циклофосфорні кислоти): у яких кількість молекул НРО 3 коливається в межах 3— 6. Метафосфорні кислоти мають циклічну будову і відносяться до досить сильних кислот: У загальному вигляді утворення метафосфорних кислот можна описати таким рівнянням: n=3
 Найважливішою з усіх кислот фосфору є ортофосфорна кислота Н 3 РО 4. В лабораторних умовах її одержують дією надлишку гарячої води на Р 2 О 5: або при окисненні фосфору азотною кислотою та гідролізу галогенідів та оксигалогенідів фосфору (V): У промисловості Екстракційний спосіб — полягає в обробці подрібнених природних фосфатів сірчаною кислотою: Термічний спосіб — складається з трьох етапів — звичайного термічного відновлення (1500— 1600°С) природних фосфатів за допомогою коксу у присутності SіO 2 до елементарного фосфору: спалювання його з утворенням фосфорного ангідриду: розчинення Р 2 O 5 у воді:
Найважливішою з усіх кислот фосфору є ортофосфорна кислота Н 3 РО 4. В лабораторних умовах її одержують дією надлишку гарячої води на Р 2 О 5: або при окисненні фосфору азотною кислотою та гідролізу галогенідів та оксигалогенідів фосфору (V): У промисловості Екстракційний спосіб — полягає в обробці подрібнених природних фосфатів сірчаною кислотою: Термічний спосіб — складається з трьох етапів — звичайного термічного відновлення (1500— 1600°С) природних фосфатів за допомогою коксу у присутності SіO 2 до елементарного фосфору: спалювання його з утворенням фосфорного ангідриду: розчинення Р 2 O 5 у воді:
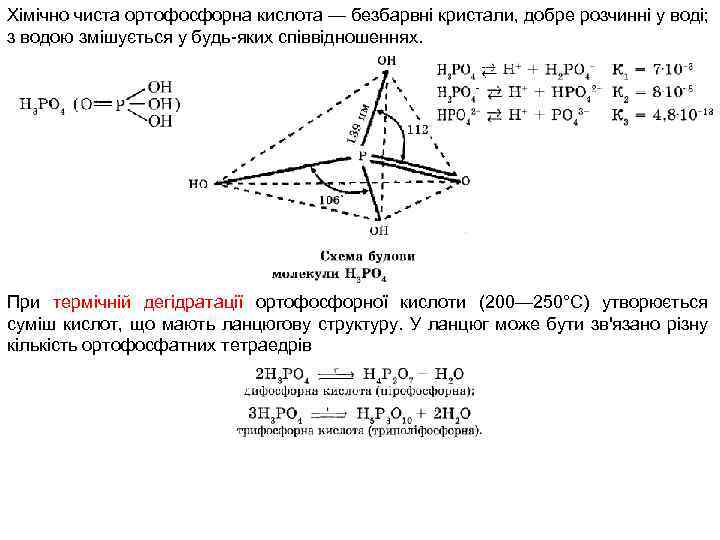 Хімічно чиста ортофосфорна кислота — безбарвні кристали, добре розчинні у воді; з водою змішується у будь-яких співвідношеннях. При термічній дегідратації ортофосфорної кислоти (200— 250°С) утворюється суміш кислот, що мають ланцюгову структуру. У ланцюг може бути зв'язано різну кількість ортофосфатних тетраедрів
Хімічно чиста ортофосфорна кислота — безбарвні кристали, добре розчинні у воді; з водою змішується у будь-яких співвідношеннях. При термічній дегідратації ортофосфорної кислоти (200— 250°С) утворюється суміш кислот, що мають ланцюгову структуру. У ланцюг може бути зв'язано різну кількість ортофосфатних тетраедрів
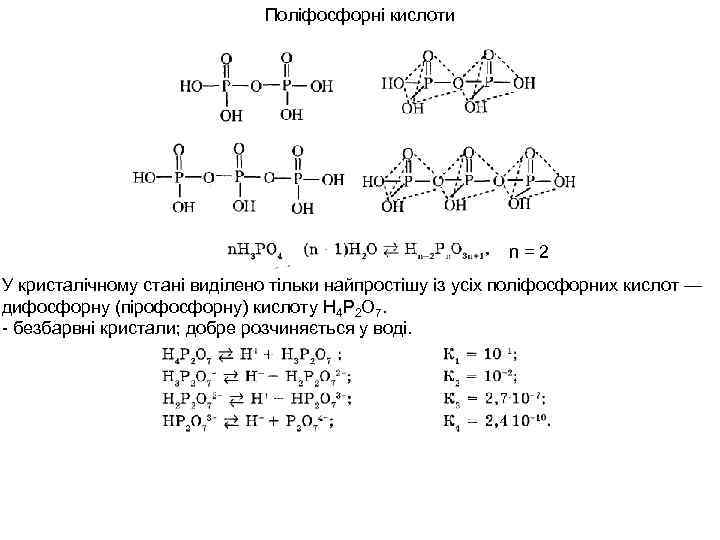 Поліфосфорні кислоти n=2 У кристалічному стані виділено тільки найпростішу із усіх поліфосфорних кислот — дифосфорну (пірофосфорну) кислоту Н 4 Р 2 О 7. - безбарвні кристали; добре розчиняється у воді.
Поліфосфорні кислоти n=2 У кристалічному стані виділено тільки найпростішу із усіх поліфосфорних кислот — дифосфорну (пірофосфорну) кислоту Н 4 Р 2 О 7. - безбарвні кристали; добре розчиняється у воді.
 Не зважаючи на те, що дифосфорна кислота чотириосновна, вона переважно утворює два типи солей: двозаміщені — кислі — Nа 2 Н 2 Р 2 О 7, Мg. Н 2 Р 2 O 7 і чотиризаміщені — середні — Na 4 Р 2 O 7, Мg 2 Р 2 O 7, що пояснюється функціональною нерівноцінністю іонів водню у молекулі кислоти. Кислі солі дифосфорної кислоти добре розчинні у воді, середні — малорозчинні (окрім солей лужних металів). Хімічно чисті дифосфати (середні солі) одержують шляхом прожарювання відповідних гідроортофосфатів: Іони мета-, піро-, та ортофосфорних кислот можна відрізнити за реакцією їх із Аg. NO 3: Іони Р 2 O 74 - і (РO 3)-n можна відрізнити по їх дії на білок. Під впливом (РО 3) -n яєчний білок скипається, а Р 2 O 74 - і РO 43 - на нього не діють. Як якісну аналітичну реакцію на іон РO 43 - використовують дію на розчини фосфатів "молібденовою рідиною"
Не зважаючи на те, що дифосфорна кислота чотириосновна, вона переважно утворює два типи солей: двозаміщені — кислі — Nа 2 Н 2 Р 2 О 7, Мg. Н 2 Р 2 O 7 і чотиризаміщені — середні — Na 4 Р 2 O 7, Мg 2 Р 2 O 7, що пояснюється функціональною нерівноцінністю іонів водню у молекулі кислоти. Кислі солі дифосфорної кислоти добре розчинні у воді, середні — малорозчинні (окрім солей лужних металів). Хімічно чисті дифосфати (середні солі) одержують шляхом прожарювання відповідних гідроортофосфатів: Іони мета-, піро-, та ортофосфорних кислот можна відрізнити за реакцією їх із Аg. NO 3: Іони Р 2 O 74 - і (РO 3)-n можна відрізнити по їх дії на білок. Під впливом (РО 3) -n яєчний білок скипається, а Р 2 O 74 - і РO 43 - на нього не діють. Як якісну аналітичну реакцію на іон РO 43 - використовують дію на розчини фосфатів "молібденовою рідиною"



