ЭЛЕМЕНТАРНЫЕ МЕХАНИЗМЫ ОБРАЗОВАНИЯ.ppt
- Количество слайдов: 20

ЭЛЕМЕНТАРНЫЕ МЕХАНИЗМЫ ОБРАЗОВАНИЯ ДИСПЕРСНЫХ СИСТЕМ

ТЕРМИНОЛОГИЯ Высокодисперсной называется гетерогенная система, состоящая из двух или более компонентов, из которых по крайней мере один диспергирован до размеров в диапазоне порядка 1 мкм 1 нм. Этот компонент называется дисперсной фазой, которая размещена в окружающей ее дисперсионной среде. Дисперсная фаза как и дисперсионная среда, могут быть твердыми (т), жидкими (ж) или газообразными (г). В двухфазных гетерогенных системах возможны комбинации т/ж, ж/ж и т. д. , где в числителе всегда дисперсная фаза, а в знаменателе - дисперсионная среда. Гетерогенные системы типа ж/ж называют эмульсиями. Системы типа т/ж, в которых частицы могут достаточно свободно перемещаться относительно друг от друга, называют золями, если же частицы в системе типа т/ж образуют в результате агрегации связную систему, то такие системы называют гелями или осадками. Высушенные гели называют ксерогелями. Дисперсные системы типа т/г или ж/г из неагрегированных частиц, называют аэрозолями, а высокопористые системы типа т/г часто называют аэрогелями.

Принципы образования высокодисперсных систем • 1. Диспергирование исходных грубодисперсных материалов до частиц заданных размеров путем механического, термомеханического и т. д. измельчения или путем химической пептизации коллоидных агрегатов • 2. Конденсация до частиц нужных размеров из состояния, предельно диспергированного до молекулярноионных размеров. Такое состояние достигается при растворении, испарении, возникает в результате химических реакций и фазовых превращений. • Пептизация - от греческ. peptos - переваренный процесс, обратный коагуляции, т. е. самопроизвольный переход от связной дисперсной системы (коллоидный агрегат, гель) в cвободно-дисперсную (золь).

1. Диспергирование

• Диспергирование связано с увеличением поверхности А и, соответственно, свободной поверхностной энергии. В простейшем случае диспергирования путем механического измельчения при отсутствии химических или агрегатных превращений работа диспергирования может быть выражена через изменение свободной энергии Gмех дисп = А + Т S • т. е. определяется межфазовым поверхностным натяжением , увеличением поверхности А и энтропии S.

• Кроме того, интенсивное механическое измельчение обычно изменяет кристаллографическую структуру материала, способствует аморфизации, а также химическому взаимодействию разнородных материалов, комплекс наблюдаемых изменений изучается механохимией. В этих случаях изменение свободной энергии определяется уравнением G = Gv + GА • где член Gv соответствует изменениям свободной энергии, обусловленным химическими и агрегатными превращениями, GА - изменениям поверхности. При этом G = NВ АВ, где NВ - число молей новообразованной фазы В, АВ - разница стандартных химических потенциалов новообразованной и исходной фазы А.

• Дополнительно в процессах агрегации дезагрегации иногда полезен учет изменений энтропии, связанный с изменением числа частиц в системе. По Фольмеру – Ребиндеру - Щукину образование Nd частиц в N 2 молях растворителя увеличивает энтропию S на SN к Nd ln(N 2 Na /Nd) = k Nd • где к - постоянная Больцмана, Na-число Авогадро, = ln(N 2 Na /Nd). • В результате можно показать, что общее изменение свободной энергии при диспергировании макроскопической фазы до монодисперсных частиц радиуса r без изменений химического и фазового состояния описывается уравнением G [ Nd/Na ][ v/r - RT ]

Фазовые превращения в гомогенных средах • В достаточно общем случае изменения свободной энергии при диспергировании определяются уравнением G = Gv + GА + T SN где последним членом во многих ситуациях можно пренебречь из-за малого его вклада. Критический размер зародышей и метастабильное состояние обусловлены тем, что в общем для фазовых переходов член Gv соответствует снижению энергии при фазовом превращении, а член GА- увеличению энергии из-за образования поверхности раздела фаз.

• Равновесная растворимость частиц C(r) связана с их размером r уравнением Фрейндлиха-Кельвина, которое для выпуклых частиц записывается в форме C/C 0 = ехр ( + 2 v/r. RT) • а при 2 v/r. RT 0 может быть представлено в виде С/С 0 = [1 + 2 v/r. RT]

• Теория образования зародышей новой фазы в исходной гомогенной среде разработана Гиббсом, Фольмером, Френкелем, Зельдовичем и др. • Подставив в уравнение изменения свободной энергии зависимость химического потенциала от радиуса кривизны и концентрации при образовании частиц фазы В в объеме макроскопической гомогенной фазы А, получим G = NB( B - A) + АAB AB = - (VB/v. B)( B - A) + АAB AB где NB - число молей образовавшегося вещества В, которое можно выразить как NB = VB/v. B , где VB -суммарный объем осадка фазы В с мольным объемом v. B, B и A - стандартные химические потенциалы фаз В и А (причем B < A), AB и АAB - поверхностное натяжение и величина межфазовой поверхности
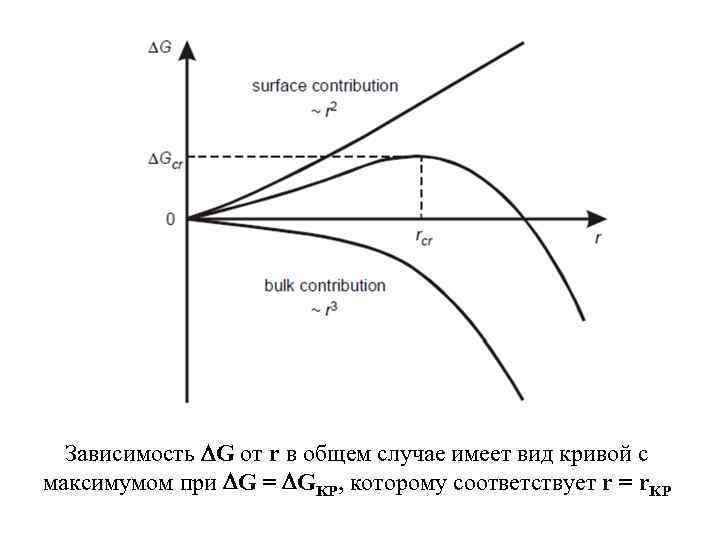
Зависимость G от r в общем случае имеет вид кривой с максимумом при G = GKP, которому соответствует r = r. KP

• Экстремальное значение Gkp определяется дифференцированием G / r = 0 при r = r. KP, в результате радиус критического зародыша r. KP равен r. KP = 2 AB v. B / [ B - A] • а соответствующая ему величина GKP, равная высоте энергетического барьера, который необходимо преодолеть для реализации возможности дальнейшего самопроизвольного роста частиц новой фазы GKP = Кф 3 v. B 2/ 2 • где Кф = (16 /3) - коэффициент, определяемый в общем случае формой зародыша, = [ B - A].
![• Скорость зародышеобразования J обычно определяется уравнениями типа J = к ехр[ -E/RT] • Скорость зародышеобразования J обычно определяется уравнениями типа J = к ехр[ -E/RT]](https://present5.com/presentation/3/19033255_133338080.pdf-img/19033255_133338080.pdf-13.jpg)
• Скорость зародышеобразования J обычно определяется уравнениями типа J = к ехр[ -E/RT] exp [ - GKP /RT ] где Е- энергия активации диффузии или других транспортных процессов, к- константа, определяющая вклад других параметров. При этом dln. J/dln(Sпер ) g* где Sпер (= P/P 0 или С/С 0) - пересыщение, g* - число молекул в критическом зародыше. Уравнение, полученное независимо Костровским с соавт. в 1978 г и Д. Каишевым в 1982 г. , называют первой теоремой нуклеации.

Гетерогенное зародышеобразование • Модель гетерогенного зародышеобразования отличается от модели гомогенного наличием геометрического фактора, учитывающего влияние поверхности. • В данной модели предполагается, что зародыш имеет куполообразную форму, что справедливо для кристаллов с изотропной или слабо изотропной поверхностью. Для кристаллов с сильно выраженной анизотропией поверхности зародыш имеет форму многогранника (пирамида, куб и т. д. ).

• Контактный угол определяется уравнением Юнга Объем куполообразного зародыша равен функция контактного угла Объемная составляющая энергии образования зародыша Поверхностная составляющая энергии образования зародыша

Суммарная энергия Радиус кривизны критического зародыша Энергия образования критического зародыша

Скорость зародышеобразования

Скорость зародышеобразования
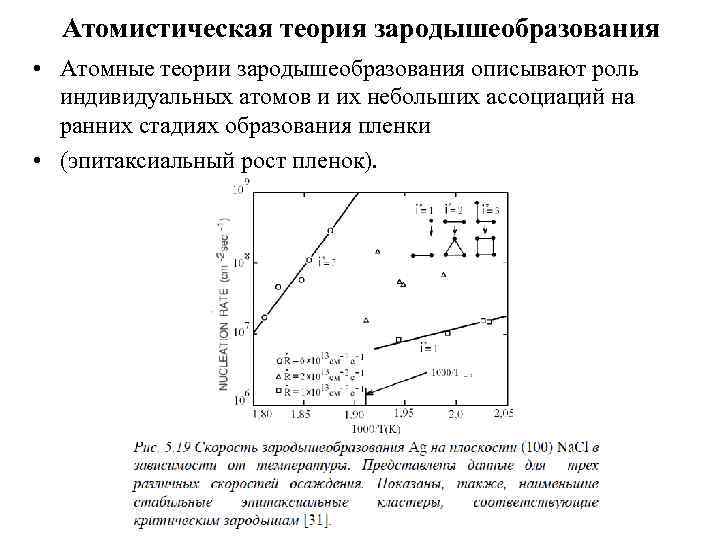
Атомистическая теория зародышеобразования • Атомные теории зародышеобразования описывают роль индивидуальных атомов и их небольших ассоциаций на ранних стадиях образования пленки • (эпитаксиальный рост пленок).
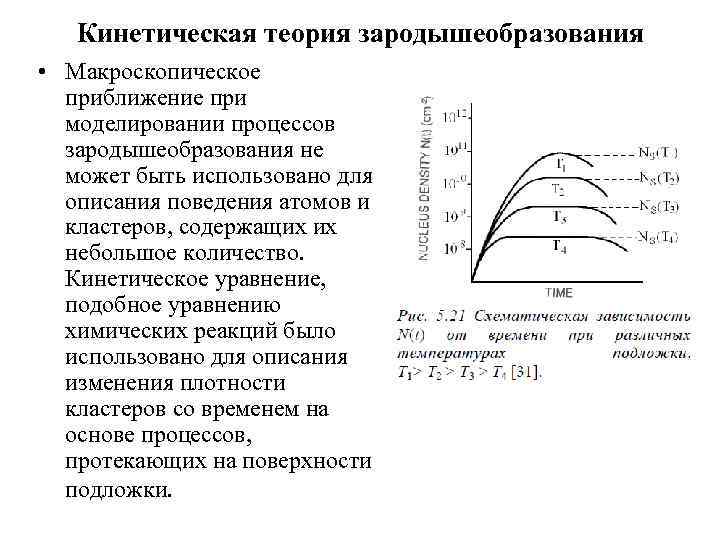
Кинетическая теория зародышеобразования • Макроскопическое приближение при моделировании процессов зародышеобразования не может быть использовано для описания поведения атомов и кластеров, содержащих их небольшое количество. Кинетическое уравнение, подобное уравнению химических реакций было использовано для описания изменения плотности кластеров со временем на основе процессов, протекающих на поверхности подложки.
ЭЛЕМЕНТАРНЫЕ МЕХАНИЗМЫ ОБРАЗОВАНИЯ.ppt