теория растворов.pptx
- Количество слайдов: 37
 ЭЛЕКТРОХИМИЯ
ЭЛЕКТРОХИМИЯ
 Предистория O Относительное понижение парциального давления пара растворителя над раствором не зависит от природы растворённого вещества и равно его мольной доле в растворе. Молекулы растворителя Молекулы растворенного вещества 2
Предистория O Относительное понижение парциального давления пара растворителя над раствором не зависит от природы растворённого вещества и равно его мольной доле в растворе. Молекулы растворителя Молекулы растворенного вещества 2
 Растворение Na. Cl
Растворение Na. Cl
 Теория ЭД O Классическая теория электролитической диссоциации была создана С. Аррениусом и В. Оствальдом в 1887 году. Аррениус придерживался физической теории растворов, не учитывал взаимодействие электролита с водой и считал, что в растворах находятся свободные ионы. Сванте Август Аррениус (Svante August Arrhenius; 1859 - 1927 Вильгельм Фридрих Оствальд (Wilhelm Friedrich Ostwald), 1853 г. -1932 г. 4
Теория ЭД O Классическая теория электролитической диссоциации была создана С. Аррениусом и В. Оствальдом в 1887 году. Аррениус придерживался физической теории растворов, не учитывал взаимодействие электролита с водой и считал, что в растворах находятся свободные ионы. Сванте Август Аррениус (Svante August Arrhenius; 1859 - 1927 Вильгельм Фридрих Оствальд (Wilhelm Friedrich Ostwald), 1853 г. -1932 г. 4
 Теория ЭД Русские химики И. А. Каблуков и В. А. Кистяковский применили для объяснения электролитической диссоциации химическую теорию растворов Д. И. Менделеева и доказали, что при растворении Ива н Алексе евич электролита происходит его Каблуко в химическое взаимодействие с (1857 - 1942) водой, в результате которого электролит диссоциирует на ионы. Влади мир Алекса ндрович Кистяко вский (1865 — 1952) 5
Теория ЭД Русские химики И. А. Каблуков и В. А. Кистяковский применили для объяснения электролитической диссоциации химическую теорию растворов Д. И. Менделеева и доказали, что при растворении Ива н Алексе евич электролита происходит его Каблуко в химическое взаимодействие с (1857 - 1942) водой, в результате которого электролит диссоциирует на ионы. Влади мир Алекса ндрович Кистяко вский (1865 — 1952) 5
 Основные понятия диссоциация растворённого вещества, характеризуется степенью диссоциации α, т. е. долей распавшихся молекул электролита. Степень диссоциации (α) — отношение числа молекул, диссоциировавших на ионы к общему числу молекул растворенного электролита. Электроли т — вещество, расплав или раствор, которое проводит электрический ток вследствие диссоциации на ионы. 6
Основные понятия диссоциация растворённого вещества, характеризуется степенью диссоциации α, т. е. долей распавшихся молекул электролита. Степень диссоциации (α) — отношение числа молекул, диссоциировавших на ионы к общему числу молекул растворенного электролита. Электроли т — вещество, расплав или раствор, которое проводит электрический ток вследствие диссоциации на ионы. 6
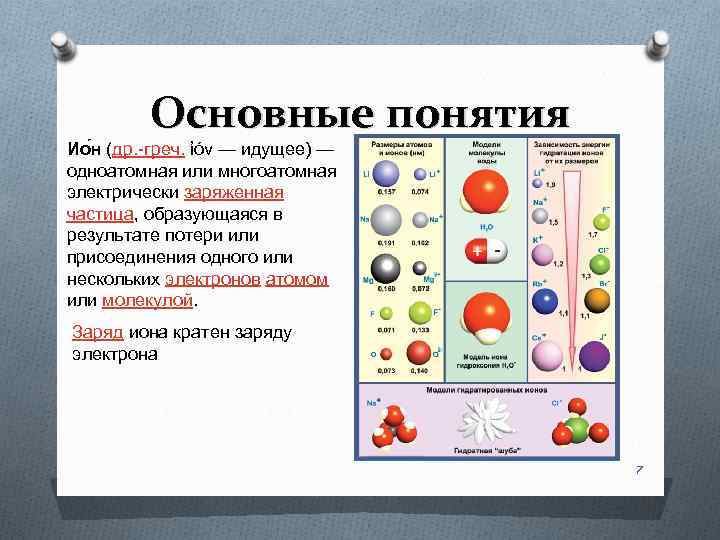 Основные понятия Ио н (др. -греч. ἰόν — идущее) — одноатомная или многоатомная электрически заряженная частица, образующаяся в результате потери или присоединения одного или нескольких электронов атомом или молекулой. Заряд иона кратен заряду электрона 7
Основные понятия Ио н (др. -греч. ἰόν — идущее) — одноатомная или многоатомная электрически заряженная частица, образующаяся в результате потери или присоединения одного или нескольких электронов атомом или молекулой. Заряд иона кратен заряду электрона 7
 Основные понятия Положительно заряженные ионы, движущиеся в растворе к отрицательному полюсу (катоду), называются катионами, а отрицательно заряженные, движущиеся к положительному полюсу (аноду) — анионами. Майкл Фа радей (1791 — 1867) Активность компонентов раствора — эффективная (кажущаяся) концентрация компонентов с учетом различных взаимодействий между ними в растворе 8
Основные понятия Положительно заряженные ионы, движущиеся в растворе к отрицательному полюсу (катоду), называются катионами, а отрицательно заряженные, движущиеся к положительному полюсу (аноду) — анионами. Майкл Фа радей (1791 — 1867) Активность компонентов раствора — эффективная (кажущаяся) концентрация компонентов с учетом различных взаимодействий между ними в растворе 8
 Постулаты ТЭД Первый постулат. В растворах электролитов ионы существуют вне зависимости от наложения или отсутствия электрического поля. Второй постулат. Растворы электролитов подчиняются законам разбавленных растворов. 9
Постулаты ТЭД Первый постулат. В растворах электролитов ионы существуют вне зависимости от наложения или отсутствия электрического поля. Второй постулат. Растворы электролитов подчиняются законам разбавленных растворов. 9
 Константа диссоциации Раствор АВ распадается на ионы А+ и ВОбратимая диссоциация: Константа диссоциации: 10
Константа диссоциации Раствор АВ распадается на ионы А+ и ВОбратимая диссоциация: Константа диссоциации: 10
 Теория Дебая - Хюккеля Электростатическое притяжение между ионами существует во всех электролитах, но в слабых электролитах, где число ионов относительно мало и поэтому они находятся далеко друг от друга, оно несущественно. Эрих Арманд Артур Йозеф Хюккель (Erich Armand Arthur Joseph Hückel) (1896 — 1980) Петер Йозеф Вильгельм Дебай (1884 — 1966) 11
Теория Дебая - Хюккеля Электростатическое притяжение между ионами существует во всех электролитах, но в слабых электролитах, где число ионов относительно мало и поэтому они находятся далеко друг от друга, оно несущественно. Эрих Арманд Артур Йозеф Хюккель (Erich Armand Arthur Joseph Hückel) (1896 — 1980) Петер Йозеф Вильгельм Дебай (1884 — 1966) 11
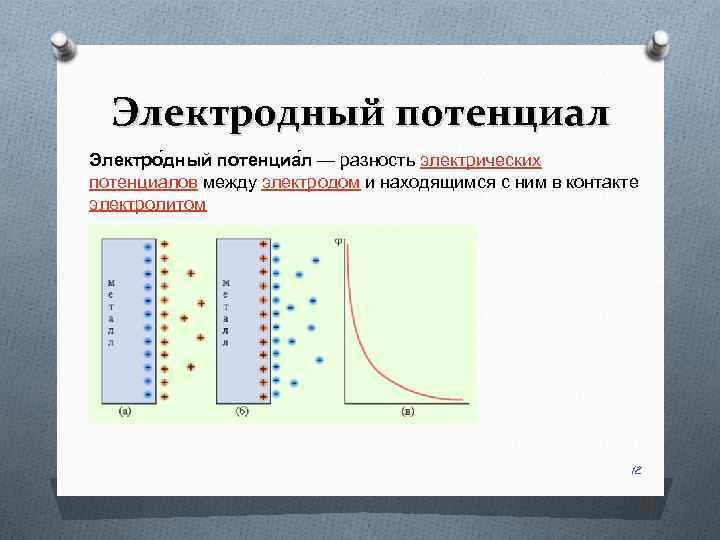 Электродный потенциал Электро дный потенциа л — разность электрических потенциалов между электродом и находящимся с ним в контакте электролитом 12
Электродный потенциал Электро дный потенциа л — разность электрических потенциалов между электродом и находящимся с ним в контакте электролитом 12
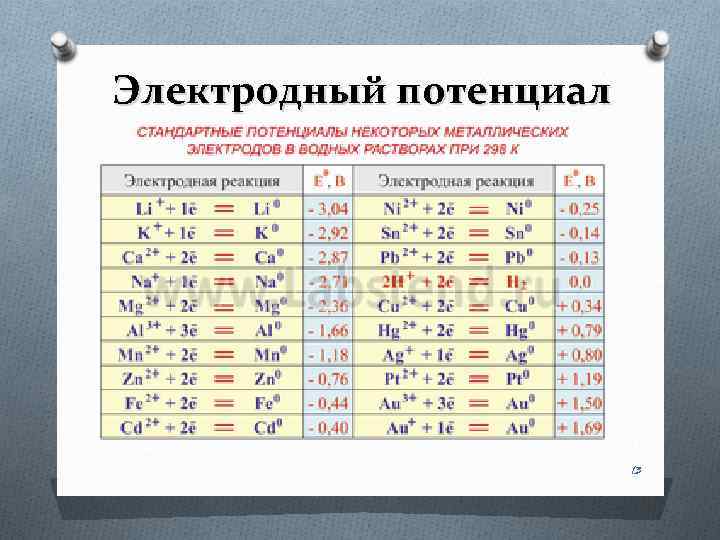 Электродный потенциал 13
Электродный потенциал 13
 Электродный потенциал Стандартный водородный электрод 14
Электродный потенциал Стандартный водородный электрод 14
 Электродный потенциал Определение стандартных электродных потенциалов металлов 15
Электродный потенциал Определение стандартных электродных потенциалов металлов 15
 16
16
 Элемент Якоби-Даниэля Джон Фредерик Даниель (John Frederick Daniell) (1790– 1845) Борис Семенович Якоби (настоящее имя Мориц Герман Якоби) (1801– 1874) 17
Элемент Якоби-Даниэля Джон Фредерик Даниель (John Frederick Daniell) (1790– 1845) Борис Семенович Якоби (настоящее имя Мориц Герман Якоби) (1801– 1874) 17
 Элемент Якоби-Даниэля 18
Элемент Якоби-Даниэля 18
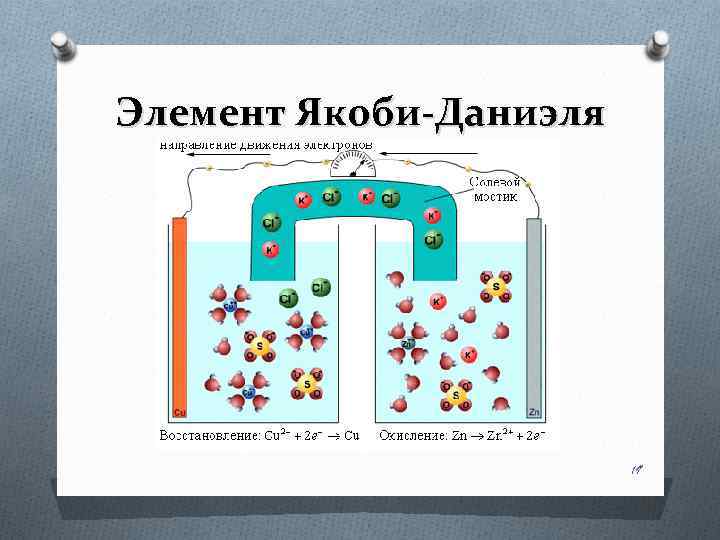 Элемент Якоби-Даниэля 19
Элемент Якоби-Даниэля 19
 Уравнение Нернста Вальтер НЕРНСТ (Nernst W. F. H. ) (1864 - 1941) 20
Уравнение Нернста Вальтер НЕРНСТ (Nernst W. F. H. ) (1864 - 1941) 20
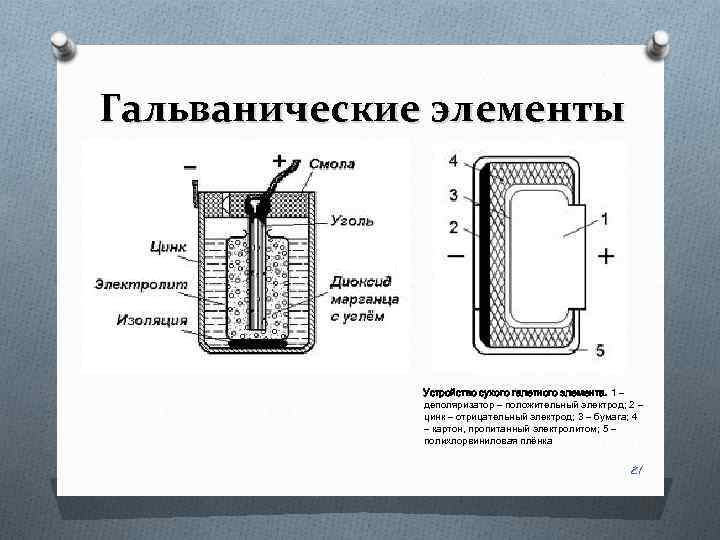 Гальванические элементы Устройство сухого галетного элемента. 1 – деполяризатор – положительный электрод; 2 – цинк – отрицательный электрод; 3 – бумага; 4 – картон, пропитанный электролитом; 5 – полихлорвиниловая плёнка 21
Гальванические элементы Устройство сухого галетного элемента. 1 – деполяризатор – положительный электрод; 2 – цинк – отрицательный электрод; 3 – бумага; 4 – картон, пропитанный электролитом; 5 – полихлорвиниловая плёнка 21
 Гальванические элементы Устройство сухого галетного элемента. 1 – деполяризатор – положительный электрод; 2 – цинк – отрицательный электрод; 3 – бумага; 4 – картон, пропитанный электролитом; 5 – полихлорвиниловая плёнка 22
Гальванические элементы Устройство сухого галетного элемента. 1 – деполяризатор – положительный электрод; 2 – цинк – отрицательный электрод; 3 – бумага; 4 – картон, пропитанный электролитом; 5 – полихлорвиниловая плёнка 22
 Гальванические элементы 23
Гальванические элементы 23
 Гальванические элементы 24
Гальванические элементы 24
 Гальванические элементы 25
Гальванические элементы 25
 Аккумуляторы 26
Аккумуляторы 26
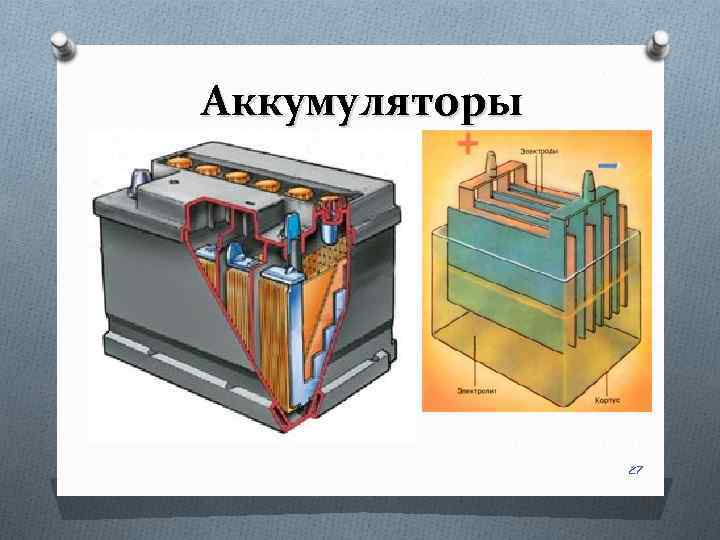 Аккумуляторы 27
Аккумуляторы 27
 Аккумуляторы 28
Аккумуляторы 28
 Аккумуляторы 29
Аккумуляторы 29
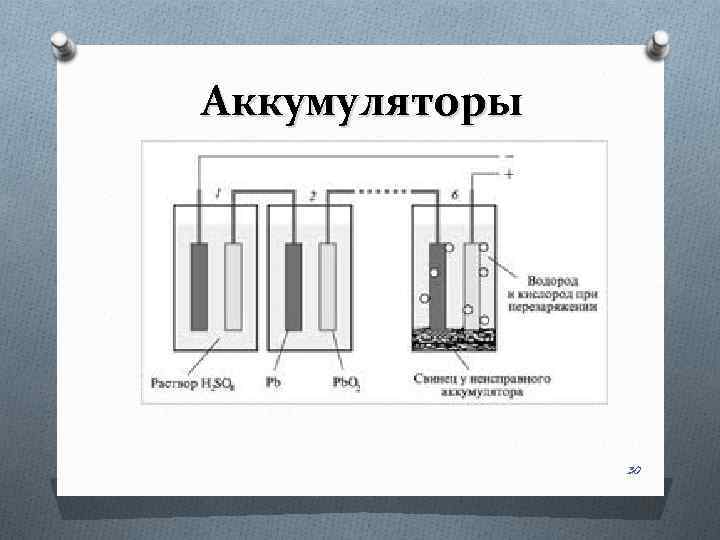 Аккумуляторы 30
Аккумуляторы 30
 Аккумуляторы 31
Аккумуляторы 31
 Аккумуляторы Li-ion аккумулятор 32
Аккумуляторы Li-ion аккумулятор 32
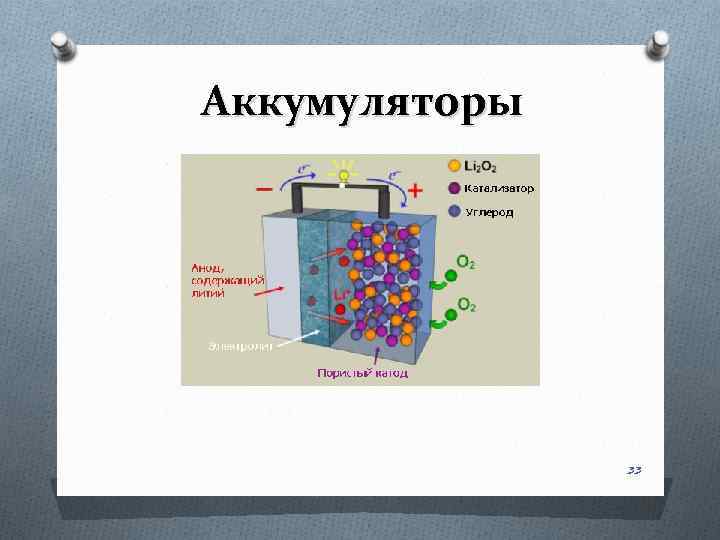 Аккумуляторы 33
Аккумуляторы 33
 p. H 34
p. H 34
 Основные понятия Сёрен Педэр Лауриц Сёренсен (Søren Peder Lauritz Sørensen; (1868 - 1939) Водоро дный показа тель, p. H — мера активности (в очень разбавленных растворах она эквивалентна концентрации) ионов водорода в растворе, и количественно выражающая его кислотность, вычисляется как отрицательный десятичный логарифм активности водородных ионов, выраженной в молях на литр: 35
Основные понятия Сёрен Педэр Лауриц Сёренсен (Søren Peder Lauritz Sørensen; (1868 - 1939) Водоро дный показа тель, p. H — мера активности (в очень разбавленных растворах она эквивалентна концентрации) ионов водорода в растворе, и количественно выражающая его кислотность, вычисляется как отрицательный десятичный логарифм активности водородных ионов, выраженной в молях на литр: 35
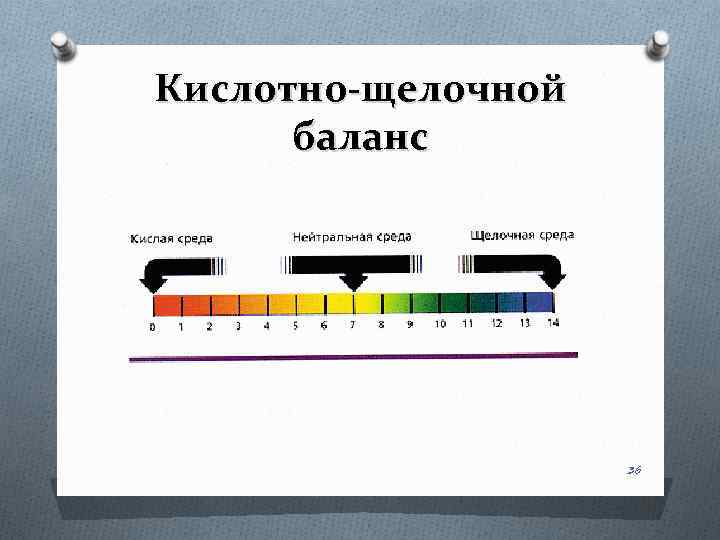 Кислотно-щелочной баланс 36
Кислотно-щелочной баланс 36
 р. Н-метрия 37
р. Н-метрия 37


