Complexes-1-common.ppt
- Количество слайдов: 21
 ЭЛЕКТРОХИМИЯ КОМПЛЕКСОВ МЕТАЛЛОВ Рекомендуемая основная литература. 1. Кравцов В. И. Равновесие и кинетика электродных реакций комплексов металлов. Л. : Химия, 1985. 2. Басоло Ф. , Пирсон Р. Механизмы неорганических реакций. М. : Мир, 1971. 3. Лэнгфорд К. , Грей Г. Процессы замещения лигандов. М. : Мир, 1969. 4. Тоуб М. , Берджесс Д. Механизмы неорганических реакций. М. : Бином, 2014. 5. Бек М. Химия равновесий реакций комплексообразования. М. : Мир. 1973. 6. Кравцов В. И. Электродные процессы в растворах комплексов металлов. Л. : ЛГУ, 1969.
ЭЛЕКТРОХИМИЯ КОМПЛЕКСОВ МЕТАЛЛОВ Рекомендуемая основная литература. 1. Кравцов В. И. Равновесие и кинетика электродных реакций комплексов металлов. Л. : Химия, 1985. 2. Басоло Ф. , Пирсон Р. Механизмы неорганических реакций. М. : Мир, 1971. 3. Лэнгфорд К. , Грей Г. Процессы замещения лигандов. М. : Мир, 1969. 4. Тоуб М. , Берджесс Д. Механизмы неорганических реакций. М. : Бином, 2014. 5. Бек М. Химия равновесий реакций комплексообразования. М. : Мир. 1973. 6. Кравцов В. И. Электродные процессы в растворах комплексов металлов. Л. : ЛГУ, 1969.
 Дополнительная литература 1. Дамаскин Б. Б. , Петрий О. А. , Цирлина Г. А. Электрохимия. Москва: Химия. 2006. 2. Бьеррум Я. Образование амминов металлов в водном растворе. М. : ИИЛ, 1961. 3. Костромина Н. А. , Кумок В. Н, Скорик Н. А. Химия координационных соединений. М. : Высшая школа, 1990. 4. Никольский Б. П. , Пальчевский В. В. , Пендин А. А. , Якубов Х. М. Оксредметрия. Л. : Химия, 1975. 5. Миронов В. Е. , Исаев И. Д. Константы устойчивости внешнесферных комплексов металлов в растворах. Изд. Красноярского ун-та. 1983.
Дополнительная литература 1. Дамаскин Б. Б. , Петрий О. А. , Цирлина Г. А. Электрохимия. Москва: Химия. 2006. 2. Бьеррум Я. Образование амминов металлов в водном растворе. М. : ИИЛ, 1961. 3. Костромина Н. А. , Кумок В. Н, Скорик Н. А. Химия координационных соединений. М. : Высшая школа, 1990. 4. Никольский Б. П. , Пальчевский В. В. , Пендин А. А. , Якубов Х. М. Оксредметрия. Л. : Химия, 1975. 5. Миронов В. Е. , Исаев И. Д. Константы устойчивости внешнесферных комплексов металлов в растворах. Изд. Красноярского ун-та. 1983.
 http: //www. sci-hub. io/ •
http: //www. sci-hub. io/ •
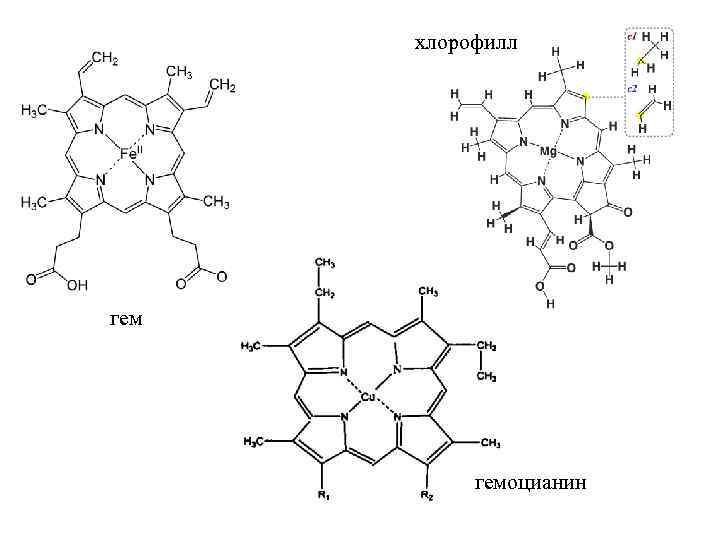 хлорофилл гемоцианин
хлорофилл гемоцианин
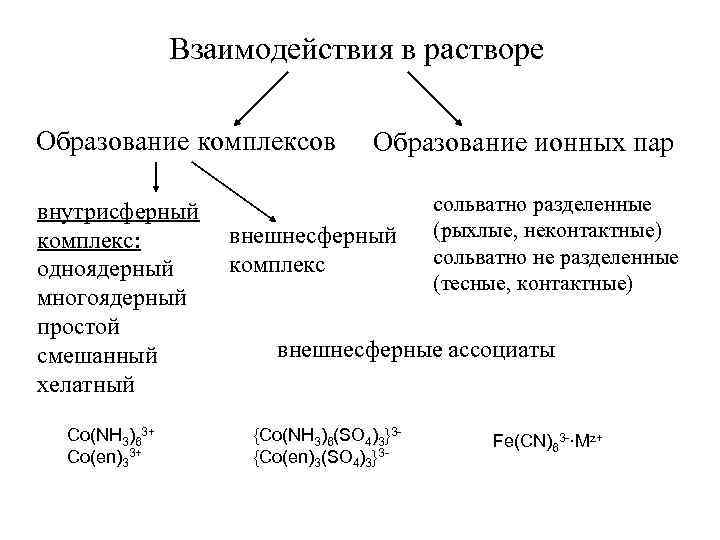 Взаимодействия в растворе Образование комплексов внутрисферный комплекс: одноядерный многоядерный простой смешанный хелатный Co(NH 3)63+ Co(en)33+ Образование ионных пар внешнесферный комплекс сольватно разделенные (рыхлые, неконтактные) сольватно не разделенные (тесные, контактные) внешнесферные ассоциаты {Сo(NH 3)6(SO 4)3}3{Сo(en)3(SO 4)3}3 - Fe(CN)63 -·Mz+
Взаимодействия в растворе Образование комплексов внутрисферный комплекс: одноядерный многоядерный простой смешанный хелатный Co(NH 3)63+ Co(en)33+ Образование ионных пар внешнесферный комплекс сольватно разделенные (рыхлые, неконтактные) сольватно не разделенные (тесные, контактные) внешнесферные ассоциаты {Сo(NH 3)6(SO 4)3}3{Сo(en)3(SO 4)3}3 - Fe(CN)63 -·Mz+
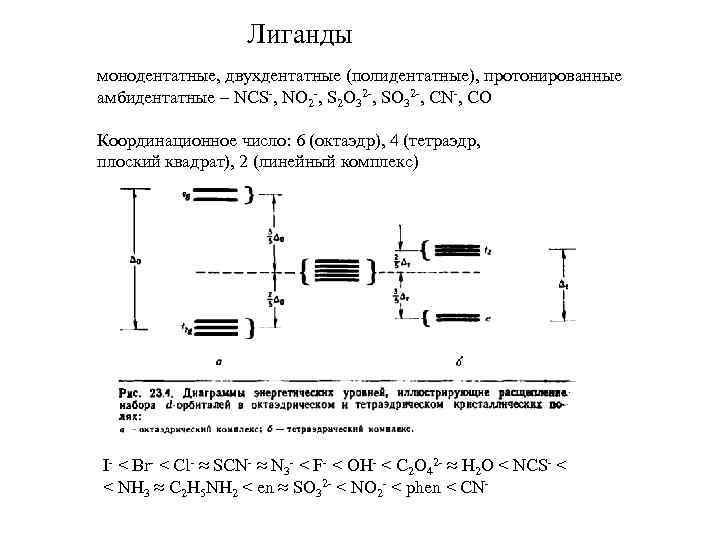 Лиганды монодентатные, двухдентатные (полидентатные), протонированные амбидентатные – NCS-, NO 2 -, S 2 O 32 -, SO 32 -, CN-, CO Координационное число: 6 (октаэдр), 4 (тетраэдр, плоский квадрат), 2 (линейный комплекс) I- < Br- < Cl- ≈ SCN- ≈ N 3 - < F- < OH- < C 2 O 42 - ≈ H 2 O < NCS- < < NH 3 ≈ С 2 H 5 NH 2 < en ≈ SO 32 - < NO 2 - < phen < CN-
Лиганды монодентатные, двухдентатные (полидентатные), протонированные амбидентатные – NCS-, NO 2 -, S 2 O 32 -, SO 32 -, CN-, CO Координационное число: 6 (октаэдр), 4 (тетраэдр, плоский квадрат), 2 (линейный комплекс) I- < Br- < Cl- ≈ SCN- ≈ N 3 - < F- < OH- < C 2 O 42 - ≈ H 2 O < NCS- < < NH 3 ≈ С 2 H 5 NH 2 < en ≈ SO 32 - < NO 2 - < phen < CN-
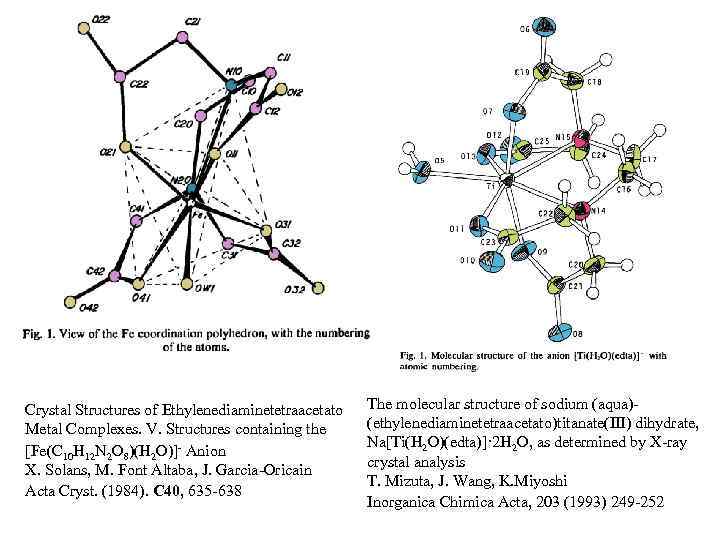 Crystal Structures of Ethylenediaminetetraacetato Metal Complexes. V. Structures containing the [Fe(C 10 H 12 N 2 O 8)(H 2 O)]- Anion X. Solans, M. Font Altaba, J. Garcia-Oricain Acta Cryst. (1984). C 40, 635 -638 The molecular structure of sodium (aqua)(ethylenediaminetetraacetato)titanate(III) dihydrate, Na[Ti(H 2 O)(edta)]· 2 H 2 O, as determined by X-ray crystal analysis T. Mizuta, J. Wang, K. Miyoshi Inorganica Chimica Acta, 203 (1993) 249 -252
Crystal Structures of Ethylenediaminetetraacetato Metal Complexes. V. Structures containing the [Fe(C 10 H 12 N 2 O 8)(H 2 O)]- Anion X. Solans, M. Font Altaba, J. Garcia-Oricain Acta Cryst. (1984). C 40, 635 -638 The molecular structure of sodium (aqua)(ethylenediaminetetraacetato)titanate(III) dihydrate, Na[Ti(H 2 O)(edta)]· 2 H 2 O, as determined by X-ray crystal analysis T. Mizuta, J. Wang, K. Miyoshi Inorganica Chimica Acta, 203 (1993) 249 -252
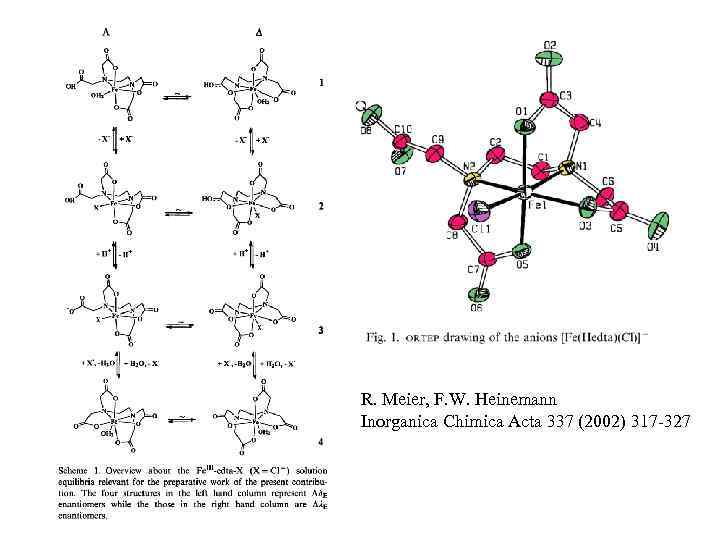 R. Meier, F. W. Heinemann Inorganica Chimica Acta 337 (2002) 317 -327
R. Meier, F. W. Heinemann Inorganica Chimica Acta 337 (2002) 317 -327
 M(H 2 O)kz+ + X(H 2 O)p = MX(H 2 O)m + (k+p-m)H 2 O Mz+ + i. X = MXi
M(H 2 O)kz+ + X(H 2 O)p = MX(H 2 O)m + (k+p-m)H 2 O Mz+ + i. X = MXi
 Методы поддержания постоянными коэффициентов активности 1. Сохраняя постоянство ионной силы 2. Используя постоянную ионную среду 3. Измерения при большой постоянной концентрации аниона или катиона, не участвующего в комплексообразовании Альтернативный метод Расчет коэффициентов активности (метод самосреды и т. п. )
Методы поддержания постоянными коэффициентов активности 1. Сохраняя постоянство ионной силы 2. Используя постоянную ионную среду 3. Измерения при большой постоянной концентрации аниона или катиона, не участвующего в комплексообразовании Альтернативный метод Расчет коэффициентов активности (метод самосреды и т. п. )
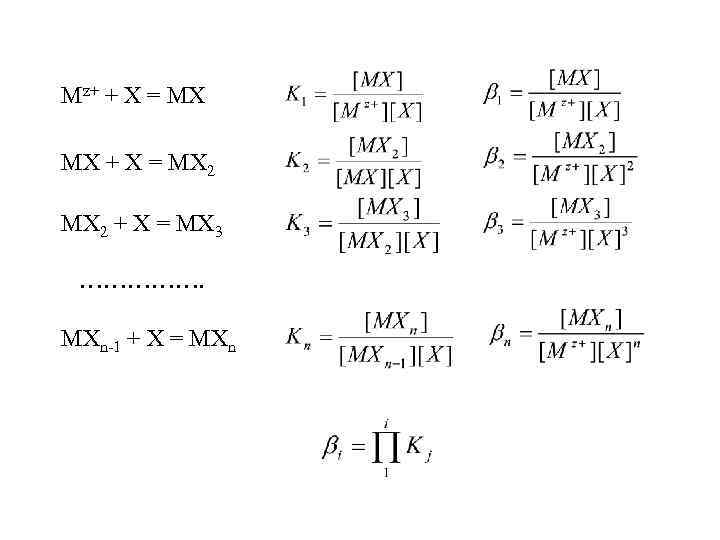 Mz+ + X = MX MX + X = MX 2 + X = MX 3 ……………. MXn-1 + X = MXn
Mz+ + X = MX MX + X = MX 2 + X = MX 3 ……………. MXn-1 + X = MXn
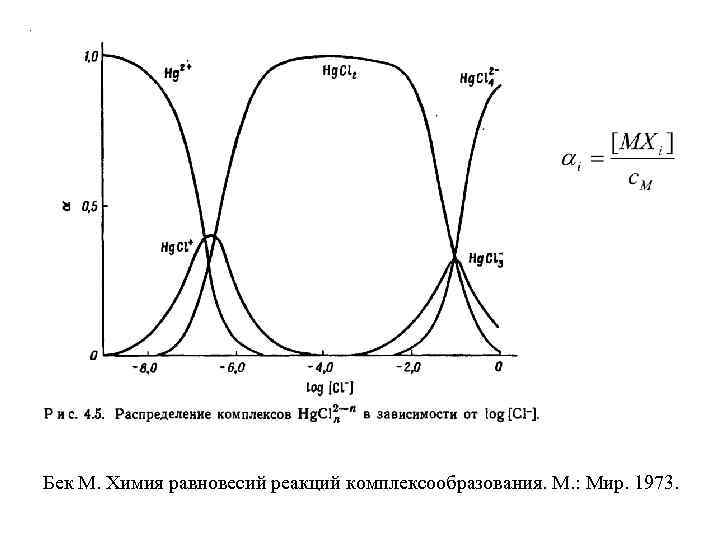 Бек М. Химия равновесий реакций комплексообразования. М. : Мир. 1973.
Бек М. Химия равновесий реакций комплексообразования. М. : Мир. 1973.
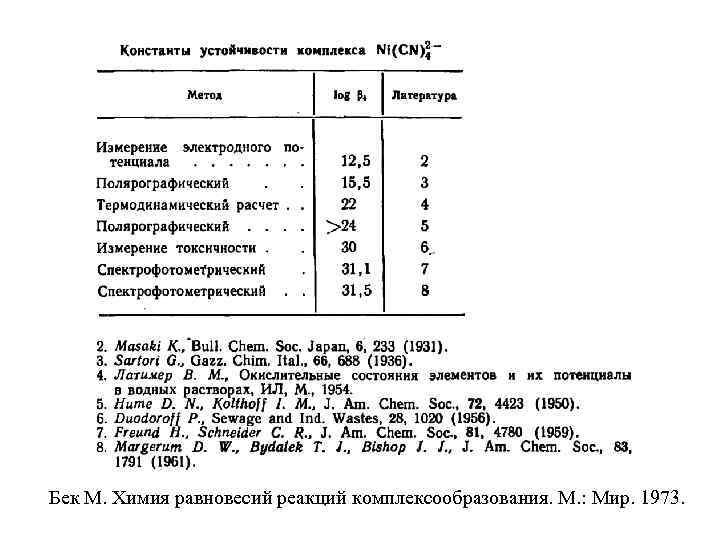 Бек М. Химия равновесий реакций комплексообразования. М. : Мир. 1973.
Бек М. Химия равновесий реакций комплексообразования. М. : Мир. 1973.
 Реакции с участием протонированных лигандов Zn 2+ + H 2 edta 2 - = Zn(edta)2 - + 2 H+ Mz+ + i. Hp. X = MXi + ip. H+ Реакции образования многоядерных комплексов p. Mz+ + q. X = Mp. Xq Реакции образования многоядерных смешанных комплексов p. Mz+ + q. X + r. Y + s. Z = Mp. Xq. Yr. Zs
Реакции с участием протонированных лигандов Zn 2+ + H 2 edta 2 - = Zn(edta)2 - + 2 H+ Mz+ + i. Hp. X = MXi + ip. H+ Реакции образования многоядерных комплексов p. Mz+ + q. X = Mp. Xq Реакции образования многоядерных смешанных комплексов p. Mz+ + q. X + r. Y + s. Z = Mp. Xq. Yr. Zs
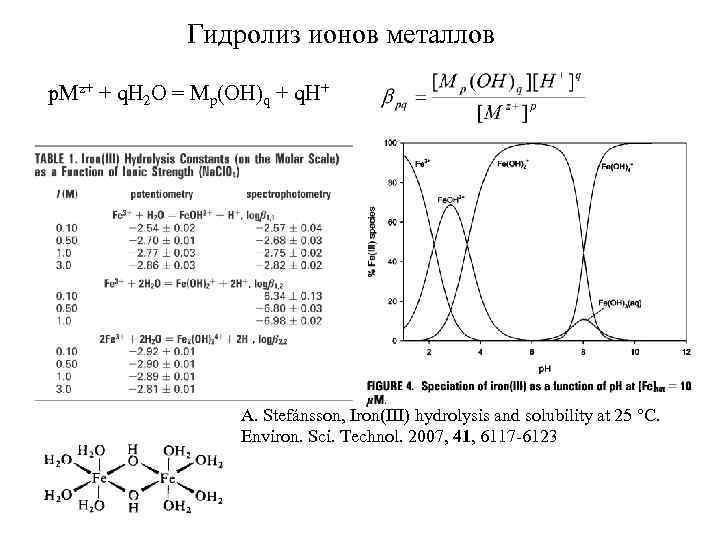 Гидролиз ионов металлов p. Mz+ + q. H 2 O = Mp(OH)q + q. H+ A. Stefánsson, Iron(III) hydrolysis and solubility at 25 °C. Environ. Sci. Technol. 2007, 41, 6117 -6123
Гидролиз ионов металлов p. Mz+ + q. H 2 O = Mp(OH)q + q. H+ A. Stefánsson, Iron(III) hydrolysis and solubility at 25 °C. Environ. Sci. Technol. 2007, 41, 6117 -6123
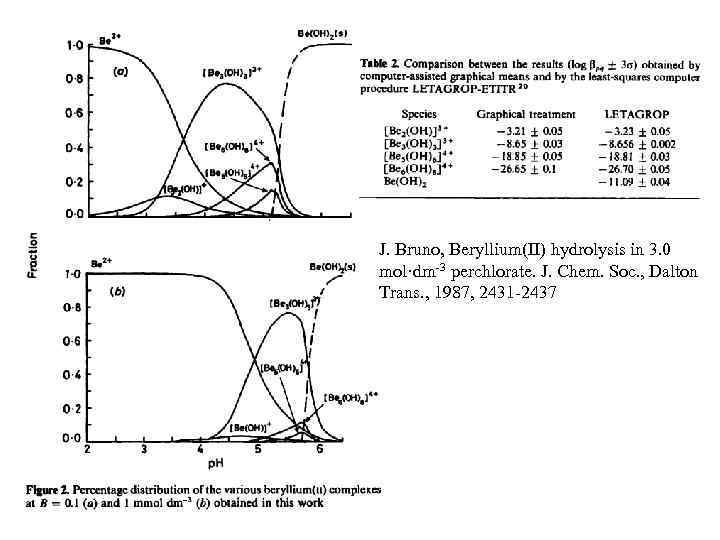 J. Bruno, Beryllium(II) hydrolysis in 3. 0 mol·dm-3 perchlorate. J. Chem. Soc. , Dalton Trans. , 1987, 2431 -2437
J. Bruno, Beryllium(II) hydrolysis in 3. 0 mol·dm-3 perchlorate. J. Chem. Soc. , Dalton Trans. , 1987, 2431 -2437
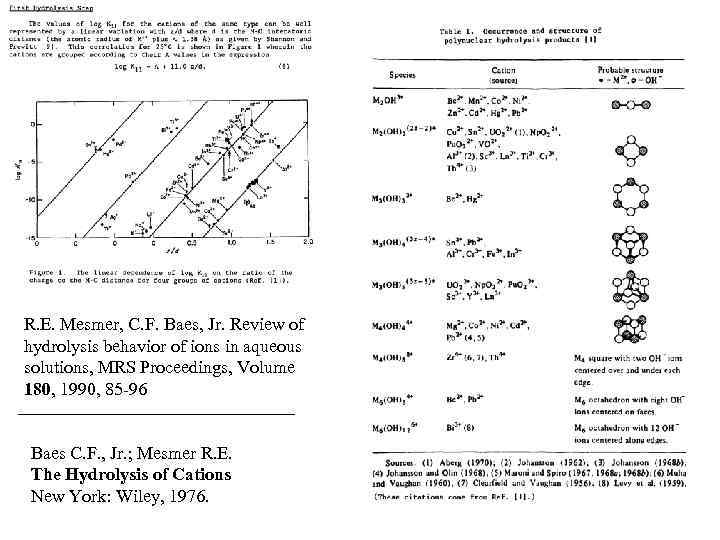 R. E. Mesmer, C. F. Baes, Jr. Review of hydrolysis behavior of ions in aqueous solutions, MRS Proceedings, Volume 180, 1990, 85 -96 Baes C. F. , Jr. ; Mesmer R. E. The Hydrolysis of Cations New York: Wiley, 1976.
R. E. Mesmer, C. F. Baes, Jr. Review of hydrolysis behavior of ions in aqueous solutions, MRS Proceedings, Volume 180, 1990, 85 -96 Baes C. F. , Jr. ; Mesmer R. E. The Hydrolysis of Cations New York: Wiley, 1976.
![Аммиачные и гидроксоаммиачные комплексы цинка(II) [NH 3 ], M p. H αi· 100 Zn(NH Аммиачные и гидроксоаммиачные комплексы цинка(II) [NH 3 ], M p. H αi· 100 Zn(NH](https://present5.com/presentation/-94620283_437470169/image-18.jpg) Аммиачные и гидроксоаммиачные комплексы цинка(II) [NH 3 ], M p. H αi· 100 Zn(NH 2+ 3 )4 αij· 100 Zn(NH 2+ 3 )3 Zn(NH 3 )3 (OH)+ Zn(NH 3 )2 (OH)2 Zn(NH 3) (OH)2 Zn(N H 3 ) (OH)3 - 0. 05 9. 8 5 17 3 30 39 2 9 - 0. 1 9. 2 0 70 7 14 9 - - - 0. 1 9. 8 5 38 4 34 21 1 2 - 0. 1 10. 40 14 1 43 27 4 11 - 0. 2 9. 8 5 61 3 27 9 - - - 0. 5 9. 8 5 82 2 14 2 - - - В. И. Кравцов и др. , Электрохимия, 52001, 37, 658 -667. Рассчитано по данным: 0. 5 12. 2 40 32 16 5 00 H. Bode, Z. anorg. allgem. Chem. 1962, 317, 3. 1. 0 12. 5 29. 5 24 6 2 Я. Бьеррум. Образование амминов 4 металлов в водном растворе. М. : Ин. лит. С. 308. 00 2. 0 12. 00 11 - 70 2 14 2 1
Аммиачные и гидроксоаммиачные комплексы цинка(II) [NH 3 ], M p. H αi· 100 Zn(NH 2+ 3 )4 αij· 100 Zn(NH 2+ 3 )3 Zn(NH 3 )3 (OH)+ Zn(NH 3 )2 (OH)2 Zn(NH 3) (OH)2 Zn(N H 3 ) (OH)3 - 0. 05 9. 8 5 17 3 30 39 2 9 - 0. 1 9. 2 0 70 7 14 9 - - - 0. 1 9. 8 5 38 4 34 21 1 2 - 0. 1 10. 40 14 1 43 27 4 11 - 0. 2 9. 8 5 61 3 27 9 - - - 0. 5 9. 8 5 82 2 14 2 - - - В. И. Кравцов и др. , Электрохимия, 52001, 37, 658 -667. Рассчитано по данным: 0. 5 12. 2 40 32 16 5 00 H. Bode, Z. anorg. allgem. Chem. 1962, 317, 3. 1. 0 12. 5 29. 5 24 6 2 Я. Бьеррум. Образование амминов 4 металлов в водном растворе. М. : Ин. лит. С. 308. 00 2. 0 12. 00 11 - 70 2 14 2 1
 Гидролиз анионов J. J. Cruywagen, J. B. B. Heyns, E. F. C. H. Rohwer, Journal of Inorganic and Nuclear Chemistry 1976; 38(11): 2033– 2036 J. J. Cruywagen , E. F. C. H. Rohwer Inorg. Chem. , 1975, 14, 3136– 3137
Гидролиз анионов J. J. Cruywagen, J. B. B. Heyns, E. F. C. H. Rohwer, Journal of Inorganic and Nuclear Chemistry 1976; 38(11): 2033– 2036 J. J. Cruywagen , E. F. C. H. Rohwer Inorg. Chem. , 1975, 14, 3136– 3137
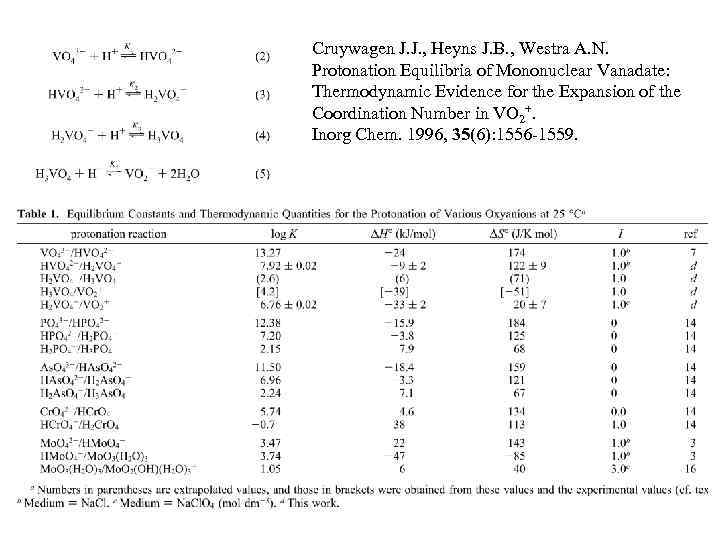 Cruywagen J. J. , Heyns J. B. , Westra A. N. Protonation Equilibria of Mononuclear Vanadate: Thermodynamic Evidence for the Expansion of the Coordination Number in VO 2+. Inorg Chem. 1996, 35(6): 1556 -1559.
Cruywagen J. J. , Heyns J. B. , Westra A. N. Protonation Equilibria of Mononuclear Vanadate: Thermodynamic Evidence for the Expansion of the Coordination Number in VO 2+. Inorg Chem. 1996, 35(6): 1556 -1559.
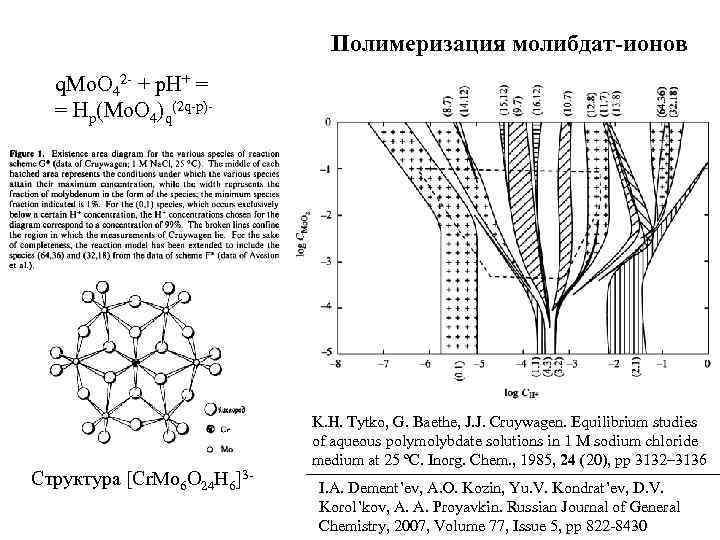 Полимеризация молибдат-ионов q. Mo. O 42 - + p. H+ = = Hp(Mo. O 4)q(2 q-p)- Структура [Cr. Mo 6 O 24 H 6]3 - K. H. Tytko, G. Baethe, J. J. Cruywagen. Equilibrium studies of aqueous polymolybdate solutions in 1 M sodium chloride medium at 25 ºC. Inorg. Chem. , 1985, 24 (20), pp 3132– 3136 I. A. Dement’ev, A. O. Kozin, Yu. V. Kondrat’ev, D. V. Korol’kov, A. A. Proyavkin. Russian Journal of General Chemistry, 2007, Volume 77, Issue 5, pp 822 -8430
Полимеризация молибдат-ионов q. Mo. O 42 - + p. H+ = = Hp(Mo. O 4)q(2 q-p)- Структура [Cr. Mo 6 O 24 H 6]3 - K. H. Tytko, G. Baethe, J. J. Cruywagen. Equilibrium studies of aqueous polymolybdate solutions in 1 M sodium chloride medium at 25 ºC. Inorg. Chem. , 1985, 24 (20), pp 3132– 3136 I. A. Dement’ev, A. O. Kozin, Yu. V. Kondrat’ev, D. V. Korol’kov, A. A. Proyavkin. Russian Journal of General Chemistry, 2007, Volume 77, Issue 5, pp 822 -8430


