7 ЭЛЕКТРОХИМИЯ ГЕТЕРОГЕННЫХ.ppt
- Количество слайдов: 30
 ЭЛЕКТРОХИМИЯ ГЕТЕРОГЕННЫХ СИСТЕМ (ЭЛЕКТРОДИКА) Лекция 7
ЭЛЕКТРОХИМИЯ ГЕТЕРОГЕННЫХ СИСТЕМ (ЭЛЕКТРОДИКА) Лекция 7
 Предмет электродики Это свойства систем, включающих заряженные межфазные границы, в том числе • «металл | раствор электролита» , • «металл | твердый электролит» , • «неметаллический материал | раствор • электролита» , • граница двух растворов и др.
Предмет электродики Это свойства систем, включающих заряженные межфазные границы, в том числе • «металл | раствор электролита» , • «металл | твердый электролит» , • «неметаллический материал | раствор • электролита» , • граница двух растворов и др.
 Электрохимический потенциал • Электрохимический потенциал — физическая величина, связывающая • химический потенциал (μ) и электрический потенциал (φ) некоторой электрохимической системы соотношением: • A = μ + e·φ • где А — работа, нарушающая электрохимическое равновесие системы; • e — элементарный заряд частицы.
Электрохимический потенциал • Электрохимический потенциал — физическая величина, связывающая • химический потенциал (μ) и электрический потенциал (φ) некоторой электрохимической системы соотношением: • A = μ + e·φ • где А — работа, нарушающая электрохимическое равновесие системы; • e — элементарный заряд частицы.
 Электрохимическая свободная энергия Гиббса
Электрохимическая свободная энергия Гиббса
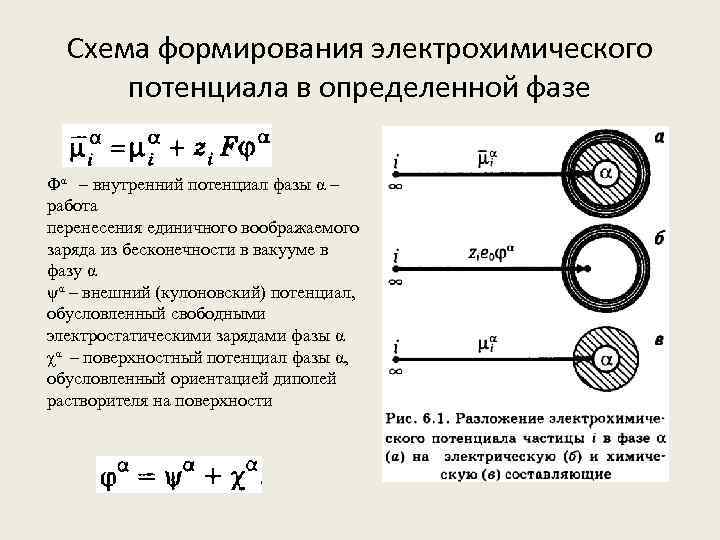 Схема формирования электрохимического потенциала в определенной фазе Φα – внутренний потенциал фазы α – работа перенесения единичного воображаемого заряда из бесконечности в вакууме в фазу α ψα – внешний (кулоновский) потенциал, обусловленный свободными электростатическими зарядами фазы α χα – поверхностный потенциал фазы α, обусловленный ориентацией диполей растворителя на поверхности
Схема формирования электрохимического потенциала в определенной фазе Φα – внутренний потенциал фазы α – работа перенесения единичного воображаемого заряда из бесконечности в вакууме в фазу α ψα – внешний (кулоновский) потенциал, обусловленный свободными электростатическими зарядами фазы α χα – поверхностный потенциал фазы α, обусловленный ориентацией диполей растворителя на поверхности
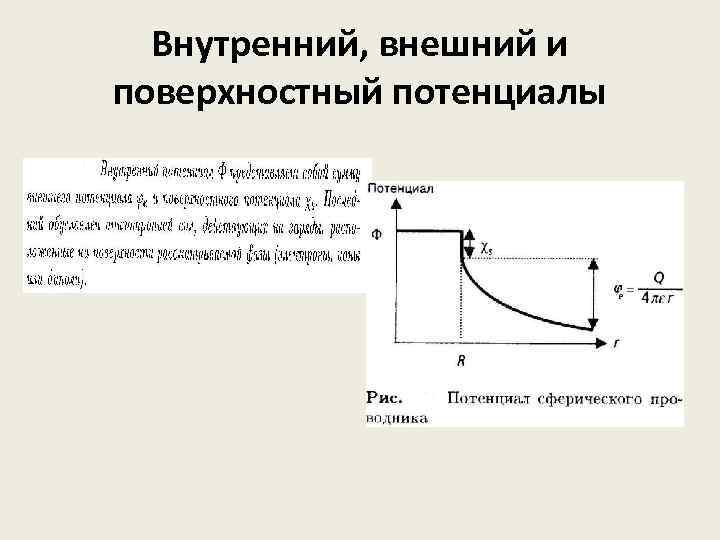 Внутренний, внешний и поверхностный потенциалы
Внутренний, внешний и поверхностный потенциалы
 Межфазный потенциал. Гальванипотенциал
Межфазный потенциал. Гальванипотенциал
 Гальвани-потенциал и вольтапотенциал
Гальвани-потенциал и вольтапотенциал
 Условие равновесия обратимой реакции с участием заряженных частиц
Условие равновесия обратимой реакции с участием заряженных частиц
 Эмиссия электронов из проводников Электрон свободен только в границах металла. Как только он пытается перейти границу «металл – вакуум» , возникает кулоновская сила притяжения между электроном и образовавшимся на поверхности избыточным положительным зарядом
Эмиссия электронов из проводников Электрон свободен только в границах металла. Как только он пытается перейти границу «металл – вакуум» , возникает кулоновская сила притяжения между электроном и образовавшимся на поверхности избыточным положительным зарядом
 Разность потенциалов на поверхности металла Вблизи от поверхности образуется электронное облако, и на границе раздела формируется двойной электрический слой с разностью потенциалов
Разность потенциалов на поверхности металла Вблизи от поверхности образуется электронное облако, и на границе раздела формируется двойной электрический слой с разностью потенциалов
 Скачки потенциала на границе металла • Так как в пределах металла электроны свободны, и их энергия взаимодействия с узлами решетки равна нулю. • За пределами металла электрон приобретает энергию W 0. Это энергия притяжения, поэтому
Скачки потенциала на границе металла • Так как в пределах металла электроны свободны, и их энергия взаимодействия с узлами решетки равна нулю. • За пределами металла электрон приобретает энергию W 0. Это энергия притяжения, поэтому
 Работа выхода электрона • Для того, чтобы покинуть металл, электрон должен преодолеть потенциальный барьер и совершить работу
Работа выхода электрона • Для того, чтобы покинуть металл, электрон должен преодолеть потенциальный барьер и совершить работу
 Равновесие на границе двух металлов
Равновесие на границе двух металлов
 Граница металла М с раствором, содержащим ионы того же металла.
Граница металла М с раствором, содержащим ионы того же металла.
 Электрохимическая цепь
Электрохимическая цепь
 Алессандро Вольта. Изобретатель источника постоянного электрического тока (1745– 1827) • Алессандро Вольта, итальянский физик, химик и физиолог, установил, что электрический ток возникал в том случае, когда между двумя металлическими дисками, например цинковым и медным, помещали пропитанный соленой водой губчатый материал (сукно или бумагу) и замыкали цепь. Последовательно соединив двадцать таких элементов, Вольта в 1800 г. создал первый химический источник тока – вольтов столб. Вольта назвал источник тока гальваническим элементом в честь своего предшественника, также итальянского ученого, Гальвани.
Алессандро Вольта. Изобретатель источника постоянного электрического тока (1745– 1827) • Алессандро Вольта, итальянский физик, химик и физиолог, установил, что электрический ток возникал в том случае, когда между двумя металлическими дисками, например цинковым и медным, помещали пропитанный соленой водой губчатый материал (сукно или бумагу) и замыкали цепь. Последовательно соединив двадцать таких элементов, Вольта в 1800 г. создал первый химический источник тока – вольтов столб. Вольта назвал источник тока гальваническим элементом в честь своего предшественника, также итальянского ученого, Гальвани.
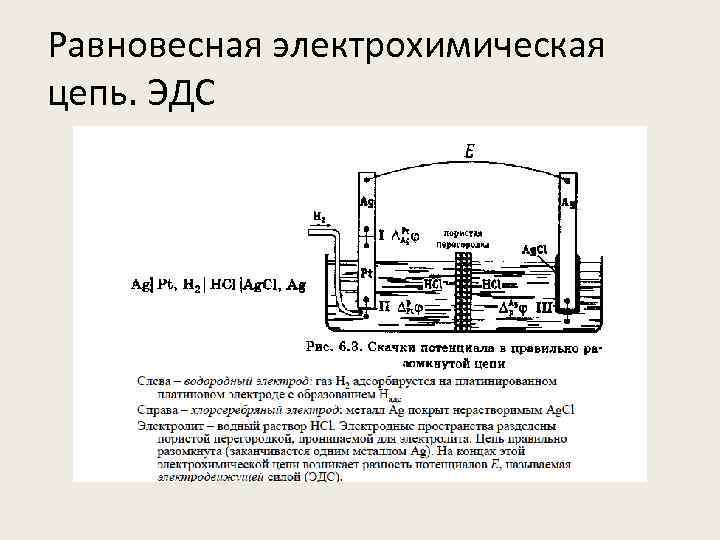 Равновесная электрохимическая цепь. ЭДС
Равновесная электрохимическая цепь. ЭДС
 Равновесие на границе Ме-Ме и Мегаз
Равновесие на границе Ме-Ме и Мегаз
 Равновесие на границе Ме-соль Ме
Равновесие на границе Ме-соль Ме
 Эмпирическое определение изменения свободной энергии
Эмпирическое определение изменения свободной энергии
 Диффузионный потенциал - это гальванипотенциал, возникающий на границе двух растворов разного состава.
Диффузионный потенциал - это гальванипотенциал, возникающий на границе двух растворов разного состава.
 Электрохимическая цепь с переносом • Электрохимическая цепь, содержащая границу двух растворов, называется цепью с переносом • М 1 |раствор 1 раствор 2 | М 1 • Пунктирная вертикальная черта указывает на существование диффузного потенциала между двумя растворами
Электрохимическая цепь с переносом • Электрохимическая цепь, содержащая границу двух растворов, называется цепью с переносом • М 1 |раствор 1 раствор 2 | М 1 • Пунктирная вертикальная черта указывает на существование диффузного потенциала между двумя растворами
 Элиминирование диффузного потенциала
Элиминирование диффузного потенциала
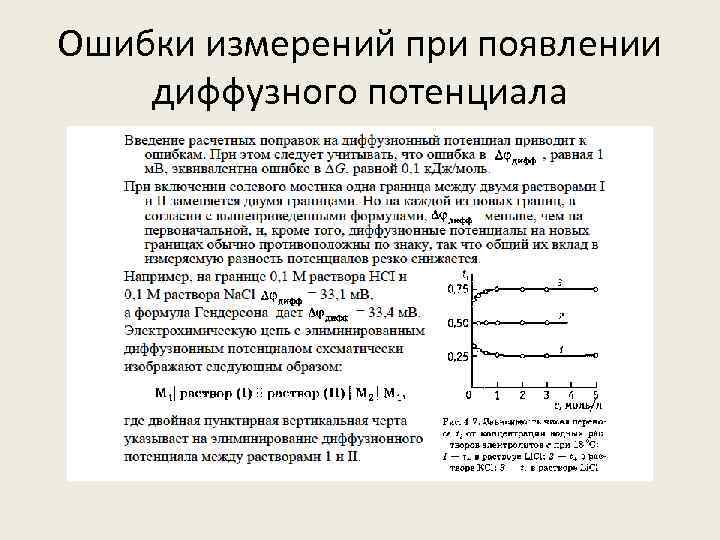 Ошибки измерений при появлении диффузного потенциала
Ошибки измерений при появлении диффузного потенциала
 Измерение электродвижущей силы E
Измерение электродвижущей силы E
 Зависимость ЭДС от активностей компонентов
Зависимость ЭДС от активностей компонентов
 уравнение Нернста для ЭДС электрохимической цепи
уравнение Нернста для ЭДС электрохимической цепи
 Вальтер Нернст. Один из основоположников физической химии (1864– 1941)
Вальтер Нернст. Один из основоположников физической химии (1864– 1941)
 Контрольные вопросы • Чем вызываются неравновесные явления в растворах электролитов • В чем основное отличие удельной и эквивалентной электропроводности • Какой механизм объясняет электропроводность воды • Каким потоком обеспечивается электропроводность • Из каких потенциалов складывается электрохимический потенциал
Контрольные вопросы • Чем вызываются неравновесные явления в растворах электролитов • В чем основное отличие удельной и эквивалентной электропроводности • Какой механизм объясняет электропроводность воды • Каким потоком обеспечивается электропроводность • Из каких потенциалов складывается электрохимический потенциал


