Гальванические элементы.ppt
- Количество слайдов: 28
 Электрохимия Гальванические элементы 1
Электрохимия Гальванические элементы 1
 План лекции ® Общие понятия ® Расчет ЭДС гальванических элементов ® Диффузионный потенциал ® Мембранный потенциал ® Потенциометрия 2
План лекции ® Общие понятия ® Расчет ЭДС гальванических элементов ® Диффузионный потенциал ® Мембранный потенциал ® Потенциометрия 2
 Гальванический элемент ® Устройство, состоящее из двух электродов, дающее возможность получать электрический ток в результате химической реакции 3
Гальванический элемент ® Устройство, состоящее из двух электродов, дающее возможность получать электрический ток в результате химической реакции 3
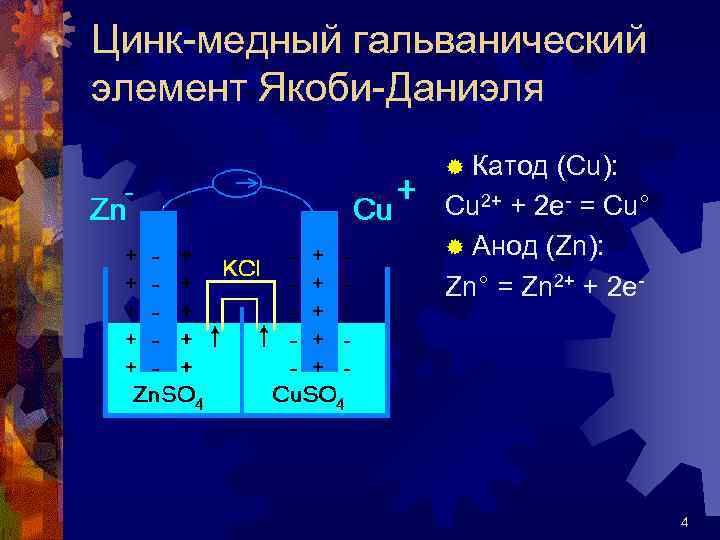 Цинк-медный гальванический элемент Якоби-Даниэля ® Катод (Сu): Cu 2+ + 2 e- = Cu° ® Анод (Zn): Zn° = Zn 2+ + 2 e- 4
Цинк-медный гальванический элемент Якоби-Даниэля ® Катод (Сu): Cu 2+ + 2 e- = Cu° ® Анод (Zn): Zn° = Zn 2+ + 2 e- 4
 ЭДС гальванического элемента, составленного из двух металлов Из потенциала положительно заряженного электрода вычитают потенциал отрицательно заряженного электрода ЭДС = Еcu - ЕZn 0, 2 T Еcu = E°Cu + ---- lg a(Cu 2+) n 0, 2 T ЕZn = E°Zn + ---- lg a(Zn 2+) n 0, 2 T a(Cu 2+) ЭДС = E°Cu - E°Zn + ------ lg -----n a(Zn 2+) ® 5
ЭДС гальванического элемента, составленного из двух металлов Из потенциала положительно заряженного электрода вычитают потенциал отрицательно заряженного электрода ЭДС = Еcu - ЕZn 0, 2 T Еcu = E°Cu + ---- lg a(Cu 2+) n 0, 2 T ЕZn = E°Zn + ---- lg a(Zn 2+) n 0, 2 T a(Cu 2+) ЭДС = E°Cu - E°Zn + ------ lg -----n a(Zn 2+) ® 5
 ЭДС зависит от: ® Положения металлов в ряду напряжений ® Соотношения ионов взятых растворов 6
ЭДС зависит от: ® Положения металлов в ряду напряжений ® Соотношения ионов взятых растворов 6
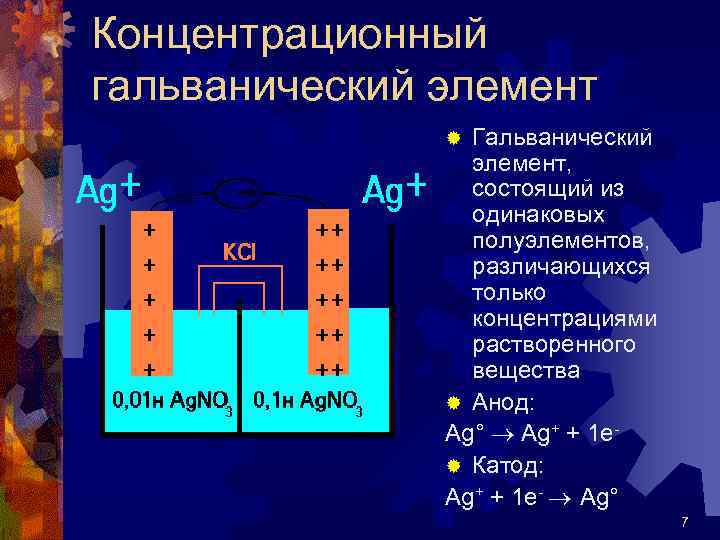 Концентрационный гальванический элемент Гальванический элемент, состоящий из одинаковых полуэлементов, различающихся только концентрациями растворенного вещества ® Анод: Ag° Ag+ + 1 e® Катод: Ag+ + 1 e- Ag° ® 7
Концентрационный гальванический элемент Гальванический элемент, состоящий из одинаковых полуэлементов, различающихся только концентрациями растворенного вещества ® Анод: Ag° Ag+ + 1 e® Катод: Ag+ + 1 e- Ag° ® 7
 ЭДC концентрационного гальванического элемента ЭДС = ЕAg 1 – EAg 2 0, 2 T ЕAg 1 = E°Ag 1 + ---- lg a(Ag 1) n 0, 2 T ЕAg 2 = E°Ag 2 + ---- lg a(Ag 2) n 0, 2 T a(Ag 1) ЭДС = ------ lg -----n a(Ag 2) ЭДС элемента зависит от соотношения активностей ионов и быстро падает во времени 8
ЭДC концентрационного гальванического элемента ЭДС = ЕAg 1 – EAg 2 0, 2 T ЕAg 1 = E°Ag 1 + ---- lg a(Ag 1) n 0, 2 T ЕAg 2 = E°Ag 2 + ---- lg a(Ag 2) n 0, 2 T a(Ag 1) ЭДС = ------ lg -----n a(Ag 2) ЭДС элемента зависит от соотношения активностей ионов и быстро падает во времени 8
 Измеряя ЭДС концентрационного элемента можно практически определить: ® Активность ионов ® Коэффициент активности ионов ® Неизвестную концентрацию раствора а=f C 9
Измеряя ЭДС концентрационного элемента можно практически определить: ® Активность ионов ® Коэффициент активности ионов ® Неизвестную концентрацию раствора а=f C 9
 Пример Цепь из двух водородных электродов: нормального – электрод сравнения и заполненного исследуемым раствором с неизвестной концентрацией Н+ – электрод определения ЭДС = ЕН° – ЕНХ; ЕН° = 0; 0, 2 Т ЕНХ = ЕН° + -----lg[H+] n 0, 2 Т ЭДС = 0 – -----lg[H+]; ЭДС = 0, 2 Т р. Н n ЭДС р. Н = -----0, 2 Т 10
Пример Цепь из двух водородных электродов: нормального – электрод сравнения и заполненного исследуемым раствором с неизвестной концентрацией Н+ – электрод определения ЭДС = ЕН° – ЕНХ; ЕН° = 0; 0, 2 Т ЕНХ = ЕН° + -----lg[H+] n 0, 2 Т ЭДС = 0 – -----lg[H+]; ЭДС = 0, 2 Т р. Н n ЭДС р. Н = -----0, 2 Т 10
 Диффузионный потенциал Разность потенциалов, возникающая на границе раздела между двумя неодинаковыми по составу или по концентрации растворами l(H+) = 315 Ом-1 см 2 l(Cl-) = 65, 5 Ом-1 см 2 ® 11
Диффузионный потенциал Разность потенциалов, возникающая на границе раздела между двумя неодинаковыми по составу или по концентрации растворами l(H+) = 315 Ом-1 см 2 l(Cl-) = 65, 5 Ом-1 см 2 ® 11
 Диффузионный потенциал усредняет скорости движения ионов при сохранении скачка потенциала на границе раздела растворов разной концентрации В результате движения ионов в электролитическом мостике возникает диффузионный потенциал, направленный противоположно ЭДС гальванического элемента Его влияние устраняют, включая между растворами электролитов насыщенный раствор KCl или KNO 3, так как подвижности ионов примерно одинаковы: l (K+) = 64, 4 Ом-1 см 2 l (Cl-) = 65, 5 Ом-1 см 2 12
Диффузионный потенциал усредняет скорости движения ионов при сохранении скачка потенциала на границе раздела растворов разной концентрации В результате движения ионов в электролитическом мостике возникает диффузионный потенциал, направленный противоположно ЭДС гальванического элемента Его влияние устраняют, включая между растворами электролитов насыщенный раствор KCl или KNO 3, так как подвижности ионов примерно одинаковы: l (K+) = 64, 4 Ом-1 см 2 l (Cl-) = 65, 5 Ом-1 см 2 12
 Диффузионные потенциалы в биологических объектах ® Потенциал повреждения (поврежденная ткань заряжается отрицательно) составляет 30 – 40 м. В 13
Диффузионные потенциалы в биологических объектах ® Потенциал повреждения (поврежденная ткань заряжается отрицательно) составляет 30 – 40 м. В 13
 Межфазовые потенциалы Возникают: ® На границе раздела между двумя несмешивающимися жидкостями; обусловлены неодинаковой растворимостью в них веществ ® На поверхности макромолекул в результате избирательного сродства поверхности к различным ионам 14
Межфазовые потенциалы Возникают: ® На границе раздела между двумя несмешивающимися жидкостями; обусловлены неодинаковой растворимостью в них веществ ® На поверхности макромолекул в результате избирательного сродства поверхности к различным ионам 14
 Мембранный потенциал ® Потенциал, возникающий на мембране с избирательной проницаемостью (пропускающей только ионы одного знака), разделяющей два раствора различного состава – СОО- : катионы – NH 3+ : анионы 15
Мембранный потенциал ® Потенциал, возникающий на мембране с избирательной проницаемостью (пропускающей только ионы одного знака), разделяющей два раствора различного состава – СОО- : катионы – NH 3+ : анионы 15
 Потенциал покоя мембранный потенциал, возникающий между внутренней и наружной сторонами клеточной мембраны, находящейся в невозбужденном состоянии: –(70 -80) м. В ® 16
Потенциал покоя мембранный потенциал, возникающий между внутренней и наружной сторонами клеточной мембраны, находящейся в невозбужденном состоянии: –(70 -80) м. В ® 16
 Возбужденное состояние клетки проницаемость мембраны для ионов Na+ Перемена знака на поверхности мембраны – деполяризация: +(40 -60) м. В 17
Возбужденное состояние клетки проницаемость мембраны для ионов Na+ Перемена знака на поверхности мембраны – деполяризация: +(40 -60) м. В 17
 Потенциал действия ® Разность между потенциалом покоя и зарядом мембраны в возбужденном состоянии (амплитуда колебания мембранного потенциала) (120 – 140 м. В) В результате активной работы К+ / Na+ насоса наступает реполяризация – клетка возвращается в состояние покоя 18
Потенциал действия ® Разность между потенциалом покоя и зарядом мембраны в возбужденном состоянии (амплитуда колебания мембранного потенциала) (120 – 140 м. В) В результате активной работы К+ / Na+ насоса наступает реполяризация – клетка возвращается в состояние покоя 18
 Потенциометрия ® Физико-химический метод анализа, в основе которого лежит измерение ЭДС цепи, составленной из индикаторного электрода и электрода сравнения 19
Потенциометрия ® Физико-химический метод анализа, в основе которого лежит измерение ЭДС цепи, составленной из индикаторного электрода и электрода сравнения 19
 Методы потенциометрии ® Прямые – определение активности и концентрации ионов или веществ в растворе ® Косвенные – определение концентрации неизвестного вещества при добавлении к нему другого (потенциометрическое титрование) 20
Методы потенциометрии ® Прямые – определение активности и концентрации ионов или веществ в растворе ® Косвенные – определение концентрации неизвестного вещества при добавлении к нему другого (потенциометрическое титрование) 20
 Прямая потенциометрия Электроды сравнения – электроды, потенциал которых практически постоянен, легко воспроизводим и не зависит от протекания побочных реакций ® Электроды определения – электроды, потенциал которых зависит от активности (концентрации) анализируемых ионов и практически не зависит от содержания других ионов в растворе Используют для измерения р. Н, концентрации биологически активных ионов: H+, Na+, K+, NH 4+, Ca 2+, NO 3 -, различных веществ в биологических средах ® 21
Прямая потенциометрия Электроды сравнения – электроды, потенциал которых практически постоянен, легко воспроизводим и не зависит от протекания побочных реакций ® Электроды определения – электроды, потенциал которых зависит от активности (концентрации) анализируемых ионов и практически не зависит от содержания других ионов в растворе Используют для измерения р. Н, концентрации биологически активных ионов: H+, Na+, K+, NH 4+, Ca 2+, NO 3 -, различных веществ в биологических средах ® 21
 Индикаторные электроды Мембранные: ионоселективные – способны определять в растворе концентрацию одного иона С твердыми мембранами ® Стеклянный ® С жидкими мембранами ® Молекулярно-селективные – позволяют определять концентрацию молекул вещества (ферментные – мембрана содержит определенный фермент) 22
Индикаторные электроды Мембранные: ионоселективные – способны определять в растворе концентрацию одного иона С твердыми мембранами ® Стеклянный ® С жидкими мембранами ® Молекулярно-селективные – позволяют определять концентрацию молекул вещества (ферментные – мембрана содержит определенный фермент) 22
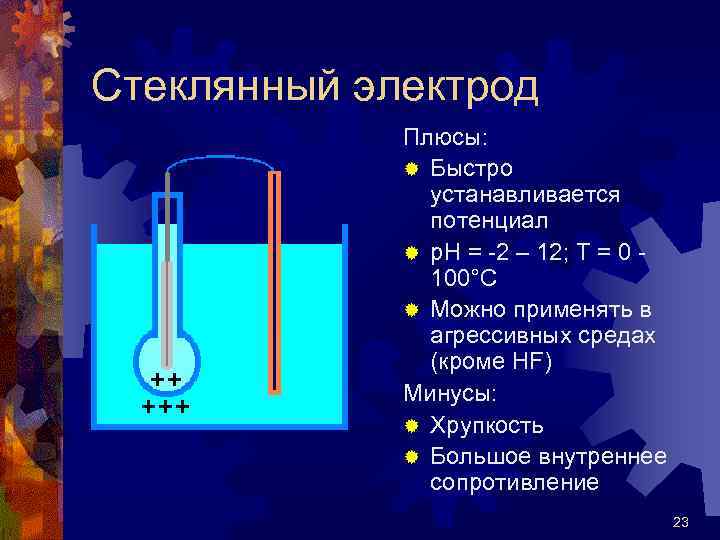 Стеклянный электрод Плюсы: ® Быстро устанавливается потенциал ® р. Н = -2 – 12; Т = 0 100°С ® Можно применять в агрессивных средах (кроме HF) Минусы: ® Хрупкость ® Большое внутреннее сопротивление 23
Стеклянный электрод Плюсы: ® Быстро устанавливается потенциал ® р. Н = -2 – 12; Т = 0 100°С ® Можно применять в агрессивных средах (кроме HF) Минусы: ® Хрупкость ® Большое внутреннее сопротивление 23
 Ионоселективные электроды ® Действие основано на возникновении мембранного потенциала на мембране с избирательной чувствительностью к данному иону (калиевый, нитратный) Ионоселективных электродов с четкой выраженностью к определенным ионам насчитывается более 20 (К+, Ca 2+, Pb 2+, Cu 2+, Cl-, NO 3 -, Cl. O 4 -, CNS-, S 2 -, CN-, F- и др. ) 24
Ионоселективные электроды ® Действие основано на возникновении мембранного потенциала на мембране с избирательной чувствительностью к данному иону (калиевый, нитратный) Ионоселективных электродов с четкой выраженностью к определенным ионам насчитывается более 20 (К+, Ca 2+, Pb 2+, Cu 2+, Cl-, NO 3 -, Cl. O 4 -, CNS-, S 2 -, CN-, F- и др. ) 24
 Мембранный электрод ® С твердыми мембранами – метеллическая или кристаллическая пластинка, содержащая тот ион, который нужно определить в растворе ® С жидкими мембранами – пористый материал, пропитанный ионогенным веществом 25
Мембранный электрод ® С твердыми мембранами – метеллическая или кристаллическая пластинка, содержащая тот ион, который нужно определить в растворе ® С жидкими мембранами – пористый материал, пропитанный ионогенным веществом 25
 Ферментные электроды ® Мочевино-селективный уреаза СО(NH 2)2 NH 4+ ® Пенициллино-селективный пенициллиназа пенициллиновая кислота Позволяют определять глюкозу, антибиотики, витамины, гормоны, аминокислоты и другие БАВ Пенициллин 26
Ферментные электроды ® Мочевино-селективный уреаза СО(NH 2)2 NH 4+ ® Пенициллино-селективный пенициллиназа пенициллиновая кислота Позволяют определять глюкозу, антибиотики, витамины, гормоны, аминокислоты и другие БАВ Пенициллин 26
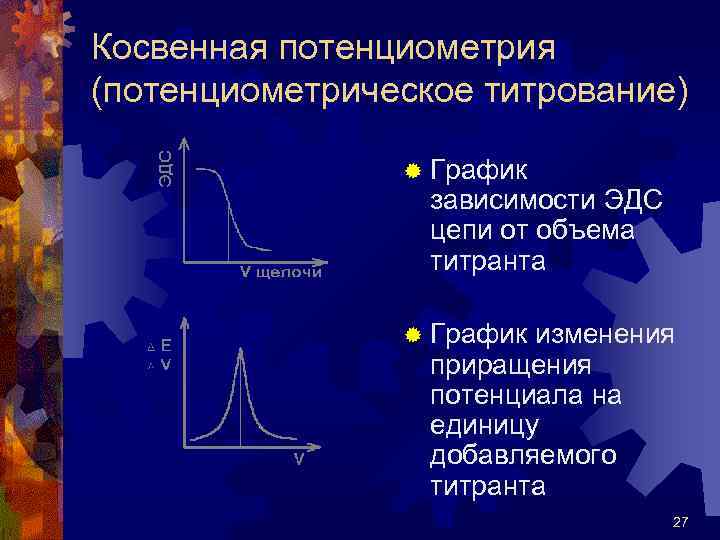 Косвенная потенциометрия (потенциометрическое титрование) ® График зависимости ЭДС цепи от объема титранта ® График изменения приращения потенциала на единицу добавляемого титранта 27
Косвенная потенциометрия (потенциометрическое титрование) ® График зависимости ЭДС цепи от объема титранта ® График изменения приращения потенциала на единицу добавляемого титранта 27
 Значение потенциометрических методов исследования ® Определение концентрации веществ в мутных и окрашенных растворах ® Определение концентрации нескольких веществ в одной порции исследуемого раствора ® Измерение р. Н среды (р. Н-метры, иономеры, полярографы) ® Определение констант диссоциации слабых кислот, аминокислот, белков, нуклеиновых кислот ® Определение констант нестойкости комплексных соединений 28
Значение потенциометрических методов исследования ® Определение концентрации веществ в мутных и окрашенных растворах ® Определение концентрации нескольких веществ в одной порции исследуемого раствора ® Измерение р. Н среды (р. Н-метры, иономеры, полярографы) ® Определение констант диссоциации слабых кислот, аминокислот, белков, нуклеиновых кислот ® Определение констант нестойкости комплексных соединений 28


