ряд напряжения получение.pptx
- Количество слайдов: 18

 Электрохимический ряд напряжений металлов Уменьшение восстановительных свойств Усиление окислительных свойств Металлы Соединения металлов Внешний вид и условия хранения Оксиды Нахождение в природе Гидроксиды Получение металлов Соли Химические свойства металлов Проверь себя
Электрохимический ряд напряжений металлов Уменьшение восстановительных свойств Усиление окислительных свойств Металлы Соединения металлов Внешний вид и условия хранения Оксиды Нахождение в природе Гидроксиды Получение металлов Соли Химические свойства металлов Проверь себя
 Внешний вид и условия хранения Li K Ba Mn Zn Cr Sn Pb Cu Sr Ca Fe Hg Na Cd Ag Mg Co Pt Al Ni Au
Внешний вид и условия хранения Li K Ba Mn Zn Cr Sn Pb Cu Sr Ca Fe Hg Na Cd Ag Mg Co Pt Al Ni Au
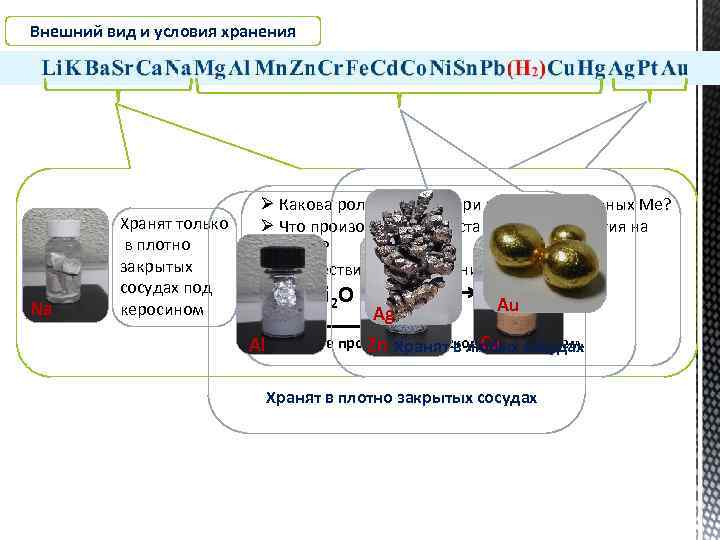 Внешний вид и условия хранения Na Хранят только в плотно закрытых сосудах под керосином Ø Какова роль керосина при хранении активных Ме? Ø Что произойдет, если оставить кусочек лития на воздухе? Ø Осуществите превращения: Li Li 2 O Ag Li. OH Li. Au 3 2 CO Объясните процессы, происходящие ссосудах Cu Al Zn Хранят в любых литием. Хранят в плотно закрытых сосудах
Внешний вид и условия хранения Na Хранят только в плотно закрытых сосудах под керосином Ø Какова роль керосина при хранении активных Ме? Ø Что произойдет, если оставить кусочек лития на воздухе? Ø Осуществите превращения: Li Li 2 O Ag Li. OH Li. Au 3 2 CO Объясните процессы, происходящие ссосудах Cu Al Zn Хранят в любых литием. Хранят в плотно закрытых сосудах
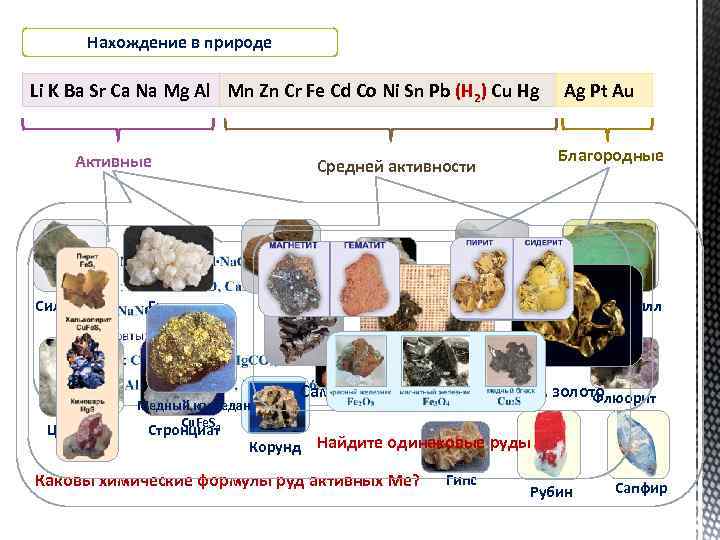 Нахождение в природе Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn Pb (Н 2) Cu Hg Активные Сильвинит Целестит Барит Медный колчедан Cu. Fe. S 2 Стронциат Благородные Средней активности Галит Магнезит Ag Pt Au Кальцит Хризоберилл Самородные серебро, платина, золото Флюорит Боксит Фосфорит Корунд Найдите одинаковые руды Каковы химические формулы руд активных Ме? Гипс Рубин Сапфир
Нахождение в природе Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn Pb (Н 2) Cu Hg Активные Сильвинит Целестит Барит Медный колчедан Cu. Fe. S 2 Стронциат Благородные Средней активности Галит Магнезит Ag Pt Au Кальцит Хризоберилл Самородные серебро, платина, золото Флюорит Боксит Фосфорит Корунд Найдите одинаковые руды Каковы химические формулы руд активных Ме? Гипс Рубин Сапфир
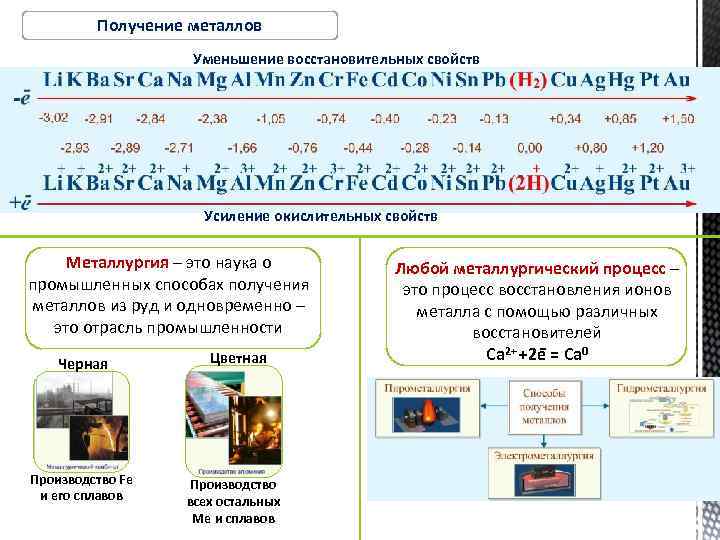 Получение металлов Уменьшение восстановительных свойств Усиление окислительных свойств Металлургия – это наука о промышленных способах получения металлов из руд и одновременно – это отрасль промышленности Черная Производство Fe и его сплавов Цветная Производство всех остальных Ме и сплавов Любой металлургический процесс – это процесс восстановления ионов металла с помощью различных восстановителей Ca 2+ +2 e = Ca 0
Получение металлов Уменьшение восстановительных свойств Усиление окислительных свойств Металлургия – это наука о промышленных способах получения металлов из руд и одновременно – это отрасль промышленности Черная Производство Fe и его сплавов Цветная Производство всех остальных Ме и сплавов Любой металлургический процесс – это процесс восстановления ионов металла с помощью различных восстановителей Ca 2+ +2 e = Ca 0
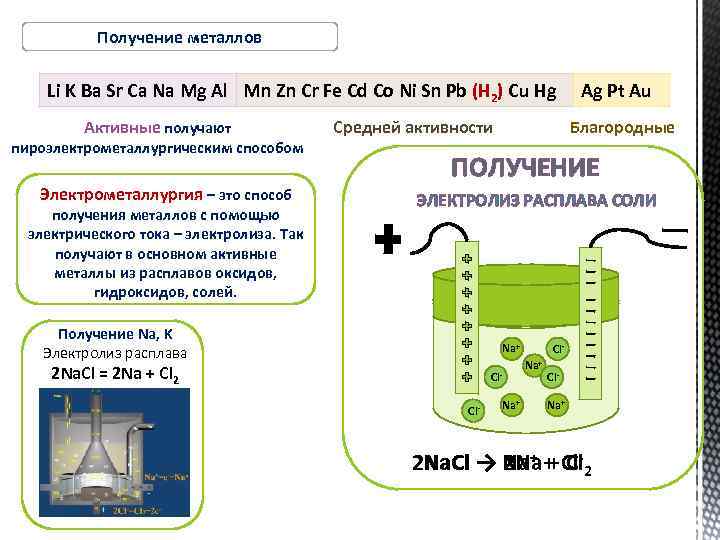 Получение металлов Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn Pb (Н 2) Cu Hg Активные получают пироэлектрометаллургическим способом Электрометаллургия – это способ получения металлов с помощью электрического тока – электролиза. Так получают в основном активные металлы из расплавов оксидов, гидроксидов, солей. Средней активности Ag Pt Au Благородные ПОЛУЧЕНИЕ ЭЛЕКТРОЛИЗ РАСПЛАВА СОЛИ Получение Na, K Электролиз расплава Na+ 2 Na. Cl = 2 Na + Cl 2 Cl. Cl- Na+ Cl. Na+ 2 Na. Cl → Na+ + Cl-2 Na. Cl 2 Na + Cl
Получение металлов Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn Pb (Н 2) Cu Hg Активные получают пироэлектрометаллургическим способом Электрометаллургия – это способ получения металлов с помощью электрического тока – электролиза. Так получают в основном активные металлы из расплавов оксидов, гидроксидов, солей. Средней активности Ag Pt Au Благородные ПОЛУЧЕНИЕ ЭЛЕКТРОЛИЗ РАСПЛАВА СОЛИ Получение Na, K Электролиз расплава Na+ 2 Na. Cl = 2 Na + Cl 2 Cl. Cl- Na+ Cl. Na+ 2 Na. Cl → Na+ + Cl-2 Na. Cl 2 Na + Cl
 Получение металлов Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn Pb (Н 2) Cu Hg Активные получают пироэлектрометаллургическим способом Средней активности Ag Pt Au Благородные Электрометаллургия – это способ получения металлов с помощью электрического тока – электролиза. Так получают в основном активные металлы из расплавов оксидов, гидроксидов, солей. Получение Аl электролизом Аl 2 O 3 Электролизер для получения Аl T 950°C, Al 2 O 3 в расплаве криолита (Na 3 Al. F 6); на катоде: Al 3+ + 3 e = Al 0 На угольном аноде (расходуется в процессе электролиза): O 2 -- 2 e = O 0; C + O = CO↑; 2 CO + O 2 = 2 CO 2↑;
Получение металлов Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn Pb (Н 2) Cu Hg Активные получают пироэлектрометаллургическим способом Средней активности Ag Pt Au Благородные Электрометаллургия – это способ получения металлов с помощью электрического тока – электролиза. Так получают в основном активные металлы из расплавов оксидов, гидроксидов, солей. Получение Аl электролизом Аl 2 O 3 Электролизер для получения Аl T 950°C, Al 2 O 3 в расплаве криолита (Na 3 Al. F 6); на катоде: Al 3+ + 3 e = Al 0 На угольном аноде (расходуется в процессе электролиза): O 2 -- 2 e = O 0; C + O = CO↑; 2 CO + O 2 = 2 CO 2↑;
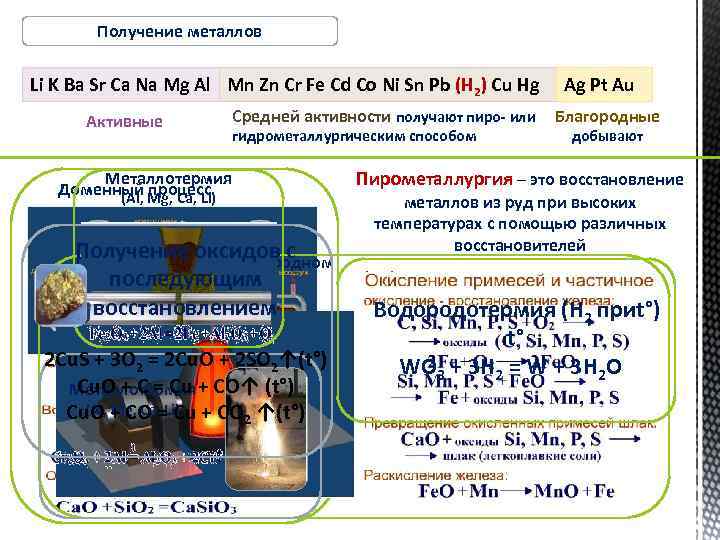 Получение металлов Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn Pb (Н 2) Cu Hg Активные Средней активности получают пиро- или гидрометаллургическим способом Металлотермия Доменный Mg, Ca, Li) (Al, процесс Получение оксидов с Получение стали в кислородном последующим конвертере восстановлением 2 Cu. S + 3 O 2 = 2 Cu. O + 2 SO 2↑(t°) Cu. O + C = Cu Металлотермия + CO↑ (t°) (Al, Mg, Ca, Cu Cu. O + CO =Li) + CO 2 ↑(t°) Ag Pt Au Благородные добывают Пирометаллургия – это восстановление металлов из руд при высоких температурах с помощью различных восстановителей Водородотермия (Н 2 приt°) t° WO 3 + 3 H 2 = W + 3 H 2 O
Получение металлов Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn Pb (Н 2) Cu Hg Активные Средней активности получают пиро- или гидрометаллургическим способом Металлотермия Доменный Mg, Ca, Li) (Al, процесс Получение оксидов с Получение стали в кислородном последующим конвертере восстановлением 2 Cu. S + 3 O 2 = 2 Cu. O + 2 SO 2↑(t°) Cu. O + C = Cu Металлотермия + CO↑ (t°) (Al, Mg, Ca, Cu Cu. O + CO =Li) + CO 2 ↑(t°) Ag Pt Au Благородные добывают Пирометаллургия – это восстановление металлов из руд при высоких температурах с помощью различных восстановителей Водородотермия (Н 2 приt°) t° WO 3 + 3 H 2 = W + 3 H 2 O
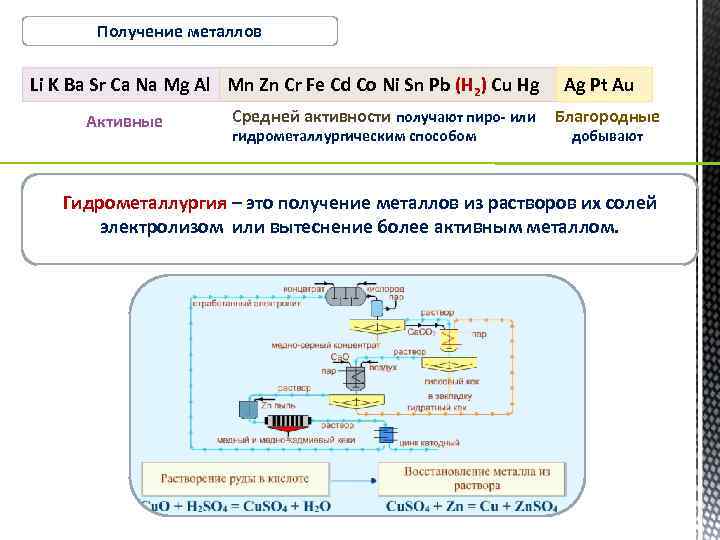 Получение металлов Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn Pb (Н 2) Cu Hg Активные Средней активности получают пиро- или гидрометаллургическим способом Ag Pt Au Благородные добывают Гидрометаллургия – это получение металлов из растворов их солей электролизом или вытеснение более активным металлом.
Получение металлов Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn Pb (Н 2) Cu Hg Активные Средней активности получают пиро- или гидрометаллургическим способом Ag Pt Au Благородные добывают Гидрометаллургия – это получение металлов из растворов их солей электролизом или вытеснение более активным металлом.
 Химические свойства металлов Окисляются при комнатной температуре При обычных условиях взаимодействуют с водой с образованием щелочи и Н 2 ↑ При комн. t°окисл. только с поверх. Окисляются только при нагревании С водой взаимодействуют только при нагревании с образованием оксида и Н 2↑ Помни! 2 Al + 6 HOH → 2 Al(OH)3 + 3 H 2↑ (если снять оксидную пленку) При t° не окисл яются С водой не взаимодействуют Коррозионная устойчивость чистых металлов усиливается Из растворов кислот вытесняют водород (исключение HNO 3) Помни! Щелочные и щелочноземельные металлы в водных растворах взаимодействуют прежде всего с Н 2 О Из растворов кислот не вытесняют водород Взаимодействуют с серной кислотой (конц. ). В зависимости от условий и восстановительных свойств Ме образуются SO 2, S, H 2 S (Fe, Ni и некоторые металлы в H 2 SO 4 (конц. ) на холоду пассивируются). Не взаим одейст вуют
Химические свойства металлов Окисляются при комнатной температуре При обычных условиях взаимодействуют с водой с образованием щелочи и Н 2 ↑ При комн. t°окисл. только с поверх. Окисляются только при нагревании С водой взаимодействуют только при нагревании с образованием оксида и Н 2↑ Помни! 2 Al + 6 HOH → 2 Al(OH)3 + 3 H 2↑ (если снять оксидную пленку) При t° не окисл яются С водой не взаимодействуют Коррозионная устойчивость чистых металлов усиливается Из растворов кислот вытесняют водород (исключение HNO 3) Помни! Щелочные и щелочноземельные металлы в водных растворах взаимодействуют прежде всего с Н 2 О Из растворов кислот не вытесняют водород Взаимодействуют с серной кислотой (конц. ). В зависимости от условий и восстановительных свойств Ме образуются SO 2, S, H 2 S (Fe, Ni и некоторые металлы в H 2 SO 4 (конц. ) на холоду пассивируются). Не взаим одейст вуют
 Химические свойства металлов Главная Взаимодействуют с разбавленной и концентрированной азотной кислотой и в зависимости от условий, восстановительных свойств металлов, концентрации кислоты образуются N 2, N 2 O, N 2 O 3, NO 2 u NH 3 (NH 4 NO 3). Al, Fe, Cr в концентрированной азотной кислоте пассивируются. С HNO 3 не реагиру ют С разбавленной H 2 SO 4 взаимодействуют с образованием Н 2 С раствором H 2 SO 4 не реагируют С HCl взаимодействуют с образованием Н 2 C HCl не реагируют Каждый впереди стоящий металл вытесняет все последующие металлы из растворов и расплавов их солей При электролизе сначала изменяется тот катион, металл которого находится правее в электрохимическом ряду напряжений металлов Примечание: среди закономерностей, связывающих ряд напряжений металлов и химические свойства Ме и их соединений, есть исключения из правил. Будьте внимательны, обратитесь к теории!
Химические свойства металлов Главная Взаимодействуют с разбавленной и концентрированной азотной кислотой и в зависимости от условий, восстановительных свойств металлов, концентрации кислоты образуются N 2, N 2 O, N 2 O 3, NO 2 u NH 3 (NH 4 NO 3). Al, Fe, Cr в концентрированной азотной кислоте пассивируются. С HNO 3 не реагиру ют С разбавленной H 2 SO 4 взаимодействуют с образованием Н 2 С раствором H 2 SO 4 не реагируют С HCl взаимодействуют с образованием Н 2 C HCl не реагируют Каждый впереди стоящий металл вытесняет все последующие металлы из растворов и расплавов их солей При электролизе сначала изменяется тот катион, металл которого находится правее в электрохимическом ряду напряжений металлов Примечание: среди закономерностей, связывающих ряд напряжений металлов и химические свойства Ме и их соединений, есть исключения из правил. Будьте внимательны, обратитесь к теории!
 Соединения металлов Растворяются в Н 2 О с образованием щелочей Оксиды не растворяются в воде Оксиды При нагревании оксиды не разлагаются При t°разлагаются Гидроксиды разлагаются в воде Гидроксиды растворяются в воде Гидроксиды при t° не разлагаются Нитраты при t° разлагаются на нитриты и О 2 Cоли, образованные сильными кислотами не гидролизуются Cоли, образованные слабыми кислотами гидролизуются (среда щелочная). Гидроксиды не растворяются в воде Гидроксиды при t° разлагаются на воду и оксиды Соли Нитраты при t° разлагаются на оксид, NO 2 и О 2 При t° разлагаются на Ме, Н 2 О и О 2 Нитраты при t° разлагаются на Ме, NO 2 и О 2 Гидролиз солей Cоли, образованные сильными кислотами, гидролизуются с образованием кислой среды Существующие и растворимые соли, образованные слабыми кислотами, гидролизуются полностью
Соединения металлов Растворяются в Н 2 О с образованием щелочей Оксиды не растворяются в воде Оксиды При нагревании оксиды не разлагаются При t°разлагаются Гидроксиды разлагаются в воде Гидроксиды растворяются в воде Гидроксиды при t° не разлагаются Нитраты при t° разлагаются на нитриты и О 2 Cоли, образованные сильными кислотами не гидролизуются Cоли, образованные слабыми кислотами гидролизуются (среда щелочная). Гидроксиды не растворяются в воде Гидроксиды при t° разлагаются на воду и оксиды Соли Нитраты при t° разлагаются на оксид, NO 2 и О 2 При t° разлагаются на Ме, Н 2 О и О 2 Нитраты при t° разлагаются на Ме, NO 2 и О 2 Гидролиз солей Cоли, образованные сильными кислотами, гидролизуются с образованием кислой среды Существующие и растворимые соли, образованные слабыми кислотами, гидролизуются полностью
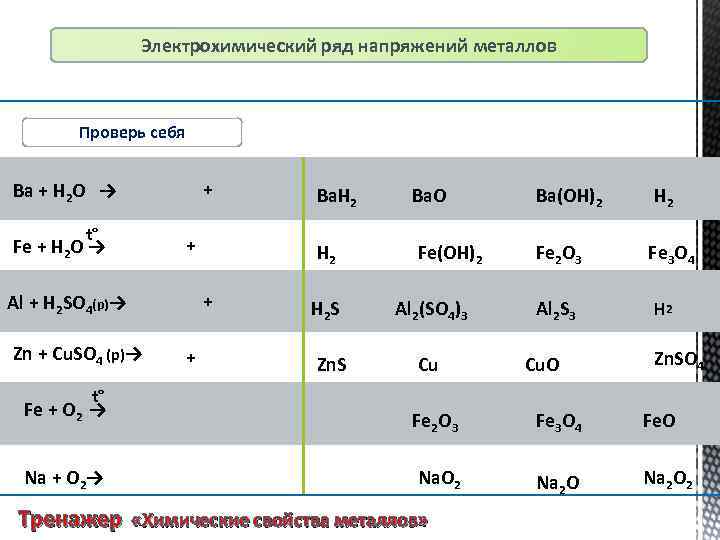 Электрохимический ряд напряжений металлов Проверь себя Ba + H 2 O → t° Fe + H 2 O → + Al + H 2 SO 4(р)→ Zn + Cu. SO 4 (р)→ + + Ba. O Ba(OH)2 H 2 + Ba. H 2 Fe(OH)2 Fe 2 O 3 Fe 3 O 4 H 2 S Zn. S Al 2(SO 4)3 Cu Al 2 S 3 Cu. O H 2 Zn. SO 4 t° Fe + O 2 → Na + O 2→ Fe 2 O 3 Fe 3 O 4 Fe. O Na. O 2 Na 2 O 2 Тренажер «Химические свойства металлов»
Электрохимический ряд напряжений металлов Проверь себя Ba + H 2 O → t° Fe + H 2 O → + Al + H 2 SO 4(р)→ Zn + Cu. SO 4 (р)→ + + Ba. O Ba(OH)2 H 2 + Ba. H 2 Fe(OH)2 Fe 2 O 3 Fe 3 O 4 H 2 S Zn. S Al 2(SO 4)3 Cu Al 2 S 3 Cu. O H 2 Zn. SO 4 t° Fe + O 2 → Na + O 2→ Fe 2 O 3 Fe 3 O 4 Fe. O Na. O 2 Na 2 O 2 Тренажер «Химические свойства металлов»
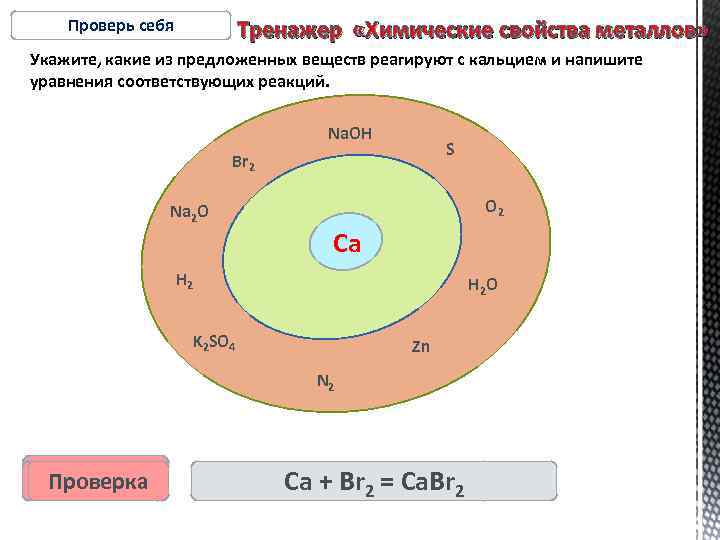 Проверь себя Тренажер «Химические свойства металлов» Укажите, какие из предложенных веществ реагируют с кальцием и напишите уравнения соответствующих реакций. Na. OH S Br 2 O 2 Na 2 O Са H 2 O K 2 SO 4 Zn N 2 Проверка Са +3 Са. О 2 = 22 Са. О 3 N 22 + Н 2 2 Са 2 Н 2 О Н Ca. S 2 Ca+++ Br 2 Са(ОН) Са + N = Ca. Н Са S = Ca. Br Ca
Проверь себя Тренажер «Химические свойства металлов» Укажите, какие из предложенных веществ реагируют с кальцием и напишите уравнения соответствующих реакций. Na. OH S Br 2 O 2 Na 2 O Са H 2 O K 2 SO 4 Zn N 2 Проверка Са +3 Са. О 2 = 22 Са. О 3 N 22 + Н 2 2 Са 2 Н 2 О Н Ca. S 2 Ca+++ Br 2 Са(ОН) Са + N = Ca. Н Са S = Ca. Br Ca
 Электрохимический ряд напряжений металлов Проверь себя Теоретические тесты с выбором ответа 1. Коэффициент перед формулой восстановителя в реакции, схема которой Ca + HNO 3 (конц. ) → Ca(NO 3)2 + N 2↑+ H 2 O а) 5; б) 10; в) 1; г) 12; 2. Коэффициент перед формулой окислителя в реакции, схема которой Zn + H 2 SO 4 (конц. ) → Zn. SO 4 + H 2 S↑ + H 2 O а) 1; б) 2; в) 4; г) 5; 3. В схеме превращений (1) (2) (3) (4) Al → Al(OH)3 → Al 2 O 3 → Al. Cl 3 → Al требуется провести электролиз расплава для осуществления реакции на этапе: а) 4; б) 2; в) 3; г) 4; г) 1; 4. В схеме превращений из теста 3 требуется провести прокаливание для осуществления реакции на этапе: а) 1; б) 2; в) 3; г) 4; б) 2; 5. При электролизе раствора Na. Cl образуются продукты а) Na; б) Na. OH; в) Cl 22; ; г) H 22; ; д) HCl; б) Na. OH; в) Cl г) H Проверка
Электрохимический ряд напряжений металлов Проверь себя Теоретические тесты с выбором ответа 1. Коэффициент перед формулой восстановителя в реакции, схема которой Ca + HNO 3 (конц. ) → Ca(NO 3)2 + N 2↑+ H 2 O а) 5; б) 10; в) 1; г) 12; 2. Коэффициент перед формулой окислителя в реакции, схема которой Zn + H 2 SO 4 (конц. ) → Zn. SO 4 + H 2 S↑ + H 2 O а) 1; б) 2; в) 4; г) 5; 3. В схеме превращений (1) (2) (3) (4) Al → Al(OH)3 → Al 2 O 3 → Al. Cl 3 → Al требуется провести электролиз расплава для осуществления реакции на этапе: а) 4; б) 2; в) 3; г) 4; г) 1; 4. В схеме превращений из теста 3 требуется провести прокаливание для осуществления реакции на этапе: а) 1; б) 2; в) 3; г) 4; б) 2; 5. При электролизе раствора Na. Cl образуются продукты а) Na; б) Na. OH; в) Cl 22; ; г) H 22; ; д) HCl; б) Na. OH; в) Cl г) H Проверка
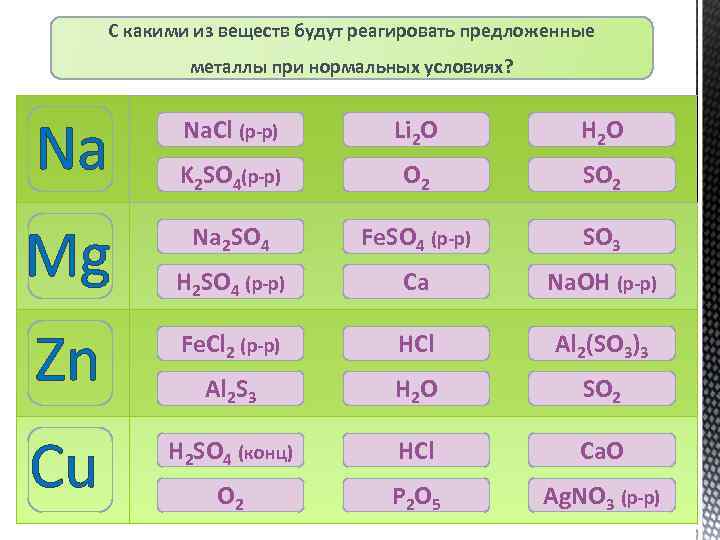 С какими из веществ будут реагировать предложенные металлы при нормальных условиях? Na Na. Cl (р-р) ошибка Li 2 O молодец H 2 O K 2 SO 4(р-р) ошибка молодец O 2 ошибка SO 2 ошибка Na 2 SO 4 Fe. SO 4 (р-р) молодец ошибка SO 3 H 2 SO 4 (р-р) молодец ошибка Ca Na. OH (р-р) ошибка Zn молодец Fe. Cl 2 (р-р) молодец HCl Al 2(SO 3)3 ошибка Al 2 S 3 ошибка H 2 O ошибка SO 2 Cu H 2 SO 4 (конц) молодец ошибка HCl ошибка Ca. O ошибка O 2 ошибка P 2 O 5 Ag. NO 3 (р-р) молодец Mg
С какими из веществ будут реагировать предложенные металлы при нормальных условиях? Na Na. Cl (р-р) ошибка Li 2 O молодец H 2 O K 2 SO 4(р-р) ошибка молодец O 2 ошибка SO 2 ошибка Na 2 SO 4 Fe. SO 4 (р-р) молодец ошибка SO 3 H 2 SO 4 (р-р) молодец ошибка Ca Na. OH (р-р) ошибка Zn молодец Fe. Cl 2 (р-р) молодец HCl Al 2(SO 3)3 ошибка Al 2 S 3 ошибка H 2 O ошибка SO 2 Cu H 2 SO 4 (конц) молодец ошибка HCl ошибка Ca. O ошибка O 2 ошибка P 2 O 5 Ag. NO 3 (р-р) молодец Mg
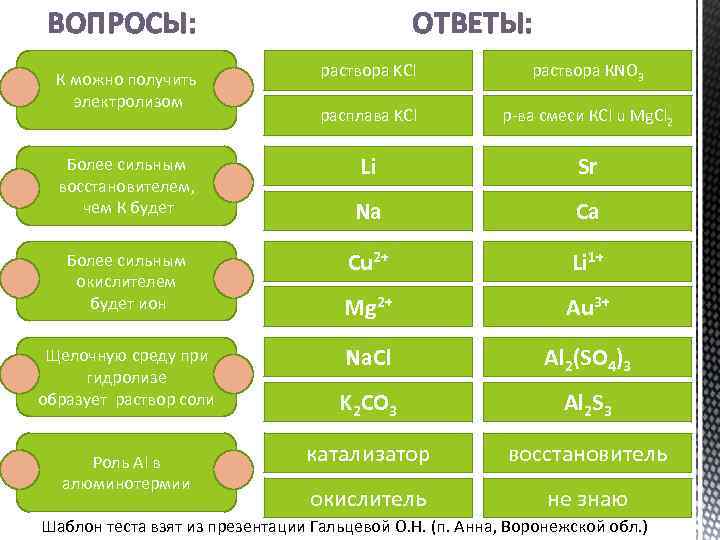 ВОПРОСЫ: К можно получить электролизом Более сильным восстановителем, чем К будет Более сильным окислителем будет ион Щелочную среду при гидролизе образует раствор соли Роль Al в алюминотермии ОТВЕТЫ: раствора KCl раствора КNO 3 расплава KCl р-ва смеси КCl u Mg. Cl 2 Li Sr Na Ca Cu 2+ Li 1+ Mg 2+ Au 3+ Na. Cl Al 2(SO 4)3 K 2 CO 3 Al 2 S 3 катализатор восстановитель окислитель не знаю Шаблон теста взят из презентации Гальцевой О. Н. (п. Анна, Воронежской обл. )
ВОПРОСЫ: К можно получить электролизом Более сильным восстановителем, чем К будет Более сильным окислителем будет ион Щелочную среду при гидролизе образует раствор соли Роль Al в алюминотермии ОТВЕТЫ: раствора KCl раствора КNO 3 расплава KCl р-ва смеси КCl u Mg. Cl 2 Li Sr Na Ca Cu 2+ Li 1+ Mg 2+ Au 3+ Na. Cl Al 2(SO 4)3 K 2 CO 3 Al 2 S 3 катализатор восстановитель окислитель не знаю Шаблон теста взят из презентации Гальцевой О. Н. (п. Анна, Воронежской обл. )


