4.Студентам- Элхимия.ppt
- Количество слайдов: 20
 Электрохимический ряд активности (ряд напряжений Р. Н. ) ЭХРН Хим. характер металла во многом обусловлен тем, насколько легко он окисляется, т. е. насколько легко его атомы могут переходить в состояние + ионов М 0 – nē Mn+ неблагородные металлы окисляются легко Li, K, Ba, Ca, Na, Mg, Al, Mn, Cr, Zn, Fe благородные металлы окисляются с большим трудом Cu, Ag, Pt, Au
Электрохимический ряд активности (ряд напряжений Р. Н. ) ЭХРН Хим. характер металла во многом обусловлен тем, насколько легко он окисляется, т. е. насколько легко его атомы могут переходить в состояние + ионов М 0 – nē Mn+ неблагородные металлы окисляются легко Li, K, Ba, Ca, Na, Mg, Al, Mn, Cr, Zn, Fe благородные металлы окисляются с большим трудом Cu, Ag, Pt, Au
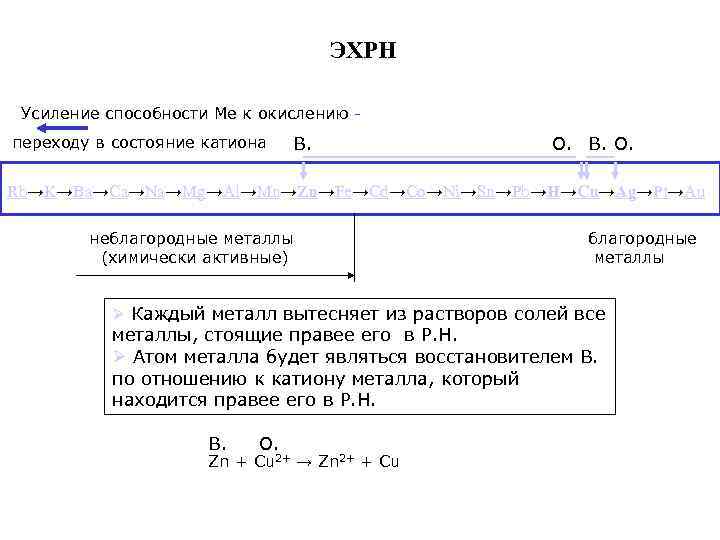 ЭХРН Усиление способности Ме к окислению переходу в состояние катиона В. О. В. О. Rb→K→Ba→Ca→Na→Mg→Al→Mn→Zn→Fe→Cd→Co→Ni→Sn→Pb→H→Cu→Ag→Pt→Au неблагородные металлы (химически активные) благородные металлы Ø Каждый металл вытесняет из растворов солей все металлы, стоящие правее его в Р. Н. Ø Атом металла будет являться восстановителем В. по отношению к катиону металла, который находится правее его в Р. Н. В. О. Zn + Cu 2+ → Zn 2+ + Cu
ЭХРН Усиление способности Ме к окислению переходу в состояние катиона В. О. В. О. Rb→K→Ba→Ca→Na→Mg→Al→Mn→Zn→Fe→Cd→Co→Ni→Sn→Pb→H→Cu→Ag→Pt→Au неблагородные металлы (химически активные) благородные металлы Ø Каждый металл вытесняет из растворов солей все металлы, стоящие правее его в Р. Н. Ø Атом металла будет являться восстановителем В. по отношению к катиону металла, который находится правее его в Р. Н. В. О. Zn + Cu 2+ → Zn 2+ + Cu
 ЭХРН Усиление способности Ме к окислению переходу в состояние катиона В. О. Rb→K→Ba→Ca→Na→Mg→Al→Mn→Zn→Fe→Cd→Co→Ni→Sn→Pb→H→Cu→Ag→Pt→Au неблагородные металлы (химически активные) благородные металлы Ø Все металлы, стоящие левее Н, будут вытеснять его из разбавленных кислот (на поверхности некоторых образуется защитная пленка) Zn + 2 Н 3 О+ → Zn 2+ + Н 2+ 2 Н 2 О
ЭХРН Усиление способности Ме к окислению переходу в состояние катиона В. О. Rb→K→Ba→Ca→Na→Mg→Al→Mn→Zn→Fe→Cd→Co→Ni→Sn→Pb→H→Cu→Ag→Pt→Au неблагородные металлы (химически активные) благородные металлы Ø Все металлы, стоящие левее Н, будут вытеснять его из разбавленных кислот (на поверхности некоторых образуется защитная пленка) Zn + 2 Н 3 О+ → Zn 2+ + Н 2+ 2 Н 2 О
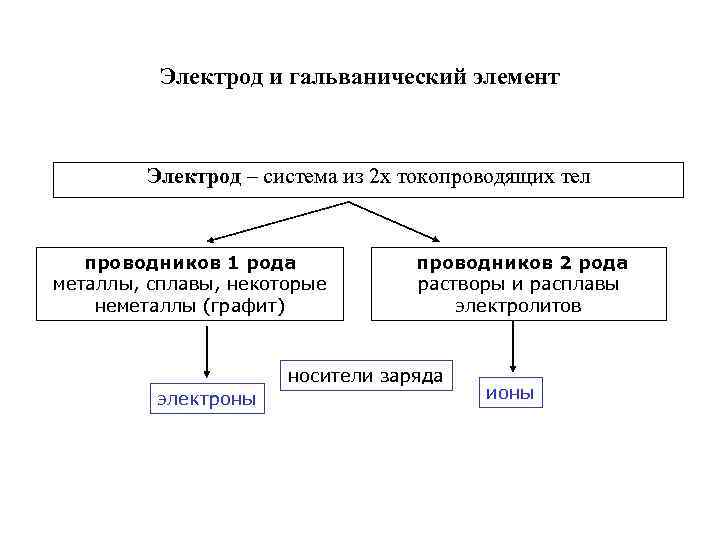 Электрод и гальванический элемент Электрод – система из 2 х токопроводящих тел проводников 1 рода металлы, сплавы, некоторые неметаллы (графит) проводников 2 рода растворы и расплавы электролитов носители заряда электроны ионы
Электрод и гальванический элемент Электрод – система из 2 х токопроводящих тел проводников 1 рода металлы, сплавы, некоторые неметаллы (графит) проводников 2 рода растворы и расплавы электролитов носители заряда электроны ионы
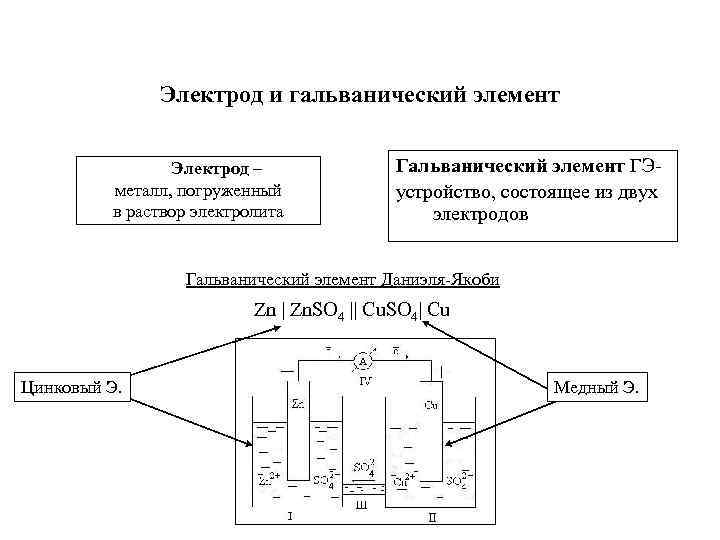 Электрод и гальванический элемент Электрод – металл, погруженный в раствор электролита Гальванический элемент ГЭ- устройство, состоящее из двух электродов Гальванический элемент Даниэля-Якоби Zn Zn. SO 4 Cu. SO 4 Cu Цинковый Э. Медный Э.
Электрод и гальванический элемент Электрод – металл, погруженный в раствор электролита Гальванический элемент ГЭ- устройство, состоящее из двух электродов Гальванический элемент Даниэля-Якоби Zn Zn. SO 4 Cu. SO 4 Cu Цинковый Э. Медный Э.
 Стандартные электродные потенциалы Ø Ø Ø СВЭ - эталон, относительно кот. ведется Стандартный отсчет электродного потенциала Е хим. водоро дный электро д реакции. СВЭ Для работа применяют стандартные условия (с. у. ): РН 2=1 атм. H+ = 1 моль/л Т=298 К Стандартный электродный потенциал Е 0 Стандартный потенциал разность потенциалов СВЭ и к-л СВЭ другого Э. (металл/раствор соли Ме), условно принят = 0 В измеренная при с. у.
Стандартные электродные потенциалы Ø Ø Ø СВЭ - эталон, относительно кот. ведется Стандартный отсчет электродного потенциала Е хим. водоро дный электро д реакции. СВЭ Для работа применяют стандартные условия (с. у. ): РН 2=1 атм. H+ = 1 моль/л Т=298 К Стандартный электродный потенциал Е 0 Стандартный потенциал разность потенциалов СВЭ и к-л СВЭ другого Э. (металл/раствор соли Ме), условно принят = 0 В измеренная при с. у.
 Стандартные электродные потенциалы
Стандартные электродные потенциалы
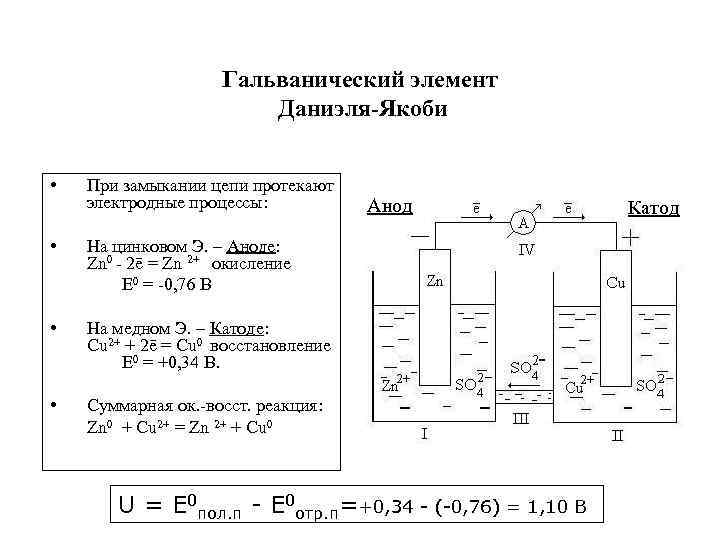 Гальванический элемент Даниэля-Якоби • При замыкании цепи протекают электродные процессы: Анод • На цинковом Э. – Аноде: Zn 0 - 2ē = Zn 2+ окисление Е 0 = -0, 76 В • На медном Э. – Катоде: Cu 2+ + 2ē = Cu 0 восстановление Е 0 = +0, 34 В. • Cуммарная ок. -восст. реакция: Zn 0 + Cu 2+ = Zn 2+ + Cu 0 U = Е 0 пол. п - Е 0 отр. п=+0, 34 - (-0, 76) = 1, 10 В Катод
Гальванический элемент Даниэля-Якоби • При замыкании цепи протекают электродные процессы: Анод • На цинковом Э. – Аноде: Zn 0 - 2ē = Zn 2+ окисление Е 0 = -0, 76 В • На медном Э. – Катоде: Cu 2+ + 2ē = Cu 0 восстановление Е 0 = +0, 34 В. • Cуммарная ок. -восст. реакция: Zn 0 + Cu 2+ = Zn 2+ + Cu 0 U = Е 0 пол. п - Е 0 отр. п=+0, 34 - (-0, 76) = 1, 10 В Катод
 Классификация гальванических элементов • Гальванические первичные элементы - устройства для прямого преобразования химической энергии, заключенных в них реагентов (окислителя и восстановителя), в электрическую. • Вторичные источники тока (аккумуляторы) – • Г. Э. , которые на основе обратимых электрохимических реакций могут многократно накапливать электрическую энергию и отдавать ее для потребления зарядка Электрическая энергия Химическая энергия разрядка
Классификация гальванических элементов • Гальванические первичные элементы - устройства для прямого преобразования химической энергии, заключенных в них реагентов (окислителя и восстановителя), в электрическую. • Вторичные источники тока (аккумуляторы) – • Г. Э. , которые на основе обратимых электрохимических реакций могут многократно накапливать электрическую энергию и отдавать ее для потребления зарядка Электрическая энергия Химическая энергия разрядка
 Уравнение электродного потенциала Уравнение Нернста § § § § Е— электродный потенциал Е 0— стандартный электродный потенциал, В R — универсальная газовая постоянная, = 8. 31 Дж/(моль·K) T — абсолютная температура, К Подставляя численные значения F — постоянная Фарадея, =96485, 35 R, F, T=298 K и переходя к lg: Кл·моль− 1 n — число электронов, участвующих в процессе и — активности соответственно окисленной и восстановленной форм вещества, участвующего в полуреакции
Уравнение электродного потенциала Уравнение Нернста § § § § Е— электродный потенциал Е 0— стандартный электродный потенциал, В R — универсальная газовая постоянная, = 8. 31 Дж/(моль·K) T — абсолютная температура, К Подставляя численные значения F — постоянная Фарадея, =96485, 35 R, F, T=298 K и переходя к lg: Кл·моль− 1 n — число электронов, участвующих в процессе и — активности соответственно окисленной и восстановленной форм вещества, участвующего в полуреакции
 Уравнение электродного потенциала Активность свободного металла принимается =1 Пример Цинковый Э. : Zn 2+ + 2 e- = Zn
Уравнение электродного потенциала Активность свободного металла принимается =1 Пример Цинковый Э. : Zn 2+ + 2 e- = Zn
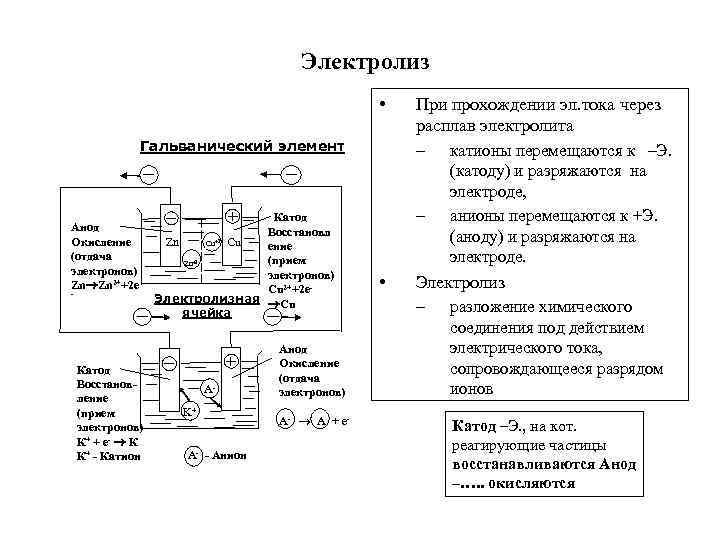 Электролиз • Гальванический элемент Анод Окисление (отдача электронов) Zn Zn 2++2 e - Катод Восстановление (прием электронов) К+ + е- К К+ - Катион Катод Восстановл Zn Cu+2 Cu ение +2 (прием Zn электронов) Cu 2++2 e. Электролизная Cu ячейка A K+ А- - Анион Анод Окисление (отдача электронов) А- А + е- При прохождении эл. тока через расплав электролита – катионы перемещаются к –Э. – • (катоду) и разряжаются на электроде, анионы перемещаются к +Э. (аноду) и разряжаются на электроде. Электролиз – разложение химического соединения под действием электрического тока, сопровождающееся разрядом ионов Катод –Э. , на кот. реагирующие частицы восстанавливаются Анод –…. . окисляются
Электролиз • Гальванический элемент Анод Окисление (отдача электронов) Zn Zn 2++2 e - Катод Восстановление (прием электронов) К+ + е- К К+ - Катион Катод Восстановл Zn Cu+2 Cu ение +2 (прием Zn электронов) Cu 2++2 e. Электролизная Cu ячейка A K+ А- - Анион Анод Окисление (отдача электронов) А- А + е- При прохождении эл. тока через расплав электролита – катионы перемещаются к –Э. – • (катоду) и разряжаются на электроде, анионы перемещаются к +Э. (аноду) и разряжаются на электроде. Электролиз – разложение химического соединения под действием электрического тока, сопровождающееся разрядом ионов Катод –Э. , на кот. реагирующие частицы восстанавливаются Анод –…. . окисляются
 Принципиальное различие № Гальванический элемент Электролизер 1 источник электрического тока потребитель эл. тока 2 Хим. энергия превращается в электрическую эл. энергия → хим. эн. 3 электрохимические процессы ок-я и восст-ия протекают самопроизвольно электрохимические процессы ок -я и восст-ия идут только под внешним воздействием эл. тока 4 Отр. электрод – А Полож. электрод – К Отр. электрод – К Полож. электрод – А
Принципиальное различие № Гальванический элемент Электролизер 1 источник электрического тока потребитель эл. тока 2 Хим. энергия превращается в электрическую эл. энергия → хим. эн. 3 электрохимические процессы ок-я и восст-ия протекают самопроизвольно электрохимические процессы ок -я и восст-ия идут только под внешним воздействием эл. тока 4 Отр. электрод – А Полож. электрод – К Отр. электрод – К Полож. электрод – А
 Электролиз в водном растворе • • При электролизе водных растворов электролитов в электродных полупроцессах может принимать участие, кроме электролита, вода. В результате разложения воды – на катоде образуется Н 2 – на аноде – О 2 Одноименные по знаку ионы воды и электролита конкурируют между собой, и разряжаться будет тот катион (на катоде) и тот анион (на аноде), которому отвечает более низкое по значению напряжение разряда.
Электролиз в водном растворе • • При электролизе водных растворов электролитов в электродных полупроцессах может принимать участие, кроме электролита, вода. В результате разложения воды – на катоде образуется Н 2 – на аноде – О 2 Одноименные по знаку ионы воды и электролита конкурируют между собой, и разряжаться будет тот катион (на катоде) и тот анион (на аноде), которому отвечает более низкое по значению напряжение разряда.
 Ряд разряжаемости на катоде наиболее неблагородные металлы менее неблагородные благородные металлы металлы K+ Na+ Mg 2+ + Al 3+ H+ Zn 2+ Fe 2+ Ni 2+ Sn 2+ Pb 2+ Cu 2+ Ag + Трудно разряжаемые ----------------------- легко Продукты электролиза в водном растворе: только Н 2 металл и Н 2 только металл
Ряд разряжаемости на катоде наиболее неблагородные металлы менее неблагородные благородные металлы металлы K+ Na+ Mg 2+ + Al 3+ H+ Zn 2+ Fe 2+ Ni 2+ Sn 2+ Pb 2+ Cu 2+ Ag + Трудно разряжаемые ----------------------- легко Продукты электролиза в водном растворе: только Н 2 металл и Н 2 только металл
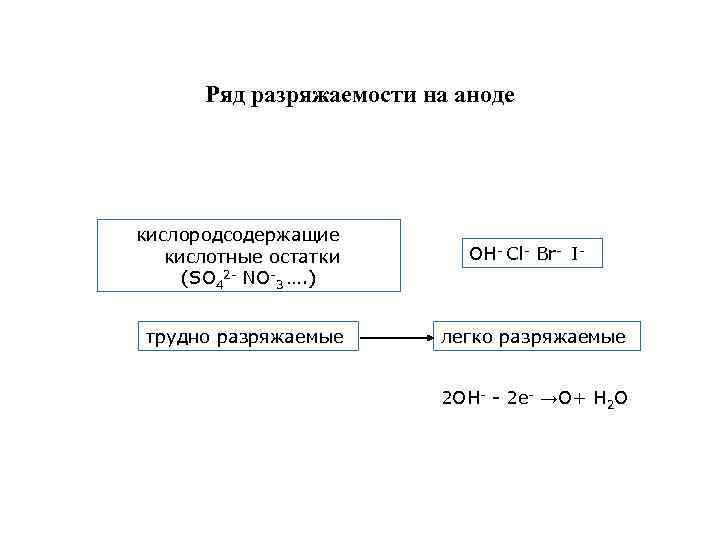 Ряд разряжаемости на аноде кислородсодержащие кислотные остатки (SO 42 - NO-3 …. ) трудно разряжаемые OH- Cl- Br- I- легко разряжаемые 2 OH- - 2 e- →O+ H 2 O
Ряд разряжаемости на аноде кислородсодержащие кислотные остатки (SO 42 - NO-3 …. ) трудно разряжаемые OH- Cl- Br- I- легко разряжаемые 2 OH- - 2 e- →O+ H 2 O
 Напряжение разложение электролита - минимальное напряжение между электродами, при котором начинает протекать электролиз Как минимум ∆Е=Еа - Ек С. у. : потенциалы разрядки анионов и катионов = Е 0 соответствующих ок. -восст. пар
Напряжение разложение электролита - минимальное напряжение между электродами, при котором начинает протекать электролиз Как минимум ∆Е=Еа - Ек С. у. : потенциалы разрядки анионов и катионов = Е 0 соответствующих ок. -восст. пар
 Законы электролиза 1) масса вещества, выделившегося на электроде при электролизе пропорционально количеству электричества, которое прошло через электролит 2) равные количества электричества выделяют на электродах эквивалентные массы веществ M – молярная масса, г/моль I – сила тока, А t – время , с F – постоянная Фарадея, 96485, 35 Кл·моль− 1 n – число электронов, участвующих в процессе q=I*t - количество электричества Meq=M/n – эквивалентная масса
Законы электролиза 1) масса вещества, выделившегося на электроде при электролизе пропорционально количеству электричества, которое прошло через электролит 2) равные количества электричества выделяют на электродах эквивалентные массы веществ M – молярная масса, г/моль I – сила тока, А t – время , с F – постоянная Фарадея, 96485, 35 Кл·моль− 1 n – число электронов, участвующих в процессе q=I*t - количество электричества Meq=M/n – эквивалентная масса
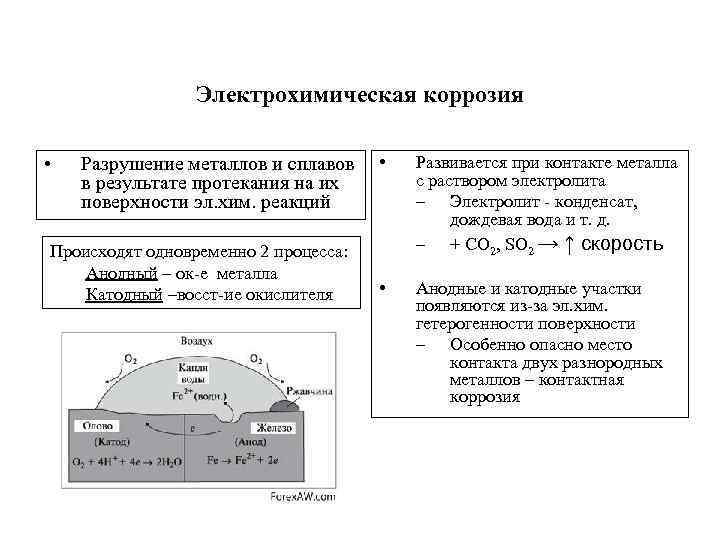 Электрохимическая коррозия • Разрушение металлов и сплавов • в результате протекания на их поверхности эл. хим. реакций Происходят одновременно 2 процесса: Анодный – ок-е металла Катодный –восст-ие окислителя • Развивается при контакте металла с раствором электролита – Электролит - конденсат, дождевая вода и т. д. – + СО 2, SO 2 → ↑ скорость Анодные и катодные участки появляются из-за эл. хим. гетерогенности поверхности – Особенно опасно место контакта двух разнородных металлов – контактная коррозия
Электрохимическая коррозия • Разрушение металлов и сплавов • в результате протекания на их поверхности эл. хим. реакций Происходят одновременно 2 процесса: Анодный – ок-е металла Катодный –восст-ие окислителя • Развивается при контакте металла с раствором электролита – Электролит - конденсат, дождевая вода и т. д. – + СО 2, SO 2 → ↑ скорость Анодные и катодные участки появляются из-за эл. хим. гетерогенности поверхности – Особенно опасно место контакта двух разнородных металлов – контактная коррозия
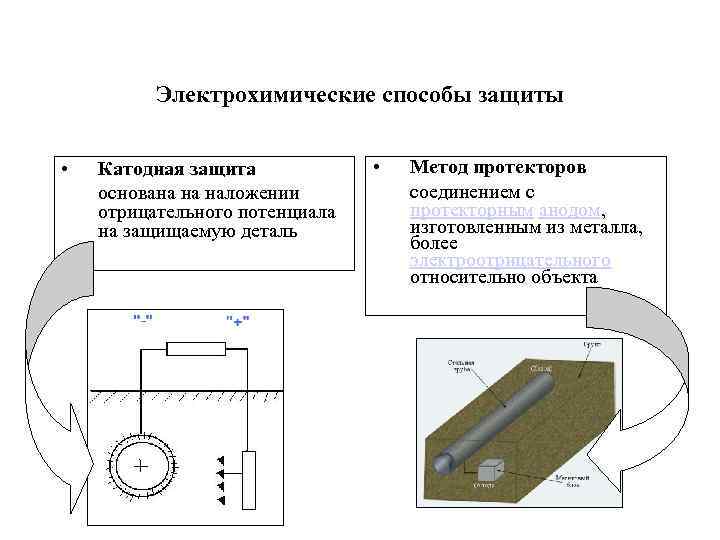 Электрохимические способы защиты • Катодная защита основана на наложении отрицательного потенциала на защищаемую деталь • Метод протекторов соединением с протекторным анодом, изготовленным из металла, более электроотрицательного относительно объекта
Электрохимические способы защиты • Катодная защита основана на наложении отрицательного потенциала на защищаемую деталь • Метод протекторов соединением с протекторным анодом, изготовленным из металла, более электроотрицательного относительно объекта


