Электр.химия.pptx
- Количество слайдов: 36
 Электрохимические методы анализа Полярографический анализ
Электрохимические методы анализа Полярографический анализ
 • Методы анализа, основанные на расшифровке поляризационных кривых (вольтамперограмм), получаемых в электролитической ячейке с поляризующимся индикаторным электродом и неполяризующимся электродом сравнения, называют вольтамперометрическим. • В качестве поляризующегося микроэлектрода применяют ртутный капельный электрод, а сам метод называют в этом случае полярографией, следуя термину, который предложил Я. Гейровский, разработавший этот метод в 1922 г.
• Методы анализа, основанные на расшифровке поляризационных кривых (вольтамперограмм), получаемых в электролитической ячейке с поляризующимся индикаторным электродом и неполяризующимся электродом сравнения, называют вольтамперометрическим. • В качестве поляризующегося микроэлектрода применяют ртутный капельный электрод, а сам метод называют в этом случае полярографией, следуя термину, который предложил Я. Гейровский, разработавший этот метод в 1922 г.
 • Идея метода: - явление поляризации Электрический ток может возникать под действием приложенной к системе электродыэлектролит внешней разности потенциалов. Изменение электрического состояния электрода (его потенциала) под действием электрического тока, проходящего через границу электродэлектролит называется поляризацией электрода. При поляризации потенциал электрода изменяется по сравнению с тем равновесным значением, которое наблюдалось в данном растворе у электрода при отсутствии тока
• Идея метода: - явление поляризации Электрический ток может возникать под действием приложенной к системе электродыэлектролит внешней разности потенциалов. Изменение электрического состояния электрода (его потенциала) под действием электрического тока, проходящего через границу электродэлектролит называется поляризацией электрода. При поляризации потенциал электрода изменяется по сравнению с тем равновесным значением, которое наблюдалось в данном растворе у электрода при отсутствии тока
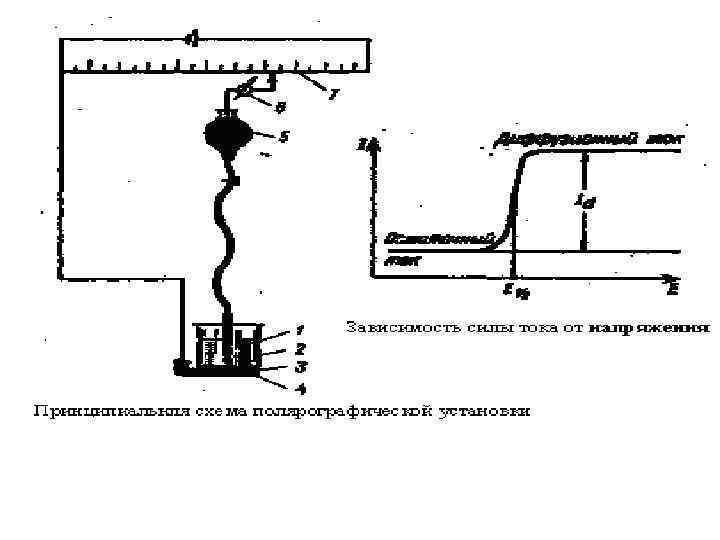
 • Зависимость тока I от приложенного напряжения Е при обратимом электродном процессе передается уравнением полярографической волны: Е = Е 1/2 + (R T / n F) ln ( Id – I ) / I, (1) Где Е 1/2 – потенциал полуволны; Id – диффузионный ток. При I = Id / 2 уравнение (1) переходит в Е = Е 1/2. (2) Это соотношение показывает независимость потенциала • полуволны от тока и, следовательно, от концентрации восстанавливающегося иона. Потенциал полуволны является, таким образом, качественной характеристикой иона в растворе данного фонового электролита, и определение потенциала полуволны составляет основу качественного полярографического анализа.
• Зависимость тока I от приложенного напряжения Е при обратимом электродном процессе передается уравнением полярографической волны: Е = Е 1/2 + (R T / n F) ln ( Id – I ) / I, (1) Где Е 1/2 – потенциал полуволны; Id – диффузионный ток. При I = Id / 2 уравнение (1) переходит в Е = Е 1/2. (2) Это соотношение показывает независимость потенциала • полуволны от тока и, следовательно, от концентрации восстанавливающегося иона. Потенциал полуволны является, таким образом, качественной характеристикой иона в растворе данного фонового электролита, и определение потенциала полуволны составляет основу качественного полярографического анализа.
 • Количественный полярографический анализ основан на уравнении Ильковича, которое связывает диффузионный ток Id с концентрацией иона с и рядом других величин: Id = 605 z D 1/2 m 2/3 t 1/6 c (3) Где z - заряд иона; D – коэффициент диффузии; m – масса ртути, вытекающей из капилляра за 1 с, мг; t – время образования капли (периода капания), с. В практике количественного полярографического анализа коэффициент пропорциональности межу концентрацией вещества и силой диффузионного тока обычно устанавливают с помощью стандартных растворов. При постоянных условиях полярографирования D, m, и t постоянны, поэтому уравнение (3) переходит в Id = k c. (4)
• Количественный полярографический анализ основан на уравнении Ильковича, которое связывает диффузионный ток Id с концентрацией иона с и рядом других величин: Id = 605 z D 1/2 m 2/3 t 1/6 c (3) Где z - заряд иона; D – коэффициент диффузии; m – масса ртути, вытекающей из капилляра за 1 с, мг; t – время образования капли (периода капания), с. В практике количественного полярографического анализа коэффициент пропорциональности межу концентрацией вещества и силой диффузионного тока обычно устанавливают с помощью стандартных растворов. При постоянных условиях полярографирования D, m, и t постоянны, поэтому уравнение (3) переходит в Id = k c. (4)
 Потенциометрический метод анализа Потенциометрические методы основаны на измерении разности потенциалов индикаторного электрода и электрода сравнения или, точнее, электродвижущих сил (ЭДС) различных цепей, поскольку экспериментально измеряется именно ЭДС, являющаяся разностью потенциалов. Равновесный потенциал индикаторного электрода связан с активностью и концентрацией веществ, участвующих в электродном процессе, уравнением Нернста: • Е = Е° + R T/(n F) ln (аокис/авосст) Е = Е° + R T /(n F) ln ([окисл] үокисл /([восст] үвосст)),
Потенциометрический метод анализа Потенциометрические методы основаны на измерении разности потенциалов индикаторного электрода и электрода сравнения или, точнее, электродвижущих сил (ЭДС) различных цепей, поскольку экспериментально измеряется именно ЭДС, являющаяся разностью потенциалов. Равновесный потенциал индикаторного электрода связан с активностью и концентрацией веществ, участвующих в электродном процессе, уравнением Нернста: • Е = Е° + R T/(n F) ln (аокис/авосст) Е = Е° + R T /(n F) ln ([окисл] үокисл /([восст] үвосст)),
 • R - универсальная газовая постоянная, равная 8, 31 Дж/(моль. К); Т - абсолютная температура; F- постоянная Фарадея (96500 Кл/моль); n - число электронов, принимающих участие в электродной реакции; аокис, авосст - активности соответственно окисленной и восстановленной форм редокссистемы; [окисл] и [восст] - их молярные концентрации; үокис, үвосст - коэффициенты активности; Е° - стандартный потенциал редокссистемы. • Подставляя Т = 298, 15 К и числовые значения констант в уравнение, получаем: • Е = Е° + (0, 059 / n) lg (аокис/авосст) • Е = Е° + (0, 059 / n) lg ([окисл] үокисл/([восст] үвосст))
• R - универсальная газовая постоянная, равная 8, 31 Дж/(моль. К); Т - абсолютная температура; F- постоянная Фарадея (96500 Кл/моль); n - число электронов, принимающих участие в электродной реакции; аокис, авосст - активности соответственно окисленной и восстановленной форм редокссистемы; [окисл] и [восст] - их молярные концентрации; үокис, үвосст - коэффициенты активности; Е° - стандартный потенциал редокссистемы. • Подставляя Т = 298, 15 К и числовые значения констант в уравнение, получаем: • Е = Е° + (0, 059 / n) lg (аокис/авосст) • Е = Е° + (0, 059 / n) lg ([окисл] үокисл/([восст] үвосст))
 Классификация электродов. • Электроды первого рода представляют собой систему из металла или неметалла, погруженного в раствор, содержащий его же ионы. Электрод из металла обратим относительно катионов, электрод из неметалла обратим относительно анионов. • Меz+/Me 0, например Cu 2+/Cu 0 Аz- /A 0, например Se 2 -/Se 0 К этой же группе электродов относятся амальгамные электроды (содержащие Hg).
Классификация электродов. • Электроды первого рода представляют собой систему из металла или неметалла, погруженного в раствор, содержащий его же ионы. Электрод из металла обратим относительно катионов, электрод из неметалла обратим относительно анионов. • Меz+/Me 0, например Cu 2+/Cu 0 Аz- /A 0, например Se 2 -/Se 0 К этой же группе электродов относятся амальгамные электроды (содержащие Hg).
 • К электродам второго рода относятся системы, в которых металл покрыт слоем труднорастворимой соли этого металла (или оксидом), а раствор содержит анионы этой соли. • Аz- /Ме. А, Ме, например Cl-/Ag. Cl, Ag Примером электродов второго рода могут служить каломельный и хлорсеребряный электроды, которые являются электродами сравнения: каломельный электрод хлорсеребряный Cl-/Hg 2 Cl 2, Hg Cl-/ Ag. Cl, Ag ½ Hg 2 Cl 2 + = Hg + Cl- Ag. Cl + = Ag + Cl-
• К электродам второго рода относятся системы, в которых металл покрыт слоем труднорастворимой соли этого металла (или оксидом), а раствор содержит анионы этой соли. • Аz- /Ме. А, Ме, например Cl-/Ag. Cl, Ag Примером электродов второго рода могут служить каломельный и хлорсеребряный электроды, которые являются электродами сравнения: каломельный электрод хлорсеребряный Cl-/Hg 2 Cl 2, Hg Cl-/ Ag. Cl, Ag ½ Hg 2 Cl 2 + = Hg + Cl- Ag. Cl + = Ag + Cl-
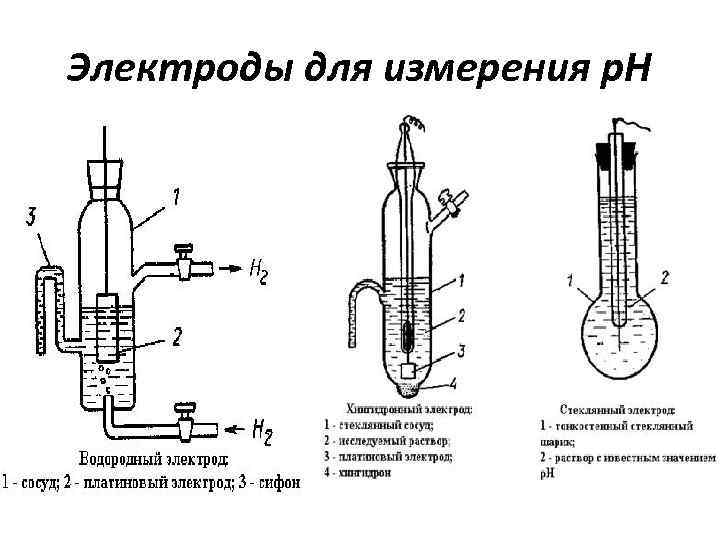 Электроды для измерения р. Н
Электроды для измерения р. Н
 • Окислительно - восстановительным электродом является хингидронный электрод (хингидрон - смесь органического соединения хинона и его восстановленной формы гидрохинона). Этот электрод реагирует практически только на Н+. • С 6 Н 4 О 2, С 6 Н 4 О 2(ОН)2, Н+/ Рt • Процесс С 6 Н 4 О 2 + 2 Н+ + 2 = С 6 Н 4 О 2(ОН)2. • Этот электрод пригоден для работы только в кислых средах и используется для определения р. Н среды. • Н 2 → 2 Н+ + 2 е. –Водородный электрод • Стеклянный электрод. • Состоит из стеклянной тонкостенной ампулы, в которую налит раствор с известной концентрацией ионов Н+. В результате обмена между катионами стекла и ионами Н+ раствора возникает разность потенциалов. При погружении ампулы в раствор с неизвестной концентрацией Н+ за счет обменных процессов между раствором и стеклом потенциал изменится. Это изменение будет зависеть от концентрации ионов Н+ в исследуемом растворе. Используется стеклянный электрод в средах при р. Н не более 9, чтобы не происходило взаимодействие стекла с раствором.
• Окислительно - восстановительным электродом является хингидронный электрод (хингидрон - смесь органического соединения хинона и его восстановленной формы гидрохинона). Этот электрод реагирует практически только на Н+. • С 6 Н 4 О 2, С 6 Н 4 О 2(ОН)2, Н+/ Рt • Процесс С 6 Н 4 О 2 + 2 Н+ + 2 = С 6 Н 4 О 2(ОН)2. • Этот электрод пригоден для работы только в кислых средах и используется для определения р. Н среды. • Н 2 → 2 Н+ + 2 е. –Водородный электрод • Стеклянный электрод. • Состоит из стеклянной тонкостенной ампулы, в которую налит раствор с известной концентрацией ионов Н+. В результате обмена между катионами стекла и ионами Н+ раствора возникает разность потенциалов. При погружении ампулы в раствор с неизвестной концентрацией Н+ за счет обменных процессов между раствором и стеклом потенциал изменится. Это изменение будет зависеть от концентрации ионов Н+ в исследуемом растворе. Используется стеклянный электрод в средах при р. Н не более 9, чтобы не происходило взаимодействие стекла с раствором.
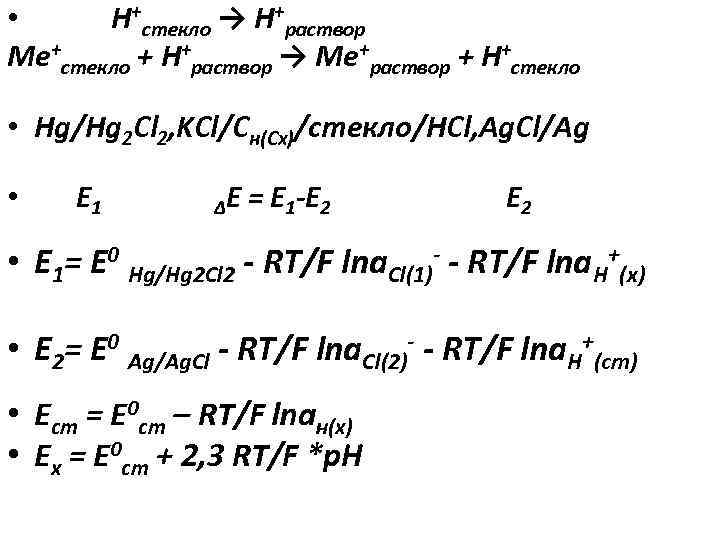 • Н+стекло → Н+раствор Ме+стекло + Н+раствор → Ме+раствор + Н+стекло • Hg/Hg 2 Cl 2, KCl/Cн(Сх)/стекло/HCl, Ag. Cl/Ag • E 1 ΔЕ = E 1 -E 2 E 2 • E 1= E 0 Hg/Hg 2 Cl 2 - RT/F lna. Cl(1)- - RT/F lna. H+(х) • E 2= E 0 Аg/Аg. Cl - RT/F lna. Cl(2)- - RT/F lna. H+(ст) • Eст = E 0 ст – RT/F lnaн(х) • Ех = Е 0 ст + 2, 3 RT/F *p. H
• Н+стекло → Н+раствор Ме+стекло + Н+раствор → Ме+раствор + Н+стекло • Hg/Hg 2 Cl 2, KCl/Cн(Сх)/стекло/HCl, Ag. Cl/Ag • E 1 ΔЕ = E 1 -E 2 E 2 • E 1= E 0 Hg/Hg 2 Cl 2 - RT/F lna. Cl(1)- - RT/F lna. H+(х) • E 2= E 0 Аg/Аg. Cl - RT/F lna. Cl(2)- - RT/F lna. H+(ст) • Eст = E 0 ст – RT/F lnaн(х) • Ех = Е 0 ст + 2, 3 RT/F *p. H
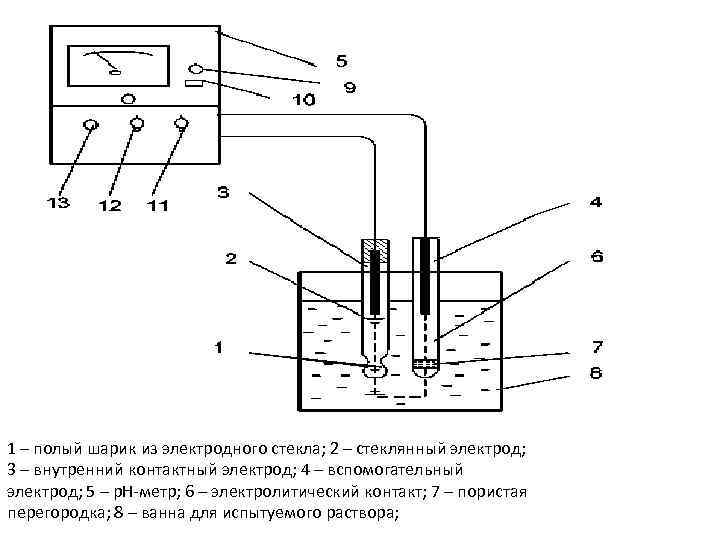 1 – полый шарик из электродного стекла; 2 – стеклянный электрод; 3 – внутренний контактный электрод; 4 – вспомогательный электрод; 5 – р. Н-метр; 6 – электролитический контакт; 7 – пористая перегородка; 8 – ванна для испытуемого раствора;
1 – полый шарик из электродного стекла; 2 – стеклянный электрод; 3 – внутренний контактный электрод; 4 – вспомогательный электрод; 5 – р. Н-метр; 6 – электролитический контакт; 7 – пористая перегородка; 8 – ванна для испытуемого раствора;
 • Е = Ек +Евсп +Евн +Ех (1) • где Ек – ЭДС контактного электрода (3); Евсп – ЭДС вспомогательного электрода (4); Евн – ЭДС, возникающая на внутренней поверхности стеклянного электрода (определяемое величиной р. Н внутреннего раствора); Ех – ЭДС, возникающая на внутренней поверхности стеклянного электрода (определяемое величиной р. Н контролируемого раствора). Ек , Евсп , Евн не зависят от свойств испытуемого раствора и при постоянной температуре являются постоянными величинами, поэтому формулу (1) можно представить в виде • Е=Ех + const
• Е = Ек +Евсп +Евн +Ех (1) • где Ек – ЭДС контактного электрода (3); Евсп – ЭДС вспомогательного электрода (4); Евн – ЭДС, возникающая на внутренней поверхности стеклянного электрода (определяемое величиной р. Н внутреннего раствора); Ех – ЭДС, возникающая на внутренней поверхности стеклянного электрода (определяемое величиной р. Н контролируемого раствора). Ек , Евсп , Евн не зависят от свойств испытуемого раствора и при постоянной температуре являются постоянными величинами, поэтому формулу (1) можно представить в виде • Е=Ех + const
 • Согласно уравнению Нернста • Ех = Е 0 ст + 2, 3 RT/F *p. H • где R – универсальная газовая постоянная, R = 8, 315· 107 эрг/град·моль; Т – температура раствора, °К; F – число Фарадея, F = 96500 кулон/г-экв; р. Н – значение водородного показателя исследуемого раствора. • Таким образом, суммарно ЭДС Е линейно зависит от р. Н исследуемого раствора. Возникающая ЭДС приводит в движение стрелку прибора, шкала которого проградуирована на различные значения р. Н.
• Согласно уравнению Нернста • Ех = Е 0 ст + 2, 3 RT/F *p. H • где R – универсальная газовая постоянная, R = 8, 315· 107 эрг/град·моль; Т – температура раствора, °К; F – число Фарадея, F = 96500 кулон/г-экв; р. Н – значение водородного показателя исследуемого раствора. • Таким образом, суммарно ЭДС Е линейно зависит от р. Н исследуемого раствора. Возникающая ЭДС приводит в движение стрелку прибора, шкала которого проградуирована на различные значения р. Н.
 Ионоселективные электроды
Ионоселективные электроды
 • Ионоселективные электроды (ИСЭ), представляет собой устройство, основным элементом которого является мембрана, проницаемая только для определенного иона и чувствительные к катионам и анионам. • ИСЭ – это электрохимические системы, в которых потенциал определяется процессами распределения ионов между мембраной и раствором. • Ионоселективные электроды имеют следующие достоинства: они не оказывают воздействия на исследуемый раствор, портативны, пригодны как для прямых определений, так и в качестве индикаторов в титриметрии. • Метод с использованием в анализе ионоселективных электродов получил название ионометрией
• Ионоселективные электроды (ИСЭ), представляет собой устройство, основным элементом которого является мембрана, проницаемая только для определенного иона и чувствительные к катионам и анионам. • ИСЭ – это электрохимические системы, в которых потенциал определяется процессами распределения ионов между мембраной и раствором. • Ионоселективные электроды имеют следующие достоинства: они не оказывают воздействия на исследуемый раствор, портативны, пригодны как для прямых определений, так и в качестве индикаторов в титриметрии. • Метод с использованием в анализе ионоселективных электродов получил название ионометрией
 Типы ионоселективных электродов • В зависимости от типа мембраны ионселективные электроды можно разделить на следующие группы: • 1. Твердые электроды с гомогенной или гетерогенной мембраной на основе ионообменных смол, стекол, осадков, моно- и поликристаллов; • 2. Жидкостные электроды (на основе ионных ассоциатов, хелатов металлов или нейтральных лигандов) и жидких ионитов хелатов - нейтральные переносчики, биологически активных веществ; • 3. Газовые электроды • 4. Энзимные (ферментные) электроды
Типы ионоселективных электродов • В зависимости от типа мембраны ионселективные электроды можно разделить на следующие группы: • 1. Твердые электроды с гомогенной или гетерогенной мембраной на основе ионообменных смол, стекол, осадков, моно- и поликристаллов; • 2. Жидкостные электроды (на основе ионных ассоциатов, хелатов металлов или нейтральных лигандов) и жидких ионитов хелатов - нейтральные переносчики, биологически активных веществ; • 3. Газовые электроды • 4. Энзимные (ферментные) электроды
 • Электроды с твердыми мембранами – Лантанфторидный электрод – Сульфидсеребряные электроды – Галогенсеребряные и некоторые другие электроды на основе серебра – Электроды на основе сульфидов некоторых двузарядных металлов – Стеклянные электроды • Электроды с жидкими мембранами – Электроды на основе жидких катионитов – Электроды на основе жидких анионитов – Нитрат-селективный электрод • Газовые электроды • Энзимные электроды
• Электроды с твердыми мембранами – Лантанфторидный электрод – Сульфидсеребряные электроды – Галогенсеребряные и некоторые другие электроды на основе серебра – Электроды на основе сульфидов некоторых двузарядных металлов – Стеклянные электроды • Электроды с жидкими мембранами – Электроды на основе жидких катионитов – Электроды на основе жидких анионитов – Нитрат-селективный электрод • Газовые электроды • Энзимные электроды
 Уравнение Никольского - Эйземана • E =E 0 + RT/Zj F ln (a. A + KA/B a. B ) • Zj –заряд иона, участвующего в обмене • KA/B – коэффициент селективности по отношению к определяемому иону А+ • KA, B = a. A/a. B • Чем меньше коэффициент для пары ионов А и В, тем более данный электрод чувствителен к изменению активности ионов А по сравнению с ионами В (выше селективность электрода относительно иона А+ )
Уравнение Никольского - Эйземана • E =E 0 + RT/Zj F ln (a. A + KA/B a. B ) • Zj –заряд иона, участвующего в обмене • KA/B – коэффициент селективности по отношению к определяемому иону А+ • KA, B = a. A/a. B • Чем меньше коэффициент для пары ионов А и В, тем более данный электрод чувствителен к изменению активности ионов А по сравнению с ионами В (выше селективность электрода относительно иона А+ )
 Характеристики ионоселективных электродов • 1. Интервал выполнения электродной функции – потенциал электрода зависит от активности иона А • 2. Селективность - KA, B - способность ИСЭ отличать различные ионы в их смешанном растворе • 3. Предел обнаружения – активность((концентрация) определяемого иона, при которой аналитический сигнал в два раза больше фонового (потенциал электрода перестает зависеть от активности иона А) • 4. Время «отклика» электрода – время, необходимое для достижения аналитической системой состояния равновесия - характеризует время достижения постоянного потенциала (чем меньше время отклика, тем лучше) (сек, мин, max – 5 мин)
Характеристики ионоселективных электродов • 1. Интервал выполнения электродной функции – потенциал электрода зависит от активности иона А • 2. Селективность - KA, B - способность ИСЭ отличать различные ионы в их смешанном растворе • 3. Предел обнаружения – активность((концентрация) определяемого иона, при которой аналитический сигнал в два раза больше фонового (потенциал электрода перестает зависеть от активности иона А) • 4. Время «отклика» электрода – время, необходимое для достижения аналитической системой состояния равновесия - характеризует время достижения постоянного потенциала (чем меньше время отклика, тем лучше) (сек, мин, max – 5 мин)
 Кондуктометрия Кондуктометрический метод анализа основан на измерении электропроводности анализируемого раствора. Электропроводностью называют величину, обратную электрическому сопротивлению R. Единицей измерения электропроводности является Ом-1 или сименс (См). Сименс равен электрической проводимости проводника сопротивлением в 1 Ом. Сопротивление раствора прямо пропорционально расстоянию между электродами l и обратно пропорционально площади их поверхности S R = χ ( l / S ), где r - удельное сопротивление (Ом. см). При l = 1 см и S = 1 см 2 имеем R=χ , • Размерность удельной электропроводности • χ Cм м-1 (Ом-1 См-1) • Удельная электрическая проводимость представляет собой электрическую проводимость 1 см 3 раствора, находящегося между двумя параллельными пластинами площадью 1 см 2, отстоящими друг от друга на 1 см.
Кондуктометрия Кондуктометрический метод анализа основан на измерении электропроводности анализируемого раствора. Электропроводностью называют величину, обратную электрическому сопротивлению R. Единицей измерения электропроводности является Ом-1 или сименс (См). Сименс равен электрической проводимости проводника сопротивлением в 1 Ом. Сопротивление раствора прямо пропорционально расстоянию между электродами l и обратно пропорционально площади их поверхности S R = χ ( l / S ), где r - удельное сопротивление (Ом. см). При l = 1 см и S = 1 см 2 имеем R=χ , • Размерность удельной электропроводности • χ Cм м-1 (Ом-1 См-1) • Удельная электрическая проводимость представляет собой электрическую проводимость 1 см 3 раствора, находящегося между двумя параллельными пластинами площадью 1 см 2, отстоящими друг от друга на 1 см.
 • Величину, обратную удельному сопротивлению, называют удельной электропроводностью c=1/r. • Удельная электропроводность (См. см-1) численно равна току (в амперах), , проходящему через слой раствора с поперечным сечением, равным единице, под действием градиента потенциала 1 В на единицу длины.
• Величину, обратную удельному сопротивлению, называют удельной электропроводностью c=1/r. • Удельная электропроводность (См. см-1) численно равна току (в амперах), , проходящему через слой раствора с поперечным сечением, равным единице, под действием градиента потенциала 1 В на единицу длины.
 • λ=λ 0 - а√N λ 0 –эквивалентная электрическая проводимость сильного электролита при бесконечном разведении, • N – нормальная концентрация раствора. • Подвижность это произведение абсолютной скорости иона на число Фарадея • λ=λ 0(+) + λ 0(-) • λ 0 для большинства ионов при комнатной температуре составляет от 30 до 70 • См* см 2/моль-экв • λ 0(Н+) = 350 λ 0(ОН-) = 199
• λ=λ 0 - а√N λ 0 –эквивалентная электрическая проводимость сильного электролита при бесконечном разведении, • N – нормальная концентрация раствора. • Подвижность это произведение абсолютной скорости иона на число Фарадея • λ=λ 0(+) + λ 0(-) • λ 0 для большинства ионов при комнатной температуре составляет от 30 до 70 • См* см 2/моль-экв • λ 0(Н+) = 350 λ 0(ОН-) = 199
 • Эквивалентной электрической проводимостью называют проводимость раствора, содержащего 1 моль эквивалента вещества и находящегося между двумя параллельными электродами, расстояние между которыми 1 см. Ее единицей измерения является • См. см 2. моль-1. Удельная и эквивалентная проводимость связаны соотношением: • λ = 1000 χ / с, где с – молярная концентрация эквивалента, моль-экв/л.
• Эквивалентной электрической проводимостью называют проводимость раствора, содержащего 1 моль эквивалента вещества и находящегося между двумя параллельными электродами, расстояние между которыми 1 см. Ее единицей измерения является • См. см 2. моль-1. Удельная и эквивалентная проводимость связаны соотношением: • λ = 1000 χ / с, где с – молярная концентрация эквивалента, моль-экв/л.
 • Методы прямой кондуктометрии основываются на том, что в области разбавленных и умеренно концентрированных растворов электрическая проводимость растет с увеличением концентрации электролита • В связи с относительно близкими значениями подвижностей ионов кондуктометрические измерения дают информацию главным образом лишь об общей концентрации ионов в растворе. Малая селективность кондуктометрического метода существенно ограничивает его применение.
• Методы прямой кондуктометрии основываются на том, что в области разбавленных и умеренно концентрированных растворов электрическая проводимость растет с увеличением концентрации электролита • В связи с относительно близкими значениями подвижностей ионов кондуктометрические измерения дают информацию главным образом лишь об общей концентрации ионов в растворе. Малая селективность кондуктометрического метода существенно ограничивает его применение.
 • В методах кондуктометрического титрования измеряют электрическую проводимость раствора после добавления небольших определенных порций титранта и находят точку эквивалентности графическим методом с помощью кривой в координатах • χ – Vтитранта (удельная электропроводность – объем раствора титранта). Практически в этом методе могут быть использованы такие химические реакции, в ходе которых происходит резкое изменение (обычно возрастание) электрической проводимости после точки эквивалентности (реакции кислотно-основного взаимодействия, осаждения и т. д. ).
• В методах кондуктометрического титрования измеряют электрическую проводимость раствора после добавления небольших определенных порций титранта и находят точку эквивалентности графическим методом с помощью кривой в координатах • χ – Vтитранта (удельная электропроводность – объем раствора титранта). Практически в этом методе могут быть использованы такие химические реакции, в ходе которых происходит резкое изменение (обычно возрастание) электрической проводимости после точки эквивалентности (реакции кислотно-основного взаимодействия, осаждения и т. д. ).
 • Токи, имеющие частоту порядка мегагерц и десятков мегагерц, называют токами высокой частоты. При таких частотах в растворе начинают играть роль эффекты молекулярной, или деформационной, и ориентационной поляризации. Поляризация обоих типов вызывает кратковременный электрический ток (ток смещения). Кроме того, поляризация молекул приводит к существенному изменению диэлектрической и магнитной проницаемостей раствора, что открывает новую возможность исследования свойств системы при титровании. • При построении кривой высокочастотного титрования показания прибора откладывают по оси ординат как функцию объема добавленного титранта. • В ячейках высокочастотного титрования электроды не соприкасаются с исследуемым раствором, что является одним из существенных достоинств метода. •
• Токи, имеющие частоту порядка мегагерц и десятков мегагерц, называют токами высокой частоты. При таких частотах в растворе начинают играть роль эффекты молекулярной, или деформационной, и ориентационной поляризации. Поляризация обоих типов вызывает кратковременный электрический ток (ток смещения). Кроме того, поляризация молекул приводит к существенному изменению диэлектрической и магнитной проницаемостей раствора, что открывает новую возможность исследования свойств системы при титровании. • При построении кривой высокочастотного титрования показания прибора откладывают по оси ординат как функцию объема добавленного титранта. • В ячейках высокочастотного титрования электроды не соприкасаются с исследуемым раствором, что является одним из существенных достоинств метода. •
 Кулонометрия • В основе кулонометрических методов лежат законы электролиза Фарадея. • Количество электропревращенного (восстановленного или окисленного) в процессе электролиза вещества прямо пропорционально количеству прошедшего электричества. • Массы различных веществ, выделенных или растворенных при прохождении одного и того же количества электричества, пропорциональны их электрохимическим эквивалентам. • Электрохимический эквивалент – это масса вещества, выделившегося на электроде (или растворившегося с электрода) в процессе электролиза при протекании единицы количества электричества, т. е. 1 Кл. •
Кулонометрия • В основе кулонометрических методов лежат законы электролиза Фарадея. • Количество электропревращенного (восстановленного или окисленного) в процессе электролиза вещества прямо пропорционально количеству прошедшего электричества. • Массы различных веществ, выделенных или растворенных при прохождении одного и того же количества электричества, пропорциональны их электрохимическим эквивалентам. • Электрохимический эквивалент – это масса вещества, выделившегося на электроде (или растворившегося с электрода) в процессе электролиза при протекании единицы количества электричества, т. е. 1 Кл. •
 • Суть законов Фарадея заключается в том, что для выделения одного моля эквивалента любого вещества в процессе электролиза необходимо затратить одно и то же количество электричества, называемое числом Фарадея F=96500 Кл/моль. m = (Q / F ). M / n , • Где Q – количество электричества (Кл), необходимое для выделения на электроде m граммов вещества с молярной массой эквивалента, равной М / n (М – молярная масса вещества; n – число электронов, участвующих в электродной реакции). Q= I . t , • Где I – сила тока, А (ампер); t – время электролиза, с (секунда). • электролиз должен протекать со 100%-ной эффективностью тока (или со 100%-ным выходом по току), что возможно только в отсутствие конкурирующих реакций.
• Суть законов Фарадея заключается в том, что для выделения одного моля эквивалента любого вещества в процессе электролиза необходимо затратить одно и то же количество электричества, называемое числом Фарадея F=96500 Кл/моль. m = (Q / F ). M / n , • Где Q – количество электричества (Кл), необходимое для выделения на электроде m граммов вещества с молярной массой эквивалента, равной М / n (М – молярная масса вещества; n – число электронов, участвующих в электродной реакции). Q= I . t , • Где I – сила тока, А (ампер); t – время электролиза, с (секунда). • электролиз должен протекать со 100%-ной эффективностью тока (или со 100%-ным выходом по току), что возможно только в отсутствие конкурирующих реакций.
 • Различают два основных вида кулонометрических определений – прямую кулонометрию и кулонометрическое титрование. • В прямой кулонометрии электрохимическому превращению непосредственно в кулонометрической ячейке подвергается анализируемое вещество. • В методе кулонометрического титрования электролизу подвергается вспомогательное вещество, а далее продукт электролиза – титрант – реагирует с определяемым веществом.
• Различают два основных вида кулонометрических определений – прямую кулонометрию и кулонометрическое титрование. • В прямой кулонометрии электрохимическому превращению непосредственно в кулонометрической ячейке подвергается анализируемое вещество. • В методе кулонометрического титрования электролизу подвергается вспомогательное вещество, а далее продукт электролиза – титрант – реагирует с определяемым веществом.
 • Кулонометрические определения могут проводиться при постоянном потенциале (потенциостатическая кулонометрия) и постоянной силе тока (амперостатическая кулонометрия). В прямой кулонометриишироко применяют потенциостатические методы. Массу определяемого вещества рассчитывают по приведенной выше формуле. • В методе кулонометрического титрования используются установки с постоянной силой тока. Содержание определяемого вещества рассчитывают по количеству электричества, израсходованного на генерацию необходимого для реакции с анализируемым веществом количества титранта.
• Кулонометрические определения могут проводиться при постоянном потенциале (потенциостатическая кулонометрия) и постоянной силе тока (амперостатическая кулонометрия). В прямой кулонометриишироко применяют потенциостатические методы. Массу определяемого вещества рассчитывают по приведенной выше формуле. • В методе кулонометрического титрования используются установки с постоянной силой тока. Содержание определяемого вещества рассчитывают по количеству электричества, израсходованного на генерацию необходимого для реакции с анализируемым веществом количества титранта.
 • Определение точки эквивалентности можно проводить потенциометрическим, амперометрическим, спектрофотометрическим и другими методами. • В кулонометрическом титровании используются химические реакции различных типов: кислотноосновные, окислительновосстановительные, комплексообразования и др. Различные восстановители (Fe 2+ , Sn 2+ , Sb 3+, As 3+ и др. ) могут быть оттитрованы, например, перманганатом, который легко генерируется из Mn. SO 4 в ячейке с платиновым анодом. При анодном растворении хрома в серной кислоте получается дихромат-ион, который также может быть использован для этого титрования. В кулонометрическом титровании широко применяют также свободный бром, генерируемый на платиновом аноде из бромида калия в соляной кислоте.
• Определение точки эквивалентности можно проводить потенциометрическим, амперометрическим, спектрофотометрическим и другими методами. • В кулонометрическом титровании используются химические реакции различных типов: кислотноосновные, окислительновосстановительные, комплексообразования и др. Различные восстановители (Fe 2+ , Sn 2+ , Sb 3+, As 3+ и др. ) могут быть оттитрованы, например, перманганатом, который легко генерируется из Mn. SO 4 в ячейке с платиновым анодом. При анодном растворении хрома в серной кислоте получается дихромат-ион, который также может быть использован для этого титрования. В кулонометрическом титровании широко применяют также свободный бром, генерируемый на платиновом аноде из бромида калия в соляной кислоте.
 • Установка для кулонометрического титрования при постоянной силе тока содержит следующие основные узлы: 1) источник постоянного тока; 2) устройство для определения количества электричества; 3) электрическую ячейку с генераторным электродом; 4) индикаторную систему для определения конца титрования; 5) хронометр для определения продолжительности электролиза. • Индикаторная система служит для индикации конечной точки титрования (к. т. т. ). Наиболее часто для этой цели используют амперометрический и потенциометрический методы. В ячейку вводят индикаторные электроды: два платиновых электрода (при амперометрической индикации) или платиновый и каломельный электроды (при потенциометрической индикации).
• Установка для кулонометрического титрования при постоянной силе тока содержит следующие основные узлы: 1) источник постоянного тока; 2) устройство для определения количества электричества; 3) электрическую ячейку с генераторным электродом; 4) индикаторную систему для определения конца титрования; 5) хронометр для определения продолжительности электролиза. • Индикаторная система служит для индикации конечной точки титрования (к. т. т. ). Наиболее часто для этой цели используют амперометрический и потенциометрический методы. В ячейку вводят индикаторные электроды: два платиновых электрода (при амперометрической индикации) или платиновый и каломельный электроды (при потенциометрической индикации).
 • Силу тока или разность потенциалов измеряют соответствующими приборами, входящими в комплект установки для титрования (блок индикации). • Иногда для определения к. т. т. используют фотометрический метод, помещая ячейку в кюветное отделение фотоэлектроколориметра и измеряя светопоглощение в ходе титрования. В отдельных случаях конец титрования устанавливают визуально, например, по появлению окраски раствора, вызванной избытком титранта.
• Силу тока или разность потенциалов измеряют соответствующими приборами, входящими в комплект установки для титрования (блок индикации). • Иногда для определения к. т. т. используют фотометрический метод, помещая ячейку в кюветное отделение фотоэлектроколориметра и измеряя светопоглощение в ходе титрования. В отдельных случаях конец титрования устанавливают визуально, например, по появлению окраски раствора, вызванной избытком титранта.


