ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА Общие вопросы Вольтамперометрия


ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА Общие вопросы Вольтамперометрия Потенциометрия Другие э/х методы

ЭХМА l Особенность ЭХМА: используются процессы, связанные с переносом электрических зарядов.
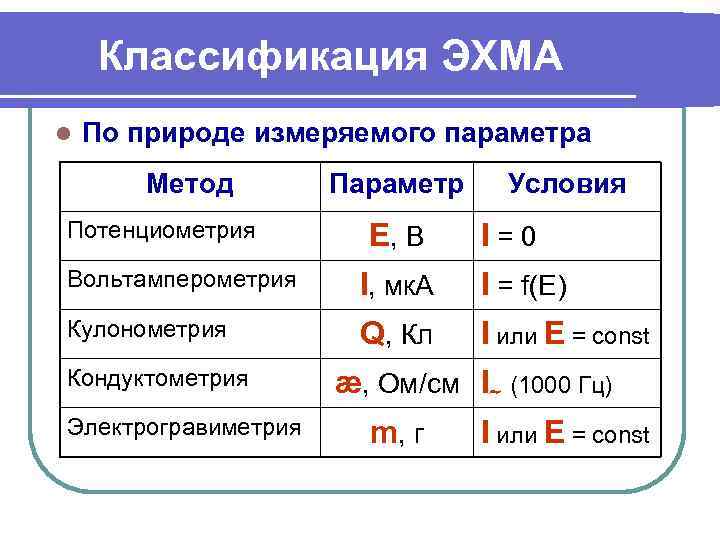
Классификация ЭХМА l По природе измеряемого параметра Метод Параметр Условия Потенциометрия Е, В I=0 Вольтамперометрия I, мк. А I = f(E) Кулонометрия Q, Кл I или E = const Кондуктометрия æ, Ом/см I~ (1000 Гц) Электрогравиметрия m, г I или E = const

Электрохимическая ячейка l Ячейка = электроды + электролит l Электрод – ГРФ, на которой направленное движение носителей заряда одного типа меняется на направленное движение носителей заряда другого типа направленное движение электронов ионов электрод ГРФ электролит

Электрохимическая ячейка l Электролит – раствор, обеспечивающий направленное движение ионов. l 2 х-электродная ячейка: ЭС и ИЭ l 3 х-электродная ячейка: ЭС, ИЭ и ВЭ l ИЭ – датчик, чувствительный к процессам, протекающим с участием электронов или ионов, т. е. к составу электролита. l ЭС – неполяризуемый электрод, имеет постоянный потенциал, который не зависит от состава электролита.
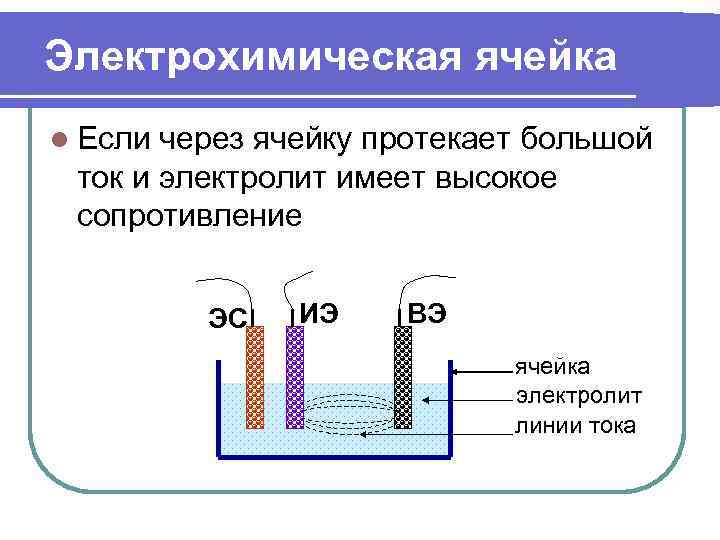
Электрохимическая ячейка l Если через ячейку протекает большой ток и электролит имеет высокое сопротивление ЭС ИЭ ВЭ ячейка электролит линии тока

Электрохимическая ячейка l Инертный электрод – материал электрода не принимает участия в химических и электрохимических реакциях, протекающих на его поверхности.
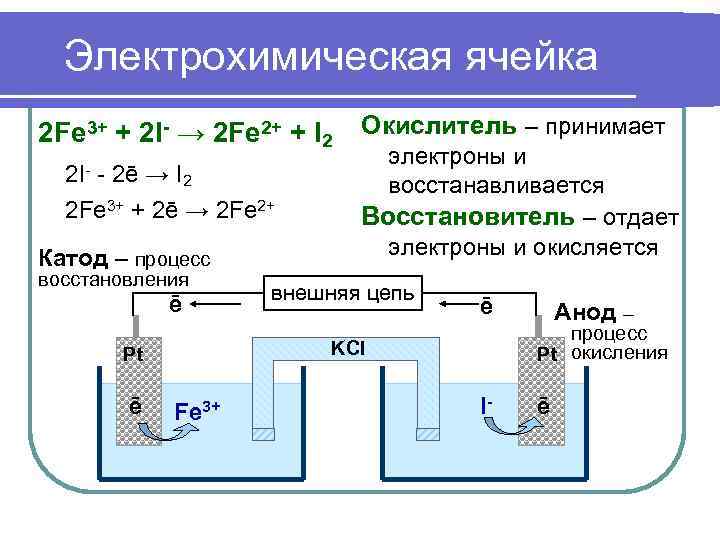
Электрохимическая ячейка 2 Fe 3+ + 2 I- → 2 Fe 2+ + I 2 Окислитель – принимает электроны и 2 I- - 2ē → I 2 восстанавливается 2 Fe 3+ + 2ē → 2 Fe 2+ Восстановитель – отдает Катод – процесс электроны и окисляется восстановления внешняя цепь ē Анод – процесс Pt KCl Pt окисления ē Fe 3+ I- ē
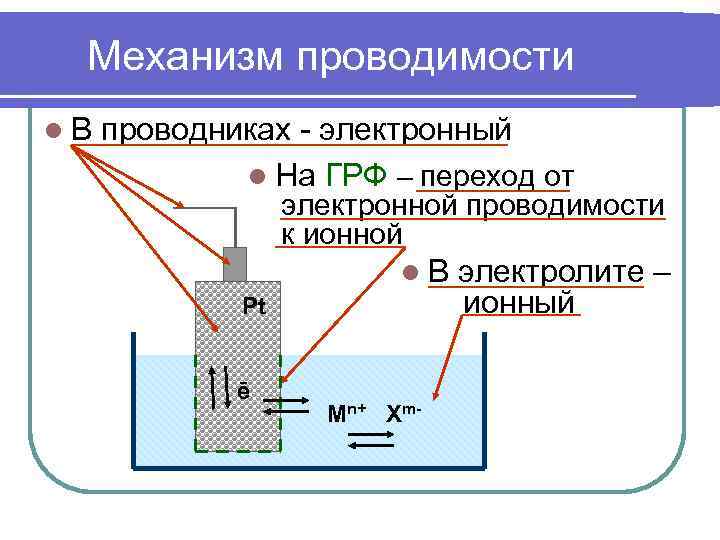
Механизм проводимости l. В проводниках - электронный l На ГРФ – переход от электронной проводимости к ионной l. В электролите – Pt ионный ē Mn+ Xm-

l На катоде – катодный ток (ток восстановления) l На аноде – анодный ток (ток окисления) l Токи, обусловленные электрохимическими реакциями, - фарадеевские. Red 1 + Ox 2 → Ox 1 + Red 2
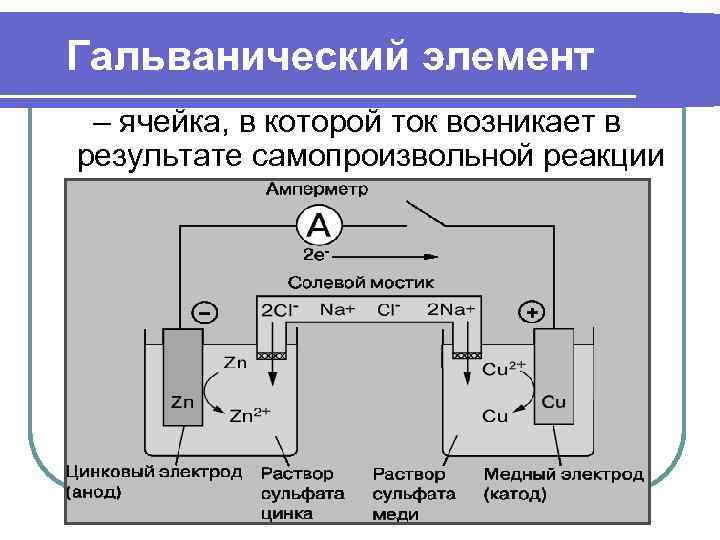
Гальванический элемент – ячейка, в которой ток возникает в результате самопроизвольной реакции

Потенциал Количественное описание окислительно- восстановительной реакции – потенциал системы: G 0 RT [Ox 1][Red 2] E = - —— + ——ln—————— n. F [Red 1][Ox 2] R – молярная газовая константа (8. 314 Дж/моль·К) n – число электронов F – константа Фарадея (96 500 Кл) E – ЭДС гальванического элемента G – энергия Гиббса, - G = А (работа по электрохимическому превращению 1 моль вещества)

СЭП Если концентрации всех компонентов равны 1 стандартный G 0 электродный E = - —— потенциал n. F Для измерения СЭП – эталон. Требования к эталону: l обратимая реакция l простая конструкция электрода l постоянный и воспроизводимый потенциал электрода
![СВЭ 2 Н+ + 2ē Н 2↑ [H+] СВЭ 2 Н+ + 2ē Н 2↑ [H+]](https://present5.com/presentation/3/3792717_444335485.pdf-img/3792717_444335485.pdf-14.jpg)
СВЭ 2 Н+ + 2ē Н 2↑ [H+] = 1 M p(H 2) = 1 атм Рt-проволока Н 2 EСВЭ = 0 В Pt-чернь Н 2 HCl
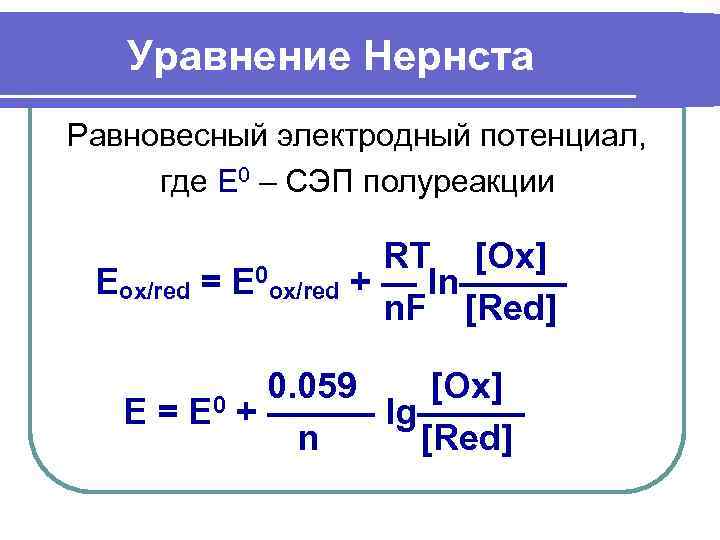
Уравнение Нернста Равновесный электродный потенциал, где Е 0 – СЭП полуреакции RT [Ox] Eox/red = E 0 ox/red + — ln——— n. F [Red] 0. 059 [Ox] E = E 0 + ——— lg——— n [Red]
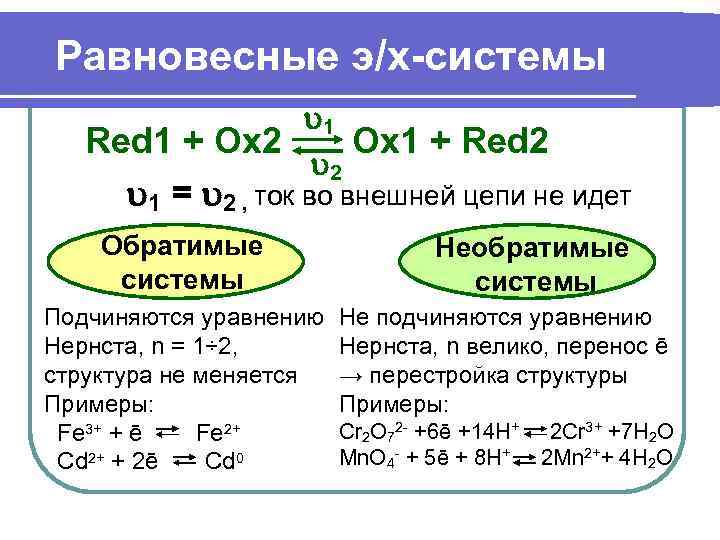
Равновесные э/х-системы 1 Red 1 + Ox 2 Ox 1 + Red 2 1 = 2 , ток во внешней цепи не идет Обратимые Необратимые системы системы Подчиняются уравнению Не подчиняются уравнению Нернста, n = 1÷ 2, Нернста, n велико, перенос ē структура не меняется → перестройка структуры Примеры: Fe 3+ + ē Fe 2+ Cr 2 O 72 - +6ē +14 H+ 2 Cr 3+ +7 H 2 O Cd 2+ + 2ē Cd 0 Mn. O 4 - + 5ē + 8 H+ 2 Mn 2++ 4 H 2 O
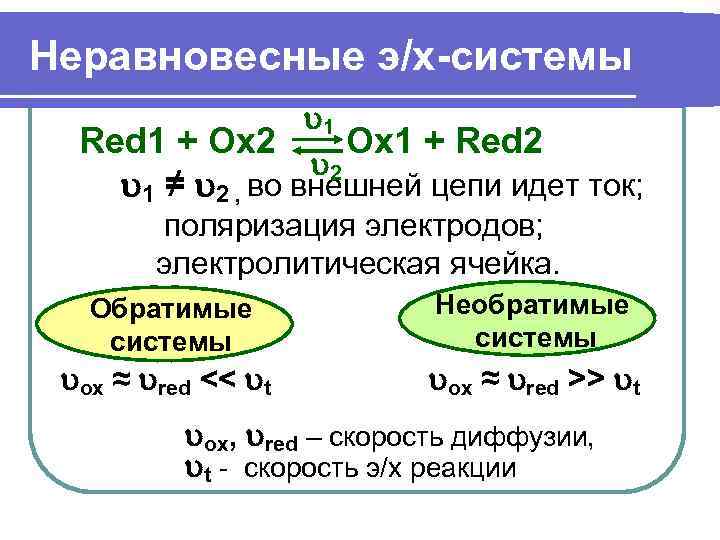
Неравновесные э/х-системы 1 Red 1 + Ox 2 Ox 1 + Red 2 2 1 ≠ 2 , во внешней цепи идет ток; поляризация электродов; электролитическая ячейка. Обратимые Необратимые системы ox ≈ red << t ox ≈ red >> t ox, red – скорость диффузии, t - скорость э/х реакции

ПОТЕНЦИОМЕТРИЯ l Потенциометрический анализ – метод определения концентрации ионов, основанный на измерении равновесного э/х потенциала ИЭ, погруженного в анализируемый раствор. l Используется уравнение Нернста, связывающее равновесный потенциал и концентрацию ионов Е = f(C)
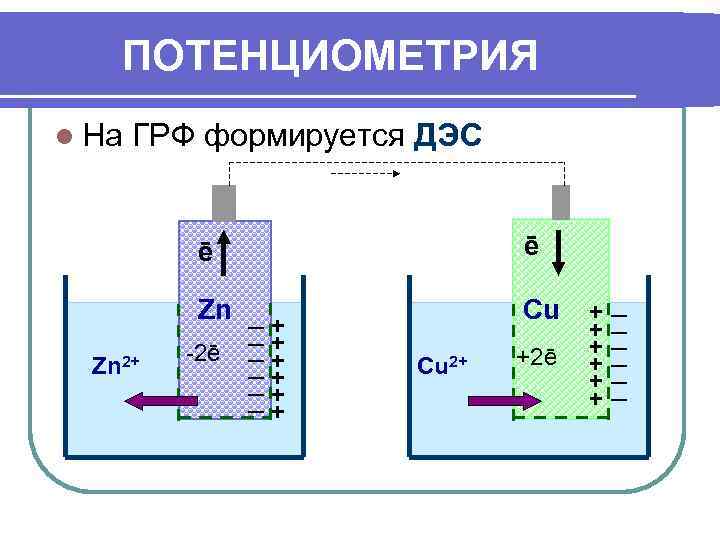
ПОТЕНЦИОМЕТРИЯ l На ГРФ формируется ДЭС ē Zn _ Cu + _ _+ + _ -2ē _ + _+ +2ē + + _ Zn 2+ Cu 2+ _+ + _ _++ +
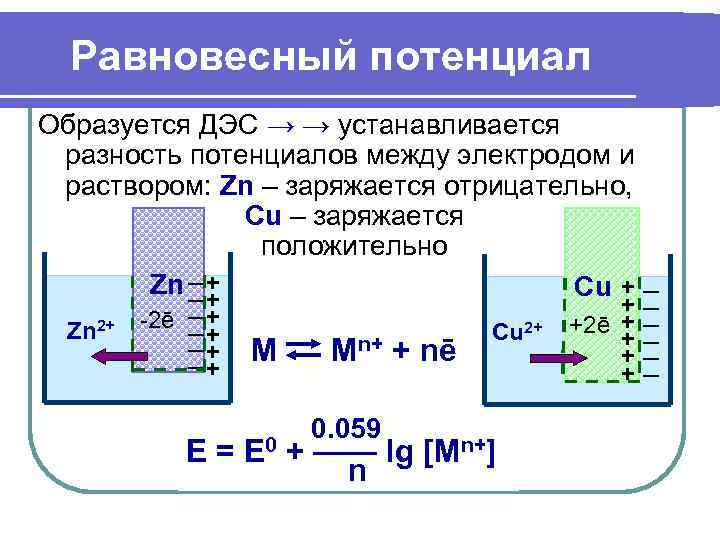
Равновесный потенциал Образуется ДЭС → → устанавливается разность потенциалов между электродом и раствором: Zn – заряжается отрицательно, Cu – заряжается положительно _+ Zn _ Cu + _ _+ +_ -2ē _ + +2ē + _ Zn +_ 2+ _+ Cu 2+ _+ М M +_ n+ + nē + +_ 0. 059 E = E 0 + —— lg [Mn+] n
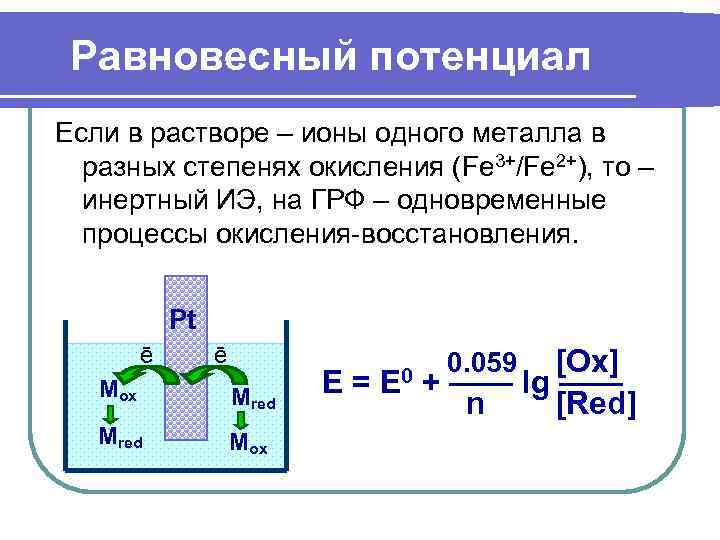
Равновесный потенциал Если в растворе – ионы одного металла в разных степенях окисления (Fe 3+/Fe 2+), то – инертный ИЭ, на ГРФ – одновременные процессы окисления-восстановления. Pt ē ē 0. 059 [Ox] Mox Mred E= E 0 + —— lg —— n [Red] Mred Mox

Потенциометрия Прямая Достоинства: потенциометрия Простота Ионометрия: Дешевизна анионометрия Экспрессность катионометрия, Возможность в т. ч. р. Н-метрия анализа «на Ферментные датчики месте» Потенциометрическое титрование

Потенциометрическое титрование Зависимость равновесного потенциала электрода от состава раствора (концентрации ионов) Достоинства по сравнению с обычным титрованием: - исключены субъективные ошибки при определении конечной точки титрования (ктт) - бóльшая чувствительность - можно титровать мутные и окрашенные растворы - можно титровать смеси веществ - можно автоматизировать процесс - высокая точность нахождения ктт

Потенциометрическое титрование Требование к индикаторному электроду: равновесный потенциал должен устанавливаться быстро. Вид Индикаторные титрования: электроды: кислотно-основное – р. Н-электроды редокс-титрование - Pt-электрод осадительное - I или II рода комплексиметрическое - III рода
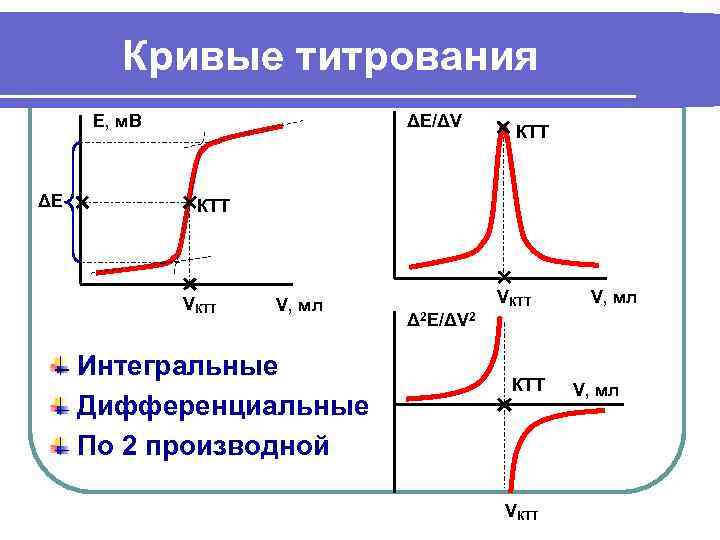
Кривые титрования Е, м. В ΔЕ/ΔV КТТ ΔЕ КТТ VКТТ V, мл VКТТ V, мл Δ 2 Е/ΔV 2 Интегральные КТТ V, мл Дифференциальные По 2 производной VКТТ

Электроды сравнения Обладают постоянным потенциалом, не зависящим от состава раствора Требования: - низкое электрическое сопротивление - отсутствие влияния на состав раствора - простота конструкции - быстрое установление потенциала - обратимый, воспроизводимый, стабильный
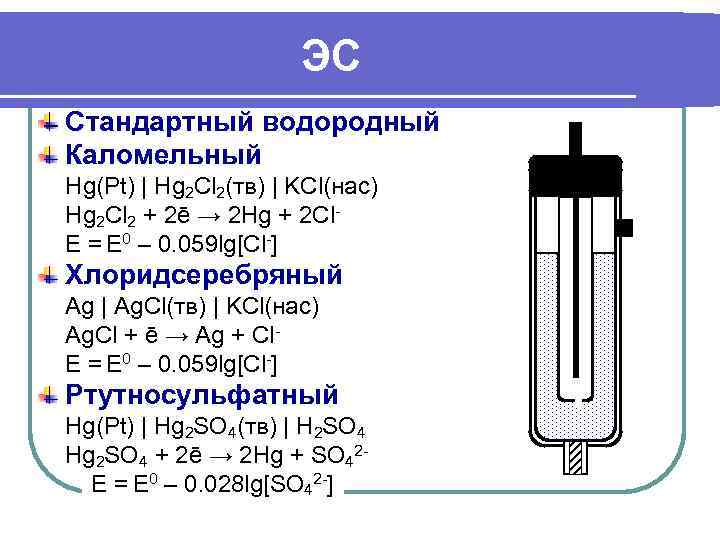
ЭС Стандартный водородный Каломельный Hg(Pt) | Hg 2 Cl 2(тв) | KCl(нас) Hg 2 Cl 2 + 2ē → 2 Hg + 2 Cl- E = E 0 – 0. 059 lg[Cl-] Хлоридсеребряный Ag | Ag. Cl(тв) | KCl(нас) Аg. Cl + ē → Аg + Cl- E = E 0 – 0. 059 lg[Cl-] Ртутносульфатный Hg(Pt) | Hg 2 SO 4(тв) | H 2 SO 4 Hg 2 SO 4 + 2ē → 2 Hg + SO 42 - E = E 0 – 0. 028 lg[SO 42 -]
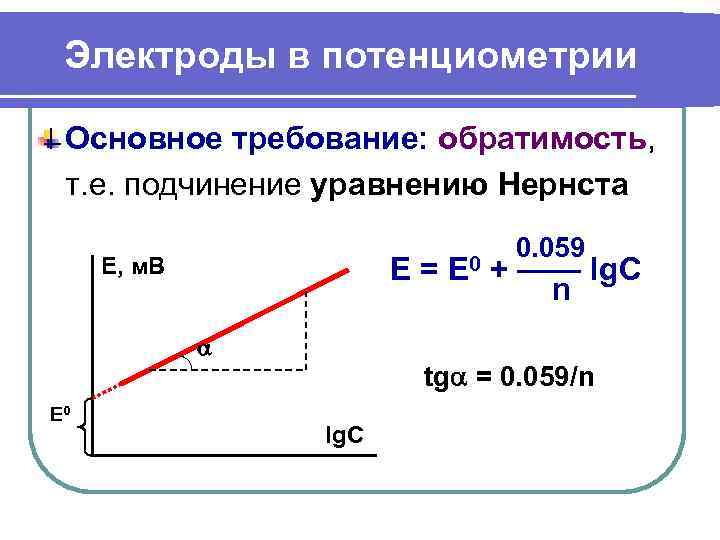
Электроды в потенциометрии Основное требование: обратимость, т. е. подчинение уравнению Нернста 0. 059 Е, м. В E= E 0 + —— lg. C n tg = 0. 059/n Е 0 lg. C

Электроды I рода Катионные: - металлические Mn+ + nē → M 0 0. 059 E = E 0 + —— lg[Mn+] n - амальгамные Mn+ + nē + Hg → 0. 059 [Mn+] M(Hg)= E 0 + —— lg ——— E n [M(Hg)] - водородный E = E 0 + 0. 059 lg[H+], E 0 = 0, 2 H+ + 2ē → H 2 E = -0. 059 p. H Анионные 0. 059 E = E 0 - —— lg[An-] An- - nē → A 0 n
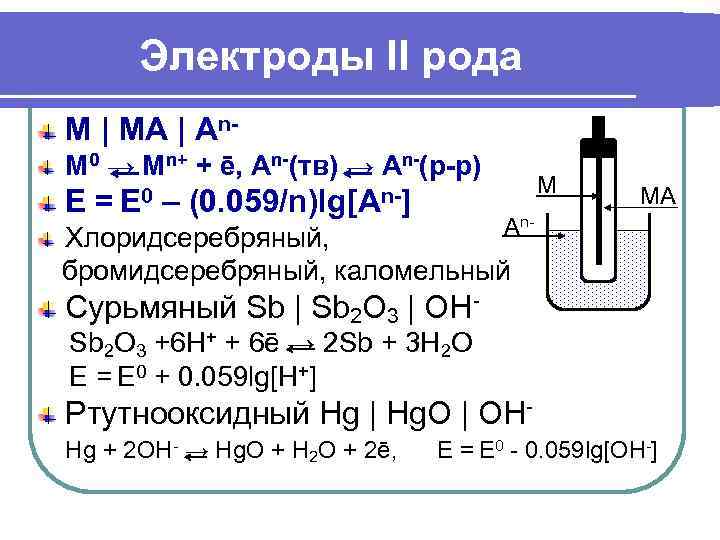
Электроды II рода M | MA | An- M 0 → Mn+ + ē, An-(тв) → An-(р-р) M MA E = E 0 – (0. 059/n)lg[An-] An- Хлоридсеребряный, бромидсеребряный, каломельный Сурьмяный Sb | Sb 2 O 3 | OH- Sb 2 O 3 +6 H+ + 6ē → 2 Sb + 3 H 2 O E = E 0 + 0. 059 lg[H+] Ртутнооксидный Hg | Hg. O | OH- Hg + 2 OH- → Hg. O + H 2 O + 2ē, E = E 0 - 0. 059 lg[ОH-]

Электроды III рода l. M | MA(нас) | M`+(р-р) l E = E 0 + (0. 059/n)lg[M`n+ ] l Ртутный l Hg | Hg 2 C 2 O 4 | Ca 2+ l Hg 2 C 2 O 4 + Ca 2+ + 2ē → Hg + Ca 2 C 2 O 4 l E = E 0 + 0. 029 lg[Ca 2+ ]
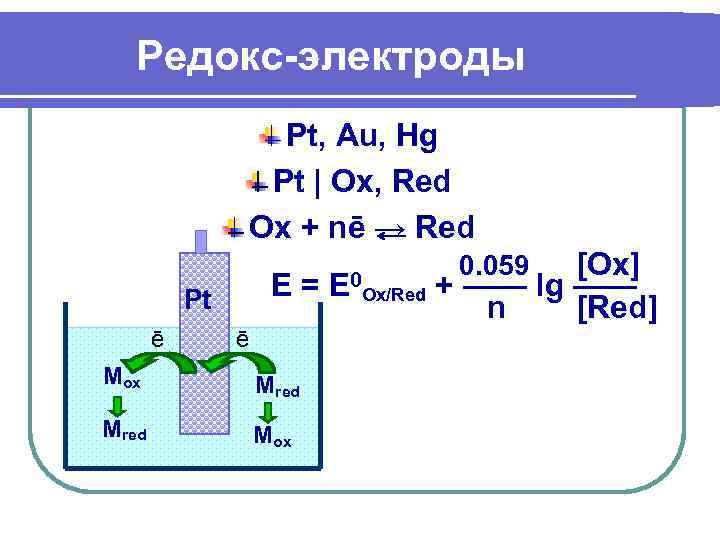
Редокс-электроды Pt, Au, Hg Pt | Ox, Red Ox + nē → Red 0. 059 [Ox] Pt E= E 0 Ox/Red + —— lg —— n [Red] ē ē Mox Mred Mox
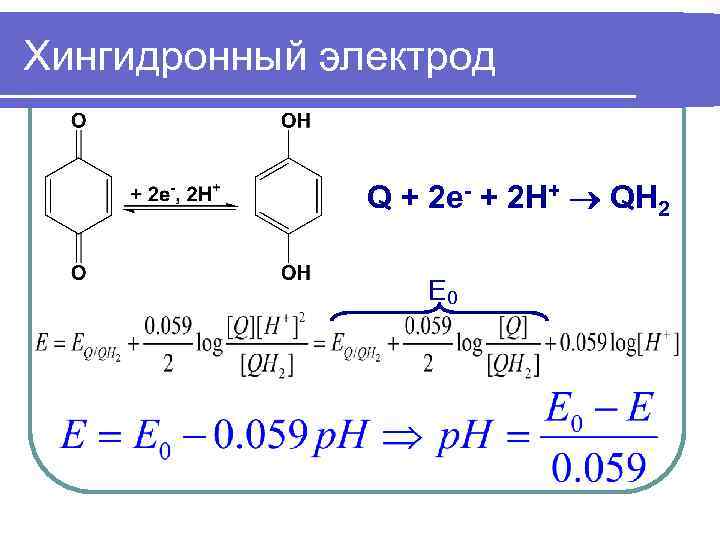
Хингидронный электрод Q + 2 e- + 2 H+ QH 2 E 0
ЭМA_2017_потенциометрия.ppt
- Количество слайдов: 33

