Потенциометрия.ppt
- Количество слайдов: 26
 Электрохимические методы анализа
Электрохимические методы анализа
 n n Электрохимические методы основаны на использовании ионообменных или электронообменных процессов, протекающих на поверхности электрода или в приэлектродном пространстве. Аналитическим сигналом (АС) в электрохимических методах являются: - напряжение или разность электрохимических потенциалов (E), - ток (I) или его интегральная величина во времени количество электричества (Q = I∙t), - совместное измерение величины тока и разности потенциалов (E, I), - электрическое сопротивление (R).
n n Электрохимические методы основаны на использовании ионообменных или электронообменных процессов, протекающих на поверхности электрода или в приэлектродном пространстве. Аналитическим сигналом (АС) в электрохимических методах являются: - напряжение или разность электрохимических потенциалов (E), - ток (I) или его интегральная величина во времени количество электричества (Q = I∙t), - совместное измерение величины тока и разности потенциалов (E, I), - электрическое сопротивление (R).
 Классификация электрохимических методов q По природе источника электрической энергии в системе (по наложению внешнего потенциала): 1) без наложения внешнего потенциала (источником электрической энергии служит электрохимическая ячейка, представляющая собой гальванический элемент) – потенциометрические 2) с наложением внешнего потенциала (через ячейку в ходе анализа протекает электрический ток) – вольтамперометрические, кондуктометрические, электрогравиметрические, кулонометрические и др. q По способу расчета концентрации вещества: прямые – э/х параметр измеряют как известную функцию концентрации раствора и по показанию прибора измеряют содержание вещества в растворе косвенные методы – методы титрования, в которых окончание титрования фиксируют на основании измерения электрических параметров системы
Классификация электрохимических методов q По природе источника электрической энергии в системе (по наложению внешнего потенциала): 1) без наложения внешнего потенциала (источником электрической энергии служит электрохимическая ячейка, представляющая собой гальванический элемент) – потенциометрические 2) с наложением внешнего потенциала (через ячейку в ходе анализа протекает электрический ток) – вольтамперометрические, кондуктометрические, электрогравиметрические, кулонометрические и др. q По способу расчета концентрации вещества: прямые – э/х параметр измеряют как известную функцию концентрации раствора и по показанию прибора измеряют содержание вещества в растворе косвенные методы – методы титрования, в которых окончание титрования фиксируют на основании измерения электрических параметров системы
 Гальванические элементы n Устройство, которое преобразует энергию химических реакций в электрическую энергию, называется гальваническим элементом (электрохимической ячейкой) - система из двух электродов, которые: 1) помещены в раствор электролита или в два разных раствора; 2) контактируют друг с другом. При любой ОВР происходит переход электронов от восстановителя к окислителю: Zn + Cu. SO 4 = Cu + Zn. SO 4 Процесс окисления Zn: Zn – 2 e = Zn 2+ (происходит на аноде -) Процесс восстановления Cu: Cu 2+ + 2 e = Cu (происходит на катоде +) n Реакции окисления и восстановления можно пространственно разделить, тогда электроны будут переходить от восстановителя к окислителю по внешнему проводнику (получим электрический ток). Принцип действия гальванического элемента основан на взаимодействии двух металлов через электролит, приводящем к возникновению в замкнутой цепи электрического тока.
Гальванические элементы n Устройство, которое преобразует энергию химических реакций в электрическую энергию, называется гальваническим элементом (электрохимической ячейкой) - система из двух электродов, которые: 1) помещены в раствор электролита или в два разных раствора; 2) контактируют друг с другом. При любой ОВР происходит переход электронов от восстановителя к окислителю: Zn + Cu. SO 4 = Cu + Zn. SO 4 Процесс окисления Zn: Zn – 2 e = Zn 2+ (происходит на аноде -) Процесс восстановления Cu: Cu 2+ + 2 e = Cu (происходит на катоде +) n Реакции окисления и восстановления можно пространственно разделить, тогда электроны будут переходить от восстановителя к окислителю по внешнему проводнику (получим электрический ток). Принцип действия гальванического элемента основан на взаимодействии двух металлов через электролит, приводящем к возникновению в замкнутой цепи электрического тока.
 Потенциометрия n Метод основан на измерении потенциала электрохимической ячейки, т. е. разности потенциалов между двумя электродами (индикаторным электродом и электродом сравнения), которые могут быть погружены в один и тот же раствор (элемент без переноса) или в два различных по составу раствора, имеющих между собой жидкостной контакт (цепь с переносом)в отсутствии тока во внешней цепи. Прямая потенциометрия – основана на применении уравнения Нернста для нахождения концентрации определяемого компонента по экспериментально измеренной ЭДС цепи или потенциалу электрода (определение р. Н и концентраций ионов с помощью ионоселективных электродов ) ¨ Потенциометрическое титрование - основано на определении точки стехиометричности по результатам титрования и измерении потенциала электрода как функции объема реагента, добавленного к пробе ¨
Потенциометрия n Метод основан на измерении потенциала электрохимической ячейки, т. е. разности потенциалов между двумя электродами (индикаторным электродом и электродом сравнения), которые могут быть погружены в один и тот же раствор (элемент без переноса) или в два различных по составу раствора, имеющих между собой жидкостной контакт (цепь с переносом)в отсутствии тока во внешней цепи. Прямая потенциометрия – основана на применении уравнения Нернста для нахождения концентрации определяемого компонента по экспериментально измеренной ЭДС цепи или потенциалу электрода (определение р. Н и концентраций ионов с помощью ионоселективных электродов ) ¨ Потенциометрическое титрование - основано на определении точки стехиометричности по результатам титрования и измерении потенциала электрода как функции объема реагента, добавленного к пробе ¨
 Электродный потенциал. Уравнение Нернста
Электродный потенциал. Уравнение Нернста
 Потенциометрическая ячейка состоит из: n n Индикаторного электрода, потенциал которого зависит от концентрации определяемого вещества Внешнего электрода сравнения, который имеет фиксированный постоянный потенциал, не зависящий от состава анализируемого раствора Е = (Еинд – Еср)+ Еj Е – потенциал ячейки (ЭДС) Еинд – потенциал индикаторного электрода Еср – потенциал электрода сравнения Еj – потенциал жидкостного соединения
Потенциометрическая ячейка состоит из: n n Индикаторного электрода, потенциал которого зависит от концентрации определяемого вещества Внешнего электрода сравнения, который имеет фиксированный постоянный потенциал, не зависящий от состава анализируемого раствора Е = (Еинд – Еср)+ Еj Е – потенциал ячейки (ЭДС) Еинд – потенциал индикаторного электрода Еср – потенциал электрода сравнения Еj – потенциал жидкостного соединения
 Изменение равновесного потенциала электрода в зависимости от концентрации ионов в растворе называется обратимостью электрода относительно данного катиона или аниона. В связи с этим рассматривают электроды первого и второго рода n Электроды первого рода – электроды, обратимые по катиону, общему с материалом электрода (их потенциал является функцией активности катиона): ¨ Металлические электроды – металл, погруженный в раствор соли этого металла. Потенциал металлического электрода зависит от активности (концентрации) ионов металла ¨ Газовые электроды – в т. ч. водородный электрод. Потенциал газового водородного электрода определяется активностью ионов водорода, т. е. р. Н ¨ Амальгамные электроды – амальгама металла (сплав металла с ртутью), погруженная в раствор, содержащий катионы того же металла. Потенциал такого электрода зависит от активности ионов металла в растворе и активности металла в амальгаме
Изменение равновесного потенциала электрода в зависимости от концентрации ионов в растворе называется обратимостью электрода относительно данного катиона или аниона. В связи с этим рассматривают электроды первого и второго рода n Электроды первого рода – электроды, обратимые по катиону, общему с материалом электрода (их потенциал является функцией активности катиона): ¨ Металлические электроды – металл, погруженный в раствор соли этого металла. Потенциал металлического электрода зависит от активности (концентрации) ионов металла ¨ Газовые электроды – в т. ч. водородный электрод. Потенциал газового водородного электрода определяется активностью ионов водорода, т. е. р. Н ¨ Амальгамные электроды – амальгама металла (сплав металла с ртутью), погруженная в раствор, содержащий катионы того же металла. Потенциал такого электрода зависит от активности ионов металла в растворе и активности металла в амальгаме
 Электроды второго рода – электроды, обратимые по аниону (т. е. их потенциал является функцией активности анионов): 1. Металл, покрытый слоем его труднорастворимой соли, погруженный в раствор, содержащий анионы этой соли – хлорсеребряный электрод Ag|Ag. Cl, KCl - серебряная проволока , покрытая малорастворимой солью Ag. Cl, погруженная в водный раствор хлорида калия: ¨ каломельный электрод Hg|Hg 2 Cl 2, KCl – металлическая ртуть, покрытая пастой малорастворимого хлорида ртути Hg 2 Cl 2 (каломели), контактирующая с водным раствором хлорида калия: Потенциал электрода второго рода зависит от активности анионов: ¨ Эти электроды обладают высокой обратимостью, стабильны, устойчиво поддерживают постоянное значение потенциала, поэтому используются в качестве электродов сравнения)
Электроды второго рода – электроды, обратимые по аниону (т. е. их потенциал является функцией активности анионов): 1. Металл, покрытый слоем его труднорастворимой соли, погруженный в раствор, содержащий анионы этой соли – хлорсеребряный электрод Ag|Ag. Cl, KCl - серебряная проволока , покрытая малорастворимой солью Ag. Cl, погруженная в водный раствор хлорида калия: ¨ каломельный электрод Hg|Hg 2 Cl 2, KCl – металлическая ртуть, покрытая пастой малорастворимого хлорида ртути Hg 2 Cl 2 (каломели), контактирующая с водным раствором хлорида калия: Потенциал электрода второго рода зависит от активности анионов: ¨ Эти электроды обладают высокой обратимостью, стабильны, устойчиво поддерживают постоянное значение потенциала, поэтому используются в качестве электродов сравнения)
 Индикаторные электроды n Классические (электронообменные) – на межфазных границах которых протекают реакции с участием е ¨ Класс 0. Инертный металл (Pt, Au), погруженный в раствор, содержащий ОВР – пару и служащий переносчиком электронов (окислительно-восстановительные электроды) ¨ Класс 1. Обратимые: металл/ион металла (электроды 1 рода) ¨ Класс 2. Обратимые: металл в равновесии с насыщенным раствором соли иона металла и избытком аниона (электроды 2 рода) ¨ Класс 3. Обратимые: металл в равновесии с двумя малорастворимыми солями с общим анионом и избытком второго катиона
Индикаторные электроды n Классические (электронообменные) – на межфазных границах которых протекают реакции с участием е ¨ Класс 0. Инертный металл (Pt, Au), погруженный в раствор, содержащий ОВР – пару и служащий переносчиком электронов (окислительно-восстановительные электроды) ¨ Класс 1. Обратимые: металл/ион металла (электроды 1 рода) ¨ Класс 2. Обратимые: металл в равновесии с насыщенным раствором соли иона металла и избытком аниона (электроды 2 рода) ¨ Класс 3. Обратимые: металл в равновесии с двумя малорастворимыми солями с общим анионом и избытком второго катиона
 Индикаторные электроды n n Мембранные (ионоселективные) электроды – на межфазных границах которых протекают ионообменные процессы. Это электроды, обратимые по тем или иным ионам (катионам или анионам), сорбируемым твердой или жидкой мембраной. Потенциал таких электродов зависит от активности тех ионов в растворе, которые сорбируются мембраной. ИСЭ - это полуэлементы, которые состоят из: ион-селективной мембраны (селективной межфазной границы), внутреннего раствора и внутреннего электрода сравнения ¨ или ион-селективной мембраны и твердофазного контакта (твердотельный электрод) ¨ вторым полуэлементом в паре является внешний электрод сравнения ¨
Индикаторные электроды n n Мембранные (ионоселективные) электроды – на межфазных границах которых протекают ионообменные процессы. Это электроды, обратимые по тем или иным ионам (катионам или анионам), сорбируемым твердой или жидкой мембраной. Потенциал таких электродов зависит от активности тех ионов в растворе, которые сорбируются мембраной. ИСЭ - это полуэлементы, которые состоят из: ион-селективной мембраны (селективной межфазной границы), внутреннего раствора и внутреннего электрода сравнения ¨ или ион-селективной мембраны и твердофазного контакта (твердотельный электрод) ¨ вторым полуэлементом в паре является внешний электрод сравнения ¨
 Типы ионоселективных электродов ¨ Первичные ионоселективные электроды n n n ¨ Электроды со стеклянной мембраной Кристаллические (твердофазные) мембранные электроды Электроды с жидкой мембраной Сложные или многомембранные ионоселективные электроды n Молекулярно-чувствительные устройства (газочувствительные или ферментные электроды) ¨ Ионселективные полевые транзисторы ¨ Прямая потенциометрия с использование ИСЭ называется ионометрией
Типы ионоселективных электродов ¨ Первичные ионоселективные электроды n n n ¨ Электроды со стеклянной мембраной Кристаллические (твердофазные) мембранные электроды Электроды с жидкой мембраной Сложные или многомембранные ионоселективные электроды n Молекулярно-чувствительные устройства (газочувствительные или ферментные электроды) ¨ Ионселективные полевые транзисторы ¨ Прямая потенциометрия с использование ИСЭ называется ионометрией
 Потенциал системы, состоящей из внешнего электрода сравнения и ИСЭ, погруженных в исследуемый раствор, описывается уравнением Никольского-Эйзенмана:
Потенциал системы, состоящей из внешнего электрода сравнения и ИСЭ, погруженных в исследуемый раствор, описывается уравнением Никольского-Эйзенмана:
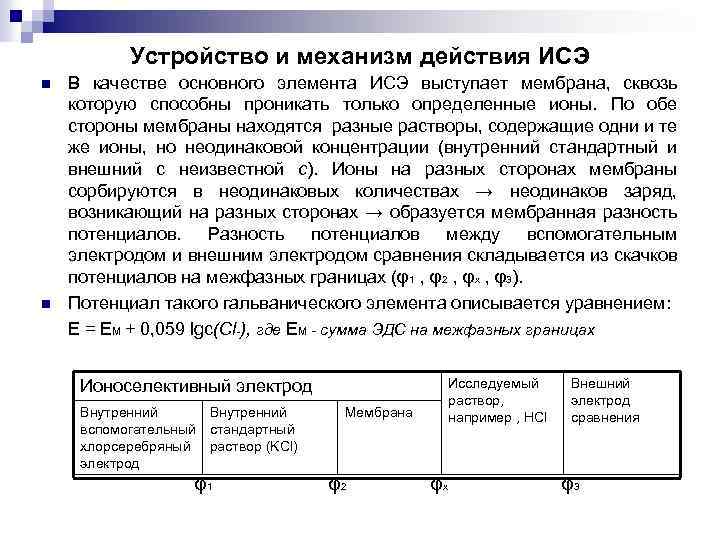 Устройство и механизм действия ИСЭ n n В качестве основного элемента ИСЭ выступает мембрана, сквозь которую способны проникать только определенные ионы. По обе стороны мембраны находятся разные растворы, содержащие одни и те же ионы, но неодинаковой концентрации (внутренний стандартный и внешний с неизвестной с). Ионы на разных сторонах мембраны сорбируются в неодинаковых количествах → неодинаков заряд, возникающий на разных сторонах → образуется мембранная разность потенциалов. Разность потенциалов между вспомогательным электродом и внешним электродом сравнения складывается из скачков потенциалов на межфазных границах (φ1 , φ2 , φх , φ3). Потенциал такого гальванического элемента описывается уравнением: E = EM + 0, 059 lgс(Cl-), где EM - сумма ЭДС на межфазных границах Исследуемый раствор, например , HCl Ионоселективный электрод Внутренний вспомогательный хлорсеребряный электрод Внутренний стандартный раствор (KCl) φ1 Мембрана φ2 φх Внешний электрод сравнения φ3
Устройство и механизм действия ИСЭ n n В качестве основного элемента ИСЭ выступает мембрана, сквозь которую способны проникать только определенные ионы. По обе стороны мембраны находятся разные растворы, содержащие одни и те же ионы, но неодинаковой концентрации (внутренний стандартный и внешний с неизвестной с). Ионы на разных сторонах мембраны сорбируются в неодинаковых количествах → неодинаков заряд, возникающий на разных сторонах → образуется мембранная разность потенциалов. Разность потенциалов между вспомогательным электродом и внешним электродом сравнения складывается из скачков потенциалов на межфазных границах (φ1 , φ2 , φх , φ3). Потенциал такого гальванического элемента описывается уравнением: E = EM + 0, 059 lgс(Cl-), где EM - сумма ЭДС на межфазных границах Исследуемый раствор, например , HCl Ионоселективный электрод Внутренний вспомогательный хлорсеребряный электрод Внутренний стандартный раствор (KCl) φ1 Мембрана φ2 φх Внешний электрод сравнения φ3
 Стеклянные электроды n Первые и наиболее распространенные электроды. С их помощью определяют р. Н растворов, концентрацию ионов Na+, K+. Состоит из: Стеклянного корпуса, в который залит стандартный раствор (0, 1 М HCl с добавкой Na. Cl или буферный раствор с добавкой хлоридов) с припаянным шариком из электродного стекла ¨ Внутреннего электрода сравнения (чаще всего хлорсеребряного) ¨ Стеклянный электрод используют в паре с хлорсеребряным внешним электродом сравнения Ag, Ag. Cl | HCl(0, 1 M) || стекло || Исследуемый || KCl | Ag. Cl, Ag раствор нас Стеклянный электрод Хлорсеребряный электрод Потенциал стеклянного электрода обусловлен обменом ионов щелочных металлов, находящихся в стекле, с ионами водорода из раствора.
Стеклянные электроды n Первые и наиболее распространенные электроды. С их помощью определяют р. Н растворов, концентрацию ионов Na+, K+. Состоит из: Стеклянного корпуса, в который залит стандартный раствор (0, 1 М HCl с добавкой Na. Cl или буферный раствор с добавкой хлоридов) с припаянным шариком из электродного стекла ¨ Внутреннего электрода сравнения (чаще всего хлорсеребряного) ¨ Стеклянный электрод используют в паре с хлорсеребряным внешним электродом сравнения Ag, Ag. Cl | HCl(0, 1 M) || стекло || Исследуемый || KCl | Ag. Cl, Ag раствор нас Стеклянный электрод Хлорсеребряный электрод Потенциал стеклянного электрода обусловлен обменом ионов щелочных металлов, находящихся в стекле, с ионами водорода из раствора.
 Электроды с твердыми мембранами n Мембраны данного вида электродов состоят из ионных кристаллов или их смесей. Это моно- или поликристаллы труднорастворимых в воде солей. В этих мембранах обычно один из двух составляющих соль ионов способен под действием электрического поля перемещаться в кристаллической решетке по ее дефектам. К электродам с твердой мембраной относятся: ¨ лантанфторидный (фторид-селективный) электрод La. F 3 сульфидсеребряные электроды Ag 2 S, ¨ галогенсеребяные электроды Ag. Х (Х — Cl, Br, I), Ag 2 S – Ag. Х ¨ электроды на основе сульфидов (халькогенидов) некоторых двухзарядных ионов металлов Ag 2 S – Cu. S.
Электроды с твердыми мембранами n Мембраны данного вида электродов состоят из ионных кристаллов или их смесей. Это моно- или поликристаллы труднорастворимых в воде солей. В этих мембранах обычно один из двух составляющих соль ионов способен под действием электрического поля перемещаться в кристаллической решетке по ее дефектам. К электродам с твердой мембраной относятся: ¨ лантанфторидный (фторид-селективный) электрод La. F 3 сульфидсеребряные электроды Ag 2 S, ¨ галогенсеребяные электроды Ag. Х (Х — Cl, Br, I), Ag 2 S – Ag. Х ¨ электроды на основе сульфидов (халькогенидов) некоторых двухзарядных ионов металлов Ag 2 S – Cu. S.
 Электроды с жидкими мембранами n n n Возникновение потенциала на границе раздела фаз обусловлено ионным обменом, связанным с различием констант распределения иона между водной и органическими фазами. Электроды на основе жидких катионитов. Электродно-активными веществами, определяющими катионную функцию мембранных жидкостных электродов, являются органические высокомолекулярные кислоты и их соли с карбоксильной, фосфорно- и тиофосфорнокислыми группами. Электроды на основе жидких анионитов. Электродно-активными веществами, имеющими положительно заряженную активную группу, являются соли аминов и четвертичных аммониевых оснований, являющихся типичными жидкими анионообменниками. Эти электроды могут быть использованы для следующих анионов: Cl. O 4 -, SCN-, I-, NO 3 -, Br-, Cl-. Существует несколько разновидностей электродов с жидким анионитом: нитрат-селективный электрод , перхлорат-селективный электрод (селективный к Cl. O 4 - ионам), фосфат-селективный электрод (селективный к HPO 42 - в разбавленных растворах в интервале р. Н = 7, 0 – 7, 5).
Электроды с жидкими мембранами n n n Возникновение потенциала на границе раздела фаз обусловлено ионным обменом, связанным с различием констант распределения иона между водной и органическими фазами. Электроды на основе жидких катионитов. Электродно-активными веществами, определяющими катионную функцию мембранных жидкостных электродов, являются органические высокомолекулярные кислоты и их соли с карбоксильной, фосфорно- и тиофосфорнокислыми группами. Электроды на основе жидких анионитов. Электродно-активными веществами, имеющими положительно заряженную активную группу, являются соли аминов и четвертичных аммониевых оснований, являющихся типичными жидкими анионообменниками. Эти электроды могут быть использованы для следующих анионов: Cl. O 4 -, SCN-, I-, NO 3 -, Br-, Cl-. Существует несколько разновидностей электродов с жидким анионитом: нитрат-селективный электрод , перхлорат-селективный электрод (селективный к Cl. O 4 - ионам), фосфат-селективный электрод (селективный к HPO 42 - в разбавленных растворах в интервале р. Н = 7, 0 – 7, 5).
 n n Газочувствительные ионоселективные электроды – для определения содержания в растворах NH 3 , CO 2, SO 2, H 2 S и др. Газовый электрод включает ионоселективный электрод и электрод сравнения, контактирующие с небольшим объемом вспомогательного (приэлектродного) раствора, который отделен от исследуемого раствора газовой прослойкой или гидрофобной газопроницаемой мембраной. В основе их действия лежат реакции с участием газов (напр. , СО 2 + H 2 O = Н+ + HCO 3 -). Газ распределяется между измеряемым и вспомогательными растворами. Образующиеся во вспомогательном растворе ионы регистрируются ионоселективным электродом. Поскольку в большинстве используемых реакций образуются ионы Н+, в газочувствительных электродах применяют в основном стеклянные ионоселективные электроды. Биоспецифичные ионоселективные электроды – ферментные, иммуноферментные, бактериальные, микробные и др. – для определения концентрации органических соединений. В основе их действия лежат реакции, катализируемые ферментами, которые превращают неионное вещество (субстрат) в ион, определяемый соответствующим ионоселективным электродом. Обычно фермент используют в иммобилизованном состоянии непосредственно на мембране ионоселективного электрода, иногда – на отдельном носителе. Ферментные электроды позволяют определить концентрацию не только субстратов, но и веществ, являющихся ингибиторами или активаторами каталитических реакций.
n n Газочувствительные ионоселективные электроды – для определения содержания в растворах NH 3 , CO 2, SO 2, H 2 S и др. Газовый электрод включает ионоселективный электрод и электрод сравнения, контактирующие с небольшим объемом вспомогательного (приэлектродного) раствора, который отделен от исследуемого раствора газовой прослойкой или гидрофобной газопроницаемой мембраной. В основе их действия лежат реакции с участием газов (напр. , СО 2 + H 2 O = Н+ + HCO 3 -). Газ распределяется между измеряемым и вспомогательными растворами. Образующиеся во вспомогательном растворе ионы регистрируются ионоселективным электродом. Поскольку в большинстве используемых реакций образуются ионы Н+, в газочувствительных электродах применяют в основном стеклянные ионоселективные электроды. Биоспецифичные ионоселективные электроды – ферментные, иммуноферментные, бактериальные, микробные и др. – для определения концентрации органических соединений. В основе их действия лежат реакции, катализируемые ферментами, которые превращают неионное вещество (субстрат) в ион, определяемый соответствующим ионоселективным электродом. Обычно фермент используют в иммобилизованном состоянии непосредственно на мембране ионоселективного электрода, иногда – на отдельном носителе. Ферментные электроды позволяют определить концентрацию не только субстратов, но и веществ, являющихся ингибиторами или активаторами каталитических реакций.
![Прямая потенциометрия n n Определение концентрации ионов, в частности [H+], с помощью уравнения Нернста Прямая потенциометрия n n Определение концентрации ионов, в частности [H+], с помощью уравнения Нернста](https://present5.com/presentation/3/30101942_177065616.pdf-img/30101942_177065616.pdf-19.jpg) Прямая потенциометрия n n Определение концентрации ионов, в частности [H+], с помощью уравнения Нернста по ЭДС гальванического элемента. Метод градуировочного графика. Проводят предварительную калибровку ИСЭ для установления зависимости между потенциалом электрода и активностью или концентрацией определяемых ионов. Для этого используют серию стандартных растворов с постоянной ионной силой (для этого вводят индифферентный электролит). Измеряют ЭДС всех эталонных растворов (электроды тщательно промывают) после установления равновесного потенциала (время отклика – 2 -3 мин). Строят градуировочный график Е-pc, где рс=-lgc, с – концентрация определяемого иона. Затем измеряют ЭДС ячейки с анализируемым раствором и по графику находят концентрацию.
Прямая потенциометрия n n Определение концентрации ионов, в частности [H+], с помощью уравнения Нернста по ЭДС гальванического элемента. Метод градуировочного графика. Проводят предварительную калибровку ИСЭ для установления зависимости между потенциалом электрода и активностью или концентрацией определяемых ионов. Для этого используют серию стандартных растворов с постоянной ионной силой (для этого вводят индифферентный электролит). Измеряют ЭДС всех эталонных растворов (электроды тщательно промывают) после установления равновесного потенциала (время отклика – 2 -3 мин). Строят градуировочный график Е-pc, где рс=-lgc, с – концентрация определяемого иона. Затем измеряют ЭДС ячейки с анализируемым раствором и по графику находят концентрацию.
 n Метод добавок стандарта. В э/х ячейку вносят известный объем V(X) анализируемого раствора с концентрацией с(Х) и измеряют ЭДС. Затем прибавляют небольшой точно измеренный объем стандартного раствора V(ст) с известной (достаточно большой) концентрацией определяемого вещества с(ст) и снова определяют ЭДС. Концентрацию определяемого компонента с(Х) в растворе рассчитывают по формуле:
n Метод добавок стандарта. В э/х ячейку вносят известный объем V(X) анализируемого раствора с концентрацией с(Х) и измеряют ЭДС. Затем прибавляют небольшой точно измеренный объем стандартного раствора V(ст) с известной (достаточно большой) концентрацией определяемого вещества с(ст) и снова определяют ЭДС. Концентрацию определяемого компонента с(Х) в растворе рассчитывают по формуле:
 Применение прямой потенциометрии n n Определение фторид-ионов с использованием фторидселективного электрода – при анализе питьевой воды, биологических жидкостей, фармацевтических препаратов и др. Ионселективный электрод на основе пластинки из монокристалла La. F 3 имеет нернстовскую электродную функцию (интервал прямолинейной зависимости потенциала от активности потенциалопределяющего иона) в интервале p. F =1 - 6 (с(F-) = 10 -1– 10 -6 моль/л) Рабочий интервал р. Н исследуемого раствора – 4, 4 -8, 0 (буфер) Уникальная селективность: не мешают значительные количества Cl-, Br- , SO 42 - , SO 32 - , NO 3 - (влияет силикат-ион)
Применение прямой потенциометрии n n Определение фторид-ионов с использованием фторидселективного электрода – при анализе питьевой воды, биологических жидкостей, фармацевтических препаратов и др. Ионселективный электрод на основе пластинки из монокристалла La. F 3 имеет нернстовскую электродную функцию (интервал прямолинейной зависимости потенциала от активности потенциалопределяющего иона) в интервале p. F =1 - 6 (с(F-) = 10 -1– 10 -6 моль/л) Рабочий интервал р. Н исследуемого раствора – 4, 4 -8, 0 (буфер) Уникальная селективность: не мешают значительные количества Cl-, Br- , SO 42 - , SO 32 - , NO 3 - (влияет силикат-ион)
 Определение р. Н растворов n n Индикаторные электроды – электроды, потенциал которых зависит от с(H+): стеклянный, водородный, хингидронный и др. Электроды сравнения – хлорсеребряный, каломельный. Стеклянный электрод: диапазон р. Н=2 -10, высокая обратимость, стабильность. ЭДС цепи со стеклянным электродом в качестве индикаторного равна Е=К+0, 059 р. Н, где К – постоянная, зависящая от материала мембраны и природы электрода сравнения. Хингидронный электрод – окислительно-восстановительный электрод: платиновая проволока, погруженная в раствор HCl, насыщенный хингидроном (соединение хинона с гидрохиноном): Pt | хингидрон, HCl С 6 Н 4 О 2 + 2 H+ +2 е = С 6 Н 4(ОН)2, Е = Е 0 – 0, 059 р. Н, диапазон р. Н=0 -8, 5 (при р. Н› 8, 5 – реакция нейтрализации) Водородный электрод (стандартный водородный электрод) – газовый электрод (электрод 1 рода) – платиновая пластинка, омываемая газообразным водородом при давлении 1 атм и погруженная в раствор кислоты с а(H+)=1 моль/л. H 2(г) = 2 H+ + 2 e-, Е = Е 0 + 0, 059 lg а(H+) = - 0, 059 p. H
Определение р. Н растворов n n Индикаторные электроды – электроды, потенциал которых зависит от с(H+): стеклянный, водородный, хингидронный и др. Электроды сравнения – хлорсеребряный, каломельный. Стеклянный электрод: диапазон р. Н=2 -10, высокая обратимость, стабильность. ЭДС цепи со стеклянным электродом в качестве индикаторного равна Е=К+0, 059 р. Н, где К – постоянная, зависящая от материала мембраны и природы электрода сравнения. Хингидронный электрод – окислительно-восстановительный электрод: платиновая проволока, погруженная в раствор HCl, насыщенный хингидроном (соединение хинона с гидрохиноном): Pt | хингидрон, HCl С 6 Н 4 О 2 + 2 H+ +2 е = С 6 Н 4(ОН)2, Е = Е 0 – 0, 059 р. Н, диапазон р. Н=0 -8, 5 (при р. Н› 8, 5 – реакция нейтрализации) Водородный электрод (стандартный водородный электрод) – газовый электрод (электрод 1 рода) – платиновая пластинка, омываемая газообразным водородом при давлении 1 атм и погруженная в раствор кислоты с а(H+)=1 моль/л. H 2(г) = 2 H+ + 2 e-, Е = Е 0 + 0, 059 lg а(H+) = - 0, 059 p. H
 Потенциометрическое титрование основано на определении точки стехиометричности по результатам потенциометрических измерений. При титровании вблизи ТС происходит резкое изменение (скачок) потенциала индикаторного электрода, который зависит от концентрации опрделяемых ионов n Реакции потенциометрического титрования должны протекать строго стехиометрично, иметь высокую скорость, идти до конца. Не требуется использование индикаторов. n Для потенциометрического титрования собирают цепь из индикаторного электрода в анализируемом растворе и электрода сравнения. В качестве индикаторных – стеклянный, ртутный, платиновый, серебряный, ионоселективные электроды. В качестве электродов сравнения - каломельный или хлорсеребряный. n Достоинства: высокая точность, большая чувствительность, возможность проводить титрование в мутных, окрашенных, неводных средах, раздельно определять компоненты смеси в одном растворе. n
Потенциометрическое титрование основано на определении точки стехиометричности по результатам потенциометрических измерений. При титровании вблизи ТС происходит резкое изменение (скачок) потенциала индикаторного электрода, который зависит от концентрации опрделяемых ионов n Реакции потенциометрического титрования должны протекать строго стехиометрично, иметь высокую скорость, идти до конца. Не требуется использование индикаторов. n Для потенциометрического титрования собирают цепь из индикаторного электрода в анализируемом растворе и электрода сравнения. В качестве индикаторных – стеклянный, ртутный, платиновый, серебряный, ионоселективные электроды. В качестве электродов сравнения - каломельный или хлорсеребряный. n Достоинства: высокая точность, большая чувствительность, возможность проводить титрование в мутных, окрашенных, неводных средах, раздельно определять компоненты смеси в одном растворе. n
 Виды потенциометрического титрования n n Кислотно-основное титрование: ¨ Индикаторный – стеклянный электрод ¨ Применение – 1) количественное определение компонентов в смеси кислот (если Кдисс различаются не менее чем на три порядка), в том числе сильных и слабых кислот, многоосновных кислот; 2) анализ многокомпонентных смесей без разделения в неводных растворителях (ледяная уксусная кислота, ацетон и др. ). Комплексонометрическое титрование: ¨ Титрант – комплексон III (ЭДТА) ¨ Индикаторный электрод – металлический (с одноименным металлом) или ионоселективный. ¨ Универсальный ртутный электрод: Hg|Hg. Y 2 - или Au(Hg)|Hg. Y 2 - где Au(Hg) - амальгамированное золото; Hg. Y 2 - - комплекс ртути с анионом ЭДТА. С его помощью могут быть оттитрованы любые катионы, которые образуют с Y 4 - комплексы с константой устойчивости, не превышающей константу устойчивости ртутного комплекса: Mg 2+, Ca 2+, Co 2+, Ni 2+, Сu 2+, Zn 2+ и др.
Виды потенциометрического титрования n n Кислотно-основное титрование: ¨ Индикаторный – стеклянный электрод ¨ Применение – 1) количественное определение компонентов в смеси кислот (если Кдисс различаются не менее чем на три порядка), в том числе сильных и слабых кислот, многоосновных кислот; 2) анализ многокомпонентных смесей без разделения в неводных растворителях (ледяная уксусная кислота, ацетон и др. ). Комплексонометрическое титрование: ¨ Титрант – комплексон III (ЭДТА) ¨ Индикаторный электрод – металлический (с одноименным металлом) или ионоселективный. ¨ Универсальный ртутный электрод: Hg|Hg. Y 2 - или Au(Hg)|Hg. Y 2 - где Au(Hg) - амальгамированное золото; Hg. Y 2 - - комплекс ртути с анионом ЭДТА. С его помощью могут быть оттитрованы любые катионы, которые образуют с Y 4 - комплексы с константой устойчивости, не превышающей константу устойчивости ртутного комплекса: Mg 2+, Ca 2+, Co 2+, Ni 2+, Сu 2+, Zn 2+ и др.
 n Окислительно-восстановительное титрование: Индикаторный электрод – электрод из инертного металла (Au, Pt) ¨ Для получения скачка необходимо, чтобы разность стандартных потенциалов ОВ-пар была велика: ∆Еº˃0, 36 В ¨ n Осадительное титрование: ¨ Индикаторные электроды – металлические (электроды 1, 2 рода) или мембранные электроды, чувствительные к определяемому иону или иону-осадителю. ¨ Применение – определение катионов серебра, ртути, цинка, свинца, анионов хлора, брома, иода и др. , смесей галогенидов (если значения констант растворимости отличаются не менее, чем в 1000 раз).
n Окислительно-восстановительное титрование: Индикаторный электрод – электрод из инертного металла (Au, Pt) ¨ Для получения скачка необходимо, чтобы разность стандартных потенциалов ОВ-пар была велика: ∆Еº˃0, 36 В ¨ n Осадительное титрование: ¨ Индикаторные электроды – металлические (электроды 1, 2 рода) или мембранные электроды, чувствительные к определяемому иону или иону-осадителю. ¨ Применение – определение катионов серебра, ртути, цинка, свинца, анионов хлора, брома, иода и др. , смесей галогенидов (если значения констант растворимости отличаются не менее, чем в 1000 раз).
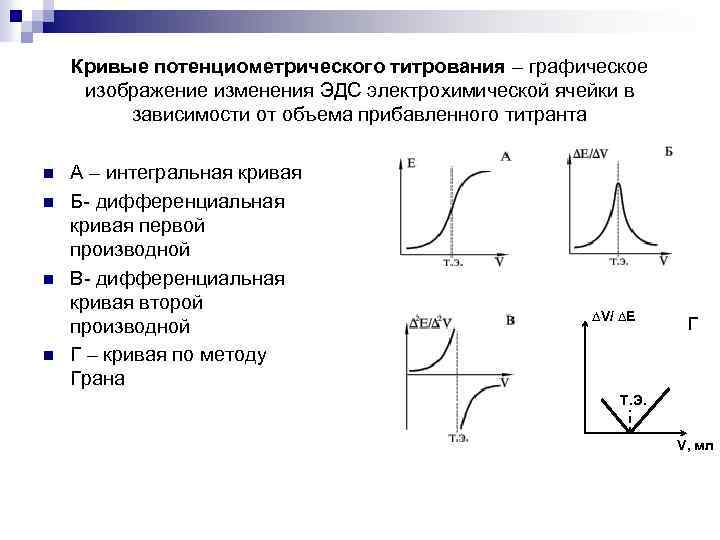 Кривые потенциометрического титрования – графическое изображение изменения ЭДС электрохимической ячейки в зависимости от объема прибавленного титранта n n А – интегральная кривая Б- дифференциальная кривая первой производной В- дифференциальная кривая второй производной Г – кривая по методу Грана ∆V/ ∆E Г Т. Э. V, мл
Кривые потенциометрического титрования – графическое изображение изменения ЭДС электрохимической ячейки в зависимости от объема прибавленного титранта n n А – интегральная кривая Б- дифференциальная кривая первой производной В- дифференциальная кривая второй производной Г – кривая по методу Грана ∆V/ ∆E Г Т. Э. V, мл


